«Российский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
| Вид материала | Автореферат |
- «Российский государственный медицинский университет Федерального агентства по здравоохранению, 568.86kb.
- «Российский государственный медицинский университет Федерального агентства по здравоохранению, 545.1kb.
- «Сибирский государственный медицинский университет Федерального агентства по здравоохранению, 927.55kb.
- Кубанский государственный медицинский университет федерального агентства по здравоохранению, 821.27kb.
- «Казанский государственный медицинский университет Федерального агентства по здравоохранению, 863.64kb.
- «Саратовский государственный медицинский университет имени В. И. Разумовского Федерального, 378.09kb.
- Гепатопротекторные свойства флавоноидов (фармакодинамика и перспективы клинического, 671.3kb.
- «ультразвуковая диагностика кишечной непроходимости» 14. 00. 27 хирургия, 401.81kb.
- «Рязанский государственный медицинский университет имени академика И. П. Павлова Федерального, 241.22kb.
- Программа подготовки аспирантов по кардиологии составили: д м. н., профессор, 643.17kb.
Примечание: I - нифедипина пролонгированного действия, II - нифедипин короткого действия, III – метилдопа, IV – атенолол, V - без медикаментозной антигипертензивной терапии до 34-й недели беременности. Критерии исключения: беременные с ГАГ, протеинурией, ПЭ, с сахарным диабетом, заболеваниями щитовидной железы.
Сравнительное изучение клинических эффектов различных групп антигипертензивных препаратов при ХАГ проводили с участием 127 пациенток, включенных в исследование после 20-ой недели беременности (Таблица 2). Группы были сопоставимы по возрасту, антропометрическим данным, паритету родов и тяжести АГ. Проводились СМАД, оценка состояния эндотелийзависимой вазодилатации, уровня гликемии натощак, показателей инсулинорезистентности и липидного профиля до начала терапии и на фоне лечения. Анализ течения беременности и родов, веса новорожденных осуществлялся на основе данных первичной документации (карта по беременности по месту наблюдения в женской консультации).
В исследовании состояния сердечно-сосудистой системы и метаболического статуса женщин детородного возраста, имевших в период беременности АГ, участвовало 84 женщины - пациентки с ХАГ (ГБ), (n=30) и ГАГ (n=25). Группу сравнения составили 29 женщины, у которых в анамнезе были беременности, протекавших без осложнений. Проводилось клиническое и лабораторное обследование. Применялись инструментальные методы исследования: ЭКГ, СМАД, тредмилметрия. В группах пациенток с АГ проводили Холтер-ЭКГ, ЭхоКГ, тестирование по визуально-аналоговой шкале общей оценки здоровья.
С целью изучения особенностей течения АГ у женщин в период менопаузы, имевших повышение АД во время беременности, были обследованы 211 рожавших женщин с АГ в постменопаузальном возрасте. В исследование вошли пациентки, которые на момент включения не получали постоянную антигипертензивную терапию. На основании репродуктивного анамнеза и выявления факта повышения АД в период беременности (ГАГ) женщины были распределены на две группы (Таблица 3). Группы были сопоставимы по возрасту, длительности АГ и менопаузы, количеству родов в анамнезе.
Таблица 3
Характеристика пациенток менопаузального возраста с АГ, включенных в исследование
| Параметр | Пациентки с ГАГ в анамнезе | Пациентки без ГАГ в анамнезе |
| Количество женщин | 97 | 114 |
| Средний возраст, годы | 62,2±1,0 (51–65) | 64,6±1,81 (48–65) |
| ИМТ, кг/м2 | 31,7±0,8* | 29,4 ±0,6 |
| Длительность АГ, годы | 9,9±2,0 | 10,4±1,2 |
| Длительность менопаузы, годы | 10,1±0,7 | 10,5±0,8 |
| Количество родов, абс.(%) | | |
| 1 | 55 (56,7) | 64 (56,1) |
| 2 | 36 (37,1) | 46 (40,4) |
| 3 | 6 (6,2) | 4 (3,5) |
| Срочные роды, % | 85 (87,6) | 100 |
| Преждевременные роды, % | 12 (12,4) | – |
Примечание: * – p<0,01, ** - P=0,00001, *** - P=0,02. Критерии исключения: вторичная АГ, сахарный диабет 2-го типа средней степени тяжести и выше, заболевания почек с протеинурией и/или признаками почечной недостаточности, перенесенный инфаркт миокарда, клинически значимая сердечная и дыхательная недостаточность, тяжелая черепно-мозговая травма или инсульт в анамнезе, курение, злоупотребление алкоголем.
В исследование по изучению эффективности антигипертензивной терапии при АГ у женщин постменопаузального возраста, имевших в анамнезе гестационные гипертензивные состояния, была включена 61 пациентка. В зависимости от особенностей течения гестационного периода были выделены две группы (Таблица 4). Группы были сопоставимы по возрасту, длительности АГ, структуре сопутствующих заболеваний. Нифедипин пролонгированного действия 40 мг назначался однократно в сутки в виде монотерапии в течение 4-х недель. Об эффективности антигипертензивной терапии судили на основании клинического измерения АД. Через 1 месяц лечения оценивался гипотензивный эффект и переносимость препарата. Женщинам, у которых целевые значения АД не были достигнуты в этот срок, дополнительно назначался эналаприл 10 мг в сутки. Через 6 месяцев антигипертензивной терапии пациентки были повторно обследованы.
Таблица 4
Исходные клинико-анамнестические данные включенных в исследование пациенток
| Параметр | Пациентки с ГАГ в анамнезе (n=23) | Пациентки без ГАГ в анамнезе (n=38) | P |
| Средний возраст, годы | 63,4±1,0 (55–65) | 65,1±1,7 (51–65) | NS |
| Длительность АГ, годы | 10,8±2,1 | 10,4±1,2 | NS |
| Длительность менопаузы, годы | 14,1±0,6 | 13,5±0,9 | NS |
| Количество родов, абс.(%) | | | |
| 1 | 13 (56,5) | 17 (44,7) | NS |
| 2 | 10 (43,5) | 20 (52,6) | |
| 3 | | 1 (2,6) | |
| ИМТ, кг/м2 | 32,8±0,9 | 29,8 ±0,8 | <0,05 |
| Ожирение, абс.(%) | 14(60,9) | 16(42,1) | NS |
| Сопутствующие заболевания, абс. (%) | | | |
| СД 2-го типа, легкое течение | 8 (34,8) | 7 (18,4) | NS |
| ИБС | 7 (30,4) | 8 (21,1) | NS |
Методы исследования
Суточное мониторирование АД у беременных выполняли прибором фирмы "Shiller" в амбулаторных условиях на 10-11, 21-22 и 32-33 неделях беременности. АД измеряли в стандартном режиме с интервалами в дневные часы 15 мин, в ночное время – 30 мин. Рассчитывали средние за сутки, день и ночь цифры систолического и диастолического АД. Степень ночного снижения АД, или суточный индекс (СИ), определяли как соотношение разницы дневного и ночного АД к дневному АД, выраженное в %. Для характеристики вариабельности АД использовали показатель стандарта отклонения (Std) систолического и диастолического АД. Временной гипертонический индекс (ВИ), или нагрузка давлением, рассчитывали для суточного систолического и диастолического АД в процентах. Суточное мониторирование АД у пациенток с АГ репродуктивного и менопаузального возрастов осуществляли портативным прибором фирмы “Meditech”.
Для оценки вариабельности сердечного ритма у женщин репродуктивного возраста проводили мониторирование ЭКГ по Холтеру, использовали прибор фирмы "Shiller". При анализе оценивали ЧСС, нарушения ритма и проводимости, динамику сегмента ST, показатели вариабельности сердечного ритма. Рассматривалась совокупность последовательных временных промежутков – интервалов RR. Для статистической характеристики использовали следующие показатели: SDNN, мс – стандартное отклонение всех NN-интервалов; SDANN, мс - стандартное отклонение средних значений NN-интервалов, вычисленных по 5-минутным промежуткам в течение всей записи; SDNN индекс, мс – среднее значение стандартных отклонений NN-интервалов, вычисленных по 5-минутным промежуткам в течение всей записи; rMSSD, мс – квадратный корень из средней суммы квадратов разностей между соседними NN-интервалами; pNN50, % – количество пар соседних NN-интервалов, различающихся более, чем на 50 мс, в течение всей записи, деленное на общее число NN-интервалов.
Исследование структурно-функционального состояния сердца проводилось эхокардиографическим методом в М-, В-режиме и допплеровских режимах в стандартных позициях по общепринятой методике Feigenbaum A. (1986). Анализировались средние значения: конечно-диастолический размер (КДР), конечно-систолический размер (КСР), толщина межжелудочковой перегородки (ТМЖП), толщина задней стенки левого желудочка (ТЗСЛЖ). Определяли конечно-диастолический объем (КДО) ЛЖ, конечно-систолический объем (КСО), минутный объем (МО), ударный объем (УО). Всем больным определяли ФВ ЛЖ методом Симпсона. Исследование диастолической функции ЛЖ проводили с помощью импульсно-волновой допплерографии [Шиллер Н., Осипов М.А., 2005]. Масса миокарда левого желудочка (ММЛЖ) рассчитывалась по формуле R.Devereux (1977 г.). Полученные объемные показатели и массы миокарда ЛЖ соотносили к площади поверхности тела и вычисляли индекс массы миокарда (ИММ), сердечный индекс (СИ), ударный индекс (УИ). Гипертрофию миокарда ЛЖ диагностировали при значениях выше 110 г/м2 [Mancia G. et al, 2007]. Ремоделирование миокарда оценивали по относительной толщине стенок (ОТС) ЛЖ – отношению суммы ТМЖП и ТЗСЛЖ к КДР ЛЖ. У женщин репродуктивного возраста, в соответствии с последними рекомендациями Комитета по номенклатуре и стандартам Американского общества эхокардиографии, за норму принимали ОТС<0,42 [ссылка скрыта et al, 2006]. У пациенток постменопаузального возраста за норму считали показатель ОТС<0,45 [Ganau A., Devereux RB. еt al. 1992]. Выделяли следующие типы ремоделирования: 1) концентрическое ремоделирование: нормальный ИММЛЖ и ОТС > 0,45; 2) концентрическая гипертрофия: увеличение ИММЛЖ и ОТС > 0,45; 3) эксцентрическая гипертрофия: увеличение ИММЛЖ при нормальной ОТС (< 0,45). Рассчитывали показатели общего периферического сосудистого сопротивления (ОПСС).
Эндотелийзависимую вазодилатацию (ЭЗВД) оценивали в пробе с реактивной гиперемией плечевой артерии с использованием ультразвука высокого разрешения [Corretti M.C., Anderson T.J., Benjamin E.J et al.2002]. Диаметр плечевой артерии измеряли через 60 сек после реактивной гиперемии. Показатели сравнивали с исходными данными. ЭЗВД оценивали как процент прироста диаметра сосуда. При ЭЗВД менее 10% судили о вазомоторной эндотелиальной дисфункции.
Тредмилметрия проводилась по протоколу Bruce, со ступенчатым наращиванием нагрузки каждые 3 мин путем увеличения скорости и угла движения ленты, оценивали продолжительность теста, максимальное значение ЧСС, АД, продолжительность восстановительного периода. Физическая работоспособность характеризовалась метаболическими единицами (МЕТ). Пробу считали отрицательной при достижении субмаксимальной величины ЧСС (85% от расчетной) без признаков ишемии миокарда на ЭКГ.
Лабораторное исследование проводили с помощью автоматических анализаторов, определяли общий холестерин (ОХЛ), холестерин липопротеидов низкой плотности (ЛПНП), липопротеидов высокой плотности (ЛПВП), триглицериды (ТГ), глюкозу натощак, мочевую кислоту, а также креатинин, мочевину, аланинаминотрасферазу (АлАТ), аспартатаминотрасферазу (АсАТ), калий, натрий, билирубин, гликированный гемоглобин (НвАс1). Уровень инсулина определялся с помощью метода иммуноферментного анализа, степень резистентности тканей к инсулину оценивалась с использованием индекса инсулинорезистентности (HOMA-IR).
Исследование когнитивной функции у пациенток с АГ менопаузального возраста проводили с использованием краткой шкалы оценки психического статуса (MMSE), или «мини-ментального теста», и теста «рисования часов». Результат MMSE - теста получали путем суммации баллов по каждому из 30 вопросов. Максимально в этом тесте можно набрать 30 баллов, что соответствует наиболее высоким когнитивным способностям. Чем меньше результат теста, тем более выражен когнитивный дефицит. Тест «рисования часов» проводили с целью диагностики зрительно-пространственных нарушений. Пациентке предлагалось самостоятельно нарисовать круг – циферблат часов, поставить 12 чисел и нарисовать стрелки, указывающие время по заданию врача. Результаты оценивали количественно по 10-балльной шкале [В.В.Захаров, 2005].
Для оценки качества жизни пациенток использовали Визуально-Аналоговую Шкалу (ВАШ) с определением женщиной состояния своего здоровья на отрезке линии от 0% (самое плохое здоровье) до 100% (идеальное здоровье).
Статистическую обработку данных проводили на персональном компьютере с помощью программы «Statistica 6.0 for Windows”. Для предоставления данных использовали показатели: среднее значение, стандартную ошибку средней, стандартное отклонение, либо медиану и интерквартильный размах, проценты и частоты. Для сравнения количественных показателей в исследуемых группах и определения различий между ними использовали критерий Стьюдента и непараметрический U критерий Манна-Уитни. Различия считали достоверными при уровне значимости р < 0,05. Для выявления отличий между группами по частоте встречаемости различных признаков использовали критерий χ2 и точный критерий Фишера с построением четырехпольных таблиц. Связь между исследуемыми показателями оценивали с помощью корреляционного анализа с определением коэффициента корреляции (r) и его уровня значимости (р). Коэффициент корреляции считали достоверным и значимым при р < 0,05. Статистической обработкой материала предусматривалось получение комбинационных таблиц, диаграмм, графиков и аналитических показателей.
РЕЗУЛЬТАТЫ
Фаза I. При проведении популяционного наблюдательного исследования соматической заболеваемости беременных, состоящих на учете в нескольких женских консультациях г. Москвы в 1995, 2000 и 2008 годах, была выявлена тенденция роста распространенности АГ с 8% до 10,7% (Таблица 5). Отмечено достоверное увеличение в 2008 году среднего возраста беременных. Пациентки с АГ во все годы наблюдения были старше в сравнении с другими участницами исследования. Это соответствует эпидемиологическим данным. Как известно, эссенциальная АГ редко манифестирует у женщин моложе 30 лет [Кушаковский М.С., 1995; Шальнова С.А., 2005]. К 2008 году отмечалось изменение соотношения перво- и повторнородящих беременных в пользу последних. Средние показатели ИМТ беременных достоверно не менялись, однако к 2008 году увеличилась доля женщин, страдающих ожирением. Отмечался рост распространенности соматической патологии у беременных, трехкратное увеличение патологии щитовидной железы, хронических заболеваний бронхо-легочной системы и желудочно-кишечного тракта. Статистически значимо возросла частота анемического синдрома. Соматическая патология была выявлена у подавляющего числа участниц исследования. Количество беременных, признанных практически здоровыми, в 2008 снизилось до 1,7% (P<0,001).
Таблица 5
Распространенность АГ при беременности, демографические показатели и сопутствующая соматическая патология у беременных
| Параметр | Беременные | Р | ||
| 1995 год (n=486) | 2000 год (n=532) | 2008 год (n=525) | ||
| АД ≥ 140/90 мм рт.ст., абс.(%) | 39(8,0) | 50(9,4) | 56(10,7) | * NS; ** NS; *** NS |
| Средний возраст, M±SD лет | 25,4± 5,6 (17-41) | 25,9±5,4 (16-43) | 28,1± 5,1 (17-46) | * NS; ** p<0,001; *** p<0,001 |
| Средний возраст пациенток с АГ против беременных-нормотоников, лет | 28,6±6,1 vs 24,9±5,3 p<0,001 | 28,5±6,3 vs 25,2±5,0 p<0,001 | 29,1±4,4 vs 27,7±5,2 p<0,001 | |
| Паритет родов, абс.(%) I II III >III | 347 (71,4) 122 (25,1) 17 (3,5) 0 | 431 (81,0) 74 (13,9) 25 (4,7) 2 (0,4) | 333 (63,4) 166 (31,6) 18 (3,4) 8 (1,5) | * 0,03; ** 0,0000; *** 0,007 |
| ИМТ, M±SD кг/м² | 23,7± 4,1 | 23,8±5,0 | 22,7± 3,7 | * NS; ** p<0,05; *** p<0,05 |
| Заболевания эндокринной системы: нарушение жирового обмена, абс.(%) | 15 (3,1) 5 (1,0) | 22 (4,2) 12(2,3) | 60 (11,4) 17 (3,2) | * 0,37; ** 0,000;*** 0,000 * 0,13; **0,3; *** 0,02 |
| Анемия, абс.(%) | 113(23,3) | 173(32,5) | 195(37,1) | * 0,001; ** 0,1; *** 0,000 |
| Заболевания системы органов дыхания, абс.(%) | 22 (4,5) | 30 (6,4) | 76 (14,5) | * NS; ** 0,000; *** 0,000 |
| Заболевания желудочно-кишечного тракта, абс.(%) | 29 (6,0) | 50 (9,4) | 99 (18,9) | * 0,04; ** 0,000; *** 0,000 |
| Заболевания мочевыделительной системы, абс.(%) | 95 (19,3) | 77 (14,5) | 45 (8,6) | *0,03; **0,003; ***0,000 |
| Преэклампсия, абс.(%) | | 30(5,6) | 50(9,5) | **0,04 |
Примечание: * - достоверность различий между группами 1995 и 2000 гг, **- между 2000 и 2008 гг, *** - между 1995 и 2008гг., ИМТ – индекс массы тела
Ухудшение соматического статуса беременных за период наблюдения ассоциируется с увеличением частоты осложнений беременности, в частности, с ростом распространенности ПЭ.
Полученные нами результаты согласуются с динамикой показателей заболеваемости беременных по России за последние десятилетия [Суханова Л.П. и соавт., 2007]. Рост соматической патологии, в определенной степени закономерный в условиях увеличения возраста беременных, сопровождается нарастанием акушерской и перинатальной заболеваемости. Становится очевидной необходимость принятия мер по борьбе с патологией гестационного периода, ряда профилактических программ для молодых женщин на этапе планирования беременности.
Фаза II. В проспективном исследовании изменений структурно-функциональных показателей сердечно-сосудистой системы и метаболического статуса в гестационный период у пациенток с различными формами АГ участвовали 519 женщин в возрасте от 18 до 42 лет (Таблица 1). Возраст и антропометрические данные группы женщин с физиологически протекающей беременностью (ФБ) и группы практически здоровых небеременных женщин достоверных статистических различий не имели. Возраст и ИМТ исходно в группе ГАГ также были сопоставимы с данными у женщин с ФБ. В группе ГБ, симптоматической АГ, ПЭ и ХАГ+ПЭ пациентки были старше по возрасту, ИМТ исходно у них был повышен. В группе ПЭ доля первородящих женщин была наибольшей. В группах ХАГ и ХАГ+ПЭ отмечалось достоверно большее число женщин, имевших на момент исследования вторую и последующие беременности. Отягощенная наследственность по АГ максимально часто встречалась у беременных с ГБ (37%). В группе ФБ и практически здоровых небеременных женщин наследственная предрасположенность по АГ отмечалась только у 4% и 6% участниц исследования, соответственно. Течение беременности пациенток с ГБ осложнилось развитием ПЭ у 68 (32%) женщин. В группе пациенток ХАГ и хроническим пиелонефритом, ПЭ была диагностирована у 46 (52,3%) беременных. Ни у одной пациентки с ХАГ не проводилась постоянная антигипертензивная терапия, нерегулярно применяли различные антигипертензивные препараты 28% женщин.
Динамика показателей суточного профиля АД при различных формах АГ представлена в Таблице 6. При неосложненном течении беременности у пациенток с ГБ регистрировался повышенный уровень АД и его вариабельность на протяжении всего гестационного периода. Динамика суточного профиля АД у пациенток с ГБ и при ФБ была одинаковой, к концу беременности наблюдалось повышение АД приблизительно на 7-8/4-5 мм рт.ст., перепад АД день-ночь снижался на 4/4%. При ФБ у женщин регистрировалось пониженное АД в сравнении с небеременными. При ХАГ в сочетании с хроническим пиелонефритом нарушения суточного ритма АД отмечались на протяжении всей беременности, к ее концу отмечалось повышение только диастолическое АД. Клиническому развитию ГАГ предшествовали: с первого триместра - повышение уровня диастолического АД, со второго - увеличение перепада давления день-ночь и вариабельности АД. Развитие ПЭ и у беременных с исходно нормальным уровнем АД, и у пациенток с ХАГ ассоциировалось со снижением перепада давления день-ночь и повышением вариабельности АД. Каждый из этих факторов участвует в формировании поражения органов-мишеней и повышает риск сердечно-сосудистых осложнений у пациентов с АГ [Verdecchia, 1999; Staessen J.A., 2001, Cuspidi C., 2008; Garcia-Ortiz L., 2009].
Снижение перепада уровня дневного и ночного АД (СИ<10%) во II триместре у всех беременных (с исходно нормальными цифрами АД и с ХАГ) увеличивало риск развития ПЭ в 2,1 раза (ОР=2,1; ДИ95%: 1,16-2,6, Р=0,001). В группе женщин-нормотоников наличие нарушенного суточного ритма АД с СИ<10% во II триместре повышало риск развития ПЭ в 3,3 раза (ОР=3,3; ДИ95%:1,02-10,3; Р=0,001). Чувствительность этого признака составила 80%, специфичность – 64%.
Таблица 6
ДИНАМИКА ПОКАЗАТЕЛЕЙ СУТОЧНОГО ПРОФИЛЯ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ
В ГРУППАХ СРАВНЕНИЯ (M±SD)
| Триместр | Показатель | Практически здоровые небеременные N=50 | ФБ N=50 | ХАГ N=146 | Хронический пиелонефрит и АГ N=42 | ХАГ + ПЭ N=114 | Гестационная АГ N=56 | ПЭ N=61 |
| I | АДкл.сист., мм рт.ст. АДкл.диаст., мм рт.ст. | 112,5±9,3** P=0,008 73,9±8,1*** P=0,0002 | 104,1±9,1 64,7±5,6 | 131,5±12,0*** 80,7±9,9*** | 124,5±14,4*** 75,9±10,7*** | 128,3±13,0*** 78,1±7,7*** | 106,7±10,0 66,3±9,2 | 115,4±11,1*** 72,1±7,9*** |
| АДсут.сист., мм рт.ст. | 103,3±8,8** P=0,01 | 96,1±7,4 | 113,5±8,4*** | 107,9±15,7*** | 114,5±12,7*** | 96,3±4,9 | 105,6±8,4 | |
| АДсут.диаст., мм рт.ст. | 70,1±5,0*** P=0,0000 | 57,9±4,9 | 68,7±7,9*** | 67,5±8,8*** | 68,8±8,0*** | 63,3±3,6*** | 60,9±4,8 | |
| STD сут.сист., мм рт.ст. | 12,1±1,6 P=0,4 | 12,8±1,9 | 15,0±2,8*** | 13,5±4,0 | 12,6±2,4 | 12,9±1,7 | 13,3±1,7 | |
| STD сут.диаст., мм рт.ст. | 10,6±1,4 P=0,5 | 11,1±1,7 | 12,7±2,1*** | 11,2±2,5 | 12,5±2,9 | 11,5±1,9 | 11,7±1,9 | |
| СИ сист., % | 14,1±4,8 | 14,2±5,3 | 14,2±6,8 | 11,8±7,0** | 10,3±5,6* | 12,6±4,5 | 13,2±3,7* | |
| СИ диаст., % | 18,7±8,5 | 19,7±6,3 | 18,1±8,4 | 14,1±7,1** | 12,3±7,6*** | 19,7±6,3 | 12,1±4,5** | |
| ВИсут.сист., % | 1,6±4,0** | 0,5±1,1 | 8,4±11,0*** | 9,8±18,1*** | 8,9±5,0*** | 0,4±0,9 | 1,7±1,9 | |
| ВИсут.диаст., % | 2,3±2,9** | 1,5±1,9 | 11,1±13,0*** | 8,8±15,4*** | 9,1±4,8*** | 2,8±3,1 | 2,8±4,1 | |
| II | АДкл.сист., мм рт.ст. АДкл.диаст., мм рт.ст. | | 103,0±8,4 60,1±5,4 | 134,9±10,0***,ʱ 80,3±8,7*** | 119,9±9,0***,ʱ 71,2±10,7***, ʱ | 133,8±10,1*** 81,4±9,0***,ʱ | 109,9±9,9 68,2±9,8* | 106,2±10,0 ʱ 70,1±8,9**, ʱ |
| АДсут.сист., мм рт.ст. | | 98,7±7,2 | 116,1±9,1***, ʱ | 105,9±7,2*** | 113,9±10,4*** | 99,0±7,4, ʱ | 111,3±7,9**,ʱ |
Таблица 6 (продолжение)
| | АДсут.диаст., мм рт.ст. | | 58,5±6,3 | 68,9±7,4*** | 66,8±6,7***, ʱ | 69,7±6,6*** | 60,9±7,2 ʱ | 65,5±5,2**,ʱ |
| STD сут.сист., мм рт.ст. | | 14,0±2,4 | 14,1±3,7 | 13,2±2,7 | 14,1±2,6 | 13,4±1,9 | 14,3±2,4ʱ | |
| STD сут.диаст., мм рт.ст. | | 11,4±1,8 | 12,1±3,1 | 11,7±3,1 | 12,5±3,0 | 11,4±2,1 | 12,6±2,4ʱ | |
| СИ сист., % | | 16,0±5,5 | 13,7±6,7 | 11,9±6,8* | 11,6±7,3** | 16,3±3,4 | 8,9±6,4**, ʱ | |
| СИ диаст., % | | 19,6±6,8 | 18,4±9,5 | 14,5±7,4* | 15,0±9,1** | 19,9±4,5 | 11,1±5,8**,ʱ | |
| ВИсут.сист., % | | 1,2±2,0 | 9,3±11,5*** | 3,3±2,5* | 9,6±15,4** | 1,0±2,9 | 7,5±8,1*** | |
| ВИсут.диаст., % | | 1,5±1,8 | 7,4±10,2*** | 6,2±10,6* | 9,8±13,3*** | 3,3±4,8 | 14,2±12,4*** | |
| III | АДкл.сист., мм рт.ст. АДкл.диаст., мм рт.ст. | | 109,8±7,9ʱ,# 66,8±6,3# | 136,6±11,6***, ʱ 81,9±9,6*** | 126,7±10,2***, ʱ,# 75,6±10,0***,# | 142,1±10,3***, ʱ,# 86,6±9,8***, ʱ,# | 128,9±10,1***, ʱ,# 71,2±10,0***, ʱ | 134,0±9,2***,ʱ,# 86,7±5,8***, ʱ,# |
| АДсут.сист., мм рт.ст. | | 101,2±6,5ʱ | 118,6±9,9***, ʱ | 105,7±6,8 | 124,8±14,6***, ʱ,# | 101,9±7,8, ʱ | 119,9±9,7***, ʱ,# | |
| АДсут.диаст., мм рт.ст. | | 62,2±8,1, ʱ,# | 72,5±6,9***, ʱ,# | 68,8±6,4*, ʱ,# | 77,8±9,7***, ʱ, # | 67,7±5,9**, ʱ,# | 71,4±5,2**, ʱ, # | |
| STD сут.сист., мм рт.ст. | | 12,2±2,3 | 13,2±2,5 | 13,0±2,4 | 15,1±3,4** | 12,7±1,7 | 12,4±1,7 | |
| STD сут.диаст., мм рт.ст. | | 11,1±1,8 | 11,2±2,0 | 12,4±2,1 | 13,2±2,4** | 11,4±1,5 | 13,0±2,4 | |
| СИ сист., % | | 10,7±5,8ʱ | 10,4±6,7ʱ | 11,0±2,8 | 9,8±7,1ʱ | 12,2±5,0ʱ | 8,2±3,5ʱ | |
| СИ диаст., % | | 16,0±7,1ʱ | 14,3±7,5ʱ | 16,1±5,3 | 11,9±8,5ʱ | 14,9±6,1ʱ | 9,2±5,6**, ʱ | |
| ВИсут.сист., % | | 1,4±0,8 | 11,3±10,8*** | 1,2±1,9 | 23,8±7,4*** | 1,1±2,0 | 17,2±9,5 | |
| ВИсут.диаст., % | | 2,4±4,1 | 8,6±8,9*** | 6,1±7,6 | 20,3±7,1** | 4,5±3,5* | 15,2±5,4*** |
Примечание: *- p<0,05, **- p<0,01, ***- p<0,001 в сравнении с группой беременных с физиологическим течением гестационного периода,
ʱ - p<0,05 в сравнении с I триместром , # - p<0,05 в сравнении со II триместром
Сочетание двух факторов - АД диастолического суточного > 60 мм рт.ст. + СИ<10% - увеличивало риск развития ПЭ в 7,4 раза (ОР=7,4 (ДИ95%:4,8-9,2, Р=0,0005). Чувствительность признака составила 75%, специфичность – 96%. Относительный риск развития ПЭ у беременных с ХАГ при СИ<10% в I триместре повышался в 4 раза (ОР=4,0; ДИ95%: 1,3-13,1, Р=0,01). Не вызывает сомнений, что для ранней диагностики ПЭ у беременных с ХАГ должен быть использован комплексный (клинико-лабораторный и инструментальный) подход, при котором показатели суточного профиля АД в первой половине беременности могут иметь решающее значение.
У беременных с ХАГ во всех группах с начала беременности отмечались повышенные показатели ИММЛЖ сердца и при неосложненной гестации, также как и при ФБ, статистически значимо не менялись (Таблица 7). У беременных с ГАГ также не отмечалось статистически значимого увеличения ИММЛЖ к началу третьего триместра. В этих группах сохранялся гиперкинетический тип кровообращения. Показатели насосной функции миокарда были сохранены, в группе ГБ в III триместре показатели УИ были наибольшими. Нарушение адаптационных механизмов, с развитием гипокинетического кровообращения, снижение сердечного и ударного индексов отмечалось при ХАГ в сочетании с хроническим пиелонефритом. Для этой группы характерно отсутствие необходимой вазодилатиции и исходно повышенные показатели ММЛЖ. В группах ПЭ и ХАГ+ПЭ отмечалось статистически значимое увеличение ИММЛЖ к началу третьего триместра. При неосложненном течении беременности у пациенток с ГБ показатели ОПСС были аналогичны показателям при ФБ. При ГАГ не было отмечено достоверного повышения ОПСС. При сочетании ХАГ и хронического пиелонефрита на протяжении всей беременности показатели ОПСС оставались одинаково повышенными. Развитию ПЭ и в группе женщин-нормотоников, и у пациенток с ХАГ предшествовало повышение ОПСС с первого триместра беременности. Признаки ремоделирования миокарда ЛЖ (ОТС > 0,37, критерии Vassopolo B., 2008) в начале III
Таблица 7
Динамика показателей ЭхоКГ у пациенток в группах сравнения (M±m)
| Триместр | Показатель | ФБ | ХАГ | Хронический пиелонефрит и АГ | ХАГ + ПЭ | Гестационная АГ | ПЭ |
| I триместр | ТЗСЛЖ, см | 0,66±0,01 | 0,88±0,05*** | 0,75±0,02*** | 0,75±0,02*** | 0,7±0,01* | 0,74±002*** |
| ТМЖП, см | 0,67±0,01 | 0,88±0,06*** | 0,77±0,01*** | 0,79±0,01*** | 0,72±0,01* | 0,77±0,01** | |
| ФВ, % | 62,5±0,48 | 63,9±1,5 | 62±0,4 | 62±0,5 | 62,7±0,4 | 62,7±0,6 | |
| СИ, л/мин*м² | 3,4±0,4 | 3,15±0,5 | 3,02±0,05 | 3,23±0,2 | 3,46±0,2 | 3,17±0,15 | |
| УИ, мл/м² | 44,6±3,2 | 39,2±3,7 | 37,7±0,2** | 40,2±1,6 | 40,95±1,6 | 37,2±0,6** | |
| ММЛЖ, г | 102,3±7,2 | 160,7±8,8** | 127,8±5,8** | 136,8±5,4** | 113,8±6,9 | 121,7±7,9 | |
| ИММЛЖ, г/м² | 63,3±3,7 | 87,4±5,9** | 74,8±2,5** | 78,9±2,1** | 66,9±2,8 | 71,5±4,1 | |
| ОПСС, дин*с*смˉ5 | 1109,7±67,2 | 1305,2±81,8 | 1349,4±74,9* | 1289,8±69,7 Т | 1115,3±90,7 | 1316,1±92,9Т | |
| I I триместр | ТЗСЛЖ, см | 0,68±0,01 | 0,92±0,1*** | 0,76±0,03** | 0,81±0,05** | 0,72±0,02 | 0,7±0,03 |
| ТМЖП, см | 0,68±0,01 | 0,94±0,13*** | 0,79±0,04** | 0,83±0,04** | 0,74±0,02Т | 0,7±0,03 | |
| ФВ, % | 62,75±0,4 | 63±1,09 | 62,8±0,4 | 64,13±0,8 | 62,4±0,6 | 64,5±0,9 | |
| СИ, л/мин*м² | 3,6±0,3 | 3,5±0,2 | 2,76±0,07 | 3,3±0,26 | 3,47±0,09 | 3,62±0,1 | |
| УИ, мл/м² | 45,3±4,2 | 52,9±3,1 | 41,6±3,3 | 42,4±2,1 | 43,0±2,5 | 39,9±2,9 | |
| ММЛЖ, г | 105,4±8 | 169,6±9,2** | 133,76±8,4** | 147,6±15,6** | 125,2±8,6** | 105,2±6,9 | |
| ИММЛЖ, г/м² | 64,6±2,9 | 92,4±4,9** | 71,6±1,5** | 80,5±7,3** | 74,7±3,7* | 62,6±7,5 | |
| ОПСС, дин*с*смˉ5 | 1134,4±47 | 1282,9±70 | 1431,6±98,3* | 1404,9±80,1** | 1218,7±96,2 | 1464,7±89** | |
| III триместр | ТЗСЛЖ, см | 0,75±0,02 | 0,86±0,05* | 0,77±0,01 | 0,84±0,02** | 0,75±0,02 | 0,78±0,02 |
| ТМЖП, см | 0,75±0,02 | 0,85±0,05* | 0,7±0,01 | 0,88±0,02** | 0,77±0,02 | 0,8±0,01* | |
| ФВ, % | 62,4±0,4 | 65,4±1,1* | 61,0±0,5 | 64,5±1,0* | 62,6±0,4 | 63,3±0,6 | |
| СИ, л/мин*м² | 3,19±0,15 | 3,67±0,3 | 2,87±0,3* | 3,36±0,1 | 3,2±0,1 | 3,06±0,1 | |
| УИ, мл/м² | 39,45±0,9 | 45,0±2,5** | 34,0±2,1** | 41,9±2,1 | 38,1±1,5 | 37,9±0,2 | |
| ММЛЖ, г | 123,4±9,4 | 164,2±9*** | 129,8±5,6* | 167,4±9,4** | 125,6±6,3 | 140,9±1,6**,ʱ | |
| ИММЛЖ, г/м² | 69,9±4,1 | 89,0±5,2** | 72,5±0,9* | 93,4±6,8** | 72,6±3,1 | 81,9±2,9**,ʱ | |
| ОПСС, дин*с*смˉ5 | 1162,5±50,9 | 1304,9±97,8 | 1429,8±94* | 1463,9±70,0** | 1240,5±84 | 1449,9±79,1** |
Примечание: ФБ – физиологически протекающая беременность, *- p<0,05, **- p<0,01, ***- p<0,001 в сравнении с группой беременных с физиологическим течением гестационного периода , ʱ - p<0,05 в сравнении с данными I триместра, Т – тенденция отличий показателей.
триместра развились у 27% беременных с ПЭ, у 32% при сочетанной патологии ХАГ и ПЭ, а также у 28% женщин с АГ и хроническим пиелонефритом. В группе ГАГ признаки ремоделирования миокарда были выявлены у 7% беременных. В группе беременных с ГБ статистически значимого изменения структуры ЛЖ за период беременности не наблюдалось, однако признаки нарушения нормальной геометрии сердца выявлялись исходно у 42%, что свидетельствует о тяжести течения гипертензивного синдрома у данной категории пациенток. При ФБ геометрия ЛЖ была нормальной у всех женщин. Таким образом, развитию ПЭ предшествуют структурные изменения миокарда ЛЖ, формирующиеся в достаточно короткое время, ограниченное гестационным периодом. Данные о высокой распространенности ремоделирования миокарда, признанного в настоящее время одним из наиболее важных маркеров развития сердечно-сосудистых осложнений и смертности, подтверждают необходимость проведения активной антигипертензивной терапии более, чем у 40% беременных с ГБ и у всех беременных в случае развития ПЭ.
Метаболический статус у беременных с различными формами АГ характеризовался нарушениями жирового, липидного и пуринового обменов. Исходные данные ИМТ пациенток с ХАГ статистически значимо были повышенными (таблица 1). Беременные в группе ПЭ также имели повышенный ИМТ. В группе ГАГ исходные данные ИМТ статистически не отличались от таковых при ФБ, однако доля пациенток с избыточной массой тела в этой группе была статистически значимо больше: 19,6% против 6%, p<0,05. На рис.2 представлены частота избыточной массы тела и ожирения в группах наблюдения исходно. Динамика прибавки веса в группах сравнения к началу III триместра была приблизительно одинаковой и составила от 11 до 16%, в среднем 7-10 кг.
Исходные показатели ИМТ при ФБ были взаимосвязаны с уровнем суточного АД (NS/r=0,45). Прибавка ИМТ к III триместру коррелировала с повышением суточного АД (r=0,6/r=0,4). При ХАГ при неосложненном
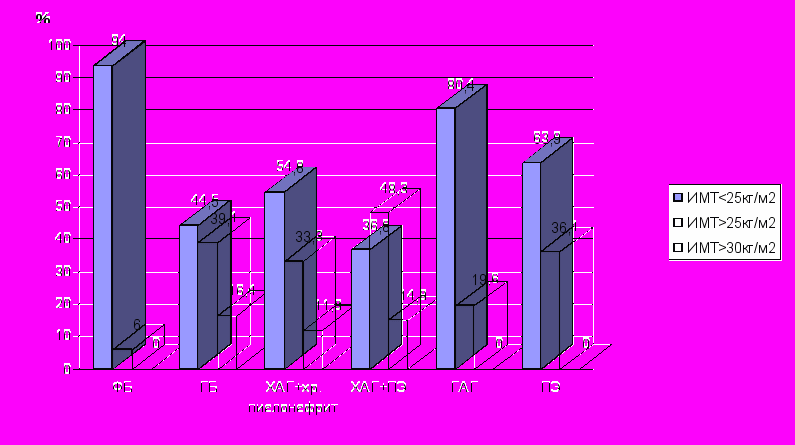
Рис.2 Частота нарушений жирового обмена в группах сравнения
течении беременности также были выявлены аналогичные взаимосвязи: исходно показатели ИМТ коррелировали с суточным АД (r=0,63/r=0,42), прибавка ИМТ к III триместру была тесно взаимосвязана с повышением АД (r=0,78/r=0,64). В группах ПЭ эти взаимосвязи были нарушены.
Нарушение жирового обмена неблагоприятно влияет на течение беременности. Относительный риск развития ПЭ у женщин с исходно нормальным уровнем АД и избыточной массой тела был увеличен в 6 раз: ОР=6,0; ДИ95%: 1,9-24,7; P=0,001.
Во всех исследуемых группах было отмечено повышение уровня ОХС и ТГ в сыворотке крови от первого триместра к началу третьего без значимых
межгрупповых отличий (Таблица 8). В группе с ХАГ при неосложненном течении беременности исходно в I триместре отмечались повышенные показатели ОХС. Уровень глюкозы крови натощак в группах сравнения на протяжении всей беременности был в пределах референтных значений. Уровень мочевой кислоты в группе ФБ повышался к началу III триместра на 23% (NS). У беременных с ГБ при неосложненном течении беременности повышение уровня мочевой кислоты составило 30% (p<0,05). В группе
Таблица 8
Динамика показателей липидного, углеводного обмена и уровня мочевой кислоты в группах сравнения (M±m)
| Триместр | Показатель | ФБ N=50 | ХАГ N=146 | Хронический пиелонефрит и АГ N=42 | ХАГ + ПЭ N=114 | Гестационная АГ N=56 | ПЭ N=61 |
| I | ОХС, ммоль/л | 4,3±0,2 | 4,9±0,2* | 4,6±0,3 | 4,9±0,4 | 4,2±0,2 | 4,9±0,4 |
| ТГ, ммоль/л | 0,91±0,09 | 0,82±0,06 | 0,73±0,1 | 0,68±0,2 | 0,72±0,01 | 0,71±0,01 | |
| ЛПНП, ммоль/л | 2,3±0,2 | 2,4±0,3 | 2,5±0,4 | 2,7±0,4 | 2,4±0,4 | 2,7±0,3 | |
| ЛПВП, ммоль/л | 1,3±0,09 | 1,5±0,1 | 1,5±0,08 | 1,6±0,2 | 1,6±0,1 | 1,6±0,2 | |
| Глюкоза, ммоль/л | 4,2±0,1 | 4,2±0,2 | 4,0±0,1 | 3,9±0,3 | 4,3±0,2 | 4,4±0,2 | |
| Мочевая кислота, мкмоль/л | 162,1±10,1 | 193,3±21,0 | 198,6±18,9 | 242,7±13,0** | 196,8±22,4 | 169,8±17,3 | |
| II | ОХС, ммоль/л | 5,4±0,3 | 5,9±0,3 | 5,4±0,4 | 6,5±0,4 | 5,8±0,3 | 6,0±0,4 |
| ТГ, ммоль/л | 1,2±0,1 | 1,3±0,2 | 1,3±0,3 | 1,3±0,2 | 1,4±0,1 | 1,8±0,4 | |
| ЛПНП, ммоль/л | 2,4±0,5 | 3,9±0,6* | 3,0±0,6 | 3,2±0,1 | 3,1±0,6 | 3,0±0,3 | |
| ЛПВП, ммоль/л | 1,5±0,1 | 1,8±0,2 | 1,5±0,2 | 1,6±0,08 | 1,5±0,1 | 1,4±0,2 | |
| Глюкоза, ммоль/л | 3,8±0,2 | 4,6±0,4 | 3,9±0,3 | 4,1±0,3 | 4,0±0,4 | 3,8±0,1 | |
| Мочевая кислота, мкмоль/л | 234,8±12,9 | 256,5±18,8 | 267,0±18,9 | 232,9±12,8 | 231±16,3 | 269,9±19,4 | |
| III | ОХС, ммоль/л | 6,2±0,2# | 7,0±0,3# | 6,6±0,4# | 6,8±0,4# | 6,5±0,4# | 6,9±0,4# |
| ТГ, ммоль/л | 2,2±0,5# | 2,4±0,4# | 2,3±0,3# | 2,6±0,2# | 2,4±0,3# | 2,5±0,3# | |
| ЛПНП, ммоль/л | 3,2±0,5 | 4,0±0,9 | 3,8±0,7 | 4,1±0,6# | 4,0±0,4# | 4,1±0,3# | |
| ЛПВП, ммоль/л | 1,8±0,1# | 1,9±0,1# | 1,42±0,09 | 2,1±0,4 | 1,8±0.1 | 1,6±0,2 | |
| Глюкоза, ммоль/л | 4,0±0,2 | 4,3±0,2 | 3,6±0,1# | 3,9±0,02 | 4,1±0,3 | 3,6±0,2# | |
| Мочевая кислота, мкмоль/л | 198,7±21,7 | 249,8±12*,# | 243,3±16,3 | 269,7±13,3** | 199,0±15,2 | 274,9±12,0***,# |
Примечание: *- p<0,05, **- p<0,01, ***- p<0,001 в сравнении с группой беременных с физиологическим течением гестационного периода, # - статистически значимые изменения показателей в сравнении с аналогичными данными I триместра
ХАГ+ПЭ повышенный уровень мочевой кислоты отмечался с I триместра, его увеличение к III триместру составило 12% (NS). В группе ПЭ увеличение уровня мочевой кислоты в сравнении с исходными данными было максимальным – 62%, p<0,001. Изменений уровня мочевой кислоты в группах ХАГ в сочетании с хроническим пиелонефритом и ГАГ не было.
В основной группе пациенток с ХАГ (ГБ, n= 214, и АГ у беременных с хроническим пиелонефритом, n=88) течение беременности осложнилось развитием ПЭ у 68 (32%) пациенток с ГБ и у 46 (52,3%) женщин с сопутствующей патологией почек. Из числа включенных в исследование пациенток ГАГ трансформировалась в ПЭ в 52% случаев.
В группе ФБ у всех женщин роды были срочными, протекали без осложнений и закончились рождением живых доношенных детей, масса новорожденных составила: Ме 3453 г (25%;75%: 3220-3650 г); рост - Ме 51,0см (25%;75%: 50,5 - 52,0 см).
При неосложненном течении беременности у пациенток с ГБ у 27 (18%) женщин отмечались признаки плацентарной недостаточности и у 25 (17%) синдром задержки развития плода. Преждевременные роды наступили у 5(3,5%) беременных. Беременность закончилась срочными родами в 96,5% случаев, оперативными – в 25%. Антенатальная гибель плода произошла в 8 случаях. Антропометрические показатели живых рожденных детей статистически значимо не отличались от аналогичных показателей группы ФБ. Вес новорожденных составил: Ме 3369 г (25%;75%: 3280-3440 г), длина тела - Ме 52,0 см (25%;75%: 50,8-52,5 см). Выделение двух подгрупп в зависимости от уровня среднесуточного АД в I триместре позволило выявить отличия. У беременных с ГБ и уровнем АД выше среднего по группе в сравнении с оставшимися пациентками вес новорожденных статистически значимо был ниже и составил 2936±190 г против 3412±74 г, p<0,001.
Признаки плацентарной недостаточности наиболее часто выявлялись у пациенток с АГ в сочетании с хроническим пиелонефритом (41%) и у женщин в группе ПЭ (38%). Синдром задержки развития плода был отмечен в этих группах в 31% и 34% случаев, соответственно. В группе АГ в сочетании с хроническим пиелонефритом два плода погибли антенатально. У пациенток с ПЭ все дети были рождены живыми. Вес новорожденных живых детей в этих группах был статистически значимо ниже в сравнении с данными группы ФБ: Ме (25%; 75%) 3070 г (2750; 3220) и 3149 г (3000; 3280) против 3453 г (3220; 3650), p<0,01, p< 0,05, соответственно.
В группе ХАГ, осложнившейся развитием ПЭ во второй половине беременности, отмечалась тенденция снижения веса плода: Ме(25%; 75%) - 3202 (3080; 3340). Мертворожденных в этой группе было трое. Оперативные роды были выполнены в 22% случаев.
В группе ГАГ проведение кесарева сечения потребовалось в 19,6% случаев. Все дети были рождены живыми. Антропометрические показатели новорожденных не отличались от показателей в группе ФБ.
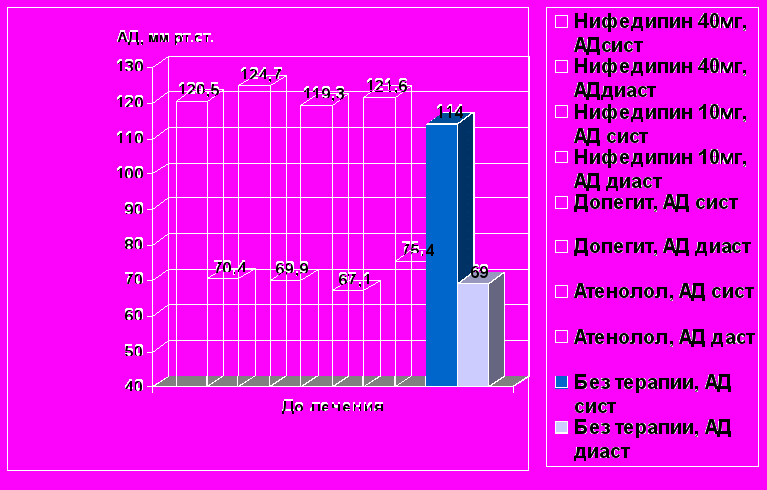
Фаза III. Исследование клинических эффектов антигипертензивных препаратов при ХАГ у беременных проводили в четырех группах: I – нифедипин 40мг, пролонгированная форма, II – нифедипин 10мг, короткодействующий, III – допегит, IV- атенолол в сравнении с группой (V) пациенток, не получавших медикаментозной терапии. Уровень офисного АД на 22-24 неделях беременности до начала терапии в I, II, III и IV группах составил 154,5±2,2/89,9±1,0 мм рт. ст., 149,7±2,1/90,9±1,6 мм рт. ст., 149,9±2,0/91,3±1,4 мм рт. ст. и 154,4±1,9/90,4±1,1 мм рт. ст., соответственно, и достоверно не отличался. В группе сравнения уровень офисного систолического АД был ниже – 142,1±1,8/87,9±1,7 мм рт. ст. (p < 0,001/NS).
Показатели среднего за сутки АД во всех группах достоверно не отличались (рис.3). Эффективность проводимой терапии оценивали на основании показателей офисного АД. Критерием эффективности считали снижение уровня клинического АД ниже 140/90 мм рт.ст. Данные среднесуточных величин АД сопоставлялись с показателями АД в группах сравнения в аналогичные сроки беременности. При повторном обследовании пациенток на 32-34-й неделях уровень среднего за сутки АД в группах статистически значимо не отличался (рис. 4).