Разработка технологий минимизации техногенного воздействия на окружающую среду предприятий по добыче и переработке рудного золота
| Вид материала | Автореферат |
| Разработка метода гальванохимического окисления трудноокисляемых органических загрязнителей сточных вод |
- Горнорудный комплекс как основной фактор техногенного воздействия на окружающую среду, 175.33kb.
- Доклад заместителя министра, 39.11kb.
- Областной экологический конкурс «эко-предприятие 2011» (далее − Конкурс) проводится, 53.78kb.
- Общие требования в области охраны окружающей среды при эксплуатации предприятий, 375.47kb.
- «Экологическое воздействие производственных процессов на окружающую среду», 44.68kb.
- «Воздействие техносферы на окружающую среду», 66.84kb.
- Предупреждение хищений и незаконного оборота золота при его добыче и переработке, 307.41kb.
- Справка о результатах деятельности ОАО «Новолипецкий металлургический комбинат», 30.79kb.
- Третья нефтегазовая конференция «экобезопасность 2012», 209.68kb.
- Вторая нефтегазовая конференция «экобезопасность 2011», 135.77kb.
Установлено, что проведение AVR-процесса в центробежно-барботажных аппаратах сопровождается не только практически полным регенеративным извлечением цианистого натрия из отработанных растворов цианирования и осаждением металлов в виде нерастворимых соединений, но и частичным окислением тиоцианатов с образованием дополнительного количества HCN. При этом количество тиоцианатов, выведенное из растворов за счет окисления и осаждения в виде CuSCN, зависит от рН, концентрации цианидов меди и тиосульфатов. Вместе с тем, результаты нашего исследования и анализ имеющихся в литературе сведений позволяют предложить механизм, в соответствии с которым конверсия тиоцианатов в ЦБА происходит как за счет окисления кислородом воздуха в присутствии меди и тиосульфатов, так и через образование тиоциана.
Однако необходимо отметить, что AVR-процесс не позволяет добиться снижения концентрации цианидов до норм ПДК. Помимо этого из растворов лишь частично извлекаются тиоцианаты, что требует проведения заключительной стадии обезвреживания, которая может быть осуществлена одним из окислительных методов.
- Разработанные комбинированные методы каталитической деструкции с использованием экологически чистых окислителей (пероксида водорода и кислорода воздуха) позволяют реализовать эффективное окисление токсичных органических загрязнителей оборотных и сточных вод вплоть до полной их минерализации, а также – процесс «деструкция – регенерация»: окисление тиоцианатов с выделением из раствора цианистого водорода и дальнейшим поглощением его щелочами.
В последние годы стремительно развивается новое направление исследований, связанное с комбинированными окислительными процессами, получившими название АОР (Advanced Oxidation Processes), суть которых заключается в жидкофазном цепном окислении примесей генерированными высокореакционными частицами – формами активированного кислорода, в первую очередь ОН-радикалами. Особую роль при этом занимают соединения железа, играющие роль катализатора разложения пероксида водорода (ПВ). Комбинированные методы потенциально являются экологически более чистыми, т.к. при их использовании принципиально возможна полная минерализация трудноокисляемых поллютантов.
Практика показывает, что окислительная деструкция загрязнителей до нетоксичных веществ оправданна лишь при глубокой доочистке воды после выделения основной массы загрязняющих веществ на предварительных стадиях обработки реагентными или регенерационными методами. В связи с этим заслуживают внимания исследования по разработке способов очистки сточных вод, в которых в одном устройстве одновременно могут протекать несколько физико-химических процессов.
Разработка метода гальванохимического окисления трудноокисляемых органических загрязнителей сточных вод
Среди комбинированных железо-пероксидных методов особое внимание заслуживает разработанный нами метод гальванохимического окисления (ГХО), основанный на самопроизвольном окислении железа, находящегося в контакте с углеродным материалом и водой, содержащей пероксид водорода. В процессе анодного растворения и/или коррозии в кислой среде металлическое железо окисляется до Fe2+ и создаются условия для протекания реакции Фентона:
Fe2+ + H2O2 → Fe3++ OH• + OH‾
Преимущества систем с использованием электрогенерированного катализатора перед классическим реагентом Фентона – снижение стоимости процесса за счет использования металлического железа вместо его солей (снижение эффекта повышения минерализации, засоления), генерирование Fe2+in situ, протекание процессов при меньших концентрациях катализатора, а также более высокие скорость деструкции и эффективность процесса.
В качестве объекта исследования были выбраны модельные растворы фенола - наиболее изученного и трудноокисляемого компонента сточных вод. Фенол является токсичным поллютантом (ПДКр.-хоз. – 0.001 мг/л) и может также рассматриваться как модельный (тестовый) объект для изучения закономерностей окисления других фенолов и токсичных органических соединений, в т.ч. флотореагентов и флокулянтов.
Величина рН является ключевым регулируемым параметром в процессе обработки сточных вод. При ГХО оптимальные условия для каталитического окисления органических примесей кислородом воздуха и ПВ в присутствии соединений железа реализуются в диапазоне рН 3-4 (кривые 1-2, рис. 4а), при этом процесс окисления протекает достаточно быстро и основное снижение концентрации субстрата наблюдается в первые минуты процесса. При значениях рН обрабатываемой воды более 4.5 (кривые 3-5, рис. 4а и 4б) процесс деструкции замедляется, что объясняется влиянием кислотности среды на скорость разложения ПВ и изменением каталитических свойств ионов железа вследствие агрегации и полимеризации с образованием труднорастворимых гидроксосоединений.
а б
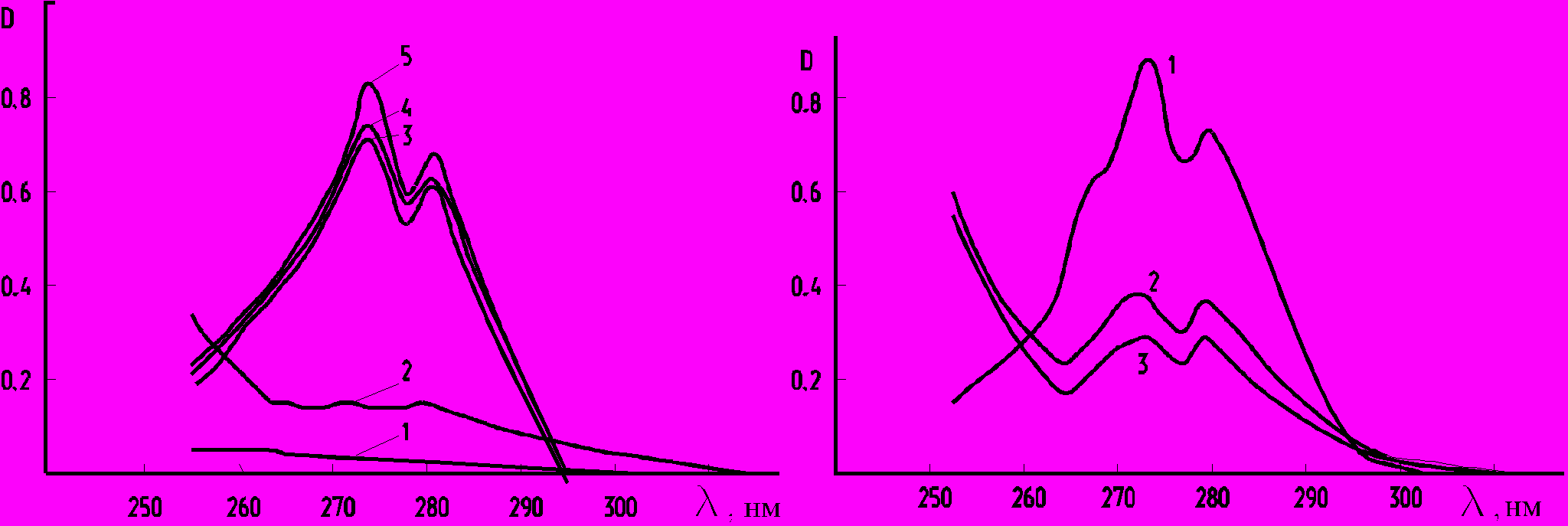
Рис.4. Изменение спектров поглощения фенола ([Ph]0 = 2.1310-4 моль/л) после ГХО: а) при различных значениях рН: 3.0 (1), 4.0 (2), 4.5 (3), 5.0 (4), 6.0 (5); расход окислителя – 100 % от стехиометрии ([ПВ] = 310-3 моль/л), при = 1 мин.; б) при рН = 4.0: 1 – исходный раствор; 2, 3 – при = 1 и 3 мин. , соответственно; расход окислителя – 50 % от стехиометрии.
Установлено, что в аэробных условиях вследствие активации молекулярного кислорода парой Fe2+/H2O2 реализуется сопряженный механизм окисления органических примесей. В этом случае количество ПВ, расходуемое на окисление определенного количества органического субстрата S, уменьшается. Увеличение эффективности деструкции органических соединений при ГХО, вероятно, происходит также вследствие изменения механизма окисления за счет быстрого электрохимического восстановления Fe2+ и двухэлектронного восстановления кислорода на катоде гальванопары железо-кокс, сопровождающегося синтезом дополнительного количества пероксида водорода:
Fe0 +2Fe3+ 3Fe2+
O2+2H++2eH2O2
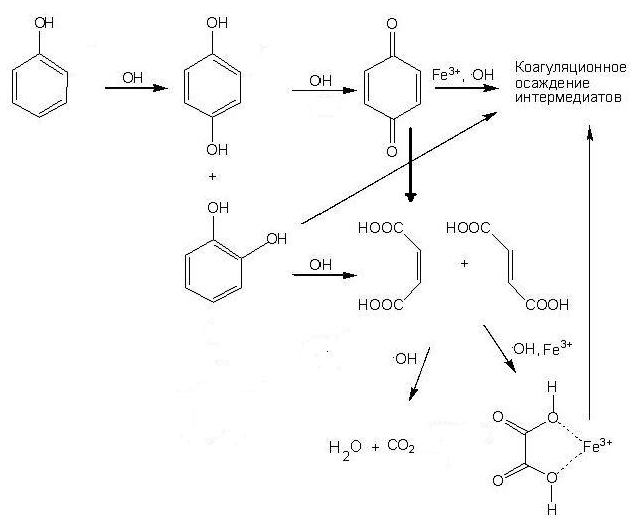
Анализ литературных и полученных нами экспериментальных данных позволяет сформулировать наиболее вероятные стадии ГХО фенола (рис.5): деструкцию собственно фенола с образованием промежуточных продуктов (двухатомных фенолов и соответствующих хинонов), которые далее окисляются до алифатических кислот (малеиновой, муравьиной и щавелевой), вплоть до полной их минерализации до СО2 и Н2О. Кроме того, поскольку в процессе образуются активные коагулянты в форме гидроксосоединений Fe3+, создаются условия для сорбционного удаления из обрабатываемой воды продуктов неполного разложения органических соединений за счет высокой хелатообразующей активности железа.
| |
| Рис.5. Возможные реакции ГХО фенола. |