Низовой Константин Александрович плоскостное сорбционное дренирование брюшной полости в сочетании с регионарной лимфотропной терапией в комплексном лечении больных с распространенным гнойным перитонитом
| Вид материала | Автореферат |
- Остеопластическая торакопластика, дополненная установкой эндобронхиального клапана,, 1378.55kb.
- Квч-терапия в комплексном лечении псориаза, 158.23kb.
- «современные технологии квч-терапии в комплексном лечении больных хроническим некалькулезным, 876.67kb.
- Электроимпульсная терапия в комплексном лечении больных мягкой артериальной гипертонией, 412.16kb.
- Лучевая терапия различными видами ионизирующего излучения в комплексном лечении больных, 785.18kb.
- На правах рукописи, 321.8kb.
- Реконструкция глубокой бедренной артерии в комплексном хирургическом лечении больных, 294.19kb.
- На правах рукописи, 856.79kb.
- Общая характеристика работы, 252.95kb.
- s ru, 98.7kb.
1 2
На правах рукописи
Низовой
Константин Александрович
ПЛОСКОСТНОЕ СОРБЦИОННОЕ ДРЕНИРОВАНИЕ БРЮШНОЙ ПОЛОСТИ В СОЧЕТАНИИ С РЕГИОНАРНОЙ ЛИМФОТРОПНОЙ ТЕРАПИЕЙ В КОМПЛЕКСНОМ ЛЕЧЕНИИ БОЛЬНЫХ С РАСПРОСТРАНЕННЫМ ГНОЙНЫМ ПЕРИТОНИТОМ
14.00.27 – хирургия
14.00.15 – патологическая анатомия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Омск – 2008
Работа выполнена в ГОУ ВПО Омской государственной медицинской академии Росздрава
Научные руководители: доктор медицинских наук, профессор
Филиппов Сергей Иванович
доктор медицинских наук, профессор
Путалова Ирина Николаевна
Официальные оппоненты: доктор медицинских наук, профессор
Возлюбленный Сергей Иванович
Департамент здравоохранения
администрации г. Омска
доктор медицинских наук, профессор
Майбородин Игорь Валентинович
Институт химической биологии
и фундаментальной медицины СО РАМН
Ведущая организация: Государственное образовательное учреждение высшего профессионального образования Новосибирский государственный медицинский университет Росздрава
Защита состоится «_____» ______________ 2008 г. в _____ часов на заседании диссертационного совета Д 208.065.01 при ГОУ ВПО Омской государственной медицинской академии по адресу: 644043, г. Омск, ул. Ленина, 12.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО Омской государственной медицинской академии Росздрава.
Автореферат разослан «____» ________________ 2008 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук,
профессор В.К. Федотов
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Распространенный гнойный перитонит (РГП) до настоящего времени сопровождается высокой летальностью от 20 до 60% (Савчук Б.Д., 1979; Буянов В.М. с соавт., 1992; Шуркалин Б.К. с соавт., 1992; Kunin N., 1991; Kronborg O., 1994; Reith H.B., 1997).
Заболевание приводит к быстрому нарастанию эндогенной интоксикации и тяжелым расстройствам гомеостаза. Особенно неблагоприятно в прогностическом отношении протекает гнойный перитонит с развитием синдрома “полиорганной недостаточности”. Фактически именно эта форма определяет высокую летальность (45 – 92,8%) при данном заболевании (Струков А.И. с соавт., 1987; Савельев В.С. с соавт., 1987; Гостищев В.К. с соавт., 2002; Christon N.V. et al., 1987).
Известно, что основным путем резорбции содержимого из брюшинной полости является лимфатическая система (Миннебаев М.М., 1984; Appantuku L.M., 1987).
Лимфатическая система является мощным антибактериальным и антитоксическим барьером, который обеспечивает иммунный контроль органов и систем организма. При развитии прогрессирующего воспалительного процесса в брюшной полости, недостаточность функций лимфатической системы, наряду с аутоинтоксикацией, является одним из основных патогенетических механизмов развития необратимых нарушений в организме.
Изучение структурно-функциональных особенностей регионарных лимфатических узлов в условиях воспаления в эксперименте позволило выявить значительное снижение их дренажной и транспортной функций, вплоть до развития полного лимфостаза (Куприянов В.В. и др., 1983; Панченков Р.Т. и др., 1984; Бородин Ю.И. и др., 1985; Шевела А.И., 1991; Майбородин И.В., 1998; Плешаков В.П., 1995).
Однако все имеющиеся в литературе сообщения об изучении структурной организации брыжеечных лимфатических узлов носят экспериментальный характер и в полной мере к человеческому организму отнесены быть не могут.
Многочисленными исследованиями доказано, что эффективность действия антибиотиков, иммуномодуляторов, ингибиторов протеаз и цитостатиков повышается при направленном введении их в лимфатическую систему (Стенгревиц А.А. и др., 1985; Левин Ю.М. и др., 1985-1987; Панченков Р.Т. и др., 1981-1986; Выренков Ю.Е. и др., 1981, 1982; Ярема И.В. и др., 1981-1983), поскольку она резорбирует из тканей метаболиты, токсины, микроорганизмы.
Применение сорбирующих веществ природного или синтетического происхождения для дренирования брюшной полости является наиболее перспективным на сегодняшний день способом санации внутренней среды организма. Механизмы дренажно-детоксикационного действия сорбентов и лимфатической системы во многом сходны. Гранулы сорбента связывают на своей поверхности за счет физико-химических свойств, вещества и токсины, поступающие из дренируемых тканей подобно тому, как это происходит в лимфатическом узле. При наличии такого временного искусственного "лимфатического узла" регионарный лимфатический аппарат испытывает меньшие нагрузки, функционирует более эффективно и подвергается меньшим структурным изменениям, т.е. достигается не только лимфокорригирующий, но и лимфопротекторный эффекты (Бородин Ю.И., 1996, Майбородин И.В., 1998).
Таким образом, состояние лимфатического региона брюшной полости во многом определяет течение РГП, а протезирование и коррекция функций лимфатической системы может значительно улучшить результаты лечения больных с РГП. В связи с этим, применение регионарной лимфотропной терапии в сочетании с плоскостным сорбционным дренированием брюшной полости в комплексном лечении больных с РГП является патогенетически обоснованным и требует дальнейшего изучения.
Цель исследования. Улучшить результаты лечения больных с распространенным гнойным перитонитом, путем применения плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией.
Задачи исследования.
Провести анализ результатов лечения больных с распространенным гнойным перитонитом при использовании традиционного метода лечения – плоскостного дренирования брюшной полости марлевыми тампонами по Н.С. Макохе.
- Изучить структурную организацию брыжеечных лимфатических узлов у больных с распространенным гнойным перитонитом до лечения и в динамике раннего послеоперационного периода при использовании марлевых тампонов для плоскостного дренирования брюшной полости.
- Разработать метод плоскостного сорбционного дренирования брюшной полости углеродным гемосорбентом ВНИИТУ-1 в сочетании с регионарной лимфотропной терапией при лечении больных с распространенным гнойным перитонитом.
- Выявить клинико-морфологические особенности дренажно-детоксикационных процессов у больных с распространенным гнойным перитонитом при применении плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией в сравнении с традиционным методом лечения.
- Используя клинико-лабораторные данные и результаты морфологического исследования брыжеечных лимфатических узлов, оценить эффективность метода плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией в комплексном лечении больных с распространенным гнойным перитонитом.
Научная новизна.
- Представленная работа является первым исследованием, в котором выявлены особенности изменений структурной организации брыжеечных лимфатических узлов у одного и того же больного с распространенным гнойным перитонитом в динамике раннего послеоперационного периода в зависимости от метода лечения.
- Впервые с позиций структурной организации регионарных лимфатических узлов показана недостаточность дренажно-детоксикационных функций лимфатического региона брюшной полости больных с распространенным гнойным перитонитом, которым производилось плоскостное дренирование брюшной полости марлевыми тампонами.
- Разработан и внедрен в клиническую практику метод плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией (патент РФ № 2306927 от 27.09.07) при лечении больных с распространенным гнойным перитонитом, позволяющий улучшить результаты лечения данной категории больных.
- Приоритетным является прижизненное клинико-морфологическое обоснование необходимости и эффективности метода плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией при лечении больных с распространенным гнойным перитонитом.
Теоретическая и практическая значимость работы.
Полученные данные о структурно-функциональной организации брыжеечных лимфатических узлов больных с распространенным гнойным перитонитом, особенностях преобразования их в зависимости от метода лечения дополняют имеющиеся представления о функциональной анатомии лимфатического региона брюшной полости и вносят определенный вклад в учение о лимфатической системе в целом.
В условиях клиники показана возможность целенаправленного воздействия на дренажную, транспортную и детоксикационную функции лимфатического региона путем применения метода плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией при лечении больных с распространенным гнойным перитонитом.
Применение метода позволило добиться снижения общей летальности и сокращения сроков стационарного лечения больных, что привело к уменьшению затрат на лечение в среднем на 3381,58 рублей на одного больного.
Внедрение результатов в практику.
Метод плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией внедрен в клиническую практику хирургического отделения МУЗ ГК БСМП №1 (644119, г. Омск, ул. Перелета, 9) при лечении больных с распространенным гнойным перитонитом.
По материалам диссертации разработаны методические рекомендации по применению метода плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией при лечении больных с распространенным гнойным перитонитом в хирургических клиниках г. Омска.
Результаты проведенных исследований внедрены в курс лекций и практических занятий по теме: “Современные методы в лечении перитонита” кафедры госпитальной хирургии ОмГМА (644119, г. Омск, ул. Перелета, 9) и в лекционный курс и практические занятия на кафедре анатомии человека ОмГМА (644043, г. Омск, ул. Партизанская, 20) в разделе “Сосудистая система”, по теме: “Лимфатическая система”.
Апробация работы.
Основные положения диссертации доложены на научной конференции с международным участием, посвященной 75-летию со дня рождения и 50-летию научно-педагогической деятельности академика РАМН Ю.И. Бородина (Новосибирск, 2004); Юбилейной научно-практической конференции, посвященной 15-летию МУЗ ГКБСМП №1 (Омск, 2005); I Сибирском съезде лимфологов с международным участием (Новосибирск, 2006); Юбилейной научной сессии, посвященной 85-летию Омской государственной медицинской академии (Омск, 2006); межрегиональной научно-практической конференции хирургов, посвященной 80-летию со дня рождения академика РАМН Л.В. Полуэктова (Омск, 2007); Всероссийском пленуме проблемных комиссий «Неотложная хирургия» и «Инфекция в хирургии» Межведомственного научного совета по хирургии МЗ и СР и РАМН совместно с V-й Всероссийской конференцией общих хирургов с международным участием (Ростов-на-Дону, 2008); расширенном заседании кафедр госпитальной хирургии, факультетской хирургии, общей хирургии с курсом торакальной хирургии, детской хирургии, хирургических болезней ПДО, оперативной хирургии и топографической анатомии, анатомии человека, патологической анатомии с курсом клинической патологии, биохимии с курсами клинической биохимии и лабораторной диагностики Омской государственной медицинской академии (24.06.2008 г).
Публикации по теме диссертации.
По теме диссертации опубликовано 13 научных работ, из них 4 в центральной печати, методические рекомендации, получен патент РФ на изобретение № 2306927 от 27.09.07.
Объем и структура диссертации. Диссертационная работа изложена на 180 страницах машинописного текста, состоит из введения, обзора литературы, описания материала и методов исследования, 2 глав собственных исследований, заключения, выводов и практических рекомендаций. Фактические данные иллюстрированы 43 рисунками и 31 таблицей. Список литературы включает 220 источников (183 отечественных и 37 иностранных авторов).
Весь материал, представленный в диссертации, получен, обработан и проанализирован лично автором.
Положения, выносимые на защиту.
При применении марлевых тампонов для плоскостного дренирования брюшной полости у больных с распространенным гнойным перитонитом развивается недостаточность дренажно-детоксикационной функции лимфатического региона, морфологическим критерием которой служит гипоплазия брыжеечного лимфатического узла, за счет уменьшения площадей основных зон лимфоидной паренхимы и синусной системы; а следствием являются длительно сохраняющиеся признаки воспаления брюшины, высокие показатели эндотоксикоза и тяжелые расстройства центральной гемодинамики.
- Метод плоскостного сорбционного дренирования брюшной полости гемосорбентом ВНИИТУ-1 в сочетании с регионарной лимфотропной терапией благодаря эффекту лимфосанации (о чем свидетельствует доброкачественная гиперплазия регионарного лимфатического узла за счет увеличения площадей коркового и мозгового вещества, корковых и мозговых синусов, Т- и В- зависимых зон) способствует активации местного иммунитета, усилению дренажной, транспортной и детоксикационной функций лимфатического региона и позволяет сократить сроки ушивания брюшной полости при открытом ведении ее, улучшить результаты лечения и снизить показатели летальности больных.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Характеристика клинического материала. Клиническая часть работы основана на анализе результатов наблюдения и исследования 122 больных (в период с 2000 по 2006 гг.) с распространенными формами гнойного перитонита. Обследованные больные были оперированы и проходили лечение в отделении гнойно-септической хирургии МУЗ ГКБСМП №1 г. Омска. При формировании выборки, критерием включения явилось наличие распространенного гнойного перитонита вторичного характера у лиц мужского и женского пола с 16 лет в любую стадию заболевания. Рандомизацию проводили методом случайных чисел. Дизайн исследования представлен на рисунке 1.
Большую часть больных составили пациенты пожилого и старческого возраста (старше 60 лет) – 47(38,5%). Мужчин было 66 (54%), женщин – 56 (46%).
Наиболее частой причиной распространенного гнойного перитонита был острый аппендицит – у 35 (28,7%) больных. Травматические повреждения органов брюшной полости явились причиной перитонита у 22 (18%) больных (из них закрытая травма живота составила 16,4%, проникающие ранения живота – 1,6%).
Среди других причин распространенного гнойного перитонита отмечали прободную язву желудка и 12-перстной кишки – у 18 (14,8%) больных; перфорацию кишки инородным телом – у 12 (9,8%) больных. Гнойно-воспалительные заболевания женских половых органов послужили источником перитонита в 7,4 % наблюдений. Дивертикулярная болезнь кишечника, осложненная перфорацией, и послеоперационные осложнения в структуре причин развития распространенного гнойного перитонита составили по 4,9%.
Значительно реже причиной перитонита явились болезнь Крона с перфорацией стенки кишки – у 5 (4,1%) пациентов, ущемленная грыжа – 3 (2,5%) больных и в одном случае (0,8%) – острый холецистит.
В первой стадии перитонита поступило 16 (13,1%) пациентов, во второй стадии – 31 (25,4%), в третьей стадии – 33 (27,1%) больных. Наибольшее количество пациентов поступило в четвертую стадию заболевания – 42 (34,4%).
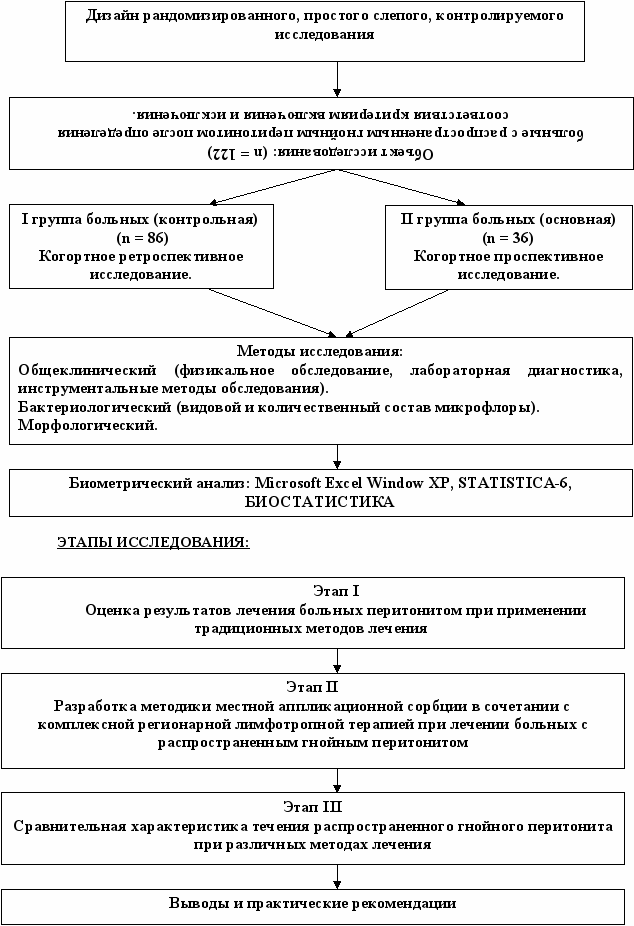
Рис. 1. Дизайн исследования.
У 54 (44,3%) больных диагностирован абдоминальный сепсис, в 41 случае (76%) он подтвержден бактериологическими методами исследования (посевами крови и мочи), у 13 (24%) больных диагноз абдоминального сепсиса установлен клинически. В состоянии инфекционно-токсического шока поступили 20 (16,4%) больных.
При бактериологическом исследовании отделяемого из брюшной полости выявили, что наиболее частым возбудителем перитонита явилась Escherichia coli – 36,9 %. Klebsiella pneumonia – 32,8 %, Pseudomonas aeruginosa – 20,5 %, Enterobacter cloacae – 8,2 %, Strеptococcus faеcalis – 8,2 %, Staphylococcus aureus – 3,3 %, Strеptococcus pyogenes – 0,8%, Proteus vulgaris – 0,8 %, дрожжеподобные грибы рода Сandida albicans – 0,8 %.
Ассоциацию микрофлоры встречали в 30,3 % случаях, моноинфекцию – в 55,7%. В 14,0 % случаях роста микрофлоры не получено.
Соответственно поставленным задачам, а также для выявления преимущества той или иной методики лечения, обследованные больные были разделены на 2 группы, в зависимости от метода лечения.
- Группа (контрольная) – 86 больных, лечение которым проводили традиционным методом. Этим пациентам производили плоскостное дренирование брюшной полости по Н.С. Макохе.
- Группа (основная) – 36 больных, в комплексном лечении которых использовали метод плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией.
Первая группа (контрольная) была сформирована из 86 больных с распространенным гнойным перитонитом, преимущественно в I – III стадиях заболевания. В комплексном лечении этих больных применяли традиционные методы санации брюшной полости: промывание ее водным раствором фурацилина, водным раствором хлоргексидина, физиологическим раствором хлорида натрия. После промывания брюшной полости 6 – 10 литрами антисептика ее осушали. Смыв с брюшины осуществляли изотоническим раствором хлористого натрия (100 мл), и затем 10 мл его забирали для бактериологического исследования. С целью профилактики послеоперационного пареза кишечника в корень брыжейки тонкой кишки вводили раствор новокаина 0,25% – 120-150 мл. По окончании санационных мероприятий производили плоскостное дренирование брюшной полости марлевыми тампонами по Н.С. Макохе (Макоха Н.С., 1984).
Вторая группа (основная) сформирована из 36 больных с распространенным гнойным перитонитом, преимущественно во II – III стадиях заболевания. В комплексном лечении этих больных применяли метод плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией (патент РФ на изобретение № 2306927 от 27.09.07). Дренирование брюшной полости осуществляли углеродным гемосорбентом ВНИИТУ-1 с суммарным объемом пор не менее 0,4 см3/г и зольностью не более 0,15%, помещенным в капроновые контейнеры. После хирургического устранения источника перитонита и интраоперационной санации брюшной полости растворами антисептиков на петли кишечника укладывали однослойную матричную марлевую салфетку. Затем по периметру лапаротомной раны в брюшную полость помещали капроновые контейнеры с гемосорбентом ВНИИТУ-1 в количестве 6 – 8 штук по 45 см3, общим объемом сорбента до 360 см3. Верхний и нижний углы лапаротомной раны ушивали единичными узловыми швами. Оставшуюся неушитой лапаротомную рану сверху накрывали марлевой салфеткой. По показаниям полость малого таза дополнительно дренировали трубчатым дренажем через контрапертурный разрез в правой или левой подвздошных областях. После завершения дренирования брюшной полости живот пациента ушивали в стерильную простынь с целью предупреждения эвентрации внутренних органов. Перевязку и смену контейнеров с сорбентом проводили на 2–3 сутки послеоперационного периода. На 4–5 сутки производили дополнительную санацию брюшной полости и ушивание лапаротомной раны при купировавшихся явлениях гнойного воспаления брюшины.
С целью лимфотропной терапии в корень брыжейки тонкой кишки во время первой санирующей операции и во время последующих перевязок, вплоть до ушивания лапаротомной раны вводили лекарственную смесь в составе: раствор новокаина 0,25% – 80-100 мл, лидаза – 16 ЕД, селемицин – 0,5 г, гепарин – 2,5 тыс.ЕД.
Для изучения особенностей течения послеоперационного периода у больных с распространенным гнойным перитонитом, которым в лечении использовали метод, основанный на сорбционном дренировании брюшной полости в сочетании с регионарной лимфотропной терапией, и сравнения эффективности этого метода с традиционно применяемым методом плоскостного дренирования брюшной полости марлевыми тампонами по Н.С. Макохе, проведено клиническое исследование, заключающееся в анализе 48 историй болезни. С этой целью дополнительно были сформированы две группы больных из числа выживших пациентов, сопоставимые по возрасту, полу, нозологии и стадиям течения заболевания:
I – группа сравнения, отобранная из числа выживших больных контрольной группы, n=24;
II – основная группа, отобранная из числа выживших больных основной группы, n=24.
В качестве основных функциональных критериев эффективности лечения использовали: снижение температуры тела и нормализацию показателей эндогенной интоксикации (количество лейкоцитов периферической крови, сдвиг лейкоцитарной формулы, СОЭ, ЛИИ, содержание ВСММ, уровень креатинина и мочевины плазмы крови), сроки ушивания лапаротомной раны, средний койко-день, затраты на лечение.
Для оценки степени тяжести состояния больных использовали интегральную систему APACHE II (Acute Physiology And Chronic Health Evaluation) для стратификации пациентов по риску внутрибольничной летальности. Для прогнозирования исхода заболевания пользовались Мангеймским индексом перитонита.
В работе использовали метод определения токсичности плазмы по уровню молекул средней массы (Габриэлян Н.И. и др., 1981; Владыка А.С. и др., 1987; Долгин М.Р. и др., 1987; Петров В.В. и др., 1993; Weinstein M.P. et al., 1983).
Количественное определение степени обсемененности тканей микроорганизмами проводили методом секторных посевов по Голду (методика Киевского института эпидемиологии и инфекционных болезней им. Л.В. Громашевского, 1986).
Лабораторные исследования выполнялись на базе бактериологической лаборатории и экспресс-лаборатории МУЗ ГКБСМП №1 (зав. Е.Н. Бирюлина).
Объектом морфологического исследования служили брыжеечные лимфатические узлы (БЛУ), которые биоптировали у 48 больных, оперированных по поводу распространенного гнойного перитонита. Биопсию брыжеечных лимфатических узлов у каждого больного производили дважды. Первый раз – во время первой санирующей операции и второй раз – перед ушиванием передней брюшной стенки (на 5-6 сутки – у больных группы сравнения и на 4-5 сутки – у больных основной группы).
Для светооптических исследований материал фиксировали в жидкости Теллесницкого (Лили Р., 1969). После обезвоживания и просветления в серии спиртов и ксилолов лимфатические узлы заключали в парафин-воск. Срезы толщиной 5-7 мкм изготовляли на ротационном микротоме. Измерение микроанатомических структур лимфатических узлов производили на срезах, окрашенных гематоксилином Майера и эозином, азур-II и эозином по Нохт-Максимову и по методу Ван Гизон (Меркулов Г.А., 1969; Волкова О.В. и др., 1971).
С помощью окулярной сетки при увеличении в 32 раза под микроскопом МБС – 10 определяли площади основных компонентов узла (Глаголев А.А., 1941; Автандилов Г.Г. и др., 1981). После этого общую площадь среза лимфоузла рассчитывали, как сумму точек, падающих на исследуемые компоненты. Для пересчета общей площади и отдельных структур изучаемых объектов в абсолютных цифрах (мм2) определяли цену деления одной точки (Христолюбова Н.Б. и др., 1974).
В лимфатических узлах определяли: общую площадь среза лимфатического узла, площади капсулы, краевого и коркового синусов, коркового плато, глубокой коры, мозговых синусов, мозговых тяжей, лимфоидных узелков без центра размножения и с центром размножения, количество их, площадь герминативных центров. Рассчитывали удельные площади коркового и мозгового вещества, Т- и В-зависимых зон. Вычисляли корково-мозговой (К/М) индекс, Т/В коэффициент (соотношение Т- и В-зависимых зон), суммарную площадь синусов.
Выделение вышеперечисленных структурных компонентов в лимфатических узлах проводили согласно Международной гистологической номенклатуре под редакцией В.В. Семченко и др. (1999) и на основании ряда обзоров (Сапин М.Р. и др., 1978; Смирнова Т.С., 1987; Белянин В.Л. и др., 1999; Belisle C., Sainte-Marie G.,1981).
Объем Т-зависимой зоны лимфоузла определяли как сумму площадей коркового плато и паракортикальной зоны. Суммарный объем преимущественно В-зависимых зон лимфоузла – как сумму площадей центров размножения и мозговых тяжей (Бородин Ю.И., Григорьев В.Н., 1986).
Клеточный состав лимфоузлов и брюшины изучали на световом микроскопе ЛОМО Микромед-2 при увеличениив 150 и 600 раз.
Морфологические исследования выполнялись на базе кафедры анатомии человека ОмГМА (зав. каф. д.м.н., проф. И.Н. Путалова).
Статистическую обработку полученных количественных данных осуществляли с помощью пакета прикладных программ ”STATISTICA-6”, согласно современным требованиям к проведению анализа медицинских данных (Гланц С., 1998; Реброва О.Ю., 2001).
На первом этапе статистического анализа определяли основные статистические характеристики изучаемых параметров (средняя, медиана, квартили, дисперсия, стандартное отклонение, стандартная ошибка, асимметрия и эксцесс). Затем проводили тест на нормальность распределения (критерий Колмогорова-Смирнова и Шапиро-Вилкоксона W-тест).
Достоверность различий двух выборок оценивали с помощью критерия Стьюдента (t) при форме распределения, близкой к нормальной (р < 0,05). Условиями использования параметрической статистики считали: 1) нормальное или близкое к нему распределение параметров в вариационных рядах; 2) равенство дисперсий признаков в двух сравниваемых группах (Реброва О.Ю., 2001). Когда выше приведенные условия не соблюдались (что характерно для медицинских исследований), использовали методы непараметрической ранговой статистики. Проверку нулевой и альтернативной гипотез для независимых выборок в двух группах проводили с помощью критерия Колмогорова-Смирнова. Для установления различия между зависимыми выборками использовали W-критерий Вилкоксона парных сравнений, а также ранговый дисперсионный анализ Фридмана (более двух групп или сроков). Для категориальных переменных применяли критерий 2 или точный критерий Фишера. Количественный материал представлен в виде таблиц, как среднее стандартное отклонение (Ms) (Гланц С., 1998; Реброва О.Ю., 2001).
Автор выражает искреннюю признательность и благодарность научным руководителям: доктору медицинских наук, профессору С.И. Филиппову и доктору медицинских наук, профессору И.Н. Путаловой за оказанную консультативную помощь в работе; коллективам кафедр госпитальной хирургии и анатомии человека ОмГМА за полезные обсуждения; главному врачу МУЗ ГК БСМП №1 П.Г. Пилипенко, нач. меду по хирургии Р.А. Арестовичу и коллективу хирургов МУЗ ГКБСМП №1 за создание благоприятных условий и поддержку работы.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Проведенное исследование показало, что традиционные методы не решают проблему лечения больных с распространенным гнойным перитонитом. Использование марлевых тампонов для плоскостного дренирования брюшной полости не дало достаточного эффекта в течение первых 14 суток послеоперационного периода. Это выразилось в длительно протекающих явлениях послеоперационной астении, электролитных и вегетативных расстройствах, персистирующем воспалении брюшины с экссудативными элементами воспаления, проявлениями выраженной интоксикации, что подтверждается более длительным лихорадочным периодом. Субфебрильная лихорадка у больных этой группы сохранялась до 14 суток послеоперационного периода.
Несмотря на то, что общая лейкоцитарная реакция у больных группы сравнения была менее выражена и даже к 2-3 суткам наблюдали временную нормализацию количества лейкоцитов периферической крови, другие показатели эндогенной интоксикации (сдвиг лейкограммы, СОЭ, ЛИИ и ВСММ) сохранялись повышенными на всем протяжении послеоперационного периода. Это относится и к таким показателям, как креатинин и мочевина. Нормализация этих показателей крови происходила, только на 11 сутки. Интегральный показатель степени тяжести состояния больных данной группы по APACHE II на 11 сутки в среднем был равен 19,23,9. Интегральный показатель степени тяжести состояния больных основной группы по APACHE II на 11 сутки был значительно ниже – 16,44,3.
Применение активного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией позволило оказать позитивное влияние на течение послеоперационного периода, что проявлялось ранней активизацией больных, более быстрым снижением показателей критериев эндогенной интоксикации. Нормализация температуры тела отмечена на 5 стуки лечения после операции. Несмотря на то, что умеренный лейкоцитоз у данной группы больных определяли в течение всего послеоперационного периода (что мы объясняем сохраняющейся реактивностью организма в послеоперационном периоде больных основной группы), на 11 сутки послеоперационного периода отмечали снижение содержания в крови веществ средней молекулярной массы (ВСММ); СОЭ к 14 суткам имела в два раза меньшее значение по отношению к группе сравнения (13,75,1 мм/час – в основной группе и 38,215,0 мм/час – в группе сравнения).
Лейкоцитарный индекс интоксикации (ЛИИ) имел тенденцию к снижению, более выраженное снижение его значений регистрировали на 7 сутки (3,53,3 у.е.).
Наиболее значимые изменения обнаружены при исследовании уровня мочевины и креатинина крови. В основной группе эти показатели приходили в норму с 1 суток и дальнейшего повышения их на протяжении всего послеоперационного периода не зафиксировано. Нормализацию этих показателей с 1 суток лечения можно объяснить лимфостимулирующим эффектом предложенного метода на лимфатическую микроциркуляцию, лимфообразование и лимфоотток от тканей брюшной полости. Полученные нами результаты согласуются с данными Р.Т. Панченкова с соавт. (1986).
Воспалительные явления в брюшной полости больных основной группы начинают купироваться уже на 3 сутки. Во время первой перевязки и смены контейнеров с сорбентом отмечали отсутствие экссудата в брюшной полости и значительное уменьшение отека париетальной и висцеральной брюшины. В основной группе ушивание передней брюшной стенки выполняли на 4,83±0,15 сутки. В группе сравнения уменьшение отека брюшины и экссудативных явлений наблюдали только к 6,04±0,19 суткам, когда и производили ушивание передней брюшной стенки. У двух больных группы сравнения к этому времени отмечали некупированные явления гнойного воспаления брюшины, сохранение пареза кишечника и наличие мутного экссудата в брюшной полости в значительном количестве. Этим больным вынужденно произведена дополнительная санация брюшной полости и редренирование ее по Н.С. Макохе.
Нарушения гемодинамики при перитоните органически связаны с развитием гиповолемии, гипопротеинемии, снижением объема циркулирующей крови и потерей электролитов. Согласно данным многочисленных исследований, в условиях распространенного воспаления брюшины происходит массивная диффузия жидкости из сосудистого русла в брюшную полость и внутрибрюшинно расположенные органы, что ведет к вовлечению в процесс значительного количества тканевой жидкости и развитию обезвоживания организма (Панченков Р.Т. с соавт., 1986; Шелестюк П.И. с соавт., 2000).
Ретроспективный анализ показателей центральной гемодинамики у пациентов группы сравнения выявил следующие недостатки, которые, на наш взгляд, во многом связаны, как с методикой дренирования брюшной полости, так и с общей тактикой интенсивной терапии до операции и в послеоперационном периоде.
Как показывают полученные данные, предоперационная подготовка больных группы сравнения и интенсивная терапия их в ближайшем послеоперационном периоде (1 сутки) не способствовала устранению тяжелой гиповолемии на фоне выраженного эндотоксикоза (таблица 1). Cущественно сниженный МОК (на 30% от нормы) и сниженные показатели интегральной реографии (УО, СИ, УИ на 89%, 77%, и 121%, соответственно, по сравнению с нормальными значениями) во многом обусловлены длительностью течения (более суток) перитонита, как очага инфекции, так и тяжелыми водно-электролитными нарушениями и декомпенсацией кислотно-основного состояния. Наличие у пациентов тяжелых расстройств в микроциркуляторном сосудистом русле и развитие синдрома "эндотелиальной утечки" в раннем послеоперационном периоде косвенно подтверждается резким снижением ОЦК (1,9±0,4 л) и низким ОПСС (688±24 динссм-5) на фоне достаточной по объему и характеру инфузионной терапии.
Тяжелые расстройства центральной гемодинамики сохранялись и на 3-4 сутки послеоперационного периода. Незначительное увеличение показателей интегральной реографии (рост МОК – на 5%, СИ – на 16% и УИ – на 42% от исходных данных) свидетельствовало о сохраняющихся патологических потерях. Ведущую роль играла потеря жидкости в межклеточное пространство, о чем свидетельствовало увеличение ОВЖ на 140% при увеличении ОЦК только на 31%. Значительное увеличение ОВЖ, также косвенно подтверждало наличие у больных синдрома "эндотелиальной утечки" на фоне интенсивной инфузионной терапии.
Как известно, ударный объем (УО), сердечный (СИ) и ударный индексы (УИ) характеризуют функцию макроциркуляторного сосудистого русла (сердечный насос, сосуды буферы, сосуды емкости). Снижение указанных показателей (УО, СИ, УИ на 23%, 61% и 51%, соответственно) в сравнении с контрольными значениями, сохранялось на 5-6 сутки послеоперационного периода у больных группы сравнения, что неблагоприятно повлияло на микроциркуляторное сосудистое русло (сосуды сопротивления, сосуды обмена, сосуды-шунты), о чем свидетельствовал сохраняющийся высокий уровень ОПСС (2809±25 динссм-5). Макроциркуляторное и микроциркуляторное сосудистые русла являются единой функциональной системой кровообращения. Полученные данные убедительно показывают, что нарушения в одном структурном звене гомеостаза сказываются на функционировании другого.
Динамика изменений центрального кровообращения у больных основной группы несколько отличается от предыдущих данных (таблица 2). Исходные гемодинамические показатели, также как у пациентов группы сравнения, можно квалифицировать, как проявления гиповолемии с аналогичными патогенетическими механизмами и степенью тяжести. Однако ко второму периоду исследования (3-4 сутки) у больных основной группы отмечали положительную динамику показателей, как макроциркуляторного, так и микроциркуляторного русел кровообращения. Регистрировали значимое увеличение МОК на 60%, УО, СИ, УИ на – 13%, 100%, 40%, соответственно, что необходимо связывать с уменьшением потерь за счет синдрома "эндотелиальной утечки", так как увеличение количества ОВЖ не превышает 19% от исходного уровня, против 140%, имевших место в группе сравнения.
Более существенное, чем в группе сравнения, прогрессивное улучшение показателей центральной гемодинамики отмечали на 5-6 сутки от начала интенсивной терапии. Показатели МОК, УО, СИ, УИ увеличиваются при сопоставлении с исходными данными на 125%, 36%, 118% и 62%, соответственно, против низких аналогичных значений у пациентов группы сравнения. Увеличение ОВЖ у больных основной группы на данный период исследования не превышает 25% от исходных данных, хотя и несколько превышает аналогичный показатель в группе контроля. И, напротив, в группе сравнения объем внеклеточной жидкости на 5-6 сутки послеоперационного периода по-прежнему превышает (на 89%) исходный показатель.
Таблица 1
Динамика изменений показателей центральной гемодинамики у больных группы сравнения I (М±m)
| Исследуемые показатели | Периоды исследования (n=24) | Контроль (n=24) | ||
| 1 сутки (I группа) | 3-4 сутки (II группа) | 5-6 сутки (III группа) | ||
| МОК, л | 3,9±0,4* | 4,1±0,4 | 4,2±0,5 | 5,1±0,3 |
| УО, мл | 39,3±4,4 | 36,0±6,1 | 48,0±5,7** | 74,3±7,7 |
| СИ, л/минм2 | 1,8±0,5** | 2,1±0,4v | 2,9±0,3* | 3,2±0,1 |
| УИ, мл/м2 | 19,2±2,3** | 27,4±2,1 | 29,1±2,2 | 42,2±2,3 |
| ОПСС, динссм-5 | 688±24** | 2372±37 | 2809±25 | 1010±32 |
| ОЦК, л | 1,9±0,4* | 2,5±0,4 | 3,6±0,4* | 5,4±0,8 |
| ОВЖ, л | 8,9±0,9 | 21,1±2,2 | 19,7±2,7 | 10,5±2,3 |
Таблица 2
Динамика изменений показателей центральной гемодинамики у больных основной группы II (М±m)
| Исследуемые показатели | Периоды исследования (n=24) | Контроль (n=24) | ||
| 1 сутки (I группа) | 3-4 сутки (II группа) | 5-6 сутки (III группа) | ||
| МОК, л | 2,8±0,4** | 4,5±0,4* | 6,3±0,5 | 5,1±0,3 |
| УО, мл | 44,0±5,4* | 50,2±6,1* | 60,0±5,7** | 74,3±7,7 |
| СИ, л/минм2 | 1,6±0,4** | 3,1±0,3 | 3,5±0,3 | 3,2±0,1 |
| УИ, мл/м2 | 24,2±2,5** | 34,4±2,1 | 39,1±2,2*** | 42,2±2,3 |
| ОПСС, динссм-5 | 607±37** | 1724±33 | 1309±25** | 1010±32 |
| ОЦК, л | 1,7±0,3** | 3,6±0,3 v | 4,5±0,5 | 5,4±0,8 |
| ОВЖ, л | 9,5±1,3 | 11,3±2,6 | 11,9±2,4 | 10,5±2,3 |
Примечание. Достоверность отличия: * - р < 0,05 при сравнении с контролем; - р < 0,05 при сравнении между I и II группами; ** - р < 0,001 при сравнении с контролем; - р < 0,001 при сравнении между II и III группами; *** - р < 0,001 при сравнении между I и III группами; - р < 0,001 при сравнении между I и II группами; v - р < 0,05 при сравнении между II и III группами.
Резюмируя эффект положительного влияния на центральную и периферическую гемодинамику предложенного метода лечения распространенного гнойного перитонита, мы пришли к выводу, что эффективность метода во многом объясняется наличием лимфосанирующего (лимфостимуляция, лимфокоррекция и лимфопротекция) эффекта на дренажно-детоксикационную функцию лимфатической системы брюшной полости. Это выражается в уменьшении отека тканей кишечника, улучшении его микроциркуляции и снижении давления в брюшной полости, что, в свою очередь, трансформируется в перераспределение метаболической нагрузки между органами детоксикации и экскреции с возрастанием роли желудочно-кишечного тракта и почек в интенсивном выведении токсических веществ. В данном случае, восстановление нарушенной микроциркуляции в кишечнике (косвенным подтверждением этого является восстановление моторной функции кишечника) приводит к уменьшению транслокации бактерий и их токсинов в брюшную полость, а восстановление дренажной функции лимфатической системы способствует детоксикации, улучшению оттока лимфы в венозную систему, что увеличивает ОЦК и улучшает показатели центральной гемодинамики.
Моторная функция кишечника, которую оценивали по восстановлению перистальтики, появлялась в основной группе значительно раньше – на 2,92±0,24 сутки, чем в группе сравнения. Перистальтика кишечника у больных группы сравнения восстанавливалась в среднем на 4,67±0,34 сутки. У больных основной группы заметно уменьшалось отделение застойного содержимого по желудочному зонду и раньше отмечали появление отхождения газов и стула (на 3,54±0,26 сутки – в основной группе и на 4,96±0,27 сутки – в группе сравнения).
В условиях гнойного воспаления брюшины в лимфатическом русле и регионарных лимфатических узлах, которые представляют собой биологический фильтр, способный задерживать микроорганизмы, токсины, продукты распада метаболитов, развивается лимфостаз и деструктивные изменения. Возникновение механической и динамической недостаточности лимфообращения нарушают полноценность лимфатического дренажа тканей (Бородин Ю.И., Григорьев В.Н., 1986; Буянов В.М. и др., 1990).
Метод плоскостного сорбционного дренирования брюшной полости гемосорбентом ВНИИТУ-1 в сочетании с регионарной лимфотропной терапией изучался нами, как способ воздействия на лимфатическую систему с целью улучшения дренажа и детоксикации тканей, процессов микроциркуляции, купирования воспалительного отека, создания бактериостатической концентрации антибиотика в лимфатическом регионе. Морфологическим критерием эффективности предложенного метода послужила оценка структурной организации брыжеечных лимфатических узлов у больных с распространенным гнойным перитонитом.
Морфометрические показатели брыжеечных лимфатических узлов больных обеих групп с распространенным гнойным перитонитом до лечения существенно не отличаются друг от друга. Для структурной организации этих узлов характерен фрагментированный морфотип (по классификации Ю.И. Бородина, 1968). В физиологических условиях такой тип строения верхних брыжеечных узлов центральной группы оправдан, поскольку на пути транспорта лимфы они располагаются не на первом этапе, а одном из последующих (Richter E., Feyerabend Th., 2004). Поэтому основными функциями этих узлов в норме являются дренаж и транспорт лимфы. В условиях воспаления брюшины нагрузка на лимфатическую систему, обеспечивающую дренаж и детоксикацию тканевой жидкости и лимфы, возрастает. Морфологическая картина гистологических препаратов регионарных лимфатических узлов (инфильтрация полиморфноядерными лейкоцитами окружающей клетчатки и капсулы узла, развивающийся синусгистиоцитоз, небольшие размеры вторичных лимфоидных узелков и их центров размножения, истонченные мозговые тяжи и переполненные различными клеточными элементами и фибрином мозговые синусы) свидетельствует о том, что лимфа, направляющаяся в узел, высоко токсичная, а транспорт ее в эфферентный сосуд нарушен. Данные В.Л. Белянина и Д.Э. Цыплакова (1999) о том, что синусный гистиоцитоз считается наиболее выраженным проявлением макрофагально-гистиоцитарной реакции и чаще всего подобная реакция гистиоцитов синусов развивается на фоне лимфостаза, свидетельствуют в пользу этого.
На фоне применения марлевых тампонов с целью плоскостного дренирования брюшной полости для лечения больных с распространенным гнойным перитонитом отмечали гипоплазию брыжеечных лимфатических узлов за счет уменьшения структурных компонентов коркового и мозгового вещества (рис. 2). Это происходит в тот период, когда в капсуле, паренхиме и синусах узла определяется лейкоцитарная инфильтрация, то есть сохраняются признаки воспаления. Диффузная или очаговая лимфогистиоцитарная инфильтрация с примесью нейтрофилов в перинодулярной клетчатке указывала на сохраняющиеся явления гнойного периаденита (некоторые лимфоузлы подверглись расплавлению). С одной стороны, обнаруженные преобразования структурной организации регионарного лимфатического узла указывают на высокую токсичность и обсемененность тканевой жидкости и лимфы, а, с другой стороны, свидетельствуют о сниженной резистентности организма. Появление в корковом веществе аттенуированных лимфоидных узелков и вторичных узелков с атрофирующимися светлыми центрами является морфологическим проявлением сниженной иммунной защиты (Белянин В.Л., Цыплаков Д.Э., 1999). Другим подтверждением этого можно считать сокращение площадей тимусзависимой (Т) и тимуснезависимой (В) зон на 16% и 30 %, соответственно (рис. 2). В структуре узла преобладает В-зависимая зона, указывающая на то, что в регионе преобладают иммунные процессы по гуморальному типу. Однако благоприятный прогноз, по мнению В.Л. Белянина, Д.Э. Цыплакова (1999), ассоциируется с наличием Т-клеточной реакции.
В изученных брыжеечных лимфатических узлах пациентов с распространенным гнойным перитонитом, которым применяли традиционный метод плоскостного дренирования брюшной полости марлевыми тампонами, в динамике послеоперационного периода обнаруживали изменения и в синусной системе. Так, определяли увеличение доли краевого синуса. В нем, как и в других синусах узла обнаруживали повышенную плотность клеточных элементов (лимфоциты, макрофаги, плазматические клетки, единичные нейтрофильные лейкоциты), что может служить признаком затруднения транспорта лимфы через узел и нарушения дренажной функции. По данным В.И. Коненкова (2007), дренажная функция является одной из защитных функций лимфатической системы.

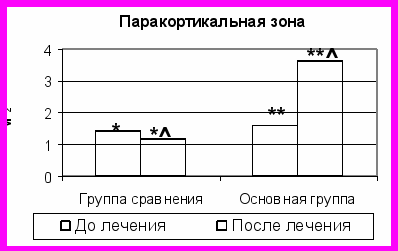
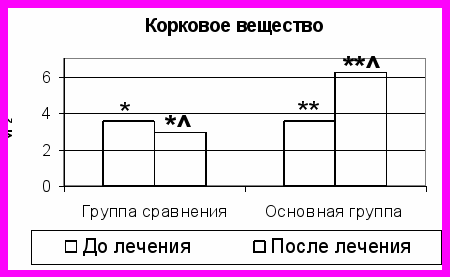
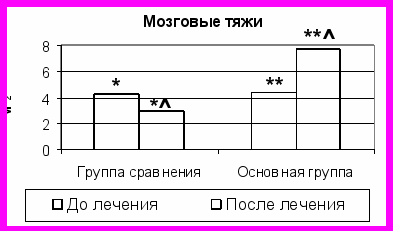
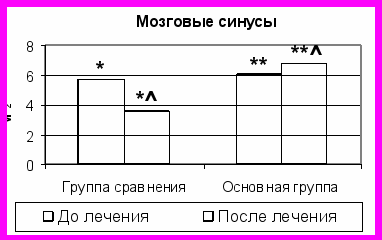
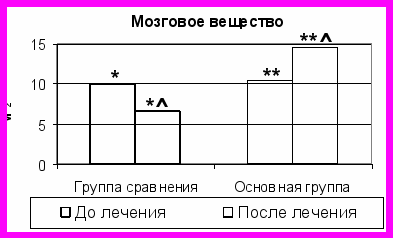
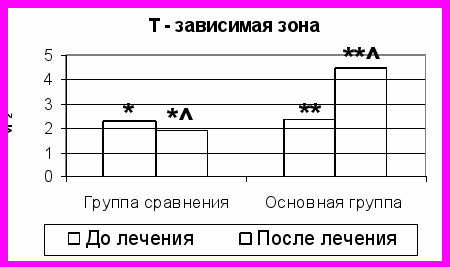
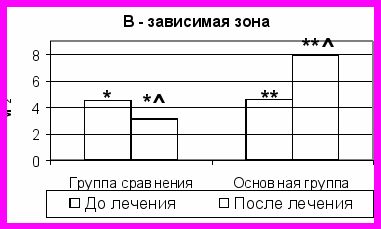
Рис. 2. Сравнительная оценка площади структурных компонентов (в мм2) брыжеечных лимфатических узлов до и после проводимого лечения.
Примечание: * - отличие достоверно между показателями группы сравнения до и после лечения (P<0,05); ** - отличие достоверно между показателями основной группы до и после лечения (P<0,05); - отличие достоверно между показателями группы сравнения и основной группы после лечения (P<0,05).
Она обеспечивает поддержание постоянства и циркуляции внутренней, межклеточной, межтканевой, интерстициальной составляющей всех тканей организма.
Преобразования брыжеечных лимфатических узлов пациентов с распространенным гнойным перитонитом на фоне плоскостного сорбционного дренирования брюшной полости в сочетании с регионарной лимфотропной терапией, по сравнению с традиционным методом лечения носят позитивный характер.
Увеличение на 43% площади среза БЛУ в динамике лечения свидетельствует о гиперплазии регионарных лимфатических узлов, в противоположность той картины, которую наблюдали в группе сравнения. Доброкачественная реактивная гиперплазия лимфатических узлов с увеличением их размеров отражает проявление высокой степени иммунологической активности в ответ на антигенный раздражитель (Белянин В.Л., Цыплаков Д.Э., 1999).
Нами отмечено увеличение площадей коркового (на 75%) и мозгового (на 39%) вещества БЛУ (рис. 2). Отсутствие явлений синусгистиоцитоза и увеличение площадей корковых и мозговых синусов (на 73% и 91%, соответственно), в сопоставлении с показателями группы сравнения, являются подтверждением не только сохраненной, но и усиленной дренажно-детоксикационной функции регионарных лимфатических узлов.
Значения показателей площади мозговых тяжей преобладают над значениями показателей площади мозговых синусов. Поэтому Т/С коэффициент до лечения в основной группе составлял 0,72+0,06, а после лечения – 1,13+0,11, в группе сравнения, наоборот, площадь мозговых синусов превышает площадь мозговых тяжей, как до лечения (Т/С коэффициент – 0,74+0,05), так и после (Т/С коэффициент – 0,84+0,08).
Выявленные преобразования основных структурных компонентов БЛУ отразились и на значении площадей Т- и В- зависимых зон (рис. 2). Значения показателей Т- зависимой зоны на фоне предложенного метода лечения увеличились (площадь – почти в 2 раза, а доля – на 73%), В- зависимой зоны (тимуснезависимой) – тоже возросли (площадь – на 73%, а доля – на 21%). В группе сравнения динамика показателей площади – противоположная, значения их уменьшились.
Метод плоскостного сорбционного дренирования брюшной полости гемосорбентом ВНИИТУ-1 в сочетании с регионарной лимфотропной терапией обладает лимфосанирующим эффектом, о чем свидетельствует доброкачественная гиперплазия регионарного лимфатического узла за счет увеличения площадей коркового и мозгового вещества, корковых и мозговых синусов, Т- и В- зависимых зон, что способствует активации местного иммунитета, усилению дренажной, транспортной и детоксикационной функций лимфатического региона.
Местное применение углеродминерального сорбента ВНИИТУ-1 обеспечило достаточно надежную местную детоксикацию, на что указывают показатели критериев эндогенной интоксикации, которые нормализовались в 2 раза быстрее, чем в группе сравнения.
В связи с тем, что сорбционное дренирование брюшной полости было дополнено лимфотропной терапией, насыщающей регионарное лимфатическое русло антибактериальным препаратом в бактериостатической концентрации и воздействующим на контаминанты значительно большее время, чем при традиционном введении, удалось в 2 раза быстрее снизить уровень обсемененности тканей брюшной полости микроорганизмами и улучшить результаты лечения по всем отдельно взятым показателям в 1,5-2 раза.
Таким образом, проведенное исследование показывает, что сорбционное дренирование брюшной полости в сочетании с регионарной лимфотропной терапией является патогенетически обоснованным и эффективным методом лечения больных с распространенным гнойным перитонитом. Этот способ позволил добиться снижения общей летальности на 13,4% и уменьшения затрат на лечение в среднем на 3381,62 рублей на одного больного.
