В строении белков одно общее: они состоят из аминокислот. Всего в состав молекул белка их входит 20 наименований
| Вид материала | Документы |
| Разрушение бактериальной клетки лизоцимом Строение клеточных мембран |
- Высокомолекулярные азотосодержащие органические вещества, молекулы которых построены, 51.51kb.
- O в молекулы аминокислот и белков. О. В. Мосин Московская государственная академия, 401.15kb.
- Биосинтез белка, 17.68kb.
- Первый. Белки под большой молекулярной массой от нескольких десятков до нескольких, 28.19kb.
- Белки, 41.04kb.
- Биосинтез белков, 64.8kb.
- Биосинтез белков, 65.92kb.
- Биосинтез белков Интегрированный урок в 10-м классе(химия и биология). Цель урока, 27.63kb.
- О в мясе, рыбе, яйцах и молочных продуктах и что все растительные белки якобы неполноценны, 37.76kb.
- Биотехнология методы получения аминокислот и белков, меченых стабильными изотопами, 499.21kb.
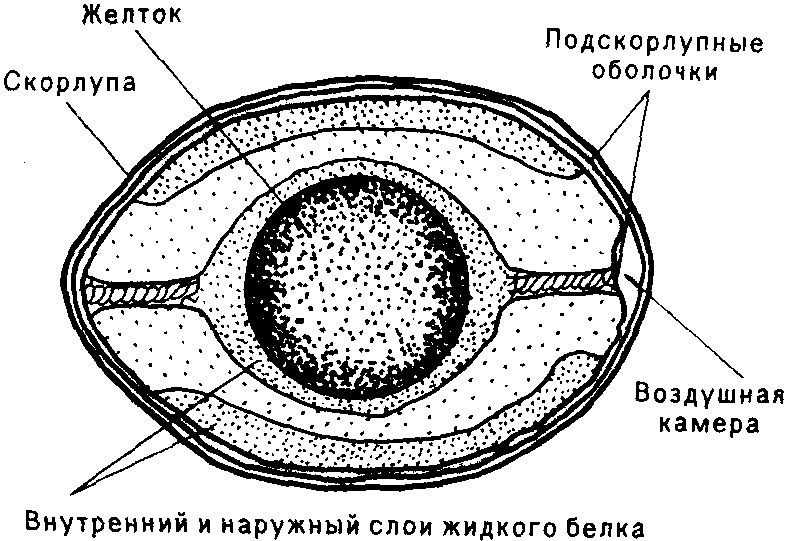
Строение куриного яйца
Чем же вызвана такая горячая привязанность человека к блюдам из яиц?
«Vita in ovo» (жизнь — из яйца) — говорили древние.
И не зря говорили. В свете достижений современной химии этот афоризм приобретает новый смысл: в состав яиц входят наиболее ценные и жизненно необходимые вещества. Но сначала несколько слов о строении яйца. Оно покрыто, как известно, тонкой оболочкой, главной составной частью которой является карбонат кальция. Если на эту оболочку капнуть кислотой, то произойдет реакция, в результате которой выделяется нестойкая угольная кислота, сразу же разлагающаяся на воду и диоксид углерода (углекислый газ).
В этом легко убедиться, опустив яйцо в уксус: оболочка его сразу растворится. Таким образом можно очистить яйцо, не разбивая его.
Наверное не все знают, что яичная скорлупа неплохо усваивается, вернее, не она сама, а кальций, находящийся в ней. Видимо, не зря в старину ее клали в щи из квашеной капусты, да и теперь иногда муку из скорлупы используют для обогащения хлебобулочных изделии кальцием.
Под скорлупой находятся две подскорлупные оболочки. В свежеснесенном яйце, как правило, весь объем заполнен содержимым. Когда же такое яйцо остынет, объем содержимого несколько уменьшается. Между подскорлупными оболочками образуется воздушная камера — пуга. В процессе хранения яиц, по мере испарения воды, пуга будет увеличиваться. Под оболочками находится белок. Он составляет около 60% содержимого яйца, а желток—около 40%. Главной составной частью яйца являются белки. Для того, чтобы не путать эти вещества с белком яйца, мы, говоря о яйце, будем называть их так, как принято в химии — протеинами. Правда, если уж быть точным, то в яйце представлены как простые белки — протеины, так и сложные белки — протеиды. В середине белка на двух жгутах (холязах) «подвешен» желток.
Всего в курином яйце содержится белковых веществ около 12,7%. В белке, как это ни странно, их содержится меньше, чем в желтке (соответственно 10,8 и 16,2%). Если учесть различие в массе белка и желтка, то окажется, что в них содержатся равные количества белковых веществ. В яичном белке это овоальбумин (60—70% от общего содержания протеинов), кональбумин (10—15%), овоглобулины и сложные белки — овомукоид (10— 14%), авидин (0,1%), лизоцим (3%). Глобулины растворяются только в воде, содержащей электролиты. Поэтому, если разбавить яичный белок водой, то овоглобулин выпадет в осадок, растворяющийся только лишь при добавлении соли.
Белки яйца считаются полноценными, так как содержат все незаменимые аминокислоты в оптимальных соотношениях. Некоторые белки яйца обладают специфическими свойствами. Рассмотрим их подробнее.
Овомукоид — сложный белок (протеин), в котором белковый и углеводный компоненты находятся в соотношении 4:1. Овомукоид дает вязкие растворы, образующие при взбивании устойчивую пену, что позволяет использовать взбитые яичные белки при изготовлении бисквитного теста, сахаро-белковых изделий (безе, меренги) и многих других. Распределен он неравномерно, и поэтому яичный белок имеет разную вязкость —вокруг желтка и под скорлупой слои менее густые.
Овомукоид обладает антиферментными свойствами: он тормозит действие трипсина — фермента поджелудочной железы, участвующего в переваривании белков пищи. Поэтому сырые яичные белки не только плохо усваиваются, но и снижают усвояемость других белков пищи. При варке яиц овомукоид денатурирует и теряет это свойство. В значительной степени уменьшается его антиферментное действие и при взбивании яичных белков, когда образуется пена и сама поверхность белка возрастает в сотни раз; в тонких пленках белок денатурирует и без нагревания (силы поверхностного натяжения деформируют молекулу белка и она теряет свои специфические свойства).
Другой белок — авидин — так же, как и овомукоид, отрицательно влияет на процесс пищеварения. Он связывает и инактивирует биотин — витамин Н, который играет большую роль в обмене веществ. Кстати, этот витамин, участвуя в переносе диоксида углерода, предохраняет тем самым от тяжелых поражений кожу, выполняет он и ряд других функций. Биотин вырабатывают микроорганизмы, обитающие в кишечнике человека, поэтому поступление этого витамина с пищей совсем не обязательно. В то же время, например, употребление сырых яиц может вызвать Н-авитаминоз, так как в этом случае микроорганизмы под влиянием авидина перестают вырабатывать биотин.
Есть в яйце и еще один своеобразный белок — лизоцим, обладающий совершенно удивительными свойствами. Само название указывает на его свойства, поскольку происходит от греческого слова lysis, т. е. растворять. Лизоцим служит хорошим ферментом, растворящим стенки бактериальной клетки. Содержится он в слезах, слюне, слизистых оболочках носа, играя роль антибактериального барьера, предохраняющего человека от попадания болезнетворных микроорганизмов.
Когда животные зализывают свои раны, они дезинфицируют их с помощью лизоцима, содержащегося в слюне. Препараты лизоцима широко используются при лечении слизистых оболочек глаз, десен, носоглотки.
Это удивительное вещество открыл в 1922 г. А. Флеминг—английский микробиолог (1881—1955). Его открытие положило начало эре антибиотиков, особенно после 1929 г., когда был открыт пенициллин. Они стали самыми сильными средствами борьбы человека с невидимыми врагами — болезнетворными микробами.
Для того, чтобы глубже понять механизм бактерицидного действия лизоцима, надо рассмотреть структуру его молекулы. Она имеет почти шарообразную форму (глобулу) и состоит из двух половинок (позиция А), между которыми имеется углубление (позиция Б). Одна половина глобулы лизоцима состоит главным образом из аминокислот, имеющих одну кислотную группу (карбоксил) и одну аминогруппу. Эти группы участвуют в образовании пептидной цепи — основы структуры белка. Таким образом,остаются свободными только неполярные СН3-группы.
Во второй половине глобулы лизоцима преобладают аминокислоты, имеющие по две аминогруппы (лейцин, изолейцин) либо по две кислотные группы (аспаргиновая, лизин, аргинин и др.). Поэтому при образовании полипептидной цепи одна из полярных групп остается свободной. Благодаря эффекту полярности, происходит ионизация карбоксильных групп на поверхности «щели» молекулы лизоцима. Важнейшей составной частью оболочки бактериальной клетки является сложный полисахарид. Его молекула состоит из остатков аминосахаров, соединенных так называемыми глюкозидными связями (позиция В). Полисахарид этот сорбируется на поверхности глобулы лизоцима, часть его цепи попадает в «щель» (углубление) и разрывается полярными группами на противоположных сторонах щели.
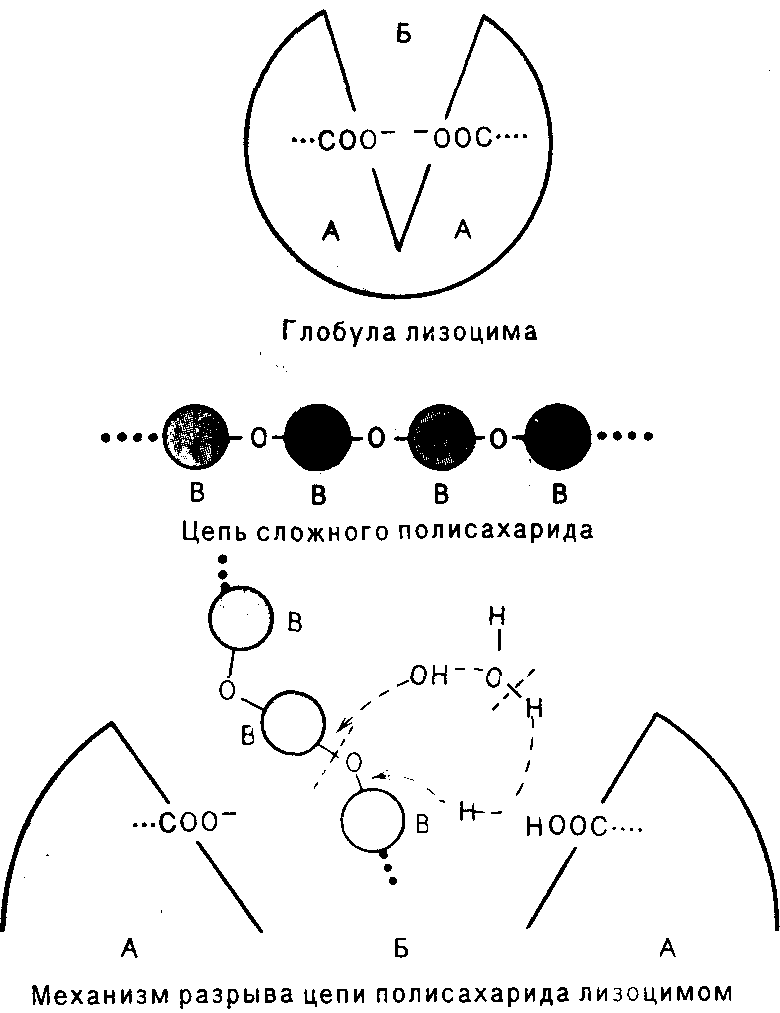
Разрушение бактериальной клетки лизоцимом
Воспользовавшись бактерицидными свойствами лизоцима, ученые Харьковского института общественного питания сберегли для народного хозяйства миллионы рублей. Исходя из того, что на птицефабриках неизбежно часть яиц бьется, вследствие чего транспортировать их нельзя, ученые предложили сливать белок и желток (раздельно) в полиэтиленовые мешки и в таком виде транспортировать. При этом учитывалось, что бактерицидные свойства лизоцима обеспечивают сохранность продукции в течение нескольких дней, особенно при пониженной температуре.
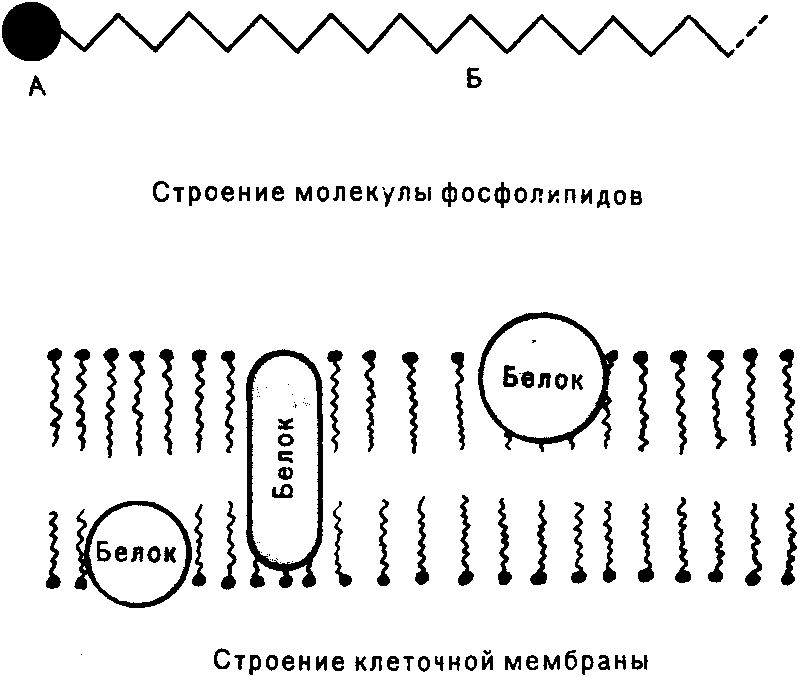
Строение клеточных мембран
Однако у лизоцима имеется и одно неприятное свойство. Если яйца были инфицированы, то лизоцим может усилить развитие бактерий, что приводит к тяжелым токсикоинфекциям. Вот почему яйца водоплавающей птицы, которые бывают часто заражены сальмонеллезом, не разрешается употреблять в пищу.
Теперь рассмотрим желток яйца. Он состоит из сложных белков (протеидов) —фосфопротеидов: вителлина, ливетина, фосфитина и др. Уже само название первого из этих белков подчеркивает их роль в обмене веществ («вита» значит «жизнь»). Что касается липидов яйца (триглицеридов, фосфатидов), то они все сосредоточены в желтке. Важнейшей отличительной особенностью липидов яйца является высокое содержание в нем таких фосфатидов, как лецитин и холин. Ни в одном продукте не сосредоточено такого количества этих биологических активных веществ. Недаром само название «лецитины» происходит от греческого названия желтка (lekilhos— желток). Основной функцией лецитинов является их участие в построении клеточных мембран.
Мембраны—это перегородки, отделяющие отдельные структурные элементы клетки друг от друга. Именно на мембранах протекают важнейшие жизненные процессы, поскольку они являются носителями важнейших биологически активных веществ, обладающих каталитическим действием. В них возникают нервные импульсы, обусловливающие сокращение и расслабление мышц, переваривание и всасывание пищи, превращение одного вида энергии в другие. Важнейшие составные части их — липиды (фосфатиды), белки и углеводы. Особую роль играют в них фосфатиды и глюколипиды. Именно они образуют двойной мембранный слой. Молекулы фосфатидов и глюколипидов состоят из полярной части (А), которой являются фосфорная кислота и сахара, и неполярной — цепи жирных кислот (Б). В двойной слой мембраны, состоящей из липидов, вкраплены молекулы белков. При различных концентрациях электролитов с двух сторон мембраны возникает разность потенциалов. Под действием различных раздражителей в мембране образуются поры, происходит разряд, который можно сравнить с пробоем прокладки конденсатора. Этот разряд и служит нервным импульсом.
Теперь становится понятным, какую огромную роль играют фосфолипиды — ведь их содержится в мембране от 55 до 57% от ее общей массы.
Велика роль и холина — он служит одним из липотропных веществ, препятствующих ожирению печени, из него же синтезируется и ацетилхолин — один из важнейших передатчиков нервных импульсов.
Жиры яиц очень хорошо сбалансированы по содержанию жизненно необходимых высоконепредельных жирных кислот.
Еще один компонент липидного комплекса желтков — холестерин. Он также жизненно важен, однако излишнее количество его способствует возникновению атеросклероза. Высокое содержание холестерина в желтке (1,6%) послужило основанием для ограничения количества яиц, используемых в рационе питания пожилых люден. Проведенные в дальнейшем глубокие исследования показали, что холестерин, поступающий с пищей, мало влияет на повышение его уровня в плазме крови.
Окраска желтка яйца обусловлена присутствием биологически активных веществ — каротиноидов (ксантофилла и каротина), которые вообще очень редко встречаются в продуктах животного происхождения.
Богаты яйца и витаминами — А, В, Ва, Д, Е, К, пантотеновой и фолиевой кислотами.
Ценен также минеральный состав яиц—в них много соединений кальция, фосфора, железа. С высоким содержанием железа связано одно любопытное явление, с которым часто сталкиваются кулинары — неожиданное потемнение поверхности желтка. В действительности же ничего неожиданного в этом явлении нет: при длительной варке яиц из серосодержащих протеидов белка выделяется сероводород, который с ионами железа дает соединение темного цвета.
Для того, чтобы не допустить потемнения, необходимо погрузить сваренные вкрутую яйца в холодную воду. Давление газов в воздушной камере яиц упадет, сероводород будет отсасываться от желтка, и поверхность желтка будет темнеть в значительно меньшей степени.
Рассмотрим теперь, какие химические процессы происходят при варке куриного яйца.
На предыдущих страницах этой книги речь шла о «денатурации белков» — изменении природных (натуральных, или нативных) свойств белков. Обычно это связано с их нагреванием. Процесс денатурации глобулярных белков заключается в том, что при повышении температуры усиливается тепловое колебательное движение полипептидных цепей, в результате слабые водородные связи между ними рвутся, вторичная структура разрушается, полипептидная цепь развертывается и перегруппировывается по-новому.
Следствием денатурации являются очень важные изменения свойств белка. Прежде всего они теряют способность к гидратации, водная защитная оболочка вокруг глобул исчезает, они соединяются вместе, укрупняются и теряют растворимость. Процесс этот называют свертыванием. Если концентрация белков была небольшая, то свернувшиеся белки образуют хлопья. Если же концентрация белков была высокой, то при денатурации образуется сплошной сгусток (гель). Именно этот процесс и происходит при варке яиц.
Свертывание яичного белка протекает следующим образом:
45—50оС — заметных изменении не наблюдается;
50—55°С — появляются местные помутнения;
55—60°С — помутнение распространяется на весь белок;
60—65°С — белок заметно густеет;
65—70°С — появляется студнеобразная нежная масса;
70—86°С — образуется гель, сохраняющий форму;
85—90°С — гель постепенно уплотняется.
Таким образом, при нагревании яиц в первую очередь изменяется белок. Благодаря тепловой денатурации белковых веществ при 50—55 °С в прозрачной массе его образуются местные помутнения, которые постепенно распространяются, и при 65°С уже вся масса белка густеет, а при 75°С он превращается в сплошную непрозрачную массу очень нежной консистенции. При 80°С получается гель, который уже сохраняет форму, а при дальнейшем нагревании (выше 85°С) становится все более и более плотным.
Степень уплотнения белкового геля зависит от продолжительности нагревания. Так, длительное хранение белка при 95°С вызывает постепенное уплотнение геля без дальнейшего нагревания.
Желток яйца начинает загустевать только при 70°С. Это обстоятельство дает возможность в процессе приготовления таких блюд, как яйцо сваренное «в мешочек», яичница-глазунья, сохранять желток в жидком виде, в то время как белок достаточно уплотняется. Если белок и желток перемешать, то в этом случае яйцо будет загустевать только при 70°С. Разведенное молоком или водой яйцо дает менее плотные гели, что позволяет готовить яичные блюда нежной консистенции (омлеты, яичные кашки —«брюи»). Однако добавление к яйцу большого количества жидкости настолько снижает концентрацию белковых золей, что при свертывании они образуют не сплошной гель, а хлопья. Достаточно нежные, но хорошо сохраняющие форму гели можно получить при добавлении к яйцу от 50 до 100% жидкости.
Поваренная соль в больших концентрациях снижает температуру свертывания белков. Поэтому если в процессе приготовления яичницы-глазуньи крупинки соли попадают на желток, то на последнем образуются пятна свернувшихся белков. Чтобы избежать этого, солить нужно только один белок или посыпать солью сковороду с жиром до того, как выливают яйца, или, наконец, посолить яичницу уже на столе.
Входящий в состав белков куриного яйца овоглобулин нерастворим в воде, но легко растворяется в присутствии солей. Поэтому если белок яйца размешать с водой, то он помутнеет,— значит, выпал в осадок овоглобулин, а если добавить в смесь поваренную соль и размешать ее, то осадок исчезает.
Антифермент овомукоид тормозит действие пищеварительного фермента трипсина, в результате чего белок сырого яйца почти не усваивается организмом. При тепловой обработке он денатурирует, теряет свои антиферментные свойства, и яйца, сваренные всмятку или «в мешочек», усваиваются организмом хорошо. Однако если яйцо сварить вкрутую, то белковые вещества начинают уплотняться и в таком виде трудно поддаются действию пищеварительных ферментов и, следовательно, плохо усваиваются.
Второе следствие денатурации глобулярных белков — это повышение их перевариваемости, потеря устойчивости против действия пищеварительных ферментов. Поэтому все продукты, содержащие белки, легче и полнее перевариваются в организме.
Благодаря постепенному свертыванию белка, яйцам можно придать различную консистенцию:
если варить их в кипящей воде в течение 3—3,5 мин, то получаются яйца «всмятку», у которых белок будет частично загустевшим, а желток— жидким;
при варке в течение 4,5—5,5 мин получаются яйца «в мешочек», имеющие полностью затвердевший белок и полужидкий желток;
через 8—10 мин варки получаются яйца, сваренные «вкрутую».
Однако переваривать яйца не следует, у сваренных «вкрутую» яиц белок должен быть в меру плотный, а желток—нежный, рассыпчатый, с незатвердевшей каплей в центре.
Для того, чтобы при варке яиц «в мешочек» получить очень тонкий, но достаточно плотный слой белка, иногда варят яйца без скорлупы: в воду добавляют уксус (50 г 3%-го уксуса на 1 л) и соль (10 г), доводят до кипения, выпускают из скорлупы яйцо и варят 3—3,5 мин.
Яйца, сваренные «всмятку», хорошо усваиваются. Однако их трудно очистить, поэтому подают их, как правило, на стол в скорлупе в горячем виде. С яиц, сваренных «в мешочек» (пашот), скорлупа снимается довольно легко, что позволяет использовать их для подачи с супами (щи зеленые, бульон) или готовить с ними сложные блюда. Вот, например, как готовят блюдо «яйца с фаршированными помидорами». У помидоров средней величины срезают верхушку, удаляют часть содержимого (ее используют затем для приготовления соусов) и фаршируют мелко нарезанными хорошо обжаренными белыми грибами (или шампиньонами), ветчиной. Затем запекают в духовке в течение 15—20 мин и кладут сверху яйцо, сваренное «в мешочек».
Смесь белка и желтка свертывается так же, как один желток. Чтобы при этом получить более нежный студень, такую смесь можно разводить молоком или водой. Затем ее наливают в чашки или формочки и проваривают на водяной бане (получается омлет паровой) или жарят, осторожно помешивая, на сковородах (омлет жареный). Молока или воды надо брать около 50% от массы яиц.
В омлетную массу можно добавлять различные мелко нарезанные продукты: ветчину, колбасу и т. д.
Яйца служат не только ценным пищевым продуктом, но и используются в чисто технологических целях, поскольку их желток является прекрасным эмульгатором — молекулы фосфолипидов обволакивают жировые шарики, образуя защитные пленки, благодаря чему можно получать стойкие эмульсии жира с водой. Молекулы фосфолипидов, адсорбируясь на поверхности капелек жира, выстраиваются следующим образом: их «хвост» (углеводородная цепь) имеет сродство с жиром, а полярная группа («головка») — сродство с водой. Это свойство используют при получении майонеза: желтки сырых яиц растирают с солью, сахаром и горчицей, добавляя малыми дозами растительное масло, непрерывно и энергично размешивая. Когда получится густая и однородная эмульсия, ее разводят уксусом. Роль эмульгатора при этом играют не только фосфолипиды желтка, но и горчица.
