Монстакова Ирина Минеевна, 1 квалификационная категория, моу сош №11, город Североуральск, Свердловская область. Предмет : химия, 10 класс. Тип урок
| Вид материала | Урок |
| Учитель биологии. Учитель химии |
- Куликова Надежда Владимировна, вторая квалификационная категория Цель урок, 113.09kb.
- Яковлева Лариса Александровна учитель химии и биологии моу «Новогеоргиевская сош» Петуховского, 47.46kb.
- Пивоварова Елена Владимировна, учитель истории и обществознания моу «Туринская средняя, 362.33kb.
- Маклакова Елена Владимировна, первая квалификационная категория, моу «Первомайская, 260.98kb.
- Ятманкина Галина Михайловна моу саврушская сош с. Савруха Похвистневский район Самарская, 34.69kb.
- Рабочая программа педагога Васиной Т. И. (I квалификационная категория) по математике, 665.92kb.
- Гусева Ольга Владимировна, учитель химии и биологии, высшая квалификационная категория, 158.84kb.
- Урока английского языка и изобразительного искусства по теме: «наши выходные», 218.23kb.
- Конкурс "Современный урок" Урок биологии в 7 классе. Тип членистоногие, 119.78kb.
- Лучкина Наталья Петровна, учитель русского языка и литературы моу «сош №6», высшая, 164.19kb.
Роль белков в организме
Учитель биологии. Из органических веществ, входящих в живую клетку, важнейшую роль играют белки. На их долю приходится около 50% массы клетки. Благодаря белкам организм приобрел возможность двигаться, размножаться, расти, усваивать пищу, реагировать на внешние воздействия и т. д.
«Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и жизнь, что приводит к разложению белка», – писал Энгельс в своих трудах.
Состав, строение, свойства белков
Учитель химии. Белки – это сложные высокомолекулярные природные соединения, построенные из
 -аминокислот. В состав белков входит 20 различных аминокислот, отсюда следует огромное многообразие белков при различных комбинациях аминокислот. Как из 33 букв алфавита мы можем составить бесконечное число слов, так из 20 аминокислот – бесконечное множество белков. В организме человека насчитывается до 100 000 белков.
-аминокислот. В состав белков входит 20 различных аминокислот, отсюда следует огромное многообразие белков при различных комбинациях аминокислот. Как из 33 букв алфавита мы можем составить бесконечное число слов, так из 20 аминокислот – бесконечное множество белков. В организме человека насчитывается до 100 000 белков.Белки подразделяют на протеины (простые белки) и протеиды (сложные белки).
Число аминокислотных остатков, входящих в молекулы, различно: инсулин – 51, миоглобин – 140. Отсюда Mr белка от 10 000 до нескольких миллионов.
Историческая справка. Первая гипотеза о строении молекулы белка была предложена в 70-х годах XIX в. Это была уреидная теория строения белка. В 1903 г. немецкий ученый Э.Г.Фишер предложил пептидную теорию, которая стала ключом к тайне строения белка. Фишер предположил, что белки представляют собой полимеры из остатков аминокислот, соединенных пептидной связью NH–CO. Идея о том, что белки – это полимерные образования, высказывалась еще в 1888 г. русским ученым А.Я.Данилевским. Эта теория получила подтверждение в последующих работах. Согласно полипептидной теории белки имеют определенную структуру.
(Демонстрация кинофрагмента «Первичная, вторичная, третичная структура белка».)
Многие белки состоят из нескольких полипептидных частиц, которые складываются в единый агрегат. Так, молекула гемоглобина (С738Н1166S2Fe4O208) состоит из четырех субъединиц. Отметим, что Mr белка яйца = 36 000, Mr белка мышц = 1 500 000.
Первичная структура белка – последовательность чередования аминокислотных остатков (все связи ковалентные, прочные) (рис. 1).
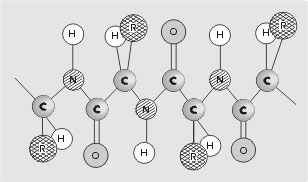 |
Рис. 1. |
Вторичная структура – форма полипептидной цепи в пространстве. Белковая цепь закручена в спираль (за счет множества водородных связей) (рис. 2).
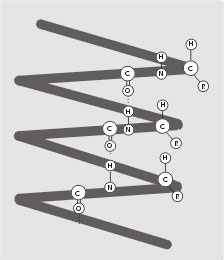 |
Рис. 2. |
Третичная структура – реальная трехмерная конфигурация, которую принимает в пространстве закрученная спираль (за счет гидрофобных связей), у некоторых белков – S–S-связи (бисульфидные связи) (рис. 3).
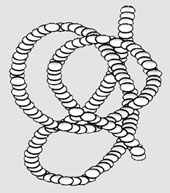 |
Рис. 3. |
Четвертичная структура – соединенные друг с другом макромолекулы белков образуют комплекс (рис. 4).
 |
Рис. 4. |
Химические свойства белков
При нагревании белков и пептидов с растворами кислот, щелочей или при действии ферментов протекает гидролиз. Гидролиз белков сводится к расщеплению полипептидных связей:
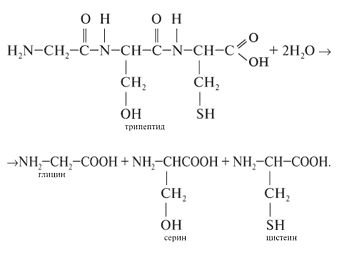
Лабораторный опыт 1.
Денатурация белков
Денатурация – нарушение природной структуры белка под действием нагревания и химических реагентов.
а) Действие спирта на белок;
б) действие солей хлорида натрия (концентрированный раствор) и ацетата свинца на белок;
в) действие HNO3 (конц.);
г) свертывание белков при кипячении.
Лабораторный опыт 2.
Цветные качественные реакции белков
а) Биуретовая реакция;
б) ксантопротеиновая реакция;
в) взаимодействие белка с ацетатом свинца при нагревании.
Учительхимии. Данные опыта 1 показывают, что загрязнение природной среды солями тяжелых металлов приводит к отрицательным последствиям для живых организмов. Природные белки теряют присущие им специфические свойства, становятся нерастворимыми, денатурируют. При отравлении людей солями тяжелых металлов используют молоко, белки которого связывают ионы таких металлов.
(Демонстрация фрагмента из 1-й части фильма «Белки, строение белковых молекул».)
