Аннотационный отчет о научно-исследовательской работе за 2010 год
| Вид материала | Отчет |
| 2-50 нм) диоксида титана различных модификаций (аморфный, анатаз, брукит, рутил |
- Отчёт онаучно-исследовательской работе гу нии но ур за 2010 год, 997.69kb.
- Отчёт о научно-исследовательской работе за 2011 год, 1208.93kb.
- Отчёт о научно-исследовательской работе за 2009 год, 851.3kb.
- Отчет о научно-исследовательской работе студентов на кафедре микробиологии, вирусологии, 353.35kb.
- Реферат отчет о научно-исследовательской работе состоит, 61.67kb.
- Отчет о научно-исследовательской работе профессорско-преподавательского состава, 617.56kb.
- Основные направления доклада проректора по научной работе профессора А. С. Калитвина, 231.85kb.
- Отчет о научно-исследовательской работе за 2011 год, 1453.45kb.
- Отчет о научно-исследовательской деятельности в 2010 году, 373.56kb.
- Отчет по научно-исследовательской работе за 2006-2010, 1170.58kb.
Блок 4. Исследование каталитических свойств полученных нанокомпозитов, дизайн наноструктурированных катализаторов нового типа
Исследована каталитическая способность новых полимерных нанокомпозитов с наночастицами меди и серебра, стабилизированными сополимером 1-винил-1,2,4-триазола с акрилонитрилом, полученным радикальной сополимеризацией соответствующих сомономеров. Синтез нанокомпозита проводили методом термического восстановления металлов из соответствующих солей CuCl2 и AgNO3 в матрице сополимера при температуре 200-250оС. Содержание меди в полученных нанокомпозитах составляет 30%, серебра 40%. Наночастицы меди имеют размеры 20-25 нм, серебра – 17-22 нм. Нанокомпозиты Cu и Ag обладают электрической проводимостью 2.510-6 и 2.410-9 См/см, соответственно, а также парамагентизмом с g-фактором сигнала ЭПР 2.005, шириной 5 Гс и интенсивностью 1019-1020 сп/г. Каталитическую активность нанокомпозитов изучали в реакции прямого окисления метанола до формальдегида. Известно, что в присутствии стандартных медных и серебрянных катализаторов указанная реакция протекает только при повышенных температурах (200оС). Проведение реакции с использованием синтезированных нами нанокомпозитов (с наноразмерными частицами нуль-валентной меди и серебра) позволило снизить температуру реакции до комнатной (25оС).
Блок 5. Изучение антимикробной активности новых серебросодержащих нанокомпозитов
Проведено исследование антимикробной активности новых водорастворимых серебросодержащих полимерных нанокомпозитов в отношении различных клинических штаммов: грамположительных микроорганизмов – Staphylococcus aureus, включая оксациллин/метициллин-чувствительные стафилококки, грамотрицательных бактерий – E.coli, Enterobacter, Klebsiella, неферментирующих бактерий – Pseudomonas aeruginosa, Acinetobacter, выделенных от больных с гнойной инфекцией и грибов – Candida. Всего было исследовано 38 штаммов микроорганизмов.
Полученные результаты показывают, что полимерные нанокомпозиты с содержанием серебра 2.7, 5.0 и 7.8% проявляют антимикробный эффект в отношении граммотрицательных музейных и госпитальных штаммов, оксациллин/метициллин-чувствительных стафилококков, микрококков, пневмококков, стрептококков, а также грибов.
Проект V.37.3.3. Синтез и исследование наноразмерных и наноструктурированных оксидных материалов и гетерогенных катализаторов на их основе.
Блок 1. Разработка методики синтеза мезопористого оксида железа с использованием в качестве темплата нанозолей кремнезема и исследование зависимости его физико-химических и каталитических свойств от условий и способа их приготовления
В развитие метода синтеза носителей с использованием в качестве темплатов кремнезема была разработана методика получения темплатов из золей кремнезема приготовленных по методу Штобера-Финка и их модификации в щелочи с целью увеличения размеров пор. На модифицированный темплат был нанесен углерод двумя способами – посредством пиролиза пропан-бутановой смеси при 720oС и посредством синтеза в поровом пространстве темплата резорцинол-формальдегидного геля с его последующим пиролизом при 720oС. После растворения кремнеземного темплата в щелочи были получены образцы мезопористого углерода с величиной удельной поверхностью 40 – 95 м2/г, объемом пор 0,2-0,6 см3/г, средним диаметром пор 12-33 нм и отсутствием микропор. Полученные образцы углерода представляют интерес для исследования возможности их применения в качестве носителей катализаторов топливных элементов.
Блок 2. Синтез композиций на основе оксида алюминия с использованием различных сурфактантов (поливинилового спирта, полиэтиленоксида, цетилтриметиламмоний бромида, мочевины). Изучение влияния условий синтеза и природы вводимых сурфактантов на структурные и текстурные характеристики, а также термическую стабильность получаемых оксидов
Изучено формирование гидроксида и оксида алюминия в зависимости от природы, содержания и условий вводимого сурфактанта. Показано, что добавление мочевины и полиэтиленоксида при синтезе гидроксида алюминия не оказывает значительного влияния на текстурные характеристики Al2O3, прокаленного при 550оС. Синтез гидроксида алюминия в присутствии цетилтриметиламонийбромида или поливинилового спирта позволяет получать мезопористый оксид алюминия в -форме, величина удельной поверхности которого может изменяться в диапазоне 370 640 м2/г, объем пор – 0.7 2.0 см3/г и средний диаметр пор – пор 6.2 13.7 нм. Исследование термостабильности образцов мезопористого оксида алюминия в диапазоне температур 550-1100оС показало их повышенную термостабильность: прокаливание при 1100оС приводит к образованию -Al2O3, при этом величина удельной поверхности составляет 130 м2/г и объем пор может достигать 1,2 см3/г; для сравнения: Al2O3, приготовленный традиционным методом осаждения, при 1100оС представляет смесь - и -Al2O3 с удельной поверхностью и объемом пор, равных 60 м2/г и 0.4 см3/г соответственно.
Блок 3. Изучение закономерностей формирования наноразмерного ( 2-50 нм) диоксида титана различных модификаций (аморфный, анатаз, брукит, рутил) в зависимости от условий синтеза.
Изучено влияние условий синтеза (природы предшественника, рН, температуры, добавок комплексообразователя и различных ПАВ) на структурно-дисперсные свойства наночастиц диоксида титана и стабильность при хранении в течение не менее 6 месяцев. Текстурные, морфологические, структурные и дисперсные характеристики наноразмерного диоксида титана, полученного гидролизом TiCl4 и Ti(i-OC3H7)4 при варьировании условий синтеза, были изучены комплексом физико-химических методов. Показано, что преобладающий диаметр наночастиц TiO2, полученных из TiCl4 и Ti(i-C3H7)4, составляет 3-7 нм. Все образцы характеризуются тонкопористой текстурой, основные параметры которой (SBET, Vпор, dпор) можно регулировать условиями синтеза. Установлено определяющее влияние рН среды на формирование диоксида титана с различной структурой при гидролизе TiCl4. При определенных условиях гидролиза TiCl4 (в присутствии щелочей) наблюдается образование крупных агломератов размером 4 - 14 мкм, способных разрушаться под действием ультразвука на мелкие агрегаты с D = 100-200 нм. При гидролизе Ti(i-OC3H7)4 агрегированных образований не наблюдается ни одним из перечисленных выше методов, а введение в дисперсионную среду комплексообразователя – ацетилацетона обеспечивает наиболее узкое распределение наночастиц TiO2 по размерам с преобладающим D = 3 нм. Золи TiO2, полученные гидролизом Ti(i-OC3H7)4, достаточно устойчивы при хранении. Дополнительно устойчивость этих золей может быть повышена введением стабилизирующей добавки метилцеллюлозы МЦ-400. Кроме того, показана возможность длительного хранения порошков, полученных высушиванием этих золей, так как при вторичном разведении их водой воспроизводятся характеристики свежеприготовленного золя.
Блок 4. Изучение влияния структуры носителя (нанокристаллическая и регулярная) в нанесенных Pd/M-TiO2 и Cu/M-TiO2 (М – Ce, Y) катализаторах на дисперсность активного компонента, электронное состояние Pd и Cu, прочность связи поверхностного кислорода и каталитические свойства в окислении СО
Исследовано влияние структуры носителя в нанесенных Cu/Ме-TiO2 и Pd/Ме-TiO2, (где Me-Ce и Y) катализаторах на физико-химические и каталитические свойства в реакции окисления СO в CO2. Методом ЭМ показано, что при нанесении меди в количестве 1-7 вес.% CuO на нанокристаллический диоксид титана анатазной модификации, состоящий из агрегатов высокодисперсных частиц анатаза с размером 3-8 нм, и последующей обработке при 650-7500С на поверхности носителя формируются высокодисперсные частицы оксида меди регулярной структуры с размером 2,5-3 нм, которые прочно связанны с поверхностью носителя. Дальнейшее повышение температуры обработки приводит к образованию грубодисперсной фазы CuO. При нанесении меди на диоксид титана с регулярной структурой анатаза, с размером кристаллов 20-40 нм, после прокаливания катализатора выше 500-5500С на поверхности анатаза образуется грубодисперсная фаза оксида меди. Показано, что модифицирование диоксида титана добавками церия и иттрия способствует формированию нанокристаллической системы со структурой анатаза, представляющей сросшиеся между собой кристаллиты анатаза, с образованием между ними межблочных границ, в которых стабилизированы ионы трехвалентного церия и иттрия. По данным РФЭС, нанесенные ионы меди (II) на модифицированных носителях стабилизируются, в основном, в области межблочных границ, где также стабилизированы ионы Се3+ и Y3+; при этом не исключено взаимодействие ионов меди с ионами церия и иттрия с образованием между ними высокодисперсных соединений, также стабилизированных в области межблочных границ. Катализаторы Cu/Cе-TiO2 и Cu/Y-TiO2 при содержании CuO 1-5 вес.% проявляют высокую термостабильность вплоть до температуры 7500С. По данным изотопного обмена кислорода, введение церия и иттрия в диоксид титана приводит к увеличению подвижности поверхностного кислорода, которая возрастает с увеличением концентрации добавки. Установлено, что катализаторы Cu/Cе-TiO2 и Cu/Y-TiO2 при содержании оксида меди 5 вес.% характеризуются достаточно высокой активностью в реакции окисления СO: температура, при которой достигается 50% конверсия CO (T50), составляет 130 и 1370С соответственно. Исследование 1 вес.% Pd/Ме-TiO2 катализаторов показало, что палладий не регистрируется методом ЭМ, что свидетельствует об образовании кластеров палладия атомного размера на поверхности анатаза с нанокристаллической структурой. Активность этого катализатора в окислении СО несколько выше по сравнению с медьсодержащими: Т50 составляет 108оС.
Блок 5. Разработка методов целенаправленного синтеза нанооксидов сложного состава на основе CuO-CeO2/Al2O3, исследование формирования твердого раствора оксидов меди в оксиде церия на поверхности оксида алюминия комплексом физико-химических методов
Разработан новый метод синтеза, позволяющий получать катализаторы CuO-CeO2/-Al2O3 различного состава, содержащие медь и церий в диапазоне 4-12%, церия– 2-6% соответственно. Методами РФА, ИКС адсорбированного СО, ПЭМВР и EDX анализа показано, что при указанном содержании оксидов меди и церия обеспечивается получение наноразмерных совместных оксидов меди и церия на поверхности оксида алюминия, при этом кислотные центры оксида алюминия, необходимые для проведения реакции паровой конверсии диметилового эфира в водород, не блокируются и остаются доступными для реагентов. Образование совместной фазы твердого раствора оксида меди в оксиде церия показано методами РФА и EDX, дисперсность частиц определена методами РФА и ПЭМВР (3-5 нм). Методом EDX установлены количественные границы существования совместных нанооксидов меди-церия на поверхности оксида алюминия, максимальное содержание оксида меди в оксиде церия составляет 30%.
Блок 6. Синтез и исследование генезиса, структуры, и фазовых превращений метастабильной наноразмерной (1,5-2,0 нм) фазы частично-гидратированного оксида Fe3+, промотированного ионами хрома, меди, алюминия и лантана, со структурой типа 2-полосного ферригидрита
Получены фазовооднородные образцы предшественников железооксидных катализаторов и катализаторы, модифицированные ионами хрома, меди, алюминия, лантана, со структурами ферригидрита, гетита, гематита. Методами ДТА и РФА показано, что при термообработке в атмосфере инертного газа при температуре 525-635oC метастабильная фаза ферригидрита превращается в фазу со структурой гематита. При обработке в реакционной среде паровой конверсии СО оксиды железа со структурой типа гетита, гематита, ферригидрита переходят в оксидную фазу со структурой типа магнетита. Разработана методика и определено количество активных Fe-центров, способных обратимо восстанавливаться под действием водородсодержащего газа и окисляться под действием N2O. Оказалось, что железооксидные и модифицированные ионами хрома и меди образцы, полученные из соединений-предшественников со структурой гематита, гетита, ферригидрита, после воздействия реакционной среды существенно отличаются по величине поверхности, в то время как количество активных центров единицы поверхности приблизительно постоянно. Наиболее развитую поверхность имеет катализатор, полученный из предшественника со структурой типа ферригидрита, модифицированного ионами хрома. Проведенные предварительные каталитические исследования показали, что модифицирование ионами хрома и лантана существенно увеличивает стабильность катализатора, а модифицирование ионами меди – повышает активность в области температур ниже 3500С.
Блок 7. Синтез гидроксидных Cr-Al образцов методом соосаждения и исследование полученных осадков и прокаленных оксидных композиций комплексом физических методов в зависимости от режима термической обработки
Методом осаждения растворов хлоридов Cr и Al раствором осадителя (NH4OH или NH4HCO3) при постоянных температуре и рН скорости осаждения с последующей термической обработкой при 110-700оС в различных атмосферах (азот, гелий, воздух) получены Cr-Al-катализаторы (95%Cr2O3) и исследованы физико-химические свойства гидроксидных и оксидных Cr-Al фаз. Установлено, что оптимальные гидроксидные предшественники формируются при осаждении NH4OH при рН 7.0-7.5. При осаждении смешанных гидроксидов при рН < 7.0 приводит к образованию основных солей типа Cr(OH)3-xClx с трудноудаляемыми ионами Cl- и СО32-, дезактивирующими активные центры катализатора. Повышение рН до 8-8.5 ухудшает текстурные характеристики гидроксидных и оксидных фаз. Показано, что прокаливание в инертной атмосфере при температурах 280–500C способствует получение высокодисперсных аморфных оксидов со стехиометрией CrO1.5, свойственной Cr2O3. Значительно большую активность в реакции газофазного гидрофторирования перхлорэтилена имеют образующиеся в окислительной среде оксиды хрома со сверхстехиометрическим кислородом CrO1.9-2.0, но их получение в высокодисперсном состоянии при одностадийной прокалке в воздухе затруднительно вследствие большой экзотермичности стадии окисления, что приводит к разложению оксидов CrO1.9 до CrO1.5 с последующим спеканием продуктов разложения и кристаллизацией грубодисперсного неактивного -Cr2O3. Образование высокодисперсных и активных хромсодержащих оксидов со стехиометрией CrO1.9-2.0 возможно при двухстадийной прокалке гидроксидных образцов сначала в азоте при 400-500ºС, затем в воздухе при 250-350ºС.
Блок 8. Исследование влияния общего содержания нанесенного хрома и природы носителя на формирование различных наноразмерных состояний оксида хрома и их роль в процессе дегидрирования. Построение кинетической модели реакции дегидрирования
Изучено состояние нанесенного оксида хрома в микросферических алюмохромовых катализаторах, приготовленных с использованием в качестве носителя продукта центробежной термоактивации гиббсита. Показано, что в исходном, прокаленном на воздухе катализаторе хром может находиться в пяти различных окисленных состояниях: в виде ионов Cr6+, связанных с поверхностью носителя (не растворимы в воде), которые образуют в условиях реакции активные, но малоселективные частицы Cr3+ (I); в виде частиц Cr6+ («свободные» хроматы, растворимые в воде), образующих при восстановлении в условиях реакции активные и селективные наночастицы Cr3+ (II); в виде ионов Cr3+ в решетке носителя (твердый раствор Cr3+ на основе γ-Al2O3), которые не участвуют в реакции дегидрирования (III); в виде активных наноразмерных частиц ( 2-3 нм) α-Cr2O3 на поверхности носителя, доля которых в катализаторе мала из-за растворения ионов (IV); в виде грубодисперсных неактивных частиц α-Cr2O3 с внедренными ионами Al3+ (твердый раствор α-Cr2O3-Al2O3) (V). Количественное содержание той или иной формы оксида хрома зависит от его общего содержания в катализаторе, природы и содержания промотирующих добавок. Предложены способы повышения содержания активных частиц Cr2O3 с целью повышения активности и селективности промышленного катализатора КДМ в реакции дегидрирования низших парафинов. На лабораторной автоматизированной установке были проведены эксперименты по исследованию кинетики реакции дегидрирования изобутана на катализаторе КДМ. Было показано, что основную реакцию дегидрирования изобутана и все побочные реакции можно учесть с помощью двух маршрутов:

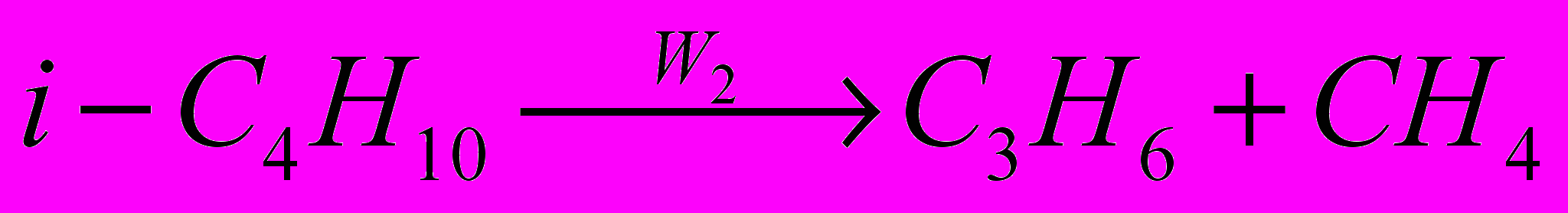
Проанализировано несколько наборов кинетических уравнений для записи скоростей реакций. Решение обратной кинетической задачи и нахождение значений кинетических параметров было осуществлено путем градиентного метода минимизации функционала. Наименьшее значение функционала, а, следовательно, и наиболее точное описание экспериментальных данных было получено для модели вида:
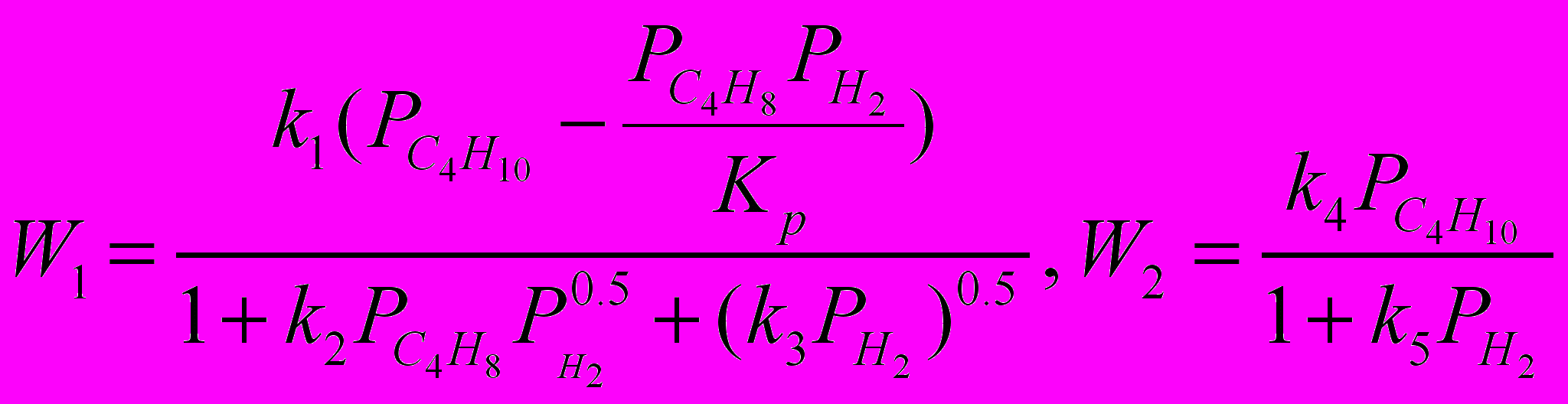
При этом значения кинетических параметров модели следующие:
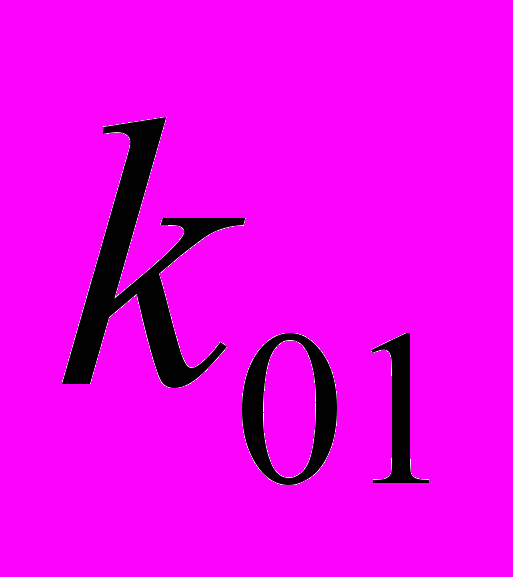 = 2.565*1011 моль*м-3*с-1*атм-1, E1 = 133 811 Дж/моль,
= 2.565*1011 моль*м-3*с-1*атм-1, E1 = 133 811 Дж/моль, 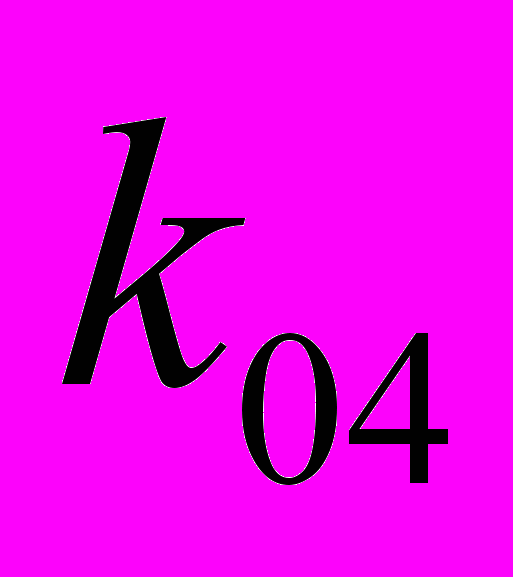 = 2.7*106 моль*м-3*с-1*атм-1, E4 = 97 844 Дж/моль, K2 = 105 атм-1. 5, K3 = 903 атм-1, K5 = 7 атм-1.
= 2.7*106 моль*м-3*с-1*атм-1, E4 = 97 844 Дж/моль, K2 = 105 атм-1. 5, K3 = 903 атм-1, K5 = 7 атм-1.Блок 9. Синтез фазовооднородных сложнозамещенных перовскитов на основе стронциевого кобальтита, стабильных в окислительной и восстановительной атмосферах.
Перовскито-подобные сложнозамещенные оксиды составов SrCo0.8-хFe0.2NbхO3-z (х=0; 0.1; 0.2; 0.3) и La0.5Sr0.5Co0.8-xFe0.2NbxO3-z (x=0, 0.2) синтезированы керамическим методом с использованием промежуточной мехактивации. Методом РФА показано формирование фазовооднородных систем со структурой перовскита для всех составов. Установлено, что допирование ниобием приводит к увеличению параметра решетки перовскита: с 3.8820Å (Nb0) до 3.9156Å (Nb0.3) для SrCo0.8-хFe0.2NbхO3-z и с 3.8378Å (Nb0) до 3.8864Å (Nb0.2) для La0.5Sr0.5Co0.8-xFe0.2NbxO3-z. Подвижность кислорода в синтезированных перовскитах SrCo0.8-хFe0.2NbхO3-z исследована методом термогравиметрии с масспектрометрическим анализом, обнаружен выход предположительно решеточного кислорода из структуры при температуре выше 400оС. РФА in situ показал сохранение структуры перовскитов SrCo0.8-хFe0.2NbхO3-z при нагреве в вакууме до 1000оС, наблюдалось лишь уширение дифракционных пиков. Однако привлечение дифракции высокого разрешения на СИ позволило обнаружить, что при 400-750оС происходит расслоение исходной фазы перовскита на две фазы с идентичной структурой, но различающейся кислородной нестехиометрией. Продемонстрировано, что обнаруженный процесс расслоения обратим, поскольку прогрев двухфазных образцов на воздухе при 400оС приводит к трансформации системы снова в однофазную.
Проект V.37.3.4. Синтез и исследование особенностей физикохимических свойств наноразмерных металлических каталитически активных 1D – 3D частиц в структуре микропористых оксидов, углеродных материалов и цеолитов.
Блок 1. Синтез и изучение особенностей физико-химических свойств наноразмерных оксидных каталитически активных 1D – 3D частиц меди и железа в структуре микропористых и мезопористых оксидов, цеолитов.
- Синтезированы образцы, содержащие наноразмерные оксидные каталитически активные 1D –3D частицы Cu и Fe в структуре микропористых и мезопористых оксидов Al2O3 и SiO2, высококремнистых цеолитов (ZSM-5, MOR, BEA) и цеолита Y при варьировании метода введения катиона переходного металла и условий термической обработки.
- Методами ЭПР, ЭСДО, ИК спектроскопии и ПЭМВР изучены закономерности формирования наноразмерных оксидных 1D – 3D частиц меди и железа, в зависимости от условий синтеза. Показано, что:
- изолированные ионы Cu2+ в катионо-обменных позициях цеолита формируются при использовании всех перечисленных методов синтеза, но доминируют в образцах, полученных ионным обменом с растворами солей меди. Изолированные Fe3+ формируются в ходе темплатного синтеза, но превращаются в (2D-3D) структуры Fen+ уже при удалении темплата. Формирование изолированных ионов Fe2+ наблюдается при ионном обмене с растворами солей Fe2+ в инертной среде;
- 1D оксидные структуры ионов меди, наблюдаемые нами ранее, формируются в ходе ионного обмена цеолита ZSM-5 с растворами солей меди в условиях, обеспечивающих формирование линейных гидроксокомплексов [Cun(OH)2n-2]2+ с n4 в растворе или локально в канале цеолита после ионного обмена. Димеры меди могут формироваться в течение термообработки;
- 2D оксидные структуры ионов меди и железа формируются в результате гидролиза акватированных ионов Cu2+(Fе3+) в слабоконцентрированных суспензиях, в результате чего локализация полигидроксо-комплекса зависит от природы соли Cu2+(Fе3+) и размера пор носителя, а состав – от соотношения ОН/Cu2+(Fе3+) и температуры; 2D структуры на поверхности кристаллитов образуются в результате последовательных окислительно-восстановительных обработок;
- 3D структуры ионов Cu2+(Fе3+) образуются при введении этих ионов методами капиллярной пропитки твердо-фазной трансформации, а также в результате принудительного гидролиза в высококонцентрированных суспензиях (1М). Проявляются в ЭСДО аналогично фазе CuO (КФП около 11000 см-1) или -Fe2O3
- Изучены окислительно-восстановительные и каталитические свойства наноразмерных оксидных 1D – 3D частиц меди и железа, стабилизированных в высококремнистых цеолитах, в реакции разложения закиси азота, восстановления оксида азота монооксидом углерода и водородом, окислении муравьиной кислоты, красителей. Показано, что
- Изолированные ионы Cu2+ восстанавливаются постадийно до Cu+ и Cu0 при температурах 200 и 400оС, изолированные ионы Fe3+ подвергаются восстановлению при температурах 400-450оС и выше;
- 1D-3D оксидные структуры ионов Cu2+(Fе3+) на в каналах и на поверхности кристаллитов носителя восстанавливаются одностадийно при температурах характерных восстановлению высокодисперсных оксидов CuO (200-240оС) и Fe2O3 (180-250oC); С уменьшением мерности структуры от 3D к 1D и размера 3D кластера наблюдается сдвиг пика поглощения водорода в область более низких температур, в частности для меди от 230оС до 160оС.
- каталитическая активность Cu-ZSM-5 в реакциях прямого разложения NO и N2O имеет S-образную зависимость от содержания меди (и уровня обмена), при этом резкий рост активности наблюдается при Cu/Al в интервале 0,3-0,4. В СКВ NO пропаном активность возрастает с увеличением Cu/Al до 0,5 и далее остается постоянной. Согласно данным физико-химических методов, в области соотношений 0,3-0,5 преобладают 1D структуры;
- формирование большого числа 2D и/или 3D структур приводит к снижению активности в окислительно-восстановительных реакциях, протекающих в газовой фазе.
- Выявлены закономерности формирования мерности, размера и морфологии оксидных частиц меди и железа и их реакционной способности в окислительно-восстановительных реакциях в зависимости от методики синтеза и структуры (химической и пространственной) оксидной матрицы.
