На правах рукописи
| Вид материала | Автореферат |
| Таблица 2.Оценка уровня алекситимии по группам сравнения. Таблица 3. Показатели качества жизни у пациентов на фоне психофармакотерапии Шкалы sf-36. |
- Печатная или на правах рукописи, 21.09kb.
- Удк 796/799: 378 , 770.24kb.
- На правах рукописи, 399.58kb.
- На правах рукописи, 726.26kb.
- На правах рукописи, 1025.8kb.
- На правах рукописи, 321.8kb.
- На правах рукописи, 552.92kb.
- На правах рукописи, 514.74kb.
- На правах рукописи, 670.06kb.
- На правах рукописи, 637.26kb.
Примечания. Различия статистически значимы между группами: * - р<0,05;
** - р<0,01.
Согласно полученным в работе результатам, у больных на ранних стадиях цереброваскулярной патологии нарушения в системе гемостаза преобладали над нарушениями липидного обмена. Изменения морфологии тромбоцитов в виде повышения количества дискоэхиноцитов, т.е. форм, инициирующих внутрисосудистый тромбоз, являются одним из ведущих патогенетических механизмов дебюта хронической ишемии головного мозга. Повышение агрегационно-адгезивной функции тромбоцитов способствует вазоконстрикции, нарушению транскапиллярного обмена и, следовательно, ухудшению церебральной микроциркуляции. Существенный вклад в нарушение микроциркуляции головного мозга вносит и повышение титров АФА, которые обусловливают прокоагулянтную активность крови и развитие претромботического состояния. Все вышеописанные изменения реологии крови негативно отражаются на кровоснабжении головного мозга, что подтверждается результатами дуплексного сканирования сосудов головного мозга.
В рамках сравнительного анализа по результатам ИФА титров АФА и ультразвуковой диагностики церебральной гемодинамики для дальнейшего психологического обследования было выделено 2 группы сравнения:
АФА(+): пациенты с цереброваскулярной болезнью и сопутствующей тромбофилической активностью крови, у которых наблюдался повышенный уровень одного или нескольких АФА, ассоциированный с высокими степенями внутричерепного венозного застоя, по данным ДС сосудов головного мозга – 34 человека (30 женщин и 4 мужчины); средний возраст 45,7±12,2.
- АФА(-): пациенты без тромбофилической активности крови, у которых по результатам дуплексного сканирования сосудов головного мозга атеросклеротические изменения преобладали над венозной дисциркуляцией – 31 человек (27 женщин и 4 мужчины) средний возраст 48,2±12,1.
Клинико-психопатологическое
и экспериментально-психологическое обследование.
Обследование с помощью методики PRIME-MD выявило высокую частоту (86%) сопутствующей психической патологии у пациентов с сосудисто-мозговой патологией. По данным ОП отмечено преобладание жалоб тревожно-депрессивного спектра в обеих группах сравнения. Пациенты в группе АФА(-) чаще предъявляли жалобы тревожного спектра и отмечали наличие приступов страха или паники, а в группе АФА(+) - жалобы депрессивного характера и такие соматические симптомы, как головная боль и головокружение. Согласно инструкции к руководству PRIME-MD соматические жалобы пациентов были расценены как связанные с сопутствующей соматической патологией (25%), доказанной лабораторными и инструментальными исследованиями, либо были обусловлены наличием тревожного или депрессивного расстройства (75%) и в дальнейшем не рассматривались в рамках соматоформных расстройств.
Большинство больных оценили свое здоровье как удовлетворительное (65%), причем в группе АФА(+) таких больных было больше (76%), чем в группе АФА(-) (52%) (р<0,01). Процент больных, расценивших состояние своего здоровья как «хорошее», у больных в группе АФА(+) был ниже (3%), чем в группе АФА(-) (26%) (р<0,01). В обеих группах сравнения отмечена одинаковая доля больных, считающих свое здоровье слабым (рис.1).
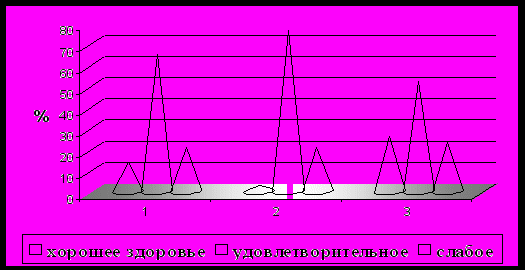
Рисунок 1. Самооценка состояния здоровья по результатам Опросника пациента методики PRIME-MD (n=100). 1 – все пациенты (n=100); 2 – группа АФА(+); 3 – группа АФА(-)
Наиболее часто у обследованных больных встречалась смешанная психическая патология: ГТР и БДР, сопровождающееся паническими атаками (ПА) (28%) или без них ГТР+БДР (15%). У 45% больных были выявлены ПА, но только в сочетании с ГТР. Лишь 14% неврологических больных не имели сопутствующей психической патологии (рис.2).
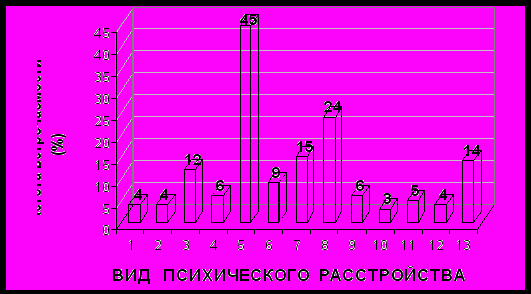
Рисунок 2. Структура нервно-психической патологии по данным методики PRIME-MD у больных с цереброваскулярной патологией (n=100).
1 – дистимия; 2 – БДР; 3 – ГТР; 4 – МДР (как сопутствующее состояние); 5 – ПА (как сопутствующее состояние); 6 - ГТР + ПА; 7 - сочетание ГТР и БДР; 8 - ГТР + БДР + ПА; 9 - дистимия + ГТР; 10 - дистимия + ГТР + ПА; 11 - МДР + ГТР + ПА; 12 - МДР + ГТР; 13 - нет диагноза (здоровы)
Сравнительный анализ показал (рис.3), что у больных в группе АФА(-) изолированное ГТР встречалось чаще (20%), чем в группе АФА (+) (6%) (р<0,01). У этих же больных зарегистрирован более высокий процент (36%) тяжелой сочетанной психической патологии (ГТР + БДР + ПА), чем в другой группе (20%) (р<0,01). Согласно критериям DSM – IV ПА встречались у больных группы АФА (-) значительно чаще (55%), чем в группе АФА(+) (35%) (р<0,05). Пациенты в группе АФА(+) чаще демонстрировали заболевания депрессивного спектра (БДР или дистимия). Наиболее часто в этой группе выявлялась сочетание БДР и ГТР (р<0,05). Не было выявлено психической патологии у 17% больных в группе АФА(+) и у 10% в группе АФА(-) (р<0,01) из чего следует, что у больных с атеросклеротическими изменениями церебральных артерий риск развития сопутствующей психической патологии выше.
Таким образом, наиболее часто у обследованных больных выявлялась смешанная психическая патология. Полученные данные свидетельствовали об ассоциации депрессии с венозной дисциркуляцией головного мозга на фоне прокоагулянтной активности крови, вследствие циркуляции высоких титров АФА. Высокая частота депрессии обусловливала тенденцию к заниженной самооценке состояния своего здоровья у этой категории больных. Преобладание атеросклеротических изменений сосудов головного мозга у больных с ДЭ, по нашим данным, ассоциировалось с преобладанием тревожной симптоматики и повышением риска развития панических расстройств.
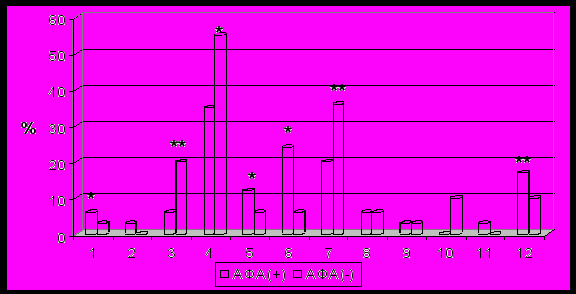
Рисунок 3. Распределение психической патологии по данным методики PRIME-MD у больных в группах сравнения, * - р<0,05 ** - р<0,01.
1 – дистимия; 2 – БДР; 3 – ГТР; 4 - ПА (как сопутствующее состояние); 5 - ГТР + ПА; 6- сочетание ГТР и БДР; 7 - ГТР + БДР + ПА; 8 - дистимия + ГТР; 9 - дистимия + ГТР + ПА; 10 - МДР + ГТР + ПА; 11 - МДР + ГТР; 12 - нет диагноза (здоровы)
Выраженность депрессивных расстройств по шкале Гамильтона в среднем не превышала степени субдепрессии (13,7±5,8 балла). Согласно градации шкалы Гамильтона (Guelfi G.D., 1993), у 40% больных была выявлена выраженная депрессия, у 45% депрессия соответствовала малому депрессивному эпизоду, 15% пациентов депрессии не имели. Анализ результатов клинического обследования по шкале Гамильтона свидетельствовал о преобладании в структуре аффективных расстройств симптомов психической и соматической тревоги. Достоверных различий результатов по шкале Гамильтона в группах сравнения выявлено не было. Отмечен прямой параллелизм между тяжестью депрессии (по шкале Гамильтона) и титрами At к β2-GPI (r=0,30; p<0,05) и АКЛ (r=0,39; p<0,05). Выявленные ассоциации между высокими титрами АФА и депрессией не противоречили данным других исследователей (Maes M. et al., 1991,1993).
В структуре личности обследованных больных выраженность алекситимического радикала в среднем по группе достоверно превышала нормативный показатель по шкале TAS – 69,8±10,8 балла (p<0,05). Очерченный алекситимичный радикал имели 30% пациентов (показатель TAS свыше 74 баллов), что расценивалось как выраженная алекситимия , 42% больных набрали от 62 до 74 баллов, что соответствовало пограничному уровню. Среди больных с выраженной алекситимией преобладали лица мужского пола (1,5:1). У 28% больных алекситимии выявлено не было (менее 62 баллов по TAS). Таким образом, у 72% больных с хронической цереброваскулярной патологией отмечается наличие алекситимического радикала в структуре личности. Корреляционный анализ выявил наличие прямого параллелизма между уровнем алекситимии и выраженностью депрессии у больных мужского пола (r=0,49; p<0,05), что свидетельствовало о значимости алекситимии как фактора риска депрессии в этой гендерной группе. Среди больных с выраженной алекситимией наибольший процент (18%) составили пациенты с ДЭ II стадии (у больных с НПНКМ и ДЭ I стадии по 6%) (р<0,05). Пограничный уровень алекситимии отмечен у 17% с ДЭ II стадии и в меньшей степени у - больных с ДЭ I стадии (14%) (р<0,05) и НПНКМ (11%) (р<0,05). Если рассматривать алекситимию как первичную врожденную личностно-психологическую характеристику, повышающую риск психосоматических расстройств, то можно предположить, что она способствует сосудистым нарушениям, и для пациентов с первичной алекситимией характерно более раннее развитие симптомов сосудисто-мозговой недостаточности, на фоне которой может происходить дальнейшее нарастание алекситимии уже как вторичной характеристики, отражающей реакцию на болезнь. Результаты исследование феномена алекситимии в группах сравнения представлены в таблице 2.
Таблица 2.Оценка уровня алекситимии по группам сравнения.
| | Все больные (n=100) | 1 группа АФА (+) (n=34) | 2 группа АФА (-) (n=31) |
| Средний возраст | 46,9±12,3 | 45,7±12,2 | 48,2±12,1 |
| Средний балл по TAS | 67,9+ 10,3 | 65,8+ 9,0 | 69,0+ 10,0 |
| Выраженная алекситимия (более 74 баллов) | 30% | 17,7%* | 32,3% |
| Пограничный уровень (62-74 балла) | 42% | 58,8%** | 38,7% |
| Отсутствие алекситимии (менее 62 баллов). | 28% | 23,5%* | 29,0% |
Примечания. Различия статистически значимы по сравнению с результатами по всей выборке: * - р<0,05 ** - р<0,01.
В группе АФА(+) реже (17,7%) выявлялась выраженная алекситимия (p<0,05), а отсутствие алекситимии наблюдалось у 23,5% больных (p<0,05). У этой категории больных отмечен более высокий процент (58,8%) пограничных показателей алекситимии по сравнению с больными АФА(-) (38,7%) (p<0,05), а корреляционный анализ выявил прямую взаимосвязь алекситимии с возрастом (r=0,4; p<0,05). Если расценивать алекситимию как вторичную характеристику, можно предположить, что венозные нарушения в системе мозгового кровообращения, ассоциированные с циркуляцией высоких титров АФА, способствуют появлению алекситимии, а на фоне развития атеросклеротических изменений церебральных сосудов происходит ее дальнейшее прогрессирование.
В ходе исследования личностно-психологических характеристик больных обнаружена повышенная по сравнению со здоровой популяцией напряженность большинства вариантов психологической защиты как глубинного внутриличностного образования, направленного на нивелирование тревоги. У обследованных больных (n=100) выявлено доминирование таких механизмов защиты, как «отрицание», «вытеснение», «интеллектуализация» и «реактивные образования» (p<0,05) и снижение выраженности «компенсации» и «замещения»(p<0,05).
Анализ механизмов психологической защиты в группах сравнения (рис.4) показал, что в группе АФА(+) отмечалось повышение выраженности таких механизмов, как «отрицание» и «реактивные образования», свидетельствовавшее о том, что для этих больных характерным является повышенная степень отрицания существующих проблем, либо подмена неприемлимых для осознания побуждений гипертрофированными, противоположными установками. Вытеснение в бессознательное психотравмирующей ситуации, смещение агрессии на более безопасный объект, бессознательное отражение собственных эмоционально неприемлимых мыслей, свойств и желаний и приписывание их другим людям не было характерно для этих больных, что проявлялось уменьшением выраженности механизмов «вытеснение», «замещение» и «проекция» даже по сравнению с нормативными данными (p<0,05). Повышение титра At к AnV ассоциировалось со снижением выраженности механизма «вытеснение» (r=-0,46; p<0,05).
В группе АФА(-) также отмечалось доминирование механизмов «отрицание» и «реактивные образования». Кроме того, у этих больных были выражены такие механизмы психологической защиты, как «регрессия», свидетельствующая о неосознанном нисхождении к ранним или более незрелым формам поведения и удовлетворения потребностей в проблемной ситуации; «компенсация», онтогенетически самый поздний и когнитивно сложный защитный механизм, предполагающий попытку преодоления реальных и воображаемых недостатков; «интеллектуализация», предполагающая произвольную схематизацию и истолкование событий для развития чувства субъективного контроля над любой ситуацией. Напряженность механизмов «регрессия» и «компенсация» выявлена только в этой группе, можно предположить, что данные виды психологической защиты характерны преимущественно для больных с церебральным атеросклерозом.
В группе обследованных больных (n=100) было выявлено наличие прямого параллелизма между выраженностью депрессии (по шкале Гамильтона) и наличием психологической защиты по типу «регрессии» (r=0,48, p<0,05) и «замещения» (r=0,30, p<0,05). В группах сравнения также отмечалась эта зависимость: в группе АФА(+) (r=0,45 и r=0,45; p<0,01), АФА(-) (r=0,44 и r=0,30; p<0,01). Полученные данные позволяют констатировать тот факт, что механизмы защиты по типу «регрессии» и «замещения» являлись самыми неблагоприятными для больных с ДЭ, повышая у них риск развития депрессии. Механизм «реактивные образования» напрямую зависел от возраста, причем в группе АФА(+) эта связь была выражена сильнее (r=0,51; p<0,01), чем в группе АФА(-)(r=0,30; p<0,01), что свидетельствовало об ослаблении этого механизма психической защиты на фоне прогрессирования с возрастом атеросклеротических изменений. Напряженность механизма «интеллектуализация» с возрастом наблюдалась в обеих группах (r=0,40 в АФА(+) и r=0,37 в АФА(-) p<0,05). Выявлено наличие прямого параллелизма между выраженностью алекситимии и наличием психической защиты по типу «вытеснения» в группе АФА(+) и во всей выборке (r=0,3; p<0,05), что свидетельствует о большей проявленности данного механизма соматизации у пациентов с ДЭ и преобладанием венозных нарушений на фоне высоких титров АФА. В группе АФА(+) была получена обратная корреляционная связь механизма «отрицание» с алекситимией (r=-0,45; p<0,05) и депрессией (r=-0,50; p<0,01). Этот факт свидетельствует о том, что, подавляя механизм «отрицание», алекситимия косвенно могла способствовать развитию депрессии у данной категории больных. Прямая зависимость между напряженностью психологических защит и выраженностью депрессии по результатам шкалы Гамильтона во всем массиве наблюдений (r=0,37; p<0,05) и в обеих группах сравнения (в АФА(+): r=0,39; p<0,05; в АФА(-): r=0,32; p<0,05) указывает на психогенный компонент аффективных нарушений у больных с хронической цереброваскулярной патологией.
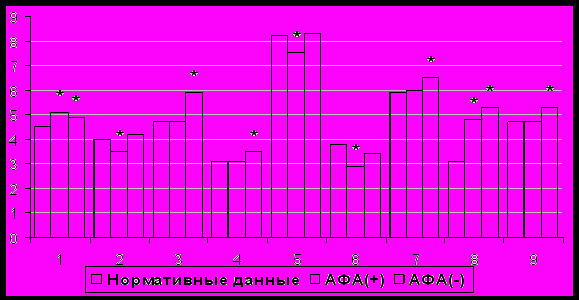
Рисунок 4. Психологическая защита у больных с хронической недостаточностью мозгового кровообращения в группах сравнения («сырые» баллы по ИЖС).
1 – отрицание; 2 – вытеснение; 3 – регрессия; 4 – компенсация; 5 – проекция; 6 – замещение; 7 – интеллектуализация; 8 – реактивные образования; 9 – степень напряженности защит. Примечание: * p<0,05 по сравнению с нормативными данными
КЖ обследованных больных (n=100) было достоверно снижено по сравнению с показателями здоровых лиц, особенно по параметрам ограничивающего влияния физического состояния RP (р<0,01) и болевого синдрома на ролевое функционирование BP (р<0,01). Обращало на себя внимание значительное снижение показателя удовлетворенности уровнем социального функционирования - общения SF (р<0,01). Исследование показало: чем более был выражен алекситимический радикал личности, тем ниже было КЖ по параметру общей оценки психического здоровья MH (r=-0,34; p<0,05). Получена обратная корреляционная связь ГГЦ и способности к физическим нагрузкам PF (r=-0,31; p<0,05). Можно предположить, что ГЦ, за счет своего негативного влияния на систему кровообращения является фактором, способствующим астенизации организма в целом.
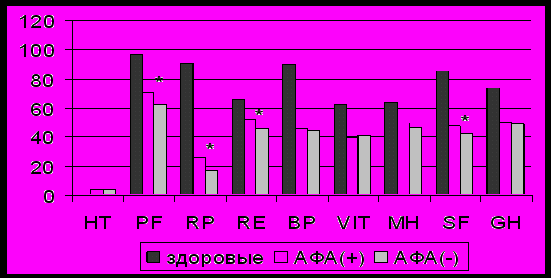
Рисунок 5. КЖ больных в группах сравнения по SF-36.
Параметры КЖ: НТ - оценка своего состояния в динамике за год; PF-способность к физическим нагрузкам; RP - влияние физического состояния на ролевое функционирование; ВР - ограничивающее влияние на функционирование болевого синдрома; GH - общее состояние здоровья; VIT -физическая активность, энергичность; SF - социальное функционирование; RE - влияние эмоционального состояния на ролевое функционирование; МН - психическое здоровье в целом.
Примечание: * - p<0,05 достоверность различий между группами сравнения
Анализ КЖ группах сравнения (рис.5) показал, что больные в группе АФА(-) отличались в худшую сторону практически по всем параметрам по сравнению с группой АФА(+), особенно по самооценке физического состояния RP (р<0,05), влиянию эмоционального состояния на ролевое функционирование RЕ (р<0,05), способности к физическим нагрузкам PF (р<0,05), социальному функционированию SF (р<0,05), что может быть обусловлено повышением тяжести ДЭ на фоне прогрессирования атеросклеротических изменений сосудов (нарастанием очаговой неврологической симптоматики, развитием психоорганического синдрома). Корреляционный анализ выявил наличие четкой взаимосвязи между уровнем депрессии по шкале Гамильтона и выраженностью некоторых параметров КЖ в обеих группах, что свидетельствует об отрицательном влиянии сопутствующей депрессии на КЖ больных. В группе АФА(+) депрессия негативно влияла не только на физическое функционирование RP (r=-0,36, р<0,05) и физическую активность VIT (r=-0,62, р<0,01), но также значительно ухудшала эмоциональное состояние RE (r=-0,69, р<0,001) и психическое здоровье в целом МН (r=-0,68, р<0,001). У больных в группе АФА(-) развитие депрессии снижало физическую активность VIT (r=-0,50, р<0,05) и социальное функционирование SF (r=-0,5, р<0,01), ухудшало самооценку больным состояния здоровья GH (r=-0,56, р<0,01), однако в меньшей степени, чем в группе АФА(+) влияло на психическое здоровье в целом МН (r=-0,46, р<0,05). В ходе исследования были выявлены взаимосвязи между параметрами качества жизни и механизмами психологической защиты, что может стать плацдармом для разработки методов психотерапевтической коррекции у пациентов ДЭ, так как компенсация психологической защиты будет способствовать улучшению качества жизни больных.
В задачи исследования входила коррекция психических расстройств у пациентов с ДЭ и оценка влияния психофармакотерапии на качество жизни и эффективность лечебных мероприятий. В связи с тем, что клинико-феноменологические особенности больных характеризовались преобладанием тревожно-депрессивной симптоматики, для исследования был выбран - антидепрессант (тразодон). Оценка динамики состояния проводилась через 10 дней и через 1 месяц после начала приема препарата. Титрование дозы проводилось индивидуально согласно инструкции к препарату. Останавливая свой выбор на препарате тразодон, мы рассчитывали на следующие эффекты: 1) уменьшение или регресс тревожно-депрессивной симптоматики благодаря антидепрессивному, анксиолитическому эффектам; 2)уменьшение соматических симптомов тревоги и депрессии (головные боли, сердцебиение, потливость, гипервентиляция и т.д.); 3) коррекция нарушений сна вследствие легкого седативного эффекта. Убедительным доказательством эффективности включения психофармакотерапии в комплексное лечение больных (рис.6) служило значительное уменьшение количества жалоб по данным Опросника пациента методики PRIME-MD (р<0,01), снижение выраженности депрессии по результатам тестирования с использованием шкалы Гамильтона (р<0,01) и Госпитальной шкалы депрессии и тревоги (р<0,01).
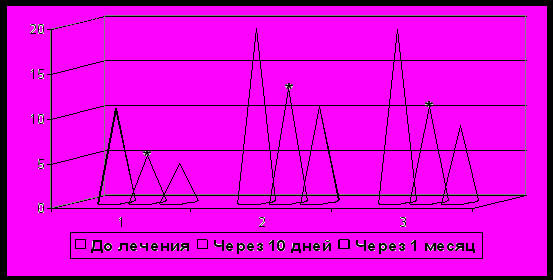
Рисунок 6. Динамика состояния на фоне приема антидепрессанта (* p<0,01 через 10 дней)
1. Количество жалоб по данным «Опросника Пациента» методики PRIME-MD; 2. Госпитальная шкала депрессии и тревоги; 3. Шкала депрессии Гамильтона.
У 6 больных с лабильностью артериального давления в первые дни приема наблюдались легкие ортостатические реакции, не потребовавшие отмены препарата. Уменьшение диссомнии наблюдалось уже на 2-3 день, что способствовало улучшению эмоционального состояния больного и, как следствие, улучшению его соматического состояния. Благодаря легкому гипотензивному эффекту тразодона у больных быстрее стабилизировался уровень артериального давления.
На фоне приема препарата отмечался значительный регресс (рис.7) симптомов, характерных для основного неврологического заболевания (головокружение, головные боли, нарушения сна, ухудшение памяти и т.д.).
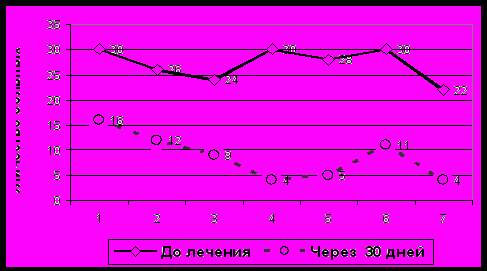
Рисунок 7. Динамика регресса жалоб, связанных с неврологическим заболеванием на фоне психофармакотерапии (p<0,01)
1 – головные боли; 2 – головокружение; 3 – ухудшение памяти; 4 – нарушения сна; 5 – нарушение концентрации внимания; 6 –повышенная утомляемость; 7 –шум в голове
Больные отмечали улучшение памяти, что было связано с улучшением способности к концентрации внимания вследствие нивелирования тревоги и способствовало нормализации когнитивных функций. Полученные данные косвенно свидетельствовали, что у подавляющего большинства больных клиническая картина ХНМК была в значительной степени обусловлена сопутствующим тревожно-депрессивным синдромом.
Таблица 3. Показатели качества жизни у пациентов на фоне
психофармакотерапии
| ШКАЛЫ SF-36. | До лечения | 30-сутки |
| PF-способность к физическим нагрузкам | 24,2±2,28 | 25,1±2,24 |
| RP-влияние физического состояния на ролевое функционирование | 24,3±2,17 | 36,6±2,32* |
| ВР-ограничивающее влияние на функционирование болевого синдрома | 47,6±3,41 | 51,6±3,84* |
| GH-общее состояние здоровья | 31,6±2,64 | 54,6±2,45** |
| VIT-физическая активность, энергичность | 32,9±2,56 | 56,3±2,98** |
| SF-социальное функционирование | 35,4±2,15 | 41,5±2,23* |
| RE-влияние эмоционального состояния на ролевое функционирование | 34,2±2,82 | 55,2±2,4** |
| МН-психическое здоровье в целом | 28,6±2,12 | 45,9±3,14** |
Примечание. * - р<0,05; ** - р<0,01 достоверная разница показателей на фоне терапии
Улучшение психического состояния сопровождалось улучшением качества жизни, что было зафиксировано при обследовании с помощью опросника SF-36 (табл. 3). Особенно изменялись в лучшую сторону следующие параметры: влияние эмоционального состояния на ролевое функционирование, способность к физическим нагрузкам, социальное функционирование, психическое здоровье в целом - то есть основные показатели психического и физического состояния пациента. Несмотря на то, что на фоне приема антидепрессанта в неврологическом статусе не было отмечено существенной динамики, самочувствие больных становилось лучше за счет нивелирования тревожно-депрессивного синдрома и регресса субъективной симптоматики.
