Идеальная жидкость
| Вид материала | Документы |
- Профессор Валерий Кирилович Кедринский Динамика одиночной полости в жидкости (математические, 40.82kb.
- Исследование адсорбции пав на границах раздела жидкость-газ и жидкость-твердое тело, 40.56kb.
- Идеальная пара для стимуляции и синхронизации охоты у коров, 170.7kb.
- Мама, папа, я – идеальная семья, 31.08kb.
- Список принятых докладов, 185.98kb.
- Идеальная модель экономического устройства общества предполагает использование механизма, 26.68kb.
- Назначение фильтров и их место в измерительной системе, 159.98kb.
- Краткий справочник по проектированию и бурению скважин на воду, 2392.28kb.
- Алексушин И. Н, 128.72kb.
- В. В. Радаев Рынок как идеальная модель и форма хозяйства, 285.76kb.
ИЗОМОРФИЗМ (от греч. isos — равный, одинаковый и morphe — форма, вид), полное подобие атомно-крист. строения и внеш. огранки кристаллов у в-в с одинаковой (по соотношению компонент) хим. ф-лой и одинаковым типом хим. связи. Открыт в 1819 нем. химиком Э. Мичерлихом на примере кристаллов КН2РO4, KH2AsO4 и NH4H2PO4. И. наз. также связанное с существованием изоморфных кристаллов св-во разл. атомов, ионов и их сочетаний замещать друг друга в крист. решётке с образованием кристаллов перем. состава (твёрдых растворов замещения). Пример совершенного И.— кристаллы квасцов КАl(SO4)•12Н2O, в к-рых одновалентные ионы К могут в любом кол-ве замещаться одновалентными ионами Rb, NH4 и др., имеющими прибл. одинаковый с ионами К кристаллохим. радиус, а трёхвалентные ионы Аl — трёхвалентными ионами Fe, Cr и др. с радиусами, близкими к радиусу Аl. Различие в кристаллохим. радиусах атомов в изоморфных кристаллах не превышает 10—15%.
Кроме совершенного (полного) И. с образованием тв. р-ров при любых соотношениях компонент, возможен ограниченный (по возможным концентрациям) И.; примером такого рода могут служить соединения BaSO4 и КМnО4. Различают изовалентный И., когда замещающие друг друга атомы или группировки имеют одинаковую валентность (напр., Na+ , К+ , NH4+), и гетеровалентный, когда валентность их различна (напр., Са2+ и Y3+ ). В последнем случае важна близость размеров замещающих друг друга атомов, а различие зарядов компенсируется вакансиями.
И. наблюдается у мн. минералов и кристаллов, используется при синтезе кристаллов, когда введением малых добавок существенно меняют или создают новые св-ва. Так, введение малых изоморфных добавок, напр. Сг3+ в корунд Al2O3, Nd3+ в гранат Y3Al5O12, превращает их в активную среду для квант. генераторов; введение изоморфных примесей в ПП кристаллы изменяет тип проводимости.
211
Изоморфные примеси используют, напр., для изменения окраски ювелирных кристаллов.
• См. лит. при ст. Кристаллохимия.
Б. К. Вайнштейн.
ИЗОСПИН, то же, что изотопический спин.
ИЗОТЕРМА (от греч. isos — равный, одинаковый и therme — тепло), линия на термодинамич. диаграмме состояния, изображающая изотермический процесс. Ур-ние И. идеального газа: pV=const, где р — давление, V — объём газа. Т. о., в координатах р, V И. представляет собой гиперболу. Для реального газа ур-ние И. имеет более сложный хар-р и переходит в ур-ние И. идеального газа только при малых давлениях или высоких темп-pax. В координатах р, V у И. ход всегда менее крут, чем у адиабаты. См. Ван-дер-Ваальса уравнение.
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС, процесс, происходящий в физ. системе при пост. темп-ре; на термодинамич. диаграммах состояния изображается изотермой. Для осуществления И. п. систему обычно помещают в термостат, теплопроводность к-рого велика, так что темп-pa системы практически не отличается от темп-ры термостата. Можно осуществить И. п. иначе: с применением источников или стоков теплоты, контролируя постоянство темп-ры с помощью термометров. К И. п. относятся, напр., кипение жидкости или плавление тв. тела при пост. давлении. В идеальном газе при И. п. произведение давления на объём постоянно (см. Бойля — Мариотта закон). При И. п. системе, вообще говоря, сообщается определ. кол-во теплоты (или она отдаёт теплоту) и совершается внеш. работа. Для идеального газа эта работа равна NkTln(V2/V1), где N — число ч-ц газа, Т — абс. темп-pa, V1 и V2— объём газа в начале и конце процесса. В тв. теле и большинстве жидкостей И. п. очень мало изменяет объём тела, если только не происходит фазовый переход.
ИЗОТОПИЧЕСКАЯ ИНВАРИАНТНОСТЬ, особая симметрия, присущая сильному взаимодействию элем. ч-ц. Существующие в природе ч-цы, обладающие сильным вз-ствием (адроны), можно разбить на группы «похожих» ч-ц, в каждую из к-рых входят ч-цы с примерно равными массами и одинаковыми внутр. хар-ками (спином, внутр. чётностью, барионным зарядом В, странностью S, «очарованием» С, «красотой» B, за исключением электрич. заряда). Такие группы наз. изотопическими мультиплетами. Сильное вз-ствие для всех ч-ц, входящих в один изотопич. мультиплет, одинаково, т. е. не зависит от электрич. заряда; в этом и состоит одно из проявлений симметрии сильного вз-ствия, наз. И. и.
Простейший пример ч-ц, к-рые могут быть объединены в один изотопич. мультиплет: протон (р) и нейтрон (n). Опыт показывает, что сильное вз-ствие протона с протоном, нейтрона с нейтроном и протона с нейтроном одинаково (если они находятся соответственно в одинаковых состояниях); это послужило исходным пунктом для установления И. и. Протон и нейтрон рассматриваются как два разных зарядовых состояния одной ч-цы — нуклона; они образуют изотопич. дублет. Другие примеры изотопич. мультиплетов: пи-мезоны (+, °, -)и -гипероны (+ ,°, -), образующие изотопич. триплеты, К-мезоны (К+, К°) и анти-К-мезоны (К-, К°), образующие два изотопич. дублета.
Электрич. заряд Q ч-цы, входящей в изотопич. мультиплет, выражается ф-лой Гелл-Мана — Нишиджимы:
Q = I3+1/2Y;
величина Y была названа гиперзарядом и до открытия в 70-х гг. новых адронов считалась равной: Y=B+S (обобщение ф-лы для Y см. в ст. Элементарные частицы). В этой ф-ле величина I3 пробегает с интервалом в единицу все значения от нек-рого максимального значения 7 (целого или полуцелого) до минимального, равного -I. Общее число значений, к-рые может принимать I3 (и Q) для данного изотопич. мультиплета, а следовательно, и число ч-ц в изотопич. мультиплете, равно 2 7+1. Величина I, определяющая это число, наз. изотопическим спином, а I3— третьей «проекцией» (или просто проекцией) изотопич. спина (названия связаны с формальной матем. аналогией с обычным спином ч-ц J и его проекцией Jz). Т. к. нуклоны существуют в двух зарядовых состояниях, то для них (и для всех др. ч-ц, входящих в изотопич. дублеты) 2I+1=2, т. е. I=1/2, а I3, может принимать два значения: +1/2 для протона (что соответствует Q=+1) и -1/2 для нейтрона (Q=0). Изотопич. триплету пионов соответствует I=1, а I3 равно +1 для + , 0 для ° и -1 для -. Ч-цы с I=0 не имеют изотопич. «партнёров» и явл. изотоппч. синглетами; к таким ч-цам относятся, напр., гипероны ° и -. Переход от одной ч-цы к другой из того же изотопич. мультиплета, не меняя величины изотопич. спина, меняет его проекцию; поэтому такой переход формально можно представить как поворот в условном «изотопическом („зарядовом") пр-ве». Тот факт, что сильное вз-ствие ч-ц, входящих в определ. изотопич. мультиплет, одинаково: не зависит от Q, т. е. от «проекции» изотопич. спина I3, можно интерпретировать как независимость (инвариантность) сильного вз-ствия от вращений в «изотопич. пр-ве» [или как существование группы симметрии
SU (2)]. Это утверждение явл. наиб. общей формулировкой И. и., и из него следует закон сохранения изотопич. спина в сильном вз-ствии (аналогично тому, как из независимости законов механики относительно вращений в обычном пр-ве следует закон сохранения момента кол-ва движения). На основе И. и. удаётся предсказать существование, массу и заряды новых ч-ц, если известны их изотопические «партнёры». Так было предсказано существование °, °, ° по известным +, -; + -;-.
И. и. имеет место и для составных систем адронов, в частности для ат. ядер. Изотопич. спин сложной системы складывается из пзотопич. спннов входящих в систему ч-ц, при этом сложение производится по тем же правилам, что и для обычного спина. Так, система из двух ч-ц с изотоппч. спинами 1/2 (напр., нуклон) и 1 (напр., -мезон) может иметь изотопич. спин I=1+1/2=3/2 или I=1-1/2=1/2. В ядрах И. и. проявляется в существовании уровней энергии с одинаковыми квант. числами для разл. изобар. Примером служат ядра 146С, 147N, 148O: осн. состояния ядер 14С, 14O и первое возбуждённое состояние 14N образуют изотопич. триплет (7=1; рис.). Все квант. числа

J=1, I=0
этих уровней одинаковы, а различие в их энергиях можно объяснить разницей электростатич. энергий из-за различия в электрич. зарядах ядер. (Осн. уровень 14N имеет изотопич. спин 7=0, поэтому у него нет аналогов в ядрах 14С и 14О.)
Из И. и. следует закон сохранения полного изотопич. спина I в процессах, обусловленных сильным вз-ствием. Этот закон приводит к определ. соотношениям между вероятностями процессов для ч-ц, входящих в один изотопич. мультиплет, а также к запрету нек-рых реакций в процессах сильного вз-ствия. Комбинация И. и. и зарядового сопряжения приводит к сохраняющейся в сильном вз-ствии величине (для ч-ц с B=S=C=b=0)— G-чётностн.
И. и. заведомо нарушается эл.-магн. вз-ствием, зависящим от электрич. зарядов ч-ц (т. е. от I3), «сила» к-рых по порядку величины составляет прибл. 1% от сильного вз-ствия. Другой источник нарушения И. и.— различие в массах u- и d-кварков, входящих в состав адронов. Указанные причины приводят к небольшому
212
различию в массах ч-ц одного изотопич. мультиплета.
И. и. представляет собой часть более широкой приближённой симметрии сильного вз-ствия — унитарной симметрии SU (3). См. Элементарные частицы.
С. С. Герштейн.
ИЗОТОПИЧЕСКИЙ МУЛЬТИПЛЕТ,
см. в ст. Изотопическая инвариантность.
ИЗОТОПИЧЕСКИЙ СПИН (изоспин, I), одна из внутр. хар-к (квант. чисел) адронов, определяющая число зарядовых состояний адрона (или число ч-ц n в изотопич. мультиплете): n=2I+1. См. Изотопическая инвариантность.
ИЗОТОПИЧЕСКИЙ ЭФФЕКТ, зависимость критич. темп-ры Тк сверхпроводящего металла от его изотопного состава; Тк возрастает при уменьшении ср. ат. массы М в-ва. Для ряда металлов при этом выполняется соотношение Тк •M1/2=const. Впервые И. э. наблюдался в 1950; было установлено, что у изотопа 198Hg Tк=-4,156 К, а у чистой ртути, имеющей естеств. изотопный состав со ср. ат. массой 200,6, Tк=4,177 К. Исследования показали также, что одновременно с Тк изменяется критическое магнитное поле Hк,0 (при Т0 К), по отношение Нк,0/Тк для разных изотопов данного сверхпроводящего металла остаётся постоянным. И. э. свидетельствует, что сверхпроводимость связана с массой образующих решётку ч-ц и обусловлена вз-ствием эл-нов с фононами (колебаниями решётки).
ИЗОТОПНАЯ ХРОНОЛОГИЯ, определение абс. возраста горных пород, минералов, следов древних человеческих культур и в целом Земли по накоплению в них продуктов распада радионуклидов (см. Радиоактивность). Идея И. х. принадлежит франц. физику П. Кюри и англ. физику Э. Резерфорду. При И. х. учитывают, что радио-акт. распад каждого радионуклида происходит с пост. скоростью и приводит к накоплению конечных стабильных нуклидов, содержание к-рых D связано с возрастом t исследуемого объекта соотношением: D = P(et-1), где Р — число атомов радионуклида, К — постоянная распада. Отсюда возраст t равен
t =1/lln(1+D/P).
В И. х. наиб. распространены свинцовый, аргоновый, стронциевый и углеродный методы. В первом используется накопление радиогенного свинца в результате распадов 238U206Pb;
235U207Pb и 232Th208Pb (см. радиоактивные ряды). Аргоновый метод основан на радиогенном накоплении Ar в калиевых минералах (40КЭЗ 40Ar, где эз — электронный захват). Стронциевый метод основан на бета-
распаде 87Rb- 87Sr. Для оценки возраста объектов меньше чем 60 000 лет
используется радиоуглеродныи метод. В земной атмосфере под действием нейтронов косм. лучей идёт яд. реакция: 14N(n,p) l4C. В результате воздух, растения и животные содержат радионуклид 14С (T1/2=5700 лет) в определённой и постоянной (в расчёте на 1 моль атомов С) концентрации. В мёртвых организмах обмен с атмосферой прекращается, и содержание 14С постепенно падает. По концентрации 14С можно установить возраст органич. остатков.
ИЗОТОПНЫЕ ИНДИКАТОРЫ (меченые атомы), вещества, имеющие отличный от природного изотопный состав, используемые в кач-ве «метки» при исследовании разл. процессов (в т. ч. в живом организме). Метод И. и. был предложен венг. радиохимиком Д. Хевеши и нем. химиком Ф. Панетом (1913). В кач-ве изотопной «метки» чаще используются радиоакт. изотопы, к-рые могут быть легко обнаружены и измерены количественно. Реже используются стабильные изотопы, техника обнаружения к-рых сложна (см. Mace-спектроскопия). В кач-ве радиоакт. «меток» применяют нуклиды: 3Н, 14С, 32Р, 35S, 45Ca, 59Fe, 60Со, 89Sr,95Zr, 95Nb, 110mAg, 131I и др. Выбор радионуклида определяется гл. обр. периодом его полураспада, типом и энергией излучения. Для обнаружения излучения используют обычно газоразрядные счётчики, сцинтилляционные счётчики, ядерные фотографические эмульсии (см. Авторадиография) и др. детекторы ч-ц. С помощью И. и. изучают распределение в-в в системе и пути их перемещения. В этих случаях И. и. вводят в систему и через определ. промежутки времени устанавливают их наличие в разл. частях системы. Для количеств. анализа пользуются, напр., методом изотопного разбавления, при к-ром к анализируемой пробе добавляют порцию меченого в-ва и по степени его разбавления судят о содержании анализируемого в-ва в пробе. Введение И. и. в определ. место молекулы делает различимыми атомы одного элемента и позволяет выяснить механизм хим. реакций и структуру молекул. Метод И. и. широко используется в физике, химии, биологии (процессы синтеза и распада хим. соединений в живой клетке, обмена в-в и др.), в технике, медицине (изотопная диагностика) и др.
• В а н г Ч., У и л л и с Д., Радиоиндикаторный метод в биологии, пер. с англ., М., 1969; Радиоактивные индикаторы в химии. Основы метода, 2 изд., М., 1975; Радиоактивные индикаторы в химии, М., 1977.
ИЗОТОПОВ РАЗДЕЛЕНИЕ, выделение отд. изотопов из естественной их смеси или обогащение смеси отд. изотопами. Первые попытки И. р. производились гл. обр. для обнаружения изотопов у стабильных элементов, для точного измерения массы их атомов и относит. содержания (см. Масс-спектроскопия). В 30-х гг. фундам. исследования в области яд. физики потребовали получения изотопов, что тогда даже в кол-вах порядка неск. мг являлось сложной задачей. Выделялись лишь небольшие кол-ва обогащённых смесей изотопов лёгких элементов. Только дейтерий начал производиться в пром. масштабах. Дальнейшее развитие техники И. р. было обусловлено появлением ядерных реакторов, для к-рых требовался U, обогащённый 235U (см. Ядерное топливо). Существует множество методов И. р. Все они основаны на различиях в св-вах изотопов и их соединений, связанных с различием масс их атомов. Для большинства элементов относит. разность масс изотопов весьма мала, что определяет сложность задачи. Эффективность методов И. р. характеризуется коэфф. разделения . Для смеси двух изотопов он равен:

где с' и 1-с' — относит. содержания лёгкого и тяжёлого изотопов в обогащённой смеси, а с" и 1-с" — в исходной смеси. Если а лишь немного больше единицы, то операцию И. р. приходится многократно повторять; только при эл.-магн. разделении >>1 (см. ниже).
Газовая диффузия через пористые перегородки. Газообразное соединение разделяемого элемента при достаточно низких давлениях (~10-3 мм рт. ст.
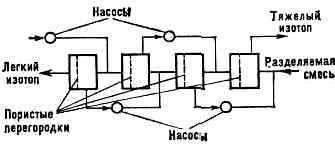
Рис. 1. Схема устройства для разделения изотопов методом газовой диффузии.
или ~0,1 Па) прокачивается через пористую перегородку (рис. 1). Лёгкие молекулы диффундируют через перегородку быстрее тяжёлых. В результате газ обогащается лёгкой компонентой по одну сторону перегородки и тяжёлой — по другую. Если разница в массах мала, то необходимо повторять процесс неск. тыс. раз. Этот метод используется на спец. газодиффуз. заводах для обогащения U (в виде газообразного UF6) изотопом 235U (~1,0043). Для получения нужной концентрации 235U требуется ок. 4000 операций разделения.
Диффузия в потоке пара (масс-диффузия). И. р. происходит в цилиндрич. сосуде (колонне), перегороженном вдоль оси диафрагмой, содержащей ок. 103 отверстий на 1 см2 (рис. 2). Газообразная изотопная смесь движется навстречу потоку вспомогат. пара. Вследствие перепада концентраций газа и пара в поперечном сечении ци-
213
линдра и большего коэфф. диффузии для более лёгких молекул происходит обогащение лёгким изотопом части газа, прошедшего сквозь поток пара в левую часть цилиндра. Обогащённая часть выводится из верхнего цилиндра вместе с осн. потоком пара, а оставшаяся в правой половине часть газа

Рис. 2. Схема устройства для разделения изотопов методом противопоточной масс-диффузий.
движется вдоль диафрагмы и выводится из аппарата. Пар конденсируется и отделяется от смеси изотопов. Процесс может осуществляться многократно. В лаб. условиях получают до 1 кг изотопов Ne, Ar, С, Kr, S. Термодиффузия. Разделит. колонка состоит из двух коаксиальных труб, поддерживаемых при разных темп-pax (рис. 3), между к-рыми находится газообразное в-во. Разность темп-р T создаёт вертик. конвекц. поток газовой смеси и одновременно вызывает непрерывно идущее поперечное термодиффуз. разделение изотопов
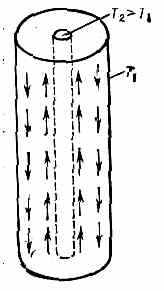
Рис. 3. Схема термодиффузионной разделит. колонки.
(см. Конвекция, Термодиффузия). Вследствие этого более лёгкие изотопы накапливаются у горячей поверхности внутр. трубы и движутся вверх. Коэфф. разделения =1+Т/Т, где — постоянная термодиффузии, зависящая от относит. разности масс изотопов, а Т=(Т1+Т2)/2. Этим методом были получены Не с содержанием 0,2% 3Не (в природной смеси — 1,5*10-5%), изотопы 18О, 15N, 13C,
20Ne, 22Ne, 35Cl, 84Kr, 86Kr с концентрацией >99,5%.
Дистилляция. Изотопы обычно имеют разл. давления насыщ. пара (p1 и р2) и точки кипения, поэтому возможно И. р. путём фракц. перегонки. При кипении жидкой смеси изотопов в образующемся паре преобладает изотоп с наименьшей темп-рой кипения. Используются фракционирующие колонны с большим числом ступеней разделения; а зависит от отношения p1/p2 и уменьшается с ростом мол. массы и темп-ры (процесс наиб. эффективен при низких темп-pax). Дистилляция использовалась при получении изотопов лёгких элементов 10В, 11B, 18O, 15N, 13С и для получения тяжёлой воды (сотен т в год).
Изотопный обмен. Для И. р. используются хим. реакции, при к-рых происходит перераспределение изотопов к.-л. элемента между реагирующими в-вами. Так, напр., если привести в соприкосновение HCl с HBr, в к-рых первонач. содержание дейтерия D в водороде было одинаковым, то в результате обменной реакции в HCl содержание D будет неск. выше, чем в HBr. Применение неск. каскадов позволяет получать дейтерий и обогащённые отд. изотопами смеси для др. лёгких элементов (N, S, О, С, Li).
Центрифугирование. В центрифуге, вращающейся с большой скоростью, более тяжёлые молекулы под действием центробежных сил концентрируются у периферии, а лёгкие молекулы — у ротора. Поток пара во внеш. части с тяжёлым изотопом направлен вниз, а во внутренней, с лёгким изотопом, вверх. Соединение неск. центрифуг в каскад обеспечивает необходимое обогащение. Центрифугирование пригодно для разделения изотопов как лёгких, так и тяжёлых элементов.
