Лекция по патологической физиологии
| Вид материала | Лекция |
- Расписание лекций по патологической физиологии на IV семестр 2011 2012 учебного года, 14.55kb.
- Расписание лекций по патологической физиологии на IV семестр 2011 2012 учебного года, 14.65kb.
- Программа по патологической физиологии кафедра общей патологии и патологической физиологии, 784.63kb.
- Введение в патологическую физиологию. Предмет, задачи, методы исследования патологической, 1024.74kb.
- Патология, 445.47kb.
- Подписано в печать Усл печ л. 5,0, 1162.15kb.
- Календарный план лекций по элективному курсу кафедры патологической физиологии Стгма, 30.57kb.
- Кафедра патологической физиологии, 390.26kb.
- И. П. Павлов в изучении вопросов физиологии никогда не отделял ее от патологической, 1115.78kb.
- Тестовые задания по патологической физиологии для обучения и контроля знаний, 2798.52kb.
Лекция по патологической физиологии
для студентов 3-го курса медицинского
факультета (специальности:
«Лечебное дело» и «Стоматология»)
Тема лекции: «Метаболический синдром (синдром Х). Этиология, патогенез, исходы»
- План лекции
1. Метаболический синдром: история изучения и определение понятия
2. Инсулинрезистентность и ее роль в развитии метаболического синдрома
3. Алиментарное ожирение абдоминального типа и метаболический синдром
4. Метаболический синдром и сердечно-сосудистая система
5. Дислепидемия как проявление метаболического синдрома
6. Сахарный диабет 2-го типа как заключительный этап развития метаболического синдрома
7. Исходы метаболического синдрома
- Из истории изучения метаболического синдрома. Определение понятия «метаболический синдром»
1. Г.Ривен (G.Reaven) в 1988 г. высказал предположение о том, что в основе значительного числа случаев возникновения артериальной гипертензии, сахарного диабета 2-го типа, атеросклероза и ишемической болезни сердца лежат инсулинорезистентность и гиперинсулинемия.
Он предложил для обозначения сочетания этих этиологических и патогенетических факторов термин «синдром Х».
В целом по данным Ривена синдром Х включает в себя гиперинсулинемию, инсулинорезистентность, повышение уровня холестерина и липопротеинов низкой плотности, понижение уровня липопротеинов высокой плотности и артериальную гипертензию.
2. Н.Каплан (N.M.Kaplan) в 1989 г., исследуя те же проблемы сердечно-сосудистой патологии, предложил термин «смертельный квартет» для объединения таких этиопатогенетических факторов как инсулинрезистентность и гиперинсулинемия, нарушение толерантности к глюкозе, алиментарное ожирение, артериальная гипертензия.
В настоящее время в патофизиологических и клинических работах данный симптомокомплекс чаще всего именуется как метаболический синдром или синдром Х
3. Таким образом, метаболический синдром характеризуется сочетанием нескольких метаболических дефектов, которые при отсутствии должного лечения с высокой вероятностью приводят к развитию таких тяжелых патологических состояний, как атеросклероз и сахарный диабет 2-го типа (инсулиннезависимый сахарный диабет).
- Клинические проявления метаболического синдрома
1. Инсулинрезистентность, гиперинсулинемия, нарушение толерантности к глюкозе
2. Алиментарное ожирение абдоминального типа
3. Артериальная гипертензия
4. Системный атеросклероз
5. Ишемическая болезнь сердца
6. Хроническая сердечная недостаточность
- Патогенетические механизмы развития инсунрезистентности и гиперинсулинемии
- Определение понятия «инсулинрезистентность»
- Определение понятия «инсулинрезистентность»
Инсулинрезистентность – это нарушение механизма биологического действия инсулина, сопровождающееся нарушением толерантности к глюкозе инсулинзависимых тканей и гиергликемией
- Инсулиновые рецепторы. Функции инсулина в клеточном метаболизме. Рецепторы глюкозы
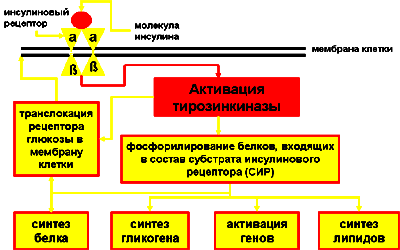
Согласно современным представлениям, на мембранах клеток находятся особые гликопротеиновые образования, являющиеся рецепторами инсулина. Наибольшее их количество
(до 250 000 рецепторов на клетку) - в гепатоцитах, а наименьшее (до 5000 рецепторов на клетку) - в жировой ткани. Таким образом, клетки организма обладают поистине бессчетным количеством инсулиновых рецепторов, однако, в норме функционирует всего до 10% от их общего количества. Другими словами, система захвата инсулина клетками многократно сдублирована, что свидетельствует о ее исключительной важности для организма.
Инсулиновый рецептор – это сложный белок, состоящий из двух пар субъединиц.
-субъединицы находятся на наружной поверхности мембраны клетки и обеспечивают контакт и соединение с молекулами инсулина. -субъединицы располагаются трансмембранно, их внутренняя (по отношению к мембране клетки) часть обладает тирозинкиназной активностью. Тирозинкиназа инсулинового рецептора обеспечивает связывание и фосфорилирование (дефосфорилирование) так называемых «СИР-белков», то есть белков субстрата инсулинового рецептора. Каскад реакций фосфорилирования белков и является основным передающим и исполнительным аппаратом клетки, благодаря чему обеспечивается выполнение функций инсулина в клетке (см. схему), в том числе, и транслокация рецепторов глюкозы в мембрану клетки и транспорт глюкозы в цитоплазму клеток инсулинозависимых тканей.
Глюкоза переносится в клетки организма двумя основными путями:
- за счет активного транспорта, связанного с затратами энергии и зависящего от
концентрации натрия в среде, из которой транспортируется глюкоза;
- за счет облегченной диффузии.
И в том, и в другом случае переносчиками глюкозы являются специальные трансмембранные белки (рецепторы глюкозы), образующие гидрофильные трансмембранные каналы.
Рецепторы, зависящие от натрия, обнаруживаются только на клетках эпителия почечных канальцев и кишечника и обеспечивают транспорт глюкозы против градиента концентрации. Рецепторы облегченной диффузии обеспечивают транспорт глюкозы по градиенту концентрации (из крови, где концентрация глюкозы достаточно высока, в клетку, где ее концентрации равна нулю) и расположены на клетках всех других тканей организма. Без посредства этих рецепторов глюкоза, не смотря на разницу ее концентрации внутри и вне клетки, пройти через мембрану не может.
Рецепторы облегченной диффузии (их насчитывается 5 видов) могут находиться как в мембране клеток, так и мембранных везикулах в протоплазме клеток. Четыре вида рецепторов не зависят от инсулина и транспортируют глюкозу в клетки без его воздействия на клеточные инсулиновые рецепторы.
Рецепторы, зависящие от инсулина, содержатся только в клетках так называемых «инсулинозависимых тканей» – скелетной и сердечной мускулатуре, жировой ткани. Под действием инсулина на инсулиновые рецепторы клеток этих тканей транспорт глюкозы в клетку возрастает в 30 – 40 раз. Резкое ускорение транспорта глюкозы связано с особенностью клеток инсулинозависимых тканей, в которых подавляющее большинство рецепторов глюкозы содержится в мембранных везикулах. Их встраивание в мембрану клеток происходит только после соединения инсулинового рецептора с молекулой инсулина, который после этого и передает сигнал, обеспечивающий быстрое передвижение везикул к мембране клетки и встраивание рецепторов глюкозы в мембрану. Схема этого процесса представлена ниже.

Из приведенного выше текста понятно, что возможность проникновения глюкозы в клетки инсулинзависимых тканей полностью зависит от соединения молекулы инсулина с инсулиновым рецептором, а также от того насколько успешно сигнал от этого соединения будет передан на исполнительный аппарат клетки. Кроме того, нужно иметь в виду, что основными потребителями глюкозы в организме являются именно инсулинзависимые ткани1, и, таким образом, отсутствие потребления этими тканями глюкозы приведет к значительному увеличению ее концентрации в крови, то есть к гипергликемии.
Ниже приведены диагностические критерии ВОЗ по определению нарушений толерантности тканей к глюкозе.
Определение уровня глюкозы в крови после приема утром натощак 75 г глюкозы:
- уровень глюкозы ниже 7ммоль/л (125 мг%) – норма;
- уровень глюкозы 7,1 – 11,1 ммоль/л (200мг%) – нарушенная толерантность к глюкозе;
- уровень глюкозы выше 11,1 ммоль/л – сахарный диабет (скорее всего инсулиннезависимый сахарный диабет).
Существует достаточно много причин, благодаря которым может быть нарушена функция инсулинового рецептора. Перечислим основные из них:
1. Мутации, вызывающие дефекты связывания инсулина с рецептором
2. Мутации, ускоряющие деградацию рецептора
3. Мутации, снижающие скорость биосинтеза рецептора
4. Мутации, затрудняющие внутриклеточный транспорт молекулы инсулина
5. Мутации, снижающие активность рецепторной тирозинкиназы
В целом, схему развития инсулинрезистентности и гиперинсулинемии можно представить в следующем виде.
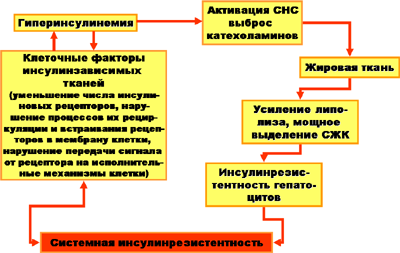
- Алиментарное ожирение как один из важных факторов развития метаболического синдрома
В самом простом смысле алиментарное ожирение можно определить как повышенное содержание жировой ткани в организме, возникающее в результате избыточного питания. Удельный вес этого страдания среди всех форм ожирения составляет 75%.
Ожирение относится к наиболее распространенным заболеваниям, с прогрессивным увеличением частоты во всех странах с высоким уровнем экономического развития. В этих странах по данным ВОЗ около 30% населения имеет массу тела, превышающую норму на 20% и более, то есть практически каждый третий страдает ожирением. Наиболее часто ожирение встречается в возрастных группах старше 50 лет, особенно у женщин. Особое значение для развития метаболического синдрома имеет так называемый «абдоминальный тип ожирения», то есть ситуация, при которой жировая ткань получает наибольшее распространение в абдоминальной области.
Висцеральная (абдоминальная) жировая ткань, в отличие от жировой ткани другой локализации, богаче иннервирована, имеет более широкую сеть капилляров и непосредственно сообщается с портальной системой. Висцеральные адипоциты имеют высокую плотность
ß-адренорецепторов и низкую плотность рецепторов к инсулину. Благодаря этому обстоятельству висцеральная жировая ткань повышенно чувствительна к липолитическому действию катехоламинов и мало реагирует на антилиполитическое действие инсулина.
В развитии алиментарного ожирения, в том числе – и ожирения абдоминального типа, играет роль целый ряд факторов, указанных на прилагаемой схеме.
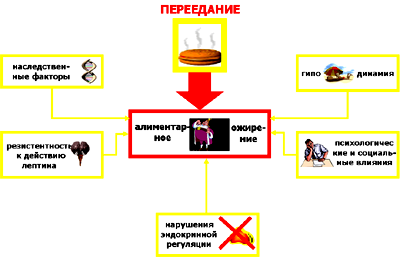
Наследственные факторы
Генетические исследования показывают, что, если потомство двух родителей с нормальной массой тела имеет лишь 10% вероятности ожирения, то возможность избыточного веса у потомства одного или обоих тучных родителей составляет 50% и 80%, соответственно. Однако имеются данные, что у приемных детей тучных родителей частота ожирения выше, чем у приемных детей родителей с нормальной массой тела. Это говорит о том, что, в развитии ожирения наряду с генетическими факторами, немаловажную роль играют и условия питания в семье.
В то же время у животных были установлены генетические дефекты, способствующие ожирению. Эти факторы приводят к снижению возбудимости гипоталамического центра сытости, в результате чего чувство насыщения возникает при приеме гораздо большего количества пищи, чем это требуется нормальным животным. Кроме того, генетически детерминированными могут быть и повышенная пролиферация адипоцитов, и дефекты многочисленных ферментов липолиза.
Центральные нейрогенные механизмы. Роль лептина в жировом обмене
Центры жирового обмена и потребления пищи локализуются в различных участках ЦНС, но главная регуляция этих процессов осуществляется в гипоталамусе. Уменьшение или увеличение содержания в этой области серотонина и триптофана может сопровождаться изменением пищевого поведения и массы тела. Кроме того, гипоталамус регулирует выброс инсулина и глюкагона, имеющих отношение и к липогенезу, и к липолизу. Таким образом, перестройка вегетативных центров может способствовать развитию ожирения.
В развитии алиментарного ожирения, значительную роль играет описанный относительно недавно гормон лептин (по своему строению и характеру действия его можно отнести и к цитокинам). Функции лептина в организме представлены на следующей схеме.
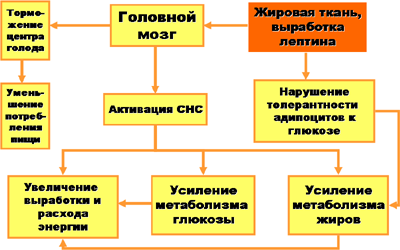
Лептин повышенно продуцируется жировой тканью при увеличении ее массы, переедании, а также при повышенной секреции инсулина и глюкокортикоидов. Соединяясь со специфическими лептиновыми рецепторами нейронов гипоталамуса, коры больших полушарий, таламуса и некоторых других структур ЦНС, лептин тормозит выработку ряда гипоталамических нейропептидов, в частности, нейропептида Y, который, по современным данным, служит стимулятором нейронов пищевого центра. Результатом этого процесса является снижение аппетита, повышение тонуса симпатической нервной системы, интенсификация процессов метаболизма. Следует указать, что у людей, страдающих ожирением, уровень лептина в крови не только не снижается, но даже может быть выше нормального. Это объясняется рядом причин, основные из которых демонстрирует прилагаемая схема.
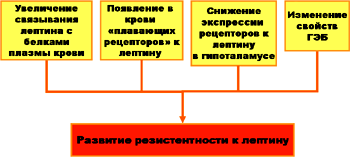
Нарушения эндокринной регуляции
Гиперинсулинизм, гиперфункция коры надпочечников, гипотиреоз снижение продукции СТГ, гипофункция половых желез, гиперпродукция адренокортикотропина - сами по себе могут играть важную роль в развитии ожирения. Однако, даже если секреция указанных гормонов является нормальной, но находится на верхней или нижней границе нормы, в условиях переедания такие состояния могут сыграть роль фактора, “помогающего” ожирению.
Метаболические особенности организма
К ожирению могут привести следующие особенности метаболизма:
- преимущественное перераспределение энергии, содержащейся в питательных веществах, на обеспечение процессов образования липидов;
- повышение эффективности извлечения энергии из питательных веществ и "отложение" избытка калорий в виде жира;
- повышение эффективности (коэффициента полезного действия) физической работы, что может снижать фактическую потребность организма в калориях, избыток которых будет накапливаться в виде жира (так, например, если какой - то род деятельности требует 5000 ккал в сутки, то через некоторое время при том же самом объеме работы калораж пищи надо снижать, поскольку у тренированного организма прежний эффект достигается с меньшими энергетическими затратами);
- угнетение липолиза, то есть подавление мобилизации триацилглицеринов из жировой ткани.
Гиподинамия
В настоящее время доля физического труда в общественно - полезной деятельности человека составляет 1%, в то время как немногим более ста лет тому назад она составляла 95%. Современное человечество поражено гиподинамией, в связи с чем снижается доля энергии, идущей на физический труд, и повышается ее доля, требуемая для обеспечения липогенеза. Кроме того, ожирение усиливает гиподинамию, что в свою очередь приводит к прогрессированию ожирения. Таким образом, замыкается "порочный круг": гиподинамия способствует развитию ожирения, а ожирение усиливает гиподинамию.
Гиперплазия жировой ткани
Установлено, что, если в организме произошло увеличение количества жировых клеток, то оно сохраняется всю жизнь. Особенно интенсивно жировая ткань может подвергаться гиперплазии у плода в последнюю треть внутриутробного развития, в раннем детском возрасте и в периоде полового созревания. Перекармливание в указанные периоды (при беременности - перекармливание матери), приводящее к увеличению количества адипоцитов, создает основу для развития ожирения и в дальнейшем.
Психологические и социально - экономические влияния
В развитии ожирения определенную роль могут играть психологические факторы. Нередко при эмоциональных нарушениях прием пищи может служить не только для удовлетворения чувства голода, но и приобретать какое - то символическое значение, например, приводить к снятию возбуждения или депрессии. Тучные лица могут сильнее, нежели люди с нормальным весом, воспринимать связанные с приемом пищи стимулы и сигналы (время дня, вид пищи, социальное окружение и т.д.), причем эти факторы начинают для данного человека играть в возбуждении аппетита более важную роль, нежели чисто физиологические моменты.
Доказано увеличение числа лиц, страдающих ожирением, по мере роста материального благосостояния общества. В то же время на распространенность этой патологии оказывает влияние и целый ряд других социальных и этнических факторов. Так, например, частота ожирения находится в обратной корреляции с уровнем образования. Важную роль в распространенности ожирения играют также эстетические представления конкретных этнических групп об идеальном телосложении.
Перечисленные семь групп факторов не являются сами по себе причиной ожирения, но могут способствовать его развитию при переедании.
- Роль метаболического синдрома в развитии сердечно-сосудистой патологии
Инсулинрезистентность и ее следствие – гиперинсулинемия приводят к повышенному возбуждению симпатической нервной системы и увеличению выработки антагонистов инсулина – катехоламинов. Под действием катехоламинов не только стимулируется липолиз жировой ткани, но и возникают гипертензия, перегрузка сердечной мышцы, что, при длительном характере этих процессов, способно привести к развитию хронической сердечной недостаточности. Схема, иллюстрирующая эти явления, приведена ниже.
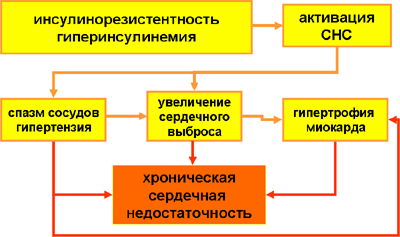
Следует иметь в виду, что и само по себе алиментарное ожирение – это также один из важных патогенных факторов в развитии гипертензии, формировании гипертонической болезни и сердечной недостаточности.
Поскольку жир хорошо васкуляризован, ожирение ведет к значительному увеличению сосудистого русла и объема циркулирующей крови (ОЦК). В результате этого увеличивается сердечный выброс, что вызывает рефлекторный спазм периферических сосудов в целях уменьшения ОЦК и снижения нагрузки на сердце. Однако этот, в основе своей защитный, механизм реализуется длительным периферическим сосудистым спазмом и стойким возрастанием артериального давления. Роль данного фактора в развитии гипертонической болезни настолько велика, что у тучных людей лечение эссенциальной гипертонии начинают с диетотерапии и только в том случае, если в течение полугода не наблюдается снижения артериального давления, приступают к применению медикаментов. Ожирение способствует развитию и сердечной недостаточности. В этом отношении роль играют следующие моменты:
- избыточный вес, ведущий к увеличению физической нагрузки на сердце;
- увеличенный ОЦК, приводящий к перегрузке миокарда;
- возросшее периферическое сопротивление из за развивающейся гипертензии;
- ожирение сердечной мышцы.
Таким образом, алиментарное ожирение и гиперинсулинемия идут «рука об руку» в формировании серьезной сердечно-сосудистой патологии. Дополнительную лепту в эти патологические процессы вносит и атеросклероз (как системный атеросклероз, так и атеросклероз коронарных сосудов), являющийся тяжелым последствием развития метаболического синдрома.
Важное место в развитии дислепидемии и ее следствия – атеросклероза принадлежит нарушениям функции печени, также страдающей при возникновении метаболического синдрома.
- Дислепидемия как проявление метаболического синдрома
В печени синтез липопротеинов очень низкой плотности (ЛПОНП - основных атерогенных агентов) возрастает при повышении концентрации инсулина. С другой стороны гиперинсулинемия подавляет активность липопротеинлипазы – фермента, регулирующего элиминацию ЛПОНП. Концентрация ЛПОНП в плазме крови значительно возрастает. Дезактивация липопротеинлипазы, в свою очередь, уменьшает образование липопротеинов высокой плотности (ЛПВП – основных антиатерогенных агентов), так как ЛПВП образуются из ЛПОНП именно под действием липопротеинлипазы. Развившаяся дислепидемия является мощным фактором, определяющим становление атеросклероза. Следует обязательно указать, что такой патогенетический механизм развития дислепидемии характерен именно для первого этапа формирования метаболического синдрома, когда гиперинсулинемия достаточно высока. Схема этого процесса приводится ниже.
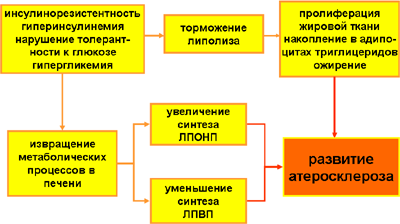
Иные механизмы, обеспечивающие состояние дислепидемии мы можем наблюдать на заключительной стадии развития метаболического синдрома. В это время продукция инсулина из-за перегруженности и гибели ß-клеток поджелудочной железы значительно снижается, а действие катехоламинов еще не прекращено. Растет липолиз жировой ткани. В результате образуется значительное количество свободных жирных кислот (СЖК), поступающих в печень по портальной системе. Под действием высоких концентраций СЖК метаболические процессы в печени извращаются. Печень становится малоспособной к синтезу ЛПВП, а образование ЛПОНП длительное время остается достаточно высоким. Уровень дислепидемии остается высоким, что и способствует развитию атеросклероза. Схема этого процесса приведена ниже.
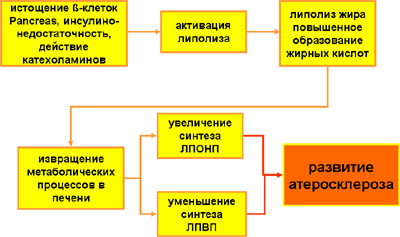
VIII. Сахарный диабет 2-го типа – заключительный этап развития метаболического синдром
Метаболический синдром при отсутствии или недостаточности соответствующей терапии неизбежно приводит и к развитию сахарного диабета 2-го типа. Схема, иллюстрирующая этот процесс, представлена ниже.
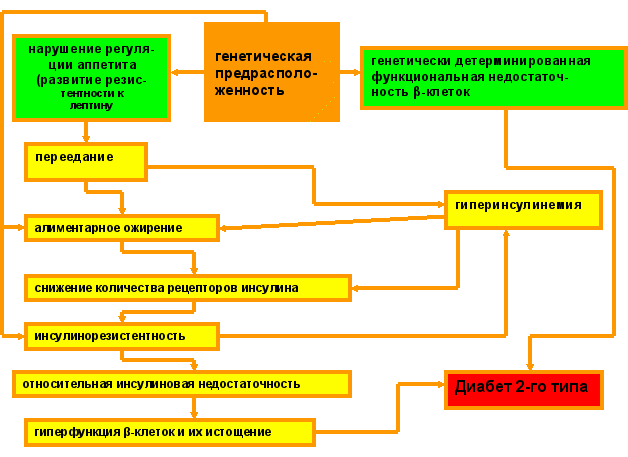
По имеющимся данным ведущую роль в развитии этой патологии играет генетически обусловленная инсулинорезистентность клеток инсулинозависимых тканей (поперечнополосатая и сердечная мускулатура, жировая ткань), а также наследственно детерминированная функциональная недостаточность -клеток островкового аппарата поджелудочной железы. Важно, что в большинстве случаев разрешающим фактором в развитии этого типа диабета является алиментарное ожирение абдоминального типа.
Наследственная предрасположенность к заболеванию сахарным диабетом 2-го типа играет значительно большую роль, чем в этиологии инсулинзависимого диабета. Об этом говорят, например, близнецовые исследования. По имеющимся данным конкордантность диабета 2-го типа у монозиготных близнецов составляет от 69 до 90% (по данным других исследований – 90 – 100%). Если у одного из родителей имеется сахарный инсулиннезависимый диабет, то в 40% случаев дети наследуют это же заболевание.
Генетические факторы, по-видимому, обуславливают не только инсулинорезистентность соответствующих тканей организма, но и сказываются на функциональной недостаточности
-клеток поджелудочной железы, а также на снижении количества инсулиновых рецепторов в результате мутации гена-рецептора. Кроме того, как правило, наследуется и склонность к алиментарному ожирению.
Патогенетический механизм, связывающий алиментарное ожирение и сахарный диабет 2-го типа можно описать следующим образом. Хотя адипоциты и содержат меньшее количество рецепторов инсулина, чем другие инсулинзависимые ткани, при ожирении общее количество этих рецепторов возрастает, в результате чего инсулин активно адсорбируется жировой тканью. Благодаря этому, в течение достаточно длительного времени в жировой ткани липолиз из-за избытка инсулина является подавленным. В то же время, вследствие адсорбции жиром значительного количества инсулина, его концентрация в крови снижается, и островковый аппарат поджелудочной железы вынужден функционировать с перенапряжением, чтобы обеспечить всем основным тканям (кроме жировой) необходимое количество инсулина. Поскольку у таких людей имеется генетически детерминированная неполноценность островкового аппарата, его более или менее длительное перенапряжение ведет к развитию истощения клеток, секретирующих инсулин, и к недостатку последнего в организме уже не из-за того, что его усиленно адсорбирует жировая ткань (хотя этот механизм продолжает иметь место еще длительное время), а в связи с тем, что -клетки резко снижают интенсивность своего функционирования. Развивается диабет. Через некоторое время количество инсулина становится недостаточным и для жировой ткани, поскольку ее продолжает оставаться много, а инсулина продуцируется мало. Тогда больной начинает интенсивно худеть, так как при обеднении жировой ткани инсулином в ней резко активируется липолиз. Как уже указывалось выше, липолиз ускоряется и в результате повышенной продукции катехоламинов.
Мы уже упоминали о том, что количество инсулиновых рецепторов в тканях лиц, страдающих сахарным диабетом 2-го типа, значительно уменьшено в результате мутации гена-рецептора инсулина. Но, помимо этого, генетически детерминированная инсулинорезистентность приводит не только к истощению -клеток, но и на определенном этапе развития этой патологии способствует к снижению чувствительности и даже блокаде имеющихся инсулиновых рецепторов. Перегрузка -клеток возрастает, они практически перестают функционировать и в результате для лечения сахарного диабета 2-го типа уже недостаточно одной диетотерапии. Больному требуется назначать регулярные инъекции инсулина.
Таким образом, основной причиной развития метаболического синдрома является инсулинрезистентность и гиперинсулинемия. Остальные проявления этого клинического синдрома можно скорее отнести к последствиям этой основной патологии.
- Исходы метаболического синдрома
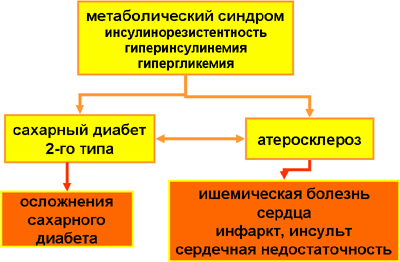
Развитие атеросклероза и сахарного диабета 2-го типа на заключительных этапах существования метаболического синдрома вызывает, в конечном итоге, именно те осложнения и сходы, которые свойственны этим тяжелым патологическим состояниям. К приводимой ниже схеме следует добавить, что системный атеросклероз повреждает не только сосуды мозга и коронарные артерии, но также неблагоприятно сказывается и на сосудистых системах других жизненно важных внутренних органов: почек, печени, поджелудочной железы, желудочно-кишечного тракта.
1 правда, много глюкозы потребляет центральная нервная система, но в нервные клетки глюкоза может поступать и без содействия инсулина, просто по градиенту ее концентрации: в клетках концентрация глюкозы равна нулю, а в плазме крови колеблется от 80 до 120мг%
