Текст лекции введение
| Вид материала | Лекции |
СодержаниеЭлектрическая синаптическая передача Химическая синаптическая передача ПД атипичных мышечных волокон – Выводы и заключение |
- Анкета участника международной научно-практической конференции «актуальные проблемы, 62.51kb.
- В. Ф. Степанов Очень мощный текст лекции, 1912.32kb.
- Конспект лекции Официально-деловой текст и его разновидности План, 200.67kb.
- Инструкция по работе с материалами внимательно прочитайте материалы лекции, 178.94kb.
- Ю. Б. Гиппенрейтер Введение в общую психологию. Лекции 1,2, 45.86kb.
- Резинько Тарасом Владимировичем (Кафедра фэч (Дубна), группа 409) Было «Введение»,, 317.41kb.
- Чекушиным Артемием Вениаминовичем (Кафедра нейтронографии(Дубна), группа 438) Было, 207.41kb.
- Название лекции: 2011. 08. 16. Йога Триада. Лекция, 430.35kb.
- Название лекции: 2011. 05. 17. Йога Триада. Лекция, 335.26kb.
- Название лекции, 2025.12kb.
ТЕКСТ ЛЕКЦИИ
Введение
Роль мембран мышечных и нервных волокон состоит в распространении информации (в случае нервов) или регулирующих сигналов (в случае мышечных волокон), то есть в проведении возбуждения (потенциала действия). Особый интерес представляет распространение возбуждения в органах, состоящих из большого количества нервных или мышечных клеток, например, распространение возбуждения в мозге или миокарде сердца. В медицине на исследовании электрических полей, генерируемых при возникновении и распространение биопотенциалов органов и тканей, основаны диагностические методы: электрокардиография, электроэнцефалография, электромиография и другие, с одним из которых – электрокардиографией – мы сегодня познакомимся. Сведения, которые вы получите на сегодняшней лекции, будут развиты и углублены в процессе изучения курсов нормальной и патологической физиологии, невропатологии, пропедевтики внутренних болезней, терапии, кардиологии и многих других.
§ 1. Распространение потенциала действия по возбудимым мембранам
При возбуждении нервного волокна (например, прямоугольным импульсом напряжения) можно зарегистрировать потенциалы действия не только в месте раздражения, но и на значительных расстояниях от него. На всем протяжении нервного волокна ПД имеют одинаковую амплитуду, но появляются с задержкой, которая пропорциональна расстоянию от места нанесения стимула. Например, в двигательном нерве ПД регистрируется на участке, расположенном от места раздражения на расстоянии 1 м, через 10 мс; отсюда следует, что скорость распространения возбуждения по нерву равна 100 м/с.
Распространение возбуждения по нерву складывается из двух последовательных процессов: 1) распространения ЭМП с затуханием (декрементом); 2) ретрансляции ПД.
Рассмотрим эти процессы более подробно. Допустим, в некоторой точке нервного волокна (аксона) развился и достиг пика ПД, т.е. произошла деполяризация мембраны (см. схему). В месте возникновения ПД потенциал внутренней части мембраны положителен, а потенциал наружной мембраны отрицателен. И в цитоплазме, и в окружающей мембрану межклеточной жидкости возникают ионные токи (локальные токи): между участками поверхности мембраны с большим потенциалом (положительно заряженными) и участками поверхности мембраны с меньшим потенциалом (отрицательно заряженными). За счет этих токов потенциал внутренней поверхности соседних невозбужденных участков мембраны повышается (становится более положительным), потенциал наружной поверхности невозбужденных участков понижается (становится более отрицательным). Трансмембранная разность потенциалов уменьшается по абсолютной величине, невозбужденные участки мембраны деполяризуются.
По мере удаления от точки возникновения ПД изменения трансмембранной разности потенциалов убывают по экспоненциальному закону (см. график) (распространение с затуханием или декрементом). В тех точках мембраны, где сдвиг трансмембранной разности потенциалов оказывается выше КМП, открываются натриевые каналы и происходит развитие новых ПД (ретрансляция потенциала действия).
Таким образом, возникающий на возбудимой мембране ПД является надпороговым стимулом для определенного участка мембраны. Естественно, что, поскольку распространение ЭМП происходит со скоростью света в среде, пассивные сдвиги трансмембранной разности потенциалов происходят быстро, и скорость распространения возбуждения по мембране зависит от величины участка, одновременно охваченного возбуждением.
Величина деполяризующего потенциала зависит от расстояния от возбужденного участка мембраны следующим образом:
Ux = U0.e-x/λ
где Ux – величина деполяризующего потенциала в точке "х"; U0 – повышение мембранного потенциала в точке возбуждения; х – расстояние от места возникновения возбуждения; λ – постоянная длины мембраны (равная расстоянию, на котором деполяризующий потенциал уменьшается в "е" раз).
Постоянная длины определяется следующими параметрами нервного волокна:
Λ =
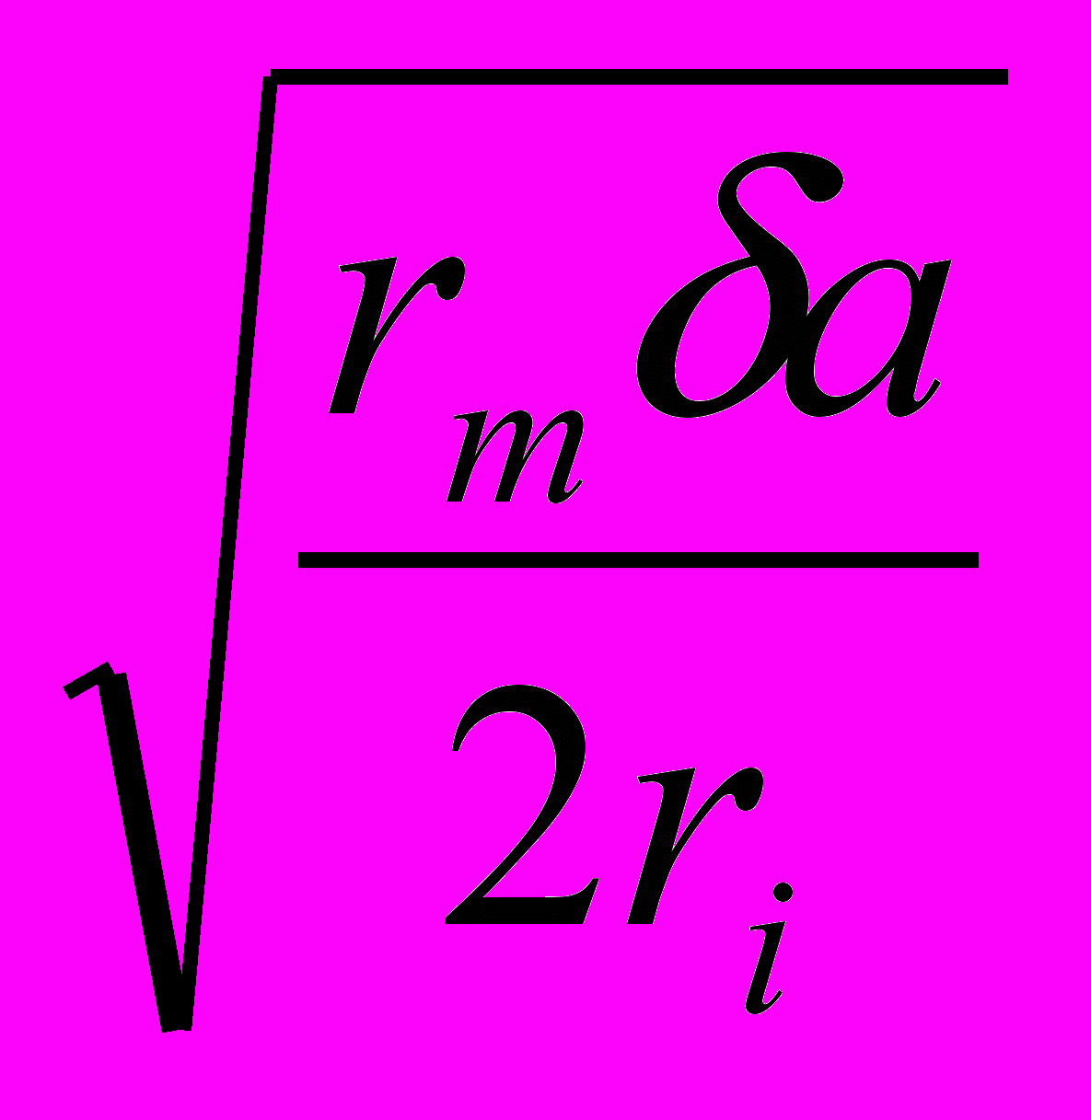
где rm – удельное электрическое сопротивление оболочки волокна; δ – толщина оболочки; а – радиус волокна; ri – удельное сопротивление цитоплазмы. Чем больше константа длины мембраны, тем меньше затухание и выше скорость распространения нервного импульса. Величина λ тем больше, чем больше радиус аксона и удельное сопротивление мембраны и чем меньше удельное сопротивление цитоплазмы.
Большую скорость распространения нервного импульса по аксону кальмара обеспечивает их гигантский по сравнению с аксонами позвоночных диаметр, равный 1-2 мм (λ ~ 2,5 мм). Эти гигантские аксоны иннервируют прежде всего его "реактивный двигатель" (полость, снабженную мощной мышечной стенкой). Сигналы к мышечному мешку поступают по гигантским нервным волокнам, когда кальмар спасается от опасности или нападает на свою жертву.
Такой способ повышения скорости распространения возбуждения посредством утолщения нервных волокон пригоден для животных, у которых мало быстропроводящих коммуникаций.
У позвоночных животных, которые имеют нервы с большим количеством проводящих волокон, возможности их утолщения ограничены размерами животного. Большая скорость передачи возбуждения в нервных волокнах достигается другими способами. Аксоны позвоночных снабжены миелиновой оболочкой.
Миелиновая оболочка образуется в процессе наматывания на аксон окружающих его шванновских клеток. Оболочка представляет собой многомембранную систему, включающую несколько десятков элементарных клеточных мембран, прилегающих друг к другу. Диффузия ионов через миелиновую оболочку невозможна (кроме того, в участках мембраны покрытых ею), отсутствуют потенциалзависимые ионные каналы. Поэтому в мякотном волокне генерация ПД возможна только там, где миелиновая оболочка отсутствует (в перехватах Ранвье или активных узлах). В среднем расстояние между перехватами Ранвье составляет около 1 мм. Мембрана перехвата Ранвье специализирована для генерации возбуждения: плотность натриевых каналов здесь примерно в 100 раз выше, чем в немиелинизированных нервных волокнах.
От перехвата к перехвату возбуждение распространяется за счет декрементного распространения ЭМП. При этом постоянная длины (λ) для этих волокон больше (так как увеличиваются сопротивление мембраны и ее толщина). Ретрансляция ПД обычно происходит на 2-3 соседних перехватах Ранвье. Более частое, чем необходимо для обеспечения нормального распространения возбуждения, расположение активных узлов служит повышению надежности нервных коммуникаций в организме. Высокое значение постоянной длины обеспечивает высокую скорость распространения возбуждения по мякотным волокнам (до 140 м/с).
Поскольку ретрансляция ПД происходит только в перехватах Ранвье, то возбуждение как бы "перепрыгивает" через миелинизированные участки мембраны; такой тип проведения возбуждения получил название сальтаторного (saltus (лат.) = скачок).
Следует отметить, что миелинизация обеспечивает повышение скорости проведения при существенной экономии энергетических ресурсов. Дело в том, что количество ионов, переносимых через мембрану в ходе развития ПД, здесь существенно меньше (транспорт ионов происходит только в перехватах Ранвье), поэтому биологические насосы (К+-Na+-АТФаза), восстанавливающие концентрационные градиенты после распространения ПД, здесь работают менее напряженно (потребление кислорода такими волокнами в 200 раз меньше, чем при непрерывном распространении нервных импульсов по безмякотным аксонам).
§ 2. Синаптическая передача.
Механизм распространения возбуждения, который мы рассмотрели, присущ непрерывной возбудимой мембране, принадлежащей отдельной клетке. Функциональный межклеточный контакт, обеспечивающий переход возбуждения с одной клетки на другую, получил название синапса (от греч. глагола "синапто" – смыкать).
Существует два принципиально различных типа синапса – электрические и химические.
Электрическая синаптическая передача возможна только при очень тесном соприкосновении взаимодействующих клеток – при расстоянии между ними не более 10-20 нанометров (часто 2-4 нм). В этом случае развитие ПД на мембране одной клетки приводит за счет возникновения локальных токов к деполяризации мембраны другой клетки, которая может оказаться выше порога генерирования ПД. Большое значение для осуществления электрической передачи нервного импульса имеет существование в области синапса особых межклеточных контактов – щелевых контактов (нексусов). При этом в каждой из двух соседних мембран находятся регулярно расположенные коннексоны (канальные белки с большим диаметром канала и, соответственно, высокой проводимостью для ионов, и даже более крупных молекул с молекулярной массой до 1000). Такие контакты обычны для ЦНС, миокарда и гладкой мускулатуры, где связанные щелевыми контактами клетки образуют функциональный синцитий (возбуждение переходит от одной клетки к другой очень быстро и без заметного снижения амплитуды потенциала действия на границе). Щелевые контакты регулируемы, они могут закрываться при снижении рН или повышении концентрации Са2+ (повреждение клеток или глубокие нарушения обмена). За счет такого механизма пораженные места изолируются от остальной части синцития, и распространение патологии ограничивается (инфаркт миокарда).
Химическая синаптическая передача осуществляется с помощью химических веществ-посредников (медиаторов). В этом случае расстояние между взаимодействующими клетками в области контакта (ширина синаптической щели) больше. Электрическое поле затухает в пределах синаптической щели и не может деполяризовать постсинаптическую мембрану. Отсюда возникает необходимость химического посредника.
Деполяризация пресинапса приводит к изменению проницаемости пресинаптической мембраны для медиатора, медиатор выбрасывается в синаптическую щель, диффундирует через нее и взаимодействует с белками-рецепторами постсинаптической мембраны. Изменение конформации белков-рецепторов при образовании комплекса "рецептор-медиатор" приводит к открытию на мембране специфических химиочувствительных ионных каналов, протекающие через которые ионные токи изменяют мембранный потенциал на мембране. В зависимости от направления изменения трансмембранного потенциала химические синапсы могут быть возбуждающими (деполяризация постсинаптической мембраны) или тормозными (гиперполяризация ПСМ). В случае возникновения ВПСП (возбуждающего постсинаптического потенциала) он с затуханием декрементом распространяется по постсинаптической мембране и может вызвать возникновение ПД на возбудимых участках мембраны принимающей сигнал клетки, если он превышает пороговый уровень.
Более детальные сведения о механизме химической синаптической передачи вы найдете в учебнике В.О. Самойлова "Медицинская биофизика" (гл. 11, § 5). Этот вопрос будет также обсуждаться на практическом занятии.
§ 3. Особенности биоэлектрогенеза мышечных волокон миокарда сердца.
Сердце выполняет в кровеносной системе роль четырехкамерного насоса, обеспечивающего движение крови по сосудам. Оно представляет собой полый мышечный орган, состоящий из четырех отделов – двух предсердий и двух желудочков. Ритмические сокращения сердца возникают под действием импульсов (ПД), зарождающихся в нем самом. Если изолированное сердце поместить в соответствующие условия, то оно будет продолжать биться с постоянной частотой. Это свойство называется автоматизмом.
Функциональным элементом сердца служит мышечное волокно – цепочка из клеток миокарда, соединенных "конец в конец" и заключенных в общую саркоплазматическую оболочку (основную мембрану). В зависимости от морфологических и функциональных особенностей различают два типа волокон миокарда:
1) волокна рабочего миокарда предсердий и желудочков, составляющие его основную массу и обеспечивающие нагнетательную функцию (типичные миокардиальные волокна = ТМВ);
2) волокна водителя ритма (пейсмекера) и проводящей системы (атипичные мышечные волокна), отвечающие за генерацию возбуждения и проведение его к клеткам рабочего миокарда.
Миокард (сердечная мышца), подобно нервным тканям и скелетным мышцам, принадлежит к возбудимым тканям. Это значит, что клетки миокарда обладают потенциалом покоя (ПП), отвечают на надпороговые стимулы генерацией потенциала действия (ПД) и способны проводить ПД без затухания (бездекрементно). Межклеточные соединения (щелевые контакты) способствуют проведению возбуждения и обеспечивают функционирование миокарда как функционального синцития (т.е. возбуждение, возникшее в каком-либо из отделов сердца, охватывает все без исключения невозбужденные волокна). Этим сердце отличается от нервов и скелетных мышц, где каждая клетка возбуждается изолированно, и ПД возникают только в тех клетках, где деполяризация превышает уровень КМП (т.е. больше пороговой).
Как и в нервных клетках и волокнах скелетных мышц, ПД в типичных миокардиальных волокнах возникает в ответ на стимул (переданный с АТМВ ПД) и начинается с быстрой реверсии мембранного потенциала от ПП (примерно - 90 мВ) до потенциала инверсии (примерно + 30 мВ). За этой фазой быстрой деполяризации (продолжительность – 1-2 мс) следует более длительная фаза плато – специфическая особенность клеток миокарда, затем наступает фаза реполяризации, по окончании которой восстанавливается ПП. Длительность ПД кардиомиоцитов составляет 200-400 мс, т.е. более чем в 100 раз превышает соответствующую величину для скелетных мышц и нервных волокон.
ПД возникает в результате изменений МП в результате изменения мембранной проницаемости для различных ионов и возникновения ионных потоков. ПП близок к К+-равновесному потенциалу; деполяризация обусловлена лавинообразно нарастающим Na+-током (однако, этот Na-Ток быстро инактивируется); фаза плато обусловлена входящим Са2+-током (медленный входящий ток) + снижение проводимости для К+, возникающее при деполяризации и уменьшающее реполяризацию; реполяризация обусловлена выходящим К+-током и снижением проводимости для иона Са2+. Медленные Са2+-каналы инактивируются специфическими блокаторами (Cd2+; нифедипином; верапамилом).
Специфическая форма ПД ТМВ имеет большое функциональное значение; дело в том, что определенным фазам ПД соответствует определенные изменения возбудимости мембраны (фазы рефрактерности), Во время длительной деполяризации мембраны (плато) Na+-каналы инактивируются, и ТМВ находится в состоянии абсолютной рефрактерности. Восстановление активности натриевых каналов происходит только после снижения МП до уровня, примерно равного – 40 мВ. Длительный рефрактерный период предохраняет сердце от слишком быстрого повторного возбуждения и повторного сокращения. Такое возбуждение, возникшее до расслабления мышечного волокна, могло бы привести к нарушению нагнетательной функции сердца (тетанус миокарда). Кроме того, длительная фаза рефрактерности препятствует круговому движению возбуждения по миокарду. Период рефрактерности больше, чем время распространения возбуждения по предсердиям или желудочкам. То есть после того, как волна возбуждения охватит предсердие или желудочек, оно угаснет.
ПД атипичных мышечных волокон – отличается отсутствием устойчивого уровня ПП. Эти клетки спонтанно деполяризуются до критического уровня. Фазы ПД – медленная диастолическая деполяризация до КМП; быстрая ДП; более или менее выраженная фаза плато; быстрая реполяризация.
Причины медленной ДП – более высокая проницаемость мембраны для натрия в покое (МП удален от равновесного К+-потенциала в сторону деполяризации); задержанное развитие К+-проводимости в фазу реполяризации приводит к приближению МП к калиевому равновесному потенциалу; затем проводимость для калия инактивируется, и МП все более отличается от равновесного калиевого потенциала, достигая в конечном итоге уровня, при котором активируются натриевые потенциалзависимые каналы.
§ 4. Проводящая система сердца. Распространение возбуждения по миокарду.
АТМВ миокарда образуют так называемую проводящую систему. Она представляет собой совокупность узлов и пучков атипичной мышечной ткани, функцией которой является генерация ПД, служащих стимулами для ТМВ, то есть задание определенного ритма сердечных сокращений. Строение проводящей системы обеспечивает строго согласованное и последовательное возбуждение и сокращение различных отделов сердца.
В норме водителем ритма является синоатриальный узел, расположенный в стенке правого предсердия в месте впадения в него верхней полой вены. Частота разрядов СА в покое составляет около 70 1/мин. От этого узла возбуждение вначале распространяется по рабочему миокарду предсердий (со скоростью порядка 1 м/с).
Единственный путь, по которому возбуждение может пройти к желудочкам, образует атриовентрикулярный узел (АВ), лежащий в предсердно-желудочковой перегородке (остальная часть атриовентрикулярного соединения образована невозбудимой соединительной тканью). В АВ узле скорость проведения значительно падает (в 20-50 раз; 0,02-0,05 м/с) за счет снижения диаметра волокон АВ-узла и поперечного их расположения Передача возбуждения - через боковые щелевые контакты. Это приводит к тому, что возбуждение "задерживается" в АВ-узле (АВ-задержка необходима для полного перехода крови из предсердий в желудочки во время сокращения предсердий).
Далее возбуждение распространяется по пучку Гиса, ножкам пучка Гиса и волокнам Пуркинье к верхушке сердца со все возрастающей (до 4-5 м/с) скоростью (увеличение диаметра АТМВ), а затем переходит на рабочие волокна миокарда, по которым распространяется в обратном направлении – от верхушки сердца к основанию. За волной возбуждения следует сокращение ТМВ миокарда.
Следует отметить, что при нарушении функции водителя ритма первого порядка (СА-узла) его роль могут выполнять другие отделы проводящей системы (им также присущ автоматизм), но направление распространения возбуждения по сердцу при этом будет нарушено (да и собственная частота генерации ПД у этих отделов проводящей системы ниже – 40-60 – у АВ-узла, у других отделов – еще меньше). Это приводит к тяжелым нарушениям насосной функции сердца (пример – полная поперечная блокада).
§ 5. Электрокардиография. Электрокардиограмма. Интегральный электрический вектор сердца.
Сложный характер распространения возбуждения по сердцу отображается в электрокардиограмме (ЭКГ), по форме которой можно судить о возбудимости и проводимости различных отделов сердца (но не о сократимости волокон миокарда!)
Если рассмотреть отдельное миокардиальное волокно, то в покое его наружная поверхность имеет положительный, а внутренняя – отрицательный потенциал. При возбуждении (ПД) возбужденный участок мембраны меняет свою полярность (см. схему). Возбужденное волокно можно рассматривать как диполь, обладающий определенным дипольным моментом. Векторная сумма дипольных моментов всех волокон миокарда называется интегральным электрическим вектором сердца (ИЭВС). Этот вектор в каждый момент времени направлен от наиболее возбужденного (электроотрицательного) к наименее возбужденному (электроположительному) участку сердца, и величина и направление его в ходе сердечного цикла многократно меняются.
Как известно, движущиеся заряды создают вокруг себя переменное электрическое поле, которое распространяется в пространстве. Поэтому работающее сердце также является источником электрического поля, которое можно зарегистрировать на поверхности тела. Для этого на различные точки поверхности тела накладывают отводящие электроды и регистрируют разность потенциалов между ними. Регистрирующий прибор (электрокардиограф) по сути представляет собой усилитель переменного тока и регистрирующее устройство (самописец). Кривая, отображающая зависимость этой разности потенциалов от времени, называется электрокардиограммой. Она представляет собой периодическое (Т = 1/ЧСС) колебание сложной формы.
Величина разности потенциалов, регистрируемой между двумя электродами, находящимися на поверхности тела человека будет зависеть от величины интегрального электрического вектора и угла между направлением этого вектора и осью отведения (проведенной между этими электродами) (см. схему). Таким образом, ЭКГ представляет собой динамику во времени проекции ИЭВС на ось отведения.
Какова же форма ЭКГ? По предсердиям возбуждение распространяется в направлении сверху вниз; это означает, что ИЭВС ориентирован по направлению к верхушке сердца. На ЭКГ регистрируется зубец Р, отображающий деполяризацию предсердий. Во время возбуждения всех отделов предсердий разность потенциалов временно исчезает, так как ПД всех предсердных клеток находятся в фазе плато. В это время возбуждение распространяется по проводящей системе желудочков, но общее количество возбужденных клеток при этом невелико и существенной разности потенциалов не возникает (сегмент PQ). Длительность этого сегмента несет информацию о величине атриовентрикулярной задержки. При переходе на рабочий миокард желудочков в сердце снова появляются значительные градиенты напряжения. Возбуждение желудочков начинается с деполяризации левой поверхности межжелудочковой перегородки (ИЭВС направлен к основанию сердца (начало комплекса QRS). Затем вектор быстро меняет направление на противоположное (к верхушке) = распространение возбуждения через стенку желудочков от эндокарда к эпикарду (регистрируется самый крупный зубец R); в последнюю очередь возбуждается участок правого желудочка в области основания легочного ствола (ИЭВС направлен вправо и вверх). Когда желудочки полностью охвачены возбуждением, разность потенциалов временно исчезает (сегмент ST). Затем следует фаза реполяризации желудочков (зубец Т), в ходе этой фазы ИЭВС ориентирован влево (это связано с тем, что разные отделы миокарда желудочков реполяризуются с разной скоростью).
Выводы и заключение
Таким образом, в ходе сегодняшней лекции вы познакомились с особенностями распространения возбуждения по возбудимым мембранам (т.е. по мембранам мышечных и нервных волокон), основными принципами передачи возбуждения с одной возбудимой клетки на другую, а также с особенностями биоэлектрогенеза такого важного и сложного органа как сердце и с происхождением электрокардиограммы, имеющей огромное значение для диагностики многих видов патологии сердца. Естественно, что эти знания будут углублены и дополнены на практическом занятии, посвященном этой теме, а в дальнейшем - на кафедрах пропедевтики внутренних болезней, кардиологии и многих других, где вы познакомитесь с изменениями электрокардиограммы при нарушениях возбудимости и проводимости различных отделов миокарда.
