Опубликовано в журнале Репродуктивное здоровье в Беларуси 2009. №4 (04). С. 94-105
| Вид материала | Документы |
СодержаниеМатериалы и методы исследования. Результаты и их обсуждение. Достоверность различий в сравнении с контролем: ** (P |
- Тема Лектор, 27.38kb.
- Экспрессия эстрогеновых и прогестероновых рецепторов в яичнике при синдроме поликистозных, 155.67kb.
- Опубликовано в журнале «Интеграция образования». 2006. №2 (43)., 368.82kb.
- Опубликовано в журнале «Здоровье для всех» 2008, 181.65kb.
- Методическое письмо. Опубликовано в журнале "Завуч начальной школы" №6 за 2001 год., 593.47kb.
- Заседание Репродуктивное здоровье и контрацепция, 325.05kb.
- Интернет-источник, 332.35kb.
- Опубликовано в журнале «Экология промышленного производства». 2007., 204.88kb.
- «Репродуктивное здоровье молодежи», 15.94kb.
- Программа IV междисциплинарной научно-практической конференции, 378.4kb.
Опубликовано в журнале Репродуктивное здоровье в Беларуси – 2009. - №4 (04). – С.94-105.
Характеристика клинико-лабораторных показателей и оценка психологического статуса у детей с хроническими аллергическими заболеваниями
Л.М.Беляева, Н.И.Панулина, Н.В.Микульчик, Д.В.Буза
Белорусская медицинская академия последипломного образования
В последнее десятилетие распространенность аллергическими заболеваниями во всем мире возросла более чем в 3 раза. По данным экспертов ВОЗ (2003), различными аллергическими реакциями и заболеваниями страдают от 25 до 43 % населения земного шара [3, 5, 7, 9, 17, 20]. Из-за высокой распространенности у детей и взрослых, аллергические заболевания все чаще называют «глобальной проблемой человечества».
Рост заболеваемости детского и взрослого населения этой патологией, в первую очередь, связан с бурным развитием химической и многих других отраслей промышленности, с выбросом отходов производства и выхлопных газов автотранспорта в атмосферу [3, 5, 7]. В отличие от ХХ века, эпохи роста сердечнососудистых заболеваний, по прогнозам ВОЗ, XXI век – становится веком аллергии. Это утверждение базируется на постоянно регистрируемом увеличении частоты аллергических заболеваний (АЗ) каждые 10 лет. Причиной подобного роста заболеваемости является не только ухудшающаяся экология, но и возросшие стрессовые нагрузки, нерациональное питание, появление новых аллергенов, бесконтрольное применение медикаментов, повышение радиационного фона и др. Таким образом, чем более цивилизованным становится мир, тем больше он «аллергизуется». Не менее важную роль в формировании аллергических заболеваний имеет так называемая "малая экология". Это понятие включает социально-экономические условия проживания, состояние жилища, наличие фактора курения. Эпидемиологические исследования последних лет показывают, что каждый четвертый человек в той или иной степени имеет симптомы A3 при контакте с бытовой химией, животными, при употреблении пищевых продуктов, лекарственных препаратов и т. д. [3, 10, 12, 13, 15].
Среди аллергических заболеваний выделяют группу классических атопических болезней. В нее входят атопическая бронхиальная астма (БА), аллергический ринит (АР) и атопический дерматит (АД), развивающиеся на фоне выраженной наследственной предрасположенности и нарушения равновесия симпатической и парасимпатической регуляции соответствующего органа или системы [1, 2, 4, 19, 21].
В настоящее время не вызывает сомнений, что одним из факторов высокого риска развития бронхиальной астмы у детей является атопический дерматит, который может считаться первым (по срокам возникновения) аллергическим заболеванием, а также начальным этапом так называемого «атопического марша»: «АД-АР-БА» или «АД-БА-АР»[2, 5, 8].
По результатам ряда проспективных исследований установлено, что при тяжелом течении атопического дерматита через 6-7 лет в среднем у 43% детей развивалась бронхиальная астма, а у 45% - аллергический ринит. Это позволяет рассматривать атопический дерматит как «входные ворота» для последующего развития атопии [5, 6, 9, 12, 16].
В последние годы отмечается четкая тенденция к увеличению числа больных с сочетанными формами кожной и респираторной аллергии. Наблюдения последних лет свидетельствуют о значительной частоте сочетания атопического дерматита и бронхиальной астмы, что получило название «дермо-респираторного синдрома». Этот термин широко используется в клинической практике, хотя и не имеет официального отражения в Международной классификации болезней. Частота сочетанных кожно-респираторных проявлений аллергии в структуре аллергических болезней у детей зависит от возраста и достигает 50-65%. «Дермо-респираторный синдром» следует рассматривать как естественный ход «аллергического марша», то есть естественное течение атопии, характеризующееся определенной возрастной последовательностью развития клинической картины и сенсибилизации. В основе его патогенеза лежит аллергическое воспаление кожи и слизистой оболочки дыхательных путей [1, 5, 9, 11, 14]. Сочетание атопического дерматита и бронхиальной астмы значительно усложняет возможность терапии и серьезно влияет на прогноз болезни и качество жизни пациентов. БА, АД и АР рассматриваются как хронические аллергические воспалительные заболевания, имеющие общие этиологические факторы и механизм развития [5, 9].
Целью нашего исследования явилось: определение характера клинико-иммунологических показателей, липидного спектра и оценка психологических особенностей у детей с различными сочетаниями хронических аллергических болезней (астма, дерматит, ринит).
Материалы и методы исследования.
Исследования проводились на базе Республиканского детского аллергологического центра (УЗ «4-я детская городская клиническая больница г.Минска»). Нами обследовано 156 детей в возрасте от 7 до 17 лет (средний возраст детей - 11,3 0,23 лет), страдающих сочетанными формами атопических заболеваний (дерматит, ринит, астма). Контрольную группу составили 50 здоровых детей (не имеющих хронических и аллергических заболеваний) аналогичного возраста и пола. Среди обследованных – 88 девочек (средний возраст - 11,6 + 0,33 года) и 68 мальчиков (средний возраст – 11,03 0,32 года).
Обследованные дети были разделены на две группы: 1-ю группу составили дети с изолированными атопическим заболеваниями (атопический дерматит или бронхиальная астма – 73 ребенка (26 - мальчики, 47 - девочки); 2-я группа – дети с различными сочетаниями аллергических заболеваний - 71 ребенок (37 – мальчики, 34 – девочки): с сочетанием астмы, дерматита и ринита - 27 детей, с сочетанием дерматита и ринита - 18 детей, с сочетание астмы и дерматита - 15 детей, с сочетанием астмы и ринита – 11 детей.
Всем детям проведено общеклиническое и аллергологическое обследование, включающее кожные скарификационные пробы с бытовыми, пищевыми, пыльцевыми и эпидермальными аллергенами. Изучен генеалогический анамнез, анамнез жизни, анамнез болезни, характер питания на первом году жизни. Степень тяжести БА и АД определяли согласно клиническим протоколов диагностики и лечения БА и АД, утвержденных Министерством здравоохранения Республики Беларусь. В рамках лабораторно-диагностического раздела иммунологическими методами проведено определение экспрессии CD-антигенов лимфоцитами и мононуклеарами периферической крови (CD3 –общая субпопуляция Т-лимфоцитов, CD4 – Т-хелперы, CD8 – Т-супрессоры, CD20 – В-лимфоциты, определение фагоцитарной активности нейтрофилов (ФП –фагоцитарный показатель, ФЧ – фагоцитарное число), концентрации иммуноглобулинов (IgG, IgA и IgM) в сыворотке крови, количественное определение общего IgE в сыворотке крови, а также определение концентрации IgG, IgA, IgAs и IgM в слюне. Определялись основные показатели липидного обмена: содержание общих липидов (ОЛ), общего холестерина (ОХС), α-холестерина (α-ХС), триглицеридов (ТГ), общих фосфолипидов (ОФЛ), липопротеинов низкой плотности (ЛПНП), липопротеинов очень низкой плотности (ЛПОНП), липопротеинов высокой плотности (ЛПВП), рассчитывали коэффициент атерогенности (КА) по формуле: КА= (ОХС – α-ХС)/α-ХС. Содержание общих липидов в сыворотке крови определяли по цветной реакции с сульфофосфованилиновым реактивом. Для определения концентрации общего холестерина в сыворотке крови использовался энзиматический метод Триндера. Концентрацию триглицеридов в сыворотке крови определяли энзиматическим колориметрическим методом, разработанным Буколо и Дэвидом. Уровень фосфолипидов в сыворотке крови определяли по содержанию в них липидного фосфора.
Для исследования выраженности реактивной и личностной тревожности у детей старше 9 лет использовалась шкала Ч.Д. Спилбергера, адаптированная Ю.Л. Ханиным, детско-подростковый вариант, позволяющий определить предрасположенность человека к возникновению состояния психологической дезадаптации под влиянием стрессовых ситуаций. Бланк шкалы самооценки тревоги Спилбергера-Ханина в детском варианте включает в себя инструкцию и 40 вопросов-суждений, 20 из которых предназначены для оценки уровня реактивной (ситуационной) тревожности (РТ) и 20 – для оценки уровня личностной тревожности (ЛТ). Итоговый показатель по каждой из шкал может находиться в диапазоне от 20 до 60 баллов, где низкий уровень тревоги – 21–30 баллов, средний – 31–45 баллов, высокий – 46 баллов и выше. Тестирование пациентов и интерпретация результатов проводились совместно с психологом.
Статистическую обработку данных, полученных в результате исследований, проводили традиционными методами вариационной статистики на персональном компьютере с использованием программ Stat soft Statistica 6.0, «Primer of Biostatistics» (Version 4.03 by Stanton A. Glantz).
Результаты и их обсуждение.
Основополагающим фактором формирования аллергических заболеваний является генетически обусловленная предрасположенность к IgЕ-ответу, причем по наследству передается не болезнь как таковая, а совокупность генетических факторов, способствующих формированию аллергической патологии [4, 5, 10, 20]. В результате проведенного нами исследования установлено, что в группе детей с изолированными атопическим дерматитом или бронхиальной астмой 56% имели наследственную отягощенность по атопическим заболеваниям, среди них у 55% - наследственность отягощена по линии матери, у 25 % - по линии отца и у 20% - по линии обоих родителей. В группе детей с сочетанием аллергических заболеваний (БА+АД+АР) у 65 % отмечалась наследственная отягощенность по атопическим болезням, причем одинаково часто и по линии матери (38 %), и по линии обоих родителей (38%), по линии отца – у 24%. При сочетании двух заболеваний (БА+АД или АД+АР или БА+АР) у 42% выявлена отягощенная наследственность (по линии матери – у 46% , по линии отца – у 46%, а по линии обоих родителей только у 8%).
При анализе анамнеза жизни и анамнеза болезни установлено, что в группе детей с сочетанием трех болезней (БА+АД+АР) начало первых аллергических проявлений на первом году жизни (в виде пищевой аллергии или атопического дерматит) отмечено у 92% детей, у детей с сочетанием двух заболеваний (БА+АД или БА+АР или АД+АР) – у 86%. По нашим данным установлено, что на первом году жизни более чем у 90% детей с различным сочетанием аллергических заболеваний развивалась пищевая аллергия, а атопический дерматит был диагностирован на первом году жизни у 72% этих пациентов. Астма и ринит на ингаляционные аллергены развиваются позже [1, 4, 8, 11, 15] и появление этих заболеваний чаще отмечается у детей в возрасте старше 5 лет (81% у детей с сочетанием трех аллергических заболеваний (БА+АД+АР) и 73% - при сочетании двух болезней (БА+АД или БА+АР или АД+АР)).
В развитии аллергических заболеваний у детей важную роль играет пищевая аллергия. Проблема пищевой аллергии у детей - это, прежде всего развитие кожной и гастроинтестинальной аллергии к белкам коровьего молока, яиц, злаков, преобладающей среди манифестных форм аллергии у детей раннего возраста, у детей с изолированным атопическим дерматитом в 64% случаев пищевая аллергия является ведущим факторов в развитии и поддержании симптомов заболевания. У детей, имеющих сочетанные формы заболевания, она имеет значение ведущего фактора только в 17% (сочетание БА+АД+АР) -18% (БА+АД или БА+АР или АД+АР) (рисунок 1).
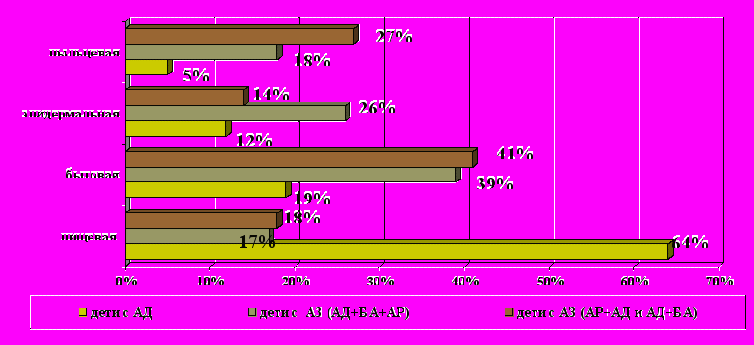
Рисунок 1 - Характер сенсибилизации у детей с сочетанием аллергических болезней
По данным литературы [1, 2, 4, 5, 8, 9, 12], существуют определенная последовательность развития сенсибилизации и возрастные особенности развития аллергических болезней у детей. С возрастом сенсибилизация к пищевым аллергенам у детей уменьшается. По результатам нашего исследования, приблизительно у половины детей с пищевой аллергией в анамнезе к 3-5 годам появляется повышенная чувствительность к ингаляционным, бытовым, пыльцевым аллергенам. У одной трети детей к этому возрасту развивается поллиноз (рисунок 2).
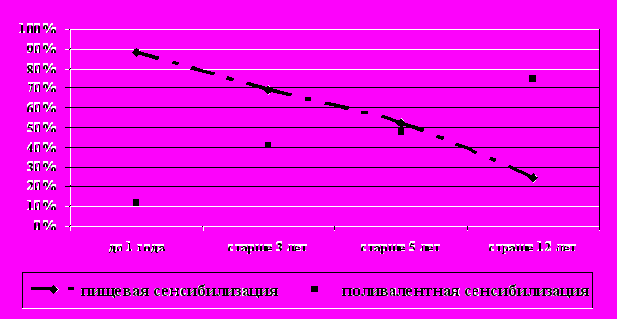
Рисунок 2 - Возрастной аспект характера сенсибилизации
Сенсибилизация к пыльцевым аллергенам является причинно-значимой в развитии аллергического процесса в среднем у 20% детей с аллергическими заболеваниями, при этом отмечается возрастание роли пыльцевой сенсибилизации в формировании аллергической патологии с увеличением возраста детей (рисунки 1, 2).
По данным аллергологического обследования (скарификационные кожные пробы, ППН) нами установлено, что 76% детей с сочетанием заболеваний БА+АД+АР имели поливалентную сенсибилизацию, а в группе детей с сочетанием двух болезней (БА+АД или БА+АР или АД+АР) – у 62%.
По результатам проведенного клинического обследования выявлено, что в группе детей имеющих сочетание трех заболеваний (БА+АД+АР) бронхиальная астма и атопический дерматит имели в основном среднюю и тяжелую степень тяжести (БА – средняя степень – 45%, тяжелая – 32%, АД – 43% и 35% соответственно). В группе пациентов с сочетанием двух заболеваний определялась чаще легкая и средняя степень тяжести БА и АД (БА- легкая степень – 33%, средняя – 41%; АД – 34% и 46% соответственно).
В развитии аллергических заболеваний определяющее значение имеют изменения в функционировании иммунной системы. Возникновение атопических болезней связано с IgE-опосредуемыми аллергическими реакциями.
По результатам исследований иммунологических показателей у детей, страдающих сочетанными формами атопических заболеваний, выявлен ряд особенностей. При сравнении с аналогичными показателями у детей в контрольной группе для детей с различными сочетаниями атопических болезней установлено достоверное повышение количества Т-лимфоцитов (CD3+-клеток) (в группе АД+АР или БА+АД или БА+АР и у детей с изолированным АД) (Р<0,05) и достоверное снижение содержания CD8+-клеток, обладающих супрессорной активностью (Р<0,01) у детей всех групп. Это обуславливает значительное повышение иммунорегуляторного индекса (соотношение CD4+/CD8+) (Р<0,01) (таблица 1).
Таблица 1 - Иммунологические показатели у обследованных детей (M±m)
| Параметры | Дети с сочетанием БА+АД +АР n=20 | Дети с сочетанием АД+АР, БА+АД, АД+АР n=32 | Дети с изолированным АД, n=41 | Контроль, n=50 |
| Средний возраст (лет) | 10,90,7 | 11,40,51 | 11,00.4 | 11,6 0,37 |
| CD3 (%) | 60,64,34 | 64,21,41* | 63,71,4* | 59,6 0,7 |
| CD3 (кл/л х106) | 1383,878,6* | 1329,8 89,1 | 1259,197,5 | 1068,9 36,9 |
| CD4 (%) | 42,73,2 | 46,41,8 | 45,91,6 | 43,4 0,4 |
| CD4 (кл/л х106) | 578,6,175,4 | 613,9 57,8 | 583,157,1 | 464,5 17,1 |
| CD8 (%) | 21,92,0** | 22,81,3** | 22,31,3** | 30,5 0,5 |
| CD8 (кл/л х106) | 294,443,3 | 311,236,1 | 288,432,7 | 322,2 10,7 |
| CD4/CD8 | 2,00,17** | 2,290,22** | 2,280,2** | 1,4 0,05 |
| CD20 (%) | 13,71,75* | 15,51,38* | 15,21,36 | 17,9 0,3 |
| CD20 (кл/л х106) | 308,643,1 | 302,135,5 | 277.828,8 | 321,2 11,8 |
| IgG (г/л) | 9,50,9 | 9,980,34 | 9,90,3 | 10,6 0,3 |
| IgA (г/л) | 1,070,06**# | 1,340,07# | 1,370,07# | 1,4 0,05 |
| IgM (г/л) | 0,880,04 | 1,080,04* | 1,090,04* | 0,9 0,04 |
| IgE (IU/ml) | 881,6167,4** | 426,8 65,2** | 406,534,1** | 104,5 12,2 |
| Эозинофилы (%) | 3,21,15 | 2,91 0,42* | 2,90,44* | 1,9 0,1 |
| Эозинофилы (кл/л х106) | 198,930,8* | 145,0 27,6 | 139,226,0 | 88,1 6,9 |
| ФП, % | 41,42,3 | 44,11,16 | 43,81,2 | 44,1 0,5 |
| ФЧ, ед. | 3,50,21** | 3,710,1** | 3,60,1** | 5,1 0, 1 |
| Ig G, мг/мл (слюны) | 0,120,03 | 0,090,01 | 0,090,01 | 0,08 0,02 |
| Ig A, мг/мл (слюны) | 0,070,01** | 0,080,01** | 0,080,01** | 0,2 0,04 |
| Ig As, мг/мл (слюны) | 0,630,01* | 0,710,11 | 0,720,1 | 0,7 0,05 |
| Ig M, мг/мл (слюны) | 0,020,005* | 0,030,007 | 0,030,006 | 0,04 0,004 |
Примечание - Достоверность различий в сравнении с контролем: * (P<0,05);
Достоверность различий в сравнении с контролем: ** (P<0,01);
Достоверность различий в сравнении между группами: # (P<0,05).
При изучении показателей гуморального звена иммунитета у детей, страдающих атопическими заболеваниями (различные их сочетания), выявлен ряд отличий (сравнение с данными контрольной группы) (таблица 1). Отмечено значительное снижение процентного содержания В-лимфоцитов (CD20+-клеток) и повышение концентрации IgЕ в сыворотке крови (Р<0,01). Дисгаммаглобулинемия у детей с различным сочетанием атопических болезней характеризовалась повышением концентрации IgМ (в группе детей с изолированным АД и с сочетанием АД+АР или БА+АД или БА+АР). Снижение концентрации IgA в сыворотке крови выявлено в группе детей с сочетанием трех аллергических заболеваний (БА+АД+АР) в сравнении с контролем и по сравнению с другими группами пациентов с аллергическими заболеваниями, в этой же группе пациентов выявлены наиболее высокие уровни IgE (более 500 IU/ml) (Р<0,01). У детей с атопическими болезнями установлена отрицательная корреляционная взаимосвязь между концентрацией IgE сыворотки крови и процентным содержанием CD8+-клеток (r=-0,67, Р<0,05). Показатель фагоцитарного числа у всех обследованных детей был достоверно сниженным по сравнению с данными контроля (Р<0,01). Для всех детей с сочетанием атопических заболеваний (БА, АД, АР) установлено достоверное снижение концентрации IgA в слюне (Р<0,05) (таблица 1).
Изучение показателей липидного спектра сыворотки крови проведено у 60 детей и подростков, из них 10 пациентов с сочетанием БА+АБ+АР, 13 детей с сочетанием АД+БА или АД+АР или БА+АР и 7 больных с изолированными АД или БА (таблица 2).
Таблица 2 - Показатели липидного спектра крови у обследованных детей
| Параметры | Пациенты с сочетанием БА+АД+АР n = 10 | Пациенты с сочетанием АД+БА, АД+АР, БА+АР n = 13 | Пациенты с изолированными АД или БА n = 7 | Контроль n = 30 |
| Средний возраст, лет | 10,90,7 | 11,40,51 | 11,00.4 | 11,6 0,37 |
| ОЛ, г/л | 4,92±0,64 | 5,95±0,56 | 6,1±0,24 | 5,31±0,66 |
| ОФЛ, ммоль/л | 2,59±0,35 | 3,13±0,2 | 2,21±0,25 | 2,29±0,54 |
| ОХС, ммоль/л | 3,76±0,18 | 4,24±0,24 | 4,12±0,35 | 3,71±0,69 |
| α-ХС, ммоль/л | 0,97±0,12* | 1,13±0,19 | 0,99±0,16 | 1,38±0,54 |
| ТГ, ммоль/л | 1,08±0,17 | 1,03±0,09 | 0,94±0,10 | 0,83±0,39 |
| ЛПОНП, ммоль/л | 1,87±0,16 | 2,02±0,26 | 1,16±0,12 | 1,29±0,33 |
| ЛПНП, ммоль/л | 2,81±0,95 | 2,13±0,08 | 2,39±0,05 | 2,52±0,6 |
| КА | 2,87±1,3* | 2,75±1,29 | 3,16±0,91* | 2,16±0,88 |
| Примечание – Достоверность различий в сравнении с контролем: * – Р<0,05. | ||||
У детей с сочетанием трех заболеваний (БА, АД и АР) установлено достоверное снижение содержания α-холестерина (α-ХС) и повышение коэффициента атерогенности при сравнении с контрольной группой (Р < 0,05).
При анализе показателей липидного спектра в зависимости от концентрации общего IgE установлено достоверное снижение уровня α-холестерина (α-ХС) и повышение коэффициента атерогенности у детей, имеющих наиболее высокие концентрации общего IgE (выше 500 Ul/ml) в сравнении с контролем (Р<0,05) (таблица 3). При сравнении показателей липидного спектра в группах детей, имеющих различные значения уровня общего IgE, установлено достоверное (Р<0,05) повышение общих липидов между группой детей с низким и средним уровнем общего IgE, а также повышение триглицеридов между группами с низким и средним, низким и высоким уровнями IgE.
Таблица 3 - Показатели липидного спектра крови у обследованных детей
| Параметры | Уровень общего IgE до 100 Ul/ml n = 7 | Уровень общего IgE от 100 до 500 Ul/ml n = 11 | Уровень общего IgE выше 500 Ul/ml n = 12 | Контроль n = 30 |
| ОЛ, г/л | 3,89±0,80 | 7,07±0,96# | 5,41±0,80 | 5,31±0,66 |
| ОФЛ, ммоль/л | 2,98±0,31 | 3,18±0,34 | 2,79±0,45 | 2,29±0,54 |
| ОХС, ммоль/л | 3,62±0,29 | 3,95±0,34 | 4,06±0,34 | 3,71±0,69 |
| α-ХС, ммоль/л | 1,15±0,29 | 1,13±0,06 | 1,02±0,16* | 1,38±0,54 |
| ТГ, ммоль/л | 0,68±0,07# | 1,14±0,24# | 1,11±0,16# | 0,83±0,39 |
| КА | 2,14±0,93 | 2,49±1,02 | 2,98±0,71* | 2,16±0,88 |
| Примечание – Достоверность различий в сравнении с контролем: * – Р<0,05; Достоверность различий в сравнении между группами: # – Р<0,05 . | ||||
При проведении корреляционного анализа установлена отрицательная корреляционная зависимость между значаниями: общего IgE и ОЛ (r= -0,51, Р<0,05) и между значаниями общего IgE и ФЛ ( r= -0,5, Р<0,05).
Установлено, что для детей, страдающих хроническими аллергическими заболеваниями: характерны особенности поведения, установлено отрицательное влияние болезни на характер и качество жизни, с учетом преувеличенного внимания к собственному состоянию здоровья это не может не отражаться на течении основного заболевания.
Проведенный с помощью теста Ч.Д. Спилбергера опрос пациентов, страдающих хроническими аллергическими заболеваниями в возрасте старше 9 лет (средний возраст 12,69±0,28 лет) выявил у подавляющего большинства обследованных детей и подростков наличие повышенного уровня тревожности как личностной (ЛТ) (рисунок 3), так и реактивной (РТ) (рисунок 4), в отличие от здоровых детей и подростков.
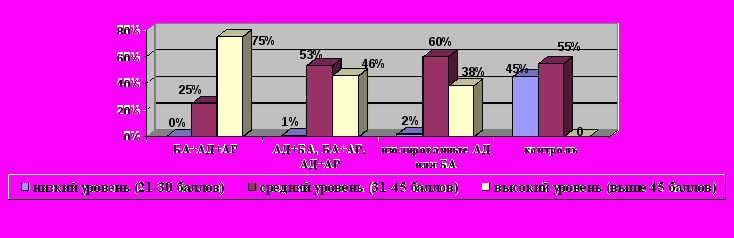 Рисунок 3- Оценка выраженности личностной тревожности по Ч.Д. Спилбергеру
Рисунок 3- Оценка выраженности личностной тревожности по Ч.Д. СпилбергеруПри оценке ЛТ большинство пациентов имели признаки умеренной тревожности – 53% в группе с сочетанием двух заболеваний (БА+АД или БА+АР или АР+АД), 60% в группе с изолированными АД или БА. Высокий уровень ЛТ определялся у 75% детей с сочетанием трех заболеваний (БА+АД+АР).
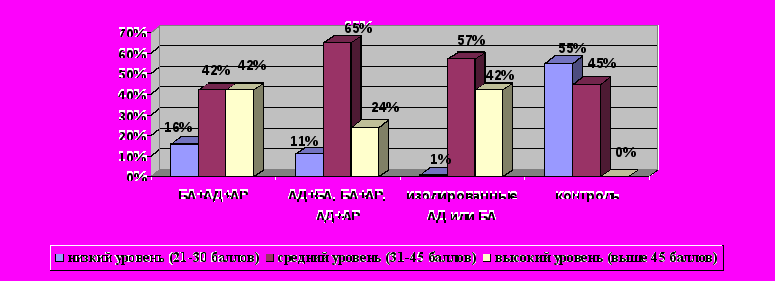 Рисунок 4 - Оценка выраженности реактивной тревожности по Ч.Д. Спилбергеру
Рисунок 4 - Оценка выраженности реактивной тревожности по Ч.Д. СпилбергеруКак видно из рисунка 4, достоверно чаще высокие уровни реактивной тревожности встречались у пациентов, страдающих сочетанными аллергическими заболеваниями (БА+АД+АР) и с изолированными АД или БА в сравнении с контрольной группой. Средний уровень РТ выявлен у 42% пациентов с сочетанием трех заболеваний (БА+АД+АР), у 65% с сочетанием двух болезней (БА+АД или БА+АР или АР+АД), у 57% с изолированным атопическим дерматитом. Низкий уровень РТ определен лишь у 1% детей с изолированными АД или БА и у 11% - 16% детей с сочетанием аллергических заболеваний, а также у большинства (55%) детей контрольной группы.
Результаты тестирования указывают на то, что достоверно чаще (Р<0,01) средний и высокий уровни тревожности как реактивной, так и личностной, встречались у детей с сочетанием аллергических заболеваний (в сумме средние и высокие показатели личностной тревожности выявлены у 100% пациентов с сочетанием БА+АД+АР, у 99% с сочетанием БА+АД или БА+АР или АД+АР, 55% здоровых детей; реактивной тревожности - в 84%, в 90%, в 99% и в 45% случаев соответственно). Это предполагает наличие у детей с аллергическими болезнями пограничных состояний с признаками угрозы самооценке, снижающих порог устойчивости к стрессовым ситуациям.
Как известно, личностная тревожность характеризует устойчивую склонность воспринимать большой круг ситуаций как угрожающие и реагировать на них состоянием тревоги. Высокая ЛТ коррелирует с наличием невротического конфликта, с эмоциональными и невротическими срывами. Реактивная тревожность характеризуется напряжением, беспокойством, нервозностью.
Среднестатистические показатели РТ и ЛТ оказались достоверно выше (Р<0,01) у детей с аллергическими заболеваниями в сравнении с показателями реактивной и личностной тревожности у детей контрольной группы (таблица 4).
Таблица 4 - Средние показатели реактивной и личностной тревожности
| Исследуемые параметры | Дети с сочетанием БА+АД, БА+АР, АД+АР I группа n = 17 | Дети с сочетанием БА+АД+АР II группа n = 26 | Дети с изолированным АД III группа n = 36 | Здоровые дети IV группа n = 30 | Р I – IV II – IV III - IV |
| ЛТ (в баллах) | 44,5 ± 0,84* | 48,8 ± 3,27* | 44,7 ±0,88 | 32,7 ± 0,93* | <0,01 |
| РТ (в баллах) | 39,8 ± 0,95 | 41,6 ± 2,86* | 45,07±1,83* | 28,9 ± 0,35 | <0,01 |
Примечание – Достоверность различий в сравнении с контролем: * – Р<0,05.
Таким образом, для детей, страдающих сочетанными аллергическими заболеваниями, характерно повышение уровней, как РТ, так и ЛТ, что с учетом преувеличенного внимания к собственному состоянию здоровья не может не отражаться на течении основного заболевания. Полученные результаты являются убедительным доказательством, определяющим показания к психотерапевтической помощи детям и подросткам с аллергическими заболеваниями с включением соответствующей коррекции в комплексную терапию этих пациентов.
Выводы:
- Клинические проявления атопических болезней у детей характеризуются последовательностью развития симптомов аллергии и сенсибилизации, как правило, с дебютом атопического дерматита на первом году жизни.
- С возрастом - спектр сенсибилизации расширяется:
- у детей старше 5-6 лет преобладает поливалентная сенсибилизация, формируется «респираторный аллергический синдром»;
- в результате - формируются сочетанные формы атопических болезней (дерматит, астма, ринит).
- Для детей, страдающих хроническими аллергическими болезнями, причем независимо от вариантов их сочетания, характерны значительные нарушения со стороны показателей иммунитета, как клеточного, так гуморального и местного, которые в целом характеризуются повышением CD3+- (Р<0,05), иммунорегуляторного индекса (Р<0,01), содержания эозинофилов в периферической крови; снижением количества CD8+- и CD20+-клеток (Р<0,01) и фагоцитарного числа (Р<0,01), а также повышением концентрации IgE в сыворотке крови, а для пациентов с сочетанием трех заболеваний (БА+АД+АР) характерно еще и снижение концентрации IgA (Р<0,05) в крови и Ig As в слюне. Полученные данные позволяют говорить о патогенетической общности всех этих заболеваний (БА, АД, АР).
- У детей в группе с сочетанием основных атопических болезней (БА+АД+АР) в показателях липидного спектра установлено достоверное (Р<0,05) снижение уровня a-холестерина и повышение коэффициента атерогенности.
- Для детей с сочетанием аллергических болезней (БА+АД+АР) характерно повышение уровней, как РТ, так и ЛТ. Это свидетельствуют о том, что повышенный уровень РТ может быть связан с тревогой вследствие госпитализации в стационар (модель нестандартной ситуации), а высокие уровни ЛТ у этих пациентов следует расценивать не только как поведенческие их индивидуальные особенности, но также и как следствие влияния основного заболевания. Полученные результаты обосновывают показания к включению соответствующей психотерапевтической коррекции в комплексную терапию пациентов с сочетанными аллергическими заболеваниями.
Литература:
- Аллергические риниты у детей (этиология, патогенез, клиника, диагностика, лечение / Л.М.Беляева, В.Ф.Жерносек, С.М.Король и др.//Метод. рекомендации. – Минск, 2002. – 22с.
- Аллергический ринит и его влияние на бронхиальную астму (ARIA) // Аллергология. – 2001.- № 3. – С. 45-56.
- Балаболкин И.И. Аллергия у детей и экология / И.И. Балаболкин // Рос. педиатр. журн. – 2002. – № 5. – С. 4 – 8.
- Балаболкин И.И. Атопия и аллергические заболевания у детей // Педиатрия. – 2003. - № 6. – С. 99-102.
- Беляева Л.М. Атопический дерматит и аллергический ринит у детей и подростков / Л.М. Беляева – Минск: ООО «В.И.З.А.ГРУПП». - 2006. – С. 8 – 135.
- Беляева Л.М. Дифференциально-диагностический комплекс клинических, иммунологических и гормональных признаков у детей школьного возраста, страдающих атопическим дерматитом / Л.М. Беляева, Н.В. Микульчик // Мед. панорама. – 2006. – № 1. – С. 16–20.
- Иммунология и аллергология. Алгоритмы диагностики и лечения / под ред. Р. М. Хаитова. М.: ГЭОТАР-МЕД. - 2003. – 111 с.
- Микульчик Н.В., Беляева Л.М., Кирильчик Е.Ю. Клинические признаки и иммунологические показатели у детей школьного возраста, страдающих атопическим дерматитом // Здравоохранение. – 2004. - № 4. - С. 32-35.
- Ревякина В.А., Филатова Т.А. От атопического дерматита до бронхиальной астмы у детей //Лечащий врач. – 2006. - № 1. - С. 16-20.
- Ревякина В. А. Атопия и атопические заболевания у детей. Consillium medicum. - 2001. - Том 3. - № 4.
- Aalberse RC, Akkerdaasjh, van Ree R. Cross-reactivity of IgE antibodies to allergens. Allergy 2001; 56: 478-490.
- Bukantz SC. Clemens von Pirquet and the concept of allergie. J Allergy Clin Immunol 2002; 109:724-726.
- Busse W.W. // Allergy and Clin.immunology.-1990; 85(4): 671-83 ;
- Edwards A. Mechanism of allergic disease / The Year in Allergy 2003 / eds. S.Holgate, S.Arshad. – Oxford, 2003. – P. 83 – 100.
- Holt PG, Jones CA. The immunology of fetuses and infants. The development of the immune system during pregnancy and early life // Allergy 2000: 55: 688-697.
- Holgate S. Abstracts 2nd International symposium on allergy management. 2000; 22-3;
- Johansson SGO, Hourinehane JOB, Bousquet J et al.A revised nomenclature for Allergy. An EAACI position statement from the EAACI nomenclature task force. Allergy 2001;56:813-824.
- Mollica F. // Ann. Allergy.-1991; 66: 490-3
- SimpsonE.L., J.M.Hanifin Atopic dermatitis // Med. Clin. North. Am. – 2006. –Vol.90, №1. – P. 149-67.
- Schmidt (-Grendelmeier) P, Simon D, Simon H-U, Adkis CA, Wüthrich B. Epidemiology, clinical features and immunology of the 'intrinsic' (non-IgE-mediated) type of atopic dermatitis (constitutional dermatitis)// Allergy 2001; 56: 841-849.
- Spergel J., Paller A. Atopic dermatitis and the atopic march//J. Allergy. Clin. Immunol. 2003; 112: 128–139.
Репродуктивное здоровье в Беларуси. – 2009. - №4 (04). – С.94-105.
