Роль генов системы биотрансформации ксенобиотиков в механизмах формирования и развития профессиональных аллергических дерматозов 14. 02. 04. Медицина труда
| Вид материала | Автореферат диссертации |
- Роль нейрогуморальной и аденилатциклазной систем в патогенезе профессиональных аллергических, 326.54kb.
- Ществ, влияя непосредственно или через изменение экспрессии генов различных белков,, 219.65kb.
- Рабочая программа дисциплины «введение в биохимическую экологию» Код дисциплины, 145.9kb.
- О. Д. Куканова история формирования культуры профессионального здоровья в россии, 88.69kb.
- Пахарукова Мария Юрьевна Изучение роли транскрипционных факторов hnf3 и рецепторов, 208.86kb.
- Особенности формирования нарушений здоровья и их профилактика у работников нефтедобывающей, 583.82kb.
- Роль социально-психологических факторов в формировании профессионального стресса при, 255.34kb.
- Стремительные успехи в секвенировании геномов эукариот выдвинули на первый план необходимость, 155.19kb.
- Г г. Москва Об утверждении Рекомендаций по организации работы кабинета охраны труда, 84.4kb.
- Программа-минимум кандидатского экзамена по специальности 03. 02. 07- «Генетика», 129.56kb.
На правах рукописи
КОЛЯСКИНА МАРИЯ МИХАЙЛОВНА
РОЛЬ ГЕНОВ СИСТЕМЫ БИОТРАНСФОРМАЦИИ КСЕНОБИОТИКОВ В МЕХАНИЗМАХ ФОРМИРОВАНИЯ И РАЗВИТИЯ ПРОФЕССИОНАЛЬНЫХ АЛЛЕРГИЧЕСКИХ ДЕРМАТОЗОВ
14.02.04. – Медицина труда
Автореферат
диссертации на соискание учёной степени
кандидата медицинских наук
Москва – 2011
Работа выполнена в Учреждении Российской академии медицинских наук Научно-исследовательском институте медицины труда РАМН
| Научный руководитель: | Доктор биологических наук, профессор Кузьмина Людмила Павловна |
| Научный консультант: | Доктор медицинских наук, профессор Измерова Наталья Ивановна |
| | |
| Официальные оппоненты: | Доктор медицинских наук, профессор Журков Вячеслав Серафимович |
| Кандидат медицинских наук Соркина Нелли Соломоновна | |
| | |
| Ведущая организация: | Государственное образовательное учреждение дополнительного профессионального образования «Российская медицинская академия последипломного образования Федерального агентства по здравоохранению и социальному развитию» |
Защита состоится «26» сентября 2011 года на заседании диссертационного совета Д.001.012.01. при Учреждении Российской академии медицинских наук Научно-исследовательском институте медицины труда РАМН по адресу: 105275 Москва, проспект Будённого, 31.
С диссертацией можно ознакомиться в библиотеке НИИ МТ РАМН.
Автореферат разослан « ____ » _____________ 2011 г.
Учёный секретарь
диссертационного совета,
доктор биологических наук, профессор Рубцова Нина Борисовна
АКТУАЛЬНОСТЬ РАБОТЫ. В последние годы широкое распространение получили геномные и протеомные исследования по изучению генетико-биохимических полиморфных систем и взаимосвязи отдельных аллельных вариантов генов с различными патологическими процессами, с интенсивностью протекания биохимических реакций, с особенностями метаболизма лекарственных средств, с предрасположенностью к различным видам спортивной деятельности и т.д. [А.И. Арчаков, 2002, В.М. Говорун, 2003, В.А. Спицын, 2006, Л.П. Кузьмина, 2010, К.О. Миронов, 2010].
Многообразие производственных химических соединений с раздражающими и сенсибилизирующими свойствами, их комплексное воздействие на организм и кожу, в частности, в сочетании с многочисленными факторами экзо- и эндогенного характера, включая генетически обусловленные особенности метаболизма, приводят к формированию и развитию профессиональных аллергических дерматозов [Н.И. Измерова, 2006, Г.Д. Селисский, 2003].
Высокая распространенность данной патологии в структуре профессиональной заболеваемости, тенденция к продолжающемуся росту обуславливают актуальность дальнейшего изучения патогенетических особенностей формирования профаллергодерматозов для выявления генетических и биохимических маркеров предрасположенности.
Комплексный и комбинированный характер воздействия химических веществ на организм, особенности токсикокинетики, популяционная и индивидуальная чувствительность к химическим веществам обуславливают особенности протекания метаболических реакций, определяющих преобладание процессов детоксикации или активации химических веществ, влияющих на сроки формирования и течение профессиональных аллергодерматозов.
Данные многочисленных исследований, выполненных в России и за рубежом, позволяют утверждать, что одним из основных биохимических процессов, определяющих индивидуальный ответ организма на воздействие ксенобиотиков, в том числе и лекарственных веществ, является биотрансформация с преимущественным участием многочисленного семейства цитохромов Р-450, ферментов конъюгации и транспортных белков [В.В. Ляхович, Цырлов И.Б., 1981, А.И. Арчаков, 2002, В.А. Спицын, 2006, D.V. Parke, 1991].
Риск развития заболеваний от воздействия веществ токсического и аллергенного действия связан с высокой активностью множественных форм цитохромов Р450 в сочетании с низкой активностью ферментов II-й фазы биотрансформации и приводит к увеличению риска развития интоксикаций, иммунопатологических процессов и формированию профессиональных и производственно-обусловленных заболеваний.
Исследования, посвященные изучению роли генетико-биохимической полиморфной цитохром Р-450 зависимой монооксигеназной системы в механизмах развития профаллергодерматозов носят ограниченный характер и требуют дальнейшего изучения для разработки патогенетически обоснованной системы лечебно-профилактических мероприятий [Л.П.Кузьмина, Н.А. Лазарашвили, 2006, Wang BJ et al, 2007, Schnuch A. et al., 1998, Westphal GA et al., 2000, Brans R. et al., 2005].
Все вышесказанное определяет актуальность изучения роли полиморфных вариантов генов системы биотрансформации ксенобиотиков в механизмах формирования и развития профессиональных аллергических дерматозов, оценки индивидуального риска развития, прогноза и индивидуализированного подбора лекарственных средств у данного контингента.
Диссертационная работа выполнена в рамках госбюджетной темы НИИ МТ РАМН № 0904 «Производственные факторы, как триггеры в развитии наиболее распространенных форм общесоматической патологии и роль медицины труда в системе их профилактики».
Цель работы - изучение роли полиморфных вариантов генов системы биотрансформации ксенобиотиков в механизмах формирования и развития профессиональных аллергических дерматозов для обоснования генетико-биохимических критериев оценки риска развития, прогноза клинического течения и мониторинга эффективности лечебно-профилактических мероприятий.
В соответствии с целью данной работы предстояло решить следующие задачи:
1. Разработать тест-систему для определения полиморфных гомо и гетерозиготных вариантов генов системы биотрансформации ксенобиотиков (Cyp1A1, Cyp3A4, Эпоксидгидролазы 1) для внедрения в клинику медицины труда.
2. Провести генотипирование ферментов системы биотрансформации ксенобиотиков (Cyp1A1, Cyp3A4, Эпоксидгидролазы 1, GSTM1, GSTT1) у больных профессиональными аллергическими дерматозами для оценки значимости их генетического биохимического полиморфизма в механизмах формирования и развития указанной нозологии.
3. Изучить состояние системы «оксиданты-антиоксиданты» у больных с профессиональными заболеваниями кожи и проанализировать зависимость изменений в данной системе от генотипических разновидностей ферментов системы биотрансформации ксенобиотиков.
4. Исследовать уровень внеклеточной ДНК и ферментативной активности нуклеаз у больных профаллергодерматозами и проанализировать зависимость изменений указанных показателей от состояния системы оксиданты-антиоксиданты.
5. Обосновать клинико-лабораторный комплекс биохимических и молекулярно-генетических показателей для прогноза индивидуального риска развития профессиональных аллергических дерматозов, оценки тяжести клинического течения, научно обоснованного проведения профилактических и лечебных мероприятий.
НАУЧНАЯ НОВИЗНА. Впервые разработана тест-система для выявления полиморфизмов генов CYP 1A1, CYP3A4, ЕРНХ1 с применением реакции пиросеквенирования для внедрения в клинику медицины труда с целью оценки риска развития профессиональных и производственно обусловленных заболеваний.
Проведено комплексное исследование генетически полиморфной цитохром Р-450 зависимой монооксигеназной системы (CYP 1A1, CYP3A4, ЕРНХ1 и делеций генов GSTM1 и GSTT1), компонентов системы оксиданты-антиоксиданты, процессов повреждения ДНК и ферментативной активности нуклеаз у больных профаллергодерматозами. Показана взаимосвязь компонентов изученных систем и их роль в патогенетических механизмах развития профаллергодерматозов от воздействия веществ раздражающего и сенсибилизирующего действия.
Показаны особенности состояния системы оксиданты-антиоксиданты в зависимости от наличия различных вариантов полиморфных генов системы биотрансформации ксенобиотиков.
Изучена особенность сроков развития и клинического течения профаллергодерматозов в зависимости от наличия различных вариантов полиморфных генов системы биотрансформации ксенобиотиков.
Впервые проведены исследования по изучению уровня внеклеточной ДНК и нуклеазной активности и выявлена взаимосвязь накопления ДНК в плазме крови в зависимости от состояния системы оксиданты-антиоксиданты у больных профессиональными заболеваниями кожи.
Определены молекулярно-генетические и биохимические критерии риска развития и прогноза течения профессиональных аллергодерматозов.
ПРАКТИЧЕСКАЯ ЗНАЧИМОСТЬ. На основании выполненных молекулярно-генетических и биохимических исследований по изучению особенностей состояния цитохром Р-450 зависимой монооксигеназной системы у больных профессиональными аллергодерматозами разработаны критерии индивидуального риска развития профессиональной патологии кожи, которые могут быть использованы в системе профилактических и лечебно-диагностических мероприятий.
Основными формами внедрения являются:
- Заявка на патент №2011132624 от 04.08.2011г. «Способ прогнозирования сроков развития профессиональных аллергических дерматозов при воздействии факторов раздражающего и сенсибилизирующего действия»
- Заявка на патент №2011133883 от 12.08.2011г. «Способ прогнозирования риска раннего развития профессиональных аллергических дерматозов»
- Результаты диссертационной работы легли в основу методических пособий для врачей «Состояние системы «оксиданты-антиоксиданты» у больных профессиональными аллергическими дерматозами (диагностика, риск развития, прогноз, профилактика)», Москва 2009г., «Проблема индивидуальной чувствительности в медицине труда» Москва 2009г. и «Биохимические и молекулярно-генетические маркеры предрасположенности к развитию профаллергодерматозов», Москва 2011г.
АПРОБАЦИЯ РАБОТЫ проведена на заседании специалистов клинического отдела профессиональных и производственно обусловленных заболеваний НИИ Медицины труда РАМН (17.06.2011г.).
Материалы диссертации доложены и обсуждены на: Научно-практической конференции молодых ученых и специалистов научно-исследовательских организаций Роспотребнадзора (Оболенск, 2010г.), Всероссийской научно-практической конференции «Производственно-обусловленные нарушения здоровья работников в современных условиях» (Шахты. 2010г.), VIII и IX Всероссийском Конгрессе «Профессия и здоровье» (Москва, 2009 и 2010гг.), в рамках IX Всероссийского Конгресса «Профессия и здоровье» проводился конкурс молодых учёных, по результатам которого данная работа удостоена диплома (I место), VII Всероссийской научно-практической конференции с международным участием «Молекулярная диагностика - 2010» (Москва, 2010г.), Пленуме отделения профилактической медицины РАМН «Научно-методические и законодательные основы обеспечения генетической безопасности факторов и объектов окружающей и производственной среды в целях сохранения здоровья человека» (Москва, 2010г.), симпозиуме «Применение комплексных программ для санаторно-курортного лечения и реабилитации больных профессиональными заболеваниями и пострадавших от производственных травм и несчастных случаев», проведенного в рамках Всероссийского Форума «Развитие санаторно-курортной помощи, восстановительной медицины и медицинской реабилитации» (Москва, 2010г.), Всероссийской научно-практической конференции с международным участием «Связь заболевания с профессией с позиции доказательной медицины» (Казань, 2011г.), Окружной конференции «Центральный федеральный округ: инновационные компании - системе здравоохранения» (Дубна, 2011г.).
ПУБЛИКАЦИИ. По теме диссертации опубликовано 17 работ.
ОБЪЁМ И СТРУКТУРА ДИССЕРТАЦИИ. Работа изложена на _____ страницах машинописного текста, состоит из введения, глав, обсуждения, выводов, списка литературы, содержащего _____ отечественных и _____ иностранных источников. Иллюстрации представлены таблицами и рисунками.
ОСНОВНЫЕ ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ:
1. В патогененетических механизмах развития профессиональных аллергодерматозов от воздействия веществ раздражающего и сенсибилизирующего действия важную роль играет сопряженность генетико-биохимической полиморфной цитохром Р-450 зависимой монооксигеназной системы, процессов перекисного окисления липидов и антиоксидантной защиты.
2. Сочетание неблагоприятных гетеро- и гомозиготных аллелей генов CYP 1A1, CYP3A4, ЕРНХ1 и делеций генов GSTM1 и GSTT1, низкий количественный уровень GSTР1 характеризуются ранним (при стаже работы во вредных условиях до 5 лет) развитием и неблагоприятным прогнозом клинического течения профессиональной патологии кожи.
3. Для оценки риска развития профессиональной патологии кожи целесообразно определять биохимические и молекулярно-генетические показатели цитохром Р-450 зависимой монооксигеназной системы, показатели системы оксиданты-антиоксиданты и уровень внеклеточной ДНК с нуклеазной активностью.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Для решения поставленных в работе задач в условиях клиники НИИ МТ РАМН был обследован 201 человек с профессиональными аллергодерматозами (экзема и аллергический дерматит). Результаты биохимических исследований сопоставлялись с контрольной группой из 40 практически здоровых лиц, не имевших заболеваний кожи и контакта с веществами раздражающего и сенсибилизирующего действия. При исследовании генетических биохимических маркеров (GSTM1, GSTT1, CYP 1A1) в качестве контроля использовались результаты анализов крови 250 практически здоровых лиц (данные профессора Спицына В.А.). При изучении полиморфизмов генов CYP 3A4 и EPHX1, полученные нами результаты сравнивались с литературными данными (с использованием базы данных NCBI). Статистическая обработка результатов проводилась с использованием компьютерной программы «Биостат».
Общее клиническое обследование больных проводилось в дерматологическом отделении клиники НИИ Медицины труда РАМН. Профессиональное заболевание кожи диагностировалось на основании профессионального маршрута больного, санитарно-гигиенической характеристики условий труда, данных анамнеза, клинической картины, течения заболевания и выявленной повышенной чувствительности к промышленным аллергенам при кожном тестировании и цитохимическом исследовании периферической крови.
Для решения поставленных в работе задач с учетом известных звеньев патогенеза аллергических заболеваний кожи и характера действующих производственных факторов был разработан комплекс биохимических и молекулярно-генетических показателей, характеризующий активность свободнорадикальных процессов и процессов антиоксидантной защиты, степень повреждения клеточной мембраны и состояние генетически полиморфной системы биотрансформации ксенобиотиков.
Для оценки интенсивности процессов перекисного окисления было определено количественное содержание продуктов перекисного окисления липидов ((диеновые конъюгаты (ДК), кетодиены (КД) и карбонилы (КБ)). Определение продуктов перекисного окисления липидов проводили в сыворотке венозной крови, взятой натощак. Определение концентрации катаболитов проводили спектрофотометрически в гексановом экстракте на спектрофотометре «Cary-50» по их коэффициентам экстинкции (εM, М-1* см-1) в максимумах поглощения против холостой пробы [Pompella, A., 1987, Klein, R.A., 1970]. Для оценки состояния тиол-дисульфидной окислительно-восстановительной системы (SH, SS и отношение SH/SS) в работе использовался метод Эллмана. Принцип метода основан на способности низкомолекулярных тиоловых соединений, при взаимодействии с реактивом Эллмана образовывать окрашенное соединение (тио-2-нитробензойная кислота), водный раствор которого имеет максимум поглощения при длине волны 412 нм. Измерение проводилось на автоматическом иммуноферментном анализаторе «DYNEX».
Количественное содержание глутатион-S-трансферазы Р 1 (GSTР1) определяли в сыворотке крови больных методом иммуноферментного анализа с использованием тест-системы «GST-pi ELISA Kit» фирмы «Immundiagnostik» (Германия) с оценкой результатов на автоматическом иммуноферментном анализаторе «DYNEX».
В ходе выполнения работы были исследованы полиморфные варианты генов глутатион-S-трансферазы М1 (ген GSTМ1), глутатион-S-трансферазы Т1 (ген GSTТ1), цитохромов Р-450 (гены CYP1A1 (*2C I462V (A>G)) и CYP3A4 (*1B A>G)), микросомальной эпоксидгидролазы 1 (ЕРНХ1 полиморфизмы H139R (A-415G) и Y113H (Т-337С)).
Для определения генетических полиморфизмов генов CYP 1A1, CYP3A4, ЕРНХ1 совместно с лабораторией постгеномных технологий (зав. лабораторией постгеномных технологий, академик РАМН В.В. Покровский) был разработан новый метод определения замены в нуклеотидной последовательности генов CYP 1A1, CYP3A4, ЕРНХ1 - метод ПЦР с применением реакции пиросеквенирования.
Используемый в основе метода принцип пиросеквенирующего синтеза обеспечивает надежность и точность полученных результатов, высокую пропускную способность, максимальную автоматизированность процесса и быстроту проведения анализа [Chen D.C. et al., 2003; Royo J.L. et al., 2009]. Пиросеквенирование является новым поколением методик секвенирования, нашедшее свое применение, как в фундаментальных исследованиях, так и в диагностических целях [Voelkerding K.V. et al, 2009]. Для пиросеквенирования использовались приборы и станция для пробоподготовки фирмы «Qiagen», Германия. Для пиросеквинирования использовались пиросеквенаторы «PyroMark Q96 MD» и «PyroMark Q24».
Анализ полиморфных систем генов GSTМ1 и GSTТ1 проводили методом полимеразной цепной реакции (ПЦР) на амплификаторе “Терцик” фирмы “ДНК-технология” (установка presice regulation, определяющая характеристику изменения температур) с использованием локусспецифических олигонуклеотидных праймеров (использованы реагенты производства ФГУН ЦНИИЭ Роспотребнадзора) и анализом продуктов реакции в 3% полиакриламидном геле с последующей окраской этидиумбромидом и визуализацией в проходящем УФ-свете.
Выделение внеклеточной ДНК проводили методом экстракции органическими растворителями. Концентрацию внеклеточной ДНК определяли флуориметрически на люминесцентном спектрометре «LS 55» («PerkinElmer», Англия) c использованием ДНК-связывающегося красителя Hoechst 33258. Нуклеазную активность определяли по увеличению интенсивности флуоресценции с использованием модельного субстрата - комплекса однонитевой ДНК с 30-звенным олигонуклеотидом R6G ACC CCC AGC GAT TAT CCА AGC GCG BHQ1, включающим флуоресцирующую группу (R6G, 5(6)-карбоксиродамин) и молекулу тушителя (BHQ1, «Синтол», Москва) (Совместно с лабораторией молекулярной биологии Медико-генетического научного центра РАМН, руководитель: д.б.н. Н.Н. Вейко).
Статистическая обработка результатов проводилась с использованием компьютерной программы "Биостат". Был применен анализ качественных и количественных признаков с применением параметрических (однофакторный дисперсионный анализ, критерий Стьюдента) и непараметрических (анализ множественных попарных сравнений с применением критерия χ2) критериев статистической обработки.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
Характеристика обследованного контингента больных и условий их труда
Условия труда оценивались нами с учётом результатов научных разработок сотрудников гигиенических подразделений института, а также по данным характеристик условий труда, представленных территориальными ЦГСЭН с мест работы заболевших.
Обследованные в условиях стационара 201 человек работали на различных предприятиях, в основном г. Москвы и Московской области. Все они контактировали с веществами сенсибилизирующего и раздражающего действия. У всех больных была выявлена повышенная чувствительность к тому или иному химическому веществу по результатам кожного тестирования (зав. отделением дерматологии д.м.н., профессор Н.И. Измерова), НСТ-теста и цитохимического исследования (зав. отделением клинической лабораторной диагностики д.м.н., профессор Л.А. Иванова): цементу и бетону - у 21 человека, органическим растворителям - у 27, соединениям хрома – у 89, солям никеля - у 78, соединениям кобальта - у 71, синтетическим смолам, клеям, краскам - у 47, антибиотикам и фармацевтическим средствам - у 19, минеральным удобрениям и ядохимикатам - у 3. Большая часть больных были заняты в строительстве, производстве строительных материалов или работали на домостроительных комбинатах - 86 человек (42,8%) и имели профессии отделочницы, плиточника, штукатура, маляра, слесаря, формовщика, монтажника, машиниста и др.
Основная масса обследованных больных (77% женщин и 23% мужчин) представлена средней и старшей возрастными группами.
Все обследованные лица (201 чел.) в зависимости от формы профессионального аллергического заболевания кожи были разделены на три группы.
Первую группу обследованных составили 139 больных профессиональной экземой. Во вторую группу (42 чел.) вошли больные профессиональным аллергическим дерматитом. В третью группу (20 чел.) вошли больные профаллергодерматозами (экзема и аллергический дерматит) в сочетании с профессиональной бронхиальной астмой.
Биохимические и молекулярно-генетические исследования.
Подсемейство цитохрома 1A принимает участие, главным образом, в активации химических веществ до канцерогенных, мутагенных и токсических эффектов. По современным представлениям, химические вещества, воздействующие на организм, в результате матаболической активации образуют продукты, способные взаимодействовать с биологическими макромолекулами и образовывать с ними комплексы - неоантигены, вызывая таким образом иммунотоксические реакции. Установлено, что 3-25 % токсических эффектов составляют анафилактические, астматические, аллергические реакции, которые способствуют формированию бронхиальной астмы, дерматитов, гепатитов, нефритов и др.
При анализе результатов распределения частоты полиморфного варианта гена CYP 1A1*2C наиболее выраженные изменения были получены в группе больных сочетанной патологией, что свидетельствует о более высокой скорости образования токсичных метаболитов у этих лиц.
Анализ особенностей клинического течения профаллергодерматозов в зависимости от генотипа CYP 1A1, выявил у 73,3% (χ2=4,08; р>0,05) лиц с наличием гетерозиготного генотипа (А/G) CYP 1A1*2C формирование заболевания при небольшом (до 5 лет) стаже работы в условиях воздействия вредных производственных факторов, у лиц с нормальной аллелью CYP 1A1 (А/А) – 52,0% (Рис.1).
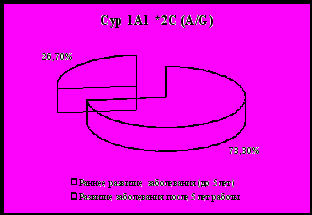

χ2=4,08; р>0,05
Рис. 1. Частота раннего развития заболевания в зависимости от генотипа Cyp 1A1
Микросомальная эпоксидгидролаза (EPXH) обеспечивает метаболизм и детоксикацию высокоактивных производных эпоксида, которые накапливаются в результате работы предшествующих ферментов. В настоящее время известно, что EPXH может находиться в двух функционально различных состояниях - «медленном» и «быстром», обусловленных мутациями в экзонах 3 и 4, соответственно. Существование фермента, как с низкой, так и с высокой активностью приводят к накоплению промежуточных токсичных метаболитов, которые приводят к усилению токсического действия химических веществ. Кроме этого промежуточные метаболиты могут связываться с нуклеиновыми кислотами, поражая при этом геном и запуская процессы мутагенеза и канцерогенеза.
При исследовании «быстрого» аллеля А-415G среди больных профессиональными аллергодерматозами было обнаружено достоверное превышение частоты встречаемости гетерозиготного генотипа (А/G) гена EPXH А-415G у 31,8% лиц (χ2 = 7,5, р <0,01) в сравнении с группой популяционного контроля 19,5%, т.е эти лица имели увеличение активности эпоксидгидролазы на 25%.
При исследовании «медленного» аллеля Т-337С, характеризующегося снижением ферментативной активности эпоксидгидролазы до 50% статистически достоверных различий по сравнению с популяционным контролем выявлено не было, однако у 57,8% лиц с гетерозиготным вариантом гена и у 53,3% лиц с гомозиготным вариантом наблюдалось более ранее развитие заболевания - до 5 лет работы с вредными производственными факторами.
Система глутатионтрансфераз является важной антиоксидантной системой, которая препятствует образованию и накоплению в организме активных форм кислорода. Глутатионопосредованная детоксикация играет ключевую роль в обеспечении резистентности клеток к перекисному окислению липидов, свободным радикалам, алкилированию белков и в предотвращении повреждений ДНК. Полиморфизм GSTM1 и GSTT1 обусловлен наличием двух аллелей: функционально активного и неактивного или нулевого.
При анализе результатов распределения частоты гомозигот по дефицитному варианту генов GSTM1 и GSTТ1, у обследованных больных в сравнении с популяционным контролем достоверных различий выявлено не было. Это связано с высокой встречаемостью данных полиморфизмов в популяции - до 46,8% для GSTM1 и до 20% для GSTТ1.
Индивидуальный анализ больных с отсутствием фермента GSTM1 выявил достоверное превышение частоты встречаемости лиц, у которых заболевание началось до 5 лет от начала работы с вредными производственными факторами во всех обследованных группах в сравнении с лицами, имеющими нормальную активность фермента (рис.2).
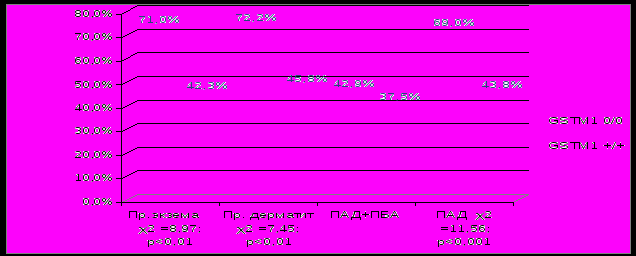
Рис. 2. Доля лиц с ранним развитием заболевания (при стаже работы до 5 лет) в зависимости от генотипа GSTM1в обследованных группах (ПАД – профаллергодерматозы, ПБА – профессиональная бронхиальная астма)
При одновременном наличии делеции по генам GSTM1 и GSTТ1 раннее развитие наблюдалось у 69,2% лиц с профессиональными заболеваниями кожи, при отсутствии делеции по обоим генам раннее развитие наблюдалось у 39,5% обследованных (рис. 3).
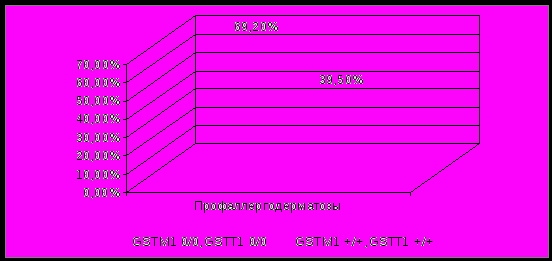
Рис.3. Доля лиц с ранним развитием заболевания (при стаже работы до 5 лет) в зависимости от генотипов GSTM1 и GSTТ1 у больных профаллергодерматозами
При воздействии комплекса неблагоприятных факторов производственной среды и трудового процесса происходит мобилизация не только системы биотрансформации ксенобиотиков, направленной на поддержание основных жизненных функций и повышение резистентности к раздражителю, но и к интенсификации свободнорадикальных процессов.
При исследовании процессов перекисного окисления липидов у всех обследованных больных выявлена гиперактивация процессов свободнорадикального окисления, характеризующаяся достоверным повышением уровня продуктов ПОЛ по сравнению с группой контроля (табл.1).
Таблица 1
Уровень продуктов перекисного окисления липидов у обследованных больных
| Группа | n | Биохимический показатель | ||
| ДК,мкмоль/л | КД, мкмоль/л | КБ, мкмоль/л | ||
| I Профессиональная экзема | 61 | 17,2±0,8*** | 3,61±0,14*** | 173,0±2,4*** |
| II Профессиональный аллергический дерматит | 22 | 18,6±1,6*** | 2,44±0,28 | 177,5±4,6*** |
| III Профаллергодерматозы и профессиональная бронхиальная астма | 20 | 14,6±1,4*** | 2,26±0,17 | 168,0±4,6*** |
| IV Контроль | 40 | 6,4±0,4 | 2,09±0,1 | 146,5±3,4 |
Примечание. Достоверность различий с контрольной группой *** р<0,001
Для выявления особенностей изменения состояния процессов перекисного окисления липидов у больных профаллергодерматозами в зависимости от воздействующего фактора все обследованные были разделены на две группы:
1-ая группа - больные профаллергодерматозами от воздействия металлов-аллергенов (Cr, Ni, Co) - 43 человека.
2-ая группа - больные профаллергодерматозами от воздействия веществ раздражающего действия (растворители, краски и др.) - 40 человек.
При проведении анализа уровня катаболитов перекисного окисления липидов в зависимости от воздействующего фактора было выявлено, что в группе аллергодерматозов от воздействия металлов-аллергенов (Cr, Ni, Co) достоверно (р<0,05) выше уровни диеновых конъюгатов, кетодиенов и карбонилов достоверно (р<0,05) выше по сравнению с группой аллергодерматозов от воздействия веществ раздражающего действия (растворители, краски и др.) (табл.2). Полученные данные согласуются с выраженностью клинического течения заболевания у лиц подвергающихся воздействию преимущественно металлов-аллергенов.
Таблица 2
Уровень продуктов ПОЛ у обследованных больных профессиональными аллергодерматозами в зависимости от воздействующего фактора
| Воздействующий фактор | n | Биохимический показатель | ||
| ДК, мкмоль/л | КД, мкмоль/л | КБ, мкмоль/л | ||
| Аллергодерматозы от воздействия металлов-аллергенов (Cr, Ni, Co) | 43 | 18,3±0,9* | 2,83±0,14* | 178,6±3,0* |
| Аллергодерматозы от воздействия веществ раздражающего действия (растворители, краски и др.) | 40 | 15,4±0,9 | 2,36±0,18 | 169,4±2,4 |
Примечание. Достоверность различий с группой аллергодерматозов от воздействия веществ раздражающего действия: * р<0,05
Ключевой системой, непосредственно вступающей в реакции окислительно-восстановительного обмена, является тиол-дисульфидная окилительно-восстановительная система, включающая такие антиоксиданты как супероксиддисмутаза, каталаза, глутатионредуктаза, глюкозо-6-фосфатдегидрогеназа. Показано, что тиол-дисульфидная система принимает участие в механизмах неспецифической резистентности, в том числе при развитии воспалительных процессов. Наличие изменений со стороны данного компонента антиоксидантной системы (АОС) может служить критерием активности воспалительных процессов в организме. Динамика изменений компонентов тиол-дисульфидной окилительно-восстановительной системы позволяет также оценить эффективность проводимых лечебно-профилактических мероприятий.
При исследовании состояния системы антиоксидантной защиты в группах больных с профессиональной экземой и профессиональным дерматитом было выявлено снижение уровня антиоксидантной защиты, которое выражалось в снижении уровня SH-групп и снижении тиол-дисульфидного соотношения (SH/SS). В группе больных с сочетанной патологией достоверных различий выявлено не было, что является, по-видимому, следствием активно проводимой терапии больным с профессиональной бронхиальной астмой (табл. 3).
Таблица 3
Уровень продуктов перекисного окисления липидов у обследованных больных профессиональными аллергодерматозами в зависимости от воздействующего фактора
| Группа | n | Биохимический показатель | |||
| SH, мкмоль/л | SS, мкмоль/л | SH/SS | GSTР, нг/мл | ||
| I Профессиональная экзема | 61 | 106,9±4,0** | 82,6±4,8 | 1,41±0,06** | 119,9±12,5 |
| II Профессиональный аллергический дерматит | 22 | 104,1±9,9* | 79,3±9,2 | 1,39±0,11** | 108,6±10,5 |
| III Профаллергодерматозы и профессиональная бронхиальная астма | 20 | 112,5±5,1 | 87,5±9,2 | 1,49±0,12 | 101,4±17,4 |
| IV Контроль | 40 | 122,4±2,9 | 79,1±1,8 | 1,60±0,02 | 107,4±7,2 |
Примечание. Достоверность различий с контрольной группой ** р<0,01, * р<0,05
Исследование количественного уровня глутатион-S-трансферазы Р не показало достоверных различий с группой контроля, однако у 30% обследованных лиц наблюдался сниженный уровень глутатион - S-трансферазы Р.
Глутатион-S-трансфераза Р является ферментом антиоксидантной защиты, поэтому представляло интерес проанализировать показатели уровня продуктов перекисного окисления липидов в зависимости от количественного содержания глутатион-S-трансферазы Р в сыворотке больных.
Проведенные исследования выявили обратную корреляцию между количественным содержанием GSTР1 и содержанием диеновых конъюгатов и кетодиенов в сыворотке больных (r = -0,35 и r = -0,33, p<0,05 соответственно), что свидетельствует о выраженных изменениях в системах перекисного окисления липидов и антиоксидантной защиты (Рис.4).
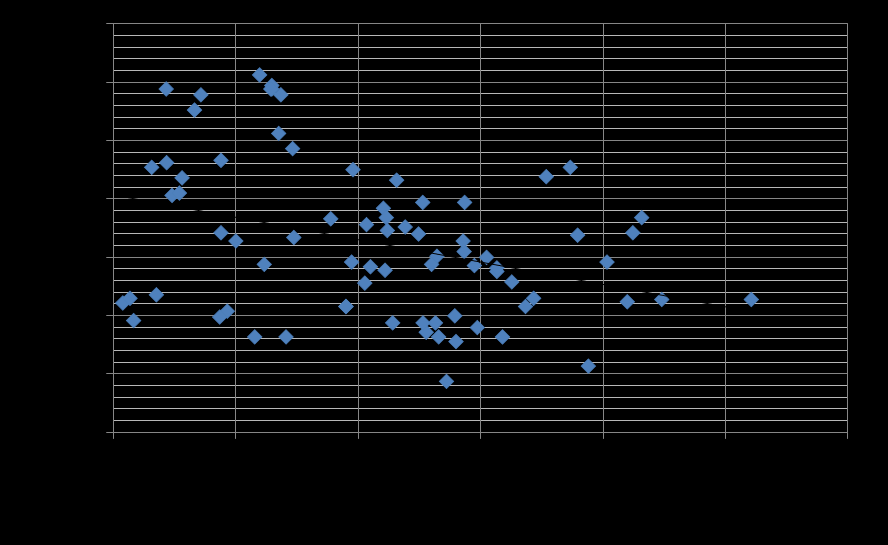

r = -0,35, p<0,05 r = -0,33, p<0,05
Рис. 4. Анализ зависимости между количественным содержанием GSTP1 в сыворотке и показателями ПОЛ
Учитывая выявленные изменения в системе оксиданты-антиоксиданты, представляло интерес исследовать количественное содержание внеклеточной ДНК и нуклеазной активности для оценки степени выраженности процессов повреждения клеточной мембраны.
Исследование уровня внеклеточной ДНК и нуклеазной активности не показало статистически достоверных различий в сравнении с группой контроля, однако при индивидуальном анализе данных показателей у обследованных лиц с наличием делеции в генах глутатион-S-трансферазы М и Т (с отсутствием ферментов глутатион-S-трансферазы М и Т) было выявлено достоверное увеличение уровня диеновых конъюгатов, внеклеточной ДНК и повышение ферментативной активности нуклеаз (рис. 5).

Рис. 5. Уровень внеклеточной ДНК и нуклеазной активности в зависимости от генотипа глутатион-S-трансферазы М и Т
Сложное взаимодействие функций отдельных генов обеспечивает стабильность и адаптивность функционирования генотипа в целом в различных условиях среды. В результате отдельных генных мутаций, которые могут определять индивидуальные особенности метаболических систем организма, включая различные белковые и другие молекулярные структуры, системные проявления гомеостаза нарушаются и изменяется способность организма выдерживать повреждающее воздействие факторов окружающей среды различной природы - производственных, экологических, инфекционных.
Нами была предпринята попытка оценить состояние больных и проанализировать сроки развития заболевания в зависимости от сочетания 3-х и более выявленных полиморфизмов по изученным генам (табл. 4).
Таблица 4
Зависимость показателей системы оксиданты-антиоксиданты и уровня внеклеточной ДНК от генов системы биотрансформации ксенобиотиков
| № | Cyp1A1 | Cyp3A4 | GSTM1 | GSTT1 | EPHX1 (быстр) | EPHX1 (медлен) | GSTP1 | Вн. ДНК | Нукл. Акт. | ДК | Диагноз | Время начала |
| 1 | + | - | + | - | + | + | N | ↑↑ | N | ↑↑ | Распр. дерматит | Через 2 года |
| 2 | - | - | + | + | + | - | ↓ | N | N | ↑↑↑ | Экзема верхн. кон. | Через 1 год |
| 3 | - | - | + | - | + | + | N | N | N | ↑↑ | Экзема верхн. кон. | Через 2 года |
| 4 | - | + | + | + | - | + | ↓ | ↑↑ | ↑↑ | ↑↑↑ | Дерматит верхн. кон. | Через 2 года |
| 5 | - | + | + | + | - | - | N | N | ↑↑ | ↑↑ | Дерматит верхн. кон. | Сразу |
| 6 | - | - | + | + | - | + | ↓ | ↑↑↑ | ↓ | ↑↑↑ | Дерматит верхн. кон. | Через 4 года |
Все больные с сочетанием нескольких редких форм полиморфных генов заболевали в течение первых пяти лет после начала работы во вредных условиях. Обращает на себя внимание и тот факт, что эти же больные имели более высокие уровни диеновых конъюгатов, повышенный уровень внеклеточной ДНК и высокую активность нуклеаз в сочетании с низким содержанием GSTР1, что свидетельствует о роли изученных систем в патогенезе профессиональных аллергических дерматозов.
Таким образом, на основании проведенных исследований и полученых результатов показана взаимосвязь компонентов изученных систем и их роль в механизмах развития и формирования профессиональных аллергических дерматозов от воздействия веществ раздражающего и сенсибилизирующего действия (рис.6).
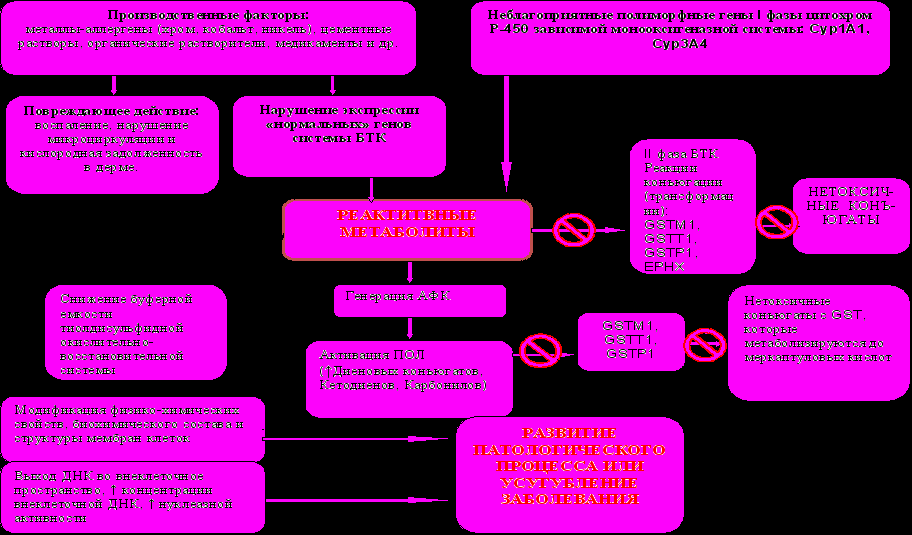
Рис.6. Взаимосвязь компонентов изученных систем и их роль в механизмах развития и формирования профессиональных аллергических дерматозов от воздействия веществ раздражающего и сенсибилизирующего действия
ВЫВОДЫ:
- У больных профаллергодерматозами выявлены полиморфные гены системы биотрансформации ксенобиотиков: CYP 1A1*2С, CYP3A4*1В, ЕРНХ1 Т-337С и ЕРНХ1 А-415G; делеции генов GSTM1 и GSTT1; нарушения в системе оксиданты-антиоксиданты и накопление внеклеточной ДНК с повышением активности нуклеаз, что свидетельствует о роли изученных систем в патогенезе профессиональных аллергических дерматозов.
- Механизм реализации наличия определенных генетико-биохимических вариантов ферментов цитохром Р-450 зависимой монооксигеназной системы включает индивидуальные особенности показателей системы оксиданты-антиоксиданты, о чем свидетельствует выявленная зависимость между некоторыми биохимическими показателями и конкретной генотипической принадлежностью. Обнаружены достоверные ассоциации: генотипов CYP 1A1*2С, GSTM1 0/0 и GSTT1 0/0, ЕРНХ1 Т-337С (С/Т), а также сочетания 2-х и более из указанных генов с повышенным уровнем диеновых конъюгатов; ЕРНХ1 Т-337С (Т/Т) и низкого уровня GSTР1.
- У больных профессиональными аллергодерматозами с делецией GSTM1 и GSTT1 (отсутствием ферментов) выявлено достоверное увеличение уровня продуктов перекисного окисления липидов, что приводит к накоплению внеклеточной ДНК и повышению ферментативной активности нуклеаз и свидетельствует о высокой степени повреждения мембран клеток.
- Выявлена обратная корреляция между количественным содержанием GSTР1 и содержанием диеновых конъюгатов и кетодиенов (r = -0,35 и r = -0,33, p<0,05 соответственно), что свидетельствует о выраженных изменениях в системах перекисного окисления липидов и антиоксидантной защиты у больных профессиональными заболеваниями кожи.
- Сочетание неблагоприятных гетеро- и гомозиготных аллелей генов CYP 1A1, CYP3A4, ЕРНХ1 и делеций генов GSTM1 и GSTT1, низкий количественный уровень GSTР1 характеризуется ранним (при стаже работы во вредных условиях до 5 лет) развитием и неблагоприятным прогнозом профессиональной патологии кожи.
- На основе проведенных исследований разработан комплекс молекулярно-генетических и биохимических показателей системы биотрансформации ксенобиотиков, включающий определение полиморфных вариантов генов CYP 1A1, CYP3A4, ЕРНХ1, делеций генов GSTM1 и GSTT1, количественного уровня GSTР1 компонентов системы оксиданты-антиоксиданты и процессов повреждения ДНК в зависимости от ферментативной активности нуклеаз для оценки риска развития и прогноза течения профессиональных аллергических дерматозов от воздействия веществ раздражающего и сенсибилизирующего действия.
СПИСОК ОПУБЛИКОВАННЫХ НАУЧНЫХ РАБОТ ПО ТЕМЕ ДИССЕРТАЦИИ
- Кузьмина Л.П., Безрукавникова Л.М., Софронова Е.В., Лазарашвили Н.А., Коляскина М.М. «Неиммунные механизмы в развитии и течении профессиональных аллергических заболеваний» Актуальные проблемы медицины труда. Сборник трудов института / под ред. Н.Ф. Измерова. - М.: ООО Фирма «Реинфор», 2009. - С.91 - 106.
- Кузьмина Л.П., Измерова Н.И., Лазарашвили Н.А., Безрукавникова Л.М., ЧикинВ.В., КоляскинаМ.М., ФоминаВ.С. Роль системы «оксиданты-антиоксиданты» и процессов повреждения ДНК в патогенезе профессиональных аллергических дерматозов.//Актуальные проблемы медицины труда. Сборник трудов института / под ред. Н.Ф.Измерова. - М.: ООО Фирма «Реинфор», 2009. - С.107 - 117.
- Кузьмина Л.П., Измерова Н.И., Коляскина М.М. Изучение функциональной активности и генотипов различных семейств цитохромов у больных профессиональными заболеваниями аллергенной природы. // Материалы VIII Всероссийского конгресса «Профессия и здоровье». Москва, 25 - 27 ноября 2009 г. - М.: Издательство «Дельта», - С.268 - 270.
- Кузьмина Л.П., Измерова Н.И., Пилат Т.Л., Лазарашвили Н.А., Безрукавникова Л.М., Софронова Е.В., Коляскина М.М., Чикин В.В., Ларкин А.В., Петинати Я.А., Фомина В.С. «Состояние системы «оксиданты-антиоксиданты» у больных профессиональными аллергическими дерматозами» (диагностика, риск развития, прогноз, профилактика). Методическое пособие для врачей. (Утверждено Научным советом по Медико-экологическим проблемам здоровья работающих, Москва 2009г.).
- Кузьмина Л.П., Измерова Н.И., Лазарашвили Н.А., Безрукавникова Л.М., Софронова Е.В., Коляскина М.М., Фомина В.С. «Проблема индивидуальной чувствительности в медицине труда». Методическое пособие для врачей. (Утверждено Научным советом по Медико-экологическим проблемам здоровья работающих, Москва 2009г.).
- Кузьмина Л.П., Коляскина М.М., Измерова Н.И., Лазарашвили Н.А., Безрукавникова Л.М. «Биохимические и молекулярно-генетические маркеры предрасположенности к развитию профаллергодерматозов». Методическое пособие для врачей. (Утверждено Научным советом по Медико-экологическим проблемам здоровья работающих, Москва 2011г.).
- Кузьмина Л.П., Лазарашвили Н.А., Коляскина М.М. и др. «N272H-полиморфизм гена СРОХ и некоторые клинико-биохимические показатели у лиц, подвергшихся воздействию ртути» Ж. «Медицинская генетика» - 2009 – Т. 8, № 5 – с.24-28.
- Кузьмина Л.П., Безрукавникова Л.М., Коляскина М.М. «Показатели тиолдисульфидного звена антиоксидантной системы, как критерии риска развития аллергических заболеваний кожи» Материалы Всероссийской научно-практической конференции «Производственно-обусловленные нарушения здоровья работников в современных условиях». Шахты, 2010. – Издательство Росиздат 2010. – с. 74-75.
- Коляскина М.М. Изучение роли тиолдисульфидного звена антиоксидантной системы и генетического биохимического полиморфизма глутатион-S-трансферазы в патогенезе профессиональных аллергических дерматозов. Современные технологии обеспечения биологической безопасности: Материалы научно-практической конференции молодых ученых и специалистов научно-исследовательских организаций Роспотребнадзора (25-27 мая 2010г.) под ред. Академика РАМН Г.Г. Онищенко.- Протвино: А-ПРИНТ ЗАО, 2010.- 418с, стр. 57-60.
- Коляскина М.М., Кузьмина Л.П., Шипулин Г.А., Миронов К. О, Дедков В.Г., Дунаева Е.А. «Разработка метода определения полиморфизмов гена цитохрома р-450 1а1 у больных профессиональными аллергодерматозами с применением реакции пиросеквенирования» Материалы VII Всероссийской научно-практической конференции с международным участием «Молекулярная диагностика - 2010» - Москва, 24-26 ноября 2010 г., Т.4.-с.264-266.
- Кузьмина Л.П., Измерова Н.И., Лазарашвили Н.А., Коляскина М.М. «Полиморфизм глутатионтрансферазы (GSTM1) у больных профессиональными аллергическими дерматозами» Материалы пленума по теме «Научно-методические и законодательные основы обеспечения генетической безопасности факторов и объектов окружающей и производственной среды в целях сохранения здоровья человека» (15-16 декабря 2010г.) под редакцией академиков РАМН Ю.А. Рахманина и Н.Ф. Измерова, Москва 2010г.-с. 96-97.
- Коляскина М.М. «Полиморфизм гена цитохрома Р-450 1А1 у больных профессиональными аллергодерматозами» Материалы пленума по теме «Научно-методические и законодательные основы обеспечения генетической безопасности факторов и объектов окружающей и производственной среды в целях сохранения здоровья человека» (15-16 декабря 2010г.) под редакцией академиков РАМН Ю.А. Рахманина и Н.Ф. Измерова, Москва 2010г.-с. 90-91.
- Кузьмина Л.П., Измерова Н.И., Спицын В.А., Лазарашвили Н.А., Коляскина М.М., Безрукавникова Л.М. «Роль эндотелиальной синтазы окиси азота в патогенезе некоторых профессиональных заболеваний» Материалы пленума по теме «Научно-методические и законодательные основы обеспечения генетической безопасности факторов и объектов окружающей и производственной среды в целях сохранения здоровья человека» (15-16 декабря 2010г.) под редакцией академиков РАМН Ю.А. Рахманина и Н.Ф. Измерова, Москва 2010г.-с. 97-98.
- Коляскина М.М., Лазарашвили Н.А., Безрукавникова Л.М. «Исследование системы антиоксидантной защиты у больных профессиональными аллергическими заболеваниями кожи» Материалы IX Всероссийского конгресса «Профессия и Здоровье» и IV Всероссийского съезда врачей-профпатологов (24-26 ноября 2010 г.). – М.-с. 266-267.
- Коляскина М.М, Кузьмина Л.П. «Использование метода определения полиморфизмов гена цитохрома Р-4501А1 с применением реакции пиросеквенирования у больных профессиональными аллергодерматозами» Материалы IX Всероссийского конгресса «Профессия и Здоровье» и IV Всероссийского съезда врачей-профпатологов (24-26 ноября 2010 г.).– М.-с.264-265.
- Кузьмина Л.П., Измерова Н.И., Коляскина М.М. «Роль полиморфных генов системы биотрансформации ксенобиотиков в патогенезе профессиональных аллергодерматозов», статья в Ж. «Медицина труда и промышленная экология» - 2011 – № 7 – с.17-23.
- Измеров Н.Ф., Кузьмина Л.П., Коляскина М.М., Лазарашвили Н.А. «Молекулярно-генетические исследования в медицине труда», статья в Ж. «Гигиена и санитария» - 2011 – № 5 – с.11-15.
