Научные основы прогноза токсичности и опасности химических веществ с учетом механизма токсического действия. 14. 02. 01 Гигиена
| Вид материала | Автореферат |
- Отравление аварийными химически опасными веществами, 33.95kb.
- Токсикомания шаг в сторону наркомании, 29.31kb.
- Показатели безопасности изделий регламентируются с учетом функционального назначения,, 184.97kb.
- Вопрос Параметры звука, 183.33kb.
- Волощенко О. И., Медяник, 2522.04kb.
- Программа спецкурса «методы расчета физико-химических свойств веществ» для студентов, 40.47kb.
- Т е м ылекций по гигиене для студентов IV курса медицинского факультета по специальностям, 21.78kb.
- Технология переработки отходов производств, использующих высокочистый кремний 05. 17., 277.13kb.
- О государственной регистрации потенциально опасных химических и биологических веществ, 360.85kb.
- «О пользе молока», 74.05kb.
По данным биохимических и теоретических исследований (Loеw G.H., 1983, 1985) можно предположить, что ключевые реакции биотрансформации для насыщенных и ненасыщенных алифатических ГСС различаются. Для предварительного прогноза на смешанной обучающей выборке соединений этих структурных рядов был проведен компьютерный эксперимент по прогнозу хронической токсичности. Массив содержал 47 соединений, для которых в базе данных WATERTOX приведены показатели хронической токсичности.
В результате компьютерного эксперимента с использованием этой выборки удалось сделать прогноз класса опасности по хронической токсичности для 8 соединений. По результатам ДСМ-прогноза 1,2–дибромэтан и 1,2-дихлорпропан, отнесены к группе высоко опасных веществ. Норматив 1,2-дихлорпропана был недавно пересмотрен с учетом зарубежных данных. Новый норматив, в отличие от старого, соответствует отнесению соединения к группе высоко опасных веществ по хронической токсичности. Для 1,2–дибромэтана утверждено значение ориентировочной допустимой дозы, соответствующее группе высокотоксичных веществ. 1,1-Дихлор-4-метилпентадиен, вещество, изученное в эксперименте, первоначально не был включен в обучающую выборку. Для этого соединения предсказан второй класс опасности по хронической токсичности. Экспериментальное значение МНД 0,26 мг/кг, что соответствует второму классу опасности. Для 1,1,2,2,3 пентахлорпропана предсказан третий класс опасности. Определенная экспериментально пороговая доза хронического эксперимента составляет 5 мг/кг, максимальная недействующая доза обычно в 5-10 раз меньше, что соответствует третьему классу опасности по принятой в данной работе классификации. По результатам прогноза 1,2,3–трихлорпропан отнесен к первому классу опасности, тогда как экспериментальное значение МНД (0,3 мг/кг) соответствует второму классу. 1,2,3–Трихлорпропан является установленным канцерогеном для многих видов животных, вероятным канцерогеном для человека (по классификации МАИР), проявляет нефротоксичность. Очевидно, его норматив должен быть пересмотрен с учетом канцерогенного эффекта.
Качественный анализ данных по острой токсичности различных спиртов для крыс и мышей позволяет выделить некоторые структурные фрагменты, наличие которых в молекуле приводит к усилению токсичности (например, двойные и тройные связи). Кроме того, насыщенные спирты с очень малым или очень большим числом атомов углерода менее токсичны, тогда как спирты с числом атомов углерода от 4 до 10 более токсичны. Такие факторы трудно характеризовать в численной форме, и они не могут быть учтены при рассмотрении с использованием регрессионного анализа. Задача может быть решена с использованием экспертных систем. На примере острой токсичности результаты ДСМ прогноза сопоставлены с результатами прогноза с использованием экспертной системы, построенной на правилах, предварительно сформулированных экспертами (продукционной системы). При сравнении работы самообучающейся ДСМ-системы и продукционной системы, оказалось, что ДСМ-система породила гипотезы, которые полностью совпали с продукциями (правилами), изначально заданными в продукционной системе.
Таблица 8. Гипотезы (структурные фрагменты), определяющие хроническую токсичность спиртов.
Гипотезы, определяющие среднюю и высокую хроническую токсичность спиртов | Гипотезы, определяющие среднюю и высокую хроническую токсичность спиртов |
 |  |
 |  |
 |  |
 |  |
| Структурный фрагмент, препятствующий проявлению высокой и средней хронической токсичности спиртов. | |
 |
Эффективность работы ДСМ системы практически та же, что и продукционной системы.
Анализ соотношения структура-хроническая токсичность спиртов методом регрессионного анализа выявил наличие большого числа соединений – “outliners”, не укладывающихся в зависимость. В связи с этим был проведен компьютерный ДСМ эксперимент на массиве данных по хронической токсичности для 38 спиртов. По его результатам, приведенным в таблице 8, присутствие в молекуле третичной бутильной группы, фторзамещеных алкильных групп, двойной связи определяет принадлежность соединения к группам высоко- или среднетоксичных соединений, тогда как наличие диметилэтаноламинной группы связано с низкой хронической токсичностью.
Для оценки возможности прогноза отдаленных эффектов с использованием ДСМ-системы проведен компьютерный ДСМ эксперимент по прогнозу канцерогенной активности полициклических ароматических углеводородов (ПАУ) на обучающей выборке из 25 ПАУ. Структура соединений описывалась кодами ФКСП, причем изменение структуры в ходе биотрансформации никак не учитывалось. Канцерогенная активность ПАУ характеризовалась по Бэджеру, в классификации которого по результатам экспериментов на млекопитающих соединения относятся к одной из 5 групп – неактивные (-), слабо активные (+), умеренно активные (++), сильно активные (+++) и чрезвычайно активные (++++).
В соответствии с предположениями, без учета биотрансформации как полнота, так и точность прогноза были недостаточны. Так, сильный канцероген бенз(а)пирен (исключенный из обучающей выборки и рассмотренный как тестовый пример) был отнесен к слабо или не канцерогенным соединениям, а не канцерогенный пентацен – к канцерогенам.
Таким образом, по результатам компьютерных экспериментов по прогнозу хронической токсичности методом ДСМ в большинстве случаев удалось сделать правильный ретроспективный прогноз классов опасности по хронической токсичности и дать прогноз для не изученных соединений. Однако прогноз для многих соединений оказался невозможным или неполным, в некоторых случаях, как при прогнозе канцерогенности – неверным, что потребовало проведения дальнейших исследований.
Возможно, причина заключается в том, что метод не учитывает возможность биоактивации в процессе биотрансформации.
Прогноз кaнцерогенности химических веществ с использованием логико-комбинаторного ДСМ метода и анализа числовых параметров
Был разработан комплексный подход, в котором параметры, характеризующие биоактивацию, были включены в ДСМ «рассуждения». Квантово-химические параметры, как и другие дескрипторы соотношений структура-активность, являются числами. До настоящего времени логико-комбинаторный ДСМ метод не применялся к числовым объектам. Для включения числовых параметров в ДСМ систему была разработана специальная алгебра интервалов. Соединение представляли в виде гибридного объекта, состоящего из числового параметра (параметров) и описания химической структуры метаболитов либо исходных соединений с помощью дескрипторов языка ФКСП или с помощью графов.
В данном разделе работы предлагаемый комбинированный подход применен для прогноза наличия и степени выраженности канцерогенного эффекта. Канцерогенез веществ многих структурных рядов определяется их биоактивацией в организме. Это было отмечено еще в ранних работах по изучению канцерогенной активности (Miller E.C., 1966, 1981). Так, канцерогенность является основным токсическим эффектом соединений ряда ПАУ. Канцерогенная и мутагенная активность различных ПАУ варьируется в очень широких пределах в зависимости от структуры углеводорода. В результате экспериментальных исследований была выявлена определяющая роль метаболической активации в канцерогенной активности ПАУ (Guengerich F.P., Shimada T., 1991). Прогноз канцерогенности ПАУ в нашей работе основан на гипотезе Джерины и Лера (Jerina P.M., Lier R.E., 1977) о том, что наиболее опасными метаболитами являются диолэпоксиды, способные образовывать аддукты с ДНК, атакуя критические нуклеофильные позиции ДНК по механизму нуклеофильного замещения первого порядка (SN1) c образованием в качестве интермедиатов триолкарбокатионов. Механизм биоактивации по пути образования диолэпоксидов признан до сих пор одним из ведущих механизмов канцерогенеза под действием ПАУ (IARC Monographs, 2010). Гипотеза состояла в том, что ключевой реакцией, лимитирующей скорость процесса биоактивации, является образование триолкарбокатионов из диолэпоксидов. В результате расчетов прогнозировали ключевую реакцию биотрансформации для данного соединения – определяли триолкарбокатион, образование которого энергетически наиболее выгодно. Из всех карбокатионов, которые могут образоваться в результате биотрансформации ПАУ, наиболее легко образуется катион, для которого разность энергии карбокатиона и диолэпоксида Екатион наименьшая.
Значение параметра Екатион, характеризующее ключевую реакцию биотрансформации для этого карбокатиона и использовалось при прогнозе.
Для определения ключевой реакции биотрансформации была составлена программа расчета параметров Екатион – разности энергий всех возможных диолэпоксидов и триолкарбокатионов методом Хюккеля (рис. 5).
По программе определяется как значение параметра, так и структура наиболее устойчивого карбокатиона, т.е. метаболита, соответствующего ключевой реакции биотрансформации.
В ходе апробации метода проведен ДСМ-эксперимент на структурах метаболитов ПАУ. Для 41 незамещенного ПАУ с использованием квантово-химического модуля генерации метаболитов были определены наиболее активные конечные метаболиты - карбокатионы. На массиве метаболитов – диолэпоксидов, предшественников этих наиболее устойчивых карбокатионов был проведен компьютерный ДСМ-эксперимент.
Метаболитам соединений был приписан экспериментально определенный уровень канцерогенной активности исходных ПАУ по Бэджеру. С использованием полученных гипотез канцерогенная активность неактивного пентацена была предсказана правильно, канцерогенная активность бенз(а)пирена была определена не полностью – он был отнесен к высоко или умеренно активным соединениям, неактивный бензо(а)нафто(2,1,8-hij)нафтацен был отнесен к умеренно активным или неактивным соединениям.
В целом прогноз согласуется с экспериментальными данными, однако недостаточная точность прогноза приводит к необходимости явного учета энергетических параметров. Согласно принятой модели, в ряду ПАУ с ростом устойчивости карбокатиона возрастает канцерогенная активность.
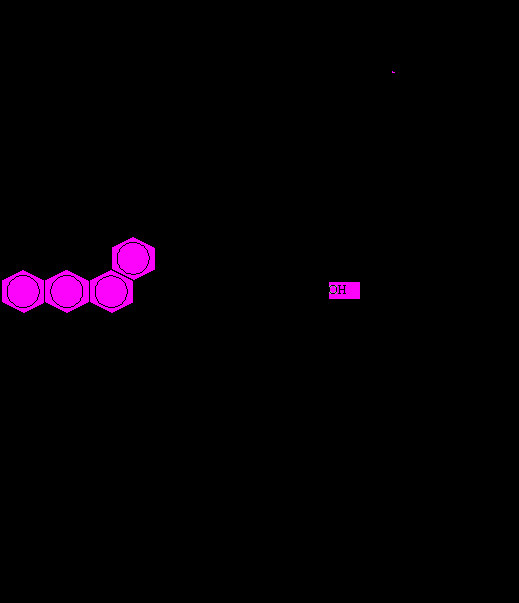
Рисунок 5. Алгоритм установления наиболее устойчивого метаболита бенз(а)антрацена (обведен кружком).
Однако помимо биоактивации с образованием диолэпоксидов, в организме могут идти и другие процессы биотрансформации: образование гидроксилированных продуктов, при окислении так называемых L-областей образуются хиноны. Согласно экспериментальным исследованиям, эти процессы биотрансформации могут привести к снижению канцерогенной активности. Возможна также биоактивация через образование катион-радикалов в результате одноэлектронного окисления (Сavalieri E.L. et al., 1995, 2005), через метилирование с последующим образованием сложных эфиров, которые связываются с ДНК также через стадию образования карбокатионов (Lehner A.F. et al., 1996), через образование орто-хинонов (ссылка скрыта., 1999, Сavalieri E.L. et al., 2002). Анализ зависимости канцерогенной активности от энергии образования конечного метаболита на пути биоактивации по модели Джерины и Лера свидетельствует, что одной этой численной характеристики недостаточно для надежного прогноза. В частности, плохо прогнозируется канцерогенная активность соединений, структура которых содержит несколько L-областей.
Высказана гипотеза, что описанный выше комплексный подход позволит улучшить результаты прогноза. ДСМ-анализ проводили на гибридных объектах, состоящих из числового параметра Екатион и описания структуры конечного метаболита – триолкарбокатиона либо исходного ПАУ с помощью дескрипторов кода ФКСП. В продолжение этих исследований были проведены компьютерные эксперименты с использованием варианта ДСМ системы с альтернативным описанием структуры химического соединения с помощью графов. Структуры ПАУ описывали с помощью k-циклических проекций (для множества молекулярных графов было построено множество подграфов, состоящих из k связанных циклов из объединения минимальных циклических базисов хотя бы одного из исходных графов). Как и в эксперименте с описанием структуры языком ФКСП, вместе со структурной частью рассматривался числовой параметр, характеризующий энергию образования наиболее активного конечного метаболита ПАУ.
При описании с помощью графов с использованием выборки из 25 ПАУ в качестве обучающей осуществлен прогноз канцерогенной активности 18-ти соединений, активность которых была известна (ретроспективный прогноз). Прогнозировалось отнесение соединения к одной из трех групп по канцерогенности: 1 группа – сильно канцерогенные, 2 группа –умеренно и слабо канцерогенные и 3 группа – не канцерогенные соединения.
В процессе тестирования язык описания был исправлен и дополнен. Так, была определена необходимость различать структуры, которым соответствуют графы, содержащие и не содержащие вершины, являющиеся началом новых ребер. Циклы, содержащие эти вершины, не должны быть концевыми. Такое различие определяется возможностью реакций присоединения кислорода к «свободным», находящимся в пара положении к друг другу, атомам углерода колец. Наличие двух таких «внутренних» сопряженных (с общим ребром) колец колец в одной молекуле сильно облегчает прохождение этой реакции, приводящей к ослаблению канцерогенной активности. Необходимо также различать «угловые» структурные фрагменты, содержащие и не содержащие циклы с вершинами, являющимися началом новых ребер.
Введение таких поправок в описание структур соединений позволило уменьшить до минимума число неправильных прогнозов. В результате канцерогенная активность только одного соединения была предсказана неправильно, активность одного соединения не удалось предсказать с использованием гипотез, сгенерированных на стадии анализа обучающей выборки, активность трех соединений предсказана частично (не полностью объяснена), точность прогноза 95% .
Полученные результаты позволили применить разработанную систему для прогноза канцерогенной активности 20 неизученных соединений. Обучающая выборка взята из литературных данных (Flesher J.W. et al., 1996). Как показали недавние экспериментальные исследования, одно из соединений обладает генотоксичностью в согласии с нашим прогнозом.
Проведенные эксперименты по сопоставлению с другими методами машинного обучения показали, что применение ДСМ-метода на данном массиве по точности дает лучшие результаты среди всех рассмотренных методов машинного обучения. В то же время использование проекций ведет к незначительному изменению числа правильных предсказаний по отношению к результатам, полученным с применением ФКСП-кодов. Однако подход, основанный на операторе проекции графов значительно сокращает временные затраты на анализ данных обучающей выборки и последующее применение полученных гипотез, с целью классификации, к данным тестовой выборки, в тоже время не приводя к большим информационным потерям (т.е. неправильным классификациям).
Структурный ряд ПАУ содержит несколько десятков соединений. Однако каждый из таких углеводородов является родоначальником большого числа замещенных производных. Например замещение метильной группой в бенз(а)антрацене можно осуществить в 12 различных положениях и получить таким образом более десятка только его монометил производных. Более ста соединений возникают при введении двух и более метильных групп. При замене в сопряженной системе некоторых атомов С на N и другие элементы могут возникать разнообразные гетероциклические производные. Все эти многие сотни и тысячи соединений не могут быть изучены экспериментально. Известно лишь, что среди замещенных ПАУ содержатся сильные канцерогены, встречающиеся в окружающей среде. Введение метильной группы в углеводород может сопровождаться резким усилением активности. Известно, что метаболизм ПАУ под действием цитохрома Р450 высоко стереоспецифичен (Silverman B.D., Lowe J.P., 1983). Поэтому для выборки ПАУ и метил замещенных ПАУ был проведен расчет исходных соединений, дигидродиолов и диолэпоксидов с полной оптимизацией геометрии полуэмпирическим квантово-химическим методом РМ3 и определено значение параметра Есс, представляющего собой разность теплот образования карбокатиона и диолэпоксида. Согласно модели, чем меньше значение параметра, тем более канцерогенным должно быть соединение.
По результатам квантово-химических расчетов для 75 соединений выборки ПАУ и их метилзамещенных производных существует область значений параметра (около 145,5-147,5 ккал/моль), соответствующая пограничной +/- активности. Предполагалось, что совместное использование ДСМ-анализа и квантово-химических расчетов должно дать возможность уточнить прогноз. Соединения с определенной активностью и пограничными значениями параметра (4 соединения) были исключены из обучающей выборки, для прогноза канцерогенной активности был проведен компьютерный ДСМ эксперимент с использованием числового параметра Есс.
Таблица 9. Прогноз канцерогенности метилзамещенных ПАУ с использованием комплексного метода прогноза
| Соединение | Есс* (ккал/моль) | Эксперимент | Результат ДСМ-прогноза |
| бенз(а)пирен | 0 | + | + |
| 2,4-диметилбензо(с)хризен | 3,48 | ? | + |
| 7,14-диметилбензо(а)тетрацен | 5,66 | ? | + |
| 1,2-диметилиндено(1,2,3-cd)пирен | 8,86 | ? | - |
| Флуорантен | 0,59 | - | |
| 5-OH- бензо(b) флуорантен | 2,68 | + | |
| Бензо(k) флуорантен | 10,25 | + | |
| Бензо(j) флуорантен | 7,49 | + | |
| дибензо(а,е)флуорантен | 2,64 | + | |
| 1-метилбензо(b)флуорантен | 3,61 | ? | + |
| 4-метилбензо(b)флуорантен | 4,86 | ? | + |
| 2,3-диметилфлуорантен | 2,91 | ? | + |
| 10,11-диметилбензо(k)флуорантен | 9,68 | ? | - |
* - за нуль принято значение Есс для бенз(а)пирена, равное 139,64 ккал/моль.
Результаты прогноза с использованием интегрированной системы совпали с экспериментальными данными. Было предсказано наличие/отсутствие канцерогенной активности соединений, для которых данные противоречивы и неизученных метил замещенных ПАУ. Результаты представлены в таблице 9.
Известно, что флуорантен и изомерные бензфлуорантены в наибольших среди ПАУ количествах присутствуют в воде. По результатам квантовохимических расчетов флуорантен по активности должен быть сопоставим с бенз(а)пиреном. Действительно установлено, что флуорантен обладает высокой мутагенной активностью. Однако в отличие от бенз(а)пирена он не связывается с цитозольным АН рецептором и не является промотором. Среди изомерных бензфлуорантенов бензо(b)флуорантен и особенно его 5-ОН-замещенный метаболит в согласии с результатами расчета должны обладать самой высокой среди изомеров генотоксичностью. Кроме того, бензо(b)флуорантен обладает высоким сродством к АН рецептору. Вероятно вследствие этого бензо(b)флуорантен является наиболее канцерогенным среди бензфлуорантенов. Самым высоким сродством к АН рецептору среди всех ПАУ обладает бензо(k)флуорантен. Это вероятно определяется наибольшей близостью линейных размеров бензо(k)флуорантена и 2,3,7,8-тетрахлордибензопарадиоксина – наилучшего агониста АН рецептора (11,06 и 10,996 Å). Такую же примерно близость размеров обнаруживают и другие ПАУ, проявляющие высокое сродство к рецептору – бенз(а)пирен и хризен (11,41Å и 11,43 Å). При этом надо учесть, что реакционная способность, в частности донорно-акцепторная способность ПАУ выше, чем у 1,2,7,8-дибензопарадиоксина. Поэтому в определении сродства к рецептору должны играть роль стерические факторы. Анализ экспериментальных данных и результатов расчетов показывает, что параметр Есс характеризует генотоксичность ПАУ, а сродство к AН рецептору определяется стерическими факторами, донорно-акцепторными свойствами и поляризумостью молекул. Такая зависимость установлена в ряду 34-х ПАУ, азааренов и их галогензамещенных производных.
Получена достоверная зависимость способности связываться с АН-рецептором, определенной в скрининговой тест-системе, в которой коэкспрессируются гены человеческого АН рецептора и транслокатора этого рецептора (ссылка скрыта. et al., 2003) от параметров, характеризующих акцепторную способность, поляризуемость и размер молекул.
С использованием параметра Есс, а также значений энергии высшей заполненной молекулярной орбитали, как параметра, характеризующего активность соединения в реакции биотрансформации через окисление по одноэлектронному механизму (Сavalieri E.L. et al., 1995, 2005), сделан ДСМ прогноз класса опасности по канцерогенному эффекту для 5 неизученных галогензамещенных ПАУ.
При исследовании зависимости структура-канцерогенная активность алифатических галогенсодержащих соединений (ГСС) была апробирована классификация по силе канцерогенного действия, поскольку для соединений этого ряда в базе данных CPDB имеются данные по величинам TD50 (TD50– доза, соответствующая вероятности образования злокачественных опухолей у 50% животных, в данном случае крыс и мышей, с учетом образования опухолей у контрольных животных, при ежедневном введении в течение всей жизни животных).
В качестве количественного критерия используется величина канцерогенного потенциала lg(М/TD50), где М – молекулярный вес. При этом низкими считались дозы, для которых lg(М/TD50) > 0, умеренными и высокими дозы, для которых -1< lg(М/TD50) < 0. К первому классу отнесены соединения, в низких дозах вызывающие образование злокачественных опухолей в различных органах у нескольких видов животных, ко второму классу – соединения, в умеренных дозах (-1
При прогнозе канцерогенности насыщенных алифатических ГСС мы исходили из гипотезы, высказанной G.H.Loew (Loew G.H., et al., 1984) что ключевой реакцией механизма токсического действия является взаимодействие стабильных высокотоксичных метаболитов – альдегидов и кетонов с ДНК.
Таблица 10. Классификация для прогноза канцерогенной опасности химических веществ
| Показатель | Высоко опасные (1 класс) | Умеренно опасные (2 класс) | Низко-умеренно опасные (3 класс) | Слабо опасные и не канцерогены (4 класс) | ||
| Канцерогенный потенциал (ср) {lg(М/TD50)} | >0 | -1 | > 0 | -1 | cp <-1 | не вызы-вает обра-зования опухолей |
| Количество видов животных с с опухолями | >1 | >1 | 1 | 1 | 1 | |
| Количество пораженных орга-нов у одного вида | >1 | >1 | 1 | 1 | 1 | |
