Н. Н. Александрова удк 616. 62-006. 6: 615. 28: 537. 363 (476) Суконко Олег Григорьевич лечение больных почечно-клеточным раком с учетом факторов прогноза автореферат диссертации
| Вид материала | Автореферат диссертации |
- Автореферат диссертации на соискание ученой степени, 672.22kb.
- Удк (616. 33 002. 44+616. 342-002. 44)-07: 616. 1 Морфо-функциональные особенности, 544.96kb.
- Автореферат диссертации на соискание ученой степени, 445.33kb.
- Рак печени и органов билиопанкреатодуоденальной зоны: современная диагностика и лечение, 411.75kb.
- «Медицинский радиологический научный центр», 269.03kb.
- Удк 615. 2/-3 03: 616. 31(035) бек 56-6 М58 Максимовская Л. Н., Рощина, 3079.44kb.
- Пособие для врачей Минск, 2006 удк 616. 8-053. 2(476), 404.21kb.
- Учебно-методическое пособие Минск 2009 удк 618. 19-006. 03 (075. 9) Ббк 57. 15я73, 956.31kb.
- Гридько Людмила Анатолиевна удк 796: 618. 3-085+616. 155. 194 Физическая реабилитация, 447kb.
- Удк 616. 69-085. 25: 616. 379-008. 64 Фармакологическая коррекция тадалафилом эректильной, 165.57kb.
Опубликованность результатов
Основные положения диссертации опубликованы в 59 печатных работах, в том числе 17 журнальных статьях, 13 статьях в научных сборниках и материалах конференций, 24 тезисах докладов.
По результатам работы получено 2 авторских свидетельства: "Способ лечения рака почки" (авт. св. СССР № 1575374, 1990 г.) и "Способ лечения рака почки" (патент РБ № 2447 от 17.11.1998 г.).
Издано методическое письмо " Способ группового прогнозирования результатов лечения операбельных больных раком почки" и 2 инструкции по применению: "Хирургическое лечение больных раком почки", "Лечение больных раком почки III стадии с учетом факторов прогноза".
Структура и объем диссертации
Диссертация написана на русском языке, состоит из введения, семи глав, заключения, выводов, практических рекомендаций и списка литературы, включающего 117 отечественных и 257 зарубежных источников. Работа изложена на 235 страницах (из них 207 страницы текста), иллюстрирована 68 таблицами и 51 рисунком.
Основные положения, выносимые на защиту
- Разработанный способ группового прогноза адекватно распределяет больных почечно-клеточным раком на прогностические классы.
- У больных с неблагоприятным прогнозом после радикальной операции показано проведение двух сеансов адъювантной термохимиотерапии в сочетании с иммунотерапией интерфероном-альфа-2b.
- Разработан прогностический комплекс по разделению больных раком почки III стадии на благоприятный и неблагоприятный классы. Для больных с неблагоприятным прогнозом показано проведение общей гипертермии как адъювантной составляющей многокомпонентного лечения, для больных с благоприятным прогнозом методом выбора является комбинированное лечение.
- Расширение объема операции в обоснованных для каждой прогностической группы пределах достоверно улучшает результаты лечения больных и увеличивает точность послеоперационного прогнозирования.
- Применение термохимиотерапии с гипергликемией у первичных больных раком почки с отдаленными метастазами достоверно повышает выживаемость больных.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
- Материал и методы исследования
1.1. Общая характеристика клинических наблюдений
Материалом диссертации послужили результаты наблюдения за 1297 больными раком почки, которые лечились в онкоурологическом отделении ГУ "НИИ онкологии и медицинской радиологии им. Н.Н. Александрова" с 1987 по 1996 гг. включительно. Среди больных было 765 (59,0%) мужчин и 522 (41,%) женщин. Преимущественный возраст больных от 50 до 70 лет, средний возраст – 56,2±0,3 года. Распространенность опухолевого процесса определялась в соответствии с TNM-классификацией Международного Противоракового союза 1997 года. Морфологический вариант почечно-клеточного рака устанавливали по классификации А.А. Карновского и А.А. Васильевой 1981 года, степень дифференцировки - в соответствии с Международной гистологической классификацией опухолей почек под редакцией Ф.И. Мостофи 1984 года (табл. 1).
Таблица 1
Общая характеристика наблюдений
| Признак | Количество больных (n = 1297) | |
| распространение опухоли по стадиям, классификация 1997 г. | I II III IV | 370 (28,5±1,3%) 61 (4,7±0,6%) 624 (48,1±1,4%) 242 (18,7±1,1%) |
| морфологический вариант | светлоклеточный темно-клеточный железистый веретеноклеточный | 958 (73,9±1,2%) 235 (18,1±1,1%) 62 (4,8±0,6%) 42 (3,2±0,5%) |
| степень дифференцировки | высокая умеренная низкая | 584 (45,0±1,4%) 551 (42,5±1,4%) 162 (12,5±0,9%) |
1.2. Методы лечения больных
Характеристика методов лечения представлена в таблице 2.
Таблица 2
Характеристика методов лечения, применяемых у больных
почечно-клеточным раком
| Метод лечения | Количество больных (n = 1297) |
| 1 | 2 | |
| Хирургический | 648 (50,0%) | |
| Комбинированный: I – крупнофракционная предоперационная лучевая терапия по 7 Гр ежедневно на опухоль и зоны регионарного метастазирования, СОД – 14 Гр, затем операция; II – крупнофракционная предоперационная лучевая терапия 7 Гр на опухоль и зоны регионарного метастазирования, э Продолжение табл. 2 мболизация почечных сосудов, на фоне острой гипоксии – второй сеанс лучевой терапии 8,5 Гр, СОД – 15,5 Гр, затем операция*. | 378 (29,1%) 342 (26,4%) 36 (2,8%) | |
| Термохимиотерапия: I – у больных с неблагоприятным прогнозом после операции проводилось два сеанса общей гипертермии с гипергликемией и химиотерапией доксорубицином 60 мг/м2; II – первый сеанс ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 60 мг/м2 проводился до операции, затем операция, после операции дополнительно сеанс ОГТ**; III – у первичных больных с отдаленными метастазами, после операции, проводились сеансы ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 60 мг/м2. Сеансы ОГТ повторялись через 1,5-2 месяца до полной регрессии опухоли или до прогрессирования, суммарная доза доксорубицина не превышала 600 мг/м2. | 100 (7,7%) 36 (2,8%) 36 (2,8%) 28 (2,2%) | |
| Термохимиотерапия с иммунотерапией: I – у больных с неблагоприятным прогнозом после операции проводилось два сеанса ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 60 мг/м2 на фоне 7 введений интерферона–альфа-2b в дозе 3 млн ЕД/м2; II – у первичных больных с отдаленными метастазами, после операции, проводились сеансы ОГТ с гипергликемией и химиотерапией доксорубицином 60 мг/м2 на фоне 7 введений интерферона–альфа-2b в дозе 3 млн. ЕД./м2. Сеансы ОГТ с иммунотерапией повторялись через 2 месяца до полной регрессии опухоли или до прогрессирования, суммарная доза доксорубицина не превышала 600 мг/м2. Всего проведено 376 сеансов ОГТ у 147 больных | 47 (3,6%) 35 (2,7%) 12 (0,9%) | |
| Прочие методы лечения: группу составляют пациенты, у которых методы лечения не соответствовали условиям протоколов исследования, или проводились дополнительные воздействия в виде паллиативной лучевой терапии, иммунотерапии, гемосорбции и т.д. | 124 (9,6%) | |
| Примечания: |
| |
1.3. Программное обеспечение исследования
Все расчеты выполнялись на персональном компьютере на базе процессора Intel (R) Celeron (TM) 400 MHz в операционной среде WINDOWS 98. На разных этапах работы использовались различные комплексы статистических программ. На первом этапе исследований применялись электронные таблицы Excel 2000 со специально разработанными программами на языке VBA, затем программный комплекс Statistica 5.0.
Данные, характеризующие состояние больных, вводились в базу в соответствии с кодификатором. Кроме того, в базу данных вводилась информация о методах лечения, реакции на проводимое лечение и судьбе больных.
Процедуры кластерного и дискриминантного видов анализа выполнялись с использованием программного комплекса Statistica 5.0.
1.4. Критерии оценки результатов лечения
Основным критерием оценки результатов лечения является выживаемость больных. Кумулятивная выживаемость и ее средняя ошибка определялись вычислением таблиц дожития по интервальному методу. Также рассчитывались медиана времени жизни больных и средняя продолжительность жизни. Достоверность различий показателей пятилетней кумулятивной выживаемости в группах больных определялись по обобщенному критерию хи-квадрат (χ2).
Оценка сопоставимости двух и более групп наблюдения и сравнение результатов лечения (динамика отдаленных метастазов, сроки появления, локализация и др.) проводились по критерию хи-квадрат. Парное сравнение некоторых параметров результатов лечения и точечной выживаемости проводилось по критерию Стьюдента-Фишера.
Статистические параметры при нулевом, либо стопроцентном значениях показателей, определялись по методу Ван-дер-Вардена.
- Применение адъювантной и неоадъювантной общей гипертермии у радикально оперированных больных почечно-клеточным раком с неблагоприятным прогнозом
2.1. Характеристика способа прогнозирования, применяемого для формирования однородных групп больных
Основой для прогнозирования результатов лечения при раке почки является Международная классификация по системе TNM. В тоже время, по мнению большинства исследователей, Международная классификация недостаточно эффективно выделяет больных с неблагоприятным прогнозом (Gospodarowicz M. K., 1995; Мавричев А.С., 1996; Серняк Ю.П., 1998; Gofrit O. N., 2001). Поэтому на современном этапе развития онкоурологии важное значение приобретает групповое прогнозирование, дополняющее систему TNM (Gospodarowicz M. K., 1995; Gilbert C., 1997; Серняк Ю.П., 1998). Вместе с тем, подобного рода исследования, как правило, ограничиваются лишь определением комплекса признаков. В литературе отсутствуют сообщения, в которых разработанные комплексы применялись бы в клинике для обоснования того или иного метода лечения рака почки.
С 1978 по 1990 годы нами впервые в онкоурологии для прогнозирования был использован метод кластерного анализа, который позволил выделить однородные группы операбельных больных раком почки (Суконко О.Г., 1990; Мавричев А.С., 1992). С 1991 г. разработанный прогностический комплекс применен в клинике для обоснования использования общей гипертермии у радикально оперированных больных раком почки в группах с неблагоприятным прогнозом в качестве адъювантного и/или неоадъювантного фактора комплексного лечения (Суконко О.Г., 1990; Мавричев А.С., 1992).
2.2. Методы лечения и выживаемость больных с неблагоприятным прогнозом
В прогностически неблагоприятных группах проведено проспективное рандомизированное исследование различных вариантов применения ОГТ. Схема протокола исследования представлена на рисунке 1. Согласно требованиям протокола все больные с неблагоприятным прогнозом распределялись на 4 подгруппы, три из которых были исследуемыми, а одна – контрольная.
В контрольной подгруппе проводилось хирургическое лечение в объеме радикальной или расширенной нефрэктомии.
Во второй подгруппе на первом этапе лечения выполнялась операция, затем, после заживления раны, проводился первый сеанс ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 50-60 мг/м2. В последующем, с интервалом в один месяц, дополнительно проводился второй сеанс ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 50-60 мг/м2.
В третьей подгруппе на первом этапе лечения также выполнялась операция, затем после заживления раны проводился первый сеанс ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 50-60 мг/м2 на фоне введения интерферона–альфа-2b. Интерферон–альфа-2b вводился внутримышечно по 3 млн. Ед/м2 в 1-, 2-, 3-, 5-, 6-, 7-й дни за час до сна. В 4-й день лечения интерферон–альфа-2b вводили за 1 час до начала общей гипертермии. Дополнительно второй сеанс ОГТ на фоне интерферона–альфа-2b проводились с интервалом в 1-1,5 месяца.
В четвертой подгруппе лечение начинали с проведения сеанса ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 50-60 мг/м2, затем через 24-48 часов выполнялась операция. Дополнительно второй сеанс ОГТ проводился обычно с интервалом в 1–1,5 месяца.

Формулы для определения места больного в прогностической группе
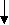

Группы с неблагоприятным прогнозом:
прогнозируемой пятилетней выживаемостью –
14,0±5,7% и 2,9±2,6%
(n = 161)







I
Операция (n=54)
II
Операция
+ ОГТ
(n=36)
III
Операция
+ ОГТ + интерферон–альфа-2b (n=35)
IV
ОГТ +
Операция
+ ОГТ
(n=36)
| I подгруппа II подгруппа – III подгруппа – IV подгруппа – | Контрольная, выполнялась только операция; Операция + ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 50-60 мг/м2; Операция + ОГТ на фоне введения интерферона–альфа-2b в течение семи дней по 3 млн. Ед/м2; ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 50-60 мг/м2 + операция + ОГТ |
Рис. 1 Схема протокола исследований
Механизм повреждающего действия ОГТ на опухоль до настоящего времени изучен недостаточно, а морфологические изменения, происходящие в опухоли почки после сеанса ОГТ с гипергликемией и химиотерапией доксорубицином вообще не изучались. Подобные исследования выполнены нами впервые у больных раком почки с неблагоприятным прогнозом, когда первый сеанс ОГТ проводился до удаления почки с опухолью (подгруппа IV).
Установлено, что термохимиотерапия с доксорубицином вызывает в опухоли почки замедление кровотока, прекращение митотической и амитотической активности клеток карцином, лизис ядер большинства клеток, посттерапевтический некроз, утолщение фиброзной капсулы в результате клеточной инфильтрации стромы на границе с опухолью
Из всех изучаемых вариантов применения ОГТ в неблагоприятной группе, наиболее эффективным оказалось сочетанное применение гипертермии, гипергликемии, химиотерапии доксорубицином на фоне введения интерферона-альфа-2b в течение 7 дней (рис. 2). В данном случае трехлетняя выживаемость больных повысилась до 65,0±8,2%, пятилетняя – до 53,8±9,0% (в контрольной подгруппе трехлетняя выживаемость равна 43,4±6,7%, p < 0,05; пятилетняя – ниже на 21,2% и составила 32,6±6,6%).
Рисунок 2
Таким образом, адъювантная термохимиотерапия на фоне иммунотерапии интерфероном-альфа-2b, является достаточно эффективным методом лечения больных раком почки с неблагоприятным прогнозом.
2.3. Сравнительная характеристика прогнозируемой и реальной пятилетней выживаемости больных раком почки
Опыт применения классификации 1986 г. проспективно показал, что идея исследования оказалась верной. Больные раком почки после радикальной операции распределялись на однородные группы, которые отличались между собой по выживаемости. В то же время выявлено, что реальная пятилетняя выживаемость с 1987 по 1996 гг. отличалась от прогнозируемой (рис. 3). Общая выживаемость больных раком почки за 10 лет увеличилась с 43,4±3,5 до 64,7±1,5% (р < 0,05). По нашему мнению это объясняется применением общей гипертермии в неблагоприятных группах, а также совершенствованием хирургической техники и расширением объема операций.
Кроме того, анализ эффективности применения классификационеных схем с учетом особенностей Международной классификации по системе TNM определил необходимость изменения подхода к прогнозированию при раке почки. Выявлена целесообразность разработки прогностического комплекса непосредственно для III стадии почечно-клеточного рака.
- Хирургическое лечение больных раком почки
Основным компонентом лечения больных раком почки является хирургический метод. Несмотря, на более, чем столетнюю историю развития хирургии рака почки, некоторые вопросы оперативного лечения окончательно не решены и сейчас. Прежде всего это касается целесообразности и объема лимфодиссекции, необходимости адреналэктомии на стороне поражения, технических особенностей удаления опухолевых тромбов из почечной и нижней полой вены.
Углубленное изучение проблем хирургического лечения рака почки в наших исследованиях направлено на решение этих вопросов, а также на определение прогностической значимости состояния регионарных лимфоузлов, наличия опухолевого тромба в почечной и полой нижней венах, метастатического поражения надпочечника на стороне поражения.
3.1. Лимфодиссекция при раке почки
Нами проведено сравнительное изучение эффективности факультативной лимфаденэктомии, выполняемой с 1987 по 1991 гг. (контрольная группа) и ограниченной лимфодиссекции, выполняемой с 1992 по 1996 гг. (исследуемая группа).
Факультативная лимфаденэктомия заключалась в удалении макроскопически измененных лимфоузлов, определяемых во время операции. Критерием служило увеличение лимфоузлов, изменение их консистенции и цвета.
Ограниченная лимфодиссекция включала удаление лимфоузлов с окружающей жировой клетчаткой единым блоком в пределах ворот почки независимо от их макроскопических изменений. При раке правой почки удаляли латерокавальные, прекавальные лимфоузлы, расположенные в пределах ворот почки и ретрокавальные по ходу почечной артерии. При поражении левой почки удалялись латероаортальные лимфоузлы в границах ворот почки, преаортальные в месте отхождения почечной артерии от аорты, интераортокавальные по ходу почечной вены до впадения в НПВ.
Основное исследование (с 1992 по 1996 гг.) включало 672 (58,6%) больных раком почки. Группа сравнения (с 1987 по 1991 гг.) составила 474 (41,4%) больных.
Из всего массива больных метастазы в лимфоузлах выявлены у 114 (9,9%) (табл. 3). Поражение одного лимфоузла установлено у 49 (4,3%), множественные метастазы определялись у 65 (5,7%) больных.
Таблица 3
В случае метастазирования в лимфоузлы, пятилетняя выживаемость пациента составляла 21,3±4,2%, а без метастазов в лимфоузлах – 69,4±1,5% (р < 0,001). Причем, при единичном метастазе пятилетняя выживаемость равнялась 31,3±7,3%, при множественном поражении – 14,2±4,6% (р < 0,01). Как видим, пятилетняя выживаемость достоверно отличалась при единичном или множественном поражении лимфоузлов, что необходимо учитывать при прогнозировании.
При изучении зависимости состояния лимфоузлов от местного распространения опухоли установлен одинаковый рост метастазирования с увеличением стадии опухолевого процесса в исследуемой и контрольной группах. Группы между собой не отличались по количеству метастазов при опухолях рТ3 и рТ4. Метастазы в лимфоузлах у больных с опухолями рТ3 определялись у 15%, а при опухолях рТ4 – у 50%. Различия были получены у пациентов с опухолями рТ1 и рТ2 (рис. 4). В исследуемой группе метастазы в лимфатических узлах при опухолях рТ1-рТ2 составили 3,1%, а в контрольной группе при данном распространении опухоли они вообще не обнаружены.
Рис. 4.
Таким образом, выполняемая нами ограниченная лимфодиссекция свидетельствует о необходимости удаления лимфоузлов даже при локализованных формах рака почки. Метастазы в макроскопически неизмененных лимфоузлах можно определить только микроскопически.
Результаты сравнения выживаемости у больных с единичным поражением лимфоузлов или множественными метастазами, при хирургическом лечении, выявили эффективность ограниченной лимфодиссекции у больных с единичными метастазами в лимфоузлах (рис. 5). Достоверные различия выживаемости получены на протяжении всего пятилетнего периоде наблюдения. При множественном поражении лимфоузлов выживаемость между исследуемой и контрольными группами достоверно не отличалась на протяжении всего периода наблюдения (рис. 6).
Рис. 5.
Рис. 6.
Следовательно, ограниченная лимфодиссекция является методом выбора у больных раком почки при опухолях рТ1-рТ2, при опухолях рТ3-рТ4 обоснована расширенная лимфодиссекция.
3.2. Распространение опухоли в почечную и нижнюю полую вены (НПВ)
Распространение опухоли в почечную и НПВ, с учетом всей базы данных, имело место у 131 (11,4%) больных. Прорастание опухоли в почечную вену определялось у 84 (7,3%) больных, в НПВ до диафрагмы – у 40 (3,5%) и выше диафрагмы – у 7 (0,6%) пациентов.
При изучении продолжительности жизни больных раком почки с распространением опухоли в магистральные вены установлена прямая зависимость пятилетней выживаемости от уровня распространения опухоли в венозной системе (рис. 7). Пятилетняя выживаемость больных при отсутствии опухолевого тромба в венах составляла 67,6±1,5%, при наличии опухолевого тромба в почечной вене – 51,5±5,7%, в НПВ до диафрагмы – 30,9±7,5% (р < 0,05). В случае инвазии опухоли выше диафрагмы, все больные умерли ко второму году наблюдения.
Рис. 7
Полученные результаты подтверждаются при анализе выживаемости больных с хирургическим методом лечения без метастазов в лимфоузлах (рис. 8). Пятилетняя выживаемость больных с опухолевым тромбом в почечной вене составляла 42,2±10,3%, без тромба – 77,4±1,9% (р < 0,05).
Рис. 8.
Таким образом, прорастание опухоли в почечную и НПВ является неблагоприятным прогностическим признаком, причем прогноз ухудшается при увеличении уровня распространения опухоли в венах.
3.3. Распространение опухоли в ипсилатеральный надпочечник
В нашей работе с 1987 по 1991 гг. адреналэктомия выполнялась при подозрении на поражение органа; с 1992 по 1996 гг. надпочечник удалялся у всех больных III, IV стадии и у больных I, II стадии – при локализации опухоли в верхнем полюсе почки.
Изучение полученных данных показало, что метастазы в надпочечнике, с учетом всей базы данных, были выявлены у 21 (1,8±0,4%) больных. Причем, при опухолях рТ1-Т2, метастазы ни у одного больного морфологически не определялись.
При анализе материала отдельно в двух группах сравнения установлено, что в исследуемой группе метастазы выявлены у 9 (2,5±0,8%) больных третьей стадии и у 8 (15,1±4,9%) – четвертой стадии (табл. 4).
Таблица 4
Распространение опухоли в надпочечник
| Исследуемая группа (n = 672) | Контрольная группа (n = 474) | ||||
| Стадия | Кол-во больных | Распростра-нение в надпочечник | Стадия | Кол-во больных | Распростра-нение в надпочечник |
| III IV | 365 53 | 9 (2,5±0,8%) 8 (15,1±4,9%) | III IV | 259 38 | 3 (1,2±0,7%) 1 (2,6±2,6%) |
| Всего больных с поражением надпоче-чника | 418 | 17 (4,1±1,0%)* | Всего больных с поражением надпоче-чника | 297 | 4 (1,3±0,7%) |
| Примечание. | * - различия достоверны по сравнению с контрольной группой (р < 0,05) |
В контрольной группе аналогичные показатели составляли 3 (1,2±0,7%) и 1 (2,6±2,6%) пациентов. Таким образом, в исследуемой группе из 418 больных третьей, четвертой стадий метастазы были у 17 (4,1±1,0%), в контрольной – из 297 у 4 (1,3±0,7%), (р < 0,05).
Распространение опухоли в надпочечник является неблагоприятным прогностическим признаком (рис. 8). В случае прорастания опухоли, пятилетняя выживаемость снижалась в 2 раза с 67,3±1,5 до 35,8±10,9% (р < 0,05). Как видим, результаты исследований свидетельствуют о целесообразности удаления надпочечника у больных раком почки III-IV стадий, независимо от локализации опухоли в почке.
- Прогноз отдаленных результатов лечения у радикально оперированных больных раком почки
4.1. Обоснование необходимости изменения стратегии прогнозирования при раке почки
Проведенные исследования показали, что расширение объема операции, наряду с применением адъювантной ОГТ у больных с неблагоприятным прогнозом позволили улучшить результаты лечения больных раком почки (рис. 10). Так пятилетняя выживаемость больных раком почки I стадии составила 86,8±1,8%, II – 80,7±5,3%, III – 57,2±2,1% и IV – 13,2±3,8%. Как видим, с вероятностью до 86% у больных I, II стадии прогноз благоприятный и наоборот после радикальной операции у 87% больных IV стадии прогноз неблагоприятный. По сути, для данных категорий больных классификация по системе TNM является оптимальной. Понятной становится необходимость в изменении стратегии прогнозирования при раке почки.
Рис. 10.
Для прогноза наибольший интерес представляет III стадия рака почки, которая от всей базы данных составляет 54,5%, а от всех вновь выявленных больных раком почки в Республике Беларусь – 30,3% (Поляков С.М. и соавт., 2003). При этом средний показатель пятилетней выживаемости – 57,2%, что не дает определенной информации о прогнозе для больных этой группы. Несмотря на выполненную радикальную операцию, у каждого второго больного раком почки III стадии появляются отдаленные метастазы, т.е. проведенное лечение нельзя считать адекватным. Понятно, что группа больных, составляющих III стадию, является изначально неоднородной, этим можно объяснить различные варианты развития болезни. Соответственно, задачей исследования мы определили выявление этой неоднородности и построение классификационной схемы для III стадии, которая позволит устранить недостаточную информативность Международной классификации по системе TNM.
Таким образом, классификация по системе TNM и предлагаемая классификационная схема для III стадии составят единый прогностический комплекс.
4.2. Классификация для III стадии рака очки
До начала исследования все 624 больных раком почки III стадии были разделены на исследуемую и экзаменационную группы. Разделение проводилось по номерам больных с использованием компьютерной программы рандомизации. Дополнительно подтверждалась сопоставимость полученных групп по основным прогностическим показателям. Далее классификационная схема и соответствующие ей решающие правила разрабатывались на исследуемой группе и проверялись на экзаменационной.
Для получения классификации использовался кластерный анализ. Первоначально при разработке классификации рассматривались все прогностически значимые признаки, выявленные на основе монофакторного и сочетанного анализов.
В оптимальную классификацию вошли следующие показатели:
- функция пораженной почки;
- СОЭ при поступлении;
- максимальный размер опухоли, определяемый после удаления почки;
- состояние регионарных лимфоузлов после операции;
- опухолевый тромб в почечной и нижней полой венах;
- степень дифференцировки опухоли.
Полученная классификационная схема позволила распределить массив больных на два однородных класса с достоверно отличающимися показателями отдаленных результатов лечения (рис. 11). Проверка результатов на экзаменационной группе показала практически полное совпадение динамики показателей выживаемости. Как следует из рисунка 11, пятилетняя выживаемость больных раком почки III стадии в первой группе составила 72,2±2,5%, во второй – 37,4±3,1% (р < 0,01). Первый класс можно считать благоприятным с точки зрения прогноза выживаемости, второй – неблагоприятным.
Рис. 11.
Таким образом, построена классификация, устраняющая недостаток TNM, позволяющая получить достоверные данные о прогнозе результатов лечения для больных III стадии.
Решающие правила для определения принадлежности больного к соответствующему классу были получены с помощью дискриминантного анализа. Для определения принадлежности каждого нового больного раком почки III стадии к соответствующей группе необходимо вычислить два следующих выражения, с учетом кодификатора признаков:
Р1 = 2,8хФПП + 0,19хСОЭ + 0,54хРО + 4,0хЛ – 0,1хОТ + 4,8хСДО + 5,9
Р2 = 3,0хФПП + 0,50хСОЭ + 0,66х РО + 10,6хЛ + 1,1хОТ + 7,4хСДО – 11,9
где ФПП – функция пораженной почки (0 – не изменена, 1 – снижена, 2 – отсутствует);
СОЭ – скорость оседания эритроцитов при поступлении (абсолютная величина в мм/час);
РО – максимальный размер опухоли, определяемый после удаления почки (абсолютная величина в см);
Л – состояние регионарных лимфатических лимфоузлов (0 – метастазы в лимфоузлах не определяются, 1 – отмечается поражение одного лимфоузла);
ОТ – опухолевый тромб в почечной и нижней полой венах (0 – опухолевый тромб не определяется, 1 – опухолевый тромб в почечной вене, 2 – опухолевый тромб в нижней полой вене до диафрагмы, 3 – опухолевый тромб в нижней полой вене выше диафрагмы);
СДО – степень дифференцировки опухоли (1 – высокая, 2 – умеренная, 3 – низкая).
Если Р1 > Р2, то больной раком почки III стадии относится к первому классу с ожидаемой пятилетней выживаемостью 72,2±2,5%, который считается прогностически благоприятным классом.
Если Р2 > Р1, то больной относится ко второму классу с ожидаемой пятилетней выживаемостью 37,4±3,1%, который считается прогностически неблагоприятным.
Приведем пример расчета: больная И., история болезни 7316/91, рак правой почки T3aN0M0 III стадия. По внутривенной урографии отмечается снижение функции правой почки (1), СОЭ при поступлении 20 мм/час. Максимальный размер опухоли, определяемый после удаления почки составил 13 см. Метастазы в регионарных лимфоузлах по данным микроскопического исследования не установлены (0), опухолевый тромб в почечной и нижней полой венах не обнаружен (0). Гистологически у больной умеренно дифференцированный почечно-клеточный рак (2).
В разработанных решающих правилах условные буквенные обозначения заменяем на реальные и проводим вычисления. При этих условиях Р1 = 29,1; Р2 = 24,5, т.е. пациентка должна быть отнесена к первому классу с благоприятным прогнозом и ожидаемой пятилетней выживаемостью 72,2±2,5%.
4.3. Характеристика эффективности методов лечения, проводимых в прогностических классах
В соответствии с известной концепцией предполагающей, что однородные группы больных, различающихся по комплексу показателей характеризующих систему: "организм больного – опухоль" должны по разному реагировать на проводимое лечение. Можно утверждать, что разработанная нами классификационная схема позволит производить оценку эффективности различных методов лечения, для выявленных нами групп. При изучении методов лечения в полученных классах оказалось, что больные, действительно, по разному реагируют на проводимое лечение (рис. 12).
Рис. 12.
В исследовании у 318 (27,7%) больных проводилось комбинированное лечение, которое включало предоперационное облучение разовой дозой 7 Гр (СОД – 14 Гр), с интервалом между фракциями в 24 часа (ВДФ – 35 ед.). Операция выполнялась через 24 часа после второго сеанса облучения. Анализ эффективности комбинированного лечения, проведенный в группах больных, определяемых по системе TNM Международной классификации 1997 г., не позволил выявить группы, для которых данный метод лечения достоверно является предпочтительным. В тоже время, в прогностически благоприятной первой группе III стадии получены достоверные различия между показателями пятилетней выживаемости для больных с хирургическим и комбинированным методами лечения. Пятилетняя выживаемость пациентов с хирургическим методом лечения составила 69,8±3,7%, комбинированным – 81,7±3,6% (χ2 = 4,1; р <0,05).
В прогностически неблагоприятной второй группе различия между хирургическим и комбинированным методом лечения не отмечено. Пятилетняя выживаемость при хирургическом лечении составила 31,9±5,9%, комбинированном – 37,3±6,4%. Вместе с тем, достоверные различия получены между хирургическим методом лечения и подгруппой, включающей все варианты общей гипертермии. При хирургическом лечении пятилетняя выживаемость составила 31,9±5,9%, в случае включения в схему лечения ОГТ –54,8±6,1% (χ2 = 5,1; p < 0,05).
Как видим, полученные результаты указывают на целесообразность применения адъювантной общей гипертермии в прогностически неблагоприятной группе больных раком почки III стадии. Комбинированное лечение, включающее предоперационное облучение в СОД 14 Гр и операцию, является методом выбора для лечения больных раком почки III стадии. Разработанная классификация является достаточно эффективной для прогнозирования продолжительности жизни больных раком почки III стадии и обоснования необходимости назначения адекватного лечения у пациентов этой группы.
- Лечение первичных больных раком почки
с отдаленными метастазами
В работе проведен ретроспективный анализ лечения первичных больных раком почки с отдаленными метастазами. Целью исследования было изучение эффективности применения ОГТ в этой крайне сложной группе больных.
Исследование основано на изучении данных о 151 первичном больном раком почки с отдаленными метастазами, оперированных с 1987 по 1996 гг. включительно. От всей совокупности оперированных больных они составили 11,6%.
На первом этапе лечебной программы у всех больных выполнялось хирургическое вмешательство, затем применялись различные методы дополнительного воздействия (рис. 13). Объем хирургического лечения, включая радикальную или расширенную нефрэктомию с удалением отдаленных метастазов, при наличии технических возможностей.
Рис. 13.
Сопоставимость была получена только между группой больных в которой после операции проводилось гормональное лечение (59 больных) и группой пациентов, где применялась ОГТ (28 больных). Соответственно, сравнительный анализ выживаемости проведен в этих двух группах.
Из гормональных препаратов назначали зитозониум или оксипрогестерон капронат. Первый сеанс ОГТ с гипергликемией и химиотерапией доксорубицином в дозе 60 мг/м2 проводили через 2 недели после заживления раны. Сеансы гипертермии повторялись через 1,5-2 месяца до полной регрессии опухоли или до прогрессирования. Число сеансов ОГТ ограничивалось допустимой суммарной дозой доксорубицина в 600 мг/м2.
Выживаемость больных определялась на 1 января 2000 г., свыше 5 лет наблюдались 143 (94,7%) больных. По всему массиву больных одногодичная выживаемость составила 37,7±3,9%, трехлетняя – 13,9±2,8% и пятилетняя – 7,2±2,4%.
Включение ОГТ с гипергликемией и химиотерапией доксорубицином в схему лечения первичных больных с отдаленными метастазами повысило одногодичную выживаемость до 50,0±9,4%, в контрольной группе она составила 23,7±5,5% (р < 0,05) (рис. 14). Полная регрессия отдаленных метастазов получена у 3,6±3,5% больных, частичная - у 14,3±4,6% и стабилизация – у 42,9±9,4%. В контрольной группе полной и частичной регрессии метастазов не отмечено, стабилизация выявлена у 8,5±3,6% (χ2 = 29,0; р < 0,01) (рис. 15).
Рис. 15
Таким образом, применение ОГТ с химиотерапией доксорубицином у первичных больных раком почки с отдаленными метастазами является обоснованным.
