Календарный план учебных занятий по дисциплине «Тяжелые металлы в экосистемах» Лектор: доцент кафедры судебной экологии, к б. н. Кулиева Г. А
| Вид материала | Лекции |
- Календарный план учебных занятий по дисциплине «Радиационная генетика» Доцент кафедры, 66.04kb.
- Календарный план учебных занятий по дисциплине «Методы контроля состояния окружающей, 249.17kb.
- Календарный план учебных занятий по дисциплине «Экспертиза объектов и продукции, 161.26kb.
- Календарный план учебных занятий по обязательной дисциплине «Архитектура вычислительных, 33.03kb.
- Календарный план учебных занятий по обязательной дисциплине «Алгебра и геометрия»,, 105.72kb.
- Календарный план учебных занятий по обязательной дисциплине «Уравнения математической, 92.11kb.
- Календарный план учебных занятий по обязательной дисциплине «Математическая логика»,, 39.04kb.
- Календарный план учебных занятий по дисциплине «Компьютерное моделирование оптических, 38.78kb.
- Календарный план учебных занятий по дисциплине «Аналитическая геометрия» (НМ), II семестр., 51.03kb.
- Календарный план учебных занятий по обязательной дисциплине «Теория конечных графов»,, 36.19kb.
РОССИЙСКИЙ УНИВЕРСИТЕТ ДРУЖБЫ НАРОДОВ
Кафедра судебной экологии
КАЛЕНДАРНЫЙ ПЛАН
учебных занятий по дисциплине «Тяжелые металлы в экосистемах»
Лектор: доцент кафедры судебной экологии, к. б. н. Кулиева Г.А.
учебных недель -19; лекции - 38 часов, семинары - 38 часов, кредиты – 3,
4 курс, 7-й семестр 2010/2011 уч. г.
| НЕДЕЛИ | ЛЕКЦИИ | Число часов | СЕМИНАРЫ | Число часов |
| 1 неделя 1.9-4.9 | Введение. Основные понятия. Постановка цели и задач курса. Краткая характеристика наиболее распространенных тяжелых металлов (ртуть, свинец, кадмий) | 2 | Вводное занятие: обсуждение тем рефератов, бально-рейтинговой системы | 2 |
| 2 неделя 6.9-11.9 | Краткая характеристика наиболее распространенных тяжелых металлов (медь, цинк, олово) | 2 | Работа над составлением таблицы «Биогеохимические свойства тяжелых металлов» | 2 |
| 3 неделя 13.9-18.9 | Краткая характеристика наиболее распространенных тяжелых металлов (хром, кобальт, никель) | 2 | Работа над составлением таблицы «Биогеохимические свойства тяжелых металлов» | 2 |
| 4 неделя 20.9-25.9 | Природные источники поступления тяжелых металлов в биосферу. Фоновое содержание тяжелых металлов в природных средах | 2 | Защита и обсуждение рефератов | 2 |
| 5 неделя 27.9-02.10 | Антропогенные источники поступления тяжелых металлов в природную среду | 2 | Контрольная работа №1 | 2 |
| 6 неделя 04.10-09.10 | Методы определения тяжелых металлов. Пробоотбор при контроле загрязнения почв. | 2 | Обсуждение методов определения тяжелых металлов | 2 |
| 7 неделя 11.10-16.10 | Миграционные процессы металлов в биогеоценозах. Биогеохимические барьеры. Коэффициенты. | 2 | Расчет коэффициентов для описания и оценки подвижности элементов в биосфере, поведения их соединений на локальном, региональ-ном и глобальном уровнях. | 2 |
| 8 неделя 18.10-23.10 | Свойства почв, влияющие на биологическую доступность тяжелых металлов и методы их регулирования | 2 | Построение схемы, иллюстрирующей миграционные процессы металлов в биогеоценозах | 2 |
| 9 неделя 25.01-30.10 | Общие аспекты токсичности тяжелых металлов для живых организмов. Необходимые элементы и их роль в организме животных и растений | 2 | Контрольная работа №2 | 2 |
| 10 неделя 1.11-6.11 | Общие аспекты токсичности тяжелых металлов для живых организмов. Естественные механизмы детоксикации | 2 | Защита и обсуждение рефератов | 2 |
| 11 неделя 8.11-13.11 | Восстановление земель, загрязненных тяжелыми металлами (известкование, применение сорбентов различной природы, др.) | 2 | Защита и обсуждение рефератов | 2 |
| 12 неделя 15.11-20.11 | Растения - гипераккумуляторы тяжелых металлов | 2 | Защита и обсуждение рефератов | 2 |
| 13 неделя 22.11-27.11 | Методы фиторемедиации | 2 | Защита и обсуждение рефератов | 2 |
| 14 неделя 29.11-4.12 | Осадки сточных вод как основной источник загрязнения природных компонентов тяжелыми металлами | 2 | Защита и обсуждение рефератов | 2 |
| 15 неделя 6.12-11.12 | Нормирование содержания тяжелых металлов в кормах и продукции животноводства | 2 | Контрольная работа №2 | 2 |
| 16 неделя 13.12-18.12 | Пробоотбор тяжелых металлов в осадках | 2 | Защита и обсуждение домашних работ | 2 |
| 17 неделя 20.12-25.12 | Обсуждение сложных вопросов курса, подготовка к экзамену | |||
ТЯЖЕЛЫЕ МЕТАЛЛЫ В ЭКОСИСТЕМАХ
Цель курса - изучение физических и биогеохимических свойств тяжелых металлов; источников поступления тяжелых металлов в биосферу, биологического действия на организм теплокровных; закономерностей миграции; путей ремедиации загрязненных территорий.
Содержание курса:
Краткая характеристика наиболее распространенных в окружающей среде тяжелых металлов. Приоритетные загрязняющие вещества (по классификации Агентства по охране окружающей среды).
Природные источники поступления тяжелых металлов в биосферу. Фоновое содержание тяжелых металлов в природных средах.
Антропогенные источники поступления тяжелых металлов в природную среду. Тепловая энергетика, транспорт, металлургия.
Методы определения тяжелых металлов. Отбор проб при контроле загрязнения почв. Атомно-абсорбционный метод определения тяжелых металлов.
Миграционные процессы металлов в биогеоценозах. Формы нахождения металлов в биогеоценозах, валовое содержание, наличие мобильных форм и биологическая доступность, способность к комплексобразованию, экстракция. Коэффициент водной миграции, коэффициент аккумуляции. Коэффициент биологического поглощения, коэффициент относительного поглощения, акропетальный коэффициент. Ряды значений коэффициента биологического поглощения металлов.
Свойства почв, влияющие на биологическую доступность металлов (количество органического вещества, фосфатов, емкость катионного обмена, уровень рН, гранулометрический состав, дренаж) и методы их регулирования. Биогеохимические барьеры.
Общие аспекты токсичности тяжелых металлов для живых организмов. Необходимые элементы и их роль в организме животных и растений. Естественные механизмы детоксикации.
Восстановление земель, загрязненных тяжелыми металлами. Физико-химические (использование сорбентов различной природы, известкование и др.) и биологические методы. Методы фиторемедиации. Растения -гипераккумуляторы тяжелых металлов. Механизмы мобилизации, поглощения и концентрирования тяжелых металлов растениями. Средообразующая роль корневой системы растений, экссудаты. Микробная трансформация соединений тяжелых металлов. Перемещение тяжелых металлов по пищевым цепям.
Конспект лекций по дисциплине
«ТЯЖЕЛЫЕ МЕТАЛЛЫ В ЭКОССИСТЕМАХ»
Краткая характеристика наиболее распространенных тяжелых металлов
Классы опасности
- 1 – As, Cd, Hg, Pb, Se, Zn, F (высоко опасные);
- 2 – B, Co, Ni, Mo, Cu, Cr (умеренно опасные);
- 3 – Ba, W, Mn, Sr (мало опасные).
Кадмий
- Атомная масса – 112,4.
- Серебристо-белый мягкий металл.
- В почвенном растворе присутствует в виде Cd2+.
- Подвижен в кислой среде.
- Концентрация в литосфере n*10-5%.
- Присутствует вместе с цинком в карбонатных и сульфидных рудах.
- Концентрируется в глинистых осадках и сланцах.
- Концентрация в магматических и осадочных породах – 0,3мг/кг.
Применение
- - гальванические покрытия;
- - красители;
- - стабилизаторы пластмасс;
- - электрические аккумуляторы;
- - кадмиевые покрытия рентгеновских экранов.
Свинец
- Атомная масса – 207,2.
- Мягкий пластичный синевато-серый металл.
- В природе существует в виде минералов галенита (PbS), англезита (PbSO4).
- Образует минералы, плохо растворимые в природных водах.
- Массовая доля в земной коре – 1,25*10-3%.
Применение
- - в производстве аккумуляторов,
- - в производстве красителей,
- - оболочка для кабелей и проводов,
- - свинцовые изделия служат экраном от радиоактивного загрязнения.
Медь
- Атомная масса – 63,5.
- Тягучий металл светло-розового цвета.
- Обладает высокой тепло- и электропроводностью.
- Образует оксиды: Cu2O, CuO, Cu2O3.
- В почве взаимодействует с органическими и минеральными соединениями.
- Массовая доля в земной коре – 0,005%.
- В природе существует в виде оксидных (куприт Cu2O) и сульфидных руд (медный колчедан CuFeS2).
Природные источники поступления ТМ в биосферу
Фоновое содержание ТМ в природных водах
Содержание ТМ в природных водах, мкг/л
| Cu | Zn | Cd | As | Sn | Pb | Ti | Cr | Co | Ni |
| 0,5-1,0 | 0,5-15 | 0,11-0,20 | 0,02-0,1 | 0,009 | 3 | 1-4000 | 0,05-2 | 0,05-0,1 | 1-3 |
Факторы, увеличивающие содержание Cu в почве
- - высокое содержание минералов тяжелой фракции и глинистых минералов;
- - тяжелый механический состав;
- - содержание коллоидов;
- - наличие органического вещества.
Накопление Cu определяется факторами:
- - адсорбцией;
- - соосаждением;
- - комплексообразованием;
- - микробиологической фиксацией
Распределение Cd по профилю почв

Среднее содержание металлов в водах морей, мкг/л
| Море | Fe | Cu | Zn | Pb |
| Балтийское | 4,7-8,6 | 1,0-8,9 | 11-35 | 2,1-26 |
| Черное | 4,0-20 | 2,6-6,1 | 0,7-4,0 | 0,1-1,32 |
| Каспийское | 4,2-7,3 | 0,6-6,1 | 22-64 | 1,6-3,8 |
Биологические барьеры обусловлены поглощением элементов организмами и гумусовыми веществами.
Механические барьеры обусловлены изменением скорости движения вод или воздуха, связанное:
со структурой почв,
плотностью сложения,
пористостью,
гранулометрический состав.
Физико-химические барьеры выявляются в зависимости от главного фактора, обусловливающего аккумуляцию мигрирующих веществ. Подразделяются на классы:
- окислительный,
- восстановительный,
- сульфидный,
- карбонатный,
- кислотный,
- щелочной,
- адсорбционный,
- испарительный,
- термодинамический.
Ряды коэффициентов концентрации
При однократном внесении осадков:
Zn>Ag>Cu>Cr>Ni>Mo>Co>Pb
(для органической системы удобрения)
Cu>Ni>Cr>Mo>Zn>Ag
(для органоминеральной системы удобрения)
При повторном внесении осадков:
Ag>Zn>Cu>Cr>Ni>Co>Zr>Pb
(для органической системы удобрения)
Ag>Cu>B>Zn>Cr>Mo>Sn>Ag
(для органоминеральной системы удобрения)
По влиянию на уровень почвенного загрязнения комплексом элементов, входящих в состав ОСВ, системы удобрений располагаются в ряд:
органоминеральная>минеральная>органическая
По влиянию на уровень почвенного загрязнения комплексом элементов, входящих в состав ОСВ, системы удобрений располагаются в ряд:
органоминеральная>минеральная>органическая
Как устанавливаются дозы внесения ОСВ?
| Оценка ила | ПДК | |||
| Zn | Cu | Ni | Cr | |
| Пригоден для частого использования | <1500 | <750 | <100 | <1500 |
| Только редкое использование | 1500-3000 | 750-1500 | 100-200 | 1500-3000 |
| Опасен при использовании даже в малых дозах | >3000 | >1500 | >200 | >3000 |
Нормирование содержания тяжелых металлов в кормах и продукции животноводства
Методика 1.
- Коэффициент перехода ТМ из корма в молоко:
КПi = Сi(M)/Сi(К),
- где КПi - коэффициент перехода i-го элемента из 1 кг корма в 1 л молока;
- Сi(М) - концентрация i-го элемента в молоке, мг/л;
- Сi(К) - концентрация i-го элемента в 1 кг корма, мг/кг.
- ПДК ТМ в рационе коров:
ПДКi (К) = ПДКi(М)/КПi
где ПДКi - предельно допустимая концентрация i-го элемента в рационе, мг/кг;
ПДКi(М) - предельно допустимая концентрация i-го элемента в молоке, мг/л;
ПКi - коэффициент перехода i-го элемента из 1 кг корма (рациона) в 1 л молока.
Предельно допустимые концентрации в рационе лактирующих коров:
0,23-0,38 мг/кг (Рb), 0,5-0,83 мг/кг (Ni),
0,76-1,25 мг/кг (Cr) и 0,16-0,50 мг/кг (Cd).
- ПДК ТМ в почве:
ПДКi(П) = ПДКi(К)/КПi
- где ПДКi(П) - предельно допустимая концентрация i-го элемента в почве, мг/кг;
- КПi - коэффициент перехода i-го элемента из почвы (из 1 кг) в 1 кг корма (рациона).
Растения - гипераккумуляторы тяжелых металлов. Методы фиторемедиации.
Фиторемедиация стала эффективным и экономически выгодным методом очистки окружающей среды только после того, как обнаружили растения-гипераккумуляторы тяжелых металлов, способные накапливать в своих листьях до 5% никеля, цинка или меди в пересчете на сухой вес - то есть в десятки раз больше, чем обычные растения. Биологическое значение этого феномена еще до конца не раскрыто: можно, например, предположить, что высокое содержание токсичных элементов защищает растения от вредителей и делает их более устойчивыми к болезням.
Использовать гипераккумуляторы для очистки почвы и воды предложили еще в начале 80-х годов. Однако до практики было еще далеко -во-первых, потому, что биомасса этих растений была невелика, а во-вторых, потому, что не была разработана технология их выращивания. Растения слабо усваивают многие тяжелые металлы - например, тот же свинец - даже при их высоком содержании в почве из-за того, что они находятся в виде малорастворимых соединений. Поэтому концентрация свинца в растениях обычно не превышает 50 мг/кг, и даже индийская горчица, генетически предрасположенная к поглощению тяжелых металлов, накапливает свинец в концентрации всего 200 мг/кг, даже если растет на почве, сильно загрязненной этим элементом.
Проблему удалось решить, когда обнаружили, что поступление тяжелых металлов в растения стимулируют вещества (например, этилендиаминтетрауксусная кислота), образующие с металлами в почвенном растворе устойчивые, но растворимые комплексные соединения. Так, стоило внести подобное вещество в почву, содержащую свинец в концентрации 1200 мг/кг, как концентрация тяжелого металла в побегах индийской горчицы возрастала до 1600 мг/кг.
Механизмы очистки воды с помощью корней и проростков могут быть разными. При удалении свинца главную роль играет, возможно, образование нерастворимых соединений и ионная сорбция. Так, на корнях индийской горчицы, находящихся в воде, образуется нерастворимый слой, который состоит преимущественно из карбоната свинца; такой же слой образуется и на корнях кукурузы. Вместе с тем свинец может связываться и с пектиновой фракцией клеточных стенок, обладающей ионообменными свойствами.
Возможность очистки почвы и воды от радионуклидов с помощью проростков подсолнечника была успешно продемонстрирована на территории бывшего завода по обогащению урана в США, в штате Огайо, а также на Украине, на небольшом водоеме в километре от четвертого реактора Чернобыльской АЭС. Концентрация урана в растениях в тридцать тысяч раз превышала его концентрацию в почве и воде, а для цезия-137 и стронция-90 эта величина составила восемь и две тысячи раз соответственно.
Дальнейшего развития методов фиторемедиации можно ожидать после того, как методами генной инженерии будут созданы растения, способные более эффективно, чем известные виды, концентрировать тяжелые металлы.
Осадки сточных вод как основной источник загрязнения природных компонентов тяжелыми металлами.
При однократном внесении осадков:
Zn>Ag>Cu>Cr>Ni>Mo>Co>Pb
(для органической системы удобрения)
Cu>Ni>Cr>Mo>Zn>Ag
(для органоминеральной системы удобрения).
При повторном внесении осадков:
Ag>Zn>Cu>Cr>Ni>Co>Zr>Pb
(для органической системы удобрения)
Ag>Cu>B>Zn>Cr>Mo>Sn>Ag
(для органоминеральной системы удобрения).
По влиянию на уровень почвенного загрязнения комплексом элементов, входящих в состав ОСВ, системы удобрений располагаются в ряд:
органоминеральная>минеральная>органическая.
По влиянию на валовое содержание элементов системы удобрений располагаются в ряд:
органоминеральная>минеральная>органическая.
Как устанавливаются дозы внесения ОСВ?
1. Zn-Эквивалент=8CNi+2CCu+CZn.
ПДК этих элементов по Zn-Эквиваленту составляет 250 мг/кг.
| 2. Оценка ила | ПДК | |||
| Zn | Cu | Ni | Cr | |
| Пригоден для частого использования | <1500 | <750 | <100 | <1500 |
| Только редкое использование | 1500-3000 | 750-1500 | 100-200 | 1500-3000 |
| Опасен при использовании даже в малых дозах | >3000 | >1500 | >200 | >3000 |
Нормирование содержания тяжелых металлов в кормах и продукции животноводства.
Методика 1.
Коэффициент перехода ТМ из корма в молоко:
КПi = Сi(M)/Сi(К),
где КПi - коэффициент перехода i-го элемента из 1 кг корма в 1 л молока;
Сi(М) - концентрация i-го элемента в молоке, мг/л;
Сi(К) - концентрация i-го элемента в 1 кг корма, мг/кг.
ПДК ТМ в рационе коров:
ПДКi (К) = ПДКi(М)/КПi
где ПДКi - предельно допустимая концентрация i-го элемента в рационе, мг/кг;
ПДКi(М) - предельно допустимая концентрация i-го элемента в молоке, мг/л;
ПКi - коэффициент перехода i-го элемента из 1 кг корма (рациона) в 1 л молока.
Предельно допустимые концентрации в рационе лактирующих коров:
0,23-0,38 мг/кг (Рb), 0,5-0,83 мг/кг (Ni),
0,76-1,25 мг/кг (Cr) и 0,16-0,50 мг/кг (Cd).
ПДК ТМ в почве:
ПДКi(П) = ПДКi(К)/КПi
где ПДКi(П) - предельно допустимая концентрация i-го элемента в почве, мг/кг;
КПi - коэффициент перехода i-го элемента из почвы (из 1 кг) в 1 кг корма (рациона).
Методика 2.
Методика 2 отличается от Методики 1 учетом вклада тяжелых металлов от конкретного кормового продукта в рацион:
ПДСi=ПДКi в молоке, мясе/Кni*100%,
где ПДСi - предельно допустимое содержание i-го тяжелого металла в рационе животного, мг;
ПДКi - предельно допустимая концентрация i-го тяжелого металла в молоке, мясе, мг/л (кг),
Кni - количественная характеристика перехода i-го тяжелого металла из рациона в 1 л (кг) молока и мяса, % введенного количества с рационом.
С учетом ПДС тяжелых металлов в рационе, вклада отдельных кормов в его суммарное загрязнение рассчитывается допустимая концентрация тяжелого металла в отдельном кормовом продукте:
ПДКi = ПДСi *А/Мi,
где ПДКi - предельно допустимая концентрация тяжелого металла в кормовом продукте, мг/кг, вносимая в рацион животного с конкретным кормом,
Мi - масса i-го кормового продукта в рационе, кг,
А - доля i-го тяжелого металла, вносимая в рацион животного с конкретным кормом.
Пробоотбор тяжелых металлов в осадках.
Установка для отбора проб твердых (а)
и жидких (б) осадков
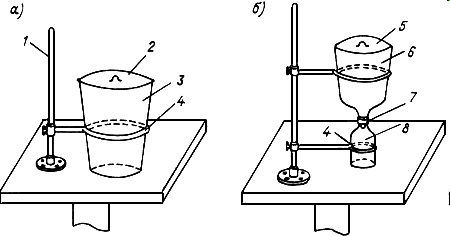
1 - штатив; 2, 5 - крышка; 3 - полиэтиленовое ведро; 4 - кольцо держателя; 6 – полиэтиленовая воронка (диаметр 23 см); 7 - навинчивающаяся крышка; 8 - полиэтиленовая колба.
Пробоотбор ртути в осадках и в воздухе
Основными антропогенными источниками ртути являются сжигание ископаемых топлив, предприятия по сжиганию отходов и крематории.
Пробы на ртуть отбираются в отдельный осадкосборник. В качестве материала воронок и осадкосборных бутылок могут быть использованы боросиликатное стекло и тефлон.
Осадки могут быть отобраны либо с помощью широкогорлых бутылей, либо используя воронки с приемными бутылками. Пробоотборник может быть постоянно открытым или автоматическим, который открывается только на время осадков. Для целей мониторинга вполне приемлемыми могут быть постоянно открытые осадкосборники на основе воронок и приемных бутылок.
Автоматические пробоотборники используются Национальной программой мониторинга Германии, Национальной программой атмосферных выпадений США, а также исследовательскими группами, работающими в районе Великих озер.
Автоматические пробоотборники имеют то преимущество, что они позволяют избежать влияния сухих выпадений частиц, хотя вклад газообразных и аэрозольных форм ртути в поток мокрых выпадений вне городов и индустриальных центров скорее всего не велик.
При продолжительных периодах пробоотбора необходимо предотвратить диффузию в отбираемую пробу осадков, поскольку она может дать вклад в содержание ртути в пробе за счет окисления в водорастворимые формы. Это легко сделать, используя капиллярную трубку между воронкой и осадкосборной бутылкой. Необходимо также защитить осадкосборную бутылку от света во избежание фотоиндуцированного восстановления ртути в отбираемой пробе осадков.
Пробоотборники должны обеспечивать работу во все сезоны года и во всех климатических условиях. Должен быть предусмотрен нагреватель для растапливания снега и для предотвращения образования льда в воронке и бутылке в зимнее время. В зависимости от климатических условий может быть полезным охлаждать отбираемую пробу в районах с высокими температурами летом. Площадь воронки и объем бутылки должны меняться от сезона к сезону, чтобы соответствовать используемому периоду пробоотбора.
Метод двойной амальгамации
Забор воздуха должен выполняться на высоте более 1,5 м над землей и на таком же расстоянии от других поверхностей (например, стен), чтобы избежать влияния локальных завихрений воздуха. Отбор суммарной газообразной ртути (TGM) из воздуха обычно производится с использованием ловушки из золота и газового счетчика (или расходомера) для определения объема воздуха.. Автоматический метод и ручной метод пробоотбора дают сравнимые результаты.
Ловушка из золота представляет собой 10-12 см трубку из кварцевого стекла, наполненную золотым адсорбентом. Золотым адсорбентом могут быть либо короткие обрезки (1-2 мм) золотой проволоки диаметром 1 мм в смеси с кварцевой крошкой как носителем, либо стеклянной (кварцевой) крошкой, покрытой тонким слоем золота. Последний вариант дает, как правило, более низкие бланковые значения.
Пробоотборная система состоит из одного защитного фильтра из кварцевой ваты и двух последовательных золотых ловушек. Метод отбора и измерения проб суммарной газообразной ртути (включая элементарную, органическую и неорганическую) основан на образовании амальгамы ртути с золотом. Суммарная газообразная ртуть захватывается поверхностью золота. При отборе две ловушки соединяются последовательно. При такой комбинации отмечается значительный проскок ртути через первую ловушку и захват существенного количества второй ловушкой.
Газообразная ртуть, отобранная с помощью золотой ловушки на станции, переносится в калиброванную золотую ловушку при пропускании газа-носителя со скоростью 30 мл/мин. Таким газом служит свободный от ртути чистый аргон (чистота >99.998%).
Предварительная обработка пробы
Перед анализом пробы на содержание ртути, уловленное золотой ловушкой, рекомендуется выполнить этап высушивания ловушки. Небольшое количество паров воды может сконденсироваться на поверхности золота и может помешать дальнейшему анализу. Для высушивания золотые ловушки нагреваются до 40-50°C и в течение 5-10 мин продуваются сухим азотом. Потери ртути при этом не происходит.
Анализ
Анализ проб воздуха на ртуть проводится обычно двойной амальгамацией. В этой процедуре золотая ловушка устанавливается в потоке газа (очищенный от ртути аргон) последовательно со второй аналитической ловушкой и далее с детектором CVAFS. Нагревание происходит с помощью нихромовой проволоки. На первом этапе ртуть термически десорбируется из первой пробоотборной ловушки и улавливается второй аналитической ловушкой. Затем вторая ловушка быстро нагревается, и ртуть поступает в прибор CVAFS.
Выполняются следующие аналитические этапы:
1. Термическая десорбция с полевой рабочей ловушки в аналитическую ловушку: 500ºC в течение 4 минут, поток газа 30 мл/мин;
2. Термическая десорбция с аналитической ячейки в детектор прибора AFS: 800ºC в течение 25 сек, поток газа 30 мл/мин;
3. Расчет содержания суммарной ртути в пробе: по площади пика выходного сигнала.
Темы семинарских занятий
Составление таблицы «Биогеохимические свойства тяжелых металлов».
- Природные и антропогенные источники поступления тяжелых металлов в окружающую среду.
- Построение схемы, иллюстрирующей миграционные процессы металлов в биогеоценозах.
- Расчет коэффициентов для описания и оценки подвижности элементов в биосфере, поведения их соединений на локальном, региональном и глобальном уровнях.
- Биологическая роль тяжелых металлов. Естественные механизмы детоксикации.
- Фиторемедиация земель, загрязненных тяжелыми металлами.
ТМ в агроэкосистемах
В связи с постоянным ростом темпов химического воздействия человека на биосферу происходит локальное, региональное и глобальное загрязнение природной среды различными токсическими веществами, в том числе и тяжелыми металлами.
В районах размещения крупных промышленных предприятий содержание металлов в природных объектах превышает природный уровень в десятки и сотни раз. Ареалы распространения техногенных выбросов вокруг промышленных комплексов охватывают площадь 18 млн. га, что составляет около 1% общей площади Российской Федерации [30]. Площадь почвенного покрова, загрязненного ТМ, составляет по ориентировочным оценкам 3,6 млн. га. Более 1 млн. га почв сельскохозяйственных угодий загрязнено особо токсичными элементами (I класс опасности) и около 2,3 млн. га – токсичными (II класс опасности) [28].
Источники поступления тяжелых металлов в агроэкосистемы можно представить в виде следующей схемы
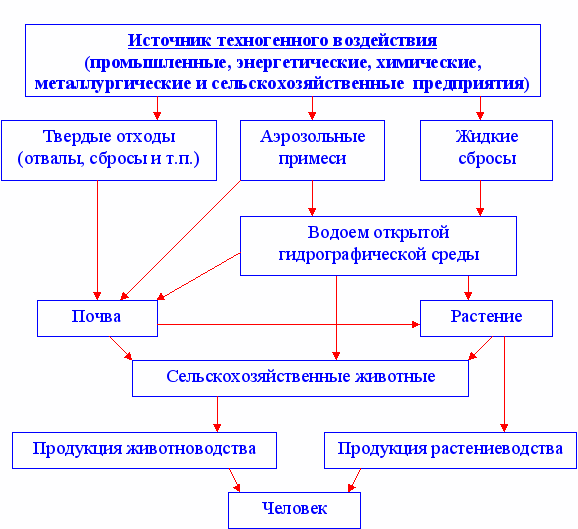
Правовая основа
На данный момент ПДК ТМ для различных типов почв не разработаны, но существуют «Гигиенические нормативы ГН 2.1.7.2041-06», согласно которым установлены ориентировочно допустимые концентрации ТМ в почвах в зависимости от механического состава и кислотности почв (так, например, для нейтральных суглинистых и глинистых почв ОДК (с учетом фона). Существуют также СанПиН 2.3.2.1078-01 (СанПиН 2.3.2.560-96) «Гигиенические требования безопасности и пищевой ценности пищевых продуктов», в которых установлены допустимые уровни содержания токсичных элементов в пищ.продуктах.
Система земледелия
Система земледелия - это комплекс взаимосвязанных агротехнических, мелиоративных и организационных мероприятий, направленных на эффективное использование земли, сохранение и повышение плодородия почвы, получение высоких и устойчивых урожаев сельскохозяйственных культур.
Составными частями системы земледелия как научно-обоснованного комплекса мероприятий являются:
агротехническая организация территории хозяйства и система севооборотов;
система обработки почвы;
система удобрений;
система мероприятий по борьбе с сорняками, вредителями и болезнями растений;
система противоэрозийных и мелиоративных мероприятий; система семеноводства;
индустриальные технологии выращивания сельскохозяйственных культур; природоохранные мероприятия.
В условиях техногенного загрязнения необходимо организовать земледелие таким образом, чтобы производимая продукция удовлетворяла установленным санитарно-гигиеническим нормативам СанПиН 2.3.2.1078-01. Для этого при разработке систем земледелия нужно учитывать следующие факторы:
- источник загрязнения, вид загрязнителя;
- основные пути воздействия загрязняющих веществ;
- уровни и масштабы загрязнения почв сельскохозяйственных угодий;
- неравномерность загрязнения сельскохозяйственных угодий;
- характеристики почвенного покрова;
- особенности сельскохозяйственных культур и технологий их возделывания;
- особенности миграции загрязнителя в системе почва-растение;
- эффективность применения защитных мероприятий.
Загрязнение сельскохозяйственных угодий химическими токсикантами
Техногенные выбросы в атмосферу от промышленных источников и транспорта распространяются на прилегающую территорию, являясь одним из основных путей поступления загрязняющих веществ на сельскохозяйственные угодья. Практически во всех промышленно развитых районах Российской Федерации отмечается загрязнение почв тяжелыми металлами. Наиболее высокая степень загрязнения характерна для территорий, прилегающих к крупным многофункциональным городам с приоритетом металлургического производства, химической промышленности и машиностроения. Зоны загрязнения сельскохозяйственных угодий отмечаются в районах расположения многих отдельных городов, таких как Новосибирск, Магнитогорск, Омск, Киров и др. Зоны влияния промышленных агломераций простираются на сотни километров: Московской - 200 км, Тульской -120 км, Среднеуральской - 300 км, Кемеровской -200 км.
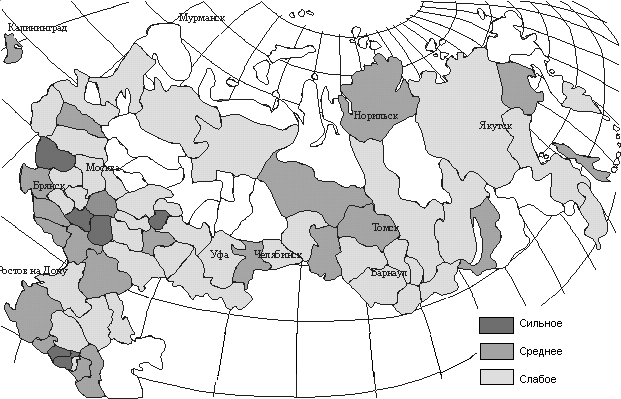
Воздействие выбросов тяжелых металлов носит ярко выраженный региональный характер, причем состав выбросов значительно отличается для различных субъектов Российской Федерации (рис. 1.2).
 А)
А)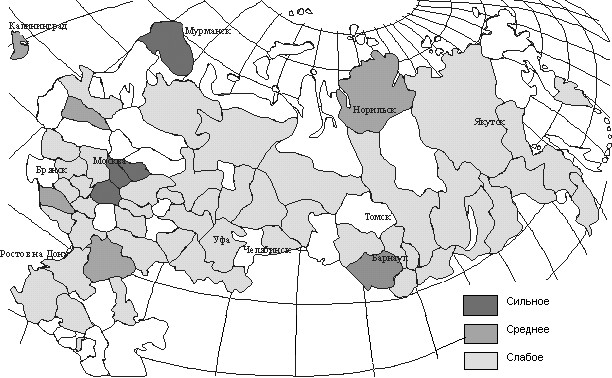 Б)
Б)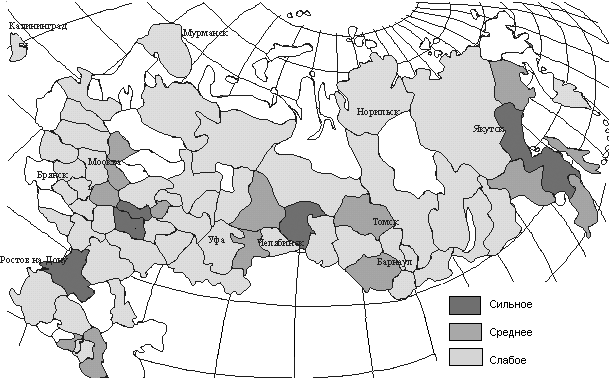 С)
С)Рис. 1.2. Распределение территории Российской Федерации по степени загрязнения приземного слоя атмосферы тяжелыми металлами (А – медь, Б – никель, С – свинец)
Наиболее опасными элементами по масштабам и объемам выбросов являются свинец и цинк среди элементов I класса опасности, а II класса – никель и медь (рис. 1.3.). В настоящее время от антропогенных источников загрязнения в почву поступает от 70% до 95% всех тяжелых металлов. Зоны, в которых содержание тяжелых металлов в почвах сельскохозяйственных угодий в десятки и сотни раз превышают ПДК, отмечаются в Кемеровской, Белгородской, Челябинской и в других областях. Средними уровнями загрязнения характеризуются районы с преобладанием металлургии и машиностроения в европейской части России, Западной Сибири и Дальнего Востока. Низкой степенью загрязнения отличаются курортные зоны, территории заповедников, регионы с низкой степенью развития промышленности.
Районы РФ, загрязненные ТМ выше ПДК.
Северный экономический район. Загрязнения почв тяжелыми металлами выше ПДК отмечается в Мурманской и Архангельской областях.
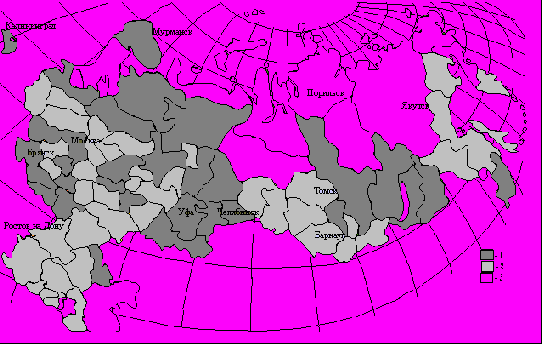
Рис. 1.3. Карта-схема загрязнения пахотных почв Российской Федерации химическими веществами I и II класса опасности. 1 – превышение ПДК (ОДК) по отдельным элементам I класса;
2 – по всем элементам ниже ПДК (ОДК); 3 – не обследованные территории
Северо-Западный экономический район. Загрязнение почв свинцом и цинком выше ПДК обнаружено в Ленинградской и Калининградской областях, а кадмием и цинком - в республике Коми.
Центральный экономический район. Повышенное содержание ТМ в почвах отмечено в 4 областях: Московской, Смоленской, Тульской и Брянской.
Центрально-Черноземный район. Наиболее загрязненные почвы находятся в Липецкой области, около 10% обследованных площадей имеют превышение ПДК по мышьяку.
Волго-Вятский район. Около 10% обследованных площадей загрязнено выше ПДК по мышьяку в Вологодской области, а по никелю - в Кировской области. Приблизительно столько же площадей загрязнено в Мордовии свинцом, хромом, цинком и медью.
Поволжский экономический район. Площадь земель с превышением ПДК составляет менее 1% от обследованных. Загрязненные угодья обнаружены в Ульяновской и Астраханской областях.
Северо-Кавказский район. Данный регион является относительно благополучным по загрязнению ТМ. Практически нигде не обнаружено превышение ПДК.
Уральский экономический район. Наибольшее загрязнение почв наблюдается в Челябинской, Свердловской областях. В меньшей степени загрязнена Оренбургская область. В остальных областях и республиках региона не отмечено превышения содержания тяжелых металлов в почвах, обследованных сельскохозяйственных угодий.
Западно-Сибирский экономический район. В этом регионе загрязненные сельскохозяйственные угодья отмечены только в Кемеровской области, где их доля составляет около 2% от обследованных.
Восточно-Сибирский и Дальневосточный экономический районы. Читинская область, Бурятия и Приморский край являются одними из самых загрязненных регионов, где превышение ПДК по свинцу наблюдается на более чем 10% обследованных территорий.
Во всех регионах с повышенным содержания тяжелых металлов в почвах отмечается и наличие в них вредных органических веществ, также содержащихся в выбросах предприятий промышленности и энергетики. Значительная часть сельскохозяйственных угодий загрязнена вредными органическими веществами сельскохозяйственного происхождения. Общая площадь химически и биологически загрязненных земель в зонах расположения крупных животноводческих комплексов и птицефабрик превышает 2.2 млн. га. Одним из наиболее токсичных газообразных выбросов энергоустановок является сернистый ангидрид SO2, который в присутствии кислорода доокисляется до SO3. При соединении с водой эти окислы образуют серную и сернистую кислоты, которые, оседая на землю в составе «кислотных дождей», наносят вред растениям, подкисляют почву, ускоряют процесс коррозии металлов, обостряют заболевания дыхательных путей человека и сельскохозяйственных животных.
Методы определения ТМ.
Пробоотбор при контроле загрязнения почв.
ТМ накапливаясь в почве в больших концентрациях становятся токсичными для растений, животных и человека. Для ТМ в принципе не существует механизмов самоочищения – они лишь перемещаются из одного природного резервуара в другой.
Трансформация соединений ТМ в почве и поступление в растения является сложной функцией, зависящей от многих переменных:
-состава почвы,
-свойств самих металлов,
-почвенно-экологических условий роста и развития растений,
-форма соединения металла в почве. Знание форм соединений металлов в почве имеет большое значение в изучении их поведения в различных компонентах биосферы, в разработке приемов и методов снижения фитотоксичности ТМ и восстановления плодородия загрязненных почв.
Биологическая доступность ТМ растениями в значительной степени определяется процессами взаимодействия их с почвой, прочностью закрепления в поглощенном состоянии. Наиболее благоприятные условия для интенсивной миграции ТМ по биологической цепи почва–растение складываются на дерново-подзолистых почвах Нечерноземной зоны. Для прогнозирования накопления ТМ в сельскохозяйственных культурах необходимо знать кинетику их поступления в растение из почвы, которая зависит прежде всего от содержания в почве тех форм, которые доступны растениям.
Соединения металлов по доступности растениям объединяют в три группы [17]:
– мобильные соединения, непосредственный резерв питания растений; к ним относятся водорастворимые, ионно-обменные, подвижные формы;
– потенциальный резерв, к которому относят прочнофиксированные соединения, требующие энергии активации для перевода в первую группу;
– стратегический резерв – формы соединений, недоступные для растений без разрушения сорбента.
Загрязнение почв ТМ изменяет численность и состав микробного сообщества, снижает интенсивность микробиологических процессов и активность почвенных ферментов. Все это ведет к снижению плодородия почв.
Обеспечение получения в загрязненных районах экологически безопасных продуктов питания, соответств.сан.гигиен.нормативам, становится приоритетным для всех стран мира. Для решения этой задачи необходимо проведение комплекса защитных мероприятий по снижению транслокации ТМ из почвы в растение.
Для разработки мероприятий по улучшению качества сельскохозяйственной продукции и понимания механизмов поглощения токсикантов растениями из почвы необходимо: располагать данными о формах нахождения ТМ в почве, показателях биологической активности почвы, накоплении ТМ в растениеводческой продукции, влиянии на продуктивность сельскохозяйственных культур.
Достоверность экспериментальных данных, являющихся основой большинства научных и практических исследований по изучению загрязнения биосферы токсическими веществами, в значительной степени обусловлена правильностью отбора проб.
Отбор проб с целью контроля содержания ТМ
- обследование больших тер-ий
При контроле загрязнения почв сельскохозяйственных угодий в каждом хозяйстве обследуется 3–5 полей, занятых основными культурами. Размер пробной площадки при однородном почвенном покрове колеблется от 1 до 5 га, а при неоднородном от 0,5 до 1 га. С каждой из этих площадок отбирают по 1-ой объединенной пробе не менее 1 раза в три года. На пахотных почвах точечные пробы отбирают на глубину до 25 см через интервалы 0–5, 5–10, 10–20 (25) см [17].
- локальный источник загрязнения
На сельскохозяйственных территориях с локальным загрязнением применяют систему концентрических окружностей, расположенных на определенных расстояниях от источника загрязнения в зависимости от площади загрязнения, указывая номера окружностей и азимут места отбора проб. В направлении основного распространения загрязняющих веществ в соответствии с «розой ветров» систему концентрических окружностей продолжают в виде сегмента, размер которого зависит от степени распространения загрязнения.
Независимо от ветрового режима пробы почв пахотного и подпахотного горизонтов отбирают по четырем румбам в следующих точках:
0,5–1,5 км,
2) 2–3 км,
3) 5–6 км от источника загрязнения.
При загрязнении обширной территории отбор проб проводят на расстоянии 10, 20, 30 км от источника загрязнения по оси переноса, обратной «розе ветров» (по доминирующему направлению разноса выброса).
Почвенные образцы необходимо отбирать на расстоянии 150–200 м от крупных автомагистралей и 50 м от проселочных дорог.
Объединенные пробы почвы, отобранные с участков, должны быть представительными. Площадки для отбора проб почвы должны быть размером 100х100 м или 100х200 м, и объединенные пробы должны составляться из единичных проб почвы, отобранных методом конверта (четыре точки в углах площадки и одна в центре). Вокруг каждой из пяти точек делается еще по четыре прикопки. Пробы почвы на целине необходимо отбирать на глубину 0–5 см, на пашне – 0–20 см (или на глубину пахотного горизонта).
Из объединенной пробы путем тщательного перемешивания составляют смешанный образец массой около 1 кг. Образцы почвы высушивают до воздушно-сухого состояния в сушилке почвенных проб с подогревом воздуха не выше 40 оС или в хорошо вентилируемом помещении при комнатной температуре. Высушенные образцы измельчают на почвенном пробоизмельчителе или в ступке и просеивают через сито с круглыми отверстиями диаметром 1–2 мм. Подготовленные почвенные образцы хранят в коробках или пакетах. Из полученнной пробы почвы берется навеска 1–2 г. тонкорастертой (до пудры) и прокаленной в течении 2–3 часов при 450–500 оС почвы. Её помещают в тефлоновый стаканчик объемом 30–50 мл и смачивают несколькими каплями бидистиллированной воды.
Далее используется универсальный способ разложения почв и других силикатных минералов смесью HCl + HNO3 + HF с конечным растворением остатка в разбавленной HNO3 для определения многих макро- и микроэлементов для различных целей [12]. Разложение проб проводят по следующей схеме: к 0,5–1 г прокаленной и смоченной бидистиллированной водой почве во фторопластиковом стаканчике приливают 3–5 мл «царской водки» (смеси концентрированных HCl и HNO3 в соотношении 1:3 по объему) и 10 мл HF, стаканчик медленно нагревают на этернитовой плитке, выпаривая содержимое до влажных солей. Обработку почвы HF повторяют 2–3 раза. Для удаления фтора сухой остаток обрабатывают концентрированной HNO3, окапывая содержимое стаканчика и выпаривая досуха (операцию повторяют 2 раза). К остатку в стаканчике приливают 10 мл разбавленной HNO3, нагревают до кипения и фильтруют в колбу на 25–50 мл. Стаканчик и фильтр несколько раз промывают 0,5н раствором HNO3, колбу доводят до метки раствором HNO3, который используется для определения элементов. В неразбавленном растворе определяют валовое содержание Mn, Zn, Cu, Co, Ni, Pb, Cd, Ba, Sr.
Определение форм нахождения ТМ в почве
Для определения массовой доли подвижных форм металлов в почвах применяется экстракция почвы при комнатной температуре (обычно 25 С) буферным раствором ацетата аммония (рН=4,8) в течение 24 часов и соотношении почва : раствор = 1 : 10 с последующим разделением фаз фильтрованием или центрифугированием [13, 14]. В вытяжках из почв ТМ определяют методом атомно-абсорбционной спектроскопии.
Для определения обменных форм соединений ТМ в почвах определяют после вытеснения их 1 М раствором ацетата аммония (рН 6,5-7).
Для определения подвижной, кислоторастворимой и труднодоступной (прочносвязанной) форм Cd, Cu, Zn определяли в вытяжках, полученных при параллельной экстракции почв 1М растворами CH3COONH4 (pH 4.8), HCl и 3М раствором HCl при соотношении фаз 1 : 10 и времени контакта 1 сутки (Методические указания…, 1985 [38]). Для этого в навески воздушно-сухой почвы массой 10 г помещали в центрифужные пробирки объемом 60 мл и приливали 50 мл 1М раствора ацетатно-аммонийного буфера. Центрифужные пробирки закрывали крышкой и выдерживали суспензию в термостате при температуре 250С в течение суток, после чего раствор отделяли от осадка фильтрованием, не перенося почву на фильтр. В пробирки приливали еще 50 мл раствора ацетатно-аммонийного буфера и проводили фильтрование с полным перенесением почвы на фильтр. Параллельно проводилась почвенная экстракция 1М, а затем и 3М раствором HCl. Для этого к помещенной в центрифужные пробирке навеске почвы массой 5 г приливали 50 мл 1М HCl, выдерживали суспензию в течении суток и отделяли жидкую фазу фильтрование с перенесением все почвы на фильтр. До анализа растворы хранили в полиэтиленовых флаконах с плотно закрывающейся крышкой. В вытяжках из почв Cd, Zn и Cu определяли методом атомно-абсорбционной спектроскопии.
Определение потенциальной активности дыхания почвы производили на газовом хроматографе модель 3700 (с использованием детектора по теплопроводности - катарометра). Интенсивность дыхания почвы характеризует процессы минерализации органического вещества.
Берется навеска 5 г почвы (воздушно-сухой, просеянной через сито 1 мм) и помещается в колбу, объемом 15 мл. Затем к дерново-подзолистой почве добавляют 1,3 мл воды (производят увлажнение почвы до оптимального уровня – 60% от полной полевой влагоемкости или 90% от наименьшей общей влагоемкости почвы). Колбы закрывают ватными пробками и далее производят инкубацию в термостате при температуре 28 оС в темноте в течение 3–7 суток. Затем добавляют 2,5 мг глюкозы на 1 г почвы, вновь увлажняют, добавляя до 1 мл дистиллированной воды, закрывают резиновой пробкой и ставят в термостат на 1 час при температуре 28 оС. После ведут анализ газовой пробы на хроматографе. Активность дыхания почвы выражают в количестве мг СО2, выделяемого 1 кг почвы за сутки.
Потенциальная активность денитрификации почвы. Денитрификация – микробиологический процесс, играющий важную роль в азотном балансе почвы.
Навеску в 5 г почвы помещают в колбу объемом 15 мл, добавляют 1,3 мл воды и инкубируют в термостате при температуре 28 оС в течении 3–7 суток. Затем вносят 5 мл водного раствора глюкозы (2,5 мг глюкозы на 1 г почвы) и KNO3 (0,4 мг на 1 г почвы). Колбы закрывают резиновыми пробками, фиксируют стальными зажимами и замещают воздух в колбах инертным газом при давление 1 атм. в течение 30 с. В каждую колбу добавляют 1 мл ацетилена, предварительно отобрав из колбы адекватный объем газа. Колбу встряхивают в течение 30–60 с, переворачивают пробкой вниз и инкубируют при температуре 28 оС в течение 24 ч. После производят анализ газовой пробы на газовом хроматографе. Перед началом анализа флаконы встряхивают. Активность денитрификации выражают в количестве N2O, выделяемой 1 кг почвы за сутки.
Если определяли активность ферментов каталазы, дегидрогеназы и инвертазы в почве, то желательно кратко указать методики определения ферментов (по книге Минеева, распечатанные методики находятся у А.Н. Кроме того, именно здесь стоит указать на то, что каталаза разлагает в почве ядовитую перекись водорода на воду и кислород, дегидрогеназа связана с процессом дыхания почвы, а инвертаза – сахаролитический фермент (разлагает в почве сахарозу на глюкозу и фруктозу). (НЕ РАССКАЗЫВАЛА!!!)
пробоотбор растений
Пробы растений отбирают на тех же участках, что и пробы почв. Для получения объединенной группы растений массой 0,5–1 кг натуральной влажности рекомендуется отбирать не менее 8–10 точечных проб.
Точечные пробы растительного материала промывают дистиллированной водой, высушивают при комнатной температуре или в сушильном шкафу при t=40–50 оС до воздушно-сухого состояния, измельчают, отбирают средние пробы и хранят в полиэтиленовых пакетах.
Объединенную пробу составляют либо из всего растения, либо раздельно из стеблей, листьев, плодов.
Для подготовки проб растений, содержащих значительное количество органического вещества, наиболее широко применяют два метода – сухое озоление и мокрое (кислотное) разложение.
Мокрое озоление. При мокром озолении образец обрабатывают концентрированными минеральными кислотами при нагревании до 100–200 оС. Мокрое озоление происходит быстро и при более низких температурах, поэтому уменьшается возможность потерь, связанная с улетучиванием элементов.
Недостаток метода - возможность внесения загрязнений с применяемыми реагентами.
Одним из лучших методов мокрого озоления органических проб является сжигание их в колбах Кьельдаля при кипячении со смесью концентрированных кислот: азотной HNO3 и хлорной HСlO4 в соотношении 3 : 1. Для этого на аналитических весах берут навеску тонко измельченной пробы от 2 до 5 г и переносят ее на дно колбы Кьельдаля емкостью 500–100 мл. Затем добавляют 30 мл смеси кислот. Колбы Кьельдаля ставят в вытяжной шкаф на несколько часов (лучше на ночь), затем приступают к нагреванию. Нагревание производят на специальных плитах с регулируемой температурой. Вначале нагревание должно быть слабым, после прекращения вспенивания нагревание можно усилить, следя затем, чтобы смесь кислот ни в коем случае не выпарилась досуха. В противном случае возможен взрыв, так как хлорная кислота при концентрировании может взрываться в присутствии следов органического вещества. Озоление вещества проводят до тех пор, пока жидкость в колбе станет совершенно прозрачной и почти бесцветной, а в колбе перестанут выделяться красновато-бурые пары оксидов азота.
После этого колбы охлаждают, содержимое количественно переносят в мерную колбу 50–100 мл, доводят до метки бидистиллированной водой. Полученные растворы используют для определения элементов, их можно хранить и транспортировать в плотно закрытой полиэтиленовой посуде [12].
Сухое озоление. Сухое озоление – довольно простой метод, применимый для многих органических проб и имеющий ряд преимуществ: не требуется вносить дополнительные реагенты, которые могут вызывать загрязнение.
Недостаток метода - потери ряда элементов вследствие улетучивания (таких как As, Pb, Cd, Cr и Zn,) поэтому при выборе способа разложения следует учитывать специфику и уровень концентрации определяемого элемента, состав пробы, а также оборудование и техническое оснащение лаборатории.
Для определения сухой минерализации органических веществ, пробу предварительно измельчают и высушивают в кварцевой чашке при температуре 105 оС до постоянной массы. Затем чашку переносят в холодный муфель и нагревают до начала обугливания. Температура муфеля постепенно повышается до 250–300 оС при открытой дверце муфеля, так как очень важно в течении первых стадий озоления обеспечить свободный доступ воздуха к озоляемому материалу. Конечное озоление проводят при температуре 350–400 оС уже при закрытой дверце муфеля до постоянной массы золы. По окончании озоления чашки вынимают из муфеля, охлаждают, взвешивают.
Затем золу смачивают несколькими каплями бидистиллированнной воды и переносят в мерную колбу на 25–60 мл раствором горячей 1н HNO3 [12]. Содержание ТМ в пробе определяли атомно-абсорбционным методом.
3.2.2. Атомно-абсорбционный метод определения ТМ
Этот метод отличается от других аналитических методов универсальностью, простотой выполнения анализа и высокой производительностью. Атомно-абсорбционный метод анализа (ААА) обеспечивает предел обнаружения многих элементов на уровне 0,1–0,01 мкг/мл и ниже, что практически оказывается достаточным для исследований почвы и растений и дает возможность предварительно не концентрировать элементы. Метод позволяет в настоящее время определить до 70 элементов, преимущественно металлов [16].
Недостатком метода является то, что исследуемые пробы должны быть переведены в раствор. Для биологических объектов он особенно ощутим, т.к. процессы предварительного озоления растений сложны, трудоемки, сопряжены с возможной потерей ряда элементов и с загрязнением проб посторонними элементами, внесением элементов, затрудняющих проведение анализа [15].
В основе метода лежит эффект резонансного поглощения излучения определенной длины волны (так называемой резонансной линии) свободными атомами определяемого элемента при прохождении этого излучения через атомный пар излучаемого образца.
Поглощение света свободными атомами описывается законом Бугера-Ламберта-Бера (см.книгу, с.171).
В результате облучения атомного пара светом появляется сравнительно небольшое число линий поглощения. Их называют резонансными (аналитическими) и используют для измерения. Высокая селективность метода, возможность определить нужный элемент в массе других основана на способности свободных атомов поглощать только свойственную данному элементу световую энергию, в результате чего атомы переходят в возбужденное состояние.
В настоящее время в качестве источников резонансного излучения широко используют лампы с полым катодом, в которых излучают возбужденные атомы именно того элемента, который подлежит определению.
Для эффективного поглощения резонансного излучения определяемый элемент, находящийся в исследуемом образце, как правило в виде каких-либо соединений, переводят в элементарное состояние (атомарные пары), при помощи атомизатора за счет высокой температуры (2000-3000 С). Наиболее эффективным способом атомизации является пламя ацетилен-воздух.
Перед проведением анализа исследуемого образца проводят серию измерений стандартных образцов,т.е. растворов определяемого элемента известной концентрации, что необходимо для построения градуировочного графика в координатах «оптическая плотность – концентрация определяемого элемента в растворе».
На рис. 5 представлена упрощенная схема атомно-абсорбционного спектрометра.
2 3
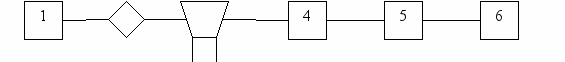
7
