«Санкт-Петербургская государственная педиатрическая медицинская академия»
| Вид материала | Автореферат диссертации |
| Хронические рубцовые стенозы гортани |
- «Санкт-Петербургская государственная педиатрическая медицинская академия», 685.21kb.
- Петербургская Государственная Педиатрическая Медицинская Академия, 194100, улица Литовская,, 26.64kb.
- «Санкт-Петербургская государственная педиатрическая медицинская академия Федерального, 682.04kb.
- Поляков Игорь Васильевич Эрман Михаил Владимирович Ведущее учреждение: гоудпо санкт-Петербургская, 348.31kb.
- Петербургская Государственная Педиатрическая Медицинская Академия, 194100, улица Литовская,, 31.72kb.
- «Санкт-Петербургская государственная педиатрическая медицинская академия Росздрава», 244.37kb.
- «Санкт-Петербургская государственная педиатрическая медицинская академия», 347.44kb.
- Рабочая программа дисциплины 11 Учебная информация, 1086.73kb.
- Биоактивных наноматериалов при раневом процессе, 438.75kb.
- В периоперационном периоде, 343.13kb.
Хронические рубцовые стенозы гортани
Всего под нашим наблюдением находилось 89 детей с хроническими рубцовыми стенозами гортани. Для возникновения рубцов в области гортани у пациентов имелись следующие причины (табл.2).
Таблица 2
Причины хронических рубцовых стенозов гортани у детей
| Причина рубцового стеноза | Число наблюдений | |
| n | % | |
| Интубация трахеи | 54 | 60,7 |
| Химический ожог | 14 | 15,7 |
| Наружная травма | 5 | 5,6 |
| Операция на гортани | 11 | 12,4 |
| Трахеостомия | 5 | 5,6 |
| ИТОГО | 89 | 100,0 |
Наиболее частой причиной хронических рубцовых стенозов гортани у детей – 54 (60,7%) наблюдения стала интубация трахеи. Показания для проведения данной манипуляции были следующие (табл.3).
Возвращаясь к табл.2 мы видим, что следующей по частоте причиной рубцовых стенозов стал химический ожог, который наблюдался у 14 пациентов, что составило 15,7%. У 9 пациентов этой группы ожог был вызван кристаллическим перманганатом калия, у 3 – жидкой щелочью, а у 2 – жидкой кислотой. У данной группы больных помимо рубцового стеноза гортани также отмечалось вовлечение в рубцовый процесс нижнего отдела глотки и входа в пищевод.
У 5 (5,6%) пациентов рубцовый стеноз гортани сформировался вследствие наружной травмы области шеи. Из них 4 получили прямой удар при падении с высоты, и один больной налетел областью шеи на натянутую проволоку во время езды на мотоцикле.
Таблица 3
Распределение больных по характеру патологии,
потребовавшей эндотрахеальной интубации
с исходом в рубцовый стеноз гортани
| Патология | Число наблюдений | |
| n | % | |
| Острый стенозирующий ларинготрахеит | 27 | 50,0 |
| Черепно-мозговая травма | 15 | 27,7 |
| Постнатальная пневмония | 6 | 11,1 |
| Операция на сердце | 3 | 5,6 |
| Утопление | 2 | 3,7 |
| Ожог | 1 | 1,9 |
| ИТОГО | 54 | 100,0 |
У 11 (12,4%) детей рубцовый стеноз сформировался как последствие эндоскопических хирургических вмешательств на гортани. У 10 пациентов после многократного удаления папиллом на голосовых складках и передней комиссуре, и у одного после иссечения врожденной кисты в области надгортанника.
И у 5 (5,6%) причиной стеноза стала собственно трахеостомия, в результате которой сформировались рубцовые изменения в гортани и трахеи.
Локализация рубцового процесса в гортани и шейном отделе трахеи у пациентов отмечалась следующая.
В вестибулярном отделе гортани рубцы наблюдались у 10 детей, что составило 11,2% от числа всех рубцовых стенозов. Преобладали циркулярные рубцы (9 наблюдений), и лишь у одного пациента выявлен передний стеноз преддверия гортани.
Рубцовый стеноз голосового отдела гортани диагностирован у 21 (23,6%) пациента. Из них у 11– передний, у 10 – задний.
Наиболее часто рубцовый стеноз выявлялся в подголосовом отделе гортани – 39 (43,9%). В том числе у 6 пациентов рубцовое сужение локализовалось в области передней стенки подголосового отдела гортани, у 28 наблюдался циркулярный стеноз и у 3 детей полный стеноз, т.е. просвет на уровне подголосового отдела вообще не визуализировался.
У 5 (6,0%) рубцовое сужение локализовалось только в области верхнего края трахеостомы.
У 14 (15,7%) было выявлено рубцовое сужение просвета в нескольких отделах гортани. Так, у 3 детей имелся вестибулярный и задний голосовой стеноз; у 3 – задний голосовой и циркулярный подголосовой; у 3 – наблюдалось полное заращение всех отделов гортани (тотальный стеноз); у 3 – сочеталось сужение подголосового отдела гортани и шейного отдела трахеи; и у 2 имел место полный отрыв гортани от трахеи с заращением просвета в сочетании с двусторонним параличом гортани.
Из 89 больных с хроническим рубцовым стенозом гортани, 57 поступили в отделение с наложенной ранее трахеостомой.
2 ребенка были доставлены в клинику из других стационаров, где после выполнения им эндотрахеальной интубации экстубировать этих пациентов не представилось возможным.
30 пациентов поступили без трахеостомы и предъявляли жалобы на затруднение дыхания и нарушения голоса.
В хирургическом лечении рубцовых стенозов гортани нами были использованы следующие методики.
Эндоскопическое хирургическое лечение произведено 27 пациентам в возрасте от 2 месяцев до 16 лет. Из них 7 (26,9%) пациентов являлись хроническими трахеоканюлярами.
По локализации и распространенности рубцового процесса пациенты, в хирургическом лечении которых использовалась эндоскопическая техника, пациенты распределились следующим образом. Детей с вестибулярными рубцовыми стенозами было 9 (в т.ч. 3 канюленосителя); с сочетанием вестибулярного и голосового стеноза - один ребенок, хронический трахеоканюляр; с рубцовыми стенозами голосового отдела гортани - 4 пациента, в т.ч. один с передним и 3 с задним (один канюленоситель); подголосовых всего 13, в т.ч. передние подголосовые у 6 (один канюленоситель) и циркулярные подголосовые у 7 (один трахеоканюляр) пациентов.
Все вмешательства выполнялась под контролем прямой опорной микро- или эндовидеоларингоскопии. Диодным лазером в контактном режиме производились радиальные разрезы рубцовой ткани, начиная от свободного края рубца и вплоть до стенки гортани. При циркулярном процессе во всех случаях производилось 4 разнонаправленных разреза, как правило, на 11, 2 , 5 и 8 часов по циферблату.
В случае локализации стеноза в подголосовом отделе непосредственно после рассечения измененных тканей производили дилатацию гортани посредством проведения интубационных трубок типа «Portex», начиная с того размера, который свободно проходил через гортань. Затем таким же образом проводили трубку на 0,5 мм большего диаметра. Таким образом, постепенно увеличивая диаметр интубационной трубки на 0,5 мм, доходили до размера трубки, адекватного возрастному.
В послеоперационном периоде пациентам назначались антибиотики широкого спектра действия и противовоспалительные препараты. Осложнений в этом периоде не наблюдалось ни в одном случае.
При повторном рассечении рубца направление радиальных лазерных разрезов менялось. Как правило, выполнялись инцизии на 2, 4 8 и 10 часов по циферблату.
При сравнении показателей автоматической спирометрии у 8 пациентов до и после эндоскопического хирургического лечения выявлено статистически достоверное улучшение проходимости дыхательных путей (p<0,05). Также у этих пациентов выявлено статистически достоверное увеличение максимального времени фонации (p<0,05).
Таким образом, использование эндоскопической лазерной микрохирургии в лечении 27 пациентов с рубцовыми стенозами гортани позволило получить удовлетворительные результаты у 25 детей. Удалось деканюлировать 6 из 7 хронических канюленосителей, что составило 85,7%.
Вместе с тем, применение данного способа было ограничено и использовалось только у пациентов с тонкими, непротяженными стенозами, а также у тех детей, которым ранее не проводилось хирургическое лечение. Кроме того, учитывались специфические особенности каждого конкретного случая (наблюдение переднего рубцового стеноза со сквозной перфорацией в рубце у передней комиссуры), которые позволяли с успехом применить эндоскопическую технику.
Ларингопластика комбинированным доступом с использованием силиконового якореобразного эндопротеза, состоящего из разделительной и фиксирующей пластин была использована для лечения передних рубцовых стенозов голосового отдела гортани.
Данное вмешательство было произведено 10 больным в возрасте от 4 до 16 лет, в том числе 3 хроническим канюленосителям. У 9 больных стеноз сформировался вследствие эндоскопического удаления папиллом гортани, у одной девочки рубец – следствие рецидива эндоскопического рассечения врожденной передней мембраны гортани
На первом, эндоскопическом этапе, выполнялась под контролем прямой опорной микровидеоларингоскопии производилось рассечение рубцовой мембраны. Вторым этапом, через наружный доступ производился разрез в щитовидном хряще и в просвет гортани между голосовыми складками вводилась разделительная пластина эндопротеза, после чего каждый из его боковых выступов поочередно размещался между наружной поверхностью близлежащей пластины щитовидного хряща и гортанной фасцией. Рана послойно ушивалась с оставлением дренажа из перчаточной резины.
Эндопротез оставлялся в гортани на время, необходимое для эпителизации раневых поверхностей голосовых складок. Этот срок составлял от 3 до 4 недель.
Все хронические канюленосители после удаления эндопротеза были деканюлированы. Трахеотомическое отверстие у этих пациентов закрылось самостоятельно.
У 4 пациентов мы исследовали средние количественные показатели отношений «поток-объем» (в % должных величин) до и после оперативного лечения. Отмечается статистически достоверное увеличение показателей ОФВ1,0, ПОС, МОС25, МОС50 и максОФВ1,0 (p<0,05), что свидетельствует об улучшении проходимости дыхательных путей. Так же у этих пациентов определяется статистически достоверное увеличение максимального времени фонации и расширение динамического диапазона (p<0,05).
Таким образом, применение ларингопластики комбинированным доступом с использованием силиконового якореобразного эндопротеза позволило получить удовлетворительные результаты у 9 из 10 (90,0%) прооперированных нами больных. Развившееся осложнение в виде смещения эндопротеза не позволило получить удовлетворительный результат у одной прооперированной нами пациентки.
Одноэтапная ларинготрахеопластика, вмешательство, направленное на расширение просвета гортани и трахеи, выполняемое из наружного доступа, при котором трахеостома не накладывалась, или деканюляция осуществлялась непосредственно по окончании операции была выполнена 4 пациентам с циркулярными рубцовыми стенозами гортани в возрасте от 2 до 12 месяцев, один из которых являлся хроническим канюленосителем.
Оперативное вмешательство проводилось под общим обезболиванием. После вводного масочного наркоза производилась оротрахеальная интубация трубкой такого размера, которая могла быть проведена через зону стеноза в подголосовом отделе. Хронические канюленосители интубировались через трахеостому. Производился разрез кожи по средней линии от верхнего края щитовидного хряща до 5 полукольца трахеи. Тупым путем обнажалась передняя стенка гортани и трахеи. Выполнялось вскрытие гортани и трахеи разрезом по средней линии пересечением перстнещитовидной связки, дуги перстневидного хряща, и первых двух полуколец трахеи. Осматривалась зона сужения в подголосовом отделе. Дополнительное иссечение тканей не производилось ни в одном наблюдении, т.к. после вскрытия просвета через переднюю ларинготрахеальную стенку, ткани, суживающие просвет гортани, распластывались по боковым и задней стенкам гортани. После чего производилась назотрахеальная интубация пациента, трубкой максимального возрастного размера. Продольный и поперечный размер образовавшегося дефекта в передней ларинготрахеальной стенке измерялись линейкой.
Затем, производился поперечный разрез в проекции V ребра справа, острым путем обнажалась хрящевая часть ребра. Надхрящница рассекалась таким образом, чтобы после резекции ребра она сохранялась на передней его поверхности. Производилась поднадхрящничная резекция фрагмента хрящевой части ребра, длиной равной продольному размеру дефекта передней ларинготрахеальной стенки плюс 1 см. Производился тщательный гемостаз и рана на груди послойно ушивалась наглухо.
Из полученного хрящевого фрагмента ребра формировался трансплантат.
Иглой с мандреном (использовались иглы для люмбальной пункции) по краю трансплантата наносились перфорационные отверстия на расстоянии не более 5 мм друг от друга, что в последующем значительно облегчало подшивание трансплантата к ларинготрахеальной стенке. После этого при помощи разработанного инструмента для выкраивания хряща край реберного хряща модифицировался таким образом, чтобы площадь поверхности трансплантата, обращенная в просвет гортани и трахеи была меньше, чем площадь поверхности, обращенная наружу, что исключало возможность его проваливания.
Следующим этапом осуществлялась установка аутотрансплантата реберного хряща в разрезе на передней стенке гортани и трахеи таким образом, чтобы его поверхность, имеющая меньшую площадь и покрытая надхрящницей, была обращена в просвет. Фиксация трансплантата к ларинготрахеальной стенке выполнялась отдельными узловыми швами нитью Викрил 4-0. Затем трансплантат укрывался вышележащими тканями, на них послойно накладывались отдельные узловые швы атравматической нитью Викрил 4-0. Под кожу устанавливались резиновые перчаточные дренажи. Накладывалась асептическая повязка.
В операционной пациент переводился на самостоятельное дыхание. Для дальнейшей реабилитации пациент переводился в отделении реанимации.
Назначались антибиотики широкого спектра для профилактики воспалительных осложнений. Проводилась санация интубационной трубки при помощи электроотсоса по мере необходимости. Осуществлялся мониторинг витальных функций. Питание первые сутки производилось через назогастральный зонд, в последующем, через естественные пути. В среднем на 12 сутки производилась попытка экстубации. Данная процедура выполнялась утром, в отделении реанимации, строго натощак. В реанимационном зале, на операционном столе пациенту производили санацию интубационной трубки, после чего она удалялась. Эффективность оценивалась клинически, по признакам стеноза гортани, по данным мониторинга, а также по газовому составу и кислотно-основному состоянию крови. В случае неэффективной процедуры после вводного наркоза вновь выполняли назотрахеальную интубацию.
Удалась экстубация у всех четырех оперированных по данной методике пациентов с рубцовыми стенозами подголосового отдела гортани (100%).
Многоэтапная ларинготрахеопластика была выполнена 36 пациентам с рубцовыми стенозами подголосового отдела гортани в возрасте на момент операции от 2 до 18 лет. Все 36 пациентов поступили в клинику с наложенной ранее трахеостомой.
В основу многоэтапной ларинготрахеопластики была положена методика, предложенная Э.А.Цветковым (1990).
Оперативное вмешательство проводилось под общим обезболиванием с интубацией больного через трахеостому.
На первом этапе операции выполнялась прямая ларинготрахеоскопия, во время которой окончательно определялась локализация, распространение, форма и возможная глубина рубцового процесса. С помощью металлического наконечника, соединенного с электроотсосом определялась пассивная подвижность черпаловидных хрящей.
Разрез кожи производился горизонтально, на уровне дуги перстневидного хряща. Гортань обнажалась тупым путем, после чего по средней линии рассекались щитоперстневидная связка, дуга перстневидного хряща. В просвет гортани вводился металлический зонд, значительно облегчавший ориентацию в рубцовых деформированных тканях. Рубцовые образования при этом не иссекались, после редрессации печатки они уплощались на боковых стенках гортани, не выступая в ее просвет, что позволяло максимально щадить слизистую оболочку. Печатка перстневидного хряща рассекалась сверху вниз, обе ее половины раздвигались в стороны. Полное вертикальное рассечение печатки тщательно контролировалось визуально и при помощи пальцевого исследования. При этом следует подчеркнуть, что даже незначительное по протяжению недорассечение печатки не позволяло мобилизовать обе половины перстневидного хряща, и, как следствие этого, восстановить просвет гортани, адекватный для дыхания. После этого пересекались поперечная и задние косые мышцы гортани, рубцово измененное межчерпаловидное пространство. Слизистая оболочка гортаноглотки сохранялась.
После дистракции обеих половин печатки перстневидного хряща в полученный просвет пролабируют передняя стенка пищевод, а в верхней трети просвета становится обозримой стенка глотки.
Расширение просвета гортани контролировалось путем прямой ларингоскопии, пальцевым исследованием и ретроградным проведением интубационных трубок соответствующего размера.
На заключительном этапе операции в гортань вводился и фиксировался эндопротез.
Для этого применялся разборный стент по Э.А.Цветкову (1990) с запаянным наглухо верхним концом. Диаметр эндопротеза соответствовал нормальному возрастному просвету гортани и трахеи.
Применялись эндопротезы двух типов.
Первый изготавливался из отрезка интубационной трубки Роrtex, один конец которого разогревался и запаивался в специальной насадке.
Второй изготавливался из силиконового жгута, имеющего круглое сечение, один из концов которого закруглялся с помощью режущего инструмента и оплавлялся на пламени спиртовки.
Нижний конец любого из этих типов эндопротезов с помощью режущего инструмента подгонялся к изгибу трахеотомической канюли, затем прошивался парафинизированными нитями, которые после введения стента в гортань фиксировались к трахеотомической канюле.
Верхний край стента устанавливался на уровне верхушек черпаловидных хрящей. Это позволяло избежать образования грануляций, а в последующем и рубцовых синехий в области голосовых и вестибулярных складок, межчерпаловидного пространства, а так же способствовало адекватному отведению черпаловидных хрящей.
После установки эндопротеза на дугу перстневидного хряща накладывался стягивающий шов нитями Викрил 3-0. Рана послойно ушивалась.
По данной методике было прооперировано 27 пациентов.
У 9 детей после установки эндопротеза образовавшийся дефект в передней ларинготрахеальной стенке был закрыт трансплантатом, выполненным из реберного аутохряща. Для этого производился поперечный разрез в проекции V ребра справа . Острым путем обнажалась хрящевая часть ребра . Надхрящница рассекалась таким образом, чтобы после резекции ребра она сохранялась на передней его поверхности. Производилась поднадхрящничная резекция фрагмента хрящевой части ребра, длиной равной продольному размеру дефекта передней ларинготрахеальной стенки плюс 1 см. Производился тщательный гемостаз и рана на груди послойно ушивалась наглухо.
Затем, из полученного хрящевого фрагмента ребра формировался трансплантат.
При помощи разработанного инструмента для выкраивания хряща край реберного хряща модифицировался таким образом, чтобы площадь поверхности трансплантата, обращенная в просвет гортани и трахеи была меньше, чем площадь поверхности, обращенная наружу, что исключало возможность его проваливания.
Следующим этапом осуществлялась установка аутотрансплантата реберного хряща в разрезе на передней стенке гортани и трахеи таким образом, чтобы его поверхность, имеющая меньшую площадь и покрытая надхрящницей, была обращена в просвет. Фиксация трансплантата к ларинготрахеальной стенке выполнялась отдельными узловыми швами нитью Викрил 4-0. Затем трансплантат укрывался вышележащими тканями, на них послойно накладывались отдельные узловые швы атравматической нитью Викрил 4-0. Под кожу устанавливались резиновые перчаточные дренажи.
Профилактика послеоперационных осложнений заключалась в следующем.
За сутки до предполагаемого оперативного лечения парентерально назначался антибиотик широкого спектра действия. Антибиотикотерапия продолжалась и в послеоперационном периоде в течение в среднем 7-9 дней. При необходимости более продолжительного курса производилась смена препарата.
Во избежании застойных явлений в бронхолегочной системе назначались препараты разжижающие мокроту и улучшающие мукоцилирный клиренс.
С целью профилактики обострения хондроперихондрита хрящей гортани смена стента у детей осуществлялась ежемесячно. Под эндотрахеальным наркозом выполнялась прямая ларингоскопия, нити, фиксировавшие стент, отрезались, а сам эндопротез удалялся через ларингоскоп щипцами. Все патологические грануляции удалялись под контролем операционного микроскопа. Визуально контролировался процесс эпителизации раневой поверхности в области передней и задней стенок гортани. Окончательное удаление эндопротеза осуществлялось после полной эпителизации внутренней поверхности гортани.
Минимальный срок эндопротезирования составил 3 месяца, максимальный – 11 месяцев, однако у большинства пациентов эндопротез устанавливался на 4-5 месяцев (рис.1).
| Месяцы |
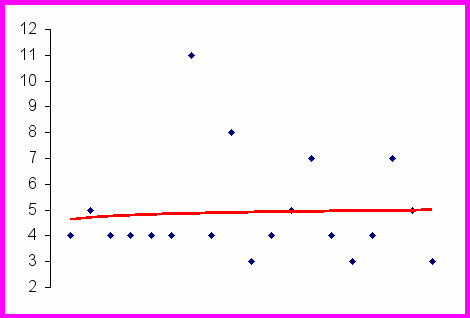 |
| Рис.1. График длительности эндопротезирования при многоэтапной ларинготрахеопластике. |
После окончательного удаления эндопротеза отмечалась разлитая гиперемия и диффузный отек слизистой оболочки гортани в местах соприкосновения и трения с эндопротезом. Подобные изменения отмечались в течение 2-4 недель. Степень их выраженности находилась в прямой зависимости от длительности ношения эндопротеза и обострения хронического хондроперихондрита.
В группе пациентов, которым многоэтапная ларинготрахеопластика производилась без использования хрящевого реберного аутотрансплантата, было деканюлировано 23 из 27 прооперированных пациентов, что составило 85,2%.
В группе, где в использовался реберный аутохрящ для замещения дефекта в передней ларинготрахеальной стенке, были деканюлированы все 9 пациентов (100%).
При сравнении этих групп с использованием четырехпольной таблицы выявлено достоверное различие в относительном количестве деканюлированных пациентов в группе, где использовался реберный аутохрящ (р<0,05).
В общем было деканюлировано 32 из 36 больных, которым была выполнена многоэтапная ларинготрахеопластика, что составило 88,9%.
У большинства больных после удаления эндопротеза и деканюляции трахеостомическое отверстие закрылось самостоятельно. Имевшие место у 3 пациентов микротрахеостомы диаметром 2-4 мм были закрыты путем пластики местными тканями.
После операции оценка функционального результата была произведена у 22 пациентов.
При визуальной оценке графика «поток-объем» у 3 пациентов имело место небольшое «плато», т.е. экспираторный график не достигал пика. У 20 пациентов проходимость дыхательных путей была нормальной, и у 2 больных имели место легкие нарушения.
Первоначально после удаления эндопротеза у всех больных имелась полная афония, которая проходила к концу месяца после деканюляции. В дальнейшем, через год, дисфония I степени имелась у 19 пациентов, у 3 больных выявлена дисфония II степени.
Таким образом, применение многоэтапной ларинготрахеопластики с редрессацией печатки перстневидного хряща с последующим эндопротезированием позволило деканюлировать 32 из 36 прооперированных пациентов (88,9%) с хроническими циркулярными и полными рубцовыми стенозами подголосового отдела гортани. Удовлетворительные функциональные результаты, подтвержденные методом автоматической спирометрии, получены у 22 больных.
Однако, в группе пациентов которым многоэтапная ларинготрахеопластика производилась без использования хрящевого реберного аутотрансплантата, было деканюлировано 23 из 27 прооперированных пациентов, что составило 85,2%, а в группе, где в использовался реберный аутохрящ были деканюлированы все 9 пациентов (100%).
При сравнении этих групп с использованием четырехпольной таблицы выявлено достоверное различие в относительном количестве деканюлированных пациентов в группе, где использовался реберный аутохрящ (р<0,05), что говорит о большей эффективности многоэтапной ларинготрахеопластики в той модификации, где используется аутотрансплантат из реберного аутохряща для закрытия дефекта в передней ларинготрахеальной стенке.
Пластика трахеостомы была произведена 5 пациентам в возрасте от 1 года до 11 лет, хроническим трахеоканюлярам, у которых рубцовые изменения локализовались непосредственно в области верхнего края трахеостомы, формируя т.н. «козырек». Удалось деканюлировать всех пятерых пациентов.
Таким образом, исходя из определенной нами структуры рубцовых стенозов, нами были разработаны алгоритмы хирургической тактики для наиболее распространенных локализаций, а именно, для подголосового и голосового отделов гортани.
Если пациент с рубцовым сужением подголосового отдела гортани находился в компенсированной стадии стеноза, а рубцовые изменения были не протяженными и не распространенными, мы использовали эндоскопическую хирургию. При отсутствии эффекта от данного метода лечения, мы выполняли многоэтапную ларинготрахеопластику (предварительно накладывая трахеостому, если ее не было).
В случае выраженной дыхательной недостаточности (стеноз гортани II-III ст.) пациентам младшего возраста мы производили одноэтапную ларинготрахеопластику. При отсутствии эффекта от данного метода лечения, пациенту накладывалась трахеостома, а затем выполнялась многоэтапная ларинготрахеопластика.
У пациентов старшего возраста в случае выраженной дыхательной недостаточности (стеноз гортани II-III ст.) выполнялась трахеостомия, а затем многоэтапная ларинготрахеопластика (рис.2).
У пациентов с передним стенозом голосового отдела гортани мы считали операцией выбора ларингопластику комбинированным доступом с использованием якореобразного эндопротеза. В случае выраженной дыхательной недостаточности (стеноз гортани II-III ст.) предварительно накладывалась трахеостома (рис.3).
Таким образом, нами было прооперировано с использованием различных методик всего 82 пациента с хроническими рубцовыми стенозами гортани, из них было 52 хронических канюленосителя, что составило 63,4% (табл.4). В 7 наблюдениях у хронических канюленосителей мы воздержались от проведения реконструктивных вмешательств в силу тяжелой сопутствующей соматической и неврологической патологии.

Рис. 2. Алгоритм хирургической тактики при рубцовых стенозах подголосового отдела гортани
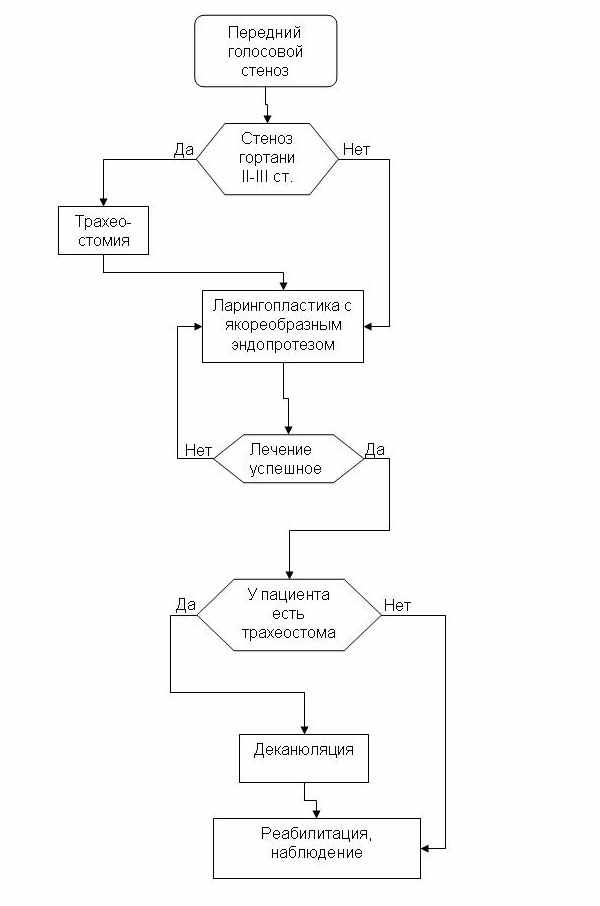
Рис. 3. Алгоритм хирургической тактики при рубцовых стенозах голосового отдела гортани.
Таблица 4
Результаты лечения рубцовых стенозов гортани
| Тип вмешательства | Число пациентов | Число канюле-носителей | Число деканюлированных пациентов | ||
| N | % | ||||
| Эндоскопическая хирургия | 27 | 7 | 6 | 85,7 | |
| Ларингопластика с якореобразным эндопротезом | 10 | 3 | 3 | 100 | |
| Одноэтапная ларинготрахеопластика | 4 | 1 | 1 | 100 | |
| Многоэтапная ларинготрахеопластика | 36 | 36 | 32 | 88,9 | |
| | Без аутотрансплантата | 27 | 27 | 23 | 85,2 |
| | С аутотрансплантатом | 9 | 9 | 9 | 100 |
| Пластика трахеостомы | 5 | 5 | 5 | 100 | |
| ВСЕГО | 82 | 52 | 47 | 90,4 | |
Используя разработанные алгоритмы лечения нами было деканюлировано 90,4% пациентов с хроническими рубцовыми стенозами гортани.
