Кластерные анионы бора b n h n 2- ( n = 10,12) в качестве лигандов вкоординационныХ соединениях металлов iб-группы и свинца(II) 02. 00. 01- неорганическая химия
| Вид материала | Автореферат диссертации |
- «Неорганическая химия», 1345.55kb.
- Конспект лекций по курсу «Неорганическая и аналитическая химия», 18.21kb.
- Примерная программа наименование дисциплины неорганическая химия рекомендуется для, 263.82kb.
- Рабочая программа дисциплины (модуля) «математический анализ», 424.74kb.
- Рабочая программа дисциплины (модуля) «Уравнения математической физики», 266.58kb.
- Рабочая программа дисциплина ‹‹Неорганическая химия›› опд. Ф. 02 Специальность 020101, 343.5kb.
- Неорганическая и аналитическая химия, 221.14kb.
- Рабочая программа дисциплины (модуля) «Линейная алгебра и аналитическая геометрия», 275.82kb.
- Общая и неорганическая химия, 261.98kb.
- Общая и неорганическая химия, 441.8kb.
IV.1 Синтез и строение комплексов Cu(II) с анионами BnHn2- (n = 10, 12), 2,2`- бипиридилом и аминогуанидином. Как уже было показано в ходе исследования, наличие в реакционном растворе одновременно солей Cu(II) и клозо-декаборатов приводит к протеканию окислительно-восстановительной реакции. С целью ее предупреждения и быстрого выведения образующихся комплексов из реакционной смеси, реакции проводили в присутствии крупного органического лиганда – 2,2`-бипиридила.
B10H102- + Cu2+ + bipy [Cu(bipy)2]B10H10∙H2O (27) +
[Cu(NCCH3)2(2-B10H9bipy)] (28)
В результате проведенного взаимодействия было выделено два комплексных соединения 27 (~80%) и 28 (~10%).
Соединение [Cu(bipy)2]B10H10∙H2O 27 представляет собой комплекс Cu(II) с внешнесферным клозо-декаборатным анионом. Состав и строение комплекса 27 определяли исходя из данных элементного анализа, ИК-спектров и магнитной восприимчивости.
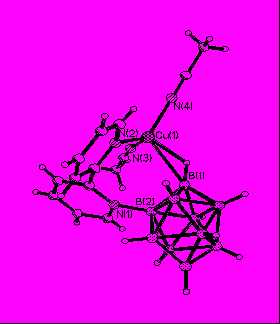 |
| Рис. 18. Строение комплекса [Cu(NCCH3)2(2-B10H9bipy)]. |
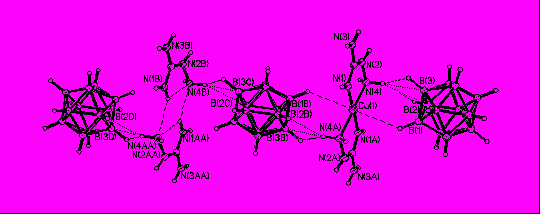 |
| Рис. 19. Строение полимерной цепочки [(HAgu)2Cu(Agu)2(B12H12)2]n. |
Комплекс Cu(II) с анионом B12H122- и аминогуанидином (Cu0.61H0.78Agu2)B12H12 ( 29) получали при взаимодействии (НAgu)2B12H12 и солей Cu2+. Структура 29 построена из комплексного соединения [Cu(Agu)2B12H12] и соли (HAgu)2B12H12 (рис. 19). Атом Cu(II) расположен в центре симметрии ½, ½, ½. Фактор заселенности этой позиции составляет 0.612(1). Плоско-квадратное окружение атома Cu(II) образуют атомы N(1) и N(4) двух молекул Agu, замыкающих пятичленные хелатные циклы (Cu-N 1.9702(13) и 2.0261(10) Å, угол N(1)CuN(4) 81.53(4)º). Молекула Agu имеет уплощенное строение. Две дополнительные связи атом Сu(II) образует с атомами Н(1) двух центросимметричных анионов B12H122- (Cu…H(1) 2.805(14) Å, угол CuHB 132.5(10)º). Катионы HAgu+ попарно связаны межмолекулярными Н-связями в центросимметричные димеры. В структуре комплексные катионы [CuAgu2]2+ и анионы B12H122- объединены взаимодействиями Сu…H(1) в цепочки. Кроме того, между катионами и анионами осуществляются многочисленные слабые вторичные взаимодействия (N)H…H(B) и (N)H…B, формирующие трехмерный каркас. В ячейках, где позиции Cu вакантны, цепочки сохраняются благодаря вторичным взаимодействиям NH…HB.
Таким образом, образование комплекса 29 можно трактовать как результат изоморфного замещения двух ионов Н+ на ион Cu2+(рис. 20). Это дало основание предположить, что комплекс 29 изоструктурен соли (AguH)2B12H12 (30), что было доказано нами в результате РСА 30. Определение структур 29 и 30 проводили при 160К. Объем элементарной ячейки 30 превышает объем ячейки 29 менее, чем на 5 Å3 (404.20(5) и 399.64(4) Å3, соответственно). По геометрии катион Agu+ в 30 заметно отличается от молекулы Agu в 29. Геометрические различия приводят к единственному заметному структурному различию – изменению размера полости в димерном катионе, который характеризуют внури- и межмолекулярные расстояния N(1)…N(4). В соли 30 эти расстояния (2.685(1) и 3.111(1) Å) существенно длиннее, чем в комплексе 29 (2.610(2) и 3.027(2) Å). Характеристики вторичных взаимодействий между катионами и анионами в структурах 29 и 30 различаются незначительно.
| (а)  (б) (б) |
| Рис. 20. Строение фрагментов [(HAgu)2Cu(Agu)2(B12H12)2]n (а) и (HAgu)2B12H12 (б). |
Анализ ИК-спектра комплекса 29 проводили в сравнении со спектром исходного - (HAgu)2B12H12 30. В ИК-спектрах 29 и 30 состояние аниона B12H122- не меняется, полоса ν(ВН) расщеплена на две компоненты при 2445 и 2415 см-1. Такое расщепление полосы ν(ВН) в 30 обусловлено, наличием взаимодействий, возникающих между NH2-группами катиона и BH-группами аниона B12H122-, последнее сохраняется и в комплексе 29. Координация молекул Agu к атому металла проявляется в существенном изменении положения валентных и деформационных колебаний NH2-групп по сравнению с таковыми в спектре 30.
IV.2 Синтез и строение комплексов Pb(II) с анионами BnHn2- (n = 10, 12). Среди непереходных элементов кластерные анионы образуют устойчивые комплексы со свинцом(II), и на сегодняшний день они являются единственными примерами комплексов непереходных металлов с анионами BnHn2-.
IV.3 Клозо-бораты Pb(II) - MBnHn (n = 10, 12). Клозо-бораты Pb(II) получали при взаимодействии карбоната Pb(II) c кислотами (H3O)2BnHn. Образующиеся гидратированные клозо-бораты MBnHn∙xH2O легко подвергаются процессу дегидратации, что приводит к образованию безводных гигроскопичных соединений. В этом отношении PbBnHn∙xH2O подобны дегидратированным клозо-боратам легких щелочно-земельных металлов. Соединения PbBnHn∙xH2O окрашены, легко растворяются в полярных органических растворителях, образуя соответствующие сольваты. Предварительные исследования, базирующиеся на изучении ИК-спектров соединений показали, что клозо-декаборат Pb(II) может быть отнесен к комплексному соединению [Pb(H2O)хB10H10], в котором нельзя исключить взаимодействия аниона В10Н102- с металлом. В ИК-спектре [Pb(H2O)хB10H10] наблюдаются колебания ν(BH) при 2485 и (BH)МHB при 2414 см-1. Что касается соединения Pb(II) с клозо-додекаборатным анионом, то согласно ИК-спектрам, соединение представляет собой аквакомплекс
[Pb(H2O)6]B12H12 - в ИК-спектрах проявляется уширенная полоса ν(BH) при ~ 2470 см-1. Отсутствие полосы колебаний (BH)МHB свидетельствует о нахождении аниона B12H122- во внешней сфере комплекса. Внутреннюю координационную сферу металла формируют молекулы воды.
IV.4 Комплексы Pb(II) с анионами BnHn2- и 2,2`-бипиридилом.
Смешанолигандные комплексы Pb(II) с анионами BnHn2- и 2,2`-бипиридилом получали по схеме.
BnHn2- + Pb 2+ + bipy [Pb(bipy)хBnHn]
В результате реакции были получены комплексы [Pb(bipy)B10H10] (31) и [Pb(bipy)2B12H12] (32), причем их состав не зависит от соотношения M : BnНn2- : L.
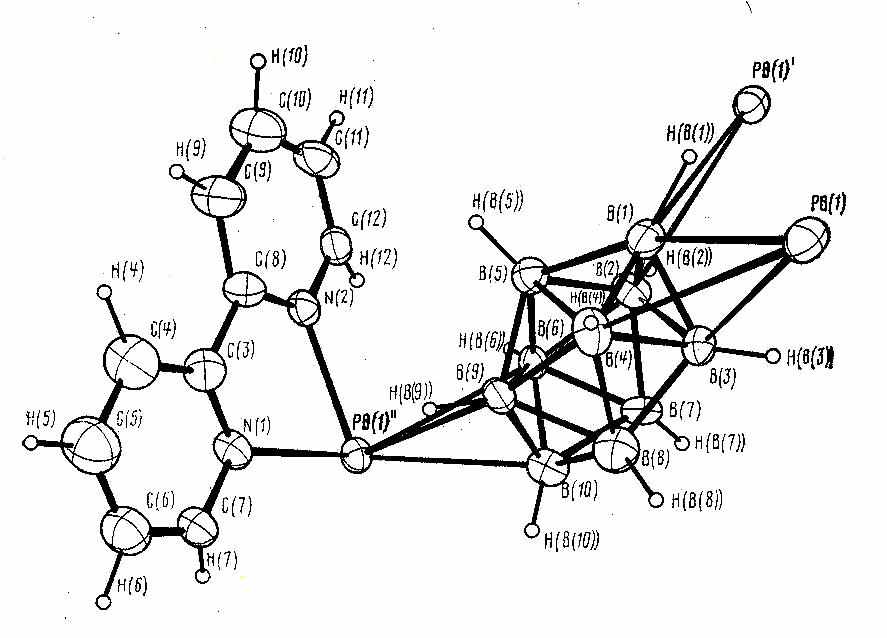
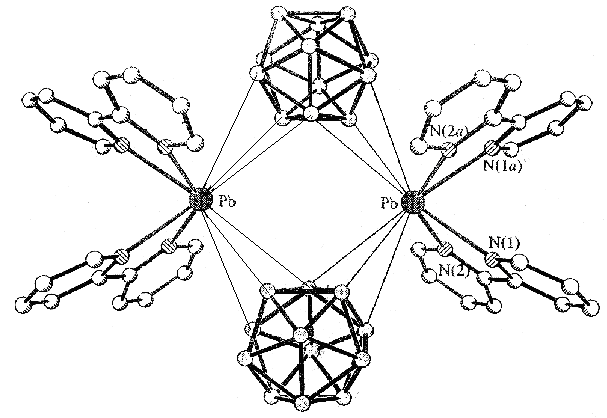
В комплексе 31 (рис. 21а) окружение атома Pb образуют молекула бипиридила (Pb-N 2.470(6) и 2.500(5) Å) и три независимых анионами B10H102-. В свою очередь каждый анион B10H102- координируется одновременно к трем атомам Pb разными способами: два аниона – апикальными гранями при противоположных вершинах полиэдра, третий – по апикальному ребру. В результате в координации участвуют 7 из 10 атомов бора кластерного аниона. Расстояния Pb-B(Н) 3.041(7)-3.376(8), Pb-H(B) 2.66(6)-3.18(5) Å, углы PbHB 90°-125° позволяют говорить о том, что во взаимодействии принимают участие атомы и бора, и водорода.
  (а) (б) |
| Рис. 21. Фрагмент структуры [Pb(bipy)(B10H10)]n (а) и димера [Pb(bipy)2(B12H12)]2 (б). |
В ИК-спектрах обоих комплексов наблюдается расщепление полос (BH) на несколько компонент 2517, 2471, 2443 и 2418 см-1 31 и 2507, 2469, 2445, 2413 см-1 32. Низкочастотные полосы при 2418 и 2413 см-1 для анионов B10H102- и B12H122-, соответственно, относятся к валентным колебаниям (BH)МHB. Координирован-ным молекулам bipy в спектрах комплексов 31, 32 соответствует повышение частоты ν(C-N) гетероцикла до 1610 см-1 и существенное перераспределение интенсивности колебаний в интервале 1600-700 см-1.
Таким образом, на примере комплексов 31 и 32 установлено, что кластерные анионы бора наравне с другими нейтральными органическими лигандами способны образовывать комплексы с непереходными металлами различного состава и строения.
IV.5 Комплексы Pb(II) с замещенными клозо-декабортными анионами B10H10-mXm2- (X = OH, OC(O)CH3, O(CH2CH2)2OEt; m = 1, 2) и 2,2`-бипиридилом. Эффективным методом уменьшения дентантности анионов BnНn2- является введение заместителя в борный остов. В этом случае следует ожидать образование комплексов, в которых борный кластер может быть координирован к металлу-комплексообразователю как с помощью экзо-полиэдрического заместителя, так и с участием BН–групп борного полиэдра. Многообразие продуктов замещения экзо-полиэдрических связей B-H в бороводородных анионах, синтезированное ранее в нашем коллективе, позволило на их основе получить и исследовать комплексы металлов различного состава и строения. Далее будут рассмотрены комплексы Pb(II) с 2,2`-бипиридилом и некоторыми замещенными клозо-декаборатного аниона - B10H10-mXm2- (X = OАс, Ас = C(O)CH3, m = 1, 2; X = OH, O(CH2CH2)2OEt, m = 1). Комплексы Pb(II) с замещенными анионами получали согласно схеме:
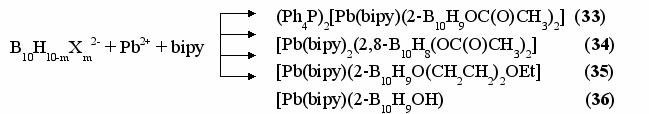
 а) а) |
 б) б) |
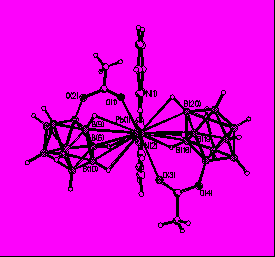
| Рис. 22. Фрагмент структуры (Ph4P)2[Pb(bipy)(2-B10H9OC(O)CH3)2] (а), [Pb(bipy)2(2,8-B10Н8(OC(O)CH3)2)] (б). |
Методом РСА монокристаллов было определено строение комплексов 33-36а. В комплексе 33 (рис. 22а) атом свинца, координирует два атомами азота молекулы bipy (Pb-N 2.551(3) и 2.581(3) Å), два атома кислорода карбоксилатных групп от двух анионов (2-B10H9OAc)2- (Pb-O 2.749(3) и 2.760(3)Å) и два полиэдрических аниона (2-B10H9OAc)2-, которые связаны с атомом металла апикальной гранью полиэдра, находящейся в противоположном от заместителя положении. Во взаимодействии участвуют атомы бора и водорода, расстояния Pb-B(Н) 2.989(5)-3.223(5), Pb-H(B) 2.60(4)-2.93(4) Å, углы PbHB 89(2)-102(2)°.
В комплексе 34 (рис. 22б) окружение атома Pb(II) формируется двумя парами атомов азота двух молекул bipy (Pb-N 2.572(5) и 2.616(5) Å) и двумя карбонильными атомами кислорода карбоксилатных групп аниона (2,8-B10H8(OAc)2)2- (Pb-O 2.756(5) Å). В комплексе 34 наблюдаются также два коротких контакта с BН–группами замещенного аниона, связывание происходит по экваториальному ребру; во взаимодействии участвуют атомы и бора, и водорода (Pb-B(4) 3.263(8), Pb-H(B4) 2.63(5) Å, угол PbHB(4) 116(2)°).
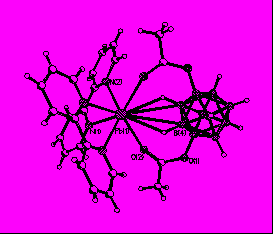
В комплексе 35а (рис. 23) в окружение атома Pb(II) входят два атома азота молекулы bipy (Pb-N 2.470(4) и 2.483(5) Å) и три атома кислорода цепочечного заместителя (2-B10H9O(CH2CH2)2OEt)2- (Pb-O 2.497(4), 2.598(4), 2.859(4) Å). Кроме того, атом Pb образует связи с апикальным атомом бора B(1) одного замещенного аниона и апикальным ребром B(1)-B(5) другого, которые объединяют комплексы в центросимметричные димеры. Во взаимодействие М-BnНn2- вовлечены атомы
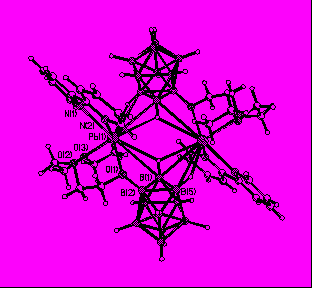 |
| Рис. 23. Фрагмент структуры [Pb(bipy)(2 B10H9O(CH2CH2)2OEt)]2∙0.5ДМФА. |
В комплексе 36а (рис. 24) кластерный анион (2-B10Н9OH)2- координируется к атому Pb только через атомы кислорода гидроксогруппы, при этом ВН-группы замещенного аниона не вступают в какие-либо взаимодействия с атомом металла.
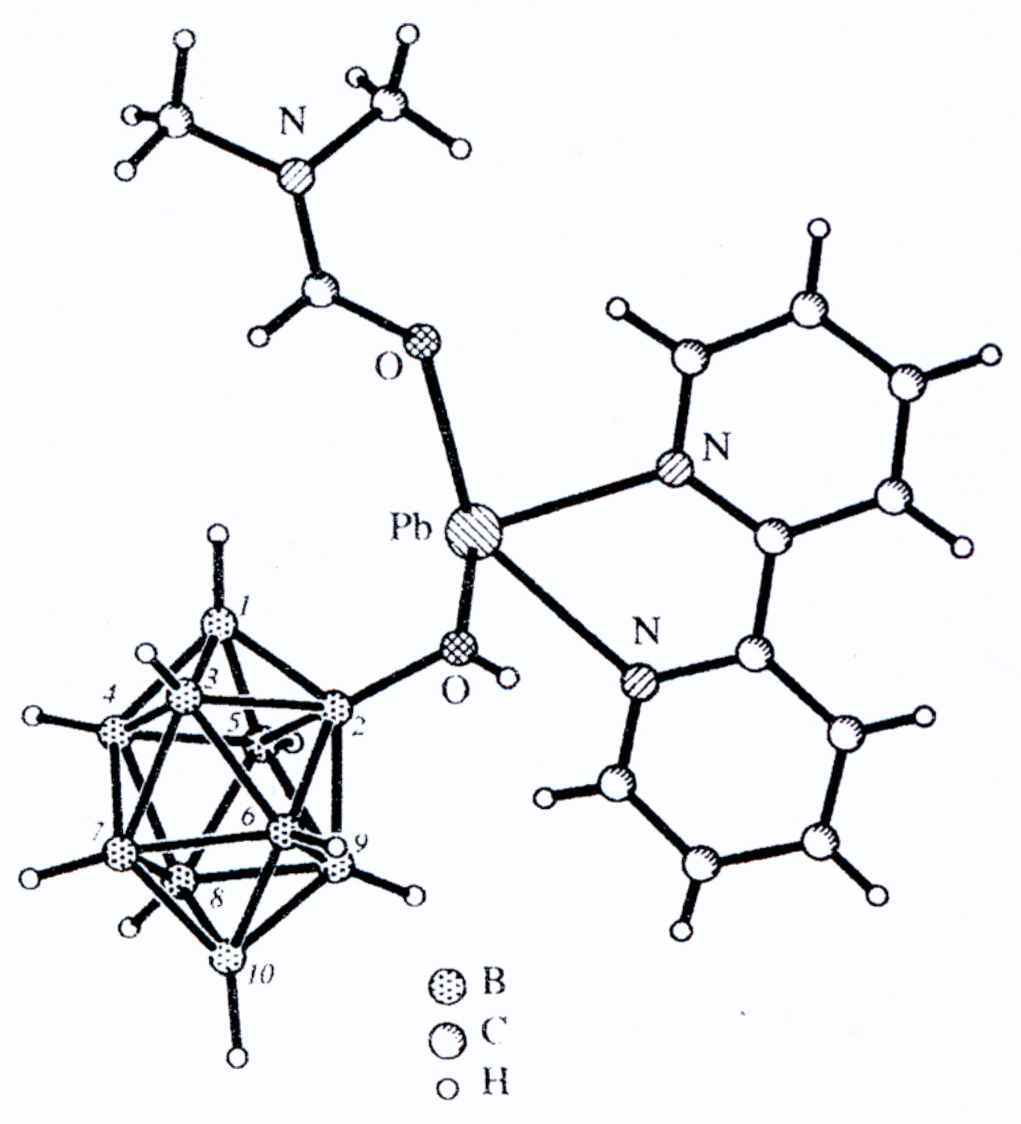 |
| Рис. 24. Фрагмент структуры [Pb(bipy)(ДМФА)(2-B10Н9OH)]∙ДМФА |
