«Технология бродильных производств и виноделие»
| Вид материала | Методические рекомендации |
- Методические рекомендации по выполнению лабораторного и научно-исследовательского практикума, 952.7kb.
- Учебное пособие по дисциплине для студентов специальности 270500 «Технология бродильных, 1164.77kb.
- Учебно-методический комплекс для студентов дневной и заочной формы обучения по специальности, 1588.96kb.
- Методические рекомендации по выполнению самостоятельной работы и изучению дисциплины, 846.76kb.
- Отчет о результатах самообследования основной образовательной программы по специальностям:, 1627.98kb.
- Рабочая программа по дисциплине опд. Ф. 12 «Микробиология» направления 260200 Производство, 368.1kb.
- Методические указания «Вопросы к зачету лабораторных работ», 128.49kb.
- Учебное пособие по дисциплине для студентов специальностей 270500 «Технология бродильных, 2133.55kb.
- Н. Г. Осенний 2012 г. Расписание, 59.13kb.
- Прикладнаямеханика лекция, доц. Воложанинов С. С. 2/150, 47.06kb.
2.2 Принципы биохимии
При всем многообразии биосферы биологические основы жизни удивительно единообразны как по наборам типов биомолекул и их внутренней организации, так и по магистральным путям химических превращений. Корни такого единообразия (но не полной идентичности) кроются в единстве происхождения, законах наследственности и эволюционном процессе на основе естественного отбора.
Живая материя подчиняется всем физическим и химическим законам, включая законы термодинамики, сохранения массы и энергии. Однако законы физики и химии, физико-химические подходы позволяют только понять устройство и работу существующей ныне живой материи, но не дают ответа на вопросы о движущих силах биологической эволюции и причинах возникновения тех или иных форм, микроструктур, биомолекул, функций.
Организмы принадлежат к открытым системам, обменивающимся с окружающей средой веществом, энергией и информацией, находящимся вдалеке от термодинамического равновесия, характеризующимся максимумом энтропии. Обменные процессы со средой организованы таким образом, что формируется особый вид неравномерного, но устойчивого состояния, при котором постоянство внутренних параметров поддерживается динамическим путем за счет уравновешивания скоростей поступления в клетку (организм) и выхода из нее в среду веществ и энергии. Благодаря такому стационарному состоянию и тесно связанному с ним гомеостазу, биохимические реакции осуществляются в достаточно узком интервале физических и химических параметров.
Приуроченность биологической жизни (метаболизма) к узкому зазору физико-химических уровней дает неоспоримый выигрыш за счет стандартизации условий для оптимальной производительности молекулярных машин, узнавания молекулами друг друга, направленности и точности действия регуляторных сигналов.
2.2.1 Принцип богатого энергией внешнего электрона
В клетке запасается, используется и превращается энергия электронов, причем, как правило, внешних валентных электронов: внутренние электронные оболочки атома энергетически инертны для метаболизма. У гетеротрофов это переход валентных электронов, осуществляющих ковалентную связь между атомами С и Н, С и С на более прочные связи Н-О-Н (вода) и О-С-О (углекислый газ). Для биологических нужд используется энергия, выделяемая при соединении атомов водорода субстратов (углеводов, жиров и др.) с кислородом. У фотоавтотрофов (источник энергии – кванты света) в первичном событии – улавливании и кратковременном (10-9 с) запасании энергии – участвуют валентные электроны хлорофилла. Затем временными аккумуляторами запасенной энергии последовательно становятся специализированные молекулы – переносчики электрона (от 10-3 до 10-5 с), АТФ и НAДФ (от 10-1 до 10 с) и, наконец, сахара (от 102 до 104 с). Если валентные электроны в продуктах реакции более прочно связываются с ядерным остовом, чем в исходных молекулах, то энергия выделяется, и, наоборот, ослабление интегральной электронно-ядерной связи приводит к поглощению энергии.
Когда электроны более тесно связываются с ядерным остовом, энергия выделяется, при обратном процессе – отдалении электронов от ядер – энергия потребляется.
- Принцип энергетического сопряжения
Направление химического превращения, в принципе всегда обратимого, определяется направлением изменения свободной энергии F=HTS, где H – энтальпия (теплосодержание); S – энтропия; T – абсолютная температура.
Самопроизвольно процессы идут только в направлении снижения свободной энергии (
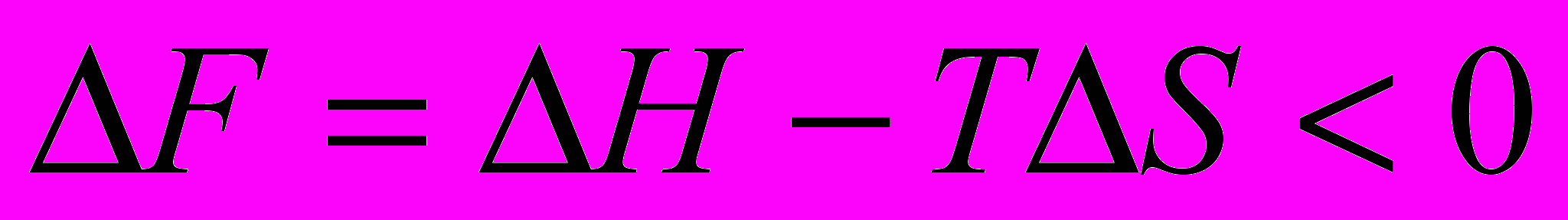 ). Поскольку величина
). Поскольку величина 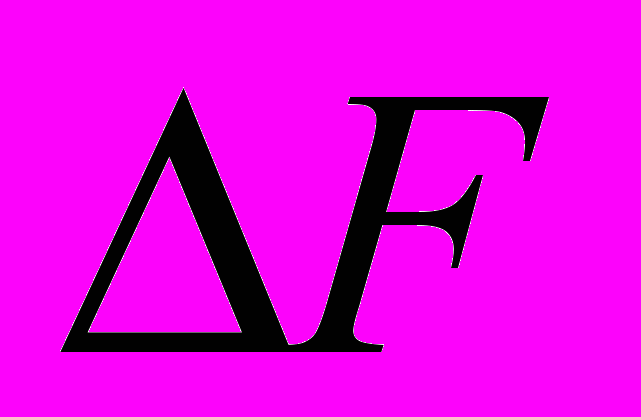 определяется как энтальпийным, так и энтропийным членом, возможно протекание не только экзотермических, но и эндотермических реакций. В последнем случае свободная энергия уменьшается за счет энтропийного члена (
определяется как энтальпийным, так и энтропийным членом, возможно протекание не только экзотермических, но и эндотермических реакций. В последнем случае свободная энергия уменьшается за счет энтропийного члена ( ) – это эндотермические (
) – это эндотермические (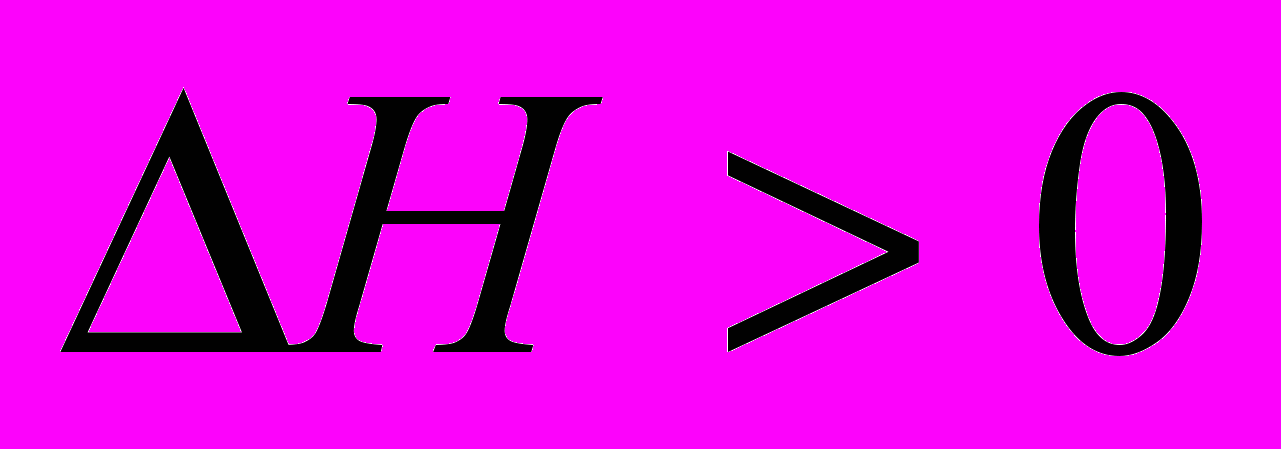 ), но экзергонические (
), но экзергонические (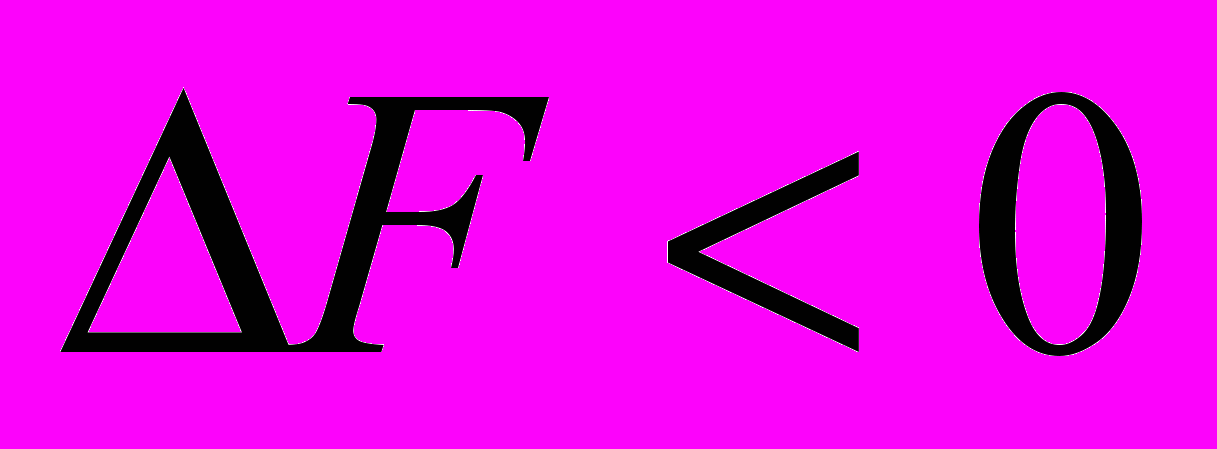 ) реакции.
) реакции.Свободная энергия сложной многокомпонентной смеси определяется как справочными значениями F для всех компонентов, так и их концентрациями:
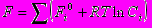 , где R=8,31 Дж/(моль·град) – универсальная газовая постоянная. Динамическое равновесие в реакции А↔В, когда концентрации веществ А и В остаются постоянными во времени, наступает при выравнивании запасов свободной энергии в исходных (А) и конечных (В) продуктах (
, где R=8,31 Дж/(моль·град) – универсальная газовая постоянная. Динамическое равновесие в реакции А↔В, когда концентрации веществ А и В остаются постоянными во времени, наступает при выравнивании запасов свободной энергии в исходных (А) и конечных (В) продуктах (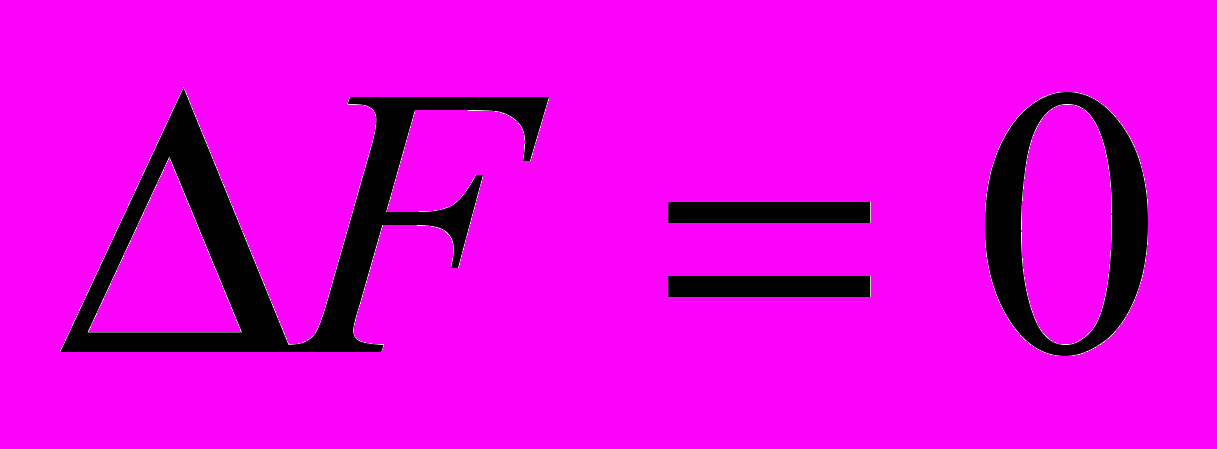 ). При этом соотношение равновесных концентраций В и А (
). При этом соотношение равновесных концентраций В и А (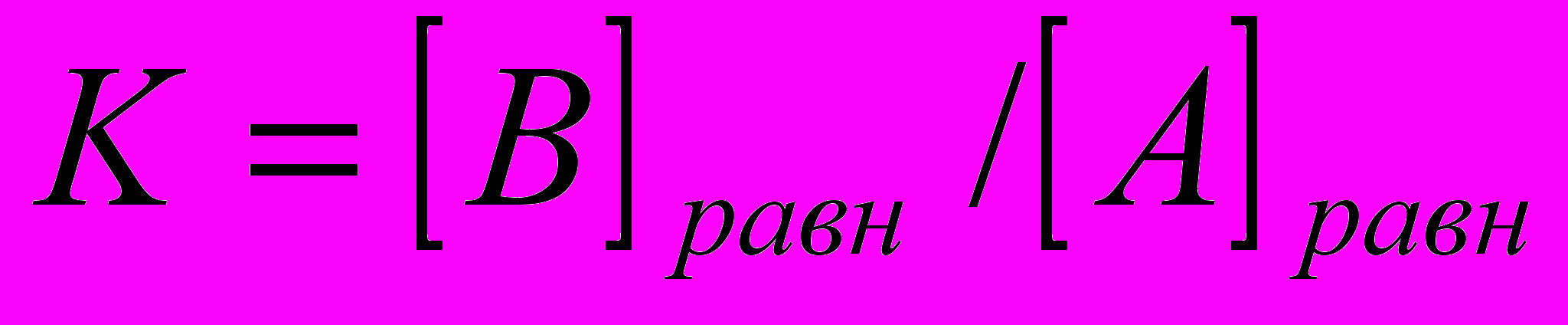 ) тем больше, чем меньше запас свободной энергии в молекулах В по сравнению с А.
) тем больше, чем меньше запас свободной энергии в молекулах В по сравнению с А.Чем объяснить множество эндергонических реакций, происходящих в клетке (биосинтез белков из аминокислот и полисахаридов из моносахаридов)? Поскольку даже простейшая реакция синтеза дисахарида сахарозы из моносахаридов глюкозы и фруктозы в сахарной свекле термодинамически запрещена, так как в этой реакции (глюкоза + фруктоза ↔ сахароза) значение F возрастает, и положение равновесия должно быть резко сдвинуто влево, тем не менее вопреки термодинамике сахароза в этих растениях накапливается. Протекание эндергонических реакций становится возможным благодаря энергетическому сопряжению их с экзергоническими реакциями. При этом организуется пространственное и временное единство между реакцией эндергонической, потребляющей энергию (
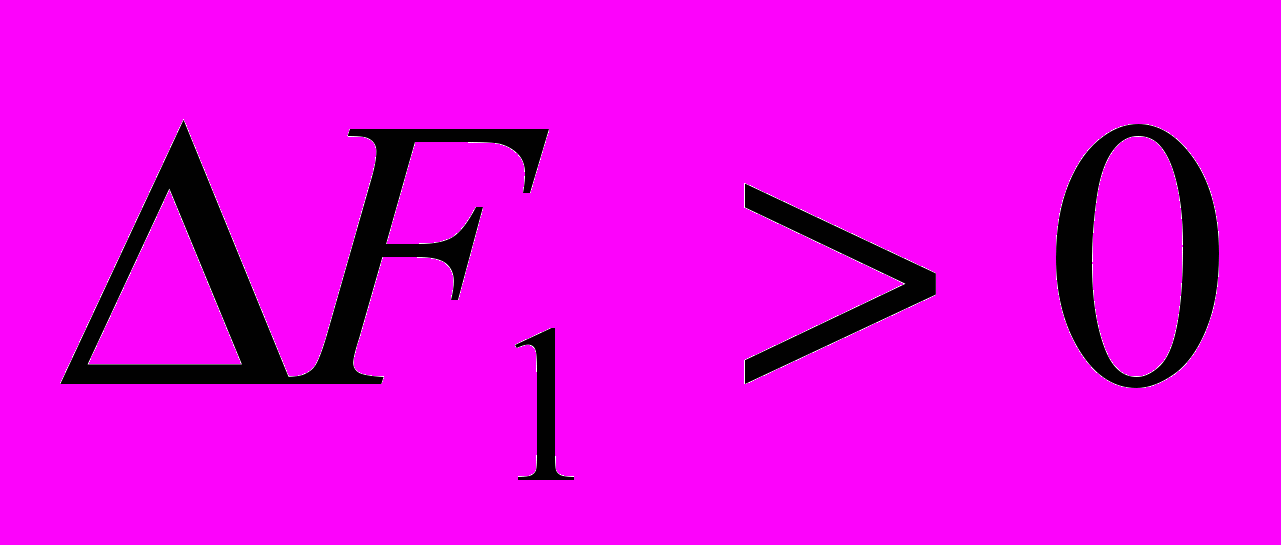 ), и реакцией экзэргонической, поставляющей свободную энергию (
), и реакцией экзэргонической, поставляющей свободную энергию (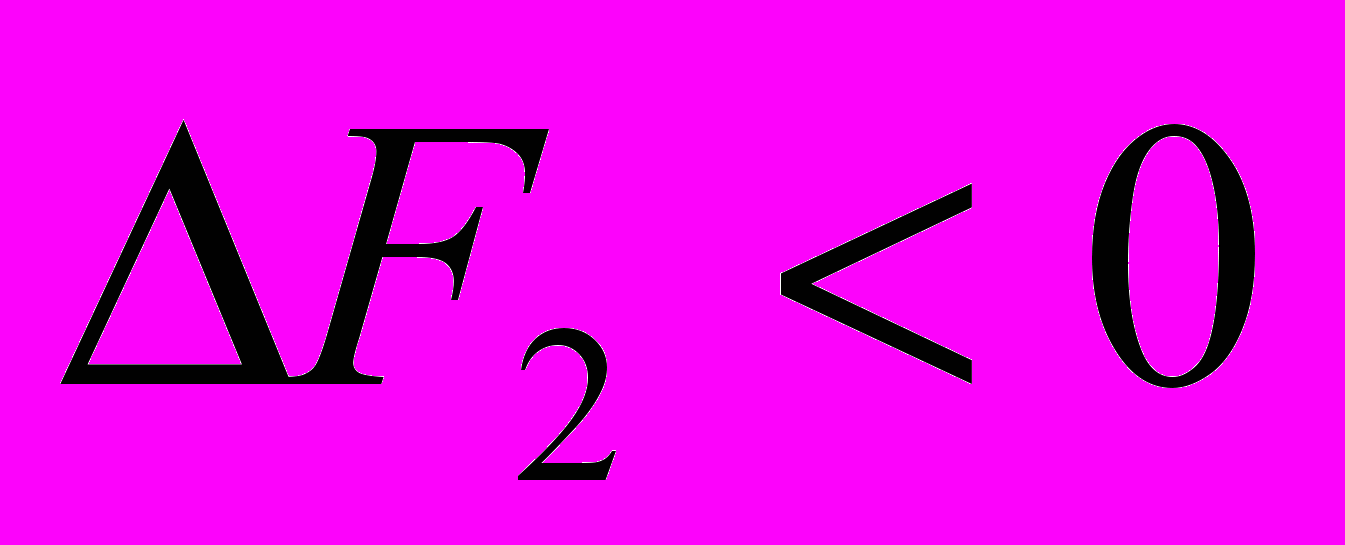 ), с таким расчетом, чтобы суммарный энергетический баланс двух реакций был отрицательным (
), с таким расчетом, чтобы суммарный энергетический баланс двух реакций был отрицательным (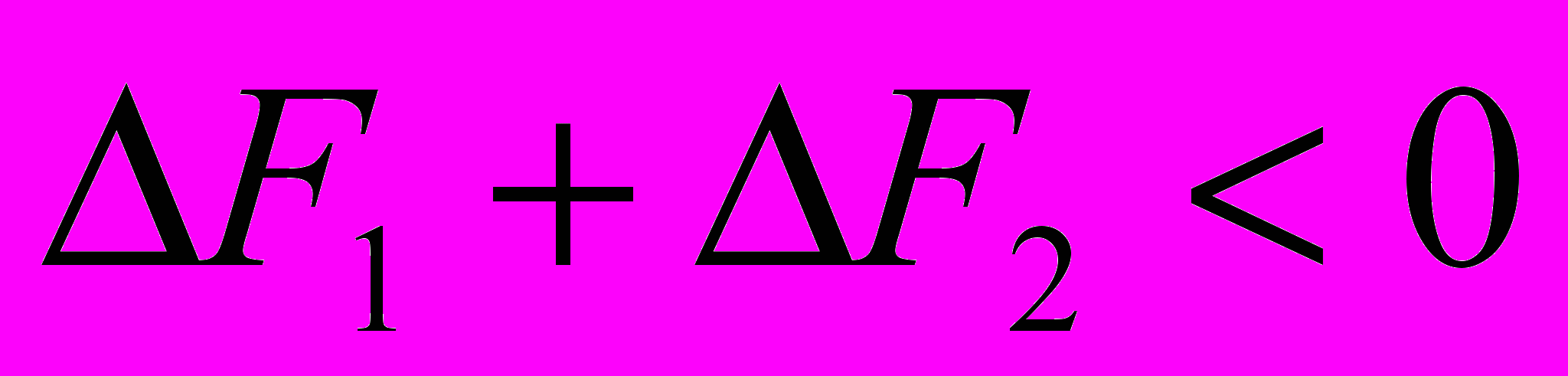 ).
).Как правило, в качестве экзергонического компонента при сопряжении выступает реакция гидролиза молекулы АТФ. При этом энергия передается как бы «из рук в руки»: один из партнеров «заряжается» энергией благодаря присоединению какой-либо части молекулы АТФ (реакции фосфорилирования, пирофосфорилирования, аденилирования), а затем осуществляется экзергоническое отщепление этой части с замыканием нужной ковалентной связи при синтезе дисахарида. Нередко сопряжение реализуется более сложно при сохранении общего принципа – суммарной экзергоничности двух (или более) реакций.
- Принцип энергетического барьера и снижение его
при «мягком» ферментативном катализе
Для каждой конкретной реакции перепад в свободной энергии определяет лишь направление превращения веществ и его стационарный (равновесный) уровень, но не скорость протекания процесса. Скорость явно экзергонического процесса может быть практически нулевой.
Для химических превращений, свойственных биосфере, величина барьеров (в отсутствие катализаторов) столь высока, что обмен веществ должен бы практически прекратиться, а сама жизнь – исчезнуть. Этого не происходит благодаря созданию в ходе эволюции высокоэффективных барьеропонижающих макромолекулярных катализаторов – ферментов.
В неживой природе протекание химической реакции происходит, как правило, в жестких условиях и осуществляется как бы взрывообразно, неупорядоченно. В противоположность этому метаболизм происходит в мягких условиях, без использования сильных воздействий. При этом молекулярный механизм ферментативной реакции строго детерминирован и неукоснительно выдерживается.
Значение ферментов в метаболизме огромно: за любым из химических превращений, присущих нормальному метаболизму биосферы, стоит свой конкретный фермент, так как в нормальном метаболизме практически нет неферментативных реакций.
- Принцип поэтапности химических превращений
в метаболических циклах
Метаболические превращения осуществляются через значительное количество промежуточных состояний. Это особенно характерно для биосинтетической ветви метаболизма, которая подобна работе в совершенстве отлаженного конвейера, когда конечный продукт создается серией строго последовательных операций. Биосинтез макромолекул из более простых происходит посредством множества последовательных модификаций исходного субстрата с передачей «обрабатываемой молекулы» от одного фермента к другому вдоль метаболической цепочки. Процесс протекает вплоть до заключительного фермента, выполняющего последнюю, завершающую операцию и выпускающего готовый продукт. При этом ферменты какого-либо одного конвейера часто организуются пространственно, формируя полиферментные комплексы. Наряду с линейными конвейерами в живой природе широко представлены и замкнутые метаболические циклы, в которых продукт последнего фермента является одновременно субстратом для первого. В разных точках цикла могут быть развилки и состыковки с другими метаболическими путями. Метаболические циклы широко представлены в катаболической, деструктивно-окислительной ветвях метаболизма. Например, цикл Кребса, предназначенный для окисления (с извлечением энергии) двухуглеродных фрагментов, образующихся при деструкции углеводов, липидов или белков. В целом для катаболизма характерно так называемое «правило воронки»: разные сложные соединения дробятся с образованием простых унифицированных фрагментов, которые затем перерабатываются в одном и том же цикле Кребса и в дыхательной цепи, осуществляющей окислительное фосфорилирование.
2.2.5 Принцип полимерных основ жизни
Биополимеры – главная молекулярная основа жизни для всей биосферы. Для нуклеиновых кислот и полисахаридов характерно огромное разнообразие. Особенно различны по свойствам белки.
Практически неограниченное разнообразие биополимеров, необходимое для обеспечения всех потребностей такого сложного «химического производства», как клетка (организм), а также для передачи по наследству признаков индивидуальности, реализуется на мономерной базе. Так, белки построены из 20 типов аминокислот, ДНК – из четырех мононуклеотидов, число основных моносахаридов, из которых состоят все природные полисахариды, также невелико (около десяти).
2.2.6 Принцип узкой функциональной специализации биомолекул
Каждая биомолекула в клетке способна выполнять одну конкретную функцию. Прежде всего, это касается крупномасштабного разделения функций в сфере макромолекулярных основ жизни – белков и нуклеиновых кислот. Биологическое назначение этих двух основополагающих для всего живого классов биополимеров четко разграничено. Сфера действия нуклеиновых кислот: хранение генетической информации, передача ее потомству и реализация в фенотип в ходе индивидуального развития посредством управления синтезом всех белков. Функция белков – выполнение всех элементарных рабочих операций, составляющих суть метаболизма, и вообще всех проявлений жизнедеятельности на молекулярном уровне.
Разделение функций продолжается и в пределах каждого из этих двух классов биополимеров. ДНК ответственна за хранение и выдачу информации, три группы РНК – мРНК, рРНК и тРНК – за разные этапы синтеза огромного количества белков с использованием взятой от ДНК четкой, однозначной инструкции. Велика дифференциация и в мире белков: они выполняют ферментативные, транспортные, биоэнергетические, структурные и регуляторные функции. Специализация этим не ограничивается. Так, каждый из многих тысяч белков катализирует вполне конкретное биохимическое превращение. Принцип специализации также широко представлен среди средних и малых биомолекул. Одни из них обслуживают ферментативные превращения (коферменты), другие – энергетику (АТФ), третьи – регуляторные контуры (циклические нуклеотиды, стероидные гормоны).
У многоклеточных организмов часто встречается ситуация, когда метаболизм отдельных клеток настроен на преимущественное выполнение небольшого числа биохимических функций: синтез антител у лимфоцитов, гормонов – у клеток желез внутренней секреции, липидный обмен в адипоцитах. Сверхпродуценты широко представлены и среди микроорганизмов (например, антибиотиков, органических кислот, спиртов и т.д.).
Благодаря такой высокой специализации функций биомолекул, их специфичности жизнь остается жизнью, избегает хаоса и неразберихи, оказывается способной воспроизводить себя как в онтогенезе, так и в филогенезе.
2.2.7 Принцип геометрического соответствия
или комплементарности как основа специфичности
Сущностью специализации молекул, высокой избирательности, специфичности их действия, начиная от способности ферментов выполнять строго определенную химическую операцию над определенным субстратом и кончая генетическими функциями репликации нуклеиновых кислот и считывания с них информации, является принцип геометрического соответствия или комплементарности (принцип узнавания). Этот принцип присущ всей биологии вообще и определяет правильность взаимодействия биополимеров как между собой, так и с малыми (средними) молекулами.
В биомолекулах находятся участки, по геометрической форме соотносящиеся между собой как ключ с замком. Геометрическое соответствие, как правило, дополняется и силовым соответствием, в том смысле, что и в «ключе», и в «замочной скважине» в нужных местах расположены функциональные группы, имеющие высокое взаимное сродство, например, противоположно заряженные участки. В результате установления межмолекулярного контакта, «комплементарное спаривание» сопровождается значительным падением свободной энергии системы, а партнеры по взаимодействию обладают высоким сродством друг к другу. Геометрическое соответствие прослеживается, например, при взаимодействии активных центров ферментов с субстратами, с их регуляторами (модуляторами) в процессах репликации ДНК, транскрипции и трансляции, при взаимодействии гормонов, токсинов и других подобных соединений с соответствующими рецепторами клетки, при специфическом взаимодействии: «клетка – клетка», «клетка – вирус».
Подобно тому, как сейфы снабжаются особо сложными замками, так и наиболее критические процессы жизнедеятельности включают в себя обширные (по протяженности контакта) и сложные (по рельефу) зоны комплементарности, представленные к тому же на каждой стадии многоэтапного процесса (например, биосинтеза белка). Банк «генетической информации» – макромолекула ДНК – подвержен постоянно действующему контролю на геометрическое соответствие с помощью бегающих по полинуклеотидным цепям ферментов темновой репарации, которые устраняют поломки.
Принцип узнавания проявляется и в конкурентной, межвидовой борьбе. Так, у микроорганизмов антагонистические взаимоотношения осуществляются с помощью выделения специфических веществ (бактериоцинов), которые связываются с рецепторами поверхности клетки-конкурента и вызывают ее гибель.
Комплементарность – мощный и непрерывно действующий инструмент наведения порядка в хаосе случайных недетерминированных соударений молекул в процессах тепловой диффузии, обеспечивающий правильность передачи генетической информации от родителей к детям, адекватность построения организма из зиготы в процессе синтеза, специфичность и тонкую регулируемость всего метаболизма клетки и организма.
2.2.8 Принцип генетического кода
Информация о наследственных свойствах организма, независимо от его размеров и сложности, размещена внутри одной или небольшого числа молекул ДНК последовательно в виде четырех типов мономеров (нуклеотидов) вдоль полинуклеотидной цепи. В ДНК закодировано химическое строение всех без исключения белков организма, причем различные сочетания трех соседних нуклеотидов (триплеты) кодируют 20 разных аминокислот белка, а последовательность триплетов кодирует последовательность расположения аминокислот в полипептидной цепи белка. Генетический код универсален для всей биосферы (от микроба до человека), что указывает на единство происхождения жизни. Столь же едины молекулярные механизмы дешифровки кода в ходе онтогенеза (транскрипция, трансляция) и безошибочной передачи записанной информации потомству (репликация ДНК).
2.2.9 Принцип структурированности и компартментализации
Во избежание смешивания реагентов множества одновременно протекающих реакций, требующих несовместимых, взаимоисключающих физико-химических условий, различные метаболические блоки и циклы размещены не равномерно в пределах клеточного пространства, а сконцентрированы в его определенных участках, компартментах – надмолекулярных структурах, т.е. структурированы. Речь идет о локализации соответствующих полиферментных ансамблей как в различных органеллах, так и в определенных участках мембран этих органелл и плазматической мембраны клетки. Компартментализация и структурированность ферментов одного и того же цикла на мембранной матрице способствуют: их производительности и эффективной работе благодаря созданию оптимальных для катализа физико-химических условий и пространственному сближению между собой партнеров ферментативного конвейера таким образом, что «полуфабрикат» переходит от одного фермента к другому как бы «из рук в руки», а не в результате безадресной диффузии; тонкому управлению работой сразу всего ансамбля ферментов благодаря изменению свойств мембранной матрицы (вязкости, упорядоченности, проницаемости, электрического потенциала).
Ферментативные конвейеры структурированы таким образом, чтобы обеспечить наилучшие условия для протекания всего многоэтапного процесса метаболизма в желательном направлении.
2.2.10 Принцип иерархии контуров регуляции и обратных связей
Кибернетические принципы управления сложными системами являются древним изобретением живой природы и служат ей давно и успешно. В каждой клетке (и организме) есть множество регуляторных контуров различной протяженности. Действие их основано по принципу отрицательной (реже положительной) обратной связи. Они способны, с одной стороны, обеспечить гармонию и согласованность в текущем метаболизме, в процессах функционирования и развития (онтогенеза), а с другой – адекватно реагировать на разнообразные изменения во внешней среде, в том числе и биологической природы. Отмечена строгая иерархическая подчиненность этих контуров и невмешательство высшего по рангу контура в дела низшего до тех пор, пока он сам успешно справляется с текущими потребностями клетки (организма). Так, в каждой клетке работают регуляторные контуры, управляющие активностью имеющегося в ней набора ферментов, транспортных и механохимических систем без изменения их численности, и регуляторные контуры, связанные с биосинтезом определенных белков. Первые управляются набором активаторов, трансдукторов или ингибиторов, непосредственно воздействующих на белки; вторые – через индукцию или репрессию генетического аппарата биосинтеза на уровнях транскрипции или трансляции. Благодаря макромолекулярной природе ферментов, их способности изменять структуру под действием разнообразных сигналов, а также генетическому управлению процессом биосинтеза создаются условия для самонастройки и регуляции всего спектра реакций метаболизма.
У высших животных (и человека) сформирована совершенная, многоуровневая регуляция физиолого-биохимических процессов – гормональная и нервная, обеспечиваемая множеством обратных связей. Как правило, сигналом к перестройке метаболической активности клетки служит стереоспецифическая сорбция регуляторной молекулы на рецепторе плазматической мембраны на поверхности клетки.
Перечисленные принципы имеют ясный энергетический или геометрический смысл и не требуют введения каких-либо новых, свойственных только живой материи физико-химических законов. В сочетании с законами биологической эволюции и естественного отбора они позволяют понять организацию и функционирование молекулярных машин в живой природе.
2.2.11 Вопросы для самоподготовки
- Какова природа основной формы энергии, используемой в процессах жизнедеятельности, и благодаря чему могут эффективно протекать эндергонические химические превращения?
- В чем главная причина, определяющая скорость любой реакции?
- Превращается ли в клетке простая молекула в сложную постепенно (или наоборот) в ходе только одного химического акта?
- В чем биологический смысл специализации биомолекул и геометрического соответствия, комплементарности?
- Для чего нужны структурированность и компартментализация биохимической работы клетки?
- Каким образом осуществляется регуляция биохимических процессов и для чего она нужна?
