Оглы функциональная морфология органов иммунной системы при хронической наркотической зависимости 14. 03. 02 патологическая анатомия 14. 03. 05 судебная медицина
| Вид материала | Автореферат |
- Рабочая программа учебной дисциплины патологическая анатомия, клиническая патологическая, 480.03kb.
- Общая патологическая анатомия, 283.39kb.
- Патологическая анатомия и дифференциальная диагностика рака большого сосочка двенадцатиперстной, 388.21kb.
- Примерная программа наименование дисциплины Патологическая анатомия, клиническая патологическая, 594.5kb.
- Скачко Борис Система оздоровления доктора Скачко при снижении иммунитета, синдроме, 145.55kb.
- Библиография и ссылки «Анатомия и морфология растений», 6.79kb.
- Промоторова Курс «Анатомия и морфология человека», 117.42kb.
- Примерная программа по дисциплине патологическая анатомия для аттестации на категорию., 363.01kb.
- Ф-программа вступительного экзамена в аспирантуру Утверждаю, 254.47kb.
- Патологическая анатомия это медико-биологическая наука, изучающая структурные и морфологические, 1590.52kb.
На правах рукописи
ГАСАНОВ АДАЛЯТ БЕЙБАЛА ОГЛЫ
Функциональная морфология
органов иммунной системы при
хронической наркотической зависимости
14.03.02 – патологическая анатомия
14.03.05 - судебная медицина
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Москва – 2010

Р
 абота выполнена в Учреждении Российской академии медицинских наук Научно-исследовательском институте морфологии человека РАМН и в Азербайджанском медицинском университете
абота выполнена в Учреждении Российской академии медицинских наук Научно-исследовательском институте морфологии человека РАМН и в Азербайджанском медицинском университетеНаучные консультанты:
доктор медицинских наук, профессор Зайратьянц
Олег Вадимович
член-корреспондент РАМН, Пиголкин
доктор медицинских наук, профессор Юрий Иванович
Официальные оппоненты:
доктор медицинских наук, профессор Пархоменко
Юрий Георгиевич
доктор медицинских наук, профессор Раденска-Лоповок
Стефка Господиновна
доктор медицинских наук, профессор Дубровин
Иван Александрович
Ведущее учреждение: ГОУ ВПО «Российский Государственный медицинский университет»
Защита диссертации состоится «_17 _» _июня 2010 г. в 12 часов на заседании диссертационного совета Д 001.004.01 Научно-исследовательского института морфологии человека РАМН по адресу; 117418, Москва, ул. Цюрупы, д. 3.
С диссертацией можно ознакомиться в библиотеке института
Автореферат разослан «_____» ____________ 2010 г.
Ученый секретарь
диссертационного совета, Михайлова
доктор медицинских наук Лилия Петровна
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Наркомания (хроническая наркотическая зависимость или интоксикация - ХНИ) – это групповое понятие, объединяющее хронические прогредиентные заболевания, вызванные употреблением наркотических средств (НС). Она характеризуется фазным течением и развитием синдромов психической зависимости, изменения толерантности к НС с тенденцией к увеличению доз, физической зависимости, а при прекращении их приема - абстиненции [Пятницкая И.Н., 1994; Рохлина М.Л., 2002; Кошкина Е.А., Киржанова В.В., 2008; Иванец Н.Н., 2008]. На основе особенностей развития и течения ХНИ, обусловленной разными НС, принято выделять три ее основных вида (опиатную, каннабиноидную, кокаиновую), а также полинаркоманию [Пиголкин Ю.И., Богомолов Д.В., 2002, Иванец Н.Н., 2008й степени].
Распространение наркомании – серьезная медико-социальная проблема, которая за последние десятилетия стала представлять угрозу безопасности России и ряда других стран. Уровень потребления НС считают влияющим на генофонд, если наркотики потребляют более 5% населения. В настоящее время в мире насчитывается около 200 млн. наркопотребителей, средняя продолжительность жизни наркоманов не превышает 10 лет, а излечиваются, т.е. не употребляют НС более года, всего 5-6%. Россия и Азербайджан занимают одни из первых мест в мире по числу наркопотребителей (около 4% населения), темпам роста их числа (в 20 раз за последние 20 лет), омоложению наркомании (в России 20% наркопотребителей моложе 16 лет), а также по распространению инъекционного употребления НС, прежде всего героина (в России – до 90% наркоманов) [Позднякова М.Е., 2002; Иванец Н.Н., 2008; Иванов В.П., 2008]. По сравнению с Россией, в Азербайджане средний возраст наркопотребителей выше (около 30% старше 35 лет) и крайне редко наркоманами становятся женщины [Эфендиев М., 2008].
Значительную проблему для здравоохранения при наркомании представляют не только отравления НС, но и инфекционные и другие заболевания, развивающиеся на фоне вторичного иммунодефицитного синдрома (ВИДС), от которых погибает до половины наркоманов. Типичны гемоконтактные инфекции (при инъекционных видах наркомании), инфекционные эндокардиты («героиновый» эндокардит), болезни органов дыхания, туберкулез, микозы (кандидоз), гнойно-воспалительные поражения кожи и мягких тканей, урогенитальные инфекции, болезни, передаваемые половым путем [Сорокина В.В., 2004; Risdahl J.M. et al., 1998; Roy S. et al., 1998; Mathias R., 1999; Saunders J.B., Richards A.H., 2002; Ocasio F.M. et al., 2004; Mathew J. et al., 2005; Cabral G.A., 2006; Friedman H., 2006].
Патогенез ВИДС при ХНИ связывают с прямым токсическим или опосредованным специфическими рецепторами влиянием НС и примесей к ним на клетки ИС и других органов и тканей (эффект зависит от путей и длительности их введения, генетической предрасположенности); поражением нейроиммуномедиаторных систем ЦНС и синдромом полиэндокринопатии с нарушением нейроэндокринных регуляторных механизмов ИС; инфекционными факторами и иммуногенными примесями к инъекционным НС; асоциальным образом жизни, сочетанием с хронической алкогольной интоксикацией (ХАИ), алиментарными и другими факторами [Солодун Ю.В. и соавт., 2001; Пиголкин Ю.И., Богомолов Д.В., 2002; Рисберг В.Ю., 2002; Иванец Н.Н., 2008; Roy S. et al., 2005].
Особенности ВИДС при наиболее распространенных видах ХНИ (опиатной, каннабиноидной и полинаркомании) изучены недостаточно. ВИДС при опиатной ХНИ проходит стадии становления, компенсации (за счет гуморального звена ИС) и декомпенсации, длительность которых индивидуальна; характеризуется повышенным апоптозом лимфоцитов, дефицитом Т-хелперов с инверсией иммунорегуляторного индекса, снижением количества NK-клеток, нарушением антителогенеза, фагоцитоза, цитокинового и хемокинового баланса [Мотавкина Н.С., Шаркова В.А., 2002; Рисберг В.Ю., 2002; Иванец Н.Н., 2008; Rezza G. et al., 1997; Friedman H. et al., 2003; Lok S.F., McMahon B., 2007]. Типично появление антител к морфину и эндогенным опиоидным пептидам, что используется как диагностический тест, возможны аутоиммунные поражения [Рисберг В.Ю., 2002; Иванец Н.Н., 2008]. При каннабиноидной ХНИ иммунные нарушения значительно менее выражены. Δ9-тетрагидроканнабиол и другие вещества, выделенные из конопли, нарушают функции Т- и В-лимфоцитов, NK-клеток, макрофагов (феномен каннабиноид-обусловленной иммунотоксичности), но обладают и дозозависимым иммуностимулирующим эффектом [Мотавкина Н.С., Шаркова В.А., 2002; Шаркова В.А., Катенкова Э.Ю., 2007; McKallip R.J. et al., 2002; Lok S.F., McMahon B., 2007]. При полинаркомании ВИДС наиболее выражен и сходен с развивающимся при опиатной ХНИ [Шаркова В.А., Катенкова Э.Ю., 2007].
Изучение структурных основ иммунных нарушений и их особенностей при разных видах ХНИ является актуальной задачей судебно-медицинской и патологоанатомической практики. Однако такие исследования немногочисленны, а полученные результаты противоречивы. При лучше изученной опиатной ХНИ, по данным одних авторов развивается генерализованная атрофия, других – сочетание атрофии Т-зон с гиперплазией В-зон лимфоидной ткани [Пиголкин Ю.И. и соавт., 2000; Кригер О.В. и соавт., 2001; Лунькова Л.К. и соавт., 2002; Орловская А.В. и соавт., 2004; Сорокина В.В., 2004; Risdahl J.M. et al., 1998; McCarthy et al., 2001]. В 80-е годы были описаны «асимптомная лимфаденопатия» и спленомегалия у опиатных наркоманов. Однако в настоящее время принято считать, что такие изменения представляют собой результат не диагностированных ВИЧ-инфекции или вирусных гепатитов [Кригер О.В. и соавт., 2001; Сорокина В.В., 2004; Иванец Н.Н., 2008; Toccanier M.F., Kapanci Y., 1985]. Единичные исследования патологической анатомии ИС при других видах ХНИ не выявили каких-либо особенностей, кроме меньшей (при каннабиноидной) или большей (при полинаркомании) тяжести изменений по сравнению с опиатной [Иванец Н.Н., 2008; Ou D.W. et al., 1997]. Недостаток знаний о морфологическом субстрате, морфогенезе и особенностях иммунных нарушений при разных видах ХНИ затрудняет разработку методов ее профилактики и лечения, а также морфологическую диагностику ее видов.
Учитывая тесную связь между иммунной и нейро-эндокринной системами, важную роль нейро-эндокринной патологии в патогенезе иммунных нарушений при наркомании, морфологические исследования ИС при ХНИ должны включать в себя одновременное изучение органов эндокринной системы. Их морфология при разных видах ХНИ остается недостаточно исследованной, хотя понимание изменений, в частности, гипофиза, надпочечников и щитовидной железы, может играть большую роль в раскрытии особенностей ВИДС при разных видах ХНИ. В единичных исследованиях, главным образом, при опиатной ХНИ, описаны неспецифические острые и хронические изменения эндокринных органов, причем ряд авторов объясняет их развитие влиянием инфекционных заболеваний, а не действием НС [Кригер О.В. и соавт., 2001; Friedman H. et al., 2001, 2003, 2005; Lok S.F., McMahon B., 2007]. Все сказанное выше определяет актуальность работы, служит обоснованием ее цели и задач.
Цель исследования
Изучить функциональную морфологию органов иммунной и эндокринной систем при хронической наркотической интоксикации и разработать критерии морфологической диагностики ее видов.
Задачи исследования
1. Изучить функциональную морфологию органов иммунной и эндокринной систем в разные сроки опиатной хронической наркотической интоксикации.
2. Исследовать функциональную морфологию органов иммунной и эндокринной систем в разные сроки каннабиноидной хронической наркотической интоксикации.
3. Изучить функциональную морфологию органов иммунной и эндокринной систем в разные сроки хронической полинаркомании.
4. Провести сравнительный анализ функционально-морфологических изменений и особенностей морфогенеза поражения органов иммунной и эндокринной систем при опиатной, каннабиноидной и полинаркомании, их сочетания с хронической алкогольной интоксикацией, вирусными (гепатиты В и С) и бактериальными инфекционными заболеваниями.
5. Разработать для внедрения в патологоанатомическую и судебно-медицинскую практику морфологические критерии диагностики различных видов хронической наркотической интоксикации в зависимости от особенностей изменений органов иммунной и эндокринной систем.
Научная новизна
Впервые с использованием комплекса морфологических методов исследования (гистологического, иммуноморфологического и морфометрического) охарактеризована патологическая анатомия вторичного иммуннодефицитного синдрома и изучен морфогенез поражения органов иммунной системы при наиболее социально значимых и распространенных видах наркомании (опиатной, каннабиноидной и полинаркомании).
Изучены структурные основы синдрома полиэндокринопатии при опиатной, каннабиноидной и полинаркомании и установлена связь поражения гипофиза, надпочечников и щитовидной железы с иммунными нарушениями.
Впервые показаны особенности морфологических изменений органов иммунной и эндокринной систем при сочетании разных видов наркомании с хронической алкогольной интоксикацией и алкоголизмом, вирусными (гепатиты В и С) и бактериальными инфекционными заболеваниями.
Впервые морфологически доказано, что опиатная наркомания отличается стадийным характером развития иммунных и эндокринных нарушений с дефицитом Т-хелперов, инверсией иммунорегуляторного индекса, нередко с гиперплазией В-зон лимфоидной ткани и формированием лимфоидных фолликулов с нарушенной архитектоникой, генерализованной лимфаденопатией и спленомегалией, сходных с наблюдаемыми при ВИЧ-инфекции. Показано, что при сочетании хронической наркотической интоксикации с вирусными гепатитами В и С более выражена гиперплазия В-зон, особенно селезенки и лимфатических узлов ворот печени. При сочетании опиатной наркомании с хронической алкогольной интоксикацией, бактериальными инфекциями характерна выраженная атрофия лимфоидной ткани.
При каннабиноидной наркомании иммунные и эндокринные нарушения развиваются только в результате многолетнего употребления наркотических средств при сочетании с хронической алкогольной интоксикацией, бактериальными инфекциями; не выявляются инверсия иммунорегуляторного индекса, стадийность развития иммунных и эндокринных нарушений, нарушение архитектоники лимфоидных фолликулов.
Полинаркомания отличается ранним формированием наиболее тяжелого синдрома вторичного иммунного дефицита с атрофией лимфоидной ткани, выраженным синдромом полиэндокринопатии, сходных с наблюдаемым при III стадии иммунных нарушений у опиатных наркоманов, но без стадийности развития изменений органов иммунной и эндокринной систем.
Практическая значимость
Изучена патологическая анатомия органов иммунной и эндокринной систем и разработаны морфологические критерии диагностики иммунных и эндокринных нарушений при опиатной, каннабиноидной и полинаркомании разной давности, в том числе, при их сочетании с хронической алкогольной интоксикацией, вирусными (гепатиты В и С) и бактериальными инфекционными заболеваниями.
Полученные данные о структурных основах синдромов вторичного иммунного дефицита и полиэндокринопатии при разных видах хронической наркотической интоксикации будут способствовать разработке новых методов профилактики и лечения опиатной, каннабиноидной и полинаркомании.
Предложенные морфологические критерии диагностики иммунных и эндокринных нарушений при разных видах наркомании (опиатной, каннабиноидной и полинаркомании) позволят повысить качество исследований в патологоанатомической и судебно-медицинской практике.
Основные положения, выносимые на защиту
1. Функциональная морфология органов иммунной и эндокринной систем при хронической опиатной, каннабиноидной и полинаркомании свидетельствует о развитии разных вариантов вторичного иммунодефицитного синдрома и синдрома полиэндокринопатии, а особенности их изменений следует использовать при морфологической диагностике разных видов наркомании в патологоанатомической и судебно-медицинской практике.
2. Опиатная наркомания отличается стадийным характером развития иммунных и эндокринных нарушений с дефицитом Т-хелперов, инверсией индекса Т-хелперы/Т-супрессоры, нередко с гиперплазией В-зон лимфоидной ткани и формированием лимфоидных фолликулов с нарушенной архитектоникой, генерализованной лимфаденопатией и спленомегалией, сходных с наблюдаемыми при ВИЧ-инфекции. При сочетании опиатной наркомании с вирусными гепатитами В и С более выражена гиперплазия В-зон, особенно селезенки и лимфатических узлов ворот печени, а с хронической алкогольной интоксикацией, бактериальными инфекциями – развивается выраженная атрофия лимфоидной ткани.
3. При каннабиноидной наркомании иммунные и эндокринные нарушения развиваются только в результате многолетнего употребления наркотических средств при сочетании с хронической алкогольной интоксикацией, бактериальными инфекциями; не выявляются стадийность развития иммунных и эндокринных нарушений, инверсия иммунорегуляторного индекса, гиперплазия В-зон лимфоидной ткани и формирование лимфоидных фолликулов с нарушенной архитектоникой.
4. Полинаркомания отличается ранним формированием наиболее тяжелого синдрома вторичного иммунного дефицита с атрофией лимфоидной ткани, выраженным синдромом полиэндокринопатии, сходных с наблюдаемым при III стадии иммунных нарушений у опиатных наркоманов, но без стадийности развития изменений органов иммунной и эндокринной систем.
Внедрение результатов работы в практику
Полученные результаты используются в практической работе Московского городского центра патологоанатомических исследований при Городской клинической больнице № 33 им. проф. А.А.Остроумова (Россия); Объединения «Судебно-медицинская экспертиза и патологическая анатомия» Минздрава Азербайджанской Республики. Материалы работы используются при чтении лекций и проведении практических занятий на кафедрах патологической анатомии ГОУ ВПО Московский государственный медико-стоматологический университет Росздрава, патологической анатомии и судебной медицины Азербайджанского медицинского университета и Азербайджанского Государственного института усовершенствования врачей им. А.Алиева.
Апробация работы
Основные положения диссертационной работы доложены и обсуждены на Научно-практической конференции, посвященной 85-летию патолого-анатомической службы НИИ Скорой Помощи им. Н.В.Склифосовского (Москва, 2005); II и III Съездах Российского общества патологоанатомов (Москва, 2006, Самара, 2009); I Съезде патологоанатомов Республики Беларусь (Минск, 2006); II Всероссийской конференции с международным участием «Клинико-морфологические аспекты эндокринопатий» (Белгород, 2006); XXVI International Congress of the International Academy of Pathology, Montreal, Quebec, Canada, 2006; III, IV Cappadocia Forensic Sciences Symposium (Avanos, Turkey, 2006, 2007); Научно-практической конференции с международным участием «Актуальные вопросы судебно-медицинской науки и практики на современном этапе» (Минск, Беларусь, 2007); V Всемирном Конгрессе по иммунопатологии и аллергии (Москва, 2007); 3rd Intercontinental Congress of Pathology, Barcelona, Spain, 2008; на межлабораторной конференции в Учреждении РАМН Научно-исследовательского института морфологии человека РАМН (Москва, июнь 2009 г.).
Публикации
По теме диссертации опубликовано 42 научные работы, в которых изложены основные положения диссертации, из них 10 – в Российских журналах, рекомендованных ВАК РФ и 2 – в международных журналах.
Структура и объем диссертации
Диссертация изложена на 390 страницах и состоит из введения, 4-х глав, общего заключения, выводов, практических рекомендаций и списка литературы. Список литературы содержит 437 источника, из которых 179 – отечественных и 258 – зарубежных авторов. Диссертация иллюстрирована 90 таблицами и 94 рисунками, графиками и схемами.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Морфологические исследования 355 аутопсийных наблюдений основной, контрольной и группы сравнения осуществляли в Учреждении РАМН Научно-исследовательский институт морфологии человека РАМН (директор – член-корр. РАМН, проф. Л.В.Кактурский), кафедрах судебной медицины (зав. – член-корр. РАМН, проф. Ю.И.Пиголкин) ГОУ ВПО Московская Медицинская Академия им. И.М.Сеченова Росздрава, патологической анатомии (зав. – проф. О.В.Зайратьянц) ГОУ ВПО Московский государственный медико-стоматологический университет Росздрава и Азербайджанского Медицинского Университета (зав. кафедрой – проф. М.Ш.Джангиров), в Объединении «Судебно-медицинская экспертиза и Патологическая анатомия» (директор – проф. Ш.М.Мусаев) Минздрава Азербайджанской Республики. Вскрытия производились в Объединении «Судебно-медицинская экспертиза и Патологическая анатомия» Минздрава Азербайджанской Республики, Московском городском центре патологоанатомических исследований при ГКБ № 33 им. А.А.Остроумова, НИИ СП им. Н.В.Склифосовского, ГКБ №№ 4, 50, 55 и др., танатологическом отделении № 6 Бюро СМЭ Департамента здравоохранения г. Москвы (зав. – к.м.н. А.Н.Кузин). В 88% случаев время от констатации смерти до начала проведения аутопсии не превышало 24 ч. Для групп сравнения и контрольной (85 умерших) были подобраны аутопсийные наблюдения, близкие по поло-возрастным особенностям основной группе (Табл. 1).
Таблица 1
Число наблюдений в основной, контрольной группах и группе сравнения
| Показатель | Группы наблюдений | Итого | ||
| Основная | Сравнения | Контрольная | ||
| Мужчины | 262 (97,0%) | 58 (89,2%) | 17 (85%) | 337 (94,9%) |
| Женщины | 8 (3,0%) | 7 (10,8%) | 3 (15%) | 18 (15,1%) |
| Всего | 270 (100%) | 65 (100%) | 20 (100%) | 355 (100%) |
Помимо образцов ткани, взятых из разных органов в ходе аутопсии в соответствие со стандартным протоколом проведения вскрытий, детально изучали органы ИС – тимус, селезенку, периферические и центральные лимфатические узлы (подмышечные, паховые, бронхопульмональные, парааортальные, брыжеечные и ворот печени), групповые и солитарные лимфоидные фолликулы кишечника, а также железы внутренней секреции, изменения которых наиболее важны для оценки состояния ИС – гипофиз, надпочечники и щитовидную железу.
В основную группу из ретроспективно изученных нескольких тысяч аутопсий умерших в 2001-2008 гг. наркоманов после тщательного отбора с учетом клинико-морфологических и судебно-химических данных были включены 270 наблюдений с наиболее распространенными и социально значимыми видами ХНИ (опиатной, каннабиноидной и полинаркомании). Из материала исследования были исключены наблюдения с ВИЧ-инфекцией, острыми или активными хроническими вирусными гепатитами, циррозами печени любой этиологии, гематологическими или онкологическими заболеваниями. Методом тонкослойной хроматографии в биопробах аутопсийного материала 1-й подгруппы основной группы (219 наблюдений опиатной ХНИ) был выявлен морфин (0,002-0,41 мг%) или морфин и компоненты героина (6-0-моноацетилморфин, кодеин); 2-й подгруппы (22 случая каннабиноидной ХНИ) – только каннабиноиды (транс-9-тетрагидроканнабинол и его метаболиты); 3-й подгруппы (29 случаев полинаркомании) – сочетание героина, транс-9-тетрагидроканнабинола и его метаболитов, препараты фенотиазинового ряда и т.д. Длительность ХНИ составила 0,5-10,5 лет (в среднем – 1,3±0,8 лет) и все наблюдения были разделены еще на 3 подгруппы: с наркоманией, длительностью менее года, от 1 до 2-х лет и 2 и более лет (Рис. 1). В изученном материале поло-возрастное распределение умерших от разных видов ХНИ соответствует показателям распространенности наркомании в России и Азербайджане. Мужчины составили 97%, женщины – 3%; возраст – 15-39 лет (средний – 26±0,6 лет), преобладали (43,3%) умершие в возрасте 21-25 лет (рис. 2 и 3).
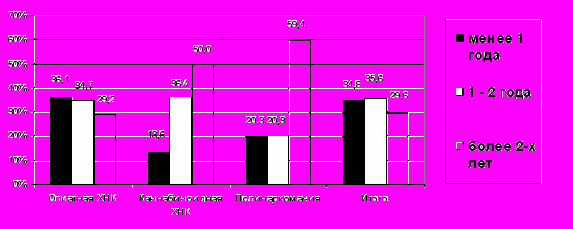
Рис. 1. Частота (%) наблюдений с различной длительностью ХНИ в разных подгруппах основной группы
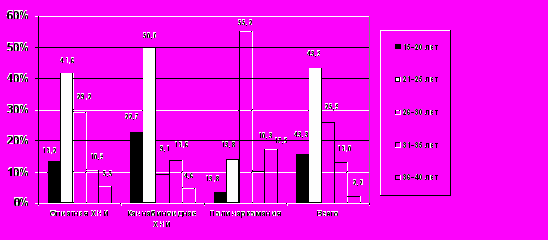 Рис. 2. Распределение (%) изученных наблюдений основной группы по возрасту
Рис. 2. Распределение (%) изученных наблюдений основной группы по возрасту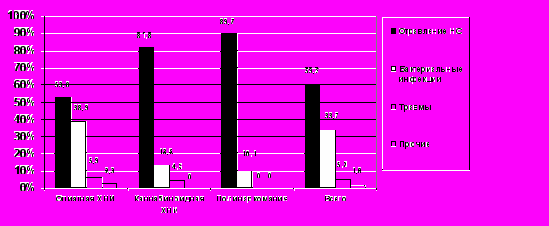
Рис. 3. Частота первоначальных причин смерти (%) в наблюдениях основной группы
Хроническая наркомания сочеталась с ХАИ или алкоголизмом по клинико-морфологическим данным в 23,7% наблюдений при опиатной ХНИ, в 18,2% – при каннабиноидной и в 100% – при полинаркомании (алкоголь в крови и/или моче – 0,03-4,6‰). Хронические неактивные вирусные гепатиты В или С выявлены при жизни и/или посмертно методом иммуноферментного анализа (на основании наличия HBsAg и антител к вирусу гепатита C) и морфологически в 88,6% наблюдений опиатной ХНИ, в 9,1% – каннабиноидной и в 88,5% – полинаркомании.
Группа сравнения включала 65 аутопсийных наблюдений умерших 62 мужчин и 3 – женщин в возрасте 21-42 лет (средний возраст 30±0,7 лет) с ХАИ или алкоголизмом (алкоголь в крови и/или моче – 0,03-6,2‰). Были исключены наркомания, ВИЧ-инфекция и вирусные гепатиты. Первоначальные причины смерти – отравление алкоголем на фоне ХАИ или алкоголизма (32,3%), алкогольные цирроз печени (16,9%), кардиомиопатия (15,4%), энцефалопатия (3,1%), туберкулез (6,2%) и др. (26,1%).
Контрольная группа состояла из 20 аутопсийных наблюдений умерших 18 мужчин и 2-х женщин в возрасте 16-35 лет (средний возраст – 32±0,8 лет) в результате механической травмы, не совместимой с жизнью (автотравмы, колото-резаных ранений, падения с высоты и др.), без заболеваний и экзогенных интоксикаций.
Методы исследования. Комплексное морфологическое исследование органов иммунной и эндокринной систем включало гистологический, гистохимические, иммуноморфологический и морфометрический методы. Материал фиксировали в 10% растворе нейтрального формалина, по стандартной методике обезвоживали в спиртах восходящей концентрации и заливали в парафин или целлоидин.
Гистологическое и гистохимическое исследования. Гистологические срезы толщиной 3-5 мкм окрашивали гематоксилином и эозином, пикрофуксином по ван Гизону. Выборочно проводили окраску суданом III (надпочечников), РAS-реакцию, реакцию Перлса (для выявления гемосидерина в селезенке), импрегнацию серебром по Футу (с целью определения границ внутридольковых периваскулярных пространств – ВПП тимуса [Зайратьянц О.В., 1991, 1992]). Лимфоидные фолликулы классифицировали по B.Kellner et al. (1966) и В.Л.Белянину и Д.Э.Цыплакову (1999), при изучении тимуса определяли степень его акцидентальной инволюции по классификации Т.Е.Ивановской (1996) и типы телец Гассаля по классификации О.В.Зайратьянца (1989).
Иммуноморфологическое исследование. Использовали депарафинированные срезы, непрямой иммунопероксидазный метод и 6 моно- и поликлональных антител (к нуклеопротеину Ki-67 - маркеру пролиферирующих клеток, антигенам CD4, CD8, IgG, IgM и IgA), изучали 55 образцов ткани тимуса, 81 – селезенки, 78 – лимфатических узлов и 51 – лимфоидных фолликулов кишечника. Гистологические срезы помещали на покрытые адгезивом (APES-ацетон) предметные стекла, эндогенную пероксидазу блокировали 3% перекисью водорода. Демаскировку антигенов производили по стандартной схеме (10-30 мин в микроволновой печи в 0,1 М растворе цитратного буфера, рH 6,0). После инкубации гистологических срезов с первичными антителами (рабочее разведение антисывороток – 1:50-100, время инкубации – 45-60 мин при температуре 37˚С), их обрабатывали вторичными биотилированными антикроличьими иммуноглобулинами. Для последующей визуализации результата реакции использовали авидин-биотиновый комплекс. Применяли фермент (пероксидазу хрена) в присутствии субстрата (перекиси водорода) и 3,3- диаминобензидина (все антитела и реагенты производства фирм Novocastra и DAKO, UK, Germany). Проводили общепринятые отрицательные и положительные контрольные процедуры на используемые реагенты и ткани.
Морфометрическое исследование. С помощью окулярной сетки Г.Г.Автандилова (1984) не менее, чем в 10 гистологических препаратах в 10 полях зрения (х200) в каждом определяли: в тимусе – удельную площадь паренхимы, стромы, коры, мозгового вещества, ВПП, телец Гассаля, в селезенке – лимфоидной ткани, ее Т- и В-зон, светлых центров лимфоидных фолликулов, в лимфатических узлах – Т- и В-зон, светлых центров лимфоидных фолликулов. При иммуноморфологическом исследовании подсчитывали число и соотношение Т-хелперов/индукторов (CD4+) и супрессоров/киллеров (CD8+), количество плазматических клеток, продуцирующих IgG, IgM и IgA, а также клеток (лимфоцитов, моноцитов и др.) с экспрессией в ядрах нуклеопротеина Ki-67. Подсчет клеток производили не менее, чем в 2-3-х гистологических препаратах в 10 полях зрения (х400) в каждом [Автандилов Г.Г., 1984, 1990, 1996].
Статистическую обработку материала проводили с помощью общепринятых методов вариационной статистики. Различия считались достоверными при 5% уровне значимости по таблице Стьюдента (р<0,05). Использовали пакет статистических программ «Statgraphix» (версия «Stadia») и статистическую компьютерную программу Statsoft Inc.99, USA.
