Гаврилин Сергей Викторович доктор медицинских наук профессор Волчков Владимир Анатольевич Ведущее учреждение: гоу дпо санкт-Петербургская медицинская академия последиплом
| Вид материала | Диплом |
- Хирманов Владимир Николаевич доктор медицинских наук профессор Карпищенко Анатолий, 277.9kb.
- Лазарев Сергей Михайлович доктор медицинских наук, профессор Баринов Владимир Семенович, 358.67kb.
- Кувакин Владимир Иванович Заслуженный деятель науки РФ доктор медицинских наук профессор, 361.78kb.
- Лучкевич Владимир Станиславович Доктор медицинских наук, профессор Кочорова Лариса, 358.38kb.
- Гембицкая Татьяна Евгеньевна профессор доктор медицинских наук Луговская Светлана Алексеевна, 231.82kb.
- Ключарева Светлана Викторовна доктор медицинских наук профессор Эмануэль Владимир Леонидович, 782.84kb.
- Котов Сергей Викторович доктор медицинских наук, профессор Савин Алексей Алексеевич, 547.92kb.
- Симерзин Василий Васильевич доктор медицинских наук, профессор Никитин Олег Львович, 452.7kb.
- Жирков Анатолий Михайлович доктор медицинских наук профессор Симбирцев Андрей Семенович, 418.79kb.
- Алексеев Владимир Николаевич доктор медицинских наук, профессор Николаенко Вадим Петрович, 172.08kb.
На правах рукописи
ШАТОВКИН
Кирилл Анатольевич
ГЕМОДИНАМИЧЕСКИЙ И ВОЛЮМЕТРИЧЕСКИЙ МОНИТОРИНГ У ПОСТРАДАВШИХ С ТЯЖЕЛОЙ ТЕРМИЧЕСКОЙ ТРАВМОЙ ПРИ НАРУШЕНИЯХ ГАЗООБМЕНА
14.01.20 – анестезиология и реаниматология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Санкт-Петербург
2011
Работа выполнена в ГУ СПб НИИ скорой помощи им. И.И. Джанелидзе
Научный руководитель:
доктор медицинских наук Шлык Ирина Владимировна
Официальные оппоненты:
доктор медицинских наук профессор Гаврилин Сергей Викторович
доктор медицинских наук профессор Волчков Владимир Анатольевич
Ведущее учреждение:
ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Федерального агентства по здравоохранению и социальному развитию»
Защита диссертации состоится «01» марта 2011 года в 13 часов на заседании совета по защите докторских и кандидатских диссертаций. Д 215.002.07 при ФГВОУ ВПО «Военно-медицинской академии им. С.М. Кирова» МО РФ (194044, г. Санкт-Петербург, ул. Академика Лебедева, 6)
С диссертацией можно ознакомиться в фундаментальной библиотеке ФГВОУ ВПО «Военно-медицинской академии им. С.М. Кирова» МО РФ
Автореферат разослан «___» января 2011 года
Ученый секретарь совета
доктор медицинских наук профессор
Богомолов Борис Николаевич
С О К Р А Щ Е Н И Я
ГФИ – глобальная фракция изгнания
ИВГОК – индекс внутригрудного объема крови
ИВСВЛ – индекс внесосудистой воды легких
ИВСВЛ/ИГКДО – расчетный индекс проницаемости легких
ИГКДО – индекс глобального конечно-диастолического объема
ИСЛЖ – индекс сократимости левого желудочка
ИТП – индекс тяжести травмы
ИУО – индекс ударного объема
КОД – расчетное коллоидно-онкотическое давление плазмы крови
ОПЛ – острое повреждение легких
ОРДС – острый респираторный дистресс-синдром
СИ – сердечный индекс
СОПЛ – синдром острого повреждения легких
СПОН – синдром полиорганной недостаточности
ЦВД – центральное венозное давление
AUC – площадь под кривой
BIPAP – двухфазное положительное давление в дыхательных путях
CPIS – клиническая шкала оценки инфекции легких.
DO2I – индекс доставки кислорода
FiO2 –концентрация кислорода на вдохе
LIS – шкала повреждения легких
O2ERI – индекс экстракции кислорода
PaO2 – парциальное напряжение кислорода в артериальной крови
PS – поддержка давлением
SaO2 – сатурация артериальной крови
ScvO2 – центральная венозная сатурация
SIMV –синхронизированная перемежающаяся принудительная вентиляция
SOFA – шкала последовательной оценки полиорганной недостаточности
VO2I – индекс потребления кислорода
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность исследования
Одной из наиболее сложных проблем в комбустиологии является лечение пострадавших с обширными ожогами и комбинированными поражениями дыхательных путей и кожи. Уже с момента получения травмы у данной категории пострадавших нарушается функционирование всех звеньев транспорта кислорода: внешнего дыхания, кровообращения и системы крови (Лупальцев В. И., Григорьева Т. Г., 2004, Клигуненко Е. Н., 2005, Hasselgren P. O., 2000). Кроме того, течение ожоговой болезни нередко осложняется развитием синдрома острого поражения легких (СОПЛ/ОРДС), который вызывают как прямые (ингаляционная травма), так и непрямые (ожоговый шок, токсемия, сепсис) повреждающие факторы (Киров М. Ю. с соавт., 2004).
Несмотря на определенные достижения в лечении больных с СОПЛ/ОРДС, летальность при этом виде осложнений, особенно у пострадавших с тяжелой термической травмой, остается достаточно высокой и достигает 50%–60% (Liffner G., 2005, Pallua N., 2006, Steinvall I., 2008). Подобное положение обусловлено во многом и тем, что синдромальный подход к диагностике нарушений газообмена в легких, основанный на оценке критериев, предложенных американо-европейской согласительной конференцией (AECC) в 1994 году, позволяет объединить пациентов с различными механизмами (легочные, внелегочные) развития гипоксемии, требующими дифференцированного подхода к терапии развившегося осложнения. Проведение инфузионно-трансфузионной терапии у тяжелообожженных с нарушениями газообмена представляет определенные сложности, вызванные, прежде всего, невозможностью точной оценки потерь жидкости с обширных ожоговых поверхностей и экстравазации ее в интерстициальное пространство, необходимостью поддержания оптимального уровня доставки кислорода и существующем при этом риске развития отека легких и компартмен-синдрома. Все это обуславливает актуальность дальнейшего изучения патогенеза, возможности ранней диагностики СОПЛ/ОРДС и мониторирования состояния пострадавшего с последующей оптимизацией интенсивной терапии.
Цель исследования
Изучение механизмов развития нарушений газообмена у тяжелообожженных на основании оценки данных инвазивного мониторинга гемодинамики и водного баланса организма для определения основных направлений интенсивной терапии развившихся осложнений.
Задачи исследования
- Изучение гемодинамики, волемического статуса и транспорта кислорода у тяжелообожженных с нарушениями газообмена c использованием метода изолированной транспульмональной термодилюции.
- Уточнение механизмов развития нарушений газообмена у пострадавших с тяжелой термической травмой в различные периоды ожоговой болезни.
- Определение информативности гемодинамических и волюметрических показателей для ранней диагностики повреждения легких у тяжелообожженных.
- Оценка информационной значимости индекса проницаемости легочных сосудов для прогнозирования развития и тяжести течения острого повреждения легких (ОПЛ), синдрома полиорганной недостаточности (СПОН) у тяжелообожженных с генерализованными инфекционными осложнениями.
- Разработка алгоритма интенсивной терапии тяжелообожженных, основанного на оценке данных гемодинамического и волюметрического мониторинга.
Научная новизна исследования
На основании клинико-лабораторных данных, показателей гемодинамического и волюметрического мониторинга определены основные механизмы нарушений газообмена у тяжелообожженных.
Показано, что в остром периоде ожоговой болезни нарушения газообмена не связаны с накоплением внесосудистой воды в легких и обусловлены ухудшением транспорта кислорода на фоне ожогового шока. В постшоковом периоде ожоговой болезни гипоксемия связана с развитием некардиогенного отека легких на фоне нарушения сосудистой проницаемости, индуцированного развитием генерализованных инфекционных осложнений.
Обоснована клиническая значимость волюметрических показателей, получаемых с использованием методики транспульмональной термодилюции для дифференциальной диагностики нарушений газообмена у пострадавших с тяжелой термической травмой.
Показана информационная значимость расчетного индекса проницаемости сосудов легких (ИВСВЛ/ИГКДО) для прогнозирования развития ОПЛ, СПОН и исхода травмы.
На основании оценки данных инвазивного гемодинамического и волюметрического мониторинга определены оптимальные значения показателей объемной преднагрузки в зависимости от степени нарушения сосудистой проницаемости, разработан лечебно-тактический алгоритм, направленный на оптимизацию интенсивной терапии у обожженных с нарушениями газообмена.
Практическая значимость работы
Определены информативные показатели мониторинга гемодинамики, волемического статуса, клинико-лабораторного исследования крови, позволяющие дифференцировано подходить к диагностике нарушений газообмена у тяжелообоженных.
Определены оптимальные пороги значений расчетного индекса проницаемости сосудов легких (ИВСВЛ/ИГКДО), обладающие высокой чувствительностью и специфичностью при прогнозировании развития СОПЛ, СПОН.
Оценена информативность индекса глобального конечно-диастолического объема (ИГКДО), как показателя, характеризующего уровень волемии.
Разработан лечебно-тактический алгоритм, основанный на оценке данных гемодинамического и волюметрического мониторинга.
Основные положения, выносимые на защиту
- Пострадавшие с тяжелой термической травмой имеют различный патогенез нарушений газообмена в зависимости от периода ожоговой болезни. В первые 72 часа после травмы гипоксемия вызвана нарушениями кровообращения и гипоперфузией легких на фоне ожогового шока. В более поздние сроки респираторные нарушения у тяжелообожженных связаны с изменением сосудистой проницаемости и накоплением внесосудистой воды легких на фоне генерализованных инфекционных осложнений.
- Комплексный подход к диагностике нарушений газообмена у тяжелообожженных, основанный на оценке клинико-лабораторных данных, а также показателей инвазивного гемодинамического и волюметрического мониторинга, позволяет дифференцировать различные механизмы развития гипоксемии и прогнозировать тяжесть течения СОПЛ.
- Использование инвазивного гемодинамического и волюметрического мониторинга с помощью технологии PiCCOplus создает предпосылки для индивидуализации лечебного алгоритма у пострадавших с тяжелой термической травмой при нарушениях газообмена.
Реализация результатов исследования
Разработанные способы диагностики и лечения, пострадавших с тяжелой термической травмой внедрены в практическую работу отдела термических повреждений НИИ СП им. И. И. Джанелидзе. Принципы проведения гемодинамического и волюметрического мониторинга внедрены в учебный процесс и изучаются на практических занятиях врачами-интернами и клиническими ординаторами.
Апробация диссертации
Результаты работы доложены на Международной конференции «Актуальные проблемы термической травмы» Санкт-Петербург, 2006; Х Съезде анестезиологов и реаниматологов, 2006; VII межрегиональной научно-практической конференции «Искусственное питание и инфузионная терапия больных в медицине критических состояний, Великий Новгород, 2007; II съезде комбустиологов России, Москва, 2008; XI съезде анестезиологов и реаниматологов, Санкт-Петербург, 2008; X Межрегиональной научно-практической конференции «Искусственное питание и инфузионная терапия больных в медицине критических состояний», Санкт-Петербург 2009; Конференции «Технологии жизнеобеспечения при критических состояниях», Москва, 2010; на XII Съезде Федерации анестезиологов и реаниматологов, Москва, 2010. Сделаны постерные доклады на 30 Международном симпозиуме по интенсивной терапии и неотложной медицине, Брюссель, 2010; на 15 Международном конгрессе по лечению ожоговой травмы, Стамбул, 2010. Апробация диссертации состоялась на заседании Ученого совета НИИ скорой помощи им И.И. Джанелидзе 24 декабря 2010 г.
Публикации
По материалам диссертации опубликованы 14 научных работ в отечественных и зарубежной медицинской литературе.
Объем и структура работы
Диссертация изложена на 165 страницах машинописного текста, состоит из введения, четырех глав (обзор научной литературы, характеристики материала и методов исследования, результаты собственных исследований, обсуждение полученных результатов), заключения, выводов и практических рекомендаций, списка использованной литературы. Текст иллюстрирован 25 рисунками и 37 таблицами. В списке литературы приведены 253 работы, из которых 66 отечественных и 187 иностранных авторов.
СОДЕРЖАНИЕ РАБОТЫ
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Для реализации цели и задач, стоящих перед исследованием, было обследовано 57 пострадавших (46 мужчин и 11 женщин), в возрасте от 18 до 62 лет, находившихся на лечении в ожоговой реанимации НИИ СП им. И. И. Джанелидзе в период с 2007-2010 г.г. Все наблюдения сделаны в ходе проспективного исследования.
Критериями включения в исследование являлось снижение индекса оксигенации менее 300 мм рт. ст. у пострадавших с ожогами кожи на площади более 30% поверхности тела и/или поражениями дыхательных путей продуктами горения тяжелой степени.
Среди пациентов, вошедших в исследование, преобладали мужчины (80,7%) с обширными ожогами кожи на площади от 30% до 65% поверхности тела. Средний возраст обследованных составил 36,1±11,6. По этиологическому фактору преобладали ожоги пламенем (75%), ожоги горячей водой составили 21%, электротравма с ожогами пламенем вольтовой дуги – 3,5%.
Среди включенных в исследование 14% составили пострадавшие с изолированными ожогами кожи и 86% – обожженные с комбинированной термоингаляционной травмой, у которых ожоги кожи сочетались с термохимическим поражением дыхательных путей различной степени тяжести. Интегральный индекс тяжести повреждения составлял от 72 до 163 усл. ед., что свидетельствовало о сомнительном и неблагоприятном прогнозе для жизни.
В зависимости от периода развития гипоксемии, все обследованные были разделены на 2 группы. Первую группу составили пострадавшие, у которых нарушения газообмена развились на 1–3 сутки после травмы, в периоде ожогового шока.
Во вторую группу вошли пострадавшие, которые были включены в исследование в более поздние сроки на 4–36 сутки после травмы. У них нарушения газообмена развивались на фоне тяжелого сепсиса и септического шока. Сравнительная характеристика пострадавших различных групп представлена в таблице 1.
Таблица 1
Характеристика групп пострадавших
| Показатели | Группа I (n=10) | Группа II (n=47) |
| Возраст | 31,7±12,2 | 36,6±11 |
| Пол, ж/м | 1/9 | 10/37 |
| Общая площадь ожогов кожи | 47±15 | 49±16 |
| Площадь глубоких ожогов | 23±13 | 25±17 |
| ИТП, усл. ед. | 107±10,6* | 120±18 |
| Прогностический индекс | -0,05 (-0,6;0,3)* | -0,2 (-0,3;-0,2) |
| Без ингаляционной травмы, чел. | 1 (10%)* | 7 (14,8%) |
| С ингаляционной травмой, чел. | 9 (90%) | 40 (85,2%) |
| Ингаляционная травма I ст. тяжести | 1 (10%)* | 19 (40,5%) |
| Ингаляционная травма II ст. тяжести | 6 (60%)* | 11 (23,4%) |
| Ингаляционная травма III ст. тяжести | 2 (20%) | 10 (21,3%) |
| Индекс оксигенации, мм рт. ст. | 271±24* | 238±42 |
| Шкала ОПЛ, баллы | 0,8±0,2* | 1,7±0,2 |
Примечание: * – различие признака между группами р<0,05
В первую группу вошли 10 пациентов, 47 пострадавших составили вторую группу. Пострадавшие были сопоставимы по полу и возрасту. У пострадавших с сепсисом был значимо выше индекс тяжести травмы.
У пострадавших второй группы тяжелый сепсис был диагностирован в 68% случаев, септический шок в 32% случаев. Количество баллов по шкалам SOFA и LIS для группы с тяжелым сепсисом на момент начала исследования составили 4,2±1,3 и 1,5±0,4 баллов, а в группе септического шока 6,8±2,6 и 2±0,6 соответственно. Основным источником генерализации инфекции являлись ожоговые раны. У 46,8% пострадавших кроме ран очаг инфекции локализовался в легких, что подтверждалось диагностированной пневмонией CPIS 5,4±2,3 балла. Больные не различались по возрасту, общей площади повреждения и глубине ожога. Однако у пострадавших с септическим шоком превалировала ингаляционная травма ΙΙ и ΙΙΙ степени тяжести, вследствие чего в данной группе прогностический индекс был значительно ниже -0,3 (-0,5;-0,2), что соответствовало неблагоприятному прогнозу для жизни (табл. 2).
Таблица 2
Характеристика пострадавших с тяжелым сепсисом и септическим шоком
| Показатели | Тяжелый сепсис | Септический шок |
| Число пострадавших | 32 (68%) | 15 (32%) |
| Возраст, лет | 35±10 | 39±13 |
| Пол (женщины/мужчины) | 5/27 | 4/11 |
| Общая площадь повреждения, (% поверхности тела) | 50±13 | 43±15 |
| Общая площадь глубоких ожогов, (% поверхности тела) | 28±15 | 27±16 |
| Без ингаляционной травмы, чел. | 5 (15,6%) | 2 (13,4%) |
| С ингаляционной травмой, чел. | 27 (84,4%) | 13 (86,6%) |
| Ингаляционная травма I ст. тяжести | 13 (40,6%) | 6 (40%) |
| Ингаляционная травма II ст. тяжести | 9 (28,2%)* | 2 (13,3%) |
| Ингаляционная травма III ст. тяжести | 5 (15,6%)* | 5 (33,3%) |
| Прогностический индекс тяжести комбинированной термической травмы | 0,04 (-0,3;0,4)* | -0,3 (-0,5;-0,2) |
| Пневмония, чел. | 12 (37,5%) | 10 (66,6%) |
| Шкала ОПЛ, баллы | 1,5±0,4* | 2±0,6 |
| SOFA, баллы | 4,2±1,3* | 6,8±2,6 |
| CPIS, баллы | 4,8±1,7* | 5,4±2,3 |
| Доза дофамин, мкг/кг/мин | 3,8±1* | 11±4 |
| Летальность | 13 (40,6%)* | 9 (60%) |
Примечание: * – различие статистически значимо между группами (р<0,05)
Выраженность нарушений газообмена оценивали на основании клинических, лабораторных, бактериологических и инструментальных методов с использованием шкал (LIS) Murray (Murray J. et al., 1988) и CPIS (Pugin J. et al., 1991). Диагноз тяжелого сепсиса и септического шока ставили на основании диагностических критериев, принятых на Чикагской согласительной конференции в 1991г. Тяжесть органной дисфункции оценивали по шкале SOFA (Vincent J. et al., 1996).
Всем пострадавшим, вошедшим в исследование проводился инвазивный мониторинг параметров состояния сердечно-сосудистой системы и волемического статуса с помощью системы PiCCOplus (PULSION, Германия). Метод основан на анализе кривой термодилюции и математических расчетов параметров формы пульсовой волны, получаемой после введения холодового индикатора в одну из центральных вен (подключичная или яремная вена) с последующей регистрацией изменения температуры термистором, расположенным в магистральной артерии. Данная методика носит название метода изолированной транспульмональной термодилюции (ТПТД).
В качестве термоиндикатора использовался охлажденный (<8 C0) изотонический кристаллоидный раствор (0,9% NaCl или 5% глюкозы). Объем вводимого термоиндикатора составлял 15 мл. Всем пострадавшим, вошедшим в исследование, термодилюция выполнялась 3 раза в сутки. Результаты заносились в первичную карту пациента. Для анализа мы использовали значение термодилюции, измерение которого происходило единовременно с забором анализа газового состава крови. В ходе работы было проведено 300 измерений термодилюции.
Использование расчетного показателя индекса проницаемости легочных сосудов, как отношение индекса внесосудистой воды легких (ИВСВЛ) к показателю объемной преднагрузки индексу глобального диастолического объема (ИГКДО), лег в основу распределения пострадавших на подгруппы в зависимости от выраженности проницаемости сосудов легких. Так же проводили математический расчет показателей индексов доставки, потребления, утилизации кислорода и коллоидно-онкотического давления плазмы (КОД).
Всем обследованным проводилась респираторная поддержка в режиме BIPAP и SIMV/PS, респираторами Savina, Carina фирмы Dräger. Объем инфузионной терапии в периоде ожогового шока рассчитывался по формуле Паркланда. Интенсивная терапия сепсиса проводилась с учетом рекомендаций, утвержденных Российской ассоциацией специалистов по хирургическим инфекциям в 2004 г. на конференции в Калуге.
Статистическая обработка результатов исследований
Обработку полученных данных проводили с помощью прикладных программ Excel, AtteStat, SPSS 13.0 и Statistica for Windows 6.0. Все данные представлены в виде средних M±m или медианы с 25% и 75% квартилями, нормальность распределения выборки оценивали при помощи критерия Шапиро-Уилка и глазомерного теста, в рамках корреляционной связи вычисляли коэффициент Пирсона и Спирмена (r), различие признаков поводили при помощи U-критерия Манна-Уитни. Прогностическую оценку тестов или показателей проводили при помощи ROC-анализа, прогностическую оценку выживаемости оценивали по кривым Каплан-Майеру с представлением цензурированных данных. Различия считали достоверными при р<0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВНИЯ
В остром периоде ожоговой болезни были обследованы тяжелообожженные, у которых развились нарушения газообмена в первые трое суток от момента травмы. На момент включения в исследование у пострадавших регистрировалась артериальная гипоксемия (PaO2, – 80±9 мм рт. ст., SaO2 – 95±1,5 %, PaO2/FiO2 – 271±24 мм рт. ст.), выявлялись билатеральные изменения на рентгенограмме органов грудной полости, тяжесть поражения легких средней степени тяжести (0,8 по Murray). Мониторинг гемодинамики и волемического статуса пострадавших с использованием технологии PiCCOplus начинали в течение первых 12 часов после травмы.
При оценке гемодинамики и волемического статуса, в первые 24 часа от момента получения травмы, были выявлены признаки выраженной гиповолемии, что подтверждалось снижением показателей, характеризующие объемную преднагрузку (ИГКДО 446±103 мл/м2 и ИВГОК 614±102 мл/м2). Кроме того, регистрировались признаки депрессии сердечной деятельности: снижение сердечного индекса (СИ 2,5±0,6 л/мин/м2), индекса ударного объема (ИУО 24±6 мл/м2), глобальной фракции изгнания (ГФИ 16±5%). Как известно, гиповолемия, нарушения производительности и сократимости сердца приводят к снижению доставки кислорода к органам и тканям, с формированием дизоксии и критической гипоперфузии (Spronk P. E., 2004, Кузьков В. В., Киров М. Ю., 2008, Tadros T. et al., 2000). При оценке транспорта кислорода у тяжелообожженных в первые часы после травмы, было выявлено снижение уровня доставки кислорода DO2I (466±106 мл/мин/м2) на фоне увеличения показателей потребления и экстракции кислорода (VO2I – 163±54 мл/мин/м2 и O2ERI – 0,34±0,14%).
Снижение центральной венозной сатурации крови (ScvO2 – 60±4%) характеризовало выраженность нарушений микроциркуляции, гипоперфузии и дисбаланса в системе транспорта кислорода. Известно, что «коридор безопасности» данного значения, по данным P. Bauer et al. (2008), должен находиться в пределах 65–75%, а среднее значение должно быть на уровне 70%. Примечательно, что даже у пострадавших с тяжелыми поражениями дыхательных путей продуктами горения в первые часы после травмы не было зарегистрировано накопление внесосудистой воды легких (7,3±0,7 мл/кг) с интерстициальным отеком, характерного для развития острого повреждения легких и респираторного дистресс-синдрома.
Проведение целенаправленной интенсивной терапии в следующие 48-72 часа (увеличение объема инфузионной терапии, назначение инотропной поддержки) под контролем показателей объемной преднагрузки ИГКДО и ИВГОК, до достижения их нижней границы рекомендуемой нормы 680 и 850 мл/м2, приводило к нормализации показателей СИ 5,8±1,4 л/мин/м2, ИУО 50±13 мл/м2, доставки кислорода 901±280 мл/мин/м2, перфузии тканей (венозная сатурация 66±9%) и улучшению газообмена в легких (PaO2/FiO2 332±80 мм рт. ст.). Однако у части пострадавших через 48 часов после травмы было отмечено прогрессирование гипоксемии и снижение индекса оксигенации 262±85 мм рт. ст. на фоне резкого снижения расчетного показателя КОД плазмы крови до 11±2 мм рт. ст., что приводило к накоплению внесосудистой воды 9±1 мл/кг и формированию отека легких (r=-0,65; p=0,006). В последующем, на фоне увеличения КОД плазмы (18,5±2,8 мм рт. ст.) происходило снижение внесосудистой воды легких и нормализация индекса оксигенации (рис 1).
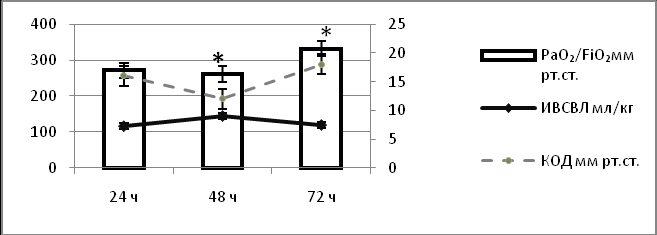
Рис. 1. Динамика индекса оксигенации, индекса внесосудистой воды легких (ИВСВЛ) и коллоидно-онкотического давления плазмы (КОД) (* – p<0,05)
Выявленная статистически значимая корреляция между показателями центральной венозной сатурацией, индексом доставки кислорода и индексом оксигенации позволяют сделать вывод о том, что нарушения газообмена у тяжелообожженных в остром периоде ожоговой болезни были связаны в основном с внелегочными причинами (рис 2.).
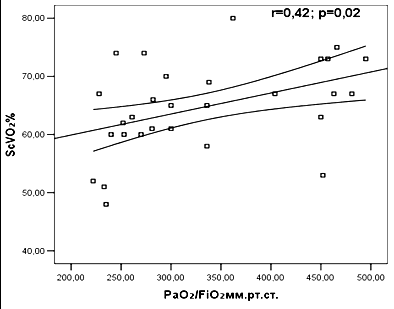
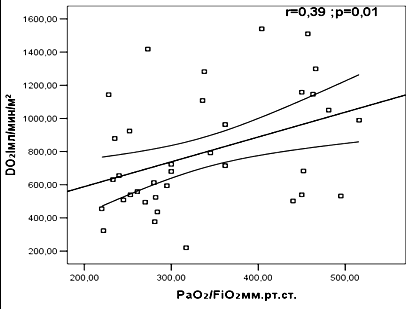
Рис. 2. Корреляционная зависимость ScVO2 (слева) и DO2I (справа) с индексом оксигенации
ScVO2 – центральная венозная сатурация; DO2I – индекс доставки кислорода.
Нарушения газообмена у обследованных пострадавших с тяжелой термической травмой в постшоковом периоде (4-36 сутки после травмы) развивались на фоне тяжелого сепсиса (68%) или септического шока (32%).
Как показал анализ результатов исследования, снижение индекса оксигенации у пострадавших с тяжелым сепсисом и септическим шоком значимо коррелировал с увеличением показателя ИВСВЛ (r=-0,73; p=0,0001), что свидетельствовало, о ведущей роли отека в патогенезе нарушений газообмена в легких у тяжелообожженных с генерализованными инфекционными осложнениями (рис. 3).
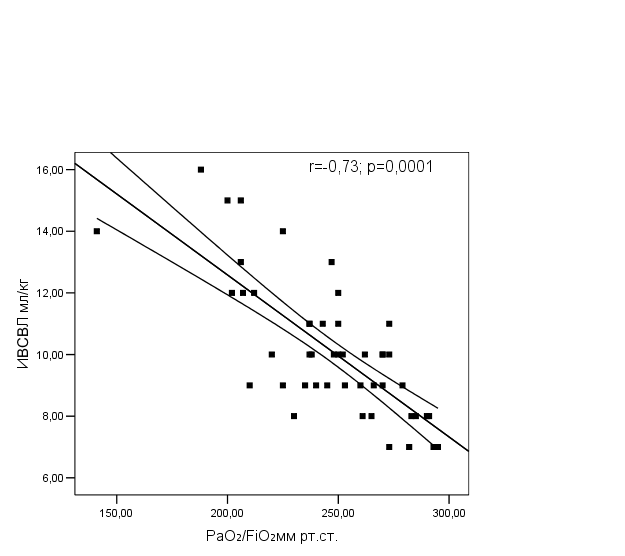 | Рис. 3. Корреляционная зависимость ИВСВЛ и индекса оксигенации у пострадавших с тяжелым сепсисом и септическим шоком ИВСВЛ – индекс внесосудистой воды легких. |
Для более дифференцированного подхода к диагностике механизмов развития отека легких у тяжелообожженных была предпринята попытка оценки проницаемости легочных капилляров. В работах ряда авторов имеются сведения о том, что относительные показатели проницаемости сосудов легких (ИВСВЛ/ЛОК, ИВСВЛ/ИВГОК, ИВСВЛ/ИГКДО) являются более информативными в плане прогнозирования и диагностики развития ранних стадий некардиогенного отека легких, чем абсолютная величина индекса внесосудистой воды легких (Steinvall I., 2008, Monnet X. et al., 2007, Галстян Г. М. и соавт., 2005). Для оценки прогностической значимости показателя (ИВСВЛ/ИГКДО) был проведен анализ его чувствительности и специфичности по отношению к шкалам Murray, SOFA, а также оценена вероятность выживаемости пострадавших.
Определение площади под операционной кривой (ROC) считается методом «золотого стандарта» при сравнении информативности различных диагностических систем. Определение порога индекса проницаемости ИВСВЛ/ИГКДО, при котором происходило снижении индекса оксигенации менее 300 мм рт. ст. и увеличение баллов по шкале ОПЛ более одного показало, что значение ИВСВЛ/ИГКДО соответствовало 0,016 усл. ед. Данная модель имела чувствительность 100% и специфичность 87,2%, площадь под операционной кривой (AUC) равнялась 0,97. Увеличение более 2 баллов по шкале SOFA регистрировалось при пороге значения ИВСВЛ/ИГКДО 0,015 усл. ед. Чувствительность и специфичность в этом случае составили 92% и 90%, площадь (AUC) равнялась 0,95 (рис 4).
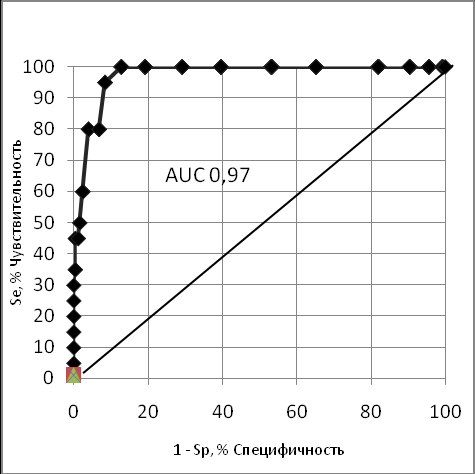 | 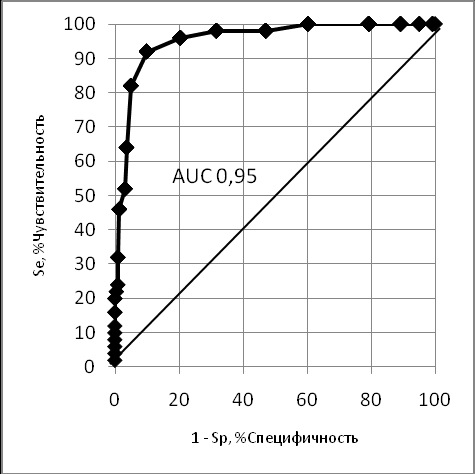 |
| Рис. 4. ROC анализ отношения ИВСВЛ/ИГКДО к шкале ОПЛ (слева), к шкале SOFA (справа) ИВСВЛ/ИГКДО – расчетный индекс проницаемости легких; ОПЛ – острое повреждение легких; SOFA – шкала последовательной оценки полиорганной недостаточности. | |
Анализ результатов вероятности выживания в течение 50 суток в зависимости от уровня выраженности сосудистой проницаемости показал, что у пострадавших с уровнем ИВСВЛ/ИГКДО более 0,015 усл. ед. составила 18%, в то время как у пострадавших с ИВСВЛ/ИГКДО менее 0,015 усл. ед. данный показатель составлял 69%, p=0,005, что свидетельствовало о прогностической значимости данного показателя (рис. 5).
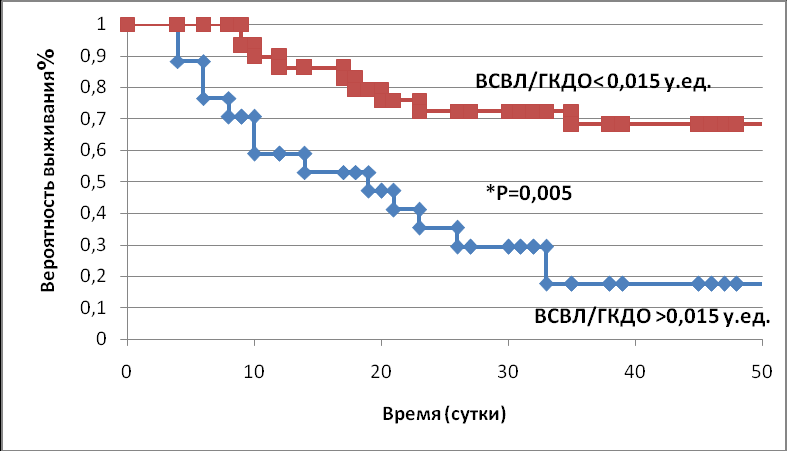
Рис. 5. Вероятность выживания у пострадавших с отношением ИВСВЛ/ИГКДО < 0,015 усл. ед. (n=28) и ИВСВЛ/ИГКДО > 0,015 усл. ед. (n=16)
ИВСВЛ/ИГКДО – расчетный индекс проницаемости легких.
Учитывая полученные данные об информативности и прогностической значимости расчетного индекса сосудистой проницаемости, на следующем этапе исследования, все пострадавшие были разделены на подгруппы в зависимости от величины отношения ИВСВЛ/ИКГДО (в норме при ИГКДО 680-800 мл/кг и ИВСВЛ 7 мл/кг отношение ИВСВЛ/ИКГДО составляет 0,008-0,010 усл. ед.) (рис. 6).
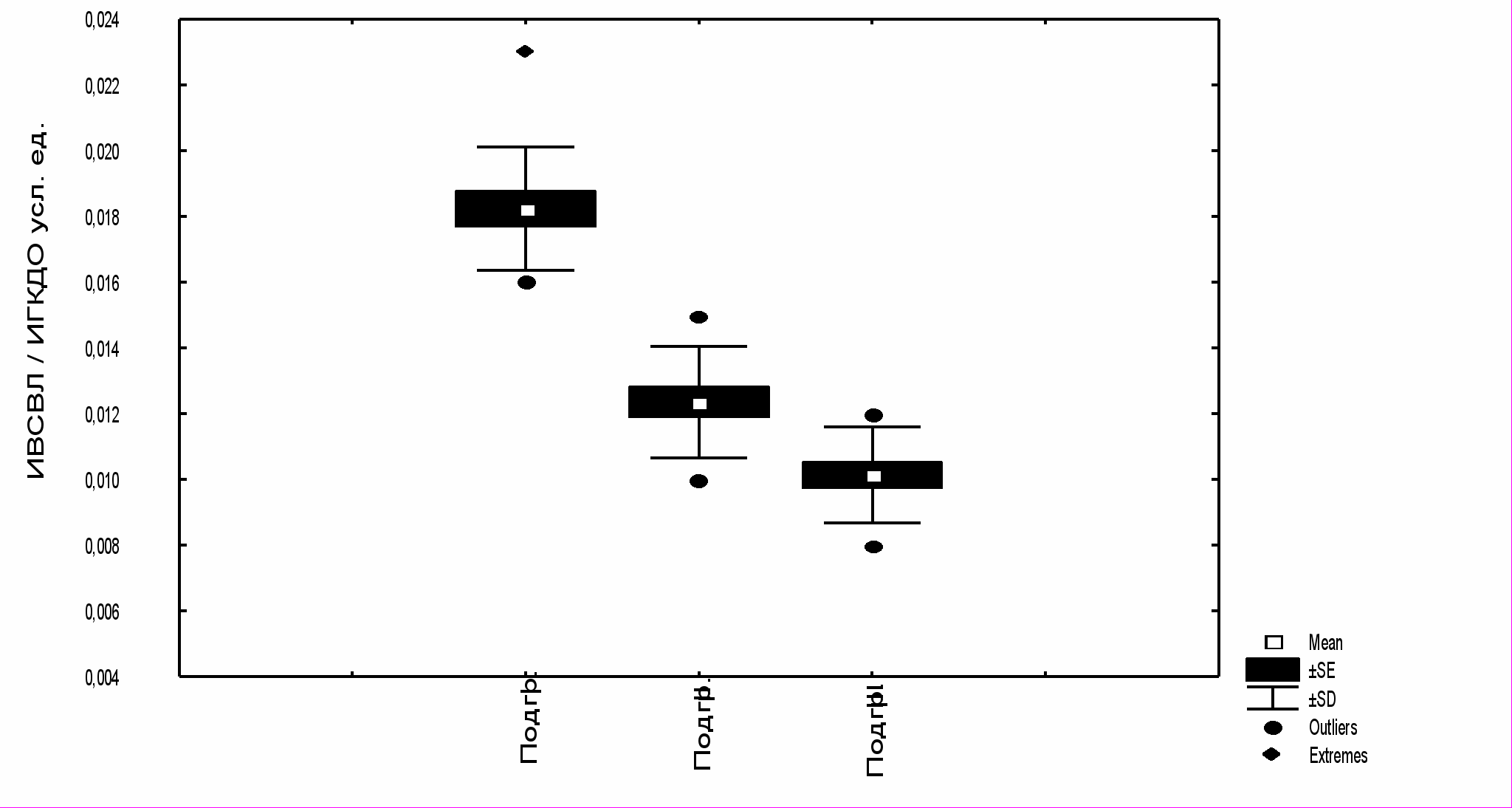
n=14
n=19
n=14
Диапазон нормальных значений
Рис. 6. Распределение пострадавших в зависимости от уровня расчетный индекс проницаемости легких (ИВСВЛ/ИГКДО)
В первую подгруппу (n=14) вошли пострадавшие с увеличенным показателем ИВСВЛ/ИКГДО в два и более раза (0,016 –0,023 усл. ед.). Вторую подгруппу (n=19) составили пострадавшие с незначительным увеличением ИВСВЛ/ИГКДО от 0,011 до 0,015 усл. ед., 14 человек с нормальными значениями ИВСВЛ/ИГКДО (0,009 – 0,01 усл. ед.) вошли в третью подгруппу.
Проведенный анализ показателей гемодинамики, волемического статуса, состояния газообмена, в зависимости от величины ИВСВЛ/ИГКДО показал, что в I подгруппе (ИВСВЛ/ИГКДО 0,016 – 0,023 усл. ед.), у всех пострадавших отмечались признаки тяжелого повреждения легких, оцененного по шкале Murray в 2±0,56 балла: снижение PaO2/FiO2 (217±39 мм рт. ст.), торокопульмональной податливости (48±12 см вод. ст.). Результаты корреляционного анализа показали, что увеличение индекса внесосудистой воды легких до 16,8±7,7 мл/кг не было связано с увеличением преднагрузки (r=0,1; p=0,5), снижением коллоидно-онкотического давления (r=-0,28; p=0,1) и сократимости левого желудочка (r=0,1; p=0,6), что подтверждало некардиогенную природу отека легких на фоне выраженной сосудистой проницаемости (табл. 3).
Таблица 3
Зависимость ИВСВЛ от показателей гемодинамики, волемического статуса и КОД у пострадавших с различным уровнем сосудистой проницаемости
| Показатель | ИВСВЛ, мл/кг | ||
| Подгруппа I (n=30) | Подгруппа II (n=60) | Подгруппа III (n=52) | |
| ИВСВЛ, мл/кг | 16,8±7,7 | 8,6±1,3 | 11,3±2,2 |
| ИГКДО, мл/м2 | r=0,1 p=0,5 | r=0,30 p=0,01* | r=0,67 p=0,0001* |
| КОД, мм рт. ст. | r=-0,28 p=0,1 | r=-0,54 p=0,0001* | r=-0,51 p=0,0001* |
| ЦВД, мм рт. ст. | r=-0,04 p=0,8 | r=0,09 p=0,4 | r=0,21 p=0,1 |
| ИСЛЖ, мм рт. ст/сек | r=0,1 p=0,6 | r=0,03 p=0,7 | r=-0,28 p=0,04* |
Примечание: * – статистически значимая корреляция р<0,05,
n – количество проведенных измерений
ИВСВЛ – индекс внесосудистой воды легких; ИГКДО – индекс глобального конечно-диастолического объема; КОД – расчетное коллоиодно-онкотическое давление плазмы крови; ЦВД – центральное венозное давление; ИСЛЖ – индекс сократимости левого желудочка.
У пострадавших II подгруппы с незначительным увеличением ИВСВЛ/ИГКДО (0,011 – 0,015 усл. ед.) нарушения газообмена происходили на фоне увеличения ИВСВЛ до 10 мл/кг, (8,6±1,3), при этом была выявлена значимая корреляционная связь между увеличением индекса внесосудистой воды легких и индексами внутригрудного и конечно-диастолического объемов крови, (r=0,30, p=0,01), а также коллоидно-онкотическим давлением (r=-0,54, p=0,0001). Обращало на себя внимание, что показатели, характеризующие преднагрузку, которые коррелировали с увеличением индекса внесосудистой воды легких, находились в пределах рекомендуемых норм (ИВГОК – 849±113 мл/м2, ИГКДО – 685±100 мл/м2 ЦВД 8,7±3,6 мм рт. ст.), что могло свидетельствовать об относительной гиперволемии на фоне сниженного онкотического давления и повышенной проницаемости сосудов (табл. 3).
В III подгруппе у пострадавших с нормальными значениями ИВСВЛ/ИГКДО (0,008 – 0,01 усл. ед.) внесосудистая вода легких (11,3±2,2 мл/кг) коррелировала с увеличенными показателями преднагрузки (ИВГОК – 1217±242 мл/м2, ИГКДО – 973±196 мл/м2, r=0,67, p=0,0001) и сниженным коллоидно-онкотическим давлением плазмы (14,9±2,4 мм рт. ст., r=-0,51, p=0,0001). Кроме того, была выявлена корреляционная связь между увеличением индекса внесосудистой воды легких и снижением индекса работы левого желудочка (1102±332 мм рт. ст./сек., r =-0,28, p=0,04) (табл. 3). Учитывая полученные данные, можно предположить, что нарушения газообмена у пострадавших третьей подгруппы развивались на фоне увеличения преднагрузки и дисфункции левого желудочка, которая могла быть обусловлена как гиперволемией, так и признаками сердечной недостаточности, развивающейся на фоне сепсиса.
Полученные данные о различных механизмах развития отека легких у пострадавших с сепсисом обусловили необходимость индивидуализации тактики интенсивной терапии. На первом этапе разработки лечебного алгоритма были предприняты попытки определения показателей, на которые можно было бы ориентироваться при назначении инфузионной терапии.
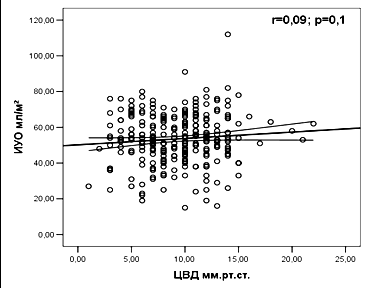
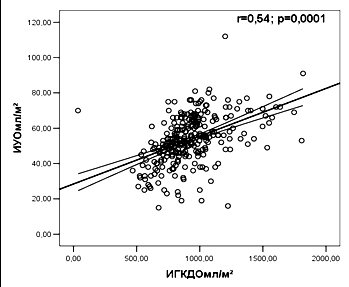
С этой целью был проведен регрессионный анализ зависимости показателей ИГКДО, ЦВД от индекса ударного объема крови. Результаты регрессионного анализа, включавшие 300 наблюдений изолированной транспульмональной термодилюции, продемонстрировали значимую корреляцию показателя объемной преднагрузки ИГКДО с индексом ударного объема (ИУО) и показателем доставки кислорода (r=0,54; p=0,0001 и r=0,21; p=0,001), в сравнении с показателем ЦВД (r=0,09; p=0,1 и r=0,05; p=0,3) (рис. 7). Полученные результаты подтвердили информативную значимость объемных показателей преднагрузки в сравнении с прессометрическим показателем (ЦВД), что обусловило их использование для оценки уровня волемии при проведении инфузионной терапии у тяжелообожженных.
 |  |
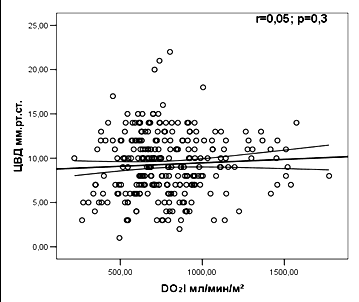 | 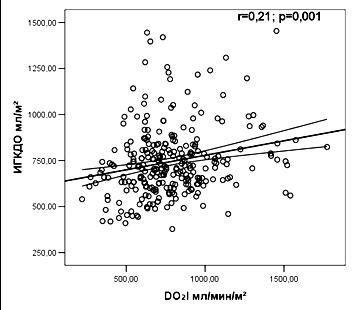 |
| Рис. 7. Регрессионные кривые зависимости ИГКДО и ЦВД с индексом ударного объема и индексом доставки кислорода (n=300) ИГКДО – индекс глобального конечно-диастолического объема; ЦВД – центральное венозное давление. | |
Волемический статус пострадавших с выраженными нарушениями сосудистой проницаемости (I подгруппа) характеризовался значительным увеличением внесосудистой воды легких на фоне нормальных показателей, характеризующих преднагрузку (ЦВД, ИВГОК и ИГКДО), что требовало постоянного мониторирования объема инфузионной терапии.
У 8 (57%) пострадавших I подгруппы, несмотря на ограничение инфузионной терапии под контролем почасового темпа диуреза, ИГКДО и ScvO2, нарастала внесосудистая вода легких (ИВСВЛ 16,8±7,7 мл/кг) и на этом фоне еще больше снижался индекс оксигенации (178±77 мм рт. ст.). Подобная динамика была обусловлена прогрессированием инфекционного процесса и усугублением нарушений сосудистой проницаемости, повлиять на которую фармакологическими средствами достаточно сложно.
Однако у 6 (43%) выживших пострадавших на фоне проводимой интенсивной терапии сепсиса, ограничительной тактики инфузионной терапии и перераспределении инфузионных сред в сторону нативных коллоидных растворов с учетом данных мониторинга гемодинамики и волемического статуса, отмечалась положительная динамика (табл. 4, рис. 8).
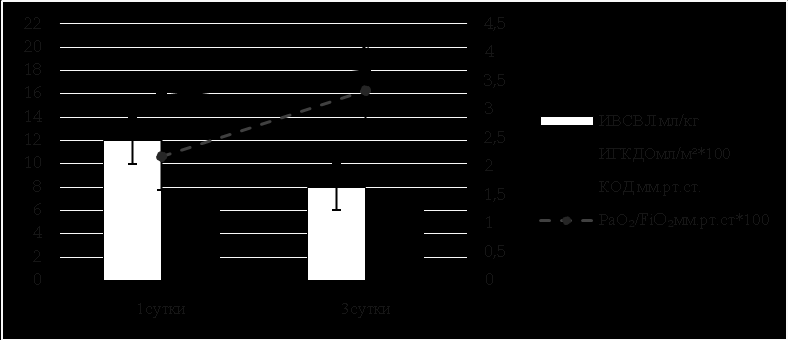
Рис. 8. Динамика волюметрических показателей, КОД и индекса оксигенации в I подгруппе (n=60) (* – p<0,05 между 1 и 3 сутками)
ИВСВЛ – индекс внесосудистой воды легких; ИГКДО – индекс глобального конечно-диастолического объема; КОД – расчетное коллоиодно-онкотическое давление плазмы крови; PaO2/FiO2 – индекс оксигенации.
Обращало внимание, что нормализация газообмена у пострадавших I подгруппы происходила при значимо более низких показателях объемной преднагрузки (ИГКДО 550 (500;610) мл/м2 и ИВГОК 695 (617;760) мл/м2) и при этом сохранялся нормальный уровень доставки кислорода (DO2I 775(638;867) мл/мин) и тканевой перфузии SсvO2 % 66 (64;67) полученный диапазон значений ИГКДО и ИВГОК можно считать оптимальным для пострадавших с ИВСВЛ/ИГКДО более 0,015 усл. ед. Однако с учетом проведенного анализа определения чувствительности порога минимального значения ИГКДО к показателю индекса доставки кислорода равному 550 мл/мин (усредненное значение), на большей выборке наблюдений (300) измерения, был выявлен порог ИГКДО равный 650 мл/м2 с чувствительностью 93% и специфичностью 63% (AUC) 0,84. Поэтому при более низких значениях показателей преднагрузки необходима обязательная оценка показателей транспорта кислорода и маркеров тканевой перфузии.
У пострадавших второй и третьей подгрупп при нормальном показателе объемной преднагрузки проводили инфузию с перераспределением в сторону нативных коллоидных растворов для увеличения показателя КОД (17,5±2,8 мм рт. ст.). При увеличенном показателе ИГКДО ограничивали инфузионную терапию, и назначали диуретики, у пострадавших с нарушением сократительной способностью миокарда применяли вазопрессорную поддержку (рис. 9).
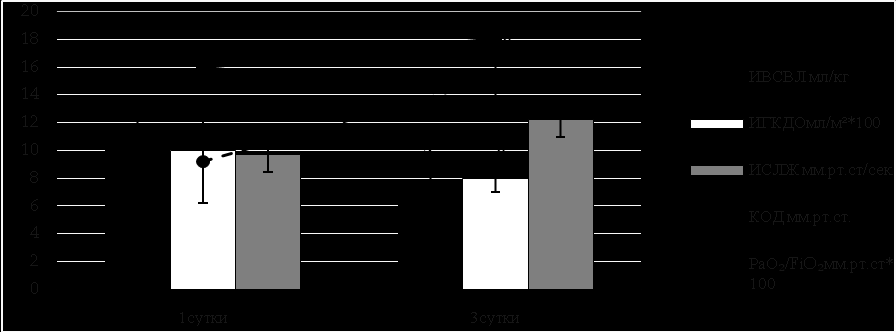
Рис. 9. Динамика волюметрических показателей, КОД и индекса оксигенации во II-III подгруппах (n=112) (* – p<0,05 между 1 и 3 сутками)
ИВСВЛ – индекс внесосудистой воды легких; ИГКДО – индекс глобального конечно-диастолического объема; КОД – расчетное коллоиодно-онкотическое давление плазмы крови; PaO2/FiO2 – индекс оксигенации; ИСЛЖ – индекс сократимости левого желудочка.
В результате это привело к увеличению индекса оксигенации, комплайнса легких, положительной рентгенологической динамике и снижению количества баллов по шкале SOFA, Murray и CPIS (табл. 4).
Таблица 4
Динамика индекса оксигенации, комплайнса и тяжести органных нарушений у пострадавших Ι, ІІ и ІІІ подгрупп
| Показатели | Ι подгруппа | ІІ подгруппа | ІІІ подгруппа | |||
| 1 сутки | 3 сутки | 1 сутки | 3 сутки | 1 сутки | 3 сутки | |
| PaO2/FiO2, мм рт. ст. | 217±54* | 333±29 | 255±29* | 306±75 | 230±35* | 309±70 |
| Комплайнс, мл/см Н2О | 43±4* | 57±9 | 50±8 | 56±12 | 46±10* | 58±15 |
| Шкала ОПЛ, баллы | 2±0,6* | 0,6±0,3 | 1,35±0,33* | 0,9±0,4 | 1,5±0,4* | 0,9±0,6 |
| SOFA, баллы | 6,8±3,4* | 3,8±0,7 | 3,9±1,2 | 4±1 | 4,9±1,7 | 4,5±2,5 |
| CPIS, баллы | 6±1,6* | 4,2±0,5 | 5±1,9 | 4,5±2 | 4,7±1,7* | 3,8±1,5 |
Примечание: * – статистически значимо р<0,05
PaO2/FiO2 – индекс оксигенации; ОПЛ – острое повреждение легких; SOFA – шкала последовательной оценки полиорганной недостаточности; CPIS – клиническая шкала оценки инфекции легких.
Своевременная фармакологическая коррекция (назначение инотропных препаратов, диуретиков), так и целенаправленная объемная нагрузка под контролем показателей внесосудистой воды легких и проницаемости легочных сосудов продемонстрировали свою эффективность, что отразилось на снижении летальности у тяжелообоженных по сравнению с прогнозируемым уровнем (табл. 5).
Таблица 5
Прогнозируемая и реальная летальность пострадавших
с генерализованными инфекционными осложнениями
| Прогностический индекс, усл. ед. | Тяжелый сепсис (n=32) | Септический шок (n=15) |
| 0,04 (-0,3;0,4) | -0,3 (-0,5;-0,2) | |
| Прогнозируемая летальность, % | 50% | 95% |
| Реальная летальность, % | 40,6% (13 чел.) | 60% (9 чел.) |
Полученные данные подтвердили необходимость дифференцированного подхода к проведению интенсивной терапии пострадавших с тяжелой термической травмой и нарушениями газообмена в зависимости от величины ИВСВЛ/ИГКДО, характеризующего сосудистую проницаемость. С учетом полученных данных, инфузионно-трансфузионная терапия у пострадавших с ожоговым сепсисом должна быть направлена на оптимизацию соотношений объемов внутри и внесосудистого сектора и нормализацию КОД. При ее проведении у пострадавших с различным уровнем сосудистой проницаемости следует ориентироваться на значения показателей гемодинамического и волюметрического мониторинга, приведенные в табл. 6.
Таблица 6
Оптимальные значения гемодинамики и волемического статуса у пострадавших с различным уровнем сосудистой проницаемости
| Перечень показателей | ИВСВЛ/ИГКДО более 0,015 | ИВСВЛ/ИГКДО менее 0,015 | ИВСВЛ/ИГКДО менее 0,012 |
| ИГКДО, мл/м2 | не более 650 | 650-750 | 750-800 |
| ИВГОК, мл/м2 | не более 700 | 700-850 | 800-950 |
| ИВСВЛ, мл/кг | <9 | <8 | <8 |
| DO2I, мл/мин/м2 | 500-600 | 500-600 | 500-600 |
| ScvO2, % | не менее 65 | не менее 65 | не менее 65 |
| СИ, л/мин/м2 | >3,5 | >3,5 | >3,5 |
| ИУО, мл/м2 | >45 | >45 | >45 |
| ГФИ, % | >25 | >25 | >25 |
| ИСЛЖ, мм рт. ст/сек | >1100 | >1100 | >1100 |
ИГКДО – индекс глобального конечно-диастолического объема; ИВГОК – индекс внутригрудного объема крови; ИВСВЛ – индекс внесосудистой воды легких; DO2I – индекс доставки кислорода; ScvO2 – центральная венозная сатурация; СИ – сердечный индекс; ИУО – индекс ударного объема; ГФИ – глобальная фракция изгнания; ИСЛЖ – индекс сократимости левого желудочка.
ВЫВОДЫ
- Гипоксемия у пострадавших с тяжелой термической травмой в остром периоде ожоговой болезни развивалась на фоне нарушений кровообращения и гипоперфузии, что подтверждалось статистически значимыми корреляционными связями индекса оксигенации, доставки кислорода и десатурации центральной венозной крови (r=0,39; p=0,01 и r=0,42; p=0,02).
- В постшоковом периоде нарушения газообмена у пострадавших с тяжелой термической травмой развивались на фоне тяжелых генерализованных инфекционных осложнений и были связаны с накоплением внесосудистой воды легких на фоне измененной сосудистой проницаемости.
- Увеличение индекса внесосудистой воды легких более 10 мл/кг и индекса проницаемости сосудов легких (ИВСВЛ/ИГКДО) более 0,015, при нормальных значениях показателя, объемной преднагрузки, индекса глобально-диастолического объема, является ранним предиктором некардиогенного отека легких, лежащего в основе нарушений газообмена в легких при синдроме острого повреждения легких и респираторном дистресс-синдроме.
- Расчетный индекс сосудистой проницаемости легких (ИВСВЛ/ИГКДО) обладает высокой чувствительностью (100%) и специфичностью (87%) в отношении развития синдрома острого повреждения легких, синдрома полиорганной недостаточности (чувствительность 92%, специфичностью 90%) у тяжелообожженных с генерализованными инфекционными осложнениями.
- Оценка данных волемического статуса индекса глобального конечно-диастолического объема, внесосудистой воды легких, расчетного индекса проницаемости сосудов легких показателей, характеризующих сократительную способность миокарда, создает предпосылки для индивидуализации лечебного алгоритма у пострадавших с тяжелой термической травмой при нарушениях газообмена.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Пострадавшим с тяжелой термической и комбинированной травмой при нарушениях газообмена и неэффективности проводимого лечения показан инвазивный гемодинамический и волюметрический мониторинг, для изучения механизмов формирования гипоксемии и дифференцированного подхода к интенсивной терапии развившихся осложнений.
- Для оценки уровня волемии и адекватности проводимой инфузионной терапии следует ориентироваться на показатель объемной преднагрузки, индекс глобального конечно-диастолического объема (ИГКДО), который, в отличие от ЦВД, значимо коррелирует с индексом ударного объема и доставкой кислорода.
- Для дифференциальной диагностики механизмов развития нарушений газообмена и отека легких следует ориентироваться на показатели индекса внесосудистой воды легких (ИВСВЛ), расчетного индекса проницаемости сосудов легких (ИВСВЛ/ИГКДО), индекса глобального конечно-диастолического объема (ИГКДО) и расчетного показателя коллоидно-онкотического давления плазмы (КОД).
- При значении расчетного индекса проницаемости сосудов легких (ИВСВЛ/ИГКДО) более 0,015 прогнозируется высокий риск развития некардиогенного отека легких, что требует особенно тщательного контроля за проводимой инфузионной терапии.
- При проведении интенсивной терапии у пострадавших с нарушениями газообмена следует ориентироваться на разработанный лечебно-тактический алгоритм, основанный на оценке волемических показателей с учетом индекса проницаемости сосудов легких.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Шлык И.В. Состояние центральной гемодинамики и волюметрического статуса при синдроме острого повреждения легких у пострадавших с тяжелой термической травмой / И.В. Шлык, К.А. Шатовкин // Материалы международной конференции «Актуальные проблемы термической травмы». –Санкт-Петербург, 2006. – С. 101–102.
- Шлык И.В. Мониторинг центральной гемодинамики и волюметрического статуса при синдроме острого повреждения легких у пострадавших с тяжелой термической травмой / И.В. Шлык, К.А. Шатовкин // Материалы десятого съезда анестезиологов и реаниматологов «Проблемные вопросы респираторной терапии». – Санкт-Петербург, 2006. – С. 488–489.
- Шлык И.В. Использование концентрированных растворов альбумина у пострадавших с тяжелой термической травмой / И.В. Шлык, К.А. Шатовкин, Т.А. Авраменко // Материалы 7 межрегиональной научно-практической конференции «Искусственное питание и инфузионная терапия больных в медицине критических состояний. – Великий Новгород, 2007. – С. 112–114.
- Шлык И.В. Состояние центральной гемодинамики и волюметрического статуса при синдроме острого повреждения легких у пострадавших с тяжелой термической травмой / И.В. Шлык, К.А. Шатовкин, К.М. Крылов // Материалы III-го съезда анестезиологов и реаниматологов Приволжского Федерального округа в Нижнем Новгороде. – Нижний Новгород, 2007. – С. 114–115.
- Самарев А.В., Малоинвазивный мониторинг у пострадавших с тяжелой термоингаляционной травмой / А.В. Самарев, М.Ю. Тарасенко, И.Ф. Шпаков, К.А. Шатовкин // Сборник научных трудов II- го съезда комбустиологов России. – Москва, 2008. – С. 89–99.
- Шатовкин К. А., Шлык И. В., Крылов К. М. Гемодинамический и волюметрический мониторинг при нарушениях газообмена в легких у пострадавших с тяжелой термической травмой / К.А. Шатовкин, И.В. Шлык, К.М. Крылов // Сборник научных трудов II- го съезда комбустиологов России. – Москва, 2008. – С. 93–94.
- Шлык И. В. Использование гемодинамического и волюметрического мониторинга при синдроме полиорганной недостаточности у пострадавших с тяжелой термической травмой / И. В. Шлык, К.А. Шатовкин, А.В. Самарев // Материалы XI-го съезда анестезиологов и реаниматологов. – Санкт-Петербург, 2007. – С. 105–106.
- Крылов К.М. Оказание медицинской помощи пострадавшим с тяжелой термической и комбинированной травмой на догоспитальном этапе / К.М. Крылов, И.В. Шлык, В.В. Губин, Т.А. Свиридова, К.А. Шатовкин // Скорая медицинская помощь. – Санкт-Петербург, 2009. – №2. – с.35-37.
- Шатовкин К.А. Острое повреждение легких у пострадавших с ожоговым сепсисом / К.А. Шатовкин, И.В. Шлык // Материалы III-го международного конгресса по респираторной поддержке. – Красноярск – 2009. – С. 122–123.
- Шатовкин К.А. Гемодинамический и волюметрический мониторинг при нарушениях газообмена у пострадавших с тяжелой термической травмой / К.А. Шатовкин, И.В. Шлык, К.М. Крылов // Материалы IV-й межрегиональной научно-практической конференции. Современные аспекты анестезиологии и интенсивной терапии. – Новосибирск, 2009. – С. 157–158.
- Shatovkin K. Haemodynamics and volhaemic stage in patients with respiratory disorders to thermal injury / К. Shatovkin, I.Shlyk // Critical Care Med. – 2010. – Vol. 14 (supll.1). – P. 212.
- Shatovkin K. Volume status and extravascular lung water in patients with pulmonary damage and burn sepsis / К. Shatovkin, I.Shlyk // Burns. –2010. – Vol. 36. – P. 743.
- Шатовкин К.А. Внесосудистая вода легких при нарушениях газообмена у пострадавших с тяжелой термической травмой / К.А. Шатовкин, И.В. Шлык // Материалы XII-го съезда федерации анестезиологов и реаниматологов научные тезисы. – Москва, 2010. – С. 475–476.
- Шатовкин К.А. Волемический статус и внесосудистая вода легких у пострадавших с ожоговым сепсисом / К.А. Шатовкин, И.В. Шлык // Материалы 9-ой научной конференции по проблеме «Ожоги», посвященной 50-летию кафедры и клиники термических поражений. – Санкт-Петербург, 2010.– С. 119–120.
