Алексеев Владимир Николаевич доктор медицинских наук, профессор Николаенко Вадим Петрович Ведущая организация: гоу дпо российская медицинская академия последиплом
| Вид материала | Диплом |
- Халиф Игорь Львович Доктор медицинских наук, профессор Бредихина Наталия Андреевна, 579.47kb.
- Котов Сергей Викторович доктор медицинских наук, профессор Савин Алексей Алексеевич, 547.92kb.
- Кувакин Владимир Иванович Заслуженный деятель науки РФ доктор медицинских наук профессор, 361.78kb.
- Бахметьев Владимир Иванович Ведущая организация : Государственное общеобразовательное, 587.63kb.
- Рохлина Майя Леоновна доктор медицинских наук, профессор Игонин Андрей Леонидович доктор, 564.38kb.
- Лучкевич Владимир Станиславович Доктор медицинских наук, профессор Кочорова Лариса, 358.38kb.
- Кильдюшев Евгений Михайлович Доктор медицинских наук, профессор Гедыгушев Исхак Ахметович, 281.92kb.
- Сергиев Владимир Петрович Член-корреспондент рамн, доктор медицинских наук, профессор, 829.91kb.
- Ключарева Светлана Викторовна доктор медицинских наук профессор Эмануэль Владимир Леонидович, 782.84kb.
- Зуев Владимир Михайлович доктор медицинских наук профессор Федорова Татьяна Анатольевна, 481.21kb.
На правах рукописи
БУТИН
Евгений Владимирович
ОЦЕНКА НЕЙРОПРОТЕКТОРНОГО ДЕЙСТВИЯ РАЗЛИЧНЫХ ПРЕПАРАТОВ У БОЛЬНЫХ
С ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМОЙ
14.01.07 – глазные болезни
А в т о р е ф е р а т
диссертации на соискание ученой степени
кандидата медицинских наук
Санкт-Петербург
2010
Работа выполнена на кафедре офтальмологии Санкт-Петербургского государственного медицинского университета имени академика И.П. Павлова.
Научный руководитель:
доктор медицинских наук, профессор Астахов Юрий Сергеевич
Официальные оппоненты:
доктор медицинских наук, профессор Алексеев Владимир Николаевич
доктор медицинских наук, профессор Николаенко Вадим Петрович
Ведущая организация: ГОУ ДПО «Российская медицинская академия последипломного образования Росздрава»
Защита диссертации состоится 28 января 2010 г. в 14 часов на заседании Диссертационного Совета при ГОУ ВПО «Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова Росздрава» по адресу: 197022, Санкт-Петербург, ул. Л. Толстого, д. 6/8.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО «Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова Росздрава».
Автореферат разослан "____"________________ 2009 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук,
профессор Дискаленко Виталий Васильевич
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Глаукома – одно из наиболее тяжелых глазных заболеваний, занимающее ведущее место среди причин слепоты и слабовидения (Нестеров А.П., 2000, Muniur A., 1998). В России по официальным данным каждый пятый среди инвалидов по зрению ослеп от глаукомы (Либман Е.С., 2000).
В течение многих лет глаукома определялась как специфическая оптическая нейропатия с экскавацией и атрофией зрительного нерва, с характерными изменениями полей зрения. Эти изменения неизменно связывались с повышенным внутриглазным давлением (ВГД) (Нестеров А.П., 2000, Emery J.M. с соавт., 1974).
Повышение ВГД, хотя и является основной причиной повреждения зрительного нерва, однако существование первичной глаукомы с нестабильным течением при нормализованном ВГД, позволяет предположить, что в патогенез глаукомы могут быть вовлечены и другие повреждающие факторы. К таким факторам относят эксайтотоксическое повреждение третьего нейрона и активацию свободно-радикальных процессов в сетчатке и зрительном нерве (Федоров С.Н. с соавт., 1981, Orgul S., Flammer J., 1995, Osborn N.N., 1999, Vorverk C., 1999).
Снижение офтальмотонуса у больных глаукомой не всегда приводит к стабилизации зрительных функций (Crick R.P., 1985, Donglas C.R., 1998). Таким образом, необходим поиск новых путей лечения первичной глаукомы. Речь идет не только о снижении внутриглазного давления до уровня более низкого, чем среднестатистическая норма, но и о путях сохранения волокон зрительного нерва или, как это принято называть, о нейропротекторном лечении (Osborne N.N., Ugarte M., Chao M., с соавт., 1999). Термин «нейропротекция» при глаукоме подразумевает, что лекарственный препарат достигает сетчатки и замедляет каскад реакций, ведущих к гибели ганглиозных клеток сетчатки и волокон зрительного нерва
(Crosson C.E., Willis J.A., Potter D.E., 1990, Velte T.J., Yu W.,
Miller R.F., 1997).
Клинические наблюдения за больными, применявшими нейропротекторные препараты, основывались на субъективной оценке сохранности зрительных функций и, в первую очередь, поля зрения (Журавлев А.И., 1986., Логинов Г.Н., 1982., Ефимова М.Н., Якубова Л.В., 1994). Эти методы позволяли определить возможность изменения зрительных функций при воздействии того или иного лекарственного препарата. Однако при наличии изменений в зрительном нерве и определенной утрате зрительных функций немаловажное значение приобретают средства, способные увеличить толерантность зрительного нерва к повышению ВГД (устойчивость) и тем самым обеспечить стабилизацию глаукомного процесса. Для ответа на этот вопрос необходимо было выяснить, как в условиях искусственного повышения ВГД будет изменяться морфофункциональное состояние зрительного нерва без лечения и при использовании различных препаратов.
Значительную роль в оценке эффективности применения тех или иных препаратов при лечении глаукомы и степени их влияния на функции зрительно-нервного аппарата и структуры головки зрительного нерва играют объективные современные методы оценки функционального состояния зрительно-нервного аппарата.
Использование средств регистрации и обработки информации, компьютерной и лазерной техники, а также знания о нейрофизиологии зрительного анализатора позволили предложить ряд совершенно новых методов обследования и расширить возможности уже имеющихся.
На сегодняшний день электрофизиологические и психофизические методы исследования позволяют избирательно оценить функции различных каналов зрительной системы (яркостных, цветовых, контрастных и т.д.), нарушение которых является специфичным для глаукомы и проявляется на разных стадиях патологического процесса (Зислина Н.Н., Шамшинова А.М., 1993).
Электрофизиологические методы исследования: электроретинография, зрительные вызванные корковые потенциалы (ЗВКП), электроокулография, позволили не только оценить функцию зрительного анализатора, определить локализацию процесса в различных слоях сетчатки, зрительном нерве и в вышележащих отделах зрительной системы, но также осуществлять раннюю диагностику глаукомы, выявлять побочное действие лекарственных препаратов, прогнозировать восстановление зрительных функций под влиянием лечения и в процессе реабилитации.
Несомненным достоинством электрофизиологических методов является то, что они неинвазивны, их результаты легко могут быть представлены как в графической, так и в цифровой формах. Стандартные условия регистрации обеспечивают высокую достоверность и воспроизводимость результатов (Шамшинова А.М., Волков В.В., 1998, Heckenlively J. R., Arden G.B., 1991, Orden V.K., 1990).
Особое значение в диагностике глаукомы занимают нагрузочные пробы (Drans S.M, 1962, Tieri O. с соавт., 1976). В нашей стране широко применяются вакуум-периметрическая проба Волкова-Сухининой-Тер-Андриасова (Волков В.В., Сухинина Л.Б., 2004), усовершенствованная вакуум-периметрическая проба (Астахов Ю.С., Даль Н. Ю., 2003).
В 2005 году разработана объективная, высокоинформативная вакуум-компрессионная проба с электрофизиологическим контролем (Морозова Н.В., Астахов Ю.С., 2003). Проба позволяет оценить толерантность зрительного нерва к повышению внутриглазного давления с помощью регистрации зрительных вызванных корковых потенциалов и применяется для диагностики глаукомы и оценки ее стабилизации при низкой остроте зрения и непрозрачных оптических средах и обладает высокой информативностью. Информативность пробы составляет 95,5%.
Современные компьютерные сканирующие лазерные системы позволяют оценить изменения структуры зрительного нерва и сетчатки в реальном времени (Mikelberg F., 1995). Для исследования структурных изменений головки зрительного нерва и слоя ганглиозных клеток сетчатки при глаукоме широко применяют лазерную офтальмоскопию, лазерную поляриметрию, оптическую когерентную томографию. Наиболее информативным лазерным методом для диагностики глаукомы является ретинальная томография (Гейдельбергская ретинальная томография – HRT). Специфичность HRT составляет от 85 до 90%, чувствительность от 63 до 81%.
Цель нашего исследования заключалась в определении влияния лекарственных препаратов на толерантность зрительного нерва к повышению ВГД у больных с различными стадиями ПОУГ при нормализованном офтальмотонусе.
Для достижения поставленной цели нами были сформулированы следующие задачи исследования:
1. Разработать метод объективного исследования толерантности зрительного нерва к повышению ВГД.
2. Изучить влияние лекарственных препаратов (Акатинол мемантина, Ретиналамина и Бетаксолола) на устойчивость зрительного нерва к индуцированному повышению офтальмотонуса у пациентов с различными стадиями глаукомы при нормализованном ВГД.
3. Определить возможность влияния Акатинол мемантина, Ретиналамина и Бетаксолола на структуру головки зрительного нерва у больных с ПОУГ.
Научная новизна исследования заключается в том, что впервые:
1. Внедрен способ определения толерантности зрительного нерва к повышенному ВГД у больных с ПОУГ.
2. Проведено изучение толерантности зрительного нерва к повышению ВГД до и на фоне применения ряда лекарственных препаратов у больных с ПОУГ I-III стадий с помощью методов:
– вакуум-компрессионной пробы с контролем зрительных вызванных потенциалов на фоне искусственного повышения внутриглазного давления с использованием вакуумной «чашечки-присоски»;
– ретинальной томографии (HRT).
Практическая значимость:
На основании выполненного исследования были разработаны метод оценки толерантности зрительного нерва к повышению ВГД и рекомендации по применению изучаемых препаратов, с учетом их нейропротекторного действия, для лечения больных с ПОУГ I-III стадий при нормализованном ВГД.
Положения, выносимые на защиту:
1.Результаты объективного метода определения морфофункциональной устойчивости зрительного нерва к дозированному искусственному повышению ВГД.
2. Целесообразность применения Акатинол мемантина, Ретиналамина и Бетаксолола для повышения устойчивости зрительного нерва в I-III стадиях глаукомы и Бетаксолола в I и II стадии ПОУГ.
Апробация работы.
По результатам исследования опубликовано 6 печатных работ. Основные положения диссертационной работы были доложены на:
– 3-й Международной Конференции для врачей центральных госпиталей, диагностических центров и военных поликлиник МО РФ. Москва, 2005 г.
– Научно-практической конференции «Человек и лекарство». Москва, 2005 г.
– Всероссийской школе офтальмологов. Москва, 2006 г.
– I Международном конкурсе молодых ученых и специалистов «Пептидные препараты-препараты XXI века. СПб, 2006.
В процессе выполнения работы представлено рационализаторское предложение. «Устройство для искусственного повышения внутриглазного давления» № 1380 СПб ГМУ им. акад. И.П. Павлова (Астахов Ю.С., Бутин Е. В., Даль Н. Ю., Соколов В. О. 2002).
Внедрение результатов в практику:
Результаты исследований внедрены в практику в СПб ГУЗ «Диагностический центр № 7 (глазной) для взрослого и детского населения»
Объем и структура работы. Диссертация состоит из введения, пяти глав, заключения, выводов, практических рекомендаций, материалов, подтверждающих внедрение результатов исследования в практику, списка литературы, включающего 72 работы отечественных и 179 иностранных авторов. Диссертация изложена на 126 страницах, содержит 13 рисунков, 21 таблицу. Всего в работе было обследовано 293 человека (472 глаза). Выполнено 2086 исследований.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы. Пациенты обследовались на базе СПб ГУЗ «Диагностический Центр №7 (глазной) для взрослого и детского населения». В исследования были включены пациенты с глаукомой при нормализованном ВГД после лазерных и или других хирургических вмешательств. Для постановки диагноза первичной открытоугольной глаукомы была использована классификация Нестерова А.П. и Бунина А.Я., 1977 года.
В группы обследования не были включены пациенты:
– с сопутствующей офтальмологической патологией (атрофией зрительного нерва, миопической болезнью, хориоретинальной дистрофией и др.).
– с общими соматическими заболеваниями (сахарный диабет, последствия нарушения мозгового кровообращения и др.).
В нашем исследовании использовались диагностические методы:
1) Стандартные офтальмологические методы исследования: визометрия для дали (проектор знаков АСР-7, ТОРСОN, Япония); авторефрактометрия (авторефрактометр RC-4000, Япония); компьютнрная периметрия («Периком», Россия); биомикроскопия с использованием различных методов освещения; офтальмобиомикроскопия с асферическими линзами (60,0 D, «Олис», Россия); офтальмоскопия с широким зрачком в прямом и обратном виде (электроофтальмоскоп ОР-2М, Россия); гониоскопия с линзой Гольдмана («Олис», Россия); тонометрия (тонометр Маклакова).
2) Специальные методы диагностики:
– вакуум-компрессионная проба с контролем зрительно вызванных корковых потенциалов с использованием «чашечки- присоски» (Морозова Н.В., Астахов Ю.С. 2005).
– ретинальная томография (HRT-II, Германия).
Методика проведения вакуум – компрессионной пробы
с контролем зрительно вызванных корковых потенциалов
на фоне искусственного повышения внутриглазного давления
с использованием «чашечки – присоски»
Все пациенты были разделены на 3 группы в зависимости от стадий глаукомного процесса: I – начальной, II – развитой, III – далекозашедшей. В ходе проведения вакуум – компрессионной пробы с контролем зрительных вызванных корковых потенциалов в каждой группе проводились следующие исследования:
– до компрессии без применения препарата.
– при компрессии без применения препарата.
– до компрессии на фоне применения препарата.
– при компрессии на фоне применения препарата.
В каждом исследовании изучались два параметра волны Р-100 ЗВКП: латентность и амплитуда.
Пациенту разъяснялись задачи исследования. Активный электрод (затылочный) накладывали на 1,5-2,0 см выше затылочного бугра по средней линии над областью проекции зрительной зоны коры головного мозга (поле 17 по Бродману). Индифферентные электроды помещали на мочках ушей. Исследование фоновых ЗВКП проводили монокулярно на стандартную вспышку света мощностью 3 Кд/м2 и частотой 0,5 Гц. Фиксировались и оценивались исходные показатели амплитуды (в мкВ) и латентности (в мс) волны Р-100 ЗВКП.
Исследование ЗВКП выполнялось на отечественном электроретинографе «МБН» (г. Москва). Прибор соответствует стандартам международного общества электрофизиологов зрительной системы (ISCEV).
Оценив исходные данные ЗВКП, измерив ВГД после капельной местной анестезии (раствор инокаина), больному накладывали на склеру снаружи от лимба, вакуумную «чашечку-присоску», соединенную гибкой полимерной трубочкой с вакуумным компрессором. Чашечка фиксировалась непосредственно за лимбом за счет постепенного создания вакуума в системе.
Степень декомпрессии под вакуумной «чашечкой-присоской» регулировалась по показанию манометра, которым снабжен компрессор.
Вакуумная компрессия проводилась с помощью вакуумного компрессора ОЭОФ-01 (Россия) и модифицированной вакуумной «чашечки-присоски» (Астахов Ю.С., Даль Н.Ю., Соколов В.О., 2002).
Дозируя уровень вакуума под склеральной чашечкой, измеряли величину ВГД, которая оценивалась стандартным тонометром Маклакова.
Использование склеральной «чашечки-присоски» позволяло осуществлять контроль за ВГД в ходе нагрузки, т.к. роговица исследуемого глаза оставалась интактной. При этом у всех пациентов добивались повышения ВГД на 10 мм рт. ст. от его исходного уровня. Компрессию проводили в течение двух минут. Через две минуты после начала компрессии повторно фиксировались ЗВКП. После этого вакуумный компрессор выключали, отсоединяли чашечку и в исследуемый глаз закапывали антисептические капли. При использовании «чашечки – присоски» не требовалось фиксации верхнего века. «Чашечка – присоска» обрабатывалась стандартными растворами антисептиков перед каждым использованием.
Методика проведения ретинальной томографии (НRT-II)
Исследование выполнялось на приборе Heidelberg Retina Tomograph– II по стандартной методике, рекомендуемой фирмой Heidelberg Engineering (Германия). Пациентам выполнялись исследования НRT-II до лекарственного препарата и на фоне его применения. В каждом исследовании для анализа структуры головки зрительного нерва изучались наиболее информативные параметры HRT: площадь нейроретинального ободка, объем нейротинального ободка, средняя толщина ретинальных нервных волокон (Куроедов А.В., Голубев С.Ю., 2004, Mikelberg F. с соавт., 1993).
Характеристика лекарственных препаратов, входящих
в данные исследования
В данной работе нами были исследованы лекарственные препараты: Акатинол мемантин, Ретиналамин и Бетаксолол 0,5%, которые по данным отечественной и зарубежной литературы могут оказывать нейропротекторный эффект при первичной открытоугольной глаукоме глаукоме.
Акатинол мемантин («MERZ», Германия) оказывает модулирующее действие на глутаматергическую систему, является неконкурентным антагонистом NMDA-рецепторов, блокирует кальциевые каналы, нормализует мембранный потенциал нейронов, оказывает нейромодулирующее действие, стимулирует передачу нервного импульса.
Ретиналамин (ретилин, «ГЕРОФАРМ», Россия) является пептидным биорегулятором (цитомедином), выделенным из сетчатки глаза крупного рогатого скота. Препарат применяется в офтальмологии и способствует сохранению регуляторных механизмов межклеточного взаимодействия в виде восстановления синтеза тканеспецифичных белков (Морозов В.Г., Хавинсон В.Х., 1997; 1998).
Бетаксолол (Бетоптик) («Alcon», США) – селективный β1-адреноблокатор, не обладающий внутренней симпатомиметической активностью и мембраностабилизирующим действием. Используется в лечении глаукомы, снижает офтальмотонус и одновременно улучшает кровоток в артериях сетчатки и зрительного нерва (Алексеев В.Н, Харьковский А.О., Егоров Е.А., 2001, Chidlow G., Melena J., Osborne N.N., 2000).
РЕЗУЛЬТАТЫ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ
До и на фоне лечения Акатинол мемантином было обследовано 57 пациентов с ПОУГ разных стадий при нормализованном внутриглазном давлении (82 глаза). С ПОУГ I стадии обследовано 30 глаз, II стадии – 28 глаз, III стадии – 24 глаза. Лечебная доза Акатинол мемантина составила 5 мг в сутки приема внутрь в течение первой недели, 10 мг в сутки в течение второй недели и 15 мг в сутки течение третьей недели. Повторные исследования ВКП с ЗВКП проводились на четвертой неделе приема препарата.
Нами была рассчитана разница между изменениями значений латентности и амплитуды волны Р-100 ЗВКП при вакуум – компрессии до начала приема Акатинол мемантина и на фоне применения препарата (р<0,01). Если разницу в изменении значений латентности и амплитуды волны Р-100 при вакуум-компрессии до и на фоне лечения Акатинол мемантином выразить в процентах по отношению к изменению параметров ЗВКП до начала лечения, то эффективность Акатинол мемантина (увеличение толерантности ДЗН к дозированному искусственному повышению ВГД) при ПОУГ I стадии по показателю латентности составила 56,9%, по показателю амплитуды – 37%, II стадии по показателю латентности – 65,8%, по показателю амплитуды – 52,2%, III стадии по латентности – 44,2%, по амплитуде – 55,5% (Рис.1).
С помощью НRТ нами обследовано 33 человека с ПОУГ разных стадий (56 глаз). С ПОУГ в I стадии было обследовано – 17 глаз, II стадии – 19 глаз, с III стадии – 20 глаз.
По данным НRТ установлено достоверное увеличение средней толщины ретинальных нервных волокон на фоне лечения Акатинол мемантином у пациентов с ПОУГ II и III стадий (р<0,05).
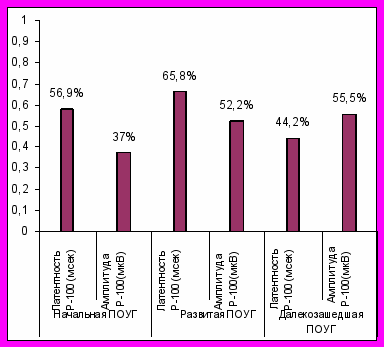
Рис.1 Эффективность Акатинол мемантина по результатам определения показателей ЗВКП (латентности и амплитуды волны Р-100) у пациентов ПОУГ I-III стадий (P<0,05)
До и на фоне инъекций Ретиналамина нами было обследовано человек 37 человек (64 глаза). С ПОУГ I стадии обследовано 21глаз, II стадии – 19 глаз, III стадии – 24 глаза.
Лечебная доза Ретиналамина составила по 5 мг в виде парабульбарных инъекций в течение 10 дней. Повторные исследования проводились на десятый день применения препарата.
При оценке зрительного нерва по данным вакуум-компрессионной пробы с контролем ЗВКП (латентности и амплитуды волны Р-100) на фоне инъекций Ретиналамина показан нейропротекторный эффект препарата у пациентов как с I, так и со II, и III стадиях ПОУГ. Эффективность Ретиналамина при ПОУГ I стадии по показателю латентности составила 42,2%, по показателю амплитуды – 49,1%, II стадии по показателю латентности – 50,1%, по показателю амплитуды – 63,7%, III стадии по латентности – 48,3%, по амплитуде – 44,7% (Рис. 2).
С помощью НRТ до и на фоне инъекций Ретиналамина было обследовано 41 человек с ПОУГ разных стадий (65 глаз). С ПОУГ I стадии – 24 глаза, II стадии – 21 глаз, III стадии – 20 глаз.
По данным НRТ установлено достоверное увеличение средней толщины ретинальных нервных волокон на фоне лечения Ретиналамином у пациентов с ПОУГ I и II стадий (р<0,05).
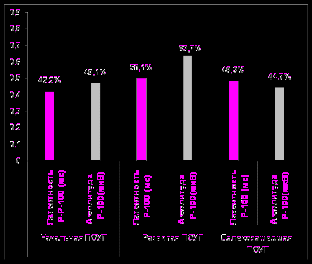
Рис.2 Эффективность Ретиналамина по результатам определения показателей ЗВКП (латентности и амплитуды волны Р-100)
у пациентов ПОУГ I-III стадий (P<0,05)
До и на фоне лечения Бетаксололом 0,5% обследовано 78 человек с ПОУГ при нормализованном внутриглазном давлении разных стадий (132) глаза. С ПОУГ в первой стадии было обследовано 55 глаз, во II – 43 глаза, и в III – 34 глаза.
Пациентам назначали инстилляции Бетаксолола 0,5% – 2 раза в день в течение десяти дней. Повторное исследование проводили на десятый день применения препарата.
При оценке состояния зрительного нерва по данным вакуум-компрессионной пробы с контролем на фоне инстилляций Бетаксолола 0,5% доказана эффективность препарата только у пациентов с I и II стадией ПОУГ (р<0,05). Эффективность Бетаксолола 0,5% при ПОУГ I стадии по показателю латентности составила 73,5%, по показателю амплитуды – 52,4%, при ПОУГ II стадии по латентности – 34,9%, по амплитуде – 19,3%.(Рис.3).
Достоверных изменений значений латентности и амплитуды на увеличение ВГД на фоне инстилляций Бетаксолола 0,5% у пациентов с ПОУГ III стадии не выявлено.
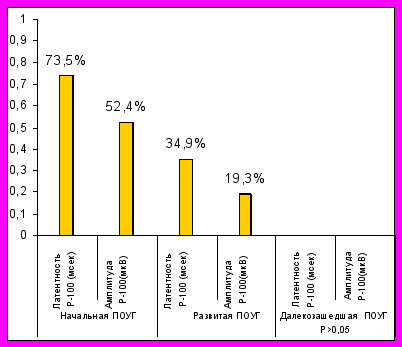
Рис. 3 Эффективность Бетаксолола 0,5% по результатам определения показателей ЗВКП (латентности и амплитуды волны Р-100) у пациентов ПОУГ I-III стадий (P<0,05)
HRT проводилось до и на фоне лечения Бетаксололом 0,5%- 47 пациентам (73 глаза). С ПОУГ I стадии – 28 глаз, II стадии -23 глаза, III стадии – 22 глаза. Повторные исследования НRТ проводились на десятый день применения препарата. По данным НRТ на фоне инстилляций Бетаксолола 0,5% увеличения площади нейроретинального пояска, объема нейроретинального пояска и средней толщины ретинальных нервных волокон у пациентов с ПОУГ I, II и III стадиях не доказано (р>0,05).
В результате исследований установлено, что Акатинол мемантин, Ретиналамин и Бетаксолол 0,5% не приводили к достоверным изменениям показателей ВГД у пациентов с ПОУГ I, II и III стадии глаукомы (р>0,05).
В ходе исследований для определения нейропротекторного действия изучаемых препаратов проводилась также оценка полей и остроты зрения. При сравнении результатов до и на фоне терапии препаратами достоверных различий в параметрах полей зрения и остроты зрения получено не было.
ВЫВОДЫ
1. Вакуум – компрессионная проба с контролем ЗВКП со склеральной «чашечкой-присоской» позволяет оценивать устойчивость зрительного нерва к повышению ВГД до и на фоне действия лекарственных препаратов у больных с первичной открытоугольной глаукомой.
2. По данным вакуум-компрессионной пробы с контролем ЗВКП доказано, что лекарственные препараты Акатинол Мемантин и Ретиналамин обладают нейропротекторным действием (увеличивают толерантность зрительного нерва к повышенному ВГД) в начальной, развитой и далекозашедшей стадиях первичной открытоугольной глаукомы.
3.
Бетаксолол 0,5% увеличивает толерантность зрительного нерва к повышенному действию ВГД только в начальной и развитой стадиях первичной открытоугольной глаукомы.
4.
По данным НRT доказано достоверное увеличение средней толщины ретинальных нервных волокон при применении Акатинол мемантина в развитой и далекозашедшей стадиях глаукомы, Ретиналамина – начальной и развитой стадиях глаукомы.
5. По данным НRТ увеличения средней толщины ретинальных нервных волокон при применении Бетаксолола 0,5% не установлено.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Вакуум – компрессионную пробу с контролем ЗВКП и HRT можно рекомендовать для определения толерантности зрительного нерва к повышению ВГД при оценке нейропротекторного эффекта различных препаратов.
2. Акатинол мемантин может быть использован перорально у больных с ПОУГ в начальной, развитой и далекозашедшей стадиях глаукомы в терапевтических дозах: 5 мг в сутки в течение первой недели, 10 мг в сутки в течение второй недели и 15 мг в течение третьей недели для повышения устойчивости зрительного нерва к условиям ишемии при глаукоме у пациентов с ПОУГ I,II и III стадии .
3. Парабульбарные инъекции Ретиналамина по 5,0 мг в сутки в течение 10 дней целесообразно применять для улучшения функциональной активности ганглиозных клеток сетчатки и их аксонов у пациентов с ПОУГ в начальной, развитой и далекозашедшей стадиях глаукомы.
4. Инстилляции Бетаксолола 0,5% (Бетоптика) 2 раза в сутки не менее 10 дней можно рекомендовать для повышения устойчивости зрительного нерва к условиям ишемии у больных с ПОУГ в начальной и развитой стадиях.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Астахов Ю.С., Бутин Е.В., Соколов В.О. К вопросу о нейропротекторном влиянии бетаксолола у больных с первичной открытоугольной глаукомой при нормализованном внутриглазном давлении // Клиническая офтальмология. – М., 2003 г. – Т.4, №3. – С. 117-119.
2. Астахов Ю.С., Бутин Е.В., Морозова Н.В., Соколов В.О. К вопросу о нейропротекторном влиянии акатинол мемантина и бетаксолола у больных первичной открытоугольной глаукомой // Всеросийская научно – практическая конференция «Глаукома: проблемы и решения»: СПб., науч. Тр. – М., 2004. – С.170174.
3. Астахов Ю.С., Бутин Е.В., Морозова Н.В., Соколов В.О. К вопросу об оценке нейропротекторного действия Акатинол Мемантина, Ретиналамина и Бетаксолола у больных с первичной открытоугольной глаукомой //Тезисы докладов 3-й Международной Конференции для врачей центральных госпиталей, диагностических центров и военных поликлиник МО РФ. НРТ клуб. 2005 г.
4. Астахов. Ю.С, Бутин Е.В., Морозова Н.В., Соколов В.О. Оценка нейропротекторного действия Ретиналамина при лечении больных с первичной открытоугольной глаукомой // Терра медика нова. – № 2. – СПб., 2006. – С. 49-54.
5. Астахов. Ю.С, Бутин Е.В., Морозова Н.В., Соколов В.О. Результаты применения ретиналамина у больных с первичной открытоугольной глаукомой // Глаукома. – № 2. – М., 2006. – С. 43-47.
6. Астахов Ю.С., Бутин Е.В., Морозова Н.В., Соколов В.О. Оценка нейропротекторного действия ретиналамина в лечении больных с первичной открытоугольной глаукомой // Ретиналамин. Нейропротекция в офтальмологии. Сборник научных статей. – СПб., Наука, 2007. – С. 38-46.
БУТИН Е.В. Оценка нейропротекторного действия различных препаратов у больных с первичной открытоугольной глаукомой // Автореф. дисс. … канд. мед. наук: 14.01.07
. – СПб.: Изд-во «ВВМ», 2008. – 20 с.
