Міністерство охорони здоров’я України
| Вид материала | Документы |
- Міністерство охорони здоров'я україни професійна спілка працівників охорони здоров'я, 111.65kb.
- Міністерство охорони здоров'я україни нака, 1199.6kb.
- Міністерство охорони здоров'я україни нака, 1116.44kb.
- Міністерство охорони здоров'я україни наказ, 1196.85kb.
- Міністерство охорони здоров'я україни, 5153.63kb.
- Міністерство охорони здоров'я україни нака, 1248.35kb.
- Міністерство охорони здоров'я україни нака, 441.54kb.
- Міністерство охорони здоров'я україни нака, 354.54kb.
- Міністерство охорони здоров'я україни наказ n 117 від, 4958.08kb.
- Міністерство охорони здоров’я України, 2017.44kb.
Міністерство охорони здоров’я України
Міністерство освіти і науки України
Сумський державний університет
2947 Методичні вказівки
до практичних занять
з дисципліни “Клініко-лабораторна діагностика”
Розділ “Біохімічні тести для діагностики
захворювань печінки”
для студентів спеціальності 7.110101
денної форми навчання
Суми
“Видавництво СумДУ”
2010
Методичні вказівки до практичних занять з дисципліни “Клініко-лабораторна діагностика”. Розділ “Біохімічні тести для діагностики захворювань печінки” / укладачі: І.В. Чорна, І.Ю. Висоцький.- Суми: Вид-во СумДУ, 2010. - 78 с.
Кафедра біохімії та фармакології
ЗМІСТ
С.
Передмова .…………………………………………………………..5
Список скорочень .…………………………………………………...6
1 Основні функції печінки ....…..….…………………………………7
2 Метаболізм білірубіну ..……………...…………...………..…...….9
3 Клініко-діагностичне значення дослідження
пігментного обміну …………………………………………..…….14
4 Біохімічні методи оцінки функцій печінки .………………………18
4.1 Проби, які характеризують метаболічну функцію печінки ..……18
4.1.1 Проби, що відображають роль печінки
в білковому обміні ...………………………………………………..18
4.1.2 Проби, що відображають роль печінки
у вуглеводному обміні ..…………………………………………….22
4.1.3 Проби, що відображають участь печінки
у ліпідному обміні ...………………………………………………..23
4.1.4 Проби, що відображають участь печінки
у пігментному обміні .………………………………………………25
4.1.5 Проби, що відображають роль печінки в обміні
мікроелементів, гормонів і біологічно активних речовин ..…………26
4.2 Ферменти як функціональні проби печінки .……………………27
4.3 Проби, що характеризують знешкоджувальну
функцію печінки ...………………………………………………….36
4.4 Проби, що відображають екскреторну
(поглинально-видільну) функцію печінки .…………………………37
5 Синдромна класифікація функціональних проб печінки .…………39
5.1 Синдром цитолізу ..….………………………………………….40
5.2 Синдром внутрішньопечінкового та позапечінкового
холестазу .....……..…..……..……..……..…..……..……..……..…43
5.3 Синдром гепатодепресії (малої недостатності печінки) ….……..47
5.4 Синдром запалення (мезенхімально-запальний) …………….….49
5.5 Синдром шунтування печінки ..…………………………………51
5.6 Синдром регенерації та пухлинного росту печінки ……..………52
6 Функціональна біохімічна характеристика основних
нозологічних форм захворювань гепатобіліарної системи …….……53
6.1 Гострий гепатит ..…………………….…………………………53
6.2 Хронічний гепатит ..…………………….………………………54
6.3 Цироз печінки .………………………….………………………55
6.4 Жовчнокам’яна хвороба ..…………………….…………………57
7 Алгоритм обстеження хворих із патологією гепатобіліарної
системи та лабораторні тести, які використовують на різних
етапах діагностики .......…………………….………………………58
8 Лабораторна діагностика спадкових порушень метаболізму білірубіну та інших захворювань печінки .....……………………….60
8.1 Спадкові порушення метаболізму білірубіну ...…………………60
8.1.1 Синдром Жильбера ....…….……………….……….…………60
8.1.2 Синдром Криглера-Найяра ...………………………………….61
8.1.3 Синдром Дабіна-Джонсона ....……..…..……..……..……..….62
8.1.4 Синдром Ротора ...….……..….……..….……..….……..….…63
8.2 Рідкісні спадкові захворювання печінки …………………….….63
8.2.1 Хвороба Вільсона .....……….…………………………………63
8.2.2 Первинний гемохроматоз .......…….……………….……….…65
8.2.3 Недостатність α1-антитрипсину .....……………………………67
9 Гепатотоксичні речовини ...……..…..……..……..……..….….….68
Список використаної літератури .....…..….……..….……..….…….73
Додаток А .......…..….……..….…..….……..….…..….……..….….75
Передмова
Печінка є органом із дуже широким функціонально-метаболічним профілем, і тому вона становить предмет великої кількості біохімічних досліджень. Головне її призначення в організмі – трансформація поживних речовин у такі фізичні та хімічні форми, які, з одного боку, могли б бути використані у подальшому організмом, а з іншого – піддані екскреції.
Біохімічні дослідження функції печінки необхідні для виявлення хвороби, діагностичного пошуку, прогнозування, оцінки тяжкості ураження та здійснення контролю за ефективністю лікування. Не існує якогось одного, універсального аналізу, але не слід також вдаватися й до безлічі різних досліджень. Чим більше проводиться необґрунтованих досліджень, тим більше шансів виявити незначущі відхилення біохімічних показників, що утруднює процес діагностики. Слід обмежуватися невеликою кількістю відносно простих досліджень, що мають високу діагностичну цінність. Зрозуміло, що результати біохімічних досліджень у діагностичному процесі не єдині. Одночасно клініцисти використовують дані анамнезу та об’єктивного дослідження, результати радіонуклідної діагностики, комп’ютерної томографії та біопсії печінки. У той же час диференційну діагностику на ранніх стадіях захворювання та оцінку характеру ураження гепатоцитів можна провести лише на основі лабораторних даних клінічної біохімії.
У методичних вказівках сформульовані чіткі критерії біохімічної диференціації жовтяниць, подані сучасні підходи до діагностики метаболічних, токсичних та вірусних захворювань печінки, наведені принципи синдромальної лабораторної діагностики уражень цього органа. Велику увагу приділено функціональним пробам печінки, алгоритмам дослідження хворих із різними нозологічними формами захворювань. Методичні вказівки містять додаток А, у якому наведено комбінації біохімічних тестів для диференційної діагностики захворювань печінки, а також діагностичну цінність різних методів дослідження.
Список скорочень
АДГ – алкогольдегідрогеназа
АлАТ – аланінамінотрансфераза
АсАТ – аспартатамінотрансфераза
ГГТП – γ-глутамілтранспептидаза
ГлДГ – глутаматдегідрогеназа
ГК – глюкуронова кислота
ІДГ – ізоцитратдегідрогеназа
ЛАП – лейцинамінопептидаза
ЛДГ – лактатдегідрогеназа
ЛПВЩ – ліпопротеїни високої щільності
ЛПДНЩ – ліпопротеїни дуже низької щільності
ЛПНЩ – ліпопротеїни низької щільності
ЛФ – лужна фосфатаза
МДГ – малатдегідрогеназа
НЕЖК – неетерифіковані жирні кислоти
5’-НТ – 5’-нуклеотидаза
ОКТ – орнітин-карбамоїлтрансфераза
СДГ – сорбітолдегідрогеназа
ТАГ – триацилгліцероли
УДФГК – УДФ-глюкуронова кислота
ФДФА – фруктозодифосфатальдолаза
Ф-1-ФА – фруктозо-1-фосфатальдолаза
ХЕ – холінестераза
1 Основні функції печінки
Печінка являє собою центральний орган, де продукується загальний обмінний пул для метаболізму білків, жирів і вуглеводів. Інша важлива функція печінки полягає в її тісному зв’язку з плазмою крові: печінка непрямо впливає на збереження рівноваги рідин і багатьох транспортних процесів, які відбуваються в плазмі. Більша частина білків плазми (альбумін, більшість глобулінів, фактори згортання крові) утворюються в печінці. Крім того, в цьому органі утворюються фосфатиди плазми й більша частина холестерину. Важливі специфічні функції печінки зумовлені її роллю в детоксифікації та екскреції ендогенних та екзогенних речовин. Разом із жовчю виділяються холестерин, жовчні кислоти та пігменти, а також кінцеві продукти порфіринового обміну й чужорідні речовини. У результаті здійснення багатьох обмінних функцій печінка постачає 1/7 частину енергії, що утворюється в організмі.
Таким чином, можна виділити такі основні функції печінки:
- обмінна або метаболічна (участь у вуглеводному, білковому, ліпідному, пігментному та інших видах обміну);
- біосинтетична;
- екскреторна;
- знешкоджувальна.
Метаболічні функції печінки подані в таблиці 1.
Таблиця 1 - Основні функції печінки
| Вид обміну | Функції |
| Вуглеводний | 1 Забезпечення постійного рівня глюкози в крові за рахунок синтезу й розпаду глікогену або в результаті глюконеогенезу (синтезу глюкози з невуглеводних метаболічних попередників: пірувату, лактату, глюкогенних амінокислот, гліцеролу) |
| 2 Перетворення галактози і фруктози у глюкозу |
Продовження табл. 1
| Вид обміну | Функції |
| | 3 Найбільш інтенсивне порівняно з іншими органами розщеплення глюкози як аеробним, так і анаеробним шляхами |
| 4 Утворення глюкуронової кислоти, що бере участь у реакціях кон’югації (механізми знешкодження погано розчинних у воді сполук), а також є сировиною для побудови глікозаміногліканів | |
| Ліпідний | 1 Синтез жирних кислот, фосфоліпідів, триацилгліцеролів, гліколіпідів |
| 2 Роль у синтезі ліпопротеїнів, в основному ЛПДНЩ і ЛПВЩ | |
| 3 Синтез і етерифікація холестерину | |
| 4 Синтез жовчних кислот, жовчоутворювальна функція | |
| 5 Розщеплення жирів до гліцерину та жирних кислот | |
| 6 Окислення жирних кислот до кетонових тіл (кетогенез), які використовуються периферичними тканинами для компенсації енергетичних затрат | |
| Білковий | 1 Синтез більшості білків плазми (в тому числі деяких факторів коагуляції, але не імуноглобулінів) |
| 2 Підтримання постійності рівня амінокислот у крові | |
| 3 Розщеплення й перебудова амінокислот (дезамінування, декарбоксилювання й переамінування) | |
| 4 Розщеплення білків до низькомолекулярних сполук, які використовуються печінкою для різних цілей – метаболічних або пластичних |
Продовження табл. 1
| Вид обміну | Функції |
| | 5 Синтез сечовини |
| 6 Розщеплення нуклеопротеїнів з утворенням амінокислот і азотистих основ, а також перетворення останніх на сечову кислоту | |
| 7 Синтез холіну, який є структурним компонентом фосфоліпідів | |
| 8 Синтез креатину | |
| 9 Знешкодження токсичних продуктів метаболізму ряду циклічних амінокислот | |
| Пігментний | 1 Катаболізм гемоглобіну та інших гемовмісних білків до білірубіну |
| 2 Метаболізм та екскреція білірубіну | |
| Обмін гормонів | 1 Метаболізм і виведення стероїдних гормонів |
| 2 Метаболізм поліпептидних гормонів | |
| Обмін вітамінів | 1 Всмоктування вітамінів (жиророзчинні вітаміни A, D, E, K) |
| 2 Синтез вітамінів (вітамін А) | |
| 3 Гідроксилювання вітаміну D у 25-гідроксихолекальциферол | |
| 4 Депонування вітамінів (A, D, E, K, РР, В1, В2, В12) | |
| 5 Інактивація та виведення з організму (вітаміни E, В2, РР та ін.) | |
| Обмін мікроелементів | Депонування мікроелементів (заліза, міді, марганцю та ін.) |
2 Метаболізм білірубіну
Жовчними пігментами називають продукти розпаду гемоглобіну та інших хромопротеїнів – міоглобіну, цитохромів і гемовмісних ферментів. До жовчних пігментів належать білірубін та уробілінові тіла – уробіліноїди.
У нормі близько 80% білірубіну утворюється при розпаді еритроцитів. За фізіологічних умов в організмі дорослої людини за одну годину руйнується 1-2·108 еритроцитів. Таким чином, протягом доби у людини, вагою 70 кг, оновлюється приблизно 6 г гемоглобіну. Еритроцити фагоцитуються макрофагами головним чином у селезінці, а також у кістковому мозку і печінці. Розпад гемоглобіну починається з розкриття циклічної структури протопорфірину: відбувається розрив α-метинового містка між двома пірольними кільцями внаслідок окиснення атома вуглецю до СО. Реакція каталізується складною ферментною системою ендоплазматичного ретикулуму – гемоксигеназою. Утворюється зелений кров’яний пігмент вердоглобін. При подальшому розпаді вердоглобіну відщеплюється білковий компонент - глобін, іон заліза, та відбувається утворення жовчного пігменту зеленого кольору – білівердину.
Залізо, що вивільняється при утворенні білівердину, включається в загальний обмін заліза й повторно використовується для синтезу гемопротеїнів чи відкладається для запасання. Глобін гідролізується протеолітичними ферментами й поповнює пул амінокислот організму.
Білівердин, відновлюючись під дією білівердинредуктази, перетворюється в пігмент червоно-коричневого кольору – білірубін. Утворений пігмент називають вільним, або некон’югованим.
Подальший метаболізм білірубіну головним чином відбувається в печінці. Однак вільний білірубін є погано розчинним у плазмі й воді, тому у крові він транспортується в комплексі з альбуміном. Для визначення вільного білірубіну в крові необхідне попереднє осадження білка спиртом чи кофеїновим реактивом. Лише після цього білірубін вступає у взаємодію з діазореактивом, тому його по-іншому називають непрямим білірубіном. Вільний (непрямий) білірубін не проходить через нирковий бар’єр і в сечу не потрапляє. У комплексі з альбуміном білірубін надходить у печінку. У подальшому метаболізм білірубіну складається з трьох процесів:
- поглинання білірубіну паренхімальними клітинами печінки (за участю цитоплазматичних транспортних білків, позначених як “Y” та “Z”);
- кон’югація білірубіну в гладкому ендоплазматичному ретикулумі гепатоцитів;
- секреція білірубіну з ендоплазматичного ретикулуму в жовч.
У печінці відбувається перехід білірубіну від альбуміну на синусоїдальну поверхню гепатоцитів за участю насичувальної системи перенесення. Ця система має дуже велику ємність і навіть при патологічних станах не лімітує швидкість метаболізму білірубіну.
У гепатоцитах білірубін зв’язується (кон’югує) з УДФ-глюкуроновою кислотою (УДФГК), завдяки чому він переходить у водорозчинну (і менш токсичну) форму. Ця реакція каталізується ферментом УДФ-глюкуроніл-трансферазою. Спочатку відбувається утворення білірубін-моноглюкуроніду (в гладкому ендоплазматичному ретикулумі гепатоцитів), а потім диглюкуроніду білірубіну (у канальцях мембрани гепатоцитів). Утворений глюкуронід білірубіну отримав назву зв’язаного, або кон’югованого, білірубіну. Він дає пряму реакцію з діазореактивом, тому по-іншому його називають прямим білірубіном.
Кон’югований (зв’язаний, прямий) білірубін – це нормальний компонент жовчі. Секреція його в жовч відбувається проти досить високого градієнта концентрації за участю механізмів активного транспорту. Цей транспорт є стадією, що лімітує швидкість метаболічної трансформації білірубіну в печінці. У кров кон’югований білірубін потрапляє в дуже невеликій кількості. Він може проходити через нирковий бар’єр, але оскільки в крові здорової людини його дуже мало, то в сечі він не визначається звичайними лабораторними методами.
У складі жовчі кон’югований білірубін надходить у тонкий кишечник, де від нього відщеплюється глюкуронова кислота (ГК) за участю специфічних бактеріальних ферментів β-глюкуронідаз; далі кишкова мікрофлора відновлює пігмент із послідовним утворенням мезобілірубіну і мезобіліногену (уробіліногену). Деяка кількість мезобіліногену утворюється вже в печінці і надходить у жовчний міхур разом із глюкуронідами білірубіну. Із тонкої кишки частина утвореного мезобіліногену (уробіліногену) всмоктується через кишкову стінку, потрапляє у ворітну вену та надходить у печінку, де повністю розщеплюється до дипіролів, тому в нормі до загального кола кровообігу та в сечу мезобіліноген (уробіліноген) не потрапляє. При ушкодженні паренхіми печінки процес розщеплення мезобіліногену (уробіліногену) до дипіролів порушується й уробіліноген переходить у кров і звідти в сечу, де окиснюється до уробіліну киснем повітря.
У нормі більша частина безколірного мезобіліногену з тонкої кишки надходить у товсту, де відновлюється в стеркобіліноген за участю анаеробної мікрофлори. Утворений безколірний стеркобіліноген у нижніх відділах товстого кишечника (головним чином у прямій кишці) при контакті з повітрям окиснюється до оранжево-жовтого стеркобіліну та виділяється з калом.
Лише невелика частина стеркобіліногену всмоктується в систему нижньої порожнистої вени (потрапляє спочатку в гемороїдальні вени) і в подальшому цей водорозчинний пігмент виділяється нирками під назвою «уробіліну» сечі. Отже, в нормі сеча людини містить у слідовій кількості похідні білірубіну (білірубіноїди), які в клінічній практиці ще мають назву уробілінових тіл. Ці слідові концентрації пігменту в сечі можуть не визначатися звичайними клініко-біохімічними методами дослідження, і тому вважають, що в сечі здорової людини «уробілін», як правило, відсутній.
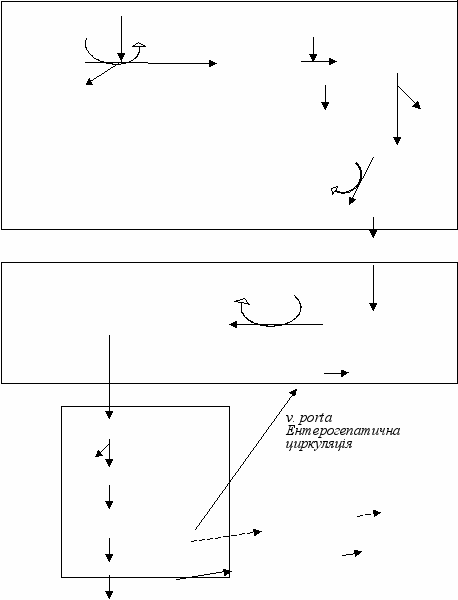
На рисунку 1 зображена схема катаболізму гемоглобіну та біотрансформації жовчних пігментів.
О2
 НАДФН+Н+ НАДФ+ Н2О
НАДФН+Н+ НАДФ+ Н2ОГемоглобін Вердоглобін Вердогемохром
гемоксигеназа гідроліз
СО
Глобін Fe2+
НАДФН+Н+ Білівердин
білівердин-
Клітини ретикуло- НАДФ редуктаза
ендотеліальної системи
Білірубін
Кров комплекс білірубіну
з альбуміном
Печінка 2УДФ 2УДФГК
Білірубін-диглюкуронід Білірубін
УДФ-глюкуроніл-
трансфераза
Мезобіліноген ди- і трипіроли
Жовч
Кишечник
Білірубін-диглюкуронід
β-глюкуронідаза
2ГК
Білірубін
відновлення Кров Сеча
Мезобіліноген
(уробіліноген) Уробіліноген Уробілін
відновлення
Стеркобіліноген Стеркобіліноген Стеркобілін
окиснення (“уробілін”)
Кал Стеркобілін
Рисунок 1 - Катаболізм гемоглобіну та біотрансформація жовчних пігментів
3 Клініко-діагностичне значення дослідження
пігментного обміну
Жовтяниця – важливий симптом порушення пігментного обміну. Як правило, виявляється клінічно за рівня білірубіну в крові 27-34 мкмоль/л. Тяжкість жовтяниці відповідає величинам білірубінемії. Так, прийнято вважати, що її легка форма відповідає концентрації білірубіну до 85 мкмоль/л; рівень білірубіну 86-169 мкмоль/л свідчить про середньотяжку форму, а вище 170 мкмоль/л – тяжку форму жовтяниці.
Виділяють три основні причини гіпербілірубінемій, які зумовлюють три форми жовтяниць: 1) посилення гемолізу еритроцитів; 2) порушення функції печінкових клітин; 3) затримка відтоку жовчі.
Гемолітичні (передпечінкові) жовтяниці поділяють на: 1) уроджені – резус-конфліктна вагітність;
2) спадкові: а) порушення структури мембрани еритроцитів – спадковий мікросфероцитоз; б) порушення обміну гемоглобіну – «фізіологічна» жовтяниця новонароджених; в) блокування ферментів гліколізу та антиоксидантного захисту в еритроцитах, недостатність ензиму глюкозо-6-фосфатази; а також таласемії, порфірії, гемоглобінопатії;
3) набуті – отруєння оцтовою кислотою, сульфаніламідами, інфекції (грип, сепсис, пневмонія), малярія, опікова хвороба, «маршовий» гемоліз, переливання несумісної групи крові, аутоімунні гемолітичні анемії.
У результаті посиленого гемолізу еритроцитів відбувається інтенсивне утворення в ретикулоендотеліальних клітинах вільного білірубіну із гемоглобіну. У той же час печінка виявляється нездатною зв’язати увесь цей білірубін із глюкуроновою кислотою, що й призводить до накопичення вільного білірубіну (непрямого) в крові та тканинах. Однак у дорослих навіть при значному гемолізі некон’югована гіпербілірубінемія, як правило, незначна (менше 68,4 мкмоль/л) унаслідок великої здатності печінки до кон’югування білірубіну. Оскільки через печінку проходить підвищений потік непрямого білірубіну, то утворюється більше й прямого білірубіну. Збільшення потоку прямого білірубіну в жовч призводить до збільшеного утворення уробіліногенів та стеркобіліногену в кишечнику. У крові: гіпербілірубінемія за рахунок вільної фракції; знижений уміст еритроцитів; збільшена кількість ретикулоцитів (посилена регенерація еритроцитів у периферичній крові); зміна форми еритроцитів (макроцитоз, мікросфероцитоз, овалоцитоз). Темне забарвлення калу та сечі за рахунок підвищеного вмісту уробілінових тіл. Жовтушність шкіри та склер помірна, шкірні покриви, як правило, бліді (за рахунок анемії); функції печінки суттєво не страждають.
«Фізіологічна» жовтяниця у новонароджених – це найбільш часта форма некон’югованої гіпербілірубінемії. Причинами її є прискорений гемоліз еритроцитів та незрілий стан печінкової системи поглинання, кон’югації (знижена активність УДФ-глюкуронілтрансферази) та секреції білірубіну. У зв’язку з тим, що білірубін, який накопичується в крові, знаходиться у некон’югованому (вільному) стані, коли його концентрація в крові перевищує рівень насичення альбуміну (34,2-42,75 мкмоль/л), він здатний долати гематоенцефалічний бар’єр. Це може призвести до гіпербілірубінемічної токсичної енцефалопатії. Для лікування такої жовтяниці ефективним є стимулювання системи кон’югації білірубіну фенобарбіталом. На сьогодні найдієвішим і перевіреним методом для зниження токсичності білірубіну при фізіологічній жовтяниці є фототерапія. Шкіру малюка освітлюють спеціальною установкою (в середньому 96 годин на курс). Під впливом УФ світла білірубін перетворюється на нетоксичні похідні, основне з яких має назву «люмірубін». У нього інший шлях виведення, і через 12 годин він виходить із організму з калом і сечею.
Паренхіматозні (печінкові) жовтяниці поділяють на:
1) спадкові: синдром Жильбера; синдром Криглера-Найяра; синдроми Дабіна-Джонсона та Ротора;
2) набуті паренхіматозні жовтяниці виникають у результаті деструктивно-дистрофічних змін у печінці або інфільтративних змін у стромі (гострі вірусні, інфекційні та токсичні гепатити, хронічний гепатит, хвороба Вільсона). Ушкодження клітин печінки призводить до порушення їх функцій:
- Порушується екскреція прямого білірубіну в жовчні капіляри, він частково потрапляє в кров, де збільшується його вміст. Підвищення концентрації в крові прямого білірубіну призводить до його появи у сечі внаслідок фільтрації через мембрану ниркових клубочків. Зниження вмісту прямого білірубіну в жовчі призводить до зменшення утворення стеркобіліногену.
- Порушується процес кон’югації вільного білірубіну, тому в крові збільшиться вміст і непрямого білірубіну. Непрямий білірубін, незважаючи на збільшення концентрації в крові, в сечу не надходить.
- Порушується процес руйнування до ди- та трипіролів мезобіліногену (уробіліногену), який у великій кількості потрапляє у загальний кровотік і виділяється з сечею.
- При патології невелика частина кон’югованого білірубіну ковалентно зв’язується з альбуміном – δ-білірубін. При лабораторному аналізі визначається як частина прямого білірубіну. Через ковалентний зв’язок із альбуміном циркулює у плазмі більше тижня після зникнення білірубіну з сечі. При паренхіматозній жовтяниці на частку δ-білірубіну припадає 89-90% від загального білірубіну.
Застою білірубіну сприяє різке ослаблення метаболічних процесів у печінці. Підвищення вмісту загального і особливо зв’язаного білірубіну в крові, а також наявність останнього в сечі не є ранніми ознаками ураження паренхіми печінки. Тому діагностичне значення цих показників невелике. Більшу роль вони відіграють у прогностичному плані: у міру загасання патологічного процесу рівень білірубіну в крові поступово знижується. Найбільш «чутливою» ознакою ураження печінки при гепатитах слугує поява уробіліну в сечі, яка спостерігається ще у дожовтяничний період. За різкого порушення функції печінки кількість уробіліну в добовому об’ємі сечі може сягати до 200 мг, тоді як у нормі він практично відсутній. У період розпалу паренхіматозного гепатиту відбувається зникнення уробіліну, оскільки стаз жовчі призводить до зменшеного виведення білірубіну та зниження утворення уробіліногену в кишечнику. У міру загасання патологічних змін жовч виділяється в більшій кількості і уробілінурія, яка знову з’являється, є сприятливою прогностичною ознакою, що свідчить про відновлення функції печінки. Тривала уробілінурія, що супроводжується іншими клінічними та біохімічними ознаками патології, розглядається як несприятливий результат захворювання.
Кров: підвищення вмісту загального білірубіну за рахунок підвищення рівнів вільного (в меншій мірі) та зв’язаного білірубінів (збільшення частки δ-білірубіну). Кал: зниження стеркобіліну (більш світле забарвлення калу). Сеча: білірубін (+), уробілінові тіла (+ або -).
Обтураційні (постпечінкові, механічні) жовтяниці поділяють на: 1) уроджені та 2) набуті. Перші – викликані атрезією або гіпоплазією жовчних протоків. Другі – зумовлені внутрішньо- або позапечінковим холестазом, що призводить до зменшення або припинення надходження жовчі в кишечник.
Внутрішньопечінковий холестаз виникає при естрогенній терапії в жінок; у деяких – під час вагітності; при первинному та вторинному біліарному цирозі печінки, при новоутвореннях печінки. У крові: гіпербілірубінемія за рахунок зв’язаної фракції; підвищена активність ЛФ за нормальних або субнормальних цифр трансаміназ; дуже високий рівень жовчних кислот; у сечі – зв’язаний білірубін.
Позапечінковий холестаз може бути викликаний жовчнокам’яною хворобою, гострим панкреатитом, раком голівки підшлункової залози. У крові на фоні гіпербілірубінемії за рахунок зв’язаної фракції відмічається різко підвищена активність трансаміназ і ЛФ. Сеча темна, піниться за рахунок наявності зв’язаного білірубіну та жовчних кислот; кал знебарвлений, жирний, глинистий через відсутність стеркобіліну та порушення всмоктування продуктів розпаду ліпідів та ліповітамінів (жовч не надходить у кишечник).
4 Біохімічні методи оцінки функцій печінки
Клінічна лабораторна діагностика має провідне значення в гепатології. Біохімічні тести не є строго специфічними, але за їх результатами можна зробити висновок про функціональний стан органа, підтвердити ураження печінки, а також судити про активність і тяжкість процесу.
Печінка має великі функціональні резерви, значну регенераційну здатність, а також множину та різноманітність функцій. У зв’язку з цим і запропоновано велику кількість методів функціонального дослідження цього органа. Це створює певні труднощі в їх підборі для розв’язання тієї або іншої клінічної задачі. Функціональні проби печінки мають різний ступінь чутливості та специфічності, а отже, і діагностичної інформативності.
