Учебная программа элективного курса 9 класс
| Вид материала | Программа |
- Программа элективного курса по русскому языку и литературе 9 класс, 83.37kb.
- Программа элективного курса 11 класс 70 часов, 4914.94kb.
- Программа элективного курса, 68 часов в год (2 ч/нед.). 10-й класс Пояснительная записка, 276.21kb.
- Программа элективного курса по экологии 9 класс «Лес и человек», 80.32kb.
- Рабочая программа элективного курса по русскому языку «секреты русской орфографии, 83.82kb.
- Рабочая учебная программа элективного курса «политическая психология» для специальностей:, 152.46kb.
- Элективный курс «Занимательное программирование» Информатика. Повышенный уровень, 167.38kb.
- Рабочая учебная программа элективного курса «история и культура народов кавказа» для, 129.37kb.
- Программа элективного курса по химии «строение и свойства кислородсодержащих органических, 667.3kb.
- Программа элективного курса Ставрополь, 186.92kb.
МОУ ГИМНАЗИЯ № 74
УЧЕБНАЯ ПРОГРАММА
ЭЛЕКТИВНОГО КУРСА
9 КЛАСС
«ХИМИЯ И ЗДОРОВЬЕ ЧЕЛОВЕКА»
16 часов
СОСТАВИТЕЛЬ:
СКОРОЩЕКА Н. В.
2005
1.ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
Одно из важнейших направлений современного образования – разработка и внедрение валеологического подхода в школьном образовании и воспитание. В рамках этой концепции образования встает проблема воспитания у учащихся потребности в здоровье формирования у них научного понимания сущности здорового образа жизни и выработки индивидуального валеологически обоснованного поведения.
Совсем недавно, встречаясь, наши предки говорили «Здравия желаю». Не правда ли, приятно осознавать, что твое здоровье кого - то интересует? Может быть, настало время, когда каждый должен задуматься над своим здоровьем и не только своим?
Знания, полученные в школе, мы не очень часто используем в повседневной жизни, конечно, если мы не связали свою жизнь с химией в профессиональном плане. Тем не менее именно этот предмет может стать источником знаний о нашем здоровье, т. к. только при изучении химии мы знакомимся с составом вещества на нашей Земле. Благодаря ему мы узнаем, каким образом эти вещества влияют на процессы жизнедеятельности организма, да и в целом на саму жизнь человека, что полезно нам и в каких количествах и, наконец, что вредно и до какой степени.
Организм человека – это сложная химическая система, которая не может функционировать самостоятельно, без взаимосвязи с окружающей средой.
Целью данного курса является формирование у учащихся знаний о здоровом образе жизни.
Задачи курса:
- актуализация изучаемого материала
- мотивация и активизация познавательной деятельности учащихся
- развитие интереса к предмету
- изучение биологической роли, источников поступления и выведение из организма химических элементов ; применение соединений в медицине, в быту.
Организм человека – это сложная химическая система, которая не может функционировать самостоятельно, без взаимосвязи с окружающей средой.
В данном курсе химические элементы и их соединения рассматриваются в соответствии с расположением в Периодической системе Д. И. Менделеева.
В связи с вышеизложенным разработан данный курс, предназначенный для учащихся 9 классов.
Возможные формы работы с данным содержанием – индивидуальная работа, сочетание коллективной и индивидуальной работы. Содержание учебно-тематического плана включает в себя проведение проб, помогающих в самоопределении школьников.
Средствами для осуществления данной работы является – создание авторских разработок, схем, заданий , а также, творческих работ – рефераты, доклады – на основе материалов и сведений, собранных самостоятельно.
2.Учебно – тематический план
| № | ТЕМА | Вид пробы | Количество часов | Учебное время | |
| теория | практика | ||||
| I. | Введение | | 1 | 1 | |
II. | Влияние химических элементов на здоровье человека | Решение задач | 15 | 9 | 6 |
| II.1. | Элементы I группы ПСХЭ Д. И. Менделеева | Решение задач | 2 | 1 | 1 |
| II.2. | Элементы II группы ПСХЭ Д. И. Менделеева | Решение задач | 2 | 1 | 1 |
| II.3. | Элементы III группы ПСХЭ Д. И. Менделеева | Решение задач | 1 | 1 | |
| II.4 | Элементы IV группы ПСХЭ Д. И. Менделеева | Решение задач | 2 | 1 | 1 |
| II.5 | Элементы V группы ПСХЭ Д. И. Менделеева | Решение задач | 3 | 2 | 1 |
| II.6 | Элементы VI группы ПСХЭ Д. И. Менделеева | Решение задач | 2 | 1 | 1 |
| II.7 | Элементы VII, VIII групп ПСХЭ Д. И. Менделеева | Решение задач | 3 | 2 | 1 |
3.Содержание тем
введение
1.Организационное занятие. Знакомство учащихся с темой учебного курса, целями и задачами.
II. Влияние химических элементов на здоровье человека
II. 1. I группа главная подгруппа
Общая характеристика. Натрий и здоровье человека. Биологическая роль натрия. Реакция организма на избыток и недостаток натрия.
Общая характеристика элементов побочной подгруппы I группы. Медь и здоровье человека. Биологические функции меди. Лечебное применение меди и ее препаратов. Реакция организма на избыток и недостаток меди. Серебро и здоровье человека. Лечебное применение серебра. Реакция организма на избыток серебра.
Вид проб
тема «Элементы I группы ПСХЭ Д. И. Менделеева»
Задача 1. В любой аптечке обязательно должна быть пищевая сода – гидрокарбонат натрия NaHCO
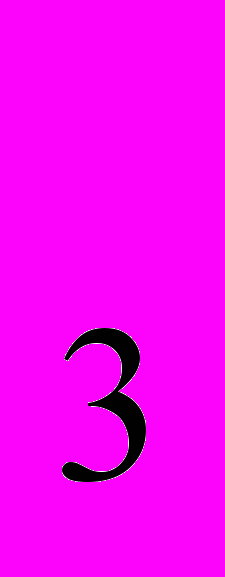 . Еще в 1845 г. немецкий врач Бульрих обнаружил, что питьевая сода устраняет изжогу – чувство жжения в нижней части пищевода при повышенной кислотности желудочного сока. Раствор, содержащий 5 г NaHCO
. Еще в 1845 г. немецкий врач Бульрих обнаружил, что питьевая сода устраняет изжогу – чувство жжения в нижней части пищевода при повышенной кислотности желудочного сока. Раствор, содержащий 5 г NaHCO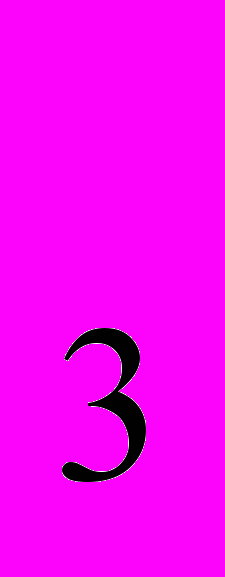 в 200 мл воды, избавит от неприятных ощущений, связанных с изжогой.
в 200 мл воды, избавит от неприятных ощущений, связанных с изжогой.Рассчитайте объем газообразного диоксида углерода, который может выделиться при реакции 5г гидрокарбоната натрия с соляной, входящей в состав желудочного сока.
Задача 2. Желудочный сок – это бесцветная жидкость, имеющая кислую реакцию благодаря присутствию соляной кислоты HCl, которая относится к числу сильных кислот, нацело диссоциирующих в водном растворе.
Рассчитайте рН желудочного сока, если массовая доля HCl в нем составляют 0,5 %. Плотность желудочного сока практически равна плотности воды.
Задача 3. При наружном применении питьевая сода нейтрализует действие кислот, попавших на кожу ( при укусах муравьев или ожогах крапивой это муравьиная кислота HCOOH).
Какая масса муравьиной кислоты может быть нейтрализована с помощью гидрокарбоната натрия, содержащегося в 10 мл его 2% - го раствора? Плотность такого раствора 1013 г/л.
Задача 4. Почему место муравьиного укуса чешется и болит? От Муравьиной кислты HCOOH, которая попадает в ранку. Это кислота – слабая, в водном растворе она диссоциирует не полностью, а частично.
Рассчитайте рН в 5% - м растворе муравьиной кислоты, если степень ее диссоциации составляет 0,01%, а плотность раствора равна 1012 г/л.
Задача 5. В результате реакции гидролиза гидрокарбоната натрия в его растворе создается слабощелочная среда.
Рассчитайте рН раствора, содержащего 10 г гидрокарбоната натрия в 200 мл воды, если степень гидролиза равна 0,01%. Считайте объем раствора равным объему воды.
Задача 6. Поваренная соль недаром служит важным компонентом пищи: это вещество в растворенном состоянии входит в состав крови и межклеточной жидкости. При сильных кровотечениях объем циркулирующей крови восполняют изотоническим раствором – 0,9%- м раствора хлорида натрия.
Рассчитайте массу катионов натрия и хлорид – ионов в 10 мл изотонического раствора. Плотность раствора равна 1005 г/л.
Вид проб
II. 2.Элементы II группы ПСХЭ Д. И. Менделеева
Общая характеристика. Магний и здоровье человека. Источники поступления магния в организм человека. Биологическая роль магния. Реакция организма на избыток магния. Применение магния в медицине. Тест на содержание магния в организме. Кальций и здоровье человека. Биологическая роль кальция. Потребность в кальции. Источники поступления кальция в организм человека. Снижение уровня кальция в организме. Приготовление пищи и кальций. Реакция организма на недостаток кальция.
Ртуть и здоровье человека. Токсические свойства ртути. Нахождение ртути в живых организмах. Помощь при острых отравлениях ртути. Цинк. Кадмий.
Задача 1. Ортофосфат кальция составляет минеральную основу костей и зубов. Другие соединения кальция участвуют в нервной и мышечной деятельности, входят в состав тканевой жидкости, ядер и стенок клеточной ткани живого организма. Суточная потребность кальция составляет от 0,8 до 2г, а источники этого элемента – молоко и кефир, творог, сыр, рыба и т. д.
Обеспечит ли суточную потребность организма в элементе кальции добавлении в пищу 1 г карбоната кальция (считая, что он усваивается полностью)?
Задача 2. Магний наряду с кальцием в виде ортофосфата образует костную ткань. Ешьте, свежую зелень, и вы обеспечите потребность своего организма в магнии, составляющую ежесуточно 0,4 г.
Сколько ортофосфата магния (в граммах) отвечает потребляемой человеком каждый день массе элемента магния?
Задача 3. Зубные пасты – это сложные системы, чаще всего содержащие карбонат кальция (мел). Природный мел нельзя использовать для изготовления. Карбонат кальция для зубных паст получают химическим осаждением из раствора гидроксида кальция: Ca(OH)
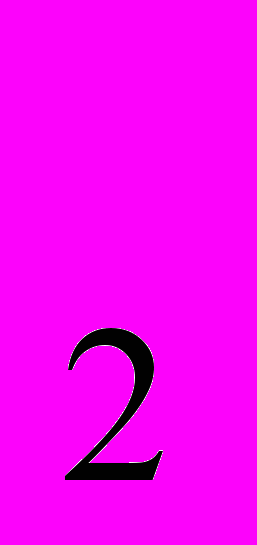 + Na
+ Na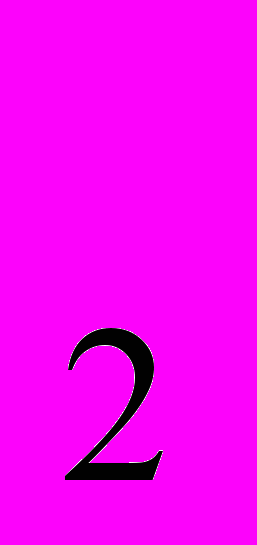 CO
CO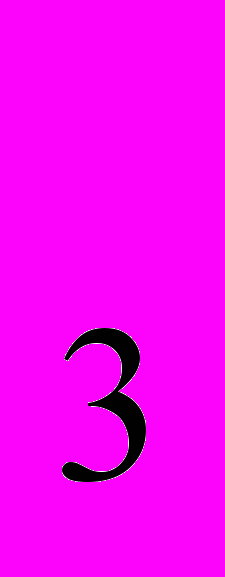
 CaCO
CaCO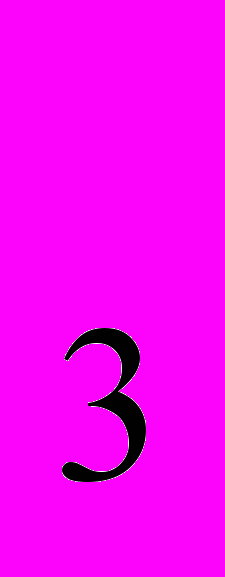
 +2NaOH.
+2NaOH.Рассчитайте массу гидроксида кальция, который требуется для получения 85 кг карбоната кальция этим способом, если выход продукта в технологическом прцессе осаждения равен 94%.
Питьевая вода содержит растворимые соли ионов Ca2+ и Mg2+ - сульфаты и карбонаты, обуславливающие ее жесткость. Повседневное употребление такой воды может привести к ряду заболеваний пищеварительного тракта. Какие из перечисленных ниже веществ могут быть применены для снижения жесткости воды:
а) карбонат калия;
б) поваренная соль;
в) фосфат натрия.
Дайте обоснованный ответ, приведя уравнения соответствующих реакций.
Вид проб
II.3. Элементы III группы ПСХЭ Д. И. Менделеева.
Бор и здоровье человека. Алюминий и здоровье человека. Биологическая роль алюминия. Источники поступления алюминия в организм человека. Реакция организма на избыток алюминия. Применение соединений алюминия в медицине.
Задача 1. Борная кислота – это белое кристаллическое вещество применяется в виде 2% -х растворов для промывания слизистых оболочек глаза и обработки пораженных инфекций участков кожи.
Рассчитайте молярную концентрацию В(ОН)
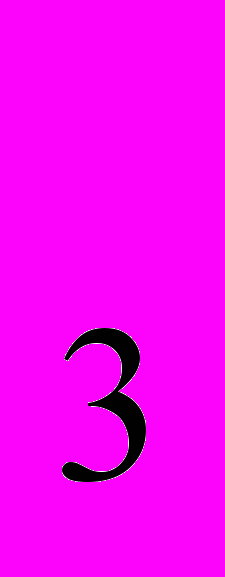 в ее 1% - м растворе . Плотность раствора равна 1002, г/л.
в ее 1% - м растворе . Плотность раствора равна 1002, г/л.Вид проб
II. 4. Элементы IV группы ПСХЭ Д. И. Менделеева.
Общая характеристика. Углерод и здоровье человека. Влияние на организм человека. Кремний и здоровье человека. Биологическая роль кремния. Источники поступления кремния в организм человека. Реакция организма на избыток и недостаток кремния.
Влияние титана, циркония и гафния на организм человека. Источники поступления.
Задача 1.Накопление углекислого газа в атмосфере становится опасным загрязнением – приводит к парниковому эффекту. Какой объем CO2 попадает в атмосферу при сжигании 100 г полиэтилена (100 шт. использованных пакетов)?
Задача 2. Растения поглощают минеральные вещества и углекислый газ и под действием ультрафиолета синтезируют глюкозу, выделяя кислород.
Задача 3. Какой объем CO2 усвоили зеленые листья сахарной свеклы для получения 100 г сахарозы, из которой можно изготовить 10 конфет (одна конфета содержит примерно 10 г сахара)?
Задача 4. Прозрачные зубные пасты на основе гелия диоксида кремния и некоторых полимеров могут содержать любые лечебные и вкусовые добавки. Для получения геля диоксида кремния SiO
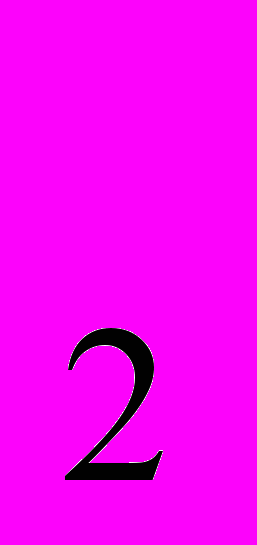 газообразный диоксид углерода пропускают через раствор, ортосиликат натрия Na
газообразный диоксид углерода пропускают через раствор, ортосиликат натрия Na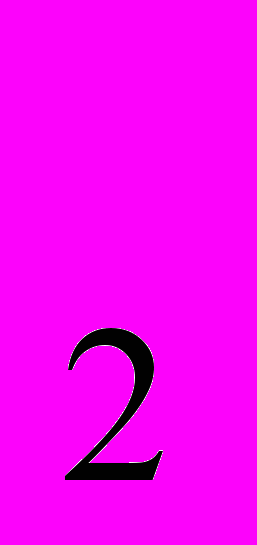 SiO
SiO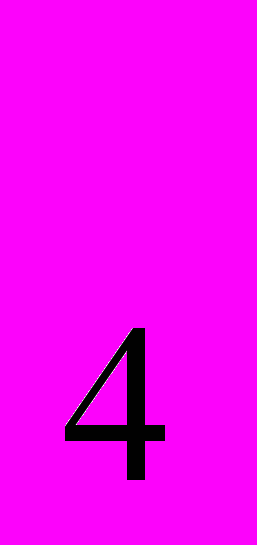 . Определите количество (в молях) выделившегося диоксида кремния, если на реакцию пошло 44, 8 л (н.у.), а потери диоксида углерода составляют 10%.
. Определите количество (в молях) выделившегося диоксида кремния, если на реакцию пошло 44, 8 л (н.у.), а потери диоксида углерода составляют 10%.Задача 5. Для ухода за кожей рук рекомендуют использовать эмульсионные кремы на основе вазелинового масла, в которых содержится до 14% пчелиного воска, 35% воды 1% тетрабората натрия Na
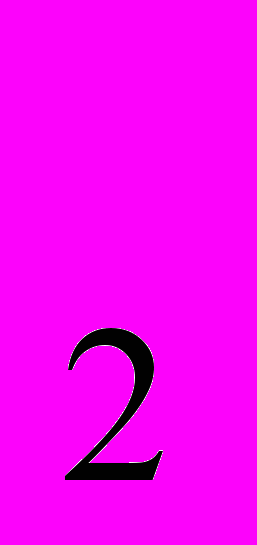 B
B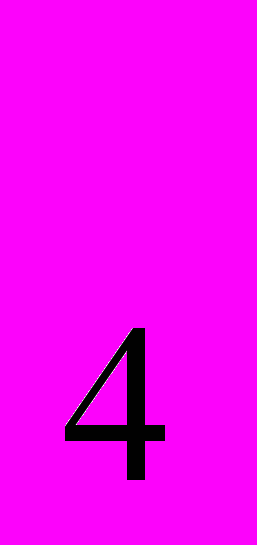 O
O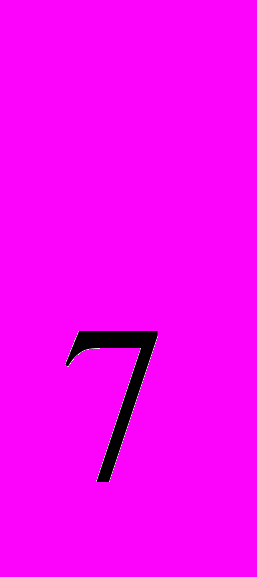 . Рассчитайте массу декагидрата тетрабората натрия Na
. Рассчитайте массу декагидрата тетрабората натрия Na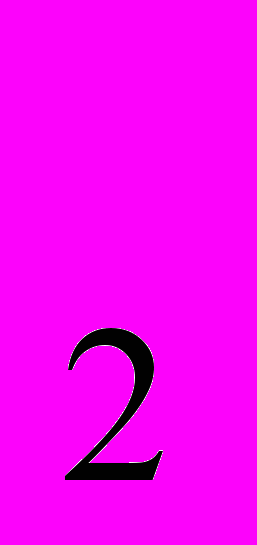 B
B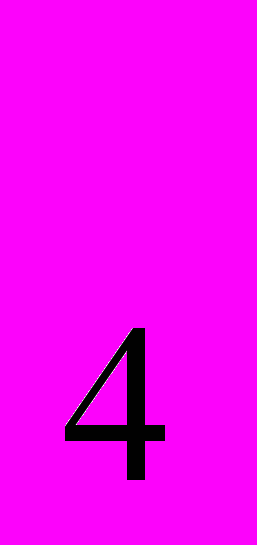 O
O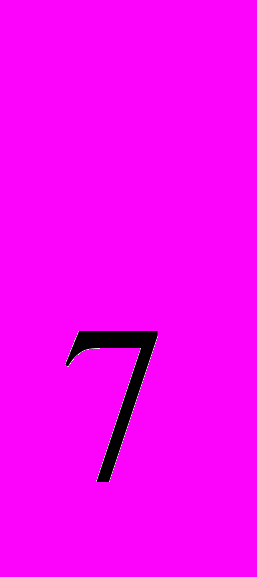 10Н
10Н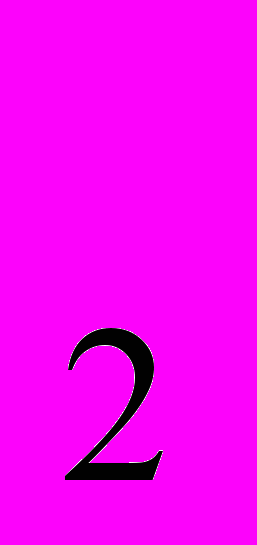 О, который требуется для приготовления 60 г такого крема.
О, который требуется для приготовления 60 г такого крема.Вид проб
II. 5. Элементы V группы ПСХЭ Д. И. Менделеева
Азот и здоровье человека. Соединения азота. Нитраты. Отравление нитратами. Фосфор и здоровье человека. Биологическая роль. Мышьяк и здоровье человека. Биологическая роль мышьяка и висмута.
Ванадий и здоровье человека.
- Азот – незаменимый биогенный элемент, поскольку входит в состав белков и нуклеиновых кислот. Атмосфера – неисчерпаемый резервуар азота, однако, основная часть живых организмов не может непосредственно использовать этот азот: он должен быть предварительно связан в виде химических соединений. Существуют азотфиксирующие бактерии, способные фиксировать азот воздуха и превращать его в доступную для растений форму. С помощью таких бактерий при хорошем урожае клевер может накапливать за сезон 150-160 кг/га азота. Какой объем воздуха в м3 содержит такую массу азота? Какую массу 10 % раствора аммиачной воды (используемой в качестве удобрений) может заменить 1 га клевера, накопивший за сезон 100 кг/га азота? (Ответ: 120 м3, 2100 кг)
- Хороший эффективный разрыхлитель для выпечки мучных изделий - гидрокарбонат аммония NH
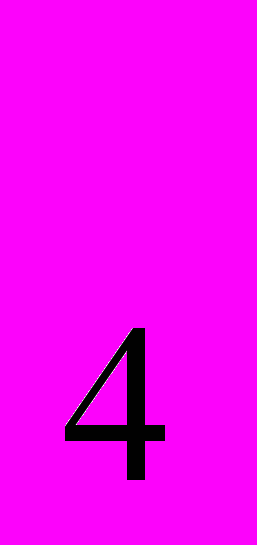 HCO
HCO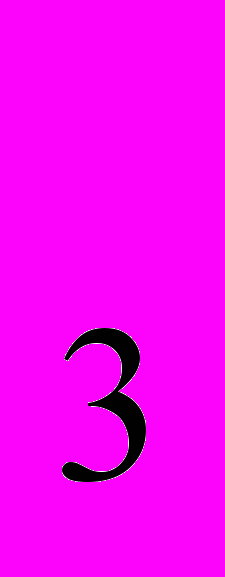 . При его разложении все продукты реакции получаются в газообразном состоянии:
. При его разложении все продукты реакции получаются в газообразном состоянии:
NH
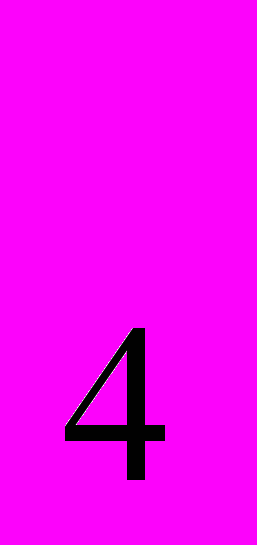 HCO
HCO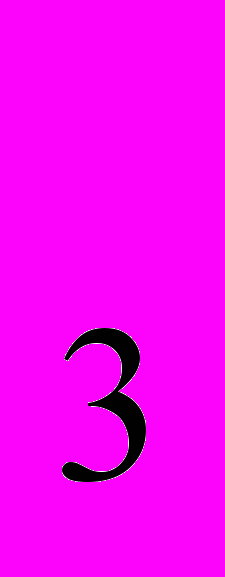
 NH
NH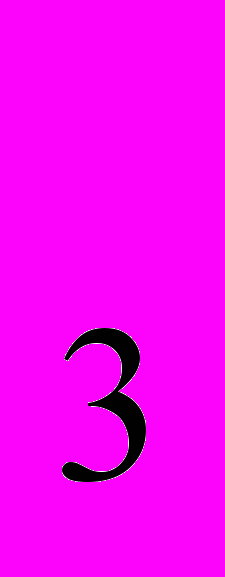
 + Н
+ Н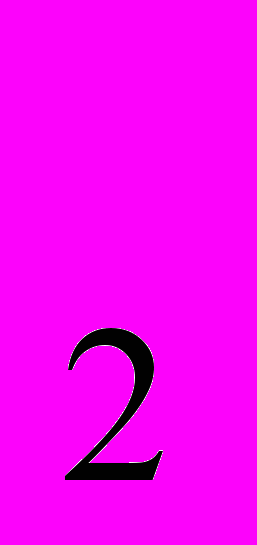 О
О  + CO2
+ CO2
Рассчитайте объем при (н. у.) газообразных продуктов разложения 0.5 г гидрокарбоната натрия.
Вид проб
II. 6. Элементы VI группы ПСХЭ Д. И. Менделеева.
Кислород и здоровье человека. Биологическая роль кислорода. Реакция организма на избыток и недостаток кислорода. Применение кислорода в медицине. Сера и здоровье. Биологическая роль серы.
Хром, молибден и здоровье человека. Биологическая роль хрома и молибдена. Реакция организма на избыток и недостаток хрома, молибдена.
Задача 1. В стратосфере на высоте 20-30 км находится слой озона O3, защищающий Землю от мощного ультрафиолетового излучения Солнца. Если бы не "озоновый экран" атмосферы, то фотоны большой энергии достигли бы поверхности Земли и уничтожили на ней все живое. Подсчитано, что в среднем на каждого жителя в воздушном пространстве над городом приходится по 150 моль озона. Сколько молекул озона и какая его масса приходится в среднем на одного жителя?
Задача 2.Одинаковое ли (и какое именно) число молекул содержится в 1г воды и в 1г кислорода? Какова роль этих веществ в биосфере Земли?
Вид проб
II.7. Элементы VII группы ПСХЭ Д. И. Менделеева.
Фтор и здоровье человека. Биологическая роль фтора. Бром и здоровье человека. Биологическая роль брома и его соединений. Источники поступления брома в организм человека. Применение брома и его соединений. Йод и здоровье человека. Биологическая роль йода. Источники поступления йода в организм. Человека. Реакция организма на недостаток йода. Хлор и здоровье человека. Применение хлора. Соляная кислота и здоровье человека.
Железо и здоровье человека. Источники поступления железа в организм человека. Круговорот железа в организме. Реакция организма на недостаток и избыток железа. Тест « Порядок ли у вас с железом?»
Задача 1.Фторсодержащие добавки, которые вводят в профилактических целях в зубные пасты, замедляют образование и распространение бактериального налета на зубах – причины грозного кариеса.
Определите массовую долю фтора в зубной пасте, содержащей 0.5 % фторида олова SnF
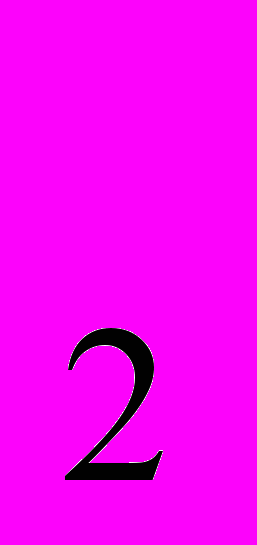 0.25 % NaF.
0.25 % NaF.Задача 2. Зубная паста "Crest" производства США содержит, как указано на упаковке , 0.454 % фторида олова (II); зубная паста «FM extra DENT» производства Болгарии содержит 0, 8% монофторфосфата натрия NaF NaPO
 . Какая из этих паст более эффективна для профилактики кариеса?
. Какая из этих паст более эффективна для профилактики кариеса?4.Литература для учителя:
- Добрынин Н. А. Биологическая роль некоторых химических элементов. Химия в школе, 1991, № 2, с. 6-13.
- Терлецкий Е, Д. С железом в крови. Химия и жизнь, 1985, №4, с. 19-22.
- Макаров К. А. Химия и здоровье . М. : Просвещение, 1985г, с.144
- Бородин С. Минерология человека, Наука и жизнь. 1995. №5. с.94- 96.
Литература для учащихся:
- Степин Б. Д. Книга по химии для домашнего чтения М.; Химия, 1994, 399с.
- Скурихин И. М. Все о пище с точки зрения химика. М.; Высш. Шк., 1991, 288с.
- Здоровье без лекарств. Энциклопедияческий справочник. Минск: 1994; 380с.
