Особенности рака и гиперпластических процессов эндометрия в сочетании с миомой матки 14. 00. 14 онкология
| Вид материала | Автореферат |
- Значение аблации эндометрия в терапии гиперпластических процессов эндометрия пациенток, 411.8kb.
- Последняя надежда или чудо своими руками, 3060.3kb.
- Диагностика больных с миомой матки и аденомиозом, 178.92kb.
- Home, 120.82kb.
- Совершенствование методов диагностики и лечения рака тела матки 14. 00. 14 онкология, 520.93kb.
- Only for you!!! Убедительная просьба не использовать документ полностью, без изменений., 493.4kb.
- Стратегия и тактика лучевой терапии в многокомпонентном лечении местно-распространенного, 1026.52kb.
- На правах рукописи, 387.05kb.
- Комплексное эндохирургическое лечение больных с субмукозной миомой матки 14. 00., 300.79kb.
- Эпидемиология рака молочной железы в иркутской области 14. 00. 14 онкология, 371.42kb.
На правах рукописи
МУНТЯН АЛИСА БОРИСОВНА
Особенности рака и гиперпластических процессов эндометрия в сочетании с миомой матки
14. 00. 14 – онкология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Томск 2007
Работа выполнена в ГУ НИИ онкологии Томского научного центра Сибирского отделения РАМН
Научный руководитель:
доктор медицинских наук, профессор Коломиец Л.А.
Официальные оппоненты:
доктор медицинских наук, профессор Сидоров С.В.
доктор медицинских наук, профессор Кох Л.И.
Ведущая организация – Российский онкологический научный центр Российской Академии медицинских наук им. Н.Н. Блохина, г. Москва
Защита диссертации состоится _________2007 г. в ___ часов на заседании диссертационного совета Д.001.32.01 при Научно-исследовательском институте онкологии Томского научного центра Сибирского отделения РАМН, по адресу: 634001, г. Томск, переулок Кооперативный, 5
С диссертацией можно ознакомиться в библиотеке НИИ онкологии ТНЦ СО РАМН
Автореферат разослан «___» _____________2007г.
Учёный секретарь диссертационного совета
доктор медицинских наук, профессор Фролова И.Г.
Актуальность. Рак тела матки занимает четвертое место в структуре заболеваемости злокачественными новообразованиями среди женского населения России, составляя 6,4-6,5% (Чиссов В.И., 1999) и первое место среди опухолей женских половых органов. За последнее десятилетие заболеваемость раком эндометрия среди онкологической патологии женской репродуктивной системы возросла с 18,6% до 27,6% (Аршафян Л.А., Новикова Е.Г., 2001г.).
Согласно данным отечественных авторов, частота сочетания рака эндометрия и миомы матки по данным операционного материала колеблется от 16,2% до 64% (Бохман Я.В., 1989г., , Мезинова Н.Н. с соавт., 1985г.,43,51,136, Линёва О.И., 2002, Сидорова И.С., 2002г. , Koshiyama M. et al., 2001). Исследование эндометрия у больных, оперированных по поводу миомы матки показало, что железистая гиперплазия эндометрия обнаруживается в 4-62,5%, полипы эндометрия – в 10-15,6%, атипическая гиперплазия – у 10-12,7%, аденомиоз – у 7,55%, рак эндометрия в 0,7-7 % случаев (Бохман Я.В., 1989г., Мезинова Н.Н. с соавт., 1985г., Сидорова И.С., 2002г., Вишневская Е.Е., 2002г, Берштейн Л.М., 2004г.).
В 75% случаев рак эндометрия развивается в постменопаузе, однако в последнее время прослеживается тенденция увеличения числа заболевших раком эндометрия женщин в перименопаузе, из них у 5% женщин в возрасте до 40 лет (Урманчеева А.Ф. с соавт, 2001г.). Отмечается возрастание выявления рака эндометрия от 1,1% у больных миомой матки, оперированных в репродуктивном возрасте, до 13,4-13,9% оперированных в постменопаузе (Сидорова И.С., 2002г.). Поэтому, по мнению ряда учёных, не регрессирующая в постменопаузе миома матки может выступать в роли «маркёра онкогинекологической патологии» (Сидорова И.С., 2002г., Вишневская Е.Е., 2002, Bohman Ya.V., 1988, Studzinski Z. et al., 2000).
Некоторые исследователи утверждают, что чаще всего рак эндометрия развивается у больных с миомой матки с мало- и бессимптомным её течением (Савельева Г.М. с соавт., 1981,Бохиан Я.В., 1985г., Мезинова Н.Н., 1985г.), другие - что риск развития рака эндометрия не зависит от размеров опухоли (Сидорова И.С., 2002г.). По данным операционного материала в 8,2% случаев бессимптомного течения миомы матки обнаруживаются атипическая гиперплазия и рак эндометрия (Мезинова Н.Н., 1985г.).
Большинство проведенных исследований показали, что для женщин, предрасположенных к развитию предраковых процессов и рака эндометрия, характерно наличие эндокринно-обменных нарушений: бесплодия, ановуляторных маточных кровотечений, ожирения, гиперлипидемии, гиперинсулинемии, сахарного диабета (Серов В.Н., 1981г., Бохман Я.В., 1989г., Мезинова Н.Н., 1985г., Бутрова С.А., 2000г., Бахидзе Е.В., Чепик О.Ф., 2002г., Артымук Н.В., Магарилл Ю.А., 2004г., Kistner R.W., 1976, Studzinski Z., Branika D., 1999). Синдром эндокринно-обменных нарушений (метаболический синдром) является одним из проявлений гормонального дисбаланса при I патогенетическом варианте рака эндометрия, а также фоном для развития пролиферативных процессов в эндометрии (Вихляева Е.М., 2000г.).
Несмотря на то, что миома матки традиционно рассматривается как доброкачественная опухоль женской половой сферы, она, так же как и пролиферативные процессы в эндометрии, сопровождается рядом эндокринно-метаболических сдвигов, а пик её заболеваемости приходится на перименопаузальный возраст (Бохман Я.В., 1985,1989гг., Мезинова Н.Н., 1985г., Савитский Г.А., 1999, Вихляева Е.М., 2000г., Гаврилов А.С., Мерекина Л.И., 2002г.).
По данным многих авторов, наличие у больных с гиперпластическими процессами эндометрия миомы матки сопровождается увеличением частоты дисфункциональных маточных кровотечений, функциональных кист и поликистоза яичников (Тихомиров А.Л., 1998, Хмельницкий О.К. 1999г., Гаврилов А.С., Мерекина Л.И., 2002г., Вихляева Е.М., Вишневская Е.Е., 2002г., Сидорова И.С., 2002г., 2000г., Берштейн Л.М., 2004г., Jongen V.H., Sluijmer A.V., 2002,), а сочетание таких факторов как миома матки и поздняя менопауза увеличивает риск развития рака эндометрия в 2 раза (Мезинова Н.Н., 1985г., Сидорова И.С., 2002г.).
Несмотря на патогенетическую неоднородность гиперпластических процессов и рака эндометрия, доказанную роль эстрогенов не только в их развитии, но и миомы матки, высокий удельный вес сочетанной патологии эндо- и миометрия, практически отсутствуют данные об особенностях клиники, системной и локальной гормонемии, синтеза эстрогенов тканями-мишенями, рецепторного статуса при сочетании гиперпластических процессов эндометрия и миомы матки.
Изучение особенностей сочетанной патологии эндо- и миометрия представляет интерес не только с точки зрения выявления возможных общих патогенетических моментов, но и в плане выявления объективных критериев онкологического риска у этих больных.
Целью исследования явилось изучение клинических, биохимических и гормональных особенностей у больных с гиперпластическими процессами и раком эндометрия в сочетании с миомой матки.
Задачи исследования:
- Выявить клинические особенности у больных раком и гиперпластическими процессами эндометрия в сочетании с миомой матки;
- Изучить гормональный профиль и рецепторный статус у больных гиперпластическими процессами и раком эндометрия в сочетании с миомой матки;
- Оценить уровень ароматазной активности в эндометрии у больных гиперпластическими процессами и раком эндометрия в сочетании с миомой матки;
- Разработать математическую модель прогноза онкологического риска у больных с гиперпластическими процессами эндометрия и миомой матки.
Научная новизна. Впервые показано, что при раке эндометрия миома матки чаще выявлялась в постменопаузе, чем в репродуктивном и перименопаузальном периодах. Менометроррагия встречалась чаще у больных раком эндометрия с миомой матки пери- и постменопаузального периодов, а бессимптомное течение рака эндометрия - у больных репродуктивного периода. У больных с гиперпластическими процессами эндометрия с миомой матки бессимптомное течение чаще наблюдалось в постменопаузе.
Впервые показано, что наличие миомы матки при раке эндометрия сопровождалось увеличением частоты встречаемости ожирения, в том числе III-IV степеней, заболеваний вен нижних конечностей, а при железистой гиперплазии – артериальной гипертензии.
Выявлено, что наличие миомы матки при раке эндометрия сопровождалось повышением уровня эстрона и снижением уровня эстрадиола и индекса свободных эстрогенов сыворотки крови в системном кровотоке, причём уровень эстрона в локальном кровотоке был выше, а уровень глобулина, связывающего половые стероиды – ниже, по сравнению с системным кровотоком.
Впервые показано, что уровень ароматазной активности в опухолевой ткани зависел от наличия миомы матки у больных раком эндометрия репродуктивного периода, причём, он был выше при выявлении миомы матки в возрастной период от 30 до 40 лет, и ниже - при выявлении миомы в возрасте старше 40 лет. У больных раком эндометрия с миомой матки, находившихся в постменопаузе, уровень активности фермента был взаимосвязан с уровнем глобулина, связывающего половые стероиды, сыворотки крови.
Впервые показано, что высокая ароматазная активность в ткани миоматозных узлов не зависела от морфологического состояния эндометрия.
Показано, что у больных раком эндометрия рецепторный фенотип ER+PR- встречался статистически значимо чаще в группе без миомы (43%), чем в группе с миомой матки (19%, p=0,05). Выявлена взаимосвязь уровня рецепторов эстрогенов в нормальном и гиперплазированном эндометрии при миоме матки с размерами матки. Показано, что активность ароматазы при раке и атипической гиперплазии эндометрия коррелировала с уровнем рецепторов эстрогенов, а при железистой гиперплазии – с уровнем рецепторов прогестерона.
Впервые разработана математическая модель прогноза онкологического риска у больных с гиперпластическими процессами и миомой матки с учётом наиболее значимых показателей: возраст, индекс массы тела, ширина матки, объём матки, уровень глобулина, связывающего половые стероиды сыворотки крови. Специфичность модели - 87 %, чувствительность – 85 %.
Теоретическая и практическая значимость. Полученные данные позволяют расширить представление о роли показателей системного и локального гормонального гомеостаза, рецепторного статуса и эндокринно-обменных нарушений в развитии гиперпластических процессов и рака эндометрия в сочетании с миомой матки. Выявленные закономерности позволили обосновать новые подходы к использованию объективных критериев формирования групп онкологического риска и разработать математическую модель прогноза развития рака эндометрия с чувствительностью – 87 %, специфичностью – 85 %.
Результаты исследования позволили выявить особенности течения рака эндометрия с миомой матки в различные возрастные периоды. При выявлении миомы матки в период постменопаузы, наличии эндокринно-обменных нарушений, заболеваний вен нижних конечностей, гепатобилиарной системы необходимо проведение морфологического исследования эндометрия с целью своевременного выявления рака этой локализации. Результаты исследования внедрены в работу ГУ НИИ акушерства, гинекологии и перинатологии ТНЦ СО РАМН, гинекологического отделения МЛПМУ родильного дома №4, отделения онкогинекологии ГУ НИИ онкологии ТНЦ СО РАМН.
Основные положения, выносимые на защиту:
- Клиническими особенностями сочетания рака эндометрия и миомы матки являются высокая частота менометроррагий, проявлений эндокринно-обменного синдрома, большая выраженность изменений в липидном спектре сыворотки крови, высокий уровень эстрона и низкий – эстрадиола и глобулина, связывающего половые стероиды сыворотки крови, по сравнению с больными без миомы матки.
- Сочетание рака эндометрия и миомы матки в репродуктивном периоде, сопровождается усилением синтеза эстрогенов в опухоли за счёт фермента ароматазы, особенно при выявлении миомы матки в возрасте от 30 до 40 лет. У больных раком эндометрия постменопаузального периода наличие миомы матки не сопровождается достоверным повышением активности ароматазы в опухоли, однако, её уровень взаимосвязан с уровнем глобулина, связывающего половые стероиды, в сыворотке крови и уровнем рецепторов эстрогенов.
- Использование прогностически наиболее значимых клинико-анамнестических показателей, таких как возраст, значение индекса свободных эстрогенов, возраст выявления миомы матки, значение индекса массы тела, степень ожирения, наличие патологии гепатобилиарной системы позволяет определить риск развития рака эндометрия у больных с гиперпластическими процессами эндометрия с миомой матки.
Апробация работы. Основные результаты работы доложены и обсуждены на конференциях молодых учёных (г. Томск, 2004, 2006 гг.); Межрегиональная научно-практическая конференция « Актуальные вопросы акушерства и гинекологии, г. Ленинск-Кузнецкий, 21-22 апреля 2005г. «Современная схема метаболизма эстрогенов у больных с гиперпластическими процессами на фоне миомы матки», ESGO 14th biennial meeting: Istanbul, Turkey, September 25-29, 2005 - Стендовые доклады: «The activity of enzymes of estrogen metabolic pathway: relation with stage, grade and hystological subtype» и « Potential use of aromatase inhibitors in the treatment of endometrial cancer».
Публикации. Основные результаты исследования опубликованы в 17 печатных работах. Получено положительное решение о выдаче патента на изобретение «Способ комплексного лечения резектабельных форм рака эндометрия» № 2005130582/14 (034277) от 17.10.2006 г.
Объём и структура диссертации. Диссертация изложена на 188 страницах машинописного текста и состоит из введения, четырёх глав, заключения, выводов практических рекомендаций и списка использованной литературы. Работа иллюстрирована 29 таблицами и 7 рисунками. Библиографический указатель содержит 98 источников отечественной и 111 зарубежной литературы.
Материал и методы исследования
В работу включены результаты исследования 252 женщин, обратившихся на консультативный прием и находившихся на стационарном лечении в онкогинекологическом отделении ГУ НИИ онкологии ТНЦ СО РАМН, с 2002 по 2006 год.
В соответствии с Международной классификацией морфологического состояния эндометрия, основанной на структурных и цитологических изменениях эндометрия (ВОЗ, 1994) и международной классификацией рака эндометрия FIGO (ВОЗ, 1992) и TNM (ВОЗ, 2002) было сформировано IV клинических группы: I группа – больные раком эндометрия (79 человек); II группа – больные с простой и комплексной гиперплазией эндометрия (82 человека); III группа – 18 больных с простой и комплексной атипической гиперплазией; IV группа – 19 больных с атрофией эндометрия. Группу контроля составили 54 пациентки без патологических изменений эндометрия.
Все больные основных групп и группы контроля в зависимости от наличия миомы матки разделены на две подгруппы: с миомой матки и без миомы матки. Больные, имеющие миому матки, обследованы в соответствии с отраслевым стандартом «Протоколы ведения больных. Общие требования» приказа Минздрава России №303 от 03.08.1999г. с оценкой следующих параметров: размеры матки, локализация узлов относительно толщины маточной стенки (подслизистая, интрамуральная, субсерозная, неуточнённая), размеры миоматозных узлов, наличие осложнений (быстрый рост опухоли, рождающийся подслизистый узел, острое нарушение питания или инфицирование узлов, железодефицитная анемия, бесплодие). Кроме того, учитывался возраст выявления миомы матки.
Обследование больных проводилось по разработанной «Карте комплексного обследования», включающей оценку возраста, общесоматического и гинекологического статуса, анализ сопутствующей гинекологической патологии и экстрагенитальных заболеваний, при раке эндометрия - стадии заболевания, гистотипа, степени дифференцировки и глубины инвазии опухоли в миометрий.
У всех больных проводили эхографию органов малого таза на аппарате сложного сканирования «Aloka SSD 500» с трансабдоминальным (3,5 МГц) и эндовагинальным (5 МГц) конвексными датчиками (Япония). Оценивали следующие биометрические показатели: длина, передне-задний размер, ширина матки, структура миометрия, М-эхо (толщина, структура), структура яичников, состояние фолликулярного аппарата.
Объем матки рассчитывали по стандартной формуле (Ландеховский Ю.Д., 1988):
 [(длина(мм)+поперечник(мм)+ширина(мм)]3
[(длина(мм)+поперечник(мм)+ширина(мм)]3Vматки(см3)= _________________________________ 1000
60,79
где: V матки – объём матки,
60,79 – постоянный коэффициент,
1000 – коэффициент пересчёта из мм3 в см3.
Для количественной оценки степени ожирения рассчитывали индекс массы тела, исходя из росто-весовых показателей по формуле (G.Brey, 1978):
Масса тела (кг)
ИМТ (индекс массы тела) = ______________
Рост (м ²)
Согласно рекомендациям ВОЗ, показатель в диапазоне 20-24,9 кг/м² расценивался как соответствие веса норме; 25-27 кг/м² - избыточная масса тела, 27-30,9 кг/м² - ожирение I-II степени, свыше 31 кг/м² - ожирение III-IV степени.
Соотношение больных в зависимости от наличия миомы матки в изучаемых группах представлено в табл. 1.
Наиболее часто миома матки встречалась у больных с железистой гиперплазией эндометрия – у 68 из 82 женщин (83%). У больных раком эндометрия миома матки выявлена у 50 из 79 женщин (63%) (р=0,020 при сравнении с группой больных с железистой гиперплазией эндометрия).
Таблица 1.
Соотношение больных в изучаемых подгруппах с миомой и без миомы матки.
-
Группы
Больные без миомы маки
Больные с миомой матки
абс.
%
абс.
%
РЭ
29
37
50
63
ЖГЭ
14
17
68
83
АГ
6
33
12
67
АЭ
5
26
14
74
Контроль
13
24
41
76
Примечание: РЭ – рак эндометрия; ЖГЭ – железистая гиперплазия эндометрия; АГ– атипическая гиперплазия эндометрия; АЭ – атрофия эндометрия.
Анализ возрастных особенностей в изучаемых группах представлен в табл.2.
Таблица 2.
Средний возраст женщин в исследуемых группах (лет).
| Группы | n | Возраст (М±m) | Р | |
| РЭ | без ММ | 29 | 55,0±10,0 | 0,642 |
| с ММ | 50 | 56,5±7,9 | ||
| ЖГЭ | без ММ | 14 | 50,0±7,2 | 0,083 |
| с ММ | 68 | 47,0±5,6 | ||
| АГ | без ММ | 6 | 47,0±10,0 | 0,083 |
| с ММ | 12 | 49,0±7 | ||
| АЭ | без ММ | 5 | 61,0±9,7 | 1,000 |
| с ММ | 14 | 52,0±8,2 | ||
| Контроль | без ММ | 13 | 39,0±3,5 | 0,553 |
| с ММ | 41 | 46,0±4,8 | ||
Примечание: РЭ – рак эндометрия; ЖГЭ – железистая гиперплазия эндометрия; АГ– атипическая гиперплазия эндометрия; АЭ – атрофия эндометрия, ММ – миома матки. Р – достигнутый уровень значимости различий между подгруппами без миомы и с миомой матки с использованием критерия Манна-Уитни.
Как видно из представленных в таблице данных, средневозрастные показатели в группе контроля и в группах больных с железистой и атипической гиперплазией эндометрия меньше средневозрастного показателя в группе больных раком эндометрия (р<0,001, р<0,001 и р=0,002 соответственно).
Забор материала для морфологического исследования проводился при выполнении гистероскопии с раздельным диагностическим выскабливанием полости матки и цервикального канала или при оперативном вмешательстве. При морфологическом исследовании злокачественных опухолей эндометрия оценивали гистологический тип и степень дифференцировки опухоли, уточняли глубину инвазии опухоли в миометрий и стадию заболевания, а так же состояние маточных труб и яичников. Удельный вес различных морфологических вариантов рака эндометрия представлен на рис. 1.
Как видно, наиболее часто встречающимся гистологическим вариантом рака эндометрия был умереннодифференцированный, удельный вес которого в подгруппе без миомы матки составил 45%, а в подгруппе с миомой - 34%. Частота встречаемости высокодифференцированной аденокарциномы у больных с миомой матки была примерно в 1,5 раза выше, чем в подгруппе без миомы – 32% и 21% соответственно (р>0,05). Удельный вес низкодифференцированных аденокарциномы эндометрия в обеих группах был примерно одинаков.
Удельный вес редких форм рака эндометрия (железисто-плоскоклеточный, мукоэпидермоидный рак) не превышал 3% в подгруппе без миомы матки и 6% - в подгруппе с миомой матки.
-
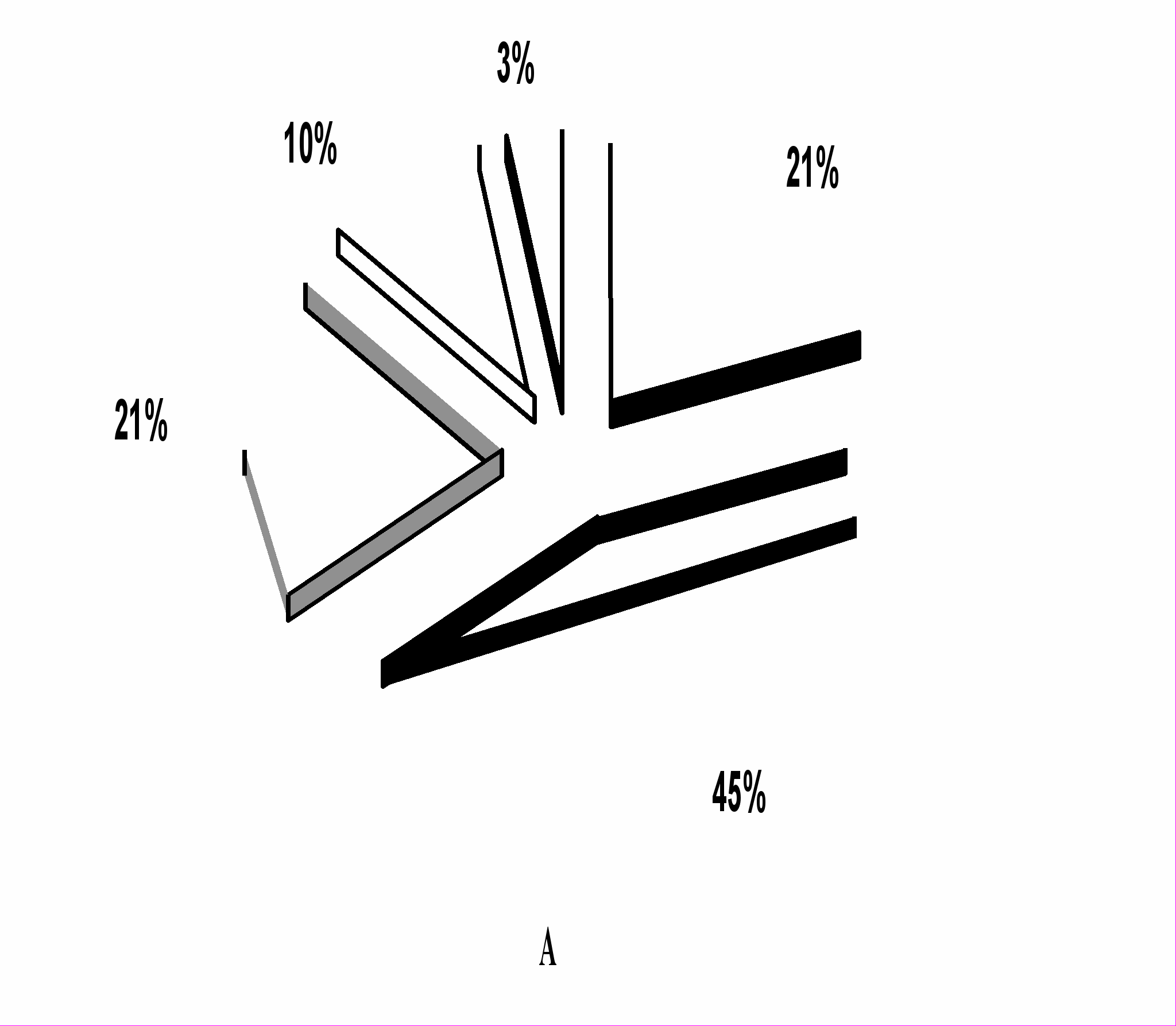

Рис. 1. Особенности морфологических вариантов рака эндометрия у больных без миомы (А) и с миомой матки (В).
П римечание:
римечание:
высокодифференцированный рак эндометрия,
 умереннодифференцированный рак эндометрия,
умереннодифференцированный рак эндометрия,
 низкодифференцированный рак эндометрия,
низкодифференцированный рак эндометрия,
 железисто-плоскоклеточный рак,
железисто-плоскоклеточный рак,
 редкие формы рака эндометрия.
редкие формы рака эндометрия.
Уровни общего холестерина, триглицеридов и липопротеинов высокой плотности определяли энзимоколориметрическим методом с помощью наборов «Biosub» для холестерина и триглицеридов, и «Fluitest» для липопротеинов очень низкой плотности (С.-Петербург). Холестерин и триглицериды определяли при помощи колориметрического теста.
Кровь для оценки концентрации половых стероидов в локальном маточном кровотоке забирали во время оперативного вмешательства в области восходящей ветви маточной артерии после мобилизации связочного аппарата и сосудистых пучков матки. В сыворотке крови, взятой из локтевой вены и локального маточного кровотока определяли уровень половых стероидных гормонов (эстрона, эстрадиола, прогестерона) и глобулина, связывающего половые стероиды (SSBG) с использованием коммерческих наборов для радиоиммунного и радиометрического анализа фирм “Immunotech” (Чехия) и “DSL” (США).
Индекс свободных эстрогенов рассчитывался по формуле [Сметник,1998]:
[эстрадиол] (нмоль/л)
ИСЭ= ____________________ х 100
[SSBG] (нмоль/л)
Активность ароматазы оценивалась по образованию тяжелой воды из меченного тритием в 1β-положении андростендиона (Берштейн Л.М., 1995, Ларионов А.А., 1997). Активность ароматазы выше 7 фмоль андростендиона/мг белка в час расценивалась как высокая.
Уровень рецепторов эстрогенов и прогестерона определяли традиционным радиолигандным методом.
Полученные данные подвергались статистической обработке при помощи программы STATIATICA 6,0 for Windows. Достоверность различий количественных показателей проверяли при помощи U-критерия Уилкоксона-Манна-Уитни. Качественные признаки сравнивались с помощью точного теста Фишера. Для определения существования функциональных связей между параметрами вычисляли коэффициент корреляции R Спирмана. Построение прогностической модели риска развития рака эндометрия у больных с гиперпластическими процессами в эндометрии с миомой матки проводилось при помощи программы SPSS 12.0 методом мультиноминальной логистической регрессии на основании выбранной оптимальной совокупности признаков.
