Отчет о научно-исследовательской работе
| Вид материала | Отчет |
- Реферат отчет о научно-исследовательской работе состоит, 61.67kb.
- Отчёт о научно-исследовательской работе за 2011 год, 1208.93kb.
- Отчёт о научно-исследовательской работе за 2009 год, 851.3kb.
- Отчёт онаучно-исследовательской работе гу нии но ур за 2010 год, 997.69kb.
- Отчет о научно-исследовательской работе профессорско-преподавательского состава, 617.56kb.
- Отчет о научно-исследовательской работе; пояснительная записка к опытно-конструкторской, 14.47kb.
- Отчет о научно-исследовательской работе (итоговый), 2484.06kb.
- Отчет о научно-исследовательской работе, 2473.27kb.
- Отчет о научно-исследовательской работе, 392.92kb.
- Задачи секции: широкое привлечение учеников к участию в научно исследовательской работе;, 67.94kb.
Реферат
Отчет 126 с., 7 ч., 45 рис., 44 табл., 2 приложения.
Ключевые слова: биохимические коллоидные системы, ферментные коллоидные системы, мембранные коллоидные системы, полимеры, иммобилизованные ОМС, иммобилизованные ферменты, супрамолекулярные ферментные комплексы, коллоидно-химические свойства, белки, полиэлектролиты, физико-механические свойства, динамическое поверхностное натяжение, модельные системы, сыворотка крови, спектральные методы.
Объекты исследования и разработки. Экспериментальное оборудование для изучения ФКС. Результаты по динамическому поверхностному натяжению и по каталитическим свойствам липаз в присутствии полиэлектролитов. Модели на основе полученных корреляций между изученными параметрами. Состав и свойства биологических жидкостей коров под воздействием внешних факторов. Изменения элементного состава поверхностных слоев волоса и кожного покрова у ценных видов пушных зверей * песцов, лисиц и норок) для применения в зоотехнии. Использование результатов НИР в учебном процессе.
Цели работы по четвертому этапу
- Инжиниринговое обеспечение экспериментального оборудования для изучения ФКС.
- Анализ результатов по динамическому поверхностному натяжению и по каталитическим свойствам липаз в присутствии полиэлектролитов.
- Построение моделей на основе полученных корреляций между изученными параметрами.
- Изучение состава и свойств биологических жидкостей коров под воздействием внешних факторов.
- Сравнительное исследование изменений элементного состава поверхностных слоев волоса и кожного покрова у ценных видов пушных зверей для применения в зоотехнии.
- Анализ и обобщение полученных на 4 этапе результатов НИР
- Анализ апробации результатов по мембранным коллоидным системам в части МКС для определения катионов тяжелых металлов спектральными методами в учебном процессе.
Метод и методология проведения работы включали: Инжиниринговое обеспечение экспериментального оборудования для изучения ФКС, включающее приборы для измерения динамического поверхностного натяжения биологических жидкостей, измерения активности ферментов, изучения гидролиза триглицеридов и получения липосом; анализ результатов по динамическому поверхностному натяжению и по каталитическим свойствам липаз в присутствии полиэлектролитов; построение моделей на основе полученных корреляций между изученными параметрами; изучение состава и свойств биологических жидкостей коров под воздействием внешних факторов методами межфазной тензиометрии и биохимического анализа; исследование изменений элементного состава поверхностных слоев волоса и кожного покрова у ценных видов пушных зверей для применения в зоотехнии; анализ и обобщение полученных на 4 этапе результатов НИР; разработка методик, создание образцов, методических рекомендаций и указаний для внедрения в учебный процесс ФГОУ ВПО МГАВМиБ.
В работе использованы следующие физико-химические методы исследования:
измерение ДПН методом максимального давления в пузырьке; биохимический анализ; корреляционный анализ; измерение спектров поглощения; измерение спектров флуоресценции, проведение элементного анализа волосяного и кожного покрова ценных пушных зверей и биохимических показателей крови.
Результаты работы
Показано, что изучение ФКС обеспечено экспериментальным оборудованием. Установлено, что величина изменения динамического поверхностного натяжения σ4 для систем панкреатической липазы с полимерами с увеличением относительного содержания фермента от 1:100 до 100:1 уменьшается в ряду ПАМА≥ПЛ>ПСС≥ПГ>БСА. Выявлено, что концентрация соли оказывает влияние на ПН смесей при коротких временах существования поверхности. При разных соотношениях компонентов в смеси увеличение концентрации соли приводит к повышению ДПН при коротких и средних временах, снижению ДПН при больших временах и равновесному значению ДПН. Наибольшие различия при разных концентрациях отмечаются при коротких временах, равновесные значения отличаются незначительно. Установлено, что динамика белков сыворотки крови коров закономерно отражает физиологические процессы, происходящие в их организме в период полового и физиологического созревания и в период функциональной зрелости. Выявлены межвидовые и межвозрастные отличия в минеральном составе (по 25 элементам) кожного и волосяного покрова у пушных зверей, показаны корреляционные связи между этими параметрами, позволяющие предсказывать дефицит необходимых элементов. Результаты по мембранным коллоидным системам для определения катионов тяжелых металлов спектральными методами внедрены в учебный процесс.
7. Проанализированы и обобщены полученные на четвертом этапе результаты НИР.
Рекомендации по внедрению результатов НИР
Разработка методик и создание биохимических коллоидных систем с использованием современных методических и инструментальных достижений позволит решить ряд актуальных фундаментальных проблем в области коллоидной химии и поверхностных явлений, а также прикладных задач биомедицины и экологии, нано- и биотехнологии, ветеринарии и зоотехнии. Биохимические коллоидные системы на основе мембран и тонких пленок позволят создать нанокомпозитные материалы для хемосенсорных устройств биологического контроля катионов биогенных металлов и малых органических молекул в воде и биологических жидкостях.
Все вышеизложенное является неотъемлемой частью научно-технического прогресса в развитии животноводства на современном этапе и будет реализовано в данной НИР на базе достижений коллоидной химии.
Выполнение НИР обеспечит достижение научных результатов мирового уровня в решении многих актуальных фундаментальных и прикладных проблем химии и биологии, медицины и экологии, нано- и биотехнологии, ветеринарии и зоотехнии; позволит завершить создание комплексной системы подготовки высококвалифицированных специалистов (от бакалавров и магистров до кандидатов и докторов наук), обладающих особыми компетенциями по профилю данной НИР, что приведет к формированию эффективного и жизнеспособного научного коллектива.
Область применения полученных результатов.
Результаты проекта должны быть включены в образовательную программу ФГОУ ВПО МГАВМиБ и использоваться в образовательном процессе на базе научного кадрового потенциала, лабораторного и испытательного оборудования научно-образовательного центра ФГОУ ВПО МГАВМиБ, в том числе в процессе проведения настоящих научно-технических работ.
Новые БКС, разработанные на основе полимеров разного типа, могут найти применение в медицине человека и животных, экологии, нано- и биотехнологии и т.д. Полученные на данном этапе результаты являются ключевыми для успешного выполнения всего проекта.
Прогнозные предположения о развитии объекта исследования.
В процессе проведения НИР должны быть разработаны технологические параметры БКС и методические рекомендации по их использованию для различных областей применения, в том числе: экспериментальные образцы; методики испытаний экспериментальных образцов; технологии получения биохимических коллоидных систем.
В ходе выполнения НИР будут получены результаты интеллектуальной деятельности (статьи, патенты и т.д.); учебно-методические комплексы, включающие учебно-методические пособия, указания и рекомендации; примерные и рабочие учебные программы, практикумы по дисциплинам «Биохимия мембран», «Физическая и коллоидная химия», «Кинетика и термодинамика ферментативных реакций», «Энзимология», «Биоэнергетика», «Бионанотехнология» и другие.
СОДЕРЖАНИЕ
| Реферат ………………………………………………………………………………….…………. | 4 |
| 4.1. Инжиниринговое обеспечение экспериментального оборудования для изучения ФКС…………………………………………………………………………………………………. | 11 |
| 4.1.1 Методы измерения динамического поверхностного натяжения биологических жидкостей…………………………………………………………………………………………… | 11 |
| 4.1.2 Метод измерения активности ферментов………………………………………………….. | 16 |
| 4.1.3 Метод изучения гидролиза триглицеридов и новых липидоподобных субстратов в монослоях под действием липаз………………………………………………………………….. | 18 |
| 4.1.4 Использование роторного испарителя для получения липосом…………………………. | 30 |
| 4.2. Анализ результатов по динамическому поверхностному натяжению и по каталитическим свойствам липаз в присутствии полиэлектролитов…………………………………..…………………………………………….. | 33 |
| 4.2.1 Влияние полиэлектролитного окружения на активность липаз из поджелудочной железы свиньи и гриба Mucor javanicus…………………………………………………………... | 33 |
| 4.2.2 Изучение динамического поверхностного натяжения систем липазы из поджелудочной железы свиньи с природными и синтетическими полиэлектролитами…….... 4.2.3 Измерение динамического поверхностного натяжения растворов липазы из поджелудочной железы свиньи в смеси с полистиролсульфонатом натрия…………………… 4.2.4 Измерение динамического поверхностного натяжения растворов липазы из поджелудочной железы свиньи в смеси с полидиаллилдиметиламмоний хлоридом…………. 4.2.5 Измерение динамического поверхностного натяжения растворов липазы из поджелудочной железы свиньи в трехкомпонентном комплексе с полистиролсульфонатом натрия и полидиаллидиметиламмоний хлоридом……………………………………………….. | 35 35 40 45 |
| 4.3. Построение моделей на основе полученных корреляций между изученными параметрами……………………………………………………………………………………….. | 48 |
| 4.3.1 Модельные системы на основе белков, липидов и солей………………………………… | 48 |
| 4.3.2 Модельные системы на основе куриных эмбрионов……………………………………… | 58 |
| 4.4. Изучение состава и свойств биологических жидкостей коров под воздействием внешних факторов…..…………………………………………………………………………… | 63 |
| 4.5. Сравнительное исследование изменений элементного состава поверхностных слоев волоса и кожного покрова у ценных видов пушных зверей для применения в зоотехнии…………………………………………………………………..……………………….. | 72 |
| 4.5.1 Закономерности изменения минерального состава волосяного покрова у стандартных норок ……………………………………………………………………………………………….. | 74 |
| 4.5.2 Закономерности изменения минерального состава волосяного покрова у серебристых песцов ………………………………………………………………………………………………. 4.5.3 Закономерности изменения минерального состава волосяного покрова у серебристо-черных лисиц ………………………………………………………………………………………. 4.5.4 Закономерности изменения поверхностной концентрации макро- и микроэлементов в кожно-волосяном покрове у разных видов пушных зверей…………………………………….. | 77 82 85 |
| 4.6. Анализ и обобщение полученных на 4 этапе результатов НИР…...…………………………………………………………………………………………….. | 101 |
| 4.7. Анализ апробации результатов по мембранным коллоидным системам в части МКС для определения катионов тяжелых металлов спектральными методами в учебном процессе………………………………………………………………………………… 4.7.1 Апробация результатов по мембранным коллоидным системам в реализации рабочих программ учебных дисциплин, практик, выпускных квалификационных работ……………… 4.7.2 Апробация результатов по мембранным коллоидным системам в профиле работы научных студенческих кружков кафедры органической и биологической химии…………… 4.7.3 Методические рекомендации по апробации результатов по мембранным коллоидным системам, содержащие фрагменты разрабатываемой проблемы по МСК и внедренные в учебный процесс…………………………………………………………………………………... ПРИЛОЖЕНИЯ Приложение 1 | 102 103 108 109 |
| 4.8. Проведение экспериментальных исследований биологических жидкостей с использованием лабораторных установок для формирования мономолекулярных пленок органических и биологических веществ, для исследования биологических мембран, клеток, синтетических и природных полимеров и другого специального оборудования………………………………………………………………………………………. | 112 |
| Приложение 2 ……………………………………………………………………………………... | 116 |
ОБОЗНАЧЕНИЯ И СОКРАЩЕНИЯ
МКС - мембранные коллоидные системы
ФКС – ферментные коллоидные системы
БКС – биохимические коллоидные системы
НКМ - нанокомпозитные материалы
ОМС - оптические молекулярные сенсоры
ММВ - малые моноламеллярные везикулы
БМВ - большие моноламеллярные везикулы
ПСС - Na-полистиролсульфонат
ПАМА - полидиаллилдиметиламмоний хлорид
ПЛ - полилизин
ПГ - полиглутамин
БСА – бычий сывороточный альбумин
УФ-область – ультрафиолетовая область
КРС – крупный рогатый скот
СОЭ – скорость оседания эритроцитов
ЛС - лекарственные средства
АГ - антигены
АТ - антитела
ПН - поверхностное натяжение
ДПН - динамическое поверхностное натяжения
УЗ - ультразвук
ПАВ - поверхностно-активные вещества
ССА - свиной сывороточный альбумин
4.1 Инжиниринговое обеспечение экспериментального оборудования для изучения ФКС
4.1.1 Методы измерения динамического поверхностного натяжения биологических жидкостей
Для исследования биологических жидкостей в большей степени подходят два метода: максимального давления в пузырьке и метод висящей капли. Метод максимального давления в пузырьке позволяет получать кривую динамического поверхностного натяжения в диапазоне времени от 0,01 до 100 секунд с воспроизводимостью не менее 0,2%. В настоящее время выпускается несколько типов приборов, работающих по этому методу PBS (Electronetics Comp., США), Sensadyn (Chem Dyne Research Corp., США), BPA-1P (Sinterface Technologies, ФРГ), MPT2 (Lauda, ФРГ).
Адаптированные для измерения биологических жидкостей приборы проводят измерения объёма жидкости от 1 мл.
Преимуществом метода висящей капли является малый объём анализируемой жидкости (менее 0,5 мл), простое и удобное термостатирование пробы, широкий диапазон измерений времени существования капли (от 10 до 10000 с и более), что дополняет возможности метода максимального давления в пузырьке. Приборы, работающие по этому методу: "ADSA-Toronto" (Канада), PAT-1 (Sinterface Technologies, ФРГ). Комбинация двух методов, позволяет проводить измерения ДПН во временном интервале от 10-3 до 104 секунд.
Метод висящей капли. Метод висящей капли используется при измерении поверхностного натяжения на приборе РАТ-1 (Topfen-Blasen-Profiltensiometer) (ФРГ, Sinterface Technologies). Его преимуществами являются малый объём анализируемой жидкости, широкий диапазон измерений времени жизни капли (от 10 до 10000с и более). Прибор РАТ-1 состоит из микродозирующего устройства, включающего шприц для жидкостной хроматографии на 0,5 мл и микрометрического регулятора (1), микродозирующей системы (7), которая через процессор управляется компьютером (6), источника света (3), объектива и специальной видеокамеры (4), обеспечивающей неискажённое изображение капли, термостатируемой ячейки (8) с каплей исследуемой жидкости (2), формируемой на кончике стального или тефлонового капилляра (Рис.1).
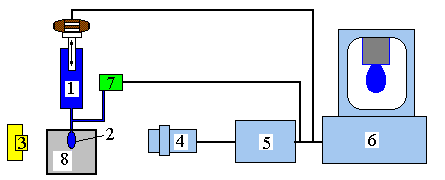
Рисунок 1 - Схема строения тензиометра РАТ-1.
1-макродозирующая система, 2-капля биологической жидкости, 3-источник света, 4-объектив и видеокамера, 5-аналогово-цифровой преобразователь, 6-компьютер, 7-микродозирующая система, 8-термостатируемая ячейка.
От видеокамеры (4) сигнал поступает в видеопроцессор (5), где происходит его преобразование из аналогового в цифровой. Затем он передаётся на компьютер (6). Для определения геометрической границы капли используется метод локального порога яркости. Граница капли определяется по максимальному градиенту яркости, как функции от координаты строки изображения, а также используется полиномиальное сглаживание каждой группы из 5 последовательных точек на границе капли. Для калибровки видеоустановки используется эталонная оптическая сетка. Экспериментальная погрешность измерений поверхностного натяжения по методу висящей капли составляет около 0,1 мН/м.
Форма капли, висящей на кончике капилляра, при прочих равных условиях определяется ее размерами. Чем больше объем капли, тем в большей степени ее форма отличается от сферической. Уравнение Лапласа описывает механическое равновесие капли, как баланс действующих на каплю сил. Избыточное давление в капле жидкости, помещенной в другую жидкость или газ, определяется главными радиусами кривизны (R1 и R2) и поверхностным (межфазным) натяжением жидкости:
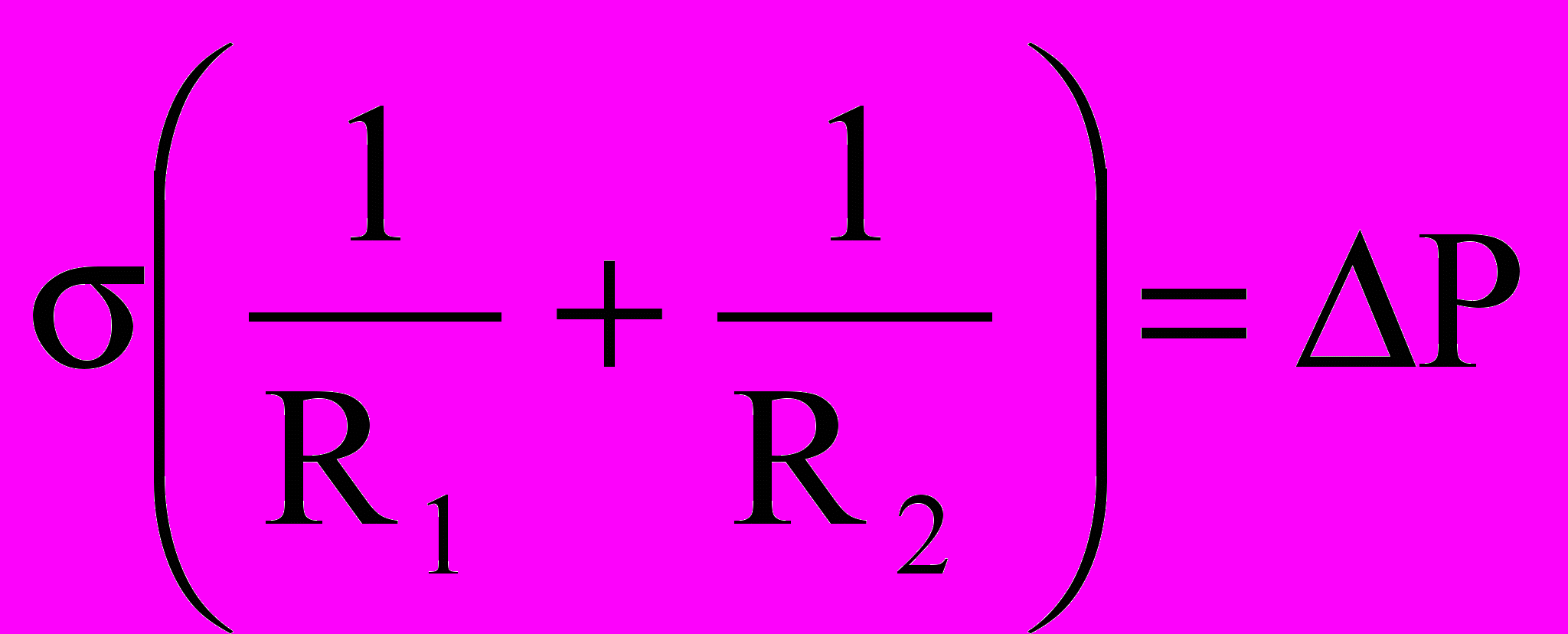 (1)
(1)где σ – поверхностное натяжение, ΔP – разность давлений между фазами. В отсутствие других внешних сил, кроме гравитации, величина разности давлений может быть выражена как линейная функция высоты капли:
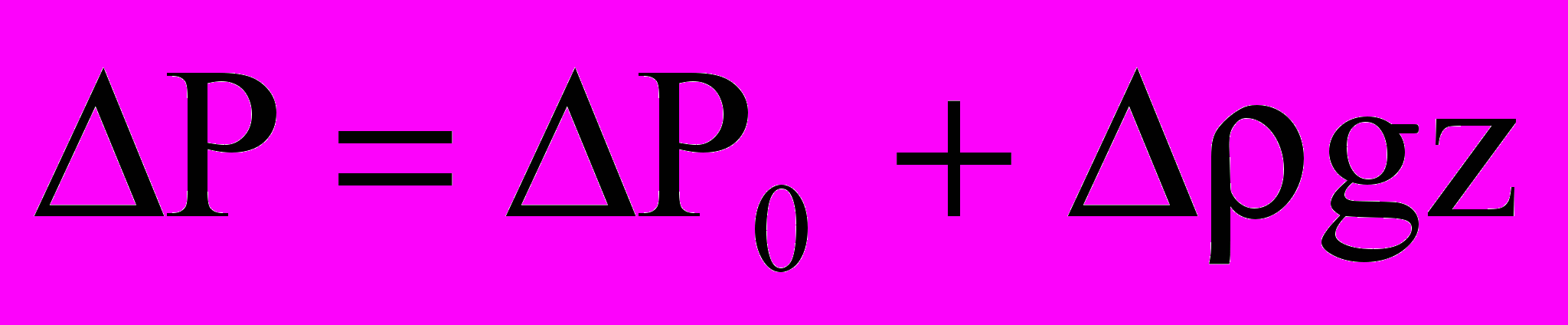 (2)
(2)где ΔP0 – разность гидростатических давлений в плоскости z=0, z – вертикальная координата, Δρ – разность плотностей двух объемных фаз, g – гравитационное ускорение. Капиллярные силы стремятся сделать каплю более сферической, тогда как гравитационные, наоборот, стремятся вытянуть каплю вдоль вертикальной оси.
Таким образом, если известно поверхностное натяжение, то форма капли (главные радиусы кривизны R1 и R2) может быть определена по уравнению Лапласа (1). Определение поверхностного натяжения по форме капли также может быть осуществлено. Rottenberg с сотрудниками предложили метод, названный методом анализа формы осесимметричных капель (ADSA), в котором форма капли автоматически анализируется, оптимизируется и сравнивается с теоретическим лапласовским профилем.
Анализ тензиограмм. Зависимость ПН от «времени жизни» поверхности обусловлена неравновесным характером процессов адсорбции-десорбции поверхностно-активных веществ (липидов, белков и т.п.) на жидкой границе раздела фаз. В начальный момент времени (t0) поверхностный слой не содержит избытка поверхностно-активных компонентов, т.е. адсорбция равна нулю, а ПН раствора и растворителя 0 одинаковы. Для большинства биологических жидкостей величина 0 близка к ПН воды и солевых растворов - 70-74 мН/м. Скорости адсорбции и понижения ПН определяются в общем случае диффузией сурфактантов к поверхности, скоростью преодоления так называемого адсорбционного барьера (электростатической, энтропийной или иной природы) и процессами перестройки адсорбированных молекул в поверхностном слое.
Многочисленные теоретические работы дополнены в последнее время теорией кинетики адсорбции без учета перестройки в поверхности, которая была разработана Уордом и Тордеем. Применение данной теории в полном виде встречает значительные затруднения вследствие интегрально-дифференциальной формы итогового уравнения (так называемое уравнение Вольтера) и необходимостью привлечения дополнительных термодинамических и кинетических соотношений. В частности, должны быть использованы уравнения изотермы адсорбции, кинетическое адсорбционное (типа уравнения Ленгмюра) и состояния поверхностного слоя. Эти уравнения были получены для случаев, когда в растворе присутствуют одно или два вещества известной природы. В случае же многокомпонентных биологических жидкостей строгий подход к решению диффузионно-кинетических проблем вряд ли возможен в настоящее время. Использование асимптотических уравнений теории кинетики адсорбции является более простым, но в то же время достаточно информативным методом анализа динамических тензиограмм.
При предельно малых временах (t0) из общего уравнения Уорда и Тордея вытекает относительно простое соотношение, которое для многокомпонентного раствора имеет вид:
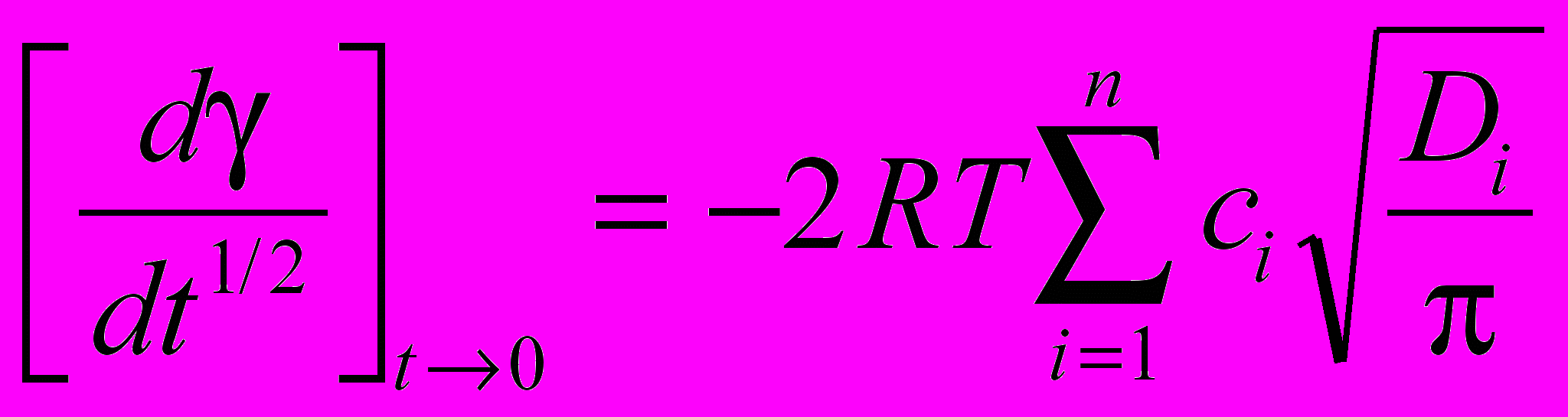 (3)
(3)где R - газовая постоянная, T - температура, сi - концентрация поверхностно-активного компонента, Di - коэффициент диффузии, i - номер компонента, n - общее число ПАВ. Производная в левой части уравнения (3) представляет собой тангенс угла наклона прямой в координатах - t1/2. Поскольку значения коэффициентов диффузии различных ПАВ имеют одинаковый порядок величины, то соотношение (3) показывает, что тангенс угла наклона прямой от t1/2 примерно пропорционален суммарной концентрации ПАВ смеси. Начальный участок кривой хорошо аппроксимируется линейной зависимостью. Точка пересечения линейного участка с осью ординат близка к поверхностному натяжению воды (в наших опытах равна 72,70,3 мН/м). Как следует из теории, величина 0 определяется солевым составом биологической жидкости. Таким образом, сравнивая углы наклона динамических тензиограмм в координатах - t1/2 можно получить информацию о суммарной концентрации поверхностно-активных компонентов в исследуемом образце биологической жидкости.
Второе важное соотношение, вытекающее из теории Уорда - Тордея (так называемое уравнение Йооса - Хансена), относится к случаям предельно больших времен жизни поверхности. Расширенное для многокомпонентной системы, оно может быть записано в виде:
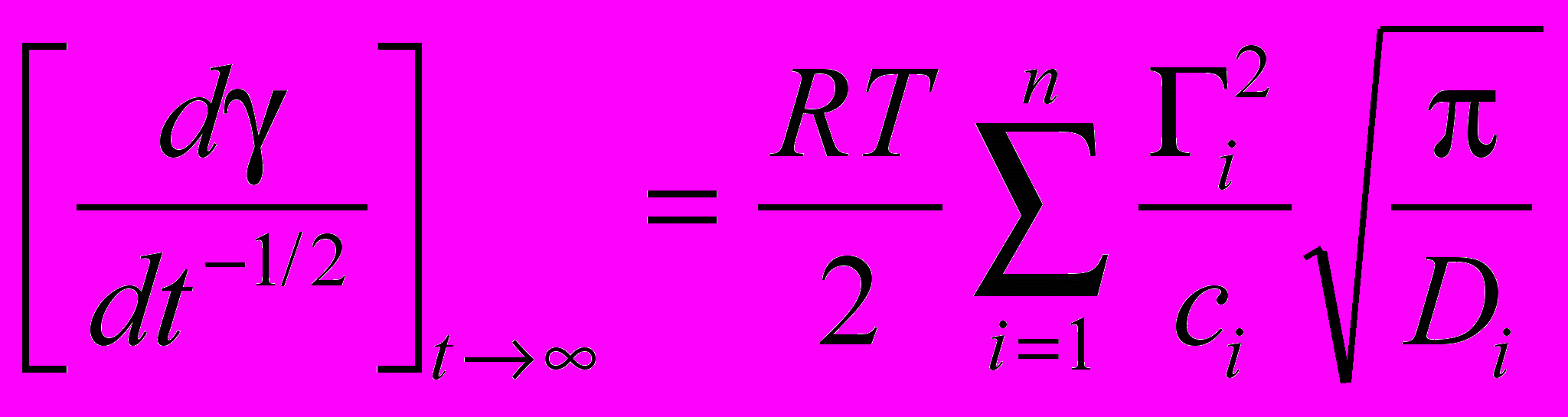 (4)
(4)где Г - величина гиббсовской (избыточной) адсорбции данного поверхностно-активного соединения.
Производная в левой части этого уравнения берется в координатах - t1/2 и рассчитывается в пределе t (т.е. t1/20). Поскольку отношение Гi/ci для многих сурфактантов является константой (так называемая константа Генри Кi = Гi/ci), то сумма в правой части уравнения (4) приближенно выражает адсорбцию всех компонентов смеси с учетом их адсорбционной активности (Ki). Таким образом, сравнивая значения производных (d/dt1/2)t для различных образцов биологических жидкостей, мы получаем информацию об изменении их состава по изменению величины адсорбции.
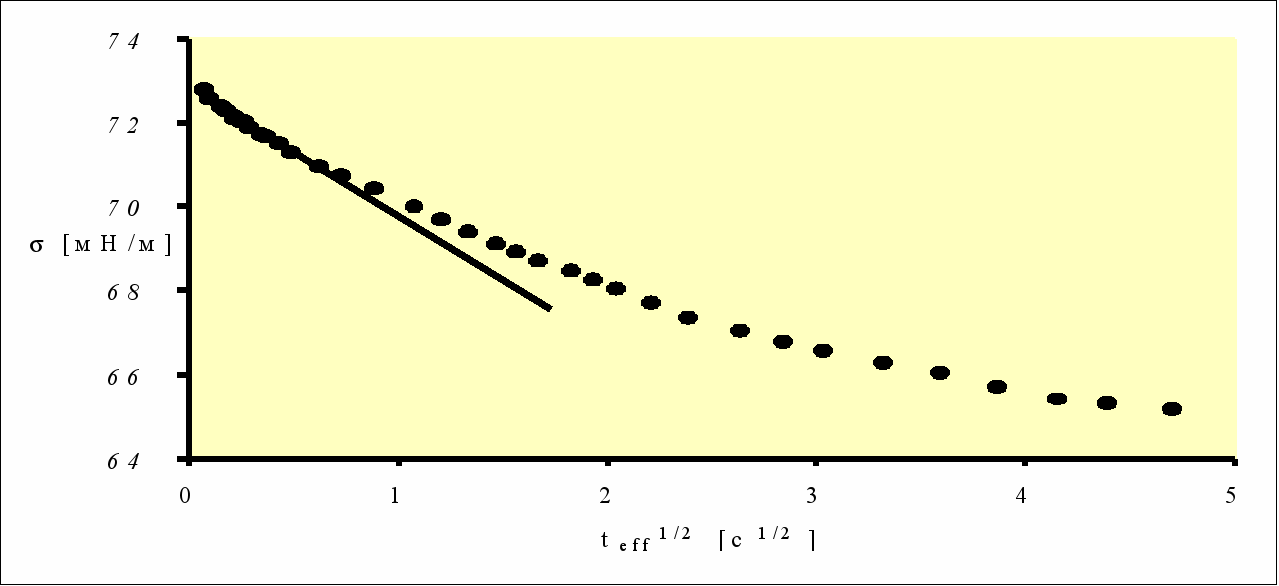
Рисунок 2 - Динамическая тензиограмма сыворотки крови человека в зависимости от teff1/2. Характеристика линейного участка 0=72,8 мН/м,
λ0=2,8 мН.м-1.с1/2
Экспериментальная зависимость имеет «квазилинейный» участок при t1/20. Точка пересечения прямой с осью ординат дает величину равновесного (т.е. приведенного к t) ДПН () . Последняя характеристика является чрезвычайно важной и может быть получена только путем экстраполяций динамической тензиограммы в координатах - t1/2.
Анализ общего решения и асимптотических уравнений для «не диффузионной» кинетики адсорбции свидетельствует, что существование адсорбционного барьера оказывает слабое влияние на выражаемую уравнением (1) зависимость от t1/2 при t, поскольку в этих условиях диффузионный поток из раствора к поверхности является наиболее медленной стадией, определяющей скорость адсорбции. В области очень коротких времен, для которых используется уравнение (3), адсорбционный барьер существует только в концентрированных растворах и поэтому им можно пренебречь в случае для биологических жидкостей человека и животных. В то же время процессы перестройки в поверхности, например, адсорбция-десорбция сегментов белковых молекул, могут замедлять кинетику адсорбции в области средних и больших времен по сравнению с диффузионным механизмом.
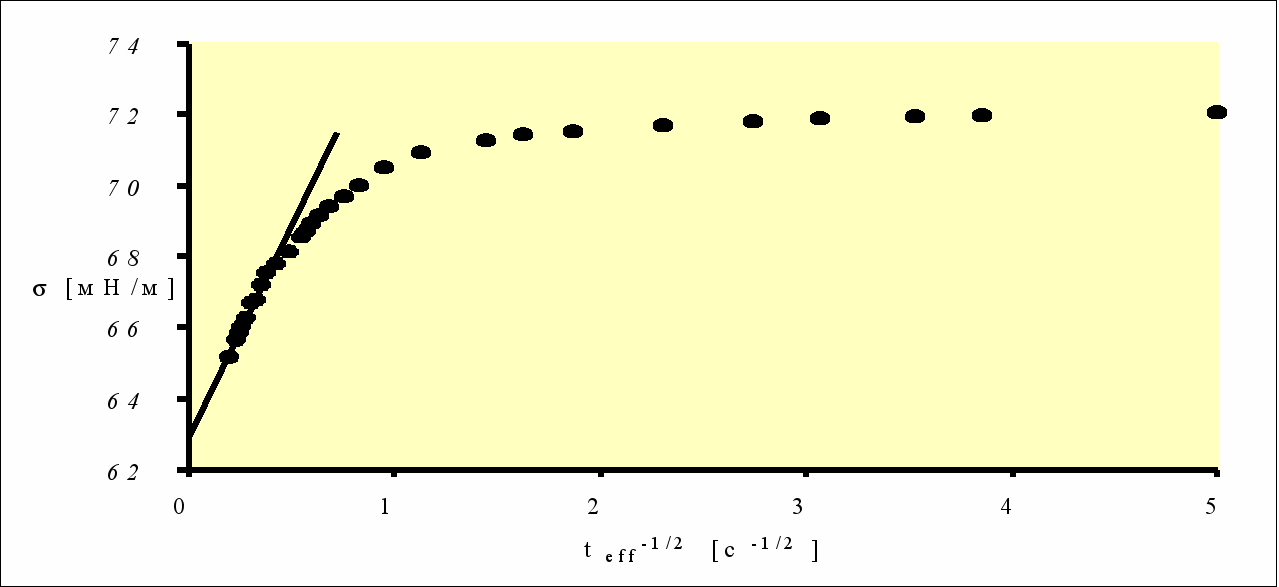
Рисунок 3 - Динамическая тензиограмма сыворотки крови человека
в зависимости от teff-1/2. Характеристика линейного участка: =62,9 мН/м,
=11,2 мН.м-1.с1/2 .
Однако в области небольших (до 3 мН/м) понижений ДПН (малых t) процесс адсорбции макромолекул контролируется диффузией. Таким образом, уравнения (3) и (4) для биологических жидкостей могут использоваться почти без ограничений.
Результаты исследований представляются в виде тензиограмм (кривых зависимости от t), на которых определяются точки, соответствующие t0,01 с (0) и t1 с (1), а также равновесному ДПН (3). Кроме того, подсчитывается угол наклона кривой (λ) в координатах (t-1/2). Значения 1, (как и 0), характеризуют как свойства растворителя, так и адсорбцию в области коротких времен, а 2 - в области средних времен жизни поверхности. Эти процессы обусловлены в основном наличием в биологических жидкостях низко и средне молекулярных поверхностно-активных веществ, тогда как для высокомолекулярных фракций (белков и других соединений) определяющими являются значения 3. При этом угол наклона прямой λ характеризует величину адсорбции и концентрацию основного компонента сыворотки.
