Молекулярные механизмы формирования множественной лекарственной резистентности у Burkholderia pseudomallei и близкородственных видов микроорганизмов 03. 00. 07 микробиология 03. 00. 15 генетика
| Вид материала | Автореферат |
- Л. И. Параллелизмы в молекулярной организации генома и проблемы эволюции. В кн.: Молекулярные, 251.18kb.
- Особенности эволюции морфологических и молекулярных признаков на примере близкородственных, 1418.11kb.
- Патогенетические компоненты лечения туберкулеза с множественной лекарственной устойчивостью, 210.94kb.
- Рабочая программа дисциплины «нормальная микрофлора человека» Код дисциплины по учебному, 110.88kb.
- 1. введение в микробиологию > 1 Предмет и задачи микробиологии. Основные свойства микроорганизмов, 1814.12kb.
- Рабочая программа дисциплины «роль микроорганизмов в жизни растений» Код дисциплины, 88.04kb.
- Рабочая программа дисциплины «экология микроорганизмов» Код дисциплины по учебному, 219.98kb.
- А. В. Низова [и др.] // Эпидемиология и инфекц болезни. 2007. N c. 7-11, 85.01kb.
- Рабочая программа дисциплины «жизнь микроорганизмов в экстремальных условиях» Код дисциплины, 123.41kb.
- Лекция 1 Введение. Основные принципы классификации микроорганизмов. Различия архебактерий,, 46.21kb.
Изменчивость детерминант устойчивости к отдельным группам антимикробных соединений и геномная вариабельность полирезистентных штаммов буркхольдерий
Мутационные изменения ДНК-гиразы А у мутантов Burkholderia с высоким уровнем устойчивости к препаратам фторхинолоновой группы. Исследования механизмов резистентности к хинолоновым антибиотикам и их фторированным производным у различных бактериальных видов демонстрируют значимую роль точечных мутаций в особом участке генов ДНК-гиразы и топоизомеразы IV, определяющем высокую резистентность к фторхинолонам – регионе QRDR (quinolone resistance determining region) (Baranwal et al., 2002; Ruiz, 2003). Мы провели анализ возможных мутационных изменений в QRDR ДНК-гиразы для оценки их значения в формировании резистентности исследуемых видов Burkholderia к препаратам фторхинолонового ряда.
Регион последовательности ДНК-гиразы А, мутационные изменения в котором определяют соответствующие аминокслотные замены во взаимодействующих с антибиотиком участках молекулы белка (QRDR), был предварительно определен нами путем поиска участка gyrA буркхольдерий, гомологичного известным QRDR ДНК-гираз, представленных в Genbank NCBI (www.ncbi.nlm.nih.gov). По результатам анализа аннотированных последовательностей gyrA B. pseudomallei, B. mallei и B. thailandensis и известных последовательностей QRDR gyrA нами были подобраны праймеры для амплификации фрагмента гена, включающего предполагаемый QRDR (табл. 6).
Табл. 6.
Характеристика олигонуклеотидных праймеров, использованных для амплификации фрагмента gyrA видов Burkholderia, предположительно включающего QRDR
| Праймер | Последовательность (5’-3’) | Т отжига, ºC | Мишени | ПЦР- фрагмент | Ампликон (пн) |
| gyrAs | CTTCCGGATGTCCGCGATGG | 60 | BMA_0435 BPSL2521 BTH_I1632 | 100 - 571 | 472 |
| gyrAas | CGACCTCGTTCAGGTTGTGC |
Поиск возможных мутационных изменений в предполагаемом QRDR ДНК-гиразы А буркхольдерий включал в себя несколько технологических этапов: амплификацию исследуемого фрагмента гена в ПЦР, анализ конформационного полиморфизма однонитевых цепей ампликонов (SSCP, single strand conformation polymorphism) и отбор вариантов с атипичными SSCP-профилями, секвенирование и сопоставление нуклеотидных последовательностей QRDR исходных штаммов и «кандидатных» мутантных последовательностей.
Изменения в SSCP-профиле QRDR gyrA были обнаружены у мутантных штаммов PfxR CazR и OfxR CazR мутантов B. pseudomallei и резистентных к фторхинолонам мутантов B. mallei (рис. 17). Секвенирование QRDR ампликонов из этих штаммов показало наличие единичных и двойных нуклеотидных замен в регионе gyrA 240 – 260 п.н., а трансляция in silico мутантных последовательностей gyrA позволила определить несколько типов аминокислотных замен в QRDR-области фермента (рис. 18).
Аминокислотная замена Thr83Ile была общей для всех исследованных мутантных штаммов. Замены Gly81Cys и Asp87Tyr были обнаружены только у PfxRCazR и OfxRCazR мутантов B. pseudomallei, соответственно. Кроме того, у одного из мутантов B. mallei была выявлена нуклеотидная замена CT в 250 нуклеотидной позиции гена, не приводящая к аминокислотной замене, и классифицированная нами как silence-мутация. Интересно, что описанные в работе Maeda Y. et al., аминокислотные замены QRDR GyrA у резистентных к хинолонам природных изолятов B. glumae также затрагивают позицию 83 последовательности белка (Maeda et al., 2004).
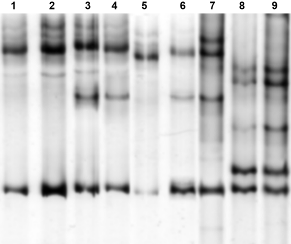
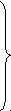
одноцепочечные
структуры
двухцепочечные
структуры
продукты
частичной реассоциации
Рис. 17. ПЦР-SSCP анализ амплифицированных фрагментов QRDR gyrA исходных штаммов и полирезистентных мутантов буркхольдерий. Электрофорез в 10 % полиакриламидном геле. Треки 1 – 9: B. pseudomallei 56770, B. pseudomallei 56770 SMCP, B. pseudomallei 56770 SMPC, B. pseudomallei 56770 SMOC, B. mallei C-5, B. mallei C-5 SMP-150-2, B. mallei C-5 SMP-150-3, B. thailandensis E264, и B. thailandensis E264 SMPC.
A
B


Рис. 18. Нуклеотидные (А) и соответствующие аминокислотные (В) замены в области QRDR ДНК-гиразы А у мутантов буркхольдерий с высоким уровнем устойчивости к антибиотикам фторхинолонового ряда.
Таким образом, полученные нами результаты демонстрируют, что мутационные изменения мишеней действия антимикробных соединений (в данном случае, ДНК гиразы А), наряду с активацией систем лекарственного эффлюкса, также вносят свой вклад в формирование наблюдаемых фенотипов множественной антибиотикоустойчивости у B. pseudomallei и B. mallei. Отметим, что сочетание мутаций gyrA и механизмов активного выведения фторхинолонов из клеток неоднократно показано у различных бактериальных патогенов (Chen, Lo, 2003; Dewi et al., 2004; Ricci et al., 2004; Payot et al., 2004).
Детекция интегроноподобных последовательностей в штаммах B. pseudomallei, B. mallei и B. thailandensis. Исследования систем генетического обмена возбудителей мелиоидоза и сапа (Меринова и др., 1990; Меринова и др., 1997; Меринова и др., 1998; Меринова и др., 2000) доказали возможность горизонтального переноса и приобретения данными микроорганизмами R-детерминант в составе мобильных генетических элементов. В настоящей работе определенное внимание было уделено поиску и первичной характеристике интегронов – генетических элементов, способных включать в свой состав индивидуальные генные кассеты (в том числе детерминанты антибиотикорезистентности) по механизму сайт-специфической рекомбинации (Hall, Collis, 1995; Rowe-Magnus, Mazel, 2001; Fluit, Schmitz, 2004; Nogrady et al., 2005).
Для скрининга сходных с интегронами последовательностей B. pseudomallei, B. mallei и B. thailandensis был использован ПЦР-анализ с праймерами, специфичными фрагментам гена интегразы IntI1 и фланкирующим последовательностям области вставки генных кассет (Bass et al., 1999). Последующий электрофоретический анализ продуктов реакции показал наличие ампликонов размерами от 100 п.н. до 1200 п.н. у отдельных штаммов B. pseudomallei и B. thailandensis (рис. 19).
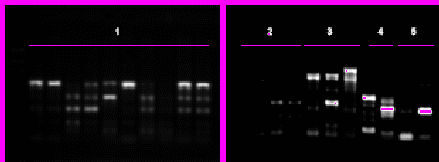
A
B
C
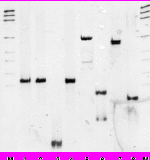
Рис. 19. (А, В) - Амплификация интегроноподобных последовательностей из штаммов различных видов Burkholderia и гетерологичных микроорганизмов. Обозначения: 1 – штаммы B. pseudomallei; 2 – штаммы B. mallei; 3 – штаммы B. thailandensis; 4 – штаммы B. cepacia; 5 – штаммы P. aeruginosa. (С) - Реамплификация очищенных ампликонов. Обозначения: М – маркерная ДНК (pGEM DNA Marker, Promega); 1 – B. pseudomallei 140; 2, 3, 4, 5 – B. thailandensis Е2996 6, 7 – B. cepacia 25416; 8 – B. cepacia 3189.
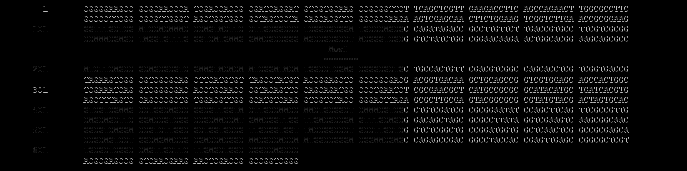
Секвенирование и поиск гомологов в Genbank показали, что продукты амплификации ДНК из штамма B. thailandensis E299 представляют собой фрагменты последовательностей транспозаз/интеграз (рис. 20), а анализ геномных регионов буркхольдерий, имеющих максимальные показатели сходства с секвенированными ампликонами продемонстрировал наличие интегроноподобных структур, включающих ген транспозазы/интегразы и гены различной функциональной направленности, в том числе CDS, аннотированные как детерминанты лекарственной устойчивости (гены эффлюкс-транспортеров MFS и RND типов) (рис. 21).
A
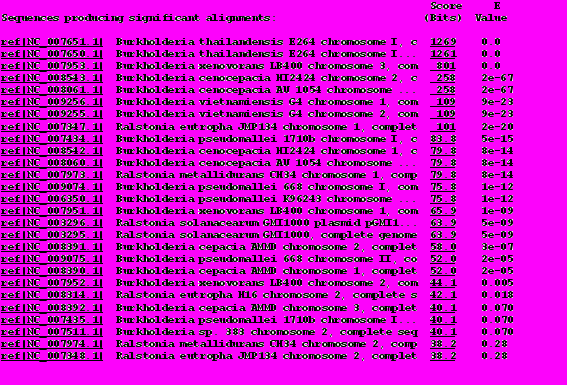
B
Рис. 20. Нуклеотидная последовательность ампликона 640 п.н. B. thailandensis E299 (A) и гомологичные ей последовательности геномов представителей Burkholderiaceae (B).
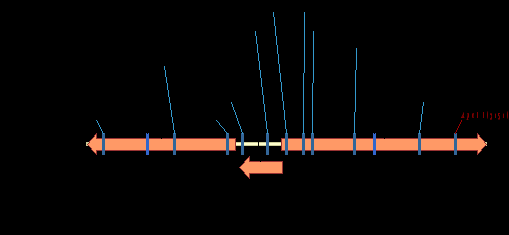

Рис. 21. Фрагмент генома B. thailandensis E264 (NC_007651), содержащий полностью идентичный секвенированной последовательности ампликона 640 п.н. штамма B. thailandensis E299 участок ДНК (помечен прямоугольником).
Генетическая гетерогенность штаммов B. pseudomallei и родственных видов с различной чувствительностью к антимикробным соединениям. Заключительная часть нашего исследования была посвящена анализу перспектив молекулярного типирования штаммов буркхольдерий с различными спектрами антибиотикорезистентности. Мы апробировали техники типирования, основанные на амплификации полиморфных ДНК с произвольным праймером (RAPD) и ПЦР-анализе с праймером, специфичным консервативному региону интеграз intI1, для дифференциации штаммов B. pseudomallei дикого типа, селекционированных полирезистентных вариантов и транспозонных мутантов со сниженной устойчивостью к отдельным классам антибиотиков.
Типирование с использованием произвольного праймера (рис. 22) показало заметную межвидовую вариабельность RAPD-паттернов и их более консервативный характер у производных того или иного штамма. Транспозонные мутанты B. pseudomallei со сниженной резистентностью к фторхинолонам и цефтазидиму были распределены в три достаточно обособленные друг от друга группы сходства RAPD-профилей, что может свидетельствовать о сходном характере генетических перестроек, вызванных инсерциями Tn5, внутри каждой из групп сходства. Интересно также, что две отдельные группы сходства RAPD-паттернов были образованы штаммами B. pseudomallei с преобладающей резистентностью к пефлоксацину, офлоксацину и цефтазидиму.
Также удалось обнаружить заметные различия в фингерпринтах содержащих интегразу фрагментов ДНК (рис. 23). Два из трех проанализированных мутантов B. pseudomallei, высокорезистентных к CAZ, PFX и OFX, оказались фактически идентичны по спектру ампликонов, тогда как один мутантный штамм оказался более сходен с исходным. Как и в случае RAPD-анализа, различные виды буркхольдерий формировали достаточно обособленные группы сходства ДНК-профилей. Полученные результаты, по нашему мнению, говорят о заметных геномных перестройках при развитии различных типов резистентности у B. pseudomallei и близкородственных бактерий, и, что может быть важно для дальнейшей разработки молекулярной эпидемиологии данных бактерий, свидетельствуют о возможности определения дополнительных молекулярных маркеров, ассоциированных с различными типами лекарственной резистентности.
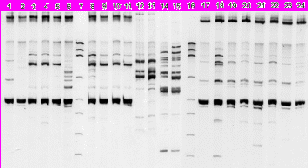
Рис. 22. Дендрограмма сходства RAPD-профилей штаммов Burkholderia с различным уровнем устойчивости к антибиотикам.. UPGMA группирование матрицы дистанций несоответствия (dd). Штаммы B. pseudomallei: 1 – 57576 SMP; 2 – 57576 SMO; 3 – 57576 SMPC, 4 – 57576 SMCO; 5 – 57576 SMCP; 6 – 57576 SMRT21; 8 – 56770; 9 – 56770 SMPC; 10 – 56770 SMCP; 11 – 56770 SMOC; 17 – 57576; 18 – 57576 TTM6-1; 19 – 57576 TTM6-3; 20 – 57576 TTM7-1; 21 – 57576 TTM7-2; 22 – 57576 TTM9-1; 23 – 57576 TTM9-2; 24 – 57576 TTM9-3. Штаммы B. thailandensis: 12 – E264; 13 – E264 SMPO. Штаммы B. cepacia: 14 – 25416; 15 – 25416 SMPC.
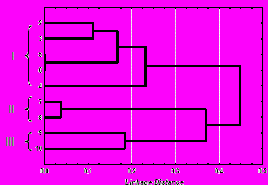
Рис. 23. Дендрограмма сходства интегразосодержащих ДНК-профилей. UPGMA группирование матрицы дистанций несоответствия (dd). Штаммы B. pseudomallei: 2 – 57576; 3 – 57576 SMCO; 4 – 56770; 5 – 56770 SMCP; 6 – 56770 SMOC. Штаммы B. thailandensis: 7 – E264; 8 – E264 SMPO. Штаммы B. cepacia: 9 – 25416; 10 – 25416 SMPC.
Таким образом, настоящие исследования по интересующей нас проблеме позволили идентифицировать основные группы молекулярных механизмов, ответственных за реализацию множественной устойчивости бактерий группы «pseudomallei» к антимикробным соединениям и разработать комплекс методических подходов для их дальнейшего более детального анализа. На основе модельной системы, включающей штаммы с измененной чувствительностью к антибиотикам, а также технологий молекулярно-генетического анализа факторов резистентности проведено комплексное исследование механизмов множественной устойчивости патогенных буркхольдерий и показаны принципиальное участие в формировании резистентности множественного типа у B. pseudomallei, B. mallei и B. thailandensis процессов снижения проницаемости клеточных мембран, экспрессии систем активного выведения ингибиторов из клеток и мутационных изменений генов внутриклеточных мишеней антимикробных соединений, а также особенности развития полирезистентности, заключающиеся в сочетанном проявлении перечисленных механизмов.
Все это дает возможность наметить ближайшие перспективы работ в области функциональной и сравнительной геномики лекарственной резистентности патогенных буркхольдерий – изучение механизмов индукции и регуляции экспрессии отдельных эффлюкс-транспортеров, получение коллекций мутантов буркхольдерий с инактивированными генами лекарственного эффлюкса, сравнительный анализ экспрессии белков клеточных мембран штаммов с измененной чувствительностью к антибиотикам с использованием техники протеомных исследований, разработка систем анализа экспрессии детерминант антибиотикорезистентности на основе технологии cDNA-чипов.
ВЫВОДЫ
- На основе модельной системы, включающей штаммы с измененной чувствительностью к антибиотикам, а также технологии молекулярно-генетического анализа факторов резистентности проведено комплексное исследование механизмов множественной устойчивости патогенных буркхольдерий. Показано сочетанное участие в формировании резистентности множественного типа у B. pseudomallei, B. mallei и B. thailandensis процессов снижения проницаемости клеточных мембран, экспрессии систем активного выведения ингибиторов из клеток и мутационных изменений генов внутриклеточных мишеней антимикробных соединений.
- Развитие у штаммов B. pseudomallei, B. mallei и B. thailandensis высокого уровня устойчивости к антибиотикам фторхинолоновой и цефалоспориновой групп сопровождается приобретением резистентности к антимикробным соединениям других классов (-лактамам, аминогликозидам, макролидам, хлорамфениколу), ряду неспецифических ингибиторов (жирным кислотам, солям желчных кислот, детергентам, красителям), а также заметным снижением вирулентности полирезистентных вариантов для экспериментальных животных.
- Установлено, что развитие лекарственной резистентности множественного типа у исследуемых видов буркхольдерий сопровождается существенными изменениями белкового состава мембран, являющимися показателем модификации их транспортных функций и проницаемости. В сравнении с исходными штаммами, у полирезистентных производных B. pseudomallei и B. thailandensis наблюдалась гиперпродукция мажорных мембранных белков 27, 39, 48, 71 и 110 kDa и значительное снижение синтеза протеинов 45 и 49 kDa. Резистентные мутанты B. mallei характеризовались снижением продукции группы мембранных белков 21, 42, 45 и 70 - 100 kDa.
- Показано, что инсерционные мутанты B. pseudomallei Bop- с дефектами в продукции мембранных протеинов 21, 27, 48, 71, 110 kDa, индуцированными включением в хромосому транспозонов Tn9 и Тn5, отличаются снижением устойчивости к препаратам цефалоспоринового и фторхинолонового ряда. Инсерционный мутант с фенотипом CazS PfxR OfxR, чувствительный к цефтазидиму, полученный на основе полирезистентного варианта B. pseudomallei 57576 SMCP CazR PfxR OfxR, демонстрирует связь утраты устойчивости к антибиотику с изменением в продукции мажорных мембранных протеинов 27 и 71 kDa.
- Структурные модификации ЛПС, выражающиеся в вариации высокомолекулярных ( > 150 kDa) и редукции низкомолекулярных (25 kDa и менее) фрагментов биополимера, снижение уровня продукции экзополисахарида и секреции экстрацеллюлярных ферментов с липазной, лецитиназной и протеолитической активностью указывают на комплексные адаптивные перестройки проницаемости клеточной оболочки и систем мембранного транспорта при развитии у буркхольдерий высокого уровня устойчивости к антибиотикам фторхинолоновой и цефалоспориновой групп.
- Выявлены существенные различия в скорости накопления и количестве аккумулированного клетками штамма дикого типа и полирезистентных мутантов B. pseudomallei бромистого этидия (стуктурного аналога фторхинолоновых соединений). Установлено, что мутантные штаммы с преобладающей устойчивостью к препаратам фторхинолоновой группы обладают отчетливо меньшей проницаемостью мембран для ингибитора и максимальной скоростью его эффлюкса. Интенсивность выведения ингибитора из клеток возбудителя возрастает при повышении температуры инкубации и наличии в среде соединения - источника углерода, что свидетельствует об энергозависимом характере изученных процессов.
- Установлено, что в присутствии верапамила - блокатора мембранного транспорта наблюдается снижение устойчивости исходных и мутантных штаммов B. pseudomallei к антимикробным соединениям фторхинолоновой группы, отдельным -лактамам, аминогликозидам, макролидам и хлорамфениколу, что подтверждает значимость механизмов эффлюкса в формировании множественной антибиотикорезистентности у возбудителя мелиоидоза.
- При проведении сравнительного анализа in silico нуклеотидных последовательностей известных и предполагаемых генов лекарственного эффлюкса B. pseudomallei, B. mallei и B. thailandensis, выполненного с использованием биоинформационного программного обеспечения на основе опубликованных в Genbank последовательностей геномов буркхольдерий, были обозначены группы детерминант множественной резистентности и подобраны олигонуклеотидные праймеры для амплификации консервативных фрагментов генов лекарственных транспортеров MFS (QacA/EmrB), SMR (QacE) и RND (AcrB/AcrD/AcrF) групп.
- На основе анализа дифференциально экспрессирующихся последовательностей эффлюкс-транспортеров у исходных штаммов и полирезистентных мутантов, культивируемых в неселектвных условиях и на средах с субъингибирующими концентрациями антибиотиков фторхинолонового и цефалоспоринового рядов, установлено участие AcrB/AcrD/AcrF, QacA/EmrB и QacE детерминант в формировании антибиотикорезистентности множественного типа у видов группы «pseudomallei». Повышенный конститутивный уровень экспрессии QacA/EmrE и AcrB/AcrD/AcrF эффлюкс-транспортеров у части полирезистентных мутантов позволяет предполагать наличие генетически закрепленных нарушениий в механизмах регуляции данных последовательностей.
- Проведенное клонирование в E. coli на векторе pUC19 AcrB/AcrD/AcrF и QacE эффлюкс-транспортеров возбудителя мелиоидоза и анализ их экспрессии в рекомбинантных клонах выявили участие этих детерминант в развитии резистентности у B. pseudomallei к препаратам фторхинолоновой и аминогликозидной групп.
- Установлено, что полирезистентные мутанты B. pseudomallei и B. mallei с высоким уровнем устойчивости к антибиотикам фторхинолонового ряда несут точечные мутации в QRDR ДНК-гиразы А, приводящие к нескольким типам аминокислотных замен в последовательности белка. Показано, что замена Thr83Ile является общей для всех исследованных мутантных штаммов, тогда как замены Gly81Cys и Asp87Tyr обнаружены только у PfxRCazR и OfxRCazR мутантов B. pseudomallei. Нуклеотидная замена CT в позиции 250 gyrA, выявленная у одного из мутантов B. mallei, не приводит к аминокислотной замене в последовательности белка и может быть классифицирована как silence-мутация.
- В результате ПЦР-анализа с использованием специфических праймеров, последующего секвенирования ампликонов и исследования гомологичных фрагментов хромосом буркхольдерий in silico установлено, что геномы штаммов B. pseudomallei и B. thailandensis несут участки, структурно сходные с интегронами и представленные генами транспозаз/интеграз и кодирующими последовательностями детерминант лекарственной устойчивости - эффлюкс-транспортеров MFS и RND семейств. Наличие интегроноподобных структур свидетельствует о потенциальной возможности формирования множественной устойчивости у данных микроорганизмов за счет аккумуляции и горизонтального переноса R-детерминант различных типов.
