Изучение эффективности комбинированного метода лечения макулярного отека при сосудистых заболеваниях глаз 14. 00. 08 глазные болезни
| Вид материала | Автореферат |
- Клинико-патогенетическое обоснование комбинированного лазерно-медикаментозного лечения, 270.48kb.
- Новые подходы к исследованию хрусталика на основе комбинированного ультразвукового, 275.38kb.
- Компьютерная дистанционная термография при заболеваниях орбиты 14. 01. 07 глазные болезни, 375.35kb.
- Экспериментальное изучение эффективности клеточной трансплантации при посттравматической, 304.86kb.
- Кафедраклиническойпсихологи и темы курсовых и дипломных работ, 101.93kb.
- Рекомендации по питанию при сердечно-сосудистых заболеваниях Какие продукты питания, 110.46kb.
- Доклад посвящен вопросам создания автоматизированной системы определения параметров, 27.09kb.
- Упражнения выполняются сидя или стоя, отвернувшись от экрана при ритмичном дыхании,, 160.25kb.
- Упражнения выполняются сидя или стоя, отвернувшись от экрана при ритмичном дыхании,, 167.02kb.
- Особенности хирургического лечения псевдоэксфолиативной глаукомы и в сочетании, 279.28kb.
На правах рукописи
Шмыкова Полина Анатольевна
Изучение эффективности комбинированного метода лечения макулярного отека при сосудистых заболеваниях глаз
14. 00. 08 – глазные болезни
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
М о с к в а – 2008
Работа выполнена в Федеральном Государственном Учреждении «Межотраслевой научно-технический комплекс «Микрохирургия глаза» имени академика С.Н. Федорова Росмедтехнологии».
Научный руководитель: доктор медицинских наук, профессор
Тахчиди Христо Периклович
Официальные оппоненты: доктор медицинских наук, профессор
Семенов Александр Дмитриевич
доктор медицинских наук, профессор
Акопян Владимир Сергеевич
Ведущая организация ГУ НИИ глазных болезней РАМН
Защита состоится « ___ » _________ 2008 г. в 14 часов на заседании диссертационного совета Д.208.014.01 при ФГУ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова Росмедтехнологии» (127486, Москва, Бескудниковский бульвар, 59А).
С диссертацией можно ознакомиться в библиотеке ФГУ «Межотраслевой научно-технический комплекс «Микрохирургия глаза» им. акад. С.Н. Федорова Росмедтехнологии».
Автореферат разослан « ___ » ________ 2008 г.
Ученый секретарь
диссертационного совета,
доктор медицинских наук Агафонова В.В.
Список сокращений
ГРБ – гемато-ретинальный барьер
ДР – диабетическая ретинопатия
КС – кортикостероиды
МО – макулярный отек
ОКТ – оптическая когерентная томография
ЦВС – центральная вена сетчатки
BRVO – Branch Retinal Vein Occlusion
BVOSG – Branch Vein Occlusion Study Group
CVOSG – Central Vein Occlusion Study Group
ETDRS – Early Treatment Diabetic Retinopathy Study
VEGF – Vascular Endothelial Growth Factor
Общая характеристика работы
Актуальность проблемы. Сосудистая патология глаз занимает ведущее место среди причин инвалидности по зрению. Основная ее часть приходится на диабетическую ретинопатию и тромбозы вен сетчатки. Тромбоз вен сетчатки стоит на втором месте после диабетической ретинопатии по тяжести течения и прогнозу. Одной из основных причин снижения зрения при данной патологии является развитие макулярного отека. Частота его возникновения составляет 42% у больных диабетом I типа и более 80% - у больных диабетом II типа. По данным Gutman et al при тромбозе височных ветвей центральной вены сетчатки (ЦВС) в 60% – 100% случаев развивается макулярный отек, причем у 1/3 – 2/3 лиц он сохраняется в течение года и более, приобретая хроническое течение. В лечении макулярных отеков широко используют консервативную терапию, а также лазерную коагуляцию сетчатки [Семенов А.Д. и др.,1994, Балашевич Л.И. и др.,2002, Измайлов А.С. 2004] . Взгляд на консервативную терапию тромбоза ретинальных вен и связанного с ним макулярного отека не всегда однозначен. Кроме того, эффективность антитромботической терапии во многом зависит от этиологии, давности венозной окклюзии и типа процесса. При диабетической ретинопатии на сегодняшний день не существует лекарственных средств, эффективность которых была бы подтверждена долговременными клиническими наблюдениями. Хирургическое лечение, предпринимаемое рядом исследователей, в частности, витрэктомия при МО с наличием витреальных тракций [Lewis H et al 1992]; декомпрессия венозной ветви, радиальная оптическая нейротомия при ретинальных окклюзиях [Osterloh M.D. et al 1988, Weizer JS et al 2003] - демонстрирует перспективность данного направления, однако высок риск интраоперационных осложнений. Общепринятым методом лечения диабетического макулярного отека, эффективность которого доказана крупными исследованиями, является лазеркоагуляция сетчатки. По данным ETDRS решетчатая лазеркоагуляция сетчатки снижает риск потери зрения у 50% пациентов с диабетом. Хотя положительное действие лазеркоагуляции в лечении макулярного отека при тромбозе ретинальных вен доказано многоцентровыми исследованиями – значительного повышения остроты зрения удается достичь в небольшом проценте случаев [CVOSG 1995]. В лечении макулярных отеков широко применяются кортикостероиды. Они уменьшают выработку медиаторов воспаления, блокируют экспрессию эндотелиального фактора роста, уменьшают проницаемость гемато-ретинального барьера. Основными путями введения кортикостероидов являются парентеральный, пара- и ретробульбарный способы. В последнее время большой резонанс получила интравитреальная методика введения кортикостероидов [Martidis A, Duker JS, Greenberg PB 2002, Antcliff RJ, Spalton DJ, Stanford MR 2001]. Но существующие пути введения лекарств несовершенны в плане точности и безопасности доставки вещества к макулярной области. Так интравитриальные инъекции кортикостероидов несут определенный риск развития эндофтальмита [Jonas JB, Kreissing I Am J Ophthalmol 2006], возникновения стероидной глаукомы [Quaram PA, Gonzales CR 2006], формирование катаракты [Thompson JT 2006]. В настоящее время большинство исследователей придерживаются мнения о предпочтительности «адресной» доставки лекарственных веществ при лечении патологии заднего отрезка глаза. Существует ряд работ, показавших, что введение лекарственных веществ и биологически активных трансплантатов в субтеноново пространство является наиболее эффективным и безопасным методом лечения заболеваний сетчатки и зрительного нерва, при его относительной простоте и доступности [А.П.Нестеров, С.Н. Басинский 1991; Сидоренко Е.И. Подыниногин Н.В. 2000]. Сравнительная оценка различных методов введения лекарственных препаратов доказала преимущество субтенонового метода [Елисеева Т.О. с соавт. 2000].
Большинство исследователей сходятся во мнении, что сочетание различных методик позволит повысить эффективность лечения макулярных отеков.
Цель работы: изучить эффективность сочетания лазеркоагуляции сечатки с введением пролонгированных кортикостероидов в заднее субтеноново пространство при лечении макулярных отеков
Задачи исследования:
- В эксперименте на кроликах оценить проницаемость оболочек глаза для лекарственных средств при их субтеноновом введении
- Разработать технологию безопасного введения кортикостероидов в субтеноново пространство глазного яблока и устройство для его осуществления
- Оценить эффективность комбинированного метода лечения диабетического макулярного отека
- Оценить эффективность комбинированного метода лечения посттромботического макулярного отека
- Исследовать функциональное состояние сетчатки с использованием микропериметрии в ходе лечения макулярных отеков.
- Определить показания и противопоказания к применению комбинированного метода лечения макулярного отека при диабетической ретинопатии и тромбозе ретинальных вен
Научная новизна
Изучена проницаемость оболочек глаза в эксперименте при моделировании субтенонового и ретробульбарного введения вещества с размером молекулы, схожим с размером молекулы Дипроспана. Доказана проницаемость склеры для Дипроспана, более выраженная при субтеноновом введении препарата, чем при ретробульбарном
Впервые установлена диагностическая ценность микропериметрии для оценки функционального состояния сетчатки в центральной зоне при макулярных отеках.
Доказана эффективность комбинированного метода лечения диффузного диабетического и посттромботического неишемического макулярного отека, включающего проведение лазеркоагуляции сетчатки с последующим введением пролонгированного кортикостероида «Дипроспана» в заднее субтеноново пространство.
Практическая значимость
Определены формы тромбоза ЦВС с вторичным макулярным отеком, для которых эффективен комбинированный метод лечения.
Использование разработанного метода лечения диффузного диабетического и посттромботического неишемического макулярного отека позволяет социально реабилитировать пациентов за счет повышения остроты и качества зрения.
Разработанный способ введения препаратов в заднее субтеноново пространство и устройство для его осуществления применим в амбулаторных условиях
Относительная безопасность субтенонового введения пролонгированных кортикостероидов в сравнении с интравитреальным введением, его эффективность, а также возможность повторных инъекций позволяет рекомендовать его для широкого использования в клинической практике.
Основные положения, выносимые на защиту
Разработанный и примененный в клинике комбинированный метод лечения диффузного диабетического и посттромботического неишемического макулярного отека является эффективным.
Введение пролонгированных кортикостероидов в заднее субтеноново пространство обеспечивает адресную доставку лекарственного вещества к заднему полюсу глаза. Это позволяет создавать депо лекарственного вещества в проекции макулярного отека с постепенной его диффузией через склеру к очагу поражения.
Микропериметрические исследования могут служить критерием эффективности лечения макулярных отеков.
Внедрение в практику
Разработанные методики внедрены в практическую деятельность ФГУ МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова Росмедтехнологии»
Апробация работы
Материалы диссертации доложены и обсуждены на II Всероссийской научной конференции молодых ученых ФГУ МНТК «Микрохирургия глаза» (Москва,2007), на научно-практической конференции «Современные технологии лечения витреоретинальной патологии (Москва,2008), на клинической конференции МНТК «Микрохирургия глаза» им. академика С.Н. Федорова (Москва,2008)
Публикации
По теме диссертации опубликовано 5 печатных работ, из них 1 в центральной печати. Получен 1 патент РФ на изобретение.
Объем и структура диссертации
Диссертация изложена на 139 страницах машинописного текста и состоит из введения, обзора литературы, 4 глав собственных исследований, заключения, выводов и списка литературы. Работа иллюстрирована клиническими примерами, содержит 12 таблиц, 22 рисунка. Список литературы включает 48 отечественных и 125 иностранных источников.
Клиническая часть работы выполнена в центре лазерной хирургии (зав. отделом – к.м.н., Г.Ф. Качалина), экспериментальная часть работы выполнена в институте проблем химической физики РАН.
СОДЕРЖАНИЕ РАБОТЫ
Критерии подбора пациентов были следующие:
- наличие диффузного диабетического макулярного отека на фоне непролиферативной диабетической ретинопатии или вторичного макулярного отека в результате окклюзии ретинальных вен;
- отсутствие витреомакулярных тракций, подтвержденное ОКТ;
- отсутствие снижения прозрачности оптических сред, препятствующего осмотру глазного дна;
- отсутствие в анамнезе глаукомы или внутриглазной гипертензии
Клинико-функциональная характеристика пациентов с диабетическим МО
Обследовано 27 пациентов с диабетической ретинопатией и диабетической макулопатией в возрасте от 52 до 75 лет. У всех пациентов наблюдался двусторонний диффузный макулярный отек (54 глаза). Таким образом, в исследование включены данные 27 пациентов- 54 глаза, парные глаза которых составили контрольную группу (27 глаз). У всех пациентов была диагностирована непролиферативная диабетическая ретинопатия . Сахарным диабетом I типа страдало 10 человек (37%), сахарным диабетом II типа – 17 человек (63%). Длительность заболевания, в среднем, составила 15-20 лет.
Исходная максимально корригированная острота зрения у обследованных пациентов составила 0,1-0,5 ( в среднем 0,24+0,03). С помощью оптической когерентной томографии в программе макулярного картирования была выявлена средняя толщина сетчатки в области фовеа (в 1 мм зоне), которая составила в среднем 509+16,22 мкм в основной группе и 477+14,37 мкм в контрольной группе, а также средний объем сетчатки в макуле ( в 6мм зоне), составивший 8,92+0,1 и 8,83+0,1 соответственно. Светочувствительность сетчатки в макулярной области и точка фиксации были определены на 12 глазах основной группы пациентов. Средняя светочувствительность при заданных параметрах исследования ( паттерн, проецирующий 45 стимулов на центральную зону 10 градусов по стратегии 4-2, стимул интенсивности типа «Goldmann» III представлялся в течении 200 мсек. при фоновом освещении 1,27 cd/m2) составила 8,3+0,5 dB, стабильная фиксация была на 7 глазах, нестабильная- на 5 глазах, преимущественно центральная фиксация на 12 глазах.
Клинико-функциональная характеристика пациентов с посттромботическим МО
В исследование включены 47 пациентов (49 глаз) с тромбозом ЦВС и ее ветвей невоспалительного генеза.Среди обследованных больных было 22 мужчины (47%) и 25 женщин (53%). Возраст пациентов варьировал от 29 до 79 лет. В 27 случаях (55%) диагностирован тромбоз центральной вены сетчатки, в 22 (45%) - тромбоз ветви центральной вены сетчатки. Основную группу составили 23 глаза, на которых планировалось проведение аргоновой лазеркоагуляции сетчатки в сочетании с введением в заднее субтеноново пространство пролонгированного кортикостероида «Дипроспан». Контрольную группу составили 26 глаз, где планировалось проведение лазеркоагуляции сетчатки без субтенонового введения кортикостероида. Давность тромбоза к моменту начала комбинированного лечения составляла 1,5-6 месяцев, в среднем 3 месяца.
Максимально корригированная острота зрения у обследованных пациентов варьируя от 0,01 до 0,5, в основной группе составляла, в среднем, 0,25+0,04, в контроле 0,26+0,04. С помощью оптической когерентной томографии в программе макулярного картирования средняя толщина сетчатки в области фовеа (в 1 мм зоне) составила в среднем 548+32 мкм в основной группе и 520+20,35- в контрольной группе, а также средний объем сетчатки в макуле ( в 6мм зоне) составил 9,33+0,1 куб. мм в основной группе и 9,58+0,1 куб. мм – в контрольной. Светочувствительность сетчатки в макулярной области и точка фиксации были определены на 8 глазах основной группы пациентов. Средняя светочувствительность при заданных параметрах исследования ( паттерн, проецирующий 45 стимулов на центральную зону 10 градусов по стратегии 4-2, стимул интенсивности типа «Goldmann» III представлялся в течении 200 мсек. при фоновом освещении 1,27 cd/m2) составила 10,27+0,1 dB, стабильная фиксация была на 5 глазах, нестабильная- на 3 глазах, преимущественно центральная фиксация на 8 глазах.
Использованные методы лечения МО диабетического и посттромботического генеза
Всем пациентам в основных группах диабетического и посттромботического макулярного отека применяли комбинированный метод лечения: после проведения лазеркоагуляции сетчатки, вводили пролонгированный кортикостероид в заднее субтеноново пространство. У пациентов контрольных групп ограничивались только лазеркоагуляцией сетчатки.
Лазерное лечение диффузного диабетического макулярного отека проведена по методике «решетки». Лазерная коагуляция сетчатки выполнялась на аргоновом коагуляторе фирмы «Novus 2000 Coherent Radiation» (США) с длиной волны 514 нм, с использованием линзы Гольдмана, в амбулаторных условиях, после медикаментозного мидриаза, под местной анестезией.
Лазерные коагуляты наносились в шахматном порядке на всю зону отека сетчатки , участки ретинальной неперфузии с признаками просачивания, микроаневризмы, дилятированные капилляры и твердые экссудаты. Лазеркоагуляты наносили вне аваскулярной зоны в пределах 500 мкм от центра макулы и до двух диаметров ДЗН (3000 мкм). Расстояние между коагулятами составляло 1 диаметр коагулята. Используемые энергетические параметры: длительность импульса 0,1-0,2 сек., мощность излучения 200-300 мВт, диаметр пятна 100-200 мкм. Мощность излучения должна была обеспечить получение кремовых коагулятов на глазном дне.
Кроме того, на 4 глазах основной группы (14,8%) и 5 глазах -контрольной (18,5%) зоны ретинального отека и отложением депозитов твердого экссудата и ватообразные фокусы располагались за пределами сосудистых аркад и перипапиллярно, что явилось основанием для проведения лазеркоагуляции и в этих областях с использованием энергитических параметров: экспозиция 0,1-0,2 сек.,мощность 250-300 мВт, диаметр пятна 350-500 мкм, расстояние между коагулятами 1-2 диаметра коагулята.
Лазерное лечение макулярного отека при тромбозе ЦВС и тромбозе ветвей ЦВС.Показанием к лазеркоагуляции сетчатки у пациентов с посттромботическим МО являлось отсутствие эффекта от медикаментозной терапии с прогрессированием макулярного отека, формирование кистовидного макулярного отека с образованием микро- и макрокист, ишемическая форма тромбоза ЦВС.
Как и при диабетическом МО, проводили аргоновую лазеркоагуляцию сетчатки, которая выполнялась под местной эпибульбарной анестезией в условиях мидриаза с использованием линзы Гольдмана. Лазеркоагуляция сетчатки выполнялась по стандартной методике «решетки». Лазеркоагуляты наносились с интервалом в один коагулят в шахматном порядке в пределах всей зоны отека сетчатки, исключая 500 мкм центральной аваскулярной зоны. Мощность излучения соответствовала получению коагулятов умеренной интенсивности. Длина волны излучения 514 нм, экспозиция 0,1 сек., диаметр пятна облучения 100-200 мкм, мощность 200-300 мВт.
В случаях тромбоза ветви ЦВС при длительно существующем ретинальном отеке (14глаз, 63,6%) одномоментно с «решеткой» была выполнена секторальная лазеркоагуляция сетчатки в области, соответствующей тромбированной вене диаметром пятна 200-500 мкм, экспозицией 0,1 сек., мощностью излучения 150-300 мкм . Расстояние между умеренно интенсивными коагулятами составляло 1/2 -1 их диаметра.
В случаях полного тромбоза ЦВС (6 глаз, 12,2% случаев) с обширными зонами ретинальной неперфузии помимо решетчатой лазеркоагуляцией в макулярной области, выполнялась панретинальная лазеркоагуляция сетчатки до преэкваториальной зоны глазного дна диаметром пятна облучения 350-500 мкм, длительностью облучения 0,1-0,2 сек., мощностью излучения 150-400 мВт. Расстояние между умеренно интенсивными коагулятами было в пределах 1/2 их диаметра. Панретинальную лазеркоагуляцию выполняли в 4 этапа с интервалом 2-4 недели.
Техника введения пролонгированного кортикостероида «Дипроспан» в заднее субтеноново пространство.
Субтеноновое введение препарата осуществляли в условиях операционной.
После проведения эпибульбарной анестезии 0.5% раствором дикаина( 3-х кратное закапывание анестетика в конъюнктивальную полость), стандартной обработки операционного поля и наложения векорасширителя, пациент фиксировал взор в направлении вниз и к носу. Под операционным микроскопом в верхненаружном секторе в 10 мм от лимба конъюнктивальными ножницами производили разрез конъюнктивы с подлежащей теноновой оболочкой. Специальную канюлю для субтеноновых инъекций, соединенную со шприцом, содержащим препарат, аккуратно продвигали к заднему полюсу глаза, к проекции макулярной области. Затем вводили 0,5 мл «Дипроспана», канюлю извлекали. Края раны сопоставляли, под конъюнктиву вводили 0,3 мл гентамицина. В течение недели после операции всем пациентам назначалась инстилляция антисептических капель «Витабакт» по 1 капле 3 раза в день.
Экспериментальное исследование проницаемости структур глаза при субтеноновом введении лекарственных веществ
Проницаемость оболочек глаза для лекарственных веществ была оценена методами спектрофотометрии и флюорометрии. В связи с тем, что используемый нами пролонгированный кортикостероид «Дипроспан» для субтенонового введения, обладает низкой эмиссионной способностью, что не позволяет определить его спектры поглощения и флюоресценции в образцах тканей и стекловидном теле- для эксперимента был выбран раствор флюоресцина. Работами ряда исследователей было доказано, что проницаемость склеры во многом зависит от молекулярного веса вещества: чем он выше, тем ниже проницаемость ( Boubriak O.A. с соавт. 2000г., Hamalainen K.M. с соавт. 1997г.). Между тем, другие авторы пришли к выводу, что размер и форма молекулы вещества в большей степени определяет проницаемость склеры, чем молекулярный вес ( Ambati J с соавт. 2000г). Учитывая тот факт, что молекулы «Дипроспана» и флюоресцеина схожи, то результат проницаемости флюоресцеина наиболее приближен к проницаемости «Дипроспана». Флюоресцеин является выраженным люминофором, что позволяет определять его электронные спектры поглощения и спектры флюоресценции. Экспериментальная работа выполнялась на 6 глазах 3 кроликов породы шиншилла весом 2,0-2,5 кг. После эпибульбарной анестезии в правые глаза животных было введено 0,3 мл 10% флюоресцина в заднее субтеноново пространство, а в левые- такое же количество ретробульбарно. Через 1 час осуществляли забор глаз с последующим выделением образцов склеры и комплекса хориоидея-сетчатка в области заднего полюса глаза, а также стекловидное тело путем аспирации шприцом (время забора материала рассчитывалось из соображений, что при внутривенном введении флюоресцина, он выводится из организма через кровоток через 30 минут, таким образом, определяемый в тканях глаза препарат через 1 час, предположительно, диффундирует через склеру из субтенонового пространства.
Электронные спектры поглощения были измерены на спектрофотометре “Specord M-40”, а спектры флюоресценции – на приборе “Элюмин 2М”.
Для снятия спектров стекловидного тела использовали кварцевые кюветы с длиной оптического пути l=1см, растворитель – дистиллированную воду.
Микропипеткой отбирали 40 мкл стекловидного тела и разбавляли 2 мл дистиллированной воды, затем снимали спектры поглощения и флюоресценции. Предварительно, для сравнения снимали спектры поглощения и флюоресценции чистого раствора флюоресцеина, который разбавляли в 2.105 раз.
Выделенные образцы склеры и комплекс хориоидея-сетчатка наносили на препаративные стекла и снимали спектры флюоресценции.
Из соотношения спектров флюоресценции стекловидного тела при разных способах введения флюоресцина выявлено, что при ретробульбарном введении достигаемая в стекловидном теле концентрация флюоресцина ~ в 15 раз меньше, чем при субтеноновом введении.
Сравнение спектров свидетельствует о том, что при ретробульбарном способе введения флюоресцина его содержание в образцах на порядок меньше, чем при субтеноновом способе введения флюоресцеина.
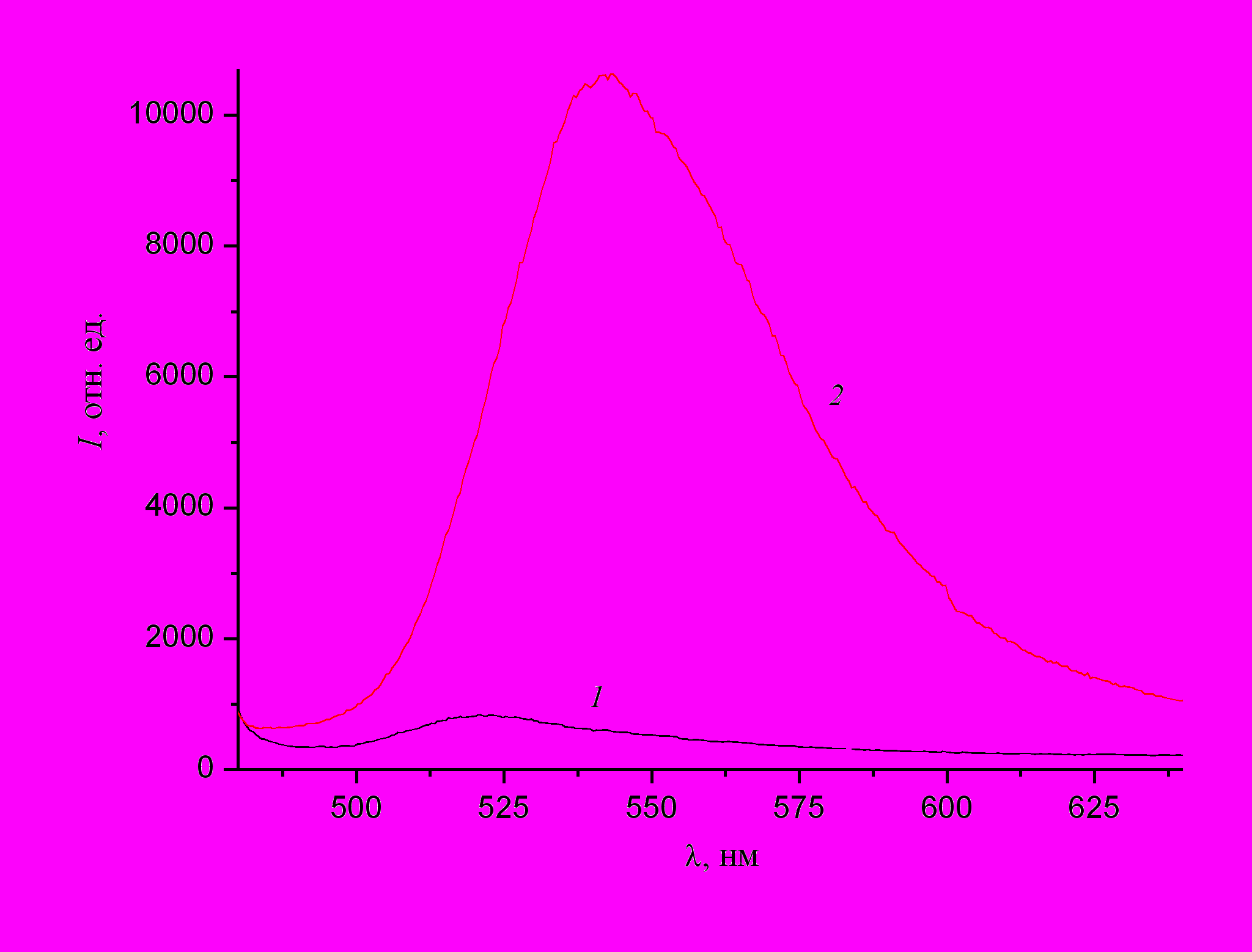

Рис.1 Спектры флюоресценции образцов Рис. 2 Спектры флюоресценции склеры при введении флюоресцеина комплекса хориоидея-сетчатка
разными способами: при введении флюоресцеина
разными способами:
1 – ретробульбарное введение, 1 – ретробульбарное введение,
2 – субтеноновое введение 2 – субтеноновое введение
Разработка инъекционной амбулаторной методики введения кортикостероидов в заднее субтеноново пространство и устройства для его осуществления.
Для возможности осуществления процедуры субтенонового введения кортикостероидов менее инвазивно (не с формированием разрезов, а через прокол конъюнктивы и подлежащей теноновой оболочки) и в амбулаторных условиях- нами было разработано специальное устройство «шприц-канюля», которая представляет собой упруго-эластичную трубку для введения в заднее субтеноново пространство лекарственных средств, содержащее шприц и инъекционную иглу, размещенную в трубке, при этом рабочая часть иглы изогнута по радиусу, соответствующему радиусу кривизны глазного яблока, а на головке инъекционной иглы установлена большим диаметром к шприцу цилиндрическая ступенчатая втулка, внутренняя поверхность которой конгруэнтна внешней поверхности головки иглы, при этом на внешней цилиндрической поверхности втулки с меньшим диаметром выполнена резьба, втулка снабжена крышкой с внутренней резьбой, а трубка выполнена над осевым отверстием крышки и заодно с ней, рабочий конец трубки оплавлен.
Способ доставки лекарственных средств к заднему полюсу глаза с использованием «шприца- канюли» заключается в следующем: после инстилляции раствора анестетика в конъюнктивальную полость, конъюнктиву с подлежащей теноновой оболочкой фиксируют хирургическим пинцетом, отступя 10мм от лимба в нижненаружном сегменте глазного яблока, затем прокалывают конъюнктиву и подлежащую тенонову оболочку концом изогнутой рабочей части инъекционной иглы устройства и вводят раствор анестетика, который находится в одном шприце с лекарственным средством, затем конец инъекционной иглы убирают внутрь трубки путем поворота крышки втулки и трубку продвигают по поыерхности склеры в заднее субтеноново пространство в направлении макулярной области, после чего вводят лекарственное средство, затем трубку извлекают из субтенонова пространства и в конъюнктивальную полость закапывают глазные капли с антибиотиком.

Рис.3 Шприц-канюля для введения лекарственных веществ в заднее субтеноново пространство
Оценка эффективности лечения макулярного отека при диабетической ретинопатии
В результате проведенного лечения и в основной и контрольной группах офтальмоскопически и по данным ФАГ было отмечено уменьшение количества микроаневризм, исчезновение или уменьшение геморрагий, частичная или ,в ряде случаев, полная резорбция депозитов экссудата, уменьшение зон ишемии и ретинального отека.
Динамика максимально корригированной остроты зрения на глазах с диффузным макулярным отеком в основной и контрольной группах представлена в табл. 1.
Таблица 1
Динамика максимально корригированной остроты зрения на глазах с диабетическим МО до и после лечения
| Сроки наблюдения | Острота зрения | |
| Основная группа (М+m) n=27 | Контрольная группа (М+m) n=27 | |
| До лечения | 0,24+0,03 | 0,25+0,03 |
| 1 мес. | 0,41+0,04 | 0,40+0,04 |
| 3 мес. | 0,42+0,05 | 0,39+0,04 |
| 6 мес. | 0,42+0,04 | 0,38+0,04 |
| 9 мес. | 0,41+0,03 | 0,37+0,04 |
| 1 год | 0,50+0,03 | 0,37+0,04* |
* разница статистически достоверна р<0,05 в группах сравнения
Анализ средних по группе значений толщины сетчатки в центральной зоне сетчатки до и после проведенного лечения отражен в табл. 2.
Таблица 2
Динамика изменения толщины сетчатки в центральной зоне у пациентов с диабетическим МО
| Сроки наблюдения | Толщина сетчатки в центральной зоне, мкм | |
| Основная группа (М+m) n=27 | Контрольная группа (М+m) n=27 | |
| До лечения | 509+16,22 | 477+14,37 |
| 1 мес. | 400+14,26 | 460+14,68* |
| 3 мес. | 390+16,40 | 416+13,95 |
| 6 мес. | 358+16,99 | 416+13,64* |
| 9 мес. | 343+11,58 | 422+14,12* |
| 12 мес. | 301+8,53 | 435+13,03* |
* разница статистически достоверна р<0,05 в группах сравнения
Кроме того, полученные с помощью ОКТ данные объема сетчатки в макуле (в 6мм зоне) позволили оценить динамику уменьшения МО не только в фовеа, но и на всем его протяжении. Анализ средних значений объема сетчатки в макуле до и после проведенного лечения выявил следующие результаты, которые отражены в табл. 3.
Таблица 3
Динамика изменения объема сетчатки в макуле у пациентов с диабетическим МО
| Сроки наблюдения | Объем сетчатки в макуле, мм³ | |
| Основная группа (М+m) n=27 | Контрольная группа (М+m) n=27 | |
| До лечения | 8,92+0,1 | 8,83+0,1 |
| 1 мес. | 8,14+0,07 | 8,21+0,07 |
| 3 мес. | 7,64+0,09 | 7,93+0,09* |
| 6 мес. | 7,23+0,1 | 7,75+0,1* |
| 9 мес. | 7,11+0,09 | 7,54+0,05* |
| 12 мес. | 6,52+0,05 | 7,32+0,07* |
* разница статистически достоверна р < 0,05 в группах сравнения
Результаты лечения диабетического МО по данным микропериметрии.
Как известно, длительно существующий макулярный отек может привести к необратимому повреждению фоторецепторов и нарушению функции пигментного эпителия сетчатки. Используемый нами метод микропериметрии позволил оценить функциональное состояние сетчатки на момент начала лечения, выявить степень снижения светочувствительности сетчатки в зоне макулярного отека, проследить динамику изменения светочувствительности сетчатки в ходе лечения. Кроме того, микропериметрия позволила объяснить низкие зрительные функции у пациентов, по данным ОКТ у которых отмечалось уменьшение толщины сетчатки в макулярной зоне, а по данным ФАГ – уменьшение диффузии красителя. Данное исследование было проведено на 12 глазах основной группы. Светочувствительность измерялась по 20 бальной шкале в dВ в центральной зоне 10º, и расценивалась как умеренно сниженная при значениях от 15dВ до 8dВ , а при значениях меньше 8dВ – выраженно сниженная.
Анализ характера фиксации (стабильная, нестабильная) выявил более высокие зрительные функции у пациентов со стабильной фиксацией.
Среднее значение светочувствительности сетчатки в макулярной области до лечения (n=12) составило 8,3+0,5dB. После проведения лазеркоагуляции сетчатки с субтеноновым введением «Дипроспана» уже на 7–е сутки отмечалось повышение светочувствительности в среднем на 2–4dB большинства тестируемых точек. Среднее значение светочувствительности в макулярной области в раннем послеоперационном периоде составило 11,0+0,8dB. На протяжении дальнейшего периода наблюдения (поздний послеоперационный период) отмечалось постепенное улучшение. Среднее значение светочувствительности в макулярной области в позднем послеоперационном периоде приблизилось к нормальным значениям и составило 13,2+1,7dB.
На 4 глазах с нестабильной фиксацией в отдаленном послеоперационном периоде было отмечено появление стабильной фиксации.
В случаях отсутствия повышения остроты зрения после проведенного лечения при положительной динамике по другим методам исследования, в том числе оптической когерентной томографии – были выявлены низкие показатели средней светочувствительности сетчатки в макулярной области (< 10 dB) при заданных параметрах исследования, что было расценено нами как необратимое повреждение фоторецепторов и снижение функциональной активности пигментного эпителия сетчатки.
Особенности комбинированного лечения диабетического МО
Необходимо отметить, что в основной группе с диабетическим МО всем пациентам было выполнено повторное введение Дипроспана на разных сроках наблюдения в течение 1 года, а пяти пациентам провели 3 инъекции.
Основанием для повторного введения кортикостероида являлась отрицательная динамика по данным ОКТ и ФАГ. На сроке наблюдения до 3–х месяцев повторное введение «Дипроспана» сделали 7 пациентам (26% случаев), на сроке наблюдения 5–6 месяцев– 9 пациентам (33% случаев) повторное введение, 3 пациентам (11%случаев)– провели 3–е введение. На сроке наблюдения 7–9 месяцев 11 пациентам (40,7% случаев) – сделали 2–е введение кортикостероида и 2 пациентам (7% случаев)– 3–е введение.
Таким образом, совокупность полученных результатов свидетельствует о большей эффективности комбинированного метода лечения диффузного диабетического макулярного отека, включающего введение пролонгированного кортикостероида «Дипроспана» в заднее субтеноново пространство после проведения лазеркоагуляции сетчатки по сравнению с лазеркоагуляцией без субтенонового введения кортикостероида на что указывают следующие данные:
- больший процент стабилизации и улучшения остроты зрения (89% и 55,5%, соответственно);
- через 1 год после проведенного лечения толщина сетчатки в центре уменьшилась в среднем на 40,8% по сравнению с данными до начала лечения в основной группе и на 8,8%– в группе контроля;
- более выраженное снижение объема сетчатки в макуле было достигнуто в основной группе по сравнению с контрольной;
- повышение светочувствительности сетчатки в макулярной области в среднем на 2–4dB большинства тестируемых точек и улучшение характера фиксации уже на 7–е сутки после проведенного лечения по данным микропериметрии
Оценка эффективности комбинированного лечения макулярного отека при тромбозе ретинальных вен
В результате проведенного лечения и в основной и контрольной группах в отдаленном периоде офтальмоскопически и по данным ФАГ было отмечено: границы диска зрительного нерва приобрели четкие контуры, «мягкий экссудат» и большинство кровоизлияний частично или полностью резорбировались. В случаях ишемического тромбоза центральной вены сетчатки значительно уменьшилась или полностью прошла отечность диска и перипапиллярной сетчатки, в зонах ишемии имела место облитерация сосудов. Следует отметить, что ни в одном случае ишемического тромбоза центральной вены сетчатки и в основной и в контрольной группах в отдаленном периоде не было отмечено формирования неоваскуляризации сетчатки и угла передней камеры. Ретинальные вены стали менее извиты и менее расширены. Восстановление ретинального кровотока происходило путем либо реканализации тромбированного сосуда, либо формированием коллатералей. Более выраженная положительная динамика, как офтальмоскопическая, так и ангиографическая была отмечена у пациентов основной группы. Так, формирование ламеллярного центрального разрыва было отмечено на 2 глазах (7,9% случаев) контрольной группы и ни в одном случае – в основной.
Динамика максимально корригированной остроты зрения на глазах с посттромботическим макулярным отеком в основной и контрольной группах представлена в табл. 4.
Таблица 4
Динамика максимально корригированной остроты зрения до и после лечения у пациентов с посттромботическим МО
Сроки наблюдения | Острота зрения | |
| Основная группа (М+m) n=23 | Контрольная группа (М+m) n=26 | |
| До лечения | 0,25+0,04 | 0,26+0,04 |
| 1 мес. | 0,46+0,06 | 0,32+0,04 |
| 3 мес. | 0,49+0,07 | 0,32+0,04 |
| 6 мес. | 0,52+0,07 | 0,33+0,04* |
| 9 мес. | 0,55+0,07 | 0,37+0,05* |
| 12 мес. | 0,56+0,07 | 0,38+0,05 |
* разница достоверна р<0,05 в группах сравнения
Улучшение максимально корригированной остроты зрения в раннем и отдаленном послеоперационним периоде было отмечено у 7 пациентов с неишемическим тромбозом центральной вены сетчатки (30,4% случаев) и у 13 пациентов с тромбозом ветви центральной вены сетчатки (56,5% случаев). Наибольшей остроты зрения удалось достичь в группе тромбоза ветви ЦВС по сравнению с группой тромбоза ЦВС.
Динамика изменения толщины сетчатки толщины сетчатки в центральной зоне до и после проведенного лечения отражен в табл. 5.
Таблица 5
Динамика изменения толщины сетчатки в центральной зоне у пациентов с посттромботическим МО
| Сроки наблюдения | толщина сетчатки в центральной зоне, мкм | |
| Основная группа (М+m) n=23 | Контрольная группа (М+m) n=26 | |
| До лечения | 548+32 | 520+20,35 |
| 1 мес. | 417+20 | 484+18,33* |
| 3 мес. | 390+21 | 465+15,72* |
| 6 мес. | 356+19 | 437+15,17* |
| 9 мес. | 342+18 | 430+16,98* |
| 12 мес. | 339+18 | 410+15,58* |
* разница статистически достоверна р<0,05 в группах сравнения
Уменьшение объема сетчатки в макуле (в 6мм зоне) происходило параллельно с резорбцией МО. Анализ средних значений объема сетчатки в макуле до и после проведенного лечения представлен в табл. 6.
Таблица 6
Динамика изменения объема сетчатки в макуле у пациентов с посттромботическим МО
| Сроки наблюдения | объем сетчатки в макуле, мм³ | |
| Основная группа (М+m) n=23 | Контрольная группа (М+m) n=26 | |
| До лечения | 9,33+0,1 | 9,58+0,1 |
| 1 мес. | 8,62+0,1 | 9,01+0,05* |
| 3 мес. | 7,84+0,05 | 8,82+0,01* |
| 6 мес. | 7,51+0,04 | 8,04+0,01* |
| 9 мес. | 7,37+0,04 | 7,81+0,04* |
| 12 мес. | 6,78+0,05 | 7,20+0,04* |
* разница статистически достоверна р<0,05 в группах сравнения
До лечения наибольшая толщина сетчатки в центральной зоне была при ишемическом тромбозе ЦВС 729+102мкм, а при неишемическом тромбозе ЦВС и тромбозе ветви ЦВС, практически, одинаковая 522+49мкм и 521+39мкм. В отдаленном периоде наблюдения толщина сетчатки в центральной зоне уменьшилась в среднем на 40,7% при ишемическом тромбозе ЦВС, на 38,9%– при неишемических тромбозах ЦВС и на 37%– при тромбозе ветви ЦВС.
Полученные данные свидетельствуют о том, что, несмотря на практически одинаковый процент уменьшения толщины сетчатки в центральной зоне к году наблюдений, заметного улучшения остроты зрения удалось достичь только при неишемических тромбозах ЦВС и тромбозах ветви ЦВС. Низкая острота зрения у пациентов с ишемическими формами ретинального тромбоза была расценена нами как результат распространенной ретинальной ишемии, приводящей к необратимому поражению внутренних слоев сетчатки. Таким образом, длительность существования макулярного отека, вызывающего необратимые нарушения функции фоторецепторов и пигментного эпителия сетчатки у пациентов с ретинальным тромбозом– играет превалирующую роль в зрительном прогнозе у пациентов с неишемическими формами тромбоза.
Выраженные функциональные нарушения сетчатки в макулярной области у пациентов с макулярным отеком при ишемическом тромбозе ЦВС на фоне положительной динамики по данным ОКТ были подтверждены данными микропериметрии.
Результаты микропериметрического исследования у пациентов с посттромботическим МО.
Данное исследование было проведено на 8 глазах основной группы. Из них на 2 глазах был ишемический тромбоз центральной вены сетчатки, на 4 глазах – тромбоз ветви центральной вены сетчатки и на 2 глазах – неишемический тромбоз центральной вены сетчатки. Среднее значение светочувствительности сетчатки в макулярной области до лечения (n=8) составило 10,27+0,1dB. После проведения лазеркоагуляции сетчатки с субтеноновым введением «Дипроспана» уже на 7–е сутки отмечалось повышение светочувствительности в среднем на 2–4dB большинства тестируемых точек. Среднее значение светочувствительности в макулярной области в раннем послеоперационном периоде составило 11,43+0,1dB. На протяжении дальнейшего периода наблюдения (поздний послеоперационный период) по мере уменьшения макулярного отека отмечалось постепенное улучшение. Среднее значение светочувствительности в макулярной области в позднем послеоперационном периоде 12,25+0,4 dB. Характер фиксации в отдаленном периоде наблюдения остался нестабильным на 2 глазах с ишемическим тромбозом центральной вены сетчатки и приобрел стабильный характер на 1 глазу с тромбозом ветви центральной вены сетчатки.
Особенности комбинированного лечения посттромботического МО.
Необходимо отметить, что в основной группе с посттромботическим МО 4 пациентам через 5 месяцев после проведенного лечения было произведено повторное введение Дипроспана. Основанием для повторного введения кортикостероида явилась отрицательная динамика по данным офтальмоскопии и ОКТ.Введение кортикостероида в заднее субтеноново пространство все пациенты перенесли хорошо, без болевых ощущений. Ни в одном случае не было отмечено повышения артериального давления после введения. На 1 глазу (4,3% случаев) в раннем послеоперационном периоде наблюдалось повышение ВГД на 5мм.рт.ст. Офтальмогипертензия купировалась назначением гипотензивных капель.
Совокупность полученных результатов свидетельствует о большей эффективности комбинированного метода лечения посттромботического макулярного отека, включающего введение пролонгированного кортикостероида «Дипроспана» в заднее субтеноново пространство после проведения лазеркоагуляции сетчатки по сравнению с лазеркоагуляцией без субтенонового введения кортикостероида на что указывают следующие данные:
- больший процент стабилизации и улучшения остроты зрения (95% и 67,6%, соответственно);
- через 1 год после проведенного лечения толщина сетчатки в центре уменьшилась в среднем на 38,1% по сравнению с данными до начала лечения в основной группе и на 21,2%– в группе контроля;
- более выраженное снижение объема сетчатки в макуле было достигнуто в основной группе по сравнению с контрольной;
- повышение светочувствительности сетчатки в макулярной области в среднем на 2–4dB большинства тестируемых точек на 7–е сутки после проведенного лечения по данным микропериметрии;
Выявлены характерные особенности резорбции посттромботического макулярного отека в ходе комбинированного лечения и установлена малая эффективность данной методики при ишемических формах ретинального тромбоза.
Вышеприведенные данные позволили нам сформулировать следующие показания и противопоказания к проведению комбинированного метода лечения, сочетающего аргоновую лазеркоагуляцию сетчатки с введением пролонгированного кортикостероида «Дипроспан» в заднее субтеноново пространство. Показанием к данному способу лечения является диффузный диабетический макулярный отек, макулярный отек при неишемическом тромбозе центральной вены сетчатки и ее ветвей. К противопоказаниям следует отнести некомпенсированный сахарный диабет, глазную гипертензию и недостаточную прозрачность оптических сред.
Выводы
- В результате изучения проницаемости оболочек глаза в эксперименте установлено, что проницаемость склеры для Дипроспана более выражена при субтеноновом введении препарата, чем при ретробульбарном;
- Разработанная технология и устройство введения кортикостероидов в субтеноново пространство глазного яблока может использоваться в амбулаторных условиях;
- Применение комбинированного метода лечения диабетического макулярного отека позволяет достичь повышения остроты зрения в 89% и ее стабилизации в 78% случаев на сроке наблюдения 1 год;
- Применение комбинированного метода лечения посттромботического макулярного отека позволяет достичь повышения остроты зрения в 78% и ее стабилизации в 95% случаев на сроке наблюдения 1 год;
- Микропериметрические исследования позволяют в ходе лечения оценить в динамике функциональное состояние макулярной области и служить критерием эффективности лечения;
- Сформулированны показания и противопоказания к применению комбинированного метода лечения макулярного отека при диабетической ретинопатии и тромбозе ретинальных вен позволяют внедрить разработанную технологию в клиническую практику.
Практические рекомендации
- Для эффективного лечения диабетического и посттромботического МО рекомендовано применение комбинированного метода лечения, сочетающего аргоновую лазеркоагуляцию сетчатки с последующим введением пролонгированного кортикостероида «Дипроспан» в заднее субтеноново пространство;
- Введение пролонгированного кортикостероида «Дипроспан» в субтеноново пространство проводится после лазеркоагуляции сетчатки в тот же день (в операционной, либо разработанным оригинальным устройством в амбулаторных условиях);
- При лечении диабетического МО повторные введения кортикостероида определяются индивидуально при отсутствии положительной динамики;
- Для оценки эффективности лечения и прогноза зрительных функций в процессе лечения целесообразно использование в комплексе методов ОКТ и микропериметрии. В случае отсутствия повышения светочувствительности сетчатки в макулярной области на фоне положительной динамики по данным ОКТ - прогноз улучшения зрительных функций неблагоприятный;
- Комбинированный метод лечения МО при ишемическом тромбозе ЦВС по эффективности не отличается от известных методов лечения;
- В раннем послеоперационном периоде необходим контроль артериального давления и внутриглазного, а у пациентов с диабетом – контроль уровня сахара крови.
Список публикаций
- Шмыкова П.А. Микропериметрия как метод оценки функционального состояния сетчатки при лечении диабетического макулярного отека // XXIX Итоговая конференция молодых ученых МГМСУ Сб.научн.работ. - М.- 2007.- С. 272-273
- Шмыкова П.А. Комбинированный метод лечения диабетического макулярного отека // Актуальные проблемы офтальмологии. II Всероссийская конференция молодых ученых: 2-я Сб.научн.работ. - М.- 2007.- С. 194-196
- Магарамов Д.А., Шмыкова П.А.,Будыка М.Ф. Экспериментально-клиническое обоснование метода субтенонового введения кортикостероидов при лечении макулярных отеков // «Современные технологии лечения витреоретинальной патологии» Сб.научн.работ.- М.- 2008.- С. 115-117
- Тахчиди Х.П., Магарамов Д.А., Пантелеев Е.Н., Шмыкова П.А. Предварительные результаты комбинированного метода лечения макулярного отека при тромбозе центральной вены сетчатки и ее ветвей // Офтальмохирургия №2.- М.- 2008- С. 20-23
- Магарамов Д.А., Шмыкова П.А. Новый инъекционный способ введения лекарственных средств в субтеноновое пространство при лечении патологии сетчатки // 3-ий Всероссийский семинар – «круглый стол» «Макула-2008». Тезисы докладов, стенограммы обсуждения и дискуссий.-Ростов-на-Дону.-2008.
Список изобретений
- Магарамов Д.А., Шмыкова П.А., Латыпов И.А. Устройство для доставки лекарственных средств к заднему полюсу глаза и способ доставки лекартсвенных средств к заднему полюсу глаза. Заявка № 2007101209/14 от 16.01.2007
Шмыкова Полина Анатольевна родилась в 1977 году в Москве. В 2000 году с отличием окончила лечебный факультет Московского Государственного Медико-Стоматологического Университета. С 2000 по 2002 гг. проходила обучение в клинической ординатуре на кафедре глазных болезней МГМСУ на базе ФГУ МНТК «Микрохирургия глаза» имени акад. С.Н. Федорова. С 2002 по 2008 гг. обучалась в очной аспирантуре на кафедре глазных болезней МГМСУ на базе Центра Лазерной хирургии ФГУ МНТК «Микрохирургия глаза» имени акад. С.Н. Федорова.
