Урок обобщения и систематизации знаний
| Вид материала | Урок |
СодержаниеИспользуемое оборудование 2. Решение упражнений и задач. 2. «Мои соседи». |
- Урок обобщения и систематизации знаний учащихся по роману Ф. М. Достоевского «Преступление, 66.68kb.
- Урок алгебры в 8 классе с применением информационных технологий по теме «Решение квадратных, 94.17kb.
- Урока: урок обобщения и систематизации знаний, 141.29kb.
- Урока: Урок обобщения и систематизации знаний по теме «Тригонометрические уравнения», 105.27kb.
- Урок обобщения, систематизации и проверки знаний по теме «Южная Америка», 104.29kb.
- О. М. Дроздова Тип урока: урок обобщения и систематизации. Тема: урок, 287.51kb.
- Конспект урока физики в 10 классе По теме: «Тепловые двигатели и их роль в жизни человека», 37.82kb.
- Рыбицкая Светлана Николаевна урок, 89.87kb.
- Панова Людмила Валентиновна моу «Большегривская сош» урок, 48.23kb.
- Задачи: рассмотреть специфику поэтики Б. Пастернака на примере конкретных произведений,, 275.35kb.
УРОК ОБОБЩЕНИЯ И СИСТЕМАТИЗАЦИИ ЗНАНИЙ
Цель урока: Обобщить и систематизировать изученный материал по темам «Строение атома. Структура Периодической системы».
Актуализировать знания учащихся о строении атома, структуре ПС, закономерности изменения свойств химических элементов. Формировать научное мировоззрение. Прививать любовь к предмету.
Тип урока: Урок обобщения и систематизации знаний
Используемые учебники и учебные пособия:
Новошинский И.И. Новошинская Н.С. Химия 8 класс
Используемое оборудование:
ПС, презентация, мультимедийное устройство, карточки с тестовыми заданиями.
Методы: беседа, фронтальная самостоятельная работа по вариантам, индивидуальная работа у доски, тестовые работы по вариантам
Ход урока:
1. Организационный момент.
Здравствуйте, садитесь.
Прошу открыть ваши тетради и записать тему урока. (Слайд 1)
Сегодня мы обобщаем и систематизируем все те знания, которые вы получили при прохождении двух предыдущих тем (Слайд 2)
Целью нашего урока будет вспомнить некоторые понятия названных тем, такие как «строение атома», «химический элемент», «валентные электроны», структуру ПСХЭ, определять с ее помощью некоторые характеристики и свойства атомов.
2. Решение упражнений и задач.
А начнём повторение мы с одной из самых крохотных частичек мироздания – атома. Его строения. (Слайд 3)
Задание № 1
А) на интерактивной доске:
Вставьте пропущенные слова.
Место химического элемента в периодической системе определяется количеством ____________ в ядре атома
2. Весь положительный заряд и почти вся масса атома сосредоточена в его ____________ .
3. Ядро имеет ___________________ заряд и состоит из
________________ и __________________.
4. Сумма чисел протонов и нейтронов соответствует
___________________________________ элемента.
5. Изотопами называют разновидности атомов с одинаковым количеством _________________, но разным количеством ___________________ в ядре атома.
6.Свойства химических элементов определяются числом ___________, находящихся на ___________________ ___________________________________
Б) фронтально: «Верю – не верю»
Ребята, вам предлагаются пять утверждений о внутреннем строении атома. Вы вправе верить им или нет. Ваша задача в тетради напротив номера утверждения, с которым вы согласны, поставить значок «+», а где не согласны «-».
Утверждения:
1.Только электроны входят в состав атома.
2.Электроны - отрицательно заряженные частицы.
3.Количество нейтронов и электронов одинаковое.
4.Относительная атомная масса равна количеству электронов.
5.Заряд ядра зависит от количества протонов.
А теперь поменяйтесь тетрадями с соседом. Внимание на экран (Слайд 4). На нём появились ответы. Сверьтесь и оцените работу. Количество правильных ответов совпадает с оценкой.
Ответы:
Нет
Да
Нет
Нет
Да
Объясните, почему высказывания 1, 3 и 4 неверны? (С места 1 – 2 ученика)
А что такое «химический элемент»? (Это определённый вид атомов)
Задание № 2
Давайте повторим произношение знаков химических элементов (Слайд 5)
А теперь проверим ваше химическое зрение
Назовите по очереди химические элементы: (с места 3 человека) (Слайд 6)
H C S P O
Cu K Zn N CL
Al Na Li Si F
Задание № 3
Вспомним строение атома. На доске изобразить строение атомов №6 и № 14, в классе по вариантам №11 и № 17 (Слайд 7)
Сравните строение атомов этих химических элементов.
Ребята, когда вы изображали строение атомов, вы указывали количество валентных электронов. Какие электроны мы называем валентными?
Задание № 4
Назовите валентные электроны, используя формулы электронных конфигураций, следующих атомов. (ЦОР - фронтально)
Задание № 5
2. Ниже приведены схемы строения атомов некоторых химических элементов. Какие из них относятся к атомам металлов, какие — к атомам неметаллов? (Слайд 8)
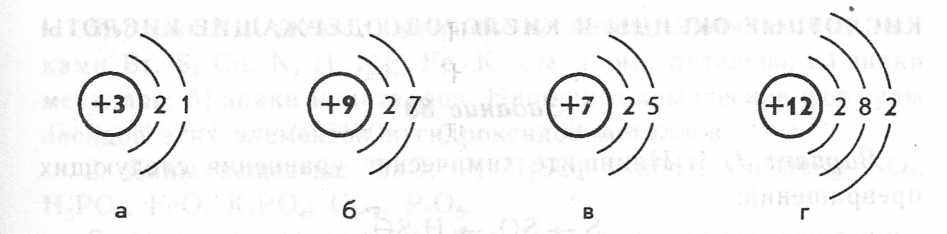

Распределите химические элементы, знаки которых приведены ниже, на две группы — металлы и неметаллы: S, Na, Р, Fe, N, Ag, А1, С, Ni (на доске)
Si, CI, К, Br, Си, I, Ca, O, Zn. (фронтально)(Слайд 9)
Задание № 6
На следующем этапе мы обратимся к Периодической таблице, но для этого мы должны вспомнить её строение. (Слайд 10)
Посмотрите внимательно на Периодическую систему. Она вся поделена на клетки горизонтальными и вертикальными рядами. Как мы их называем? Расскажите мне о них поподробнее, используя план ответа на экране. (К ПС вызываются по одному 2 человека)
План ответа:
Определение.
Количество в периодической системе.
Деление на составляющие (какие?).
Как их найти?
Как обозначаются?
Физический смысл.
Задание № 7
Найди элемент в периодической системе: (Слайд 11)
1. Это было известно еще до нашей эры. Правитель Персии Кир (2500 лет до н.э.) в военных походах питьевую воду сохранял в сосудах из этого металла.
...в Древней Индии накаленные стержни этого металла погружали в воду и потом ее использовали для обмывки ран, вода, приобретала лечебные свойства: в ней погибали микроорганизмы. Этот металл располагается в 4 периоде 1 группе побочной подгруппы, назовите его. (серебро)
2.Элемент находится в главной подгруппе VII группы 3 периода. Вещество, состоящее из атомов этого элемента, применяют для обеззараживания питьевой воды и уничтожения полевых грызунов. (хлор)
3. Недостаток селена в организме приводит к выпадению шерсти у овец, появлению уродливой формы копыт и рогов у сельскохозяйственных животных и, поэтому, добавляется в рацион животных при возникновении названных отклонений в их развитии. Он находится 4 периоде 6 группе главной подгруппе. (Селен)
4. Для повышения урожайности томатов в качестве удобрения применяют соединения элемента электронная конфигурация атома которого1S2 2S22р3. Определите, какой это элемент. (Азот)
5. Элемент, являющийся необходимой составляющей костей и зубов
имеет строение внешнего энергетического уровня: 2s22p5? (фтор)
Задание № 8
А) Найди соответствие (на интерактивной доске) (Слайд 12)
Ниже указаны сведения, полученные исходя из периодической системы химических элементов. Подберите те, которые тесно связаны друг с другом. Покажите эти связи в виде стрелок между данными списками
1) порядковый номер элемента,
2) число энергетических уровней в атоме,
3) число электронов в атоме,
4) число электронов внешнего слоя атома,
номер периода в периодической системе,
число нейтронов в ядре,
число протонов в ядре,
заряд ядра атома,
номер группы в периодической системе
Б) (фронтально) Впишите в строчку цифры, характеризующие строение атома калия
(1 вар), хлора (2вар): (на доске)
1) заряд ядра атома: _
2) число электронных слоев: _
3) распределение электронов по энергетическим уровня: ____
Проверьте вариант соседа (1вар: 19, 4, 2881. 2 вар: 17, 3, 287) (Слайд 13)
Задание № 9
Рассмотрите фрагмент – анимацию и поясните увиденное (ЦОР - фронтально)
Как изменяются свойства атомов элементов в периоде?
Как изменяются свойства атомов элементов в группе?
Почему свойства химических элементов периодически повторяются?
Задание № 10
2. «Мои соседи». (Слайд 14)
Необходимо указать знаком ---► ослабление металлических свойств и усиление неметаллических свойств в следующих пятерках элементов.
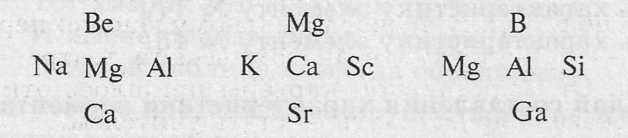
Задание № 11
(На интерактивной доске) (Слайд 15)
Распределите химические элементы О, CI, F, N, S, Р:
а) по порядку возрастания зарядов ядер их атомов;
б) на три группы сходных химических элементов;
в) на два ряда элементов, сходных по числу электронных слоев в атомах.
С современными и историческими видами периодической системы нас познакомит…
(сообщение с презентацией)
Задание № 12
Тест по вариантам (Слайд 16)
1 вариант
1. В ряду Na Mg Al Si металлические свойства
1) усиливаются
2) ослабевают
3) не изменяются
4) изменяются периодически
2. Наиболее сильные металлические свойства проявляет:
1) Sr
2) Mg
3)Са
4) Be
3. В периоде слева направо
1) радиус атома уменьшается
2) число электронов на внешнем уровне атома не меняется
3) число электронных уровней увеличивается
4) заряд ядра атома не меняется
4. Наиболее ярко выражены неметаллические свойства у простого вещества, образованного атомами, которые имеют строение электронной оболочки
1) 2, 8, 4
2) 2, 8, 5
3) 2, 8, 6
4) 2, 8, 7
5.Усиление металлических свойств элементов, расположенных в А-группах периодической системы, обусловлено
1) увеличением атомной массы элемента
2) увеличением общего числа электронов
3) увеличением атомного радиуса элемента
4) увеличением номера периода
2 вариант
1. В ряду F Сl Br I неметаллические свойства
1) усиливаются
2) ослабевают
3) не изменяются
4) изменяются периодически
2. Наиболее сильные неметаллические свойства проявляет:
1) С1
2) Р
3) Si
4) S
3. В группе сверху вниз
1) радиус атома не меняется
2) число электронов на внешнем уровне атома не меняется
3) число электронных уровней уменьшается
4) заряд ядра атома не меняется
4. Наиболее ярко выражены неметаллические свойства у простого вещества, образованного атомами, которые имеют строение электронной оболочки
1) 2, 7
2) 2, 8, 7
3) 2, 8, 8, 7
4) 2, 8, 6
5. Металлические свойства химических элементов, составляющих главную подгруппу первой группы периодической системы Д.И.Менделеева, по мере возрастания зарядов ядер их атомов
1) усиливаются; 2)ослабевают; 3) не изменяются.
Взаимопроверка (Слайд 17)
3. Итог урока
Молодцы, ребята! Вижу, что вы хорошо изучили строение атома, структуру ПС, эти знания нам пригодятся на всем протяжении изучения химической науки, даже до 11 класса. Сегодня вы получили следующие оценки за урок:….
3. Домашнее задание
Ребус «Найди клад!»
