Модуль Поверхневі явища. Дисперсні системи. Високомолекулярні речовини та їх розчини Донецьк 2011
| Вид материала | Документы |
- Тема. Будова речовини. Атоми та молекули. Взаємодія молекул. Явище дифузії. Мета, 108.53kb.
- Сучасна колоїдна хімія це велика, самостійна частина хімічної науки, що вивчає дисперсний, 136.55kb.
- Науково-практичної інтернет-конференції економічна політика країн єс 17 жовтня 2011, 3470.85kb.
- Янки, заочеревинного простору, малого тазу, верхніх та нижніх кінцівок методичні вказівки, 1038.09kb.
- Ренція «комплексне використанння природних ресурсів» (12 грудня 2011 року, м. Донецьк,, 2132.33kb.
- З хімії для вступу на перший курс навчання до Вінницького національного технічного, 99.03kb.
- Програма для загальноосвітніх навчальних закладів 7 9 класи пояснювальна записка, 286.52kb.
- Завідувач кафедри М. П. Рагозін затверджено: на засіданні навчально-видавничої ради, 230.44kb.
- Явища природи. Механічні явища. 5 клас. Мета, 60.42kb.
- Назва реферату: Значення м’ясних страв у харчуванні, їх класифікація Розділ, 96.33kb.
Заняття 24
Окремі класи дисперсних систем. Колоїдні поверхнево-активних речовин. Дослідження міцелоутворення в розчинах ПАР
Актуальність теми
Колоїдними поверхнево-активними речовинами називають ПАР, здатні утворювати міцелярні системи. У виробництві фармацевтичних препаратів широко застосовують КПАР – похідні ефірів жирних кислот. Застосування КПАР пов'язане з їх поверхневою активністю, здатністю до змочування, емульгуючою дією, солюбілізацією, здатністю до гелеутворення. Катіонактивні ПАР застосовують як бактерицидні, фунгіцидні, дезинфікуючі засоби. Твіни – це емульгатори, плюроніки – солюбілізатори вітамінів, антибіотиків, шампунів, зубних паст. Лужні солі вищих карбонових кислот викорситовують як емульгатори, солюбілізатори, стабілізатори мазей і кремів.
Цілі навчання
Загальна мета:
ВМІТИ трактувати окремі класи дисперсних систем та використання КПАР у фармації.
Конкретні цілі:
ВМІТИ:
- Трактувати окремі класи дисперсних систем.
- Досліджувати колоїдні поверхнево-активні речовини (КПАР).
- Інтерпретувати міцелоутворення в колоїдних ПАР та їх використання у фармації.
- Визначити критичну концентрацію міцелоутворення.
- Описувати склад та властивості водних розчинів колоїдних ПАР.
Зміст навчання
Теоретичні питання:
- Окремі класи дисперсних систем. Їх різноманітність.
- Колоїдні поверхнево-активні речовини.
- Класифікація колоїдних ПАР.
- Причини міцелоутворення.
- Крітична концентрація міцелоутворення (ККМ).
- Солюбілізація.
- Використання КПАР в фармації.
Граф логічної структури теми “Окремі класи дисперсних систем. КПАР”
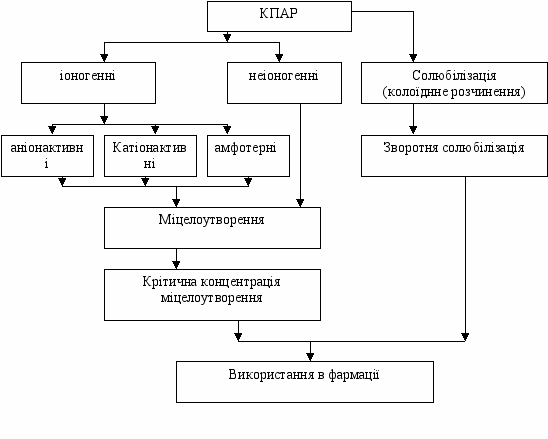 Джерела інформації
Джерела інформаціїОсновна література:
- Фізична і колоїдна хімія / В.І. Кабачний, Л.К. Осипенко, Л.Д. Грицан та ін.; Під ред. В.І.Кабачного. – Харьків: вид-во УукФА „Прапор”, 1999. –с. 328-335.
- Физическая и коллоидная химия/ В.И. Кабачный, л.к. Осипенко, Л.Д. Грицан; Под ред. В.И. Кабачного.- Харьков: изд-во НФаУ, 2005. – с. 304-310.
- Фізична та колоїдна хімія. Збірник задач / В.І. Кабачний, Л.К. Осипенко, Л.Д. Грицан та ін.; Під ред. В.І.Кабачного. – Харьків: вид-во НФАУ „Золоті сторінки”, 2001. – с. 142-157.
- Лекції з фізичної та колоїдної хімії.
Додаткова література:
- Биофизическая химия / Л.П. Садовничая, В.Г. Хухрянский, А.Я. Цыганенко; Под ред. Л.П. Садовничая.- Киев: изд-во „Высшая школа”, 1986. – с.234-238.
- Физическая и коллоидная химия / М.И. Равич-Щербо, В.В.Новиков.; Под ред. М.И.Равич- Щербо.- Москва: изд-во «Высшая школа», 1975.- с. 214-215.
Орієнтовна основа дії
Алгоритм виконання лабораторної роботи № 4
“Дослідження міцелоутворення в розчинах колоїдних ПАР”
- Виконати дослід 1: Визначення ККМ розчинів ПАР.
- За допомогою рефрактометра виміряти показники заломлення розчинів ПАР з відомою концентрацією.
- Дані дослідження та розрахунки занести до таблиці.
- Побудувати графік залежності ∆n = ƒ (lg с). За графіком знайти ККМ.
- За допомогою рефрактометра виміряти показники заломлення розчинів ПАР з відомою концентрацією.
- Виконати дослід № 2: Солюбілізація гідрофобної речовини міцелярним розчином колоїдного ПАР.
- Приготувати розчини ПАР, вивчити мутність та в'язкість.
- Результати занести до таблиці.
- Приготувати розчини ПАР, вивчити мутність та в'язкість.
- Виконати дослід № 3: Водні розчини колоїдних ПАР, їх опис та властивості. Спостереження занести до таблиці.
Набір завдань для перевірки досягнення конкретних цілей навчання
Тест 1
В фізико-хімічній лабораторії в наявності є такі речовини: хлорід натрію, поліетилен, олеат калію, желатину, йоду. Вкажіть, які з перерахованих вище речовин відносяться к колоїдним ПАР.
А. Йод
В. олеат калію
C. хлорід натрію
D. поліетілен
E. желатин
Тест 2
Для стабілізації суспензій та емульсій використовують ПАР, які за своєю будовою:
A. Дифільні
B. Гідрофільні
C. Гідрофобні
D. Речовини органічного походження
E. Полярні
Тест 3
В фармацевтичній промисловості викостовують міцелярні розчини ПАР при виготовленні водорозчиних засобів з нерозчиних в воді речовин, наприклад, вітаміни А та Е. В розчині якої речовини критична концентрація міцелоутворення має найменше значення?
A. С11Н23СООNа
B. С15Н31СООNа
C. С13Н27СООNа
D. С17Н35СООNа
E. С12Н35СООNа
Тест 4
Міцелярні розчини ПАР використовують в фармацевтичної галузі як стабілізатори та солюбілізатори. Для якого з приведених ПАР треба чекати найбільше значення ККМ?
A. С10Н21SО3Nа
B. С12Н25SО3Nа
C. С16Н33SО3Nа
D. С14Н29SО3Nа
E. С9Н29SО3Nа
Тест 5
При виготовленні ряда лікарських форм для підвищення розчинності окремих компонентів, що входять до їх складу, додають колоїдні ПАР. Яке фізико-хімічне явище положено в основу цього процесу?
A. Солюбілізація
B. Коагуляція
C. Екстракція
D. Дифузія
E. Седиментація.
Еталони відповідей до цільових навчальних завдань:
Тест 1 – В, Тест 4- Е.
Короткі методичні вказівки до роботи на практичному занятті
На початку заняття перевіряється підготовленість студентів до заняття шляхом усного опитування, або тестування, проводиться інструктаж з техніки безпеки з хімічними реактивами. Далі студенти студенти працюють самостійно у відповідності до ООД, викладених у методичних вказівках. Рішення ситуаційних задач оформлюється в робочому журналі. Далі проводиться поточний контроль за темою (набори тестів). Потім розглядаються результати самостійної роботи, аналізуються помилки, підводяться підсумки заняття.
