Модуль Поверхневі явища. Дисперсні системи. Високомолекулярні речовини та їх розчини Донецьк 2011
| Вид материала | Документы |
- Тема. Будова речовини. Атоми та молекули. Взаємодія молекул. Явище дифузії. Мета, 108.53kb.
- Сучасна колоїдна хімія це велика, самостійна частина хімічної науки, що вивчає дисперсний, 136.55kb.
- Науково-практичної інтернет-конференції економічна політика країн єс 17 жовтня 2011, 3470.85kb.
- Янки, заочеревинного простору, малого тазу, верхніх та нижніх кінцівок методичні вказівки, 1038.09kb.
- Ренція «комплексне використанння природних ресурсів» (12 грудня 2011 року, м. Донецьк,, 2132.33kb.
- З хімії для вступу на перший курс навчання до Вінницького національного технічного, 99.03kb.
- Програма для загальноосвітніх навчальних закладів 7 9 класи пояснювальна записка, 286.52kb.
- Завідувач кафедри М. П. Рагозін затверджено: на засіданні навчально-видавничої ради, 230.44kb.
- Явища природи. Механічні явища. 5 клас. Мета, 60.42kb.
- Назва реферату: Значення м’ясних страв у харчуванні, їх класифікація Розділ, 96.33kb.
Заняття 17.
Адсорбція на межі розчин-газ, тверде тіло-розчин. Визначення питомої поверхні твердого адсорбенту
Актуальність теми
Адсорбція – процес самодовільної зміни концентрації компонента у поверхневому шарі, порівняно з об’ємом фази. У житті велике значення має таке явище, як адсорбція. При різноманітних отруєннях хворий звертається до лікаря, який часто прописує використання адсорбентів, таких як активоване вугілля, ентеросгель. Явище сорбції використовують в синтезі лікарських препаратів, під час приготування ліків в аптеках. В технологічній карті приготування лікарських засобів є стадія очищення від домішок. Для очищення лікарських засобів використовують адсорбенти. Але потрібно вірно та ефективно підібрати адсорбент. Тому важливо знати закономірності адсорбції на межі поділу фаз.
Цілі навчання
Загальна мета:
ВМІТИ трактувати адсорбцію на межі поділу фаз.
Конкретні цілі:
ВМІТИ:
- Трактувати адсобцію на межі розчин-газ.
- Трактувати асдорбцію на межі тверде тіло- розчин
- Інтерпретувати використання різних видів адсорбентів на межі поділу фаз.
- Визначати адсорбцію ПАР, розрахувати питому поверхню адсорбенту.
Зміст навчання
Теоретичні питання:
- Адсорбція на межі розчин-газ. Адсорбційні плівки.
- Правило Дюкло-Траубе.
- Адсорбція на межі тверде тіло – розчин. Молекулярна адсорбція із розчинів.
- Адсорбція електролітів. Класифікація іонів (за походженням, за складом, за знаком заряду обмінюваних іонів).
- Іонообмінна рівновага. Використання іонообмінників в фармації.
- Використання процесів адсорбції в фармації.
Граф логічної структури теми “Адсорбція на межі розчин-газ, тверде тіло-розчин”
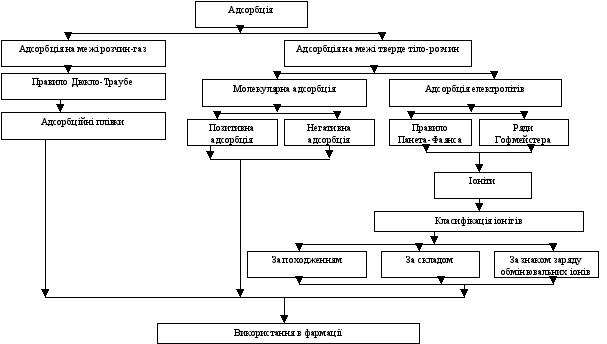
Джерела інформації
Основна література:
- Фізична і колоїдна хімія / В.І. Кабачний, Л.К. Осипенко, Л.Д. Грицан та ін.; Під ред. В.І.Кабачного. – Харьків: вид-во УукФА „Прапор”, 1999. –с. 246-257.
- Физическая и коллоидная химия/ В.И. Кабачный, л.к. Осипенко, Л.Д. Грицан; Под ред. В.И. Кабачного.- Харьков: изд-во НФаУ, 2005. – с. 209-231.
- Физическая и коллоидная химия. Руководство к лабораторным работам / В.И. Кабачный, Л.К. Осипенко, Л.Д. Грицан и др.; Под ред. В.И. Кабачного. – Харьков: изд-во НФАУ, 2005. – с. 104-115.
- Лекції з фізичної та колоїдної хімії.
Додаткова література:
- Фізична та колоїдна хімія. Збірник задач / В.І. Кабачний, Л.К. Осипенко, Л.Д. Грицан та ін.; Під ред. В.І.Кабачного. – Харьків: вид-во НФАУ „Золоті сторінки”, 2001. – с. 124-136.
- Физическая и коллоидная химия / М.И. Равич-Щербо, В.В.Новиков.; Под ред. М.И.Равич-Щербо.- Москва: изд-во «Высшая школа», 1964.- с. 170-194.
- Физическая и коллоидная химия / М.И. Равич-Щербо, В.В.Новиков.; Под ред. М.И.Равич-Щербо.- Москва: изд-во «Высшая школа», 1975.- с. 153-168.
- Биофизическая химия / Л.П. Садовничая, В.Г. Хухрянский, А.Я. Цыганенко; Под ред. Л.П. Садовничая.- Киев: изд-во „Высшая школа”, 1986. – с.166-183.
Орієнтовна основа дії
Алгоритм виконання лабораторної роботи №1
«Визначення питомої поверхні твердого адсорбенту»
1. Виміряти показник заломлення дистильованої води (n0) та вихідного розчину ПАР(n1). Середнє арифметичне значення n0 і n1 записати до таблиці.
2. К розчину ПАР додати 8 г очищеного активованого вугілля та залишити на 1 годину, періодично помішуючи.
3. Через 1 годину адсорбент відокремити фільтруванням. Виміряти показник заломлення фільтрату (n2). Середнє арифметичне значення записати до таблиці.
4. Розрахувати параметри адсорбції за відповідними формулами.
5. Результати роботи оформити в журналі.
Набір завдань для перевірки досягнення конкретних цілей навчання
Тест 1
В якості основ для приготування свічок та лініментів, стабілізації емульсій та в якості солюблізаторів використувують ПАР, ураховуючи коефіцієнт Траубе. Цей коефіцієнт дорівнює:
А. 1-2
В. 2-3
С. 0-1
D. 3-3,5
Е. 4-4,5
Тест 2
Поверхнева активність біологічних розчинів нижча, ніж води, тому гідрофобні речовини будуть накопичуватися у стінок судин, тим самим полегшуючи проникливість крізь мембрану. Таким чином буде утворюватися поверхневий натяг, на який впливає довжина вуглеводневого радикалу. Яким правилом буде описуватися ця залежність?
А. Вант-Гоффа
В. Дюкло-Траубе
С. Антонова
D. Шульце-Гарді
Е. Ребиндера
Тест 3
В адсорбційній терапії використовують величину граничної адсорбції ПАР на межі розчин –газ. Який фактор впливає на цю величину?
А. Площа функціонвльної групи ПАР
В. Довжина вуглеводневого радикалу
C. Ізотонічний коефіцієнт
D. Ступінь дисоціації
E. Концентрація
Тест 4
В виготовленні деяких лікарських засобів використовують адсорбцію іонів із розчину на твердому тілі іонообмінними смолами. Яке правило при цьому використовується?
A.Правило Вант-Гоффа
B.Правило Дюкло-Траубе
C.Правило Шульца-Гарді
D.Правило Ребиндера
E.Правило Паннета Фаянсу
Тест 5
Якщо багато молекул в розчині, то вони розподіляються упорядковано, одна поряд з одною, а їх гідрофільні частини виступають над водною поверхнею, утворюючи «Частокіл Ленгмюра». Дайте визначення цьому поняттю.
A. Це - насичений моношар ПАР на межі поділу рідина–тверда поверхня
B. Це - насичений моношар ПАР на межі поділу тверда поверхня –газ
C. Це - подвійний електричний шар
D. Це - насичений моношар ПАР на межі поділу рідина–газ
E. Це - шар йонів на протилежно зарядженій поверхні
Тест 6
Обчисліть площу S0, що припадає на молекулу стеаринової кислоти С17Н35СООН в насиченому моношарі на поверхні поділу вода-повітря, якщо відомо, що 0,1·10-6 кг стеаринової кислоти покриває поверхню води площею 5·10-2м.
А. S0= 24∙10-20 м2
B. S0= 30∙10-20 м2
C. S0= 11∙10-20 м2
D. S0= 1∙10-20 м2
E. S0= 100∙10-20 м2
Еталони відповідей до цільових навчальних завдань:
Тест1-Д, Тест 5- Д,
Тест 6 - A
| Дано: S = 5·10-2м m = 0,1·10-6 кг | Розв’язання: 1. Молекулярна маса С17Н35СООН = 284 моль/ літр 2. Знаходимо гранічну адсорбцію С17Н35СООН
| ||||||||||||
S0 =? |
Відповідь: S0= 24∙10-20 м2
Короткі методичні вказівки до роботи на практичному занятті
На початку заняття перевіряється підготовленість студентів до заняття шляхом тестування, або усного опитування, проводиться інструктаж з техніки безпеки з хімічними реактивами. Далі студенти знайомляться з методиками експериментальної роботи. Черговим пропонується організувати робоче місце для групи. Студенти працюють самостійно у відповідності до ООД, викладених у методичних вказівках. По закінченні роботи студенти записують свої спостереження, проводять необхідні розрахунки. Далі проводиться підсумковий контроль за темою (набори тестів). Потім розглядаються результати самостійної роботи, аналізуються помилки, підводяться підсумки заняття.
