Методы анализа биологичеcки активных веществ и их свойства
| Вид материала | Документы |
- Контрольная работа По дисциплине физико-химические свойства и методы контроля качества, 77.41kb.
- План лекций по химии для студентов 1 курса специальности 060201. 65 «Стоматология», 220.47kb.
- Темы лекций по аналитической химии: Общие положения и принципы аналитической химии, 23.35kb.
- План лекций по дисциплине «Токсикологическая химия» для студентов IV курса специальности, 18.73kb.
- План работы площадок (кроме холлов 1-2 этажей) в рамках Всероссийского фестиваля науки, 126.35kb.
- Производство и применение биологических средств защиты растений на основе энтомофагов,, 37.05kb.
- Лекция № Тема: «Методы и свойства», 168.5kb.
- I. электрохимические методы анализа, 355.17kb.
- Задачи в области управления активами в настоящий момент Пути совершенствования активных, 271.14kb.
- Биотехнология белковых лекарственных веществ. Рекомбинантные белки, принадлежащие, 79.62kb.
Качественный анализ
1. Лактонная проба (предложена Г.А.Кузнецовой). Параллельно проводят контрольный опыт.
Методика: 1 мл извлечения, содержащего кумарины, наливают в две пробирки.
В одну добавляют 0,5 мл 10%-ного раствора натрия гидроксида.
Обе пробирки нагревают на водяной бане, затем в обе прибавляют 4 мл дистиллированной воды и хорошо перемешивают.
Если в пробирке, куда добавляли щелочь, раствор остался желтым и прозрачным, значит, реакция положительная, так как образуется желтая растворимая в воде соль кумаровой кислоты.
В контрольной пробирке при добавлении воды раствор мутнеет, кумарины не растворяются в воде и выпадают в осадок.
При подкислении щелочного раствора лактонное кольцо замыкается и кумарины выпадают в осадок.


2. Реакция образования азокрасителя. Реакция проводится с продуктами, полученными после реакции разрыва лактонного кольца.
Методика: В пробирку добавляют 1 мл свежеприготовленного диазореактива. Чаще всего, в качестве диазореактива используют диазосульфаниловую кислоту. Образуется азокраситель от желтого до вишнево-красного цвета.
- Для идентификации кумаринов используют методы бумажной и тонкослойной хроматографии. При этом используют системы растворителей:
- н-бутанол-уксусная кислота-вода БУВ (4:1:5)
- н-гексан-бензол-метанол (5:4:1);
- петролейный эфир-бензол-метанол (5:4:1);
Идентифицируют кумарины по характерной флюоресценции в УФ свете или проявляют хромогенными реактивами.
В качестве проявляющих реактивов служат 1%-ный спиртовый раствор алюминия хлорида, 10%-ный раствор щелочи или пары аммиака.
Широкие возможности для обнаружения в растениях и сырье кумаринов, не только их суммы, но и отдельных соединений, открылись после внедрения хроматографического анализа. При этом указанные реактивы используют и для обработки хроматограмм.
4. Хроматографические методы удобны для выделения индивидуальных кумаринов.
Количественное определение.
Для количественного определения кумаринов в лекарственном РС используют гравиметрические, титриметрические и физико- химические методы анализа.
По существующей нормативной документации для количественного определения кумаринов в лекарственном растительного сырье используют физико-химические методы анализа.
1. Полярографический метод. Определение кумаринов в плодах пастернака.
Основан на восстановлении кумаринов на ртутно-капельном электроде в альфа-пироновом кольце по месту двойной связи в положении 3,4. Присоединяют галоген - йод, в качестве реактива используют тетраэтиламмоний йодид. Содержание комариное в пересчете на ксантотоксин не менее 1%.
- Спектрофотометрический метод. Основан на способности кумаринов поглощать монохроматический свет при определенной длине волны в зависимости от концентрации исследуемого раствора. Используют
для определения содержания простых кумаринов в траве донника лекарственного (не менее 0.4%) и пиранокумаринов в корневищах и корнях вздутоплодника сибирского (не менее 3 %). Получают хлороформное извлечение из сырья и измеряют у него оптическую плотность с помощью спектрофотометра.
3. Хроматоспектрофотометрический метод. Применяют для определения содержания фуранокумаринов в плодах амми большой, псоралеи костянковой, листьях инжира.
Стадии определения:
1. Получение хлороформного извлечения из сырья.
2. Разделение суммы кумаринов методом хроматографии на бумаге в системе растворителей, указанной в нормативной документации.
3. Идентификация кумаринов в УФ-свете по характерному свечению.
4. Элюирование веществ с бумаги. Каждое вещество отдельно элюируют 95 %-ным этанолом.
5. Измерение оптической плотности растворов с помощью спектрофотометра при длине волны, указанной в нормативной документации.
6. Расчет содержание каждого соединения с учетом удельного показателя поглощения.
Плоды амми большой: бергаптена и изопимпинеллина не менее 0,6 %.
Плоды псоралеи костянковой: псоралена и изопсоралена не менее 0,9 %.
Листья инжира: псоралена и бергаптена не менее 0,7%, отдельно псоралена менее 0,42 %.
4. Гравиметрический (весовой) метод.
Основан на избирательной растворимости отдельных кумаринов в различных растворителях и способности лактонного кольца кумарина к раскрытию и обратному замыканию в зависимости от рН среды.
Используется редко только для определения суммы кумаринов.
5. Фотоэпектроколориметрический метод.
Основан на измерении оптической плотности окрашенного раствора, полученного по реакции азосочетания с солями диазония при определенной длине волны.
Содержание суммы кумаринов рассчитывают по калибровочному графику, построенному по известному веществу.
Алкалоиды - Различают
общие качественные реакции, с помощью которых доказывается присутствие алкалоидов в сырье или в извлечении из сырья, и
частные качественные реакции, с помощью которых доказывают или индивидуальный алкалоид или определенную группу алкалоидов.
Общие реакции –
это либо реакции осаждения, либо реакции окрашивания.
Реакции осаждения основаны на способности алкалоидов к комплексообразованию. Образующиеся комплексы нерастворимы или мало растворимы в воде.
Общеалкалоидные осадочные реактивы можно разделить на несколько групп:
1 группа. Йод и его растворы.
Образуют с алкалоидами перйодиды, плохо растворимые в воде:
1) пары йода используют для открытия алкалоидов на хроматограммах;
2) раствор йода в KJ (реактив Вагнера, реактив Бушарда).
С алкалоидами образуют бурые, трудно растворимые в воде осадки.
2 группа. Комплексные йодиды металлов:
- Реактив Драгендорфа - калия тетрайодовисмутат (KBiJ4) - образует оранжевые или красно-бурые нерастворимые осадки.
Реакцию с реактивом Драгендорфа, согласно действующей НД, используют для обнаружения (проявления) алкалоидов крестовника плосколистного на хроматограмме.
2) Реактив Майера - тетрайодомеркурат калия (K2HgJ4) - образует осадки белого или желтоватого цвета.
Реакцию с реактивом Майера широко используют для проверки полноты экстракции алкалоидов при их количественном определении в сырье красавки обыкновенной, белены черной, дурмана обыкновенного, анабазиса безлистного.
3 группа. Реакгивы комплексных неорганических кислот (высокомолекулярные органические вещества кислого характера):
1) Реактив Бертрана - раствор кремневольфрамовой кислоты
(SiO2 . 12 WO3 . 4 H2O ) - образует белый аморфный осадок. Реакцию с реактивом Бертрана используют:
- для подтверждения наличия алкалоидов в извлечении из листа барбариса и травы пассифлоры (качественные реакции);
- для проверки полноты экстракции алкалоидов при их количественном определении в траве плауна-баранца и чистотела, листьях и корнях барбариса;
2) реактив Шейблера - раствор фосфорно-вольфрамовой кислоты (НзРО4 .12 WО3 . 2Н2О) - образует белые аморфные осадки;
3) реактив Зоненштейна - раствор фосфорно-молибденовой кислоты (НзРО4 • 12МоОз 2Н2О) - образует желтоватые аморфные осадки.
Все эти реактивы высокочувствительны и часто используются в исследовательских работах.
4 группа. Органические вещества кислотного характера:
1) раствор пикриновой кислоты - дает осадки желтого цвета.
Реакцию используют для осаждения алкалоида скополамина при его гравиметрическом определении в семенах дурмана индейского;
2) раствор танина - образует беловатые или бурые осадки.
Танин используют в качестве противоядия при отравлении алкалоидами. Танин блокирует поступление и всасывание алкалоидов.
Реакции окрашивания (частные реакции)
основаны на окислении, конденсации, дегидратации алкалоидов концентрированными кислотами и другими окислителями.
Используют:
- конц. H2SO4 - качественная реакция на корень барбариса (берберин) получается оранжево-красное окрашивание,
и на наличие алкалоидов в очищенном извлечении (сухой остаток) из корневищ с корнями чемерицы – образуется бурое окрашивание;
2) конц.HNO3 - качественная реакция на корень барбариса (берберин) - красно-бурое окрашивание;
3) раствор H2O2 - качественная реакция на корень барбариса (берберин) - фиолетовое окрашивание;
4) раствор K2Cr2O7 и конц.H2SO4 - качественная реакция на стрихнин - красно-фиолетовое окрашивание;
5) раствор K2Cr2O7 и конц.НNO3 - качественная реакция на бруцин - оранжево-красное окрашивание.
Две последние реакции на наличие алкалоидов в очищенном извлечении из семян чилибухи.
6) реакция на алкалоиды спорыньи - алкалоиды переводят в соли винной кислоты и добавляют реактив Ван-Урка (конц.H2SO4 + FeCl3 + п-диметиламинобензальдегид) – образуется фиолетовое окрашивание.
Эту реакцию используют для подтверждения подлинности сырья, а также в методе количественного определения алкалоидов.
В анализе могут быть использованы:
- реактив Эрдмана - смесь конц.HNОз и конц.Н2SO4 ;
- реактив Марки - раствор формалина в конц. H2SO4;
- реактив Фреде - раствор молибдата натрия в конц. H2SO4.
Окраска в зависимости от алкалоидов различна.
Для некоторых алкалоидов существуют групповые качественные реакции, такие как: «реакция Витали-Морена» (тропановые алкалоиды),
«мурексидная проба» (на пуриновые алкалоиды),
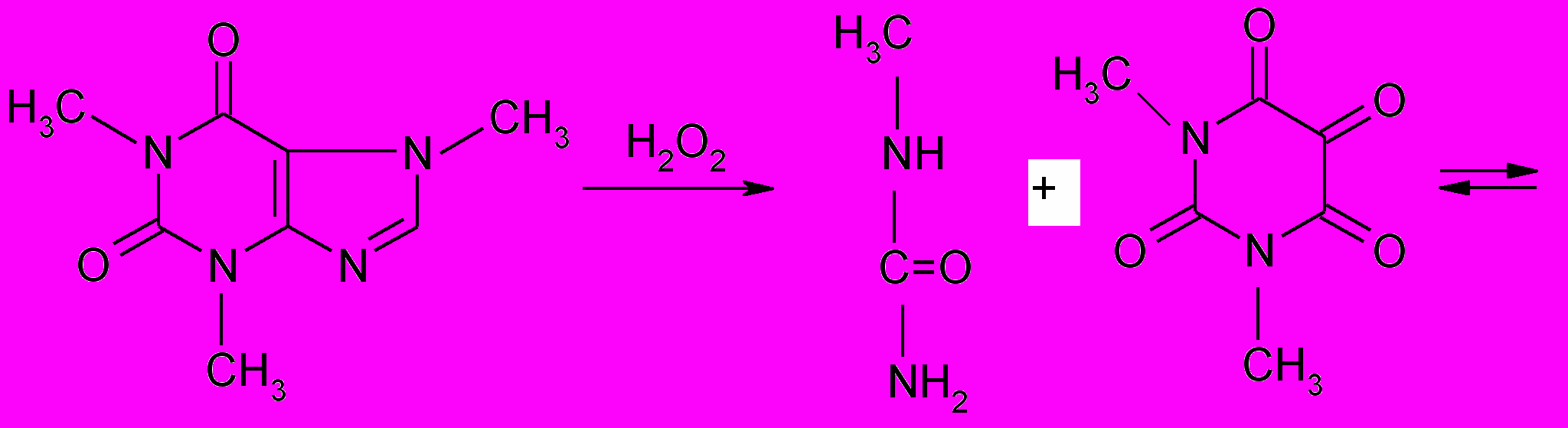
метил- 1,3-диметилаллоксан
мочевина


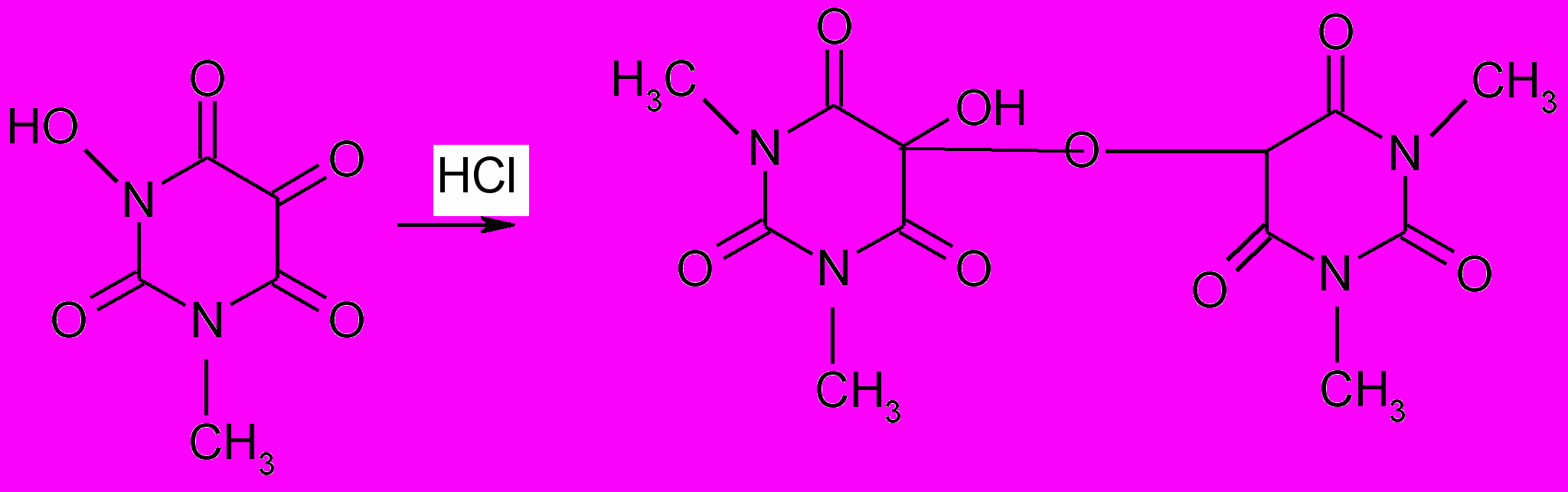
1,3-диметилалуровая тетраметилаллоксантин
кислота
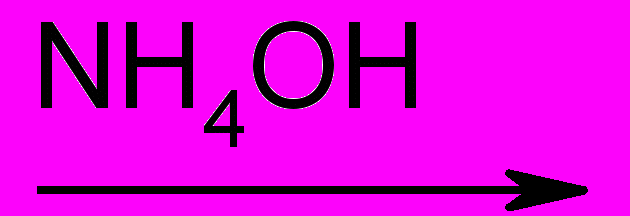
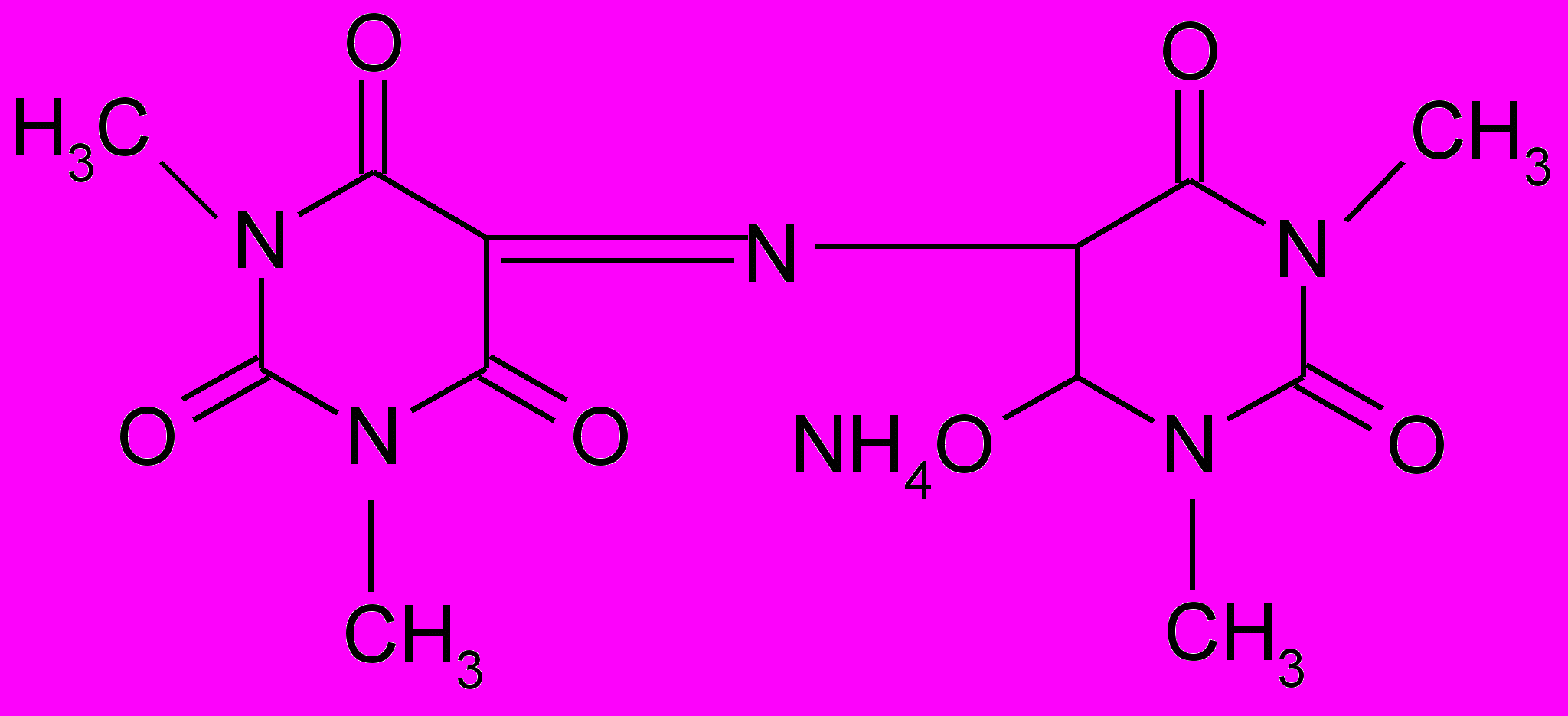
аммонийная соль тетраметилпурпуровой кислоты
Эта реакция основана на разрушении молекулы пурина при нагревании с окислителем (перекисью водорода, бромной водой, азотной кислотой). Происходит образование смеси производных аллоксана и его изомера диалуровой кислоты. Взаимодействуя между собой, они образую метилированные производные аллоксантина, которые под действием избытка раствора аммиака приобретают пурпурно-красное окрашивание. Окраска обусловлена появлением аммонийной соли метилированного производного пурпуровой кислоты.
Таким образом, общей специфической качественной реакции на алкалоиды не существует.
Если проводят поиск алкалоидсодержащих растений, то всегда выполняют 5-10 реакций с общеалкалоидными реактивами, т.к. чувствительность реакций различна. Обычно эти реакции выполняют капельным способом на стеклянных пластинках.
Для выделения или разделения суммы алкалоидов пользуются методом хроматографии на бумаге.
Для обнаружения алкалоидов достаточно нанести на полоску фильтровальной бумаги каплю испытуемого раствора и "проявить" соответствующим реактивом.
Количественное определение алкалоидов
Единой методики количественного определения содержания алкалоидов в растительном сырье не существует, т.к. их химическая структура, физические кие свойства различны.
Разработаны индивидуальные методики определения содержания алкалоидов или групповые методики (определение тропановых алкалоидов). Все методики количественного определения алкалоидов в растительном сырье многоэтапные. Относительная точность их невелика.
В ходе анализа обычно выделяют следующие этапы (стадии):
1. Извлечение суммы алкалоидов из сырья.
Алкалоиды извлекают в виде солей или в виде оснований.
Alk-соли - В этом случае сырье обрабатывают слабыми растворами органических или минеральных кислот, соли которых хорошо растворимы в воде или спирте. Используют винную, лимонную, уксусную, серную, соляную и другие кислоты.
В извлечение попадают углеводы, белки и другие сопутствующие вещества.
Alk-основания – В этом случае сырье смачивают концентрированным раствором аммиака. Едкие щелочи не используют, т.к. они образуют феноляты, вызывают гидролиз, изомеризацию алкалоидов.
Раствор аммиака вытесняет алкалоиды-основания из солей.
Алкалоиды-основания извлекают органическим растворителем (эфиром, хлороформом, бензолом и др.). В извлечение попадают воски, каротиноиды, фенольные соединения.
Извлечение проводят многократно новыми порциями до полного истощения. Полученные порции объединяют.
2. Очистка извлечения от балластных веществ.
Обычно проводят путем двух- или трехкратной сменой растворителя. Реже используют ионообменную или адсорбционную хроматографию.
3. Разделение суммы алкалоидов и выделение индивидуальных алкалоидов.
Выполняют в тех случаях, когда оценку качества сырья проводят не по сумме алкалоидов, а по содержанию индивидуального алкалоида, определяющего основное фармакологическое действие сырья.
Разделение основано на различных физико-химических свойствах
алкалоидов, извлеченных из сырья:
- на способности перегоняться с водяным паром.
Например, пахикарпин из суммы алкалоидов травы софоры толстоплодной отделяют путем отгонки его с водяным паром;
- на различной растворимости алкалоидов в органических растворителях.
Например, колхамин из суммы алкалоидов клубнелуковиц безвременника отделяют, используя его плохую растворимость в ацетоне;
- на различной растворимости полученных комплексов с общеалкалоидньми реактивами, т.е. используют реакции осаждения. Например, скополамин из суммы алкалоидов семян дурмана индейского отделяют в виде солей пикриновой кислоты (пикрата).
Для разделения используют также различные виды хроматографии.
4. Собственно количественное определение проводят различными методами:
- гравиметрический (весовой) метод.
Алкалоиды переводят в весовую форму, осадок отделяют, высушивают, взвешивают.
Этим методом определяют алкалоиды-основания клубнелуковиц безвременника. плауна-баранца; алкалоиды-соли травы крестовника плосколистного, семян дурмана индейского, листьев барбариса;
2) титриметрические методы:
а) ацидиметрического прямого титрования (алкалоиды побегов анабазиса, травы софоры толстоплодной, семян чилибухи);
Ь) ацидиметрического обратного титрования (алкалоиды листьев и корней красавки, листьев белены, листьев дурмана обыкновенного, травы термопсиса ланцетного, корневищ с корнями чемерицы),
с) для определения алкалоидов чая используют йодометрический метод обратного титрования;
d) титрование в неводных средах:
- точку эквивалентности определяют, используя индикатор на алкалоиды
(корневища кубышки, травы барвинка малого, клубней с корнями стефании гладкой);
- точку эквивалентности определяют потенциометрически (алкалоиды травы чистотела)
3) физико-химические (инструментальные) методы:
а) фотоэлектроколориметрический метод (алкалоиды коробочек мака снотворного, рожков спорыньи, травы мачка желтого, листьев катарантуса розового, листьев унгернии Виктора, травы крестовника плосколистного, травы софоры толстоплодной, травы паслена дольчатого, клубней с корнями стефании гладкой);
Ь) спектрофотометрический метод (алкалоиды корней барбариса, семян и травы термопсиса очередноцветкового, травы маклейи, плодов стручкового перца);
с) полярографический метод (алкалоиды семян термопсиса ланцетного, корневищ кубышки желтой).
прозрачка
Так, например, количественное определение алкалоидов группы тропана в листьях красавки, белены, дурмана Государственная Фармакопея XI (вып.2, ст. 13, 17, 24) предлагает проводить ацидиметрическим методом (вариант обратного титрования).
Метод основан на способности тропановых алкалоидов-оснований образовывать соли под действием кислоты хлористоводородной, т.е. на слабых основных свойствах алкалоидов; избыток кислоты хлористоводородной титруют раствором натрия гидроксида.
При этом, предварительно алкалоиды переводят в форму оснований, извлекают их из сырья эфиром, проводят очистку методом двукратной смены растворителей, удаляют экстрагент и растворяют сухой остаток суммы оснований алкалоидов в кислоте хлористоводородной (НС1), избыток которой оттитровывают щелочью.
Содержание суммы алкалоидов вычисляют в процентах в пересчете на гиосциамин в абсолютно сухом сырье.
Этапы определения:
- подготовительный;
- экстракция из сырья: алкалоиды переводят в форму оснований, извлекают из сырья эфиром без нагревания;
- очистка полученного извлечения: проводят методом двукратной смены растворителей;
- непосредственно количественное определение: удаление экстрагента, растворение сухого остатка суммы оснований алкалоидов в кислоте хлористоводородной (алкалоиды-основания переводят в форму солей); титрование избытка кислоты хлористоводородной натрия гидроксидом;
- расчет результатов по формуле, сопоставление с данными нормативной документации.
Подобное определение рекомендовано и для травы термопсиса ланцетного (ГФ-Х1, вып. 2, ст. 59).
Оценку количественного содержания алкалоидов в семенах чилибухи (ГФ Х, ст.606) проводят ацидиметрическим методом (прямое титрование).
При этом, предварительно алкалоиды переводят в форму оснований, извлекают из сырья эфиром, проводят экстракционную очистку, удаляют экстрагент, растворяют сухой остаток суммы оснований алкалоидов в этаноле и титруют хлористоводородной кислотой (НС1).
Количественное определение алкалоидов в сырье спорыньи проводят
элетроколориметрическим методом (ГФ-Х, ст. 599).
12. Анализ сырья, содержащего СГ.
Качественные реакции на СГ проводят с очищенным спиртовым извлечением из растительного сырья.
Все реакции на СГ можно разделить на 3 группы:
- реакции на углеводную часть молекулы (2-дезоксисахара) (реакция Келлер-Килиани);
- на стероидную структуру (реакция Либермана-Бухарда);
- на лактонное ненасыщенное кольцо.
1. Реакции на стероидную структуру.
Основаны на способности стероидного ядра СГ подвергаться дегидратации под действием кислотных реагентов (уксусный ангидрид, конц. серная кислота, трихлоруксусная кислота) с образованием окрашенных комплексных соединений. Образующиеся в результате реакций окрашивания меняются во времени, поэтому необходимо наблюдать их в момент соприкосновения реактивов, а затем отмечать изменение окраски в течение 10-15 минут.
Для СГ обычно проводят реакции:
1. Реакция Либермана-Бурхарда. При взаимодействии СГ со смесью уксусного ангидрида и конц. серной кислотой появляется розовое окрашивание, переходящее в зеленое.
2. Реакция Розенгейма. При взаимодействии СГ с 90% водным раствором трихлоруксусной кислоты появляется розовое окрашивание, переходящее в лиловое и затем в синее.
3. Реакция с хлоридом сурьмы (III). СГ при взаимодействии с хлоридом сурьмы в среде уксусного ангидрида образуют лиловое окрашивание
