I. Данные по итогам эпидсезонов кэ за 2002-2006 гг. 5 Заведующая паразитологическим отделом фгуз «Центр гигиены и эпидемиологии в Санкт-Петербурге» Л. П. Антыкова. 5 Временные характеристики эпидемического сезона 6 клиническая эффективность йодантипирина при клещевом энцефалите 12
| Вид материала | Документы |
- План основных организационных мероприятий фгуз «Центр гигиены и эпидемиологии в Оренбургской, 290.58kb.
- Фгуз «Центр гигиены и эпидемиологии в Пермском крае», г. Пермь, ул. Куйбышева,, 52.02kb.
- Клиническая эффективность йодантипирина в терапии хронических гепатитов в и с эффективность, 114.07kb.
- Методическое пособие для работников молочной промышленности фгуз «центр гигиены и эпидемиологии, 2337.13kb.
- План мероприятий, приуроченных к Всемирному дню борьбы со спид в Республике Алтай Мероприятия, 35.2kb.
- Список органов по сертификации и испытательных лабораторий, осуществляющих аттестацию, 91.11kb.
- План основных организационных мероприятий фгуз «Центр гигиены и эпидемиологии в Оренбургской, 775.63kb.
- Ения здравоохранения «Центр гигиены и эпидемиологии в Республике Саха (Якутия)», 1137.13kb.
- Теоретические и методические основы, 877.57kb.
- Эколого-эпидемиологические аспекты клещевых инфекций на юге тюменской области, 264.26kb.
КЛИНИЧЕСКАЯ ЭФФЕКТИВНОСТЬ ЙОДАНТИПИРИНА
ПРИ КЛЕЩЕВОМ ЭНЦЕФАЛИТЕ
Результаты клинического испытания по применению йодантипирина у заболевших клещевым энцефалитом
А.В. Лепехин, заведующий кафедрой инфекционных болезней с эпидемиологией СГМУ г. Томска, член-корреспондент Сибирской Академии Высшей школы, д.м.н., профессор.
А
 .С. Саратиков, заведующий кафедрой фармакологии СГМУ г. Томска. д.м.н., профессор.
.С. Саратиков, заведующий кафедрой фармакологии СГМУ г. Томска. д.м.н., профессор.Е.В. Портнягина, ассистент кафедры инфекционных болезней с эпидемиологией СГМУ. к.м.н., доцент.
Постоянной угрозой здоровью населения Сибири является наличие очагов тяжелого заболевания вирусной этиологии – клещевого энцефалита (КЭ). За последние 15–20 лет заболеваемость в Сибирском регионе возросла в 10–15 раз, превышая средний показатель по Российской Федерации в 8 раз. В клинике для специфической профилактики и этиотропной терапии КЭ используют человеческий противоэнцефалитный иммуноглобулин. Этот препарат, как показал С.О. Григорян с соавторами, подавляет у человека основную естественную противовирусную систему защиты – образование интерферона. До последнего времени в мире отсутствовали средства, повышающие неспецифическую резистентность организма к вирусу КЭ.
В результате многолетних исследований кафедры фармакологии СГМУ, кафедры микробиологии Новосибирского медицинского института и Проблемной лаборатории синтеза лекарственных веществ Томского политехнического университета, при участии Томского НИИ вакцин и сывороток получен и детально исследован оригинальный противовирусный препарат, индуктор интерферона йодантипирин.
Клиническое испытание йодантипирина проведено в клинике инфекционных болезней СГМУ. В проведенном исследовании из 130 больных лихорадочной формой клещевого энцефалита 50 человек получали йодантипирин (1 группа), 46 пациентов – иммуноглобулин (2 группа) и 34 больным назначали комбинированную терапию: иммуноглобулин + йодантипирин (3 группа).
Йодантипирин применяли в виде таблеток по 100 мг внутрь после еды по следующей схеме: по 300 мг 3 раза в день в течение первых двух дней, по 200 мг 3 раза в день в течение последующих 2-х дней и по 100 мг 3 раза в день в течение следующих 5 дней. Иммуноглобулин, титрованный против вируса клещевого энцефалита (титр 1:80), вводили по 3–6 мл внутримышечно в течение 3 суток. Кроме того, всем больным проводилась патогенетическая и симптоматическая терапия.
Результаты лечения оказались следующими. Продолжительность лихорадочного периода у больных, получавших специфический иммуноглобулин, в среднем составила 3,7 суток. Данный период оказался достоверно короче по времени у пациентов, лечившихся йодантипирином: 2,7 + 0,3 (Р < 0,05), причем у половины больных нормализация температуры тела отмечена в первые два дня приема препарата. У больных на фоне совместного применения йодантипирина и иммуноглобулина температура тела нормализовалась на 4 день от начала терапии, т. е. данный период оказался у них достоверно продолжительнее, чем у лиц из 1-й группы (Р < 0,01). Существенные различия зарегистрированы и в продолжительности ряда других симптомов. У пациентов, получавших йодантипирин, общеинфекционные проявления заболевания купировались быстрее, чем у пациентов из групп сравнения: головная боль – в 1,4 и 1,9 раза, тошнота в – 1,8 и 2 раза, слабость в – 1,4 и 1,6 раза. Аналогичные результаты получены и при наблюдении ряда других симптомов: боль в глазных яблоках исчезала в среднем в 1,7 раза быстрее у больных из первой группы, чем у пациентов, получавших иммуноглобулин, и в 1,5 раза быстрее, чем у пациентов, получавших комбинированную терапию; светобоязнь прекращалась также быстрее соответственно в 2 и 1,6 раз.
Постинфекционный астенический синдром среди перенесших лихорадочную форму клещевого энцефалита наблюдался значительно реже у лиц, получавших в острый период заболевания йодантипирин, чем у реконвалесцентов из групп сравнения. Продолжительность указанного синдрома была также короче у лиц, входивших в первую группу.
Также мы изучали состояние иммунной системы у больных клещевым энцефалитом и влияние на нее различных схем лечения. В остром периоде изменения в балансе иммунологических показателей прежде всего касались
Т-клеточного звена иммунитета: было выявлено снижение количества
Т-лимфоцитов, их супрессорной и хелперной фракций, а также снижение количества больших гранулярных лимфоцитов и значительное угнетение естественной и антителозависимой цитотоксичности лимфоцитов.
У всех пациентов, принимавших сравниваемые препараты, в период ранней реконвалесценции количество Т-лимфоцитов увеличивалось, нормализация же уровня ТФР-Т-лимфоцитов происходила быстрее под влиянием йодантипирина. На фоне терапии специфическим иммуноглобулином и йодантипирином отмечена нормализация содержания БГЛ, иммуноглобулинов класса Ig М, индекса АЗЦТ. Через 1 месяц после лечения наблюдали статистически достоверное увеличение индекса естественной цитотоксичности лимфоцитов, а через 6 месяцев у реконвалесцентов, получавших в остром периоде заболевания йодантипирин, данный индекс даже превысил подобный показатель у здоровых доноров. Следовательно, оба препарата оказывают положительное влияние на показатели иммунологического статуса при клещевом энцефалите, но данный эффект проявляется несколько быстрее при лечении йодантипирином.
Установлено также, что йодантипирин не оказывает депрессивного действия на формирование специфического гуморального иммунитета. Кроме того, продолжительность антигенемии вируса клещевого энцефалита была короче у лиц, леченных этим препаратом.
Таким образом, применение йодантипирина свидетельствует о значительной терапевтической эффективности его при лихорадочной форме клещевого энцефалита. Препарат не оказывает депрессивного влияния на клеточный и гуморальный иммунитет. Учитывая хорошую переносимость данного препарата, отсутствие побочных эффектов при его применении, мы считаем целесообразным использование йодантипирина в качестве лечебного средства при клещевом энцефалите.
РЕЗУЛЬТАТЫ ПРОФИЛАКТИЧЕСКОГО ИСПЫТАНИЯ ПРЕПАРАТА ЙОДАНТИПИРИН ПРИ ЗАРАЖЕНИИ ВИРУСОМ КЛЕЩЕВОГО ЭНЦЕФАЛИТА ПОСЛЕ ПРИСАСЫВАНИЯ ВИРУССОДЕРЖАЩЕГО КЛЕЩА
Н.С. Зинченко – Главный врач ТОЦГСЭН.
Е.Н. Топовская – Зам. главного врача по эпид. вопросам.
О.А. Сокерина – Зав. паразитологическим отделением.
Клещевой энцефалит (КЭ) – вирусное трансмиссивное заболевание, широко распространенное по территории России. По обобщенным данным заболеваемость КЭ в отдельных регионах России колеблется от 20 до 37 на 100 000 населения, а число лиц, подвергшихся нападению клещей обычно на 1,5–2 порядка выше. Единственным препаратом, обладающим достаточно эффективным действием при экстренной профилактике КЭ, является специфический иммуноглобулин. Крайне высокая стоимость этого виростатика и недостаточное его количество, порой делает просто невозможным его использование, не только с целью экстренной профилактики КЭ, но и в лечении больных данной патологией. Поэтому объясним интерес поиска новых эффективных и дешевых препаратов для профилактики КЭ.
Участники исполнения: Томский областной центр санэпиднадзора (ТОЦГСЭН) – эпидемиологический и паразитологические отделы. Иммунологическая и вирусологическая лаборатории, клиника инфекционных болезней СГМУ, НПО «Вирион» г. Томск.
Цель и задачи исследования: изучение профилактической эффективности йодантипирина при заражении людей вирусом КЭ в сравнении с профилактическим действием специфического иммуноглобулина.
Структура исследований: люди, подвергшиеся заражению вирусом КЭ и получавшие с профилактической целью йодантипирин (460 человек), а также контрольная группа (11195 человек), получавшие с профилактической целью специфический иммуноглобулин.
Объем исследования: клинический и лабораторный (по данным результатов анализов клинико-диагностической и вирусологической лабораторий), позволяющий провести общепринятое клиническое, неврологическое обследование и длительность антигенемии.
Сроки проведения исследований: июль 1992 – август 1995 гг.
Результаты исследований:
Профилактические испытаний йодантипирина проведены на пунктах серопрофилактики г. Томска сотрудниками ТОЦГСЭН.
Характеристика препарата в соответствии с аннотацией: йодантипирин – фирменное название препарата, выпускаемого в таблетках. Одна таблетка йодантипирина содержит 100 мг 1-фенил-2,3-диметил-4-йод-пиразолона-5.
Свойства: йодантипирин обладает противовоспалительными, антивирусными, иммуностимулирующими и интерфероногенными свойствами. Он является активным индуктором интерферона «позднего типа». Наибольшая активность препарата проявляется в отношении неполиемиелитных энтеровирусов Коксаки и ECHO, вирусов везикулярного стоматита, клещевого энцефалита, гриппа и парагриппа. Препарат малотоксичен. Не обладает мутагенным, эмбриотоксическим, иммунотоксическим и аллергогенным действием.
Показания: йодантипирин рекомендуется для лечения и профилактики клещевого энцефалита.
Противопоказания: не установлены.
Побочные реакции: непродолжительные и встречаются от 0,1 до 14 % в виде головной боли, потливости, мышечных и суставных болей, сухости во рту, сыпи на коже.
Дозировка: во всех случаях после установления факта присасывания вируссодержащего клеща и наличии вируса в крови человека йодантипирин назначался по следующей схеме: по 0,3 г (3 таблетки) 3 раза в день в течении .первых двух дней, по 0,2 г (2 таблетки) 3 раза в день в течение следующих двух дней и по 0,1 г (1 таблетка) 3 раза в день в течение следующих пяти дней. В группе сравнения вводился специфический иммуноглобулин в титре 1/20–1/40 по 3 мл.
На первом этапе в задачу исследования входило установление защитного действия сравниваемых препаратов по принципу «да» или «нет», т. е. развилось или нет заболевание после применения данных препаратов с профилактической целью (таблица 1).
Как видно из таблицы 1, заболевание среди пациентов, принимавших йодантипирин, возникло только в 2 случаях, что составило 0,43 %, в то время как в группе сравнения – 1,79 %.
Таблица 1
Развитие заболевания после профилактического применения сравниваемых препаратов
| Препараты | Кол-во людей, получавших препараты | Количество заболевших | % | Р |
| Йодантипирин | 460 | 2 | 0,43 | < 0,01 |
| Специфический иммуноглобулин против вируса клещевого энцефалита | 11195 | 201 | 1,79 |
Следовательно, из полученных результатов можно сделать заключение о том, что применение с профилактической целью йодантипирина почти в 4 раза (Р<0,01) обладает лучшим защитным действием, по сравнению со специфическом иммуноглобулином направленного действия.
Вторым этапом исследования эффективности сравниваемых препаратов явилось изучение вопроса о длительности сохранения антигена вируса КЭ в крови пациентов после профилактического применения йодантипирина и специфического иммуноглобулина направленного действия.
Исследование проводилось у 73 пациентов, получавших йодантипирин и у 56 пациентов, получавших специфический иммуноглобулин.
Определение антигена вируса КЭ проводилось через 1,2 и 5,7 месяцев после проведения профилактики соответствующими препаратами.
Как видно из таблицы 2 антиген вируса КЭ после профилактического введения йодантипирина сохранялся на протяжении первого месяца в 50,7 % случаев, а после профилактического введения специфического иммуноглобулина – в 82,1 % случаев. По истечении двух месяцев антиген вируса КЭ в крови сохранялся примерно в одинаковом проценте случаев и составил 4,1 % после профилактического применения йодантипирина и 3,57 % после введения специфического иммуноглобулина.
Исследования, проведенные через 5–7 месяцев, показали, что у лиц, получавших как йодантипирин, так и иммуноглобулин показатели сохранения вируса в крови также примерно одинаковы и составляют 1,37 % и 1,78 % соответственно. Интересно отметить, что при наличии в крови антигена вируса КЭ клинического развития заболевания в этих группах сравнения не произошло, по крайней мере, в сроки наблюдения. Следовательно, сравнительное изучение профилактического действия обоих препаратов показало, что исчезновение антигена вируса КЭ из крови инфицированных при применении йодантипирина происходит в течение первого месяца после присасывания клеща почти в 50 % случаев, в то время как при введении специфического иммуноглобулина только в 17,9 % случаев.
Таблица 2
Длительность сохранения вируса после проведения
профилактики сравниваемыми препаратами
| Препараты | Антиген вируса КЭ обнаружен | ||
| 1 мес. (абс./%) | 2 мес. (абс./%) | 5-7 мес. (абс./%) | |
| Йодантипирин (73 чел.) | 37/50,7 | 3/4,1 | 1/1,37 |
| Специфический иммуноглобулин против вируса КЭ | 46/82,1 | 2/3,57 | 1/1,78 |
Таким образом, проведенное исследование по профилактике развития заболевания препаратом йодантипирин (основная группа) и специфическим иммуноглобулином против вируса КЭ (группа сравнения) показало:
йодантипирин обладает достаточно высоким профилактическим действием по сравнению со специфическим иммуноглобулином против вируса КЭ (Р<0,01).
Способствует более быстрому исчезновению антигена вируса КЭ из организма инфицированного.
Исходя из вышеизложенного, считаем, что препарат йодантипирин может использоваться в качестве медикаментозного средства экстренной профилактики клещевого энцефалита.
ХИМИОПРОФИЛАКТИКА КЛЕЩЕВОГО ЭНЦЕФАЛИТА
Информационное письмо от центра государственного санитарно-эпидемиологического надзора
в Иркутской области
Кауров П.К. – главный врач ИОЦГСЭН.
В последние годы ежегодно отмечается рост обращаемости населения в лечебные учреждения по поводу присасывания клещей.
Таблица 1
Заболеваемость клещевым энцефалитом и обращаемость,
по поводу присасывания клещей, населения Иркутской области
за 2001–2003 гг.
| | 2001 | 2002 | 2003 |
| Заболеваемость клещевым энцефалитом | 317 | 317 | 202 |
| Обращаемость с укусами клещей | 9583 | 9358 | 9768 |
Несмотря на это, рост заболеваемости этой инфекцией удается сдерживать, чему немало способствует широкое проведение экстренной специфической профилактики.
До последнего времени единственным препаратом, используемым для этой цели, оставался противоклещевой иммуноглобулин. Однако, высокая стоимость противоклещевого иммуноглобулина значительно ограничивает его применение для экстренной профилактики и лечения КЭ.
В связи с этим в последние годы для специфической профилактики и лечения КЭ стал применяться противовирусный препарат – йодантипирин. Это препарат широкого спектра действия с антивирусным, противовоспалительным и иммуномодулирующим эффектом. Изучение защитного механизма йодантипирина (А.В. Лепехин, 1996–1997 гг.) показало, что одним из ведущих факторов его профилактического действия является выраженная стимуляция выработки α- и β-интерферонов. Уже через 4 часа после приема препарата уровень этих противовирусных белков у большинства людей увеличивается в десятки, а через 12–24 часа в сотни и тысячи раз. При этом происходит значительная стимуляция клеточного и гуморального иммунитета. В 1996 г. препарат был разрешен Министерством Здравоохранения РФ для применения в качестве средства для экстренной профилактики и лечения клещевого энцефалита. Следовательно, йодантипирин является препаратом выбора для профилактики и лечения КЭ.
Сотрудниками Томского областного центра ГСЭН были проведены профилактические испытания йодантипирина на пунктах серопрофилактики г. Томска.
Группе людей после установления факта присасывания вируссодержащих клещей и наличии вируса в крови в крови человека йодантипирин назначался по следующей схеме: по 0,3 г. (3 таблетки) 3 раза в день в течение первых двух дней, по 0,2 г. (2 таблетки) 3 раза в день в течение следующих пяти дней. В группе сравнения вводился специфический иммуноглобулин в титре 1/20–1/40 по 3 мл.
По результатам испытаний эффективность йодантипирина не уступает и даже превосходит эффективность специфического противоклещевого иммуноглобулина.
В последние годы йодантипирин применяется и в Иркутской области.
Таблица 2
Эффективность специфической противоклещевой профилактики,
проведенной противоклещевым иммуноглобулином
и йодантипирином жителям Иркутской области в 2001–2003 гг.
| Год | Специфический иммуноглобулин против вируса клещевого энцефалита | Йодантипирин | ||||
| Кол-во людей, получавших препарат | Из них заболевших | % | Кол-во людей, получавших препарат | Из них заболевших | % | |
| 2001 | 2873 | 17 | 0,5 | 1803 | 5 | 0,2 |
| 2002 | 2002 | 20 | 1,0 | 1170 | 3 | 0,2 |
| 2003 | 2418 | 2 | 0,08 | 1790 | 1 | 0,05 |
Из наших данных видно, что удельный вес заболевших после проведения экстренной профилактики противоклещевым иммуноглобулином выше (0,08–1,0), чем после применения йодантипирина (0,05–0,2).
В настоящее время разработаны схемы применения йодантипирина как при выходе в очаг (в течение всего периода пребывания в эпидемичном очаге по КЭ по 200 мг. (2 таблетки один раз в сутки)), так и в случае присасывания клеща:
1–2 день – по 3 таблетки (300 мг.) – 3 раза в сутки;
3–4 день – по 2 таблетки (200 мг.) – 3 раза в сутки;
5–9 день – по 1 таблетке (100 мг.) – 3 раза в сутки;
Йодантипирин можно приобрести в аптечной сети и всегда иметь при себе, так как для его хранения не требуется особых условий.
Недостатки йодантипирина связаны, в основном, с невозможностью применения в детском возрасте и лицам с повышенной чувствительностью к данному препарату или ко всем препаратам йода.
Учитывая положительный опыт применения йодантипирина, накопленный в Иркутской области, можно считать возможным применение этого препарата, наравне с противоклещевым иммуноглобулином, для проведения специфической профилактики КЭ лицам с 14 лет.
КЛИНИЧЕСКАЯ ЭФФЕКТИВНОСТЬ ЙОДАНТИПИРИНА ПРИ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКЕ С ПОЧЕЧНЫМ СИНДРОМОМ
ЙОДАНТИПИРИН - НОВЫЙ ПРОТИВОВИРУСНЫЙ
ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ
ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ
Е.К. Алехин, зав. кафедрой фармакологии БГМУ г. Уфы, д.м.н., профессор.
Д.Х. Хунафина, зав. кафедрой инфекционных болезней с эпидемиологией
и курсом ИПО, д.м.н. профессор.
Геморрагическая лихорадка с почечным синдромом (ГЛПС) является наиболее распространенной на территории Российской Федерации (РФ) природноочаговой инфекцией. Особенно актуальна проблема ГЛПС в республике Башкортостан, где расположен один из самых крупных и активных в мире очагов ГЛПС. Территория Республики Башкортостан на протяжении десятилетий, характеризуется высокой эпидемической активностью и общепризнанно считается самым напряженным очагом в РФ. Крупные вспышки ГЛПС в Башкортостане были отмечены в 1983 г (167 на 100 тыс. населения) и в 1994 г. (100,7 на 100 тыс. населения). Самая крупная вспышка заболевания наблюдалась в 1997 году, составив 224,5 в Республике и в 574,9 в г. Уфе на 100 тысяч населения.
Летальность, как показатель тяжести течения ГЛПС, составляет до 1-2 % в европейских и до 5-10 % в дальневосточных районах России. В Башкортостане на протяжении последних лет летальность не превышает 0,3-0,85 %, но вследствие высокой заболеваемости остается значительной.
Установлено существование не менее 10 серотипов вируса ГЛПС, из которых на сегодня изучено и охарактеризовано 5 серотипов: Hantaan (HTN), Seoul (SIO), Puumala (PUU), Prospect Hill (PHV), Sin Nombre (SNV). Hantaan вызывает тяжелую форму заболевания в Азии, Восточной Европе и на Дальнем Востоке. Seoul - этиологический агент менее тяжелой формы ГЛПС в Азии. Puumala - обуславливает более легкий европейский вариант течения болезни, Prospect Hill - не является патогенным для человека. Sin Nombre – приводит к развитию «хантавирусного пульмонарного синдрома», регистрируемого в Америке, имеющего очень тяжелое течение и сопровождающегося высокой летальностью.
ГЛПС характеризуется тяжелым течением, вовлечением в патологический процесс практически всех органов и систем, развитием серьезных осложнений: инфекционно-токсического шока, острой почечной недостаточности, ДВС-синдрома, нередко являющихся причиной летального исхода.
Несмотря на недостаточную изученность механизмов патогенеза ГЛПС, большинство исследователей рассматривают эту инфекцию как генерализованный васкулит с развитием иммунокомплексного интерстициального нефрита, диссеминированной внутрисосудистой коагулопатии, с обязательным участием иммунологических и нейроэндокринных механизмов. Известно, что ведущим в развитии и течении заболевания являются гормональная и иммунная системы человека, определяющие исходы болезни. От состоятельности этих систем зависит тяжесть течения болезни и прогноз.
ГЛПС характеризуется картиной Т-клеточного дефицита, выражающегося снижением CD4 и инверсией соотношения CD4/CD8, на фоне активации В-клеточного звена иммунитета и увеличения числа натуральных киллеров CD 16 и CD95 лимфоцитов; повышением количества сывороточного интерферона в плазме крови в сочетании с резким угнетением способности лейкоцитов продуцировать альфа-интерферон во все периоды заболевания; повышением активности системы гипофиз-надпочечники и нарушением согласованности между тиреотропной деятельностью гипофиза и функцией щитовидной железы; значительной активацией перекисного окисления липидов и депрессией антиоксидантной системы крови. Степень выраженности выявленных изменений зависит от тяжести течения ГЛПС.
Полученные результаты не носят специфического характера. Они типичны для «острой фазы» вирусной инфекции и связаны с повреждающим действием вируса ГЛПС на клетки организма, что требует коррекции выявленных нарушений в динамике болезни.
Важнейшей проблемой является лечение ГЛПС, т.к. отсутствуют эффективные средства этиопатогенетической терапии и профилактики заболевания. Создание вакцины на основе региональных штаммов ГЛПС хотя и весьма перспективно, но представляет сложную задачу. Кроме того, вакцина полностью не исключает случаев заболеваемости.
В связи с ясной этиологией заболевания, кардинальное изменение ситуации с ГЛПС можно ожидать только от эффективных этиотропных воздействий, конечно, не исключая разработку и использование средств, влияющих на патогенез заболевания.
Представляются особенно перспективными препараты, сочетающие способность индуцировать образование эндогенного интерферона и непосредственно антивирусную активность. При ряде заболеваний использование индукторов интерферона имеет ряд преимуществ перед введением экзогенных интерферонов. Во-первых, индукторы стимулируют выработку собственных интерферонов, которые не обладают иммуногенностью. Во-вторых, синтез интерферона находится под контролем белков-репрессоров и не достигает уровня, способного оказать повреждающего воздействия на организм. В-третьих, стоимость лечения индукторами интерферона существенно ниже, чем экзогенными интерферонами.
К числу таких препаратов относится йодантипирин.
Йодантипирин (1-фенил-2,3-диметил-4йодпйазолон) относится к группе нестероидных противовоспалительных средств, производных пиразолона, обладает противовоспалительными, антивирусными, иммуностимулирующими и интерфероногенными свойствами. Препарат является активным индуктором α- и -интерферонов, существенно повышает активность фибробластов и индуцирует их антивирусную резистентность, задерживает проникновение вируса в клетку за счет стабилизирующего действия на биологические мембраны, значительно стимулирует продукцию антител.
В 2001 году препарат был разрешен Министерством здравоохранения РФ для применения в качестве средства для комплексного лечения геморрагической лихорадки с почечным синдромом.
Схема применения препарата для лечения ГЛПС: йодантипирин должен быть назначен в течение 5 дней от начала заболевания по 0,2 г 3 раза в день в течение первых четырех дней, затем по 0,1 г 3 раза в день в течение следующих пяти дней.
Достоинства препарата
Йодантипирин оказывает противовирусное действие на вирус ГЛПС (имеется дозозависимое подавление йодантипири-ном специфического свечения антигена вируса ГЛПС в условиях in vitro). Оказывает положительное влияние на клиническое течение болезни (сокращая продолжительность интоксикационного и болевого синдрома), нормализует показатели мочевины и креатинина в крови, регулирует показатели клеточного иммунитета и стимулирует выработку интерферона.
Недостатки препарата связаны, в основном, с повышенной чувствительностью к данному препарату или ко всем препаратам, содержащим йод.
В соответствии с разрешением Фармакологического государственного комитета МЗ РФ проведены клинические испытания йодантипирина в клинической инфекционной больнице № 4 г. Уфы.
Целью данного исследования было изучение йодантипирина в качестве средства для лечения ГЛПС в клинических условиях.
Оценивая положительный эффект терапии мы, в первую очередь, учитывали клинические критерии оценки эффективности.
У пациентов со среднетяжелым течением ГЛПС, получавших йодантипирин, продолжительность таких симптомов как лихорадка, олигурия, боль в пояснице и животе оказалась достоверно меньшей, чем у больных контрольной группы. Также выявлено существенное снижение в разгар болезни пиковых показателей мочевины и креатинина в основной группе.
У больных тяжелой формой ГЛПС, получавших испытуемый препарат, продолжительность лихорадки, болей в пояснице тоже достоверно отличались. В то же время разница в длительности олигурии, болей в животе и головных болей у больных обеих групп была несущественной. Пиковые показатели креатинина были достоверно ниже в основной группе, а мочевины – не имели статистически значимой разницы.
Йодантипирин в разработанной нами схеме приема хорошо переносился больными, побочных эффектов и аллергических реакций зарегистрировано не было. Хотя следует отметить, что его пероральное применение может быть ограничено у больных с выраженной рвотой, развивающейся в разгар болезни. Выявленное положительное влияние йодантипирина на клиническое течение ГЛПС, по нашим данным, обусловлено противовирусным и иммунокорригирующим действием препарата. Об этом свидетельствует анализ показателей иммунного и интерферонового статуса у больных сравниваемых групп.
Заключение
Включение йодантипирина в комплексное лечение больных геморрагической лихорадкой с почечным синдромом оказывает положительное влияние на клиническое течение болезни, нормализующее на показатели гиперазотемии, повышает способность лейкоцитов продуцировать α-интерферон.
КЛИНИЧЕСКАЯ ЭФФЕКТИВНОСТЬ ЙОДАНТИПИРИНА
ПРИ ГРИППЕ И ОРВИ
ЙОДАНТИПИРИН – НОВОЕ ЭФФЕКТИВНОЕ СРЕДСТВО
ДЛЯ ПРОФИЛАКТИКИ ГРИППА
И ДРУГИХ ОРВИ
А.В. Лепехин, заведующий кафедрой инфекционных болезней с эпидемиологией СГМУ (г. Томск), д.м.н., профессор.
А.С. Саратиков, заведующий кафедрой фармакологии СГМУ, Заслуженный деятель науки РФ, д.м.н., профессор.
Н.С. Бужак, доцент кафедры инфекционных болезней с эпидемиологией СГМУ, зав. клиникой инфекционных болезней СГМУ, к.м.н.
В результате изучения многочисленных производных пиразолона установлено, что они, помимо противовоспалительного и обезболивающего действия, существенно (в 2–2,5 раза) повышают функциональную активность клеток культуры фибробластов эмбриона человека, сокращая длительность всех параметров митотического цикла. Не обладая прямым вирулицидным действием в клеточных культурах (фибробласты эмбриона человека, Нер-2, L-4), они ингибируют репродукцию ряда РНК- и ДНК-содержащих вирусов. Введение атомов галогена, особенно йода, в ароматический радикал соединений усиливает этот эффект. Наиболее перспективным оказался йодантипирин (1-фенил-2,3-диметил-4-йодпиразолон).
В двойном слепом клинико-эпидемиологическом опыте нами установлено, что йодантипирин высокоэффективен при применении у людей, контактировавших с больными гриппом в периоды эпидемических вспышек гриппа А и В. Прием препарата осуществляли по двум схемам: I – по 200 мг два раза в неделю; II – по 100 мг в течение 7 дней, после трехдневного перерыва – повторение курса; длительность приема йодантипирина по обеим схемам – в течение всего эпид. сезона. Под наблюдением находились работники двух предприятий г. Томска: на первом – 97 человек, из которых 36 не получали йодантипирин (контрольная группа), а 61 – принимали препарат по I схеме (основная группа); на втором – 344 человека, 172 из них получали йодантипирин по II схеме и 172 – препарат не получали (контроль).
По результатам учета заболеваемости гриппом и другими ОРВИ в основных и контрольных группах рассчитывали индексы эффективности (К) и показатели защищенности (Е) по формулам: К = В/А; Е = (В х А) / В х 100, где А – доля заболевших среди лиц, получавших йодантипирин; В – доля заболевших среди лиц, не получавших йодантипирин. Кроме того, оценивали тяжесть клинического течения инфекции у заболевших, частоту и выраженность побочных реакций при приеме йодантипирина, а также картину периферической крови, функциональное состояние печени (активность АлАТ, АсАТ и щелочной фосфатазы), субпопуляционный состав лимфоцитов, фагоцитарную активность нейтрофилов, исследовали уровень основных классов иммуноглобулинов (IgM, IgG, IgA) и циркулирущих иммунных комплексов (ЦИК). Оценивали также динамику интерферонообразования путем количественного определения α-интерферона в сыворотке крови.
Профилактическое действие йодантипирина оценивали по величине заболеваемости гриппом и другими ОРВИ в основных и контрольных группах. Результаты исследования показали, что заболеваемость в группе людей, принимавших йодантипирин по I схеме, составила 9,8 %, а в соответствующей контрольной группе – 33,3 %, т. е. индекс эффективности в этом случае равнялся 3,4, а показатель защищенности составил 70,6 %. Заболеваемость среди лиц, принимавших препарат по II схеме, составила 4,71 %, а в контрольной группе – 42,4 %; таким образом, прием йодантипирина по II схеме позволил снизить заболеваемость в 9,2 раза (индекс эффективности этой схемы – 9,2; показатель защищенности – 89,1 %).
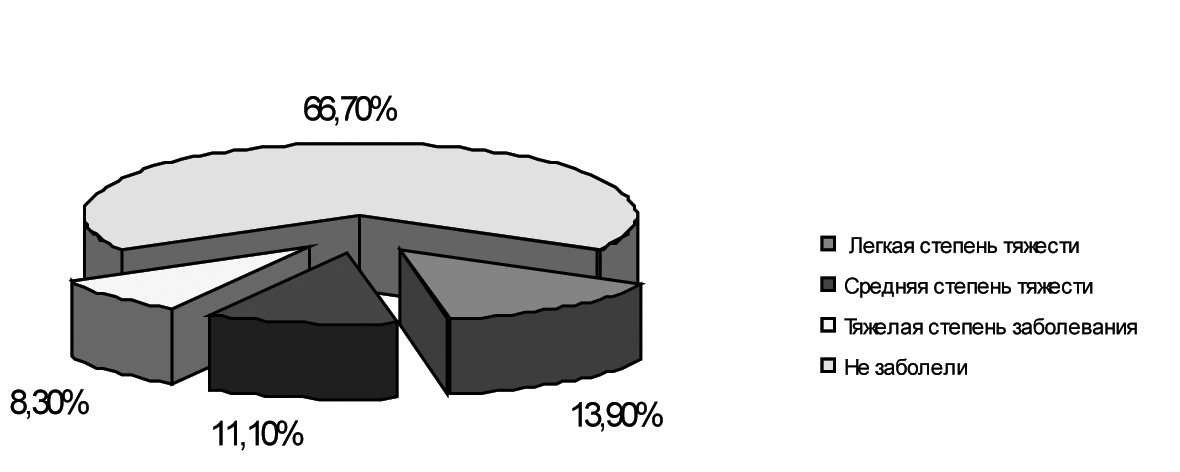
Рис. 1. Заболеваемость в контрольной группе
(не принимали йодантипирин)
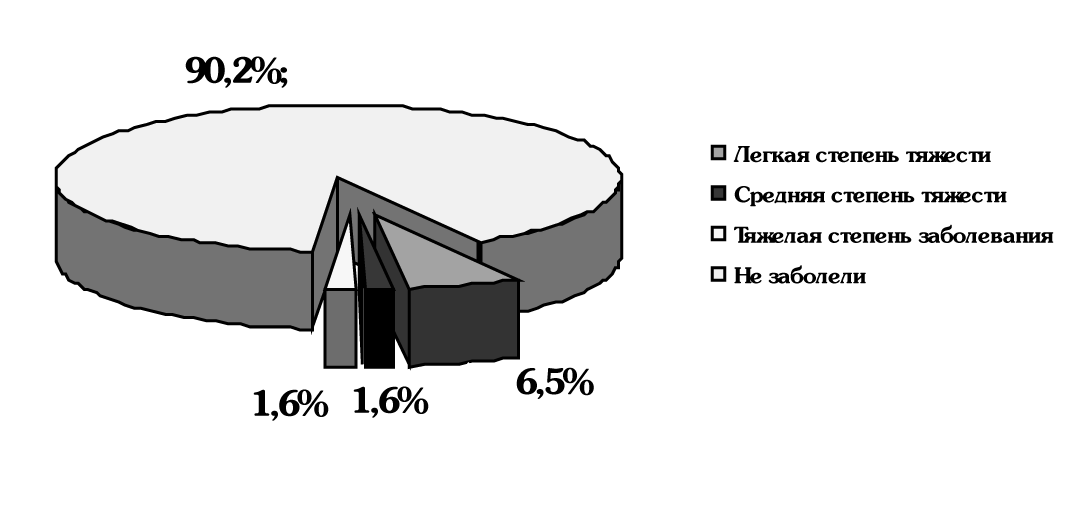
Рис. 2. Заболеваемость в исследуемой группе
(принимали йодантипирин по I схеме)
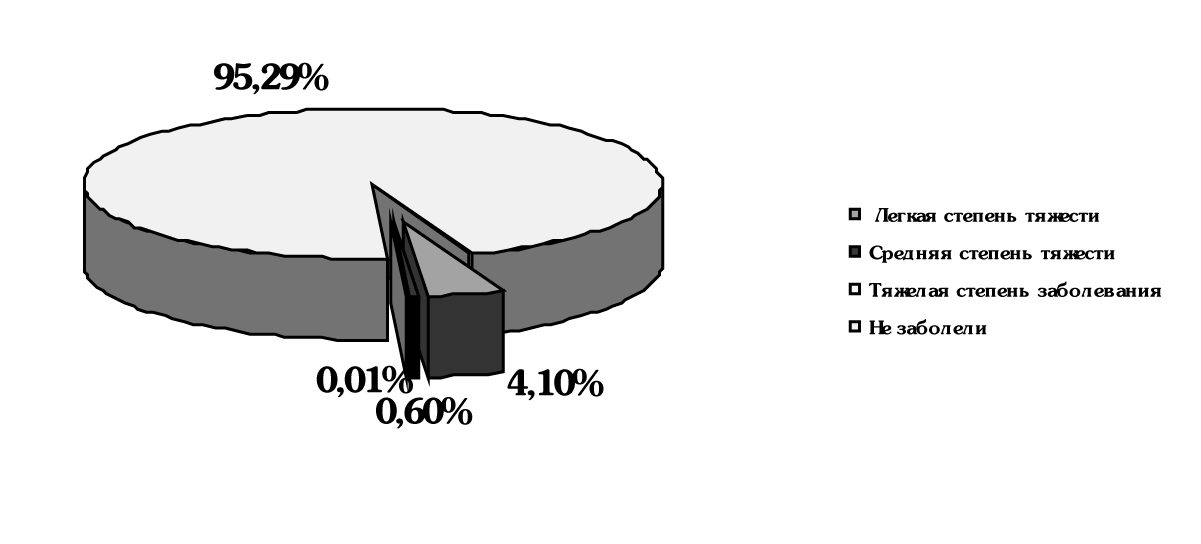
Рис. 3. Заболеваемость в исследуемой группе
(принимали йодантипирин по II схеме)
Клинические симптомы болезни у людей, принимавших йодантипирин, характеризовались слабыми катаральными явлениями, кратковременной субфебрильной температурой, отсутствием интоксикации; за медицинской помощью заболевшие не обращались. Клинические проявления заболевания у лиц, не принимавших йодантипирин, отличались большей тяжестью и длительностью проявлений патологических симптомов: у них чаще отмечалась лихорадка выше 38 °С (длительность – 3 дня), выраженные интоксикация и катаральные явления.
Побочный эффект от приема препарата по I схеме наблюдался у 5 человек из 61 (8,2 %): двое (3,3 %) отметили незначительные боли в эпигастральной области: один (1,6 %) – умеренные боли в правом подреберье, один (1,6 %) – першение в горле, один (1,6 %) – общее легкое недомогание.
При назначении йодантипирина по II схеме побочные явления регистрировались у 5 человек из 172 (2,9 %): у трех (1,7 %) – кратковременные головные боли, у одного (0,6 %) – тошнота, у одного (0,6 %) – жидкий стул. Побочные явления были кратковременными и слабовыраженными. Таким образом, прием йодантипирина по II схеме вызывал побочные реакции в 2,8 раза реже, чем его применение по I схеме. Наш опыт показал, что йодантипирин способствует нормализации картины периферической крови у тех добровольцев, которые до начала приема препарата имели повышенную СОЭ и сдвиг лейкоцитарной формулы в ту или иную сторону.
Контроль динамики изменений биохимических показателей функционального состояния печени позволил заключить, что в выбранных дозировках йодантипирин не оказывает токсического действия на гепатобилиарную систему взрослых людей.
Анализируя данные иммунологического мониторинга в группе лиц, получавших йодантипирин по I схеме, можно сделать вывод о том, что динамика изученных показателей в целом соответствует механизмам развития иммунного ответа на ранних его стадиях. Через 14 дней после начала приема препарата выявлена активизация клеточного звена иммунитета: статистически значимо увеличивается абсолютное количество лейкоцитов, лимфоцитов и практически всех субпопуляций последних. Особенно существенно возрастало содержание CD3+ лимфоцитов (зрелые Т-клетки), что, по всей вероятности, может свидетельствовать о включении классического пути активации Т-лимфоцитов. Увеличивалось также количество CD8+ клеток (Т-киллеры/супрессоры), активно регулирующих межклеточные взаимодействия, а также не только абсолютное, но и относительное количество В-лимфоцитов и натуральных киллеров (CD72+ и CD16+), выполняющих функции клеток-эффекторов. К концу наблюдения все усредненные показатели клеточного иммунитета в этой группе возвращались к исходному уровню.
При изучении факторов гуморального иммунитета у лиц этой группы установлено значительное нарастание концентрации IgM в сыворотке крови, достигающее максимума на 28 день наблюдения, постепенное снижение содержания IgG и относительная стабильность IgA. В процессе приема йодантипирина в периферической крови достоверно увеличивается количество ЦИК и несколько повышается процент фагоцитирующих клеток без существенных изменений их функциональной активности (фагоцитарного числа). В группе людей, получавших йодантипирин по II схеме, столь активной перестройки иммунной системы не отмечалось.
РЕЗЮМЕ
Представленные данные терапевтической эффективности препарата йодантипирина у людей, контактировавших с больными гриппом в периоды эпидемических вспышек ОРВИ, показали, что данный препарат оказывает весьма выраженный эффект как индуктор интерферона. Наиболее действенной, эффективной и интенсивной по интерфернообразованию является схема приема йодантипирина по 100 мг в течение 7 дней с повторением указанного курса через каждые 3 дня в период эпидемического сезона. Клинические проявления ОРВИ у лиц, принимавших йодантипирин с профилактической целью, но заболевших, характеризовались легким течением и быстрым выздоровлением; побочные явления йодантипирина были кратковременными и незначительными.
КЛИНИЧЕСКАЯ ЭФФЕКТИВНОСТЬ ЙОДАНТИПИРИНА В ТЕРАПИИ ХРОНИЧЕСКИХ ГЕПАТИТОВ В и С
ЭФФЕКТИВНОСТЬ ЙОДАНТИПИРИНА В ЛЕЧЕНИИ ХРОНИЧЕСКИХ ГЕПАТИТОВ В И С
аспирант кафедры терапии М.А. Внушинская,
д.м.н., профессор Э.И. Белобородова – Сибирский государственный медицинский университет, г. Томск.
По данным ВОЗ более 1/3 населения планеты инфицированы различными формами вирусных гепатитов. Вирусные гепатиты – частая причина развития цирроза печени и первичного рака печени, от которых умирают ежегодно в мире около 2 млн человек. Широкое распространение вирусных гепатитов позволяет рассматривать их лечение как медико-социальную проблему, а разработку противовирусной терапии как первостепенную задачу клинической гепатологии.
В клинической практике лечение вирусных поражений печени в фазе репликации включает использование экзогенного интерферона. Однако отмечается его невысокая эффективность (30–40 %) и большое число побочных явлений в виде гипертермии, диспепсии, депрессии, выпадения волос, импотенции, лейкопении, тромбоцитопении. Необходимо отметить и тот факт, что большинство применяемых в клинической практике препаратов экзогенного интерферона выпускаются за рубежом и являются дорогостоящими, а следовательно, малодоступны для широких слоев населения. Этим и определяется настоятельная необходимость внедрения в практику здравоохранения новейших достижений науки, новых методов лечения. Перспективным является применение нового класса препаратов – индукторов синтеза эндогенного интерферона, в силу их доступности, хорошей переносимости и минимальных побочных эффектов, а также сочетания противовирусной и иммуномодулирующей активности.
Учеными Сибирского государственного медицинского университета и Томского политехнического университета разработан новый противовирусный препарат – йодантипирин. Это соединение существенно повышает функциональную активность клеток культуры фибробластов эмбриона человека и индуцирует их антивирусную резистентность. Установлена противовирусная активность йодантипирина в отношении группы энтеровирусов Коксаки и ЕСНО, вируса везикулярного стоматита герпеса. Испытание интерфероногенной активности йодантипирина, проведенное в 1989 году в НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи, показало, что это соединение является активным индуктором b-интерферона “позднего” типа (титр интерферона в сыворотке крови мышей в ответ на введение йодантипирина нарастает в течение суток с 8 до 256 ИЕ50/мл).
Цель данного исследования: Изучение эффективности нового отечественного индуктора интерферона – йодантипирин у больных хроническим вирусным гепатитом В и С умеренной степени активности, в сравнении с другим известным индуктором ИФН – Амиксином.
Материалы и методы исследования:
Представлены результаты наблюдения 95 больных хроническим вирусным гепатитом, которые были разделены на три группы, в зависимости от вида применяемой терапии.
1 группа (26 человек) – монотерапия йодантипирином в дозе 200 мг в сутки после еды 4 раза в неделю;
2 группа (группа сравнения – 13 человек) – терапия известным индуктором интерферона амиксином в дозе 250 мг в сутки в течение первых двух дней, затем по 125 мг через 48 часов в течение месяца с повторением курса через месяц;
3 группа (контрольная – 11 человек) – традиционная терапия реафероном в дозе 3 МЕ внутримышечно 3 раза в неделю. Длительность терапии во всех группах составила 6 месяцев. Диагноз хронического гепатита исходил из ведущих критериев этиологии, стадии заболевания и степени активности. Все подгруппы пациентов с хроническим гепатитом были сопоставимы по полу, возрасту, давности заболевания.
В обследование всех больных входило определение основных биохимических показателей, позволяющих судить о функциональном состоянии печени: АЛТ и АСТ в сыворотке крови, активность щелочной фосфатазы, общий белок крови и его фракции. Процессы перекисного окисления оценивались определением малонового диальдегида. Исследование пигментного обмена заключалось в определении уровня общего билирубина и его фракций в сыворотке крови.
С целью проверки этиологии процесса и оценки репликативной активности вируса в сыворотке крови определяли ДНК HBV методом ПЦР.
При лечении йодантипирином отмечено уменьшение проявлений заболевания у 69 % пациентов с HBV уже к концу первого месяца лечения. Максимум клинического эффекта достигался к концу третьего месяца лечения и поддерживался в последующие месяцы наблюдения практически у всех больных. Судя по динамике субъективных признаков заболевания, во 2-й и 3-й группах максимальный эффект был менее выраженным и достигался позднее, к концу 5–6 месяцев лечения.
Положительное действие йодантипирина на астенический и диспептический синдромы проявлялось в уменьшении слабости, утомляемости, повышении работоспособности, нормализации настроения, уменьшения выраженности тошноты, горечи во рту, улучшении аппетита, стабилизации веса. Заметно уменьшались ощущения тяжести и боли в правом подреберье. В группе сравнения чаще сохранялись жалобы на слабость, повышенную утомляемость. В контрольной группе (3), у подавляющего большинства больных оставались жалобы на подавленное настроение, чувство безнадежности, утрату прежних интересов. Проявления болевого и диспептического синдромов сохранялись чаще, чем в 1 и 2 группах. На фоне лечения йодантипирином практически все пациенты отметили нормализацию температуры, значительное уменьшение артралгий, миалгий, кожного зуда.
В процессе лечения отмечена положительная динамика в объективной симптоматике заболевания в 1 и 2 группах лечения на 3-й месяц лечения, в контрольной группе – несколько позже, к 5-му месяцу, выразившаяся в уменьшении гепатомегалии, пальпаторном улучшении консистенции печени, купировании проявлений желтухи.
Ценным свойством йодантипирина явилось и его антихолестатическое действие, несколько превосходящее подобный эффект Амиксина и Реаферона у пациентов с HВV, HСV.
Таким образом йодантипирин оказывал достаточно выраженный терапевтический эффект на клиническую симптоматику хронического вирусного гепатита В и С, аналогично уже применяемым препаратам. Он гораздо эффективнее, чаще и в более ранние сроки по сравнению с Амиксином и Реафероном, купировал или уменьшал ряд ведущих проявлений астенического, диспептического, болевого синдромов, желтухи, гепатомегалии, субфебрилитета, артралгий. Каких либо побочных эффектов в процессе применения йодантипирин не выявлено.
Важным свойством йодантипирина явилась его способность индуцировать “лабораторную” ремиссию у пациентов с HBV. Начало редукции основных лабораторных симптомов отмечено в 1 и 2 группах к концу первого месяца лечения, а максимум эффекта достигался к третьему месяцу лечения и сохранялся в последующие месяцы наблюдения. В контрольной (3) группе начало редукции лабораторных симптомов отмечено в более поздние сроки, к концу третьего месяца лечения, эффект был менее выраженным (см. таблицу)
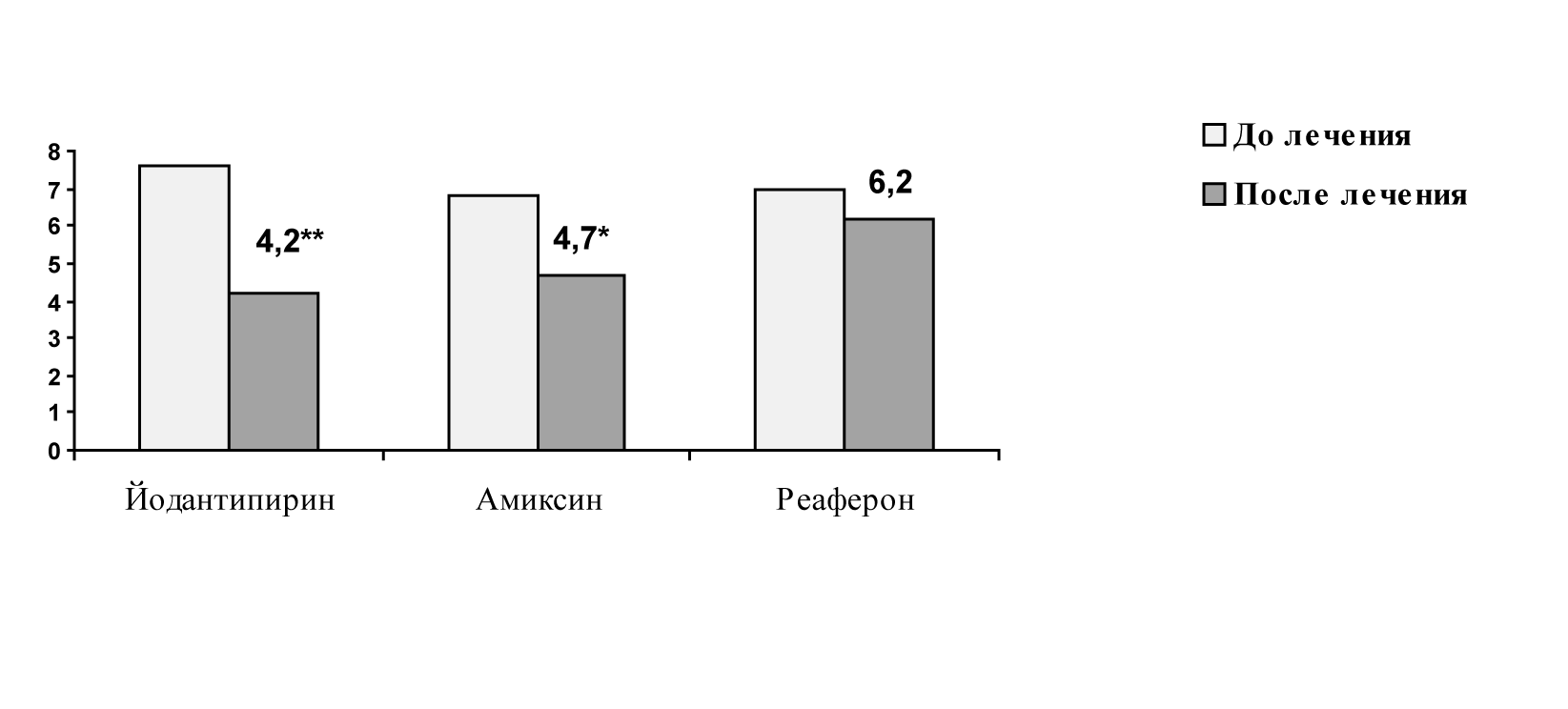
После курсового применения йодантипирина отмечалось достоверное снижение уровня МДА. В группах сравнения, после лечения амиксином, антиоксидантный эффект был менее выражен, а у больных в контрольной группе, получавших реаферон, нормализации показателей МДА не происходило, хотя выявлена тенденция к его снижению.
Рисунок. Динамика уровней МДА у больных хроническим гепатитом В после курсового лечения (6 мес.) Примечание: достоверность различий до и после лечения (*-Р<0,05)
Мембраностабилизирующий, антицитолитический и антиоксидантный эффекты йодантипирина в совокупности способствовали улучшению функционального состояния печеночной паренхимы. Это нашло отражение, в частности, в усилении белково-синтетической функции печени. У пациентов на фоне лечения йодантипирином наблюдалось большее увеличение общего белка, содержания альбуминов, а также уровня ПТИ и фибриногена.
Ценным свойством йодантипирина явилось и его антихолестатическое действие, несколько превосходящее подобный эффект амиксина и реаферона. Это выражалось в снижении активности щелочной фосфатазы (в 2,2 (Р<0,01) раза), нормализации содержания прямого билирубина, что соответствует литературным данным об улучшении пигментной и экскреторной функции печени.
Таким образом, результаты исследования позволяют констатировать значительную клиническую эффективность йодантипирина, обусловленную его противовирусный иммуномодулирующим и противовоспалительным действием, превосходящую терапевтическую активность амиксина и реаферона.
Каких либо побочных эффектов в процессе применения йодантипирина не выявлено.
Таблица
Динамика биохимических показателей
у больных хроническим гепатитом В после курсового лечения (6 мес.)
| Показатели | 1 группа (п=26) | 2 группа (п=13) | 3 группа (п=11) | |||
| Act (Е/л) | 95,0±0,29 | 26,0±0,97* | 94,0±0,37 | 32,0±0,94* | 94,0±0,72 | 40,0±0,46* |
| Алт (Е/л) | 115,0±0,83 | 30,0±0,91* | 105,0±0,79 | 35,0±0,39* | 110,0±0,61 | 42,0±0,72* |
| Общий билирубин мкмоль/л | 21,5±0,58 | 13,8±0,64* | 21Д±0,52 | 17,2±0,33* | 22,6±0,25 | 15,5±0,36* |
| Прямой билирубин мкмоль/л | 4,68±0,25 | 1,17±0,21* | 4,31±0,15 | 2Д±0,20* | 4,20±0,81 | 1,4±0,20* |
| Щелочная фосфатаза (е/л) | 133,0±0,37 | 60,0±0,98* | 104,0±0,99 | 71,0±0,54* | 96,5±0,91 | 63,0±0,92* |
| Общий белок (г/л) | 75,0±0,28 | 81,0±0,79* | 78,6±0,65 | 88,5±0,29* | 76,5±0,29 | 78,0±0,29* |
| Альбумины (г/л) | 42,0±0,45 | 50,0±0,64* | 43,4±0,68 | 48,0±0,58 | 48,0±0,56 | 48,0±0,57 |
| ?-глобулины (г/л) | 24,0±0,60 | 12,0±0,34* | 25,4±0,49 | 15,0±0,64* | 23,2±0ДЗ | 18,0±0,68* |
| ГГТП (U/L) | 23,0±0,98 | 12,0±0,57* | 10,9±0,35 | 11,0±0,35 | 32,2±0,54 | 17,3±0,71* |
| Тимоловая проба(Ед) | 5,4±0,32 | 2,0±0,11 | 4,8±0,22 | 2,5±0Д4* | 4,9±0,44 | 2,5±0,27* |
| ПТИ (%) | 88Д±0,45 | 90,0±0,40* | 86,3±0,6 | 88,0±0,52* | 84,5±0,50 | 86,0±0,5* |
| Фибриноген (г/л) | 2,46±0,31 | 2,95±0,21* | 2,51±0,25 | 2,93±0,20* | 2,44±0,28 | 2,87±0,28* |
| Холестерин (моль/л) | 5,2±018 | 4,6±0,17 | 5,0±0,15 | 4,7±0,17 | 5Д±0Д8 | 4,5±0,19 |
Примечание: достоверность различий до и после лечения (* - р<0,05).
Выводы и практические рекомендации.
- Йодантипирин – (1 фенил-2-3- диметил-4-йодпирозолон) в дозе 200мг в сутки 4 раза в неделю при курсовом(6 мес.) применении обладает противовирусной активностью у пациентов с хроническим вирусным гепатитом В и С умеренной степени активности,I стадии хронизации в фазе репликации.
- При курсовом применении йодантипирин, начиная с первого месяца, оказывает терапевтический эффект, максимум которого приходится на конец 3-го месяца лечения и более выраженный по сравнению с Амиксином:
- полностью купирует или ослабляет основные клинические проявления заболевания;
- положительно воздействует на функциональное состояние печени, купируя и ослабляя выраженность цитолитического,холестатического, мезенхимально-воспалительного синдромов, улучшая поглотительную, белковосинтети-ческую и выделительную функции.
- Йодантипирин при курсовом применении проявляет более выраженное, по сравнению с Амиксином ингибирующее действие на процессы ПОЛ у пациентов с HВV и HСV.
- Йодантипирин у больных HВV и HСV в большей степени, чем Амиксин обладает иммуномодулирующей активностью.
- При разовом и курсовом применении Йодантипирин хорошо переносится больными и не вызывает каких –либо побочных эффектов.
- Эндогенная интерферонизация безопаснее и эффективнее применения эндогенного интерферона.
Йодантипирин может быть рекомендован в качестве лечебного средства при хронических вирусных гепатитах В и С умеренной степени активности, I стадии хронизации (без признаков цирроза) в репликативной фазе.
Обследование больных хроническими вирусными гепатитами должно быть комплексным и включать, наряду с общеклиническими, лабораторными, инструментальными методами. Изучение иммунного и интерферонового статуса, что позволит определить возможности иммунитета и оценить эффективность проводимой терапии.
ЙОДАНТИПИРИН В КОМПЛЕКСНОЙ ТЕРАПИИ ГЕНИТАЛЬНОГО ОСТРОКОНЕЧНОГО КОНДИЛОМАТОЗА
Н.В. Шперлинг
Сибирский государственный медицинский университет
Кафедра дерматовенерологии
Зав. кафедрой – проф. П.Н. Пестерев
Научный руководитель – проф. П.Н. Пестерев
Генитальный остроконечный кондиломатоз (ГОК) в мире по числу случаев (около 30 миллионов в год) занимает третье место после трихомониаза и хламидиоза. Резистентность заболевания к терапии, высокая частота рецидивов (до 70 %) представляют клиническую проблему. Учитывая вирусную этиологию ГОК, вызываемого вирусом папилломы человека, перспективным направлением в лечении этого заболевания является разработка иммунотропной терапии. Одним из основных звеньев в цепи процессов формирования противовирусной защиты организма является система интерферона.
Препарат йодантипирин (1-фенил-2,3-диметил-4-йодпирозалон) разрешен Министерством Здравоохранения РФ для применения в медицинской практике. (Приказ МЗ и МП РФ от 13.08.96 № 316; Регистрационное удостоверение № ЛС 002505.) является индуктором эндогенного интерферона. Препарат уменьшает дегрануляцию тучных клеток, что предупреждает освобождение различных медиаторов воспаления, подавляюще влияет на ферменты, синтезирующие простагландины, а также тормозит синтез арахидоновой кислоты. Кроме того, йодантипирин снижает проницаемость мембран, что важно в процессе торможения воспаления. Одним из энергетических компонентов противовоспалительного действия является снижение интенсивности биологического окисления и торможение связанных с ним процессов фосфорилирования и угнетения образования АТФ в митохондриях. Препарат ингибирует репродукцию РНК- и ДНК-содержащих вирусов при участии генома клетки. Антивирусное действие осуществляется на стадии транскрипции генетической информации и является результатом феномена образования и выделения клетками человека видонеспецифичных антивирусных ингибиторов. Йодантипирин является эффективным индуктором интерферона: через 6 часов после введения препарат стимулирует образование интерферона в лейкоцитах. Препарат оказывает мембраностабилизирующее действие, что также обусловливает торможение проникновение вируса в клетку. Наряду с этим йодантипирин обладает иммуномодулирующей активностью, выражающейся в способности к индукции синтеза вируснейтрализующих антител, стимуляции клеточного иммунитета – зрелых Т-лимфоцитов, натуральных киллеров, хелперов, индукторов. Тормозит активность Т-супрессоров, модулирует клеточный, гуморальный иммунитеты.
Лечебно-профилактическое действие йодантипирина при вирусных инфекциях обусловлено сочетанием его противовоспалительной, вируснейтрализующей, интерферониндуцирующей, иммунокоррегирующей активности.
Эффективно применение йодантипирина при гриппе, парагриппе, ОРВИ, клещевом энцефалите, неполиомиелитные энтнровирусы Коксаки и ЕСНО, вирусные везикулярные стоматиты, герпес I и II, геморрагическая лихорадка, цитомегаловирусная инфекция. При приеме внутрь препарат быстро попадает в кровь, а его элиминация из организма осуществляется за счет почечной экскреции.
Детальные токсикологические исследования показали, что йодантипирин малотоксичен, не обладает мутагенными, эмбриотоксическими, тератогенными, аллергогенными и иммунотоксическими свойствами. Препарат хорошо переносится.
Свойство препарата влиять на вирус, вызывающий генитальный остроконечный кондиломатоз выявлено на основании интерпретации данных клинических наблюдений за данной категорией больных. Режим применения препарата установлен на основании клинических наблюдений за группами больных генитальным остроконечным кондиломатозом.
Клиническое применение нового метода лечения
Данным способом было пролечено 68 человек с экзофитной формой генитального остроконечного кондиломатоза и размерами бородавок до 0,5 см. Из них женщины (в возрасте от 16 до 57 лет) составили 60,3 % (со средними размерами бородавок от 0,1 до 0,5 см – 24 человека; с малыми размерами до 0,1 см – 17 человек; всего 41 человек). Мужчины (в возрасте от 17 до 58 лет) составили 39,7 % (со средними размерами бородавок от 0,1 до 0,5 см – 15 человек; с малыми размерами до 0,1 см – 12 человек; всего 27 человек). Кондиломатозные разрастания локализовались: у женщин – преимущественно в области больших и малых половых губ, клитора, устья уретры и прилегающих кожных покровов; у мужчин на эпителии крайней плоти, головки и уздечки полового члена, прилегающих кожных покровах.
Клинические наблюдения по применению йодантипирина для лечения генитального остроконечного кондиломатоза показали, что в течение 2-х лет после проведенной терапии не было зарегистрировано ни одного случая рецидива заболевания и проявлений индивидуальной непереносимости препарата. Это свидетельствует о высокой терапевтической эффективности йодантипирина и целесообразности его применения для лечения генитального остроконечного кондиломатоза.
Пример (выписка из амбулаторной карты):
Больная Ш., 20 лет, обратилась на прием к дерматовенерологу 7 июня 2000 года с жалобами на зуд в области входа во влагалище в течение 3 месяцев, который усилился в последние 2 недели, а также выделения из половых путей с резким запахом. Менструации регулярные, умеренные, безболезненные. Последняя менструация с 19 по 23 мая 2000 г. Беременностей – 0, половая жизнь с 19 лет, контрацепция – иногда презерватив.
Генитальный статус. Наружные половые органы сформированы правильно, уретра и бартолиниевы железы без особенностей. В области вульвы, преимущественно на задней спайке, множественные ворсинчатые разрастания до 0,5 см красного цвета с резким запахом. Стенки влагалища гиперемированы, шейка матки эрозирована, придатки без патологических изменений, выделения – умеренные бели. Выставлен предварительный диагноз: остроконечные кондиломы вульвы, подострый неспецифический вульвовагинит, псевдоэрозия шейки матки. По результатам дальнейшего обследования выявлено:
- мазок на степень чистоты влагалища от 7 июня 2000 г. – лейкоциты – единичные в поле зрения, плоский эпителий – большое количество, флора – кокковая, гонококки, трихомонады отсутствуют;
- цитологическое исследование от 7 июня 2000 г. – шейка матки – эпителий без особенностей, отпечаток с вульвы – гиперплазия плоского эпителия;
- множественные пойкилоциты (пойкилоцитоз – патогномичный признак остроконечного кондиломатоза);
- кольпоскопия от 13 июня 2000 г. – незаконченная зона трансформации.
С учетом результатов исследований выставлен диагноз: аногенитальные бородавки вульвы, псевдоэрозия шейки матки.
Больная получала традиционное лечение: местное лечение солковагином (две аппликации с интервалом в одну неделю). После аппликации на 3–5 день происходило отторжение кондилом. Полная эпителизация слизистой завершилась к концу первой недели. При контрольном осмотре через 1,5 месяца выявлен рецидив заболевания в виде появления новых разрастаний прежней локализации размерами до 0,3 см. Цитологическое исследование от 20 августа 2000 г. выявило наличие пойкилоцитов. Назначен новый курс лечения: одновременно с местной обработкой солковагином по прежней схеме добавлен индуктор эндогенного интерферона йодантипирин по 100 мг 2 раза в день в течение 25 дней и в последующем по 100 мг 1 раз в день в течение 50 дней. Через две недели отмечалось исчезновение остроконечных кондилом. При контрольных осмотрах через 1,3,5,6 и 12 месяцев рецидивов не отмечено. Цитологическое исследование от 28 декабря 2000 г. без патологии. Больная снята с учета 14 декабря 2001 года.
Заключение
Таким образом, предлагаемый способ лечения генитального остроконечного кондиломатоза позволяет добиться стойкого клинического эффекта у больных остроконечным кондиломатозом с размерами бородавок до 0,5 см, а именно снизить частоту рецидивов заболевания. Это, несомненно, определяет предложенный способ лечения как более эффективный по сравнению с известными на сегодняшний день способами терапии данной нозологии. Кроме того, отсутствие аллергенных свойств и побочных эффектов йодантипирина, а также пероральный способ его применения, позволяющий избежать постинъекцтонных осложнений, относительная дешевизна и доступность приобретения препарата в сети аптек, изготовление йодантипирина отечественными производителями позволяют широко применять данный способ лечения практически у всех больных, обратившихся по поводу генитального остроконечного кондиломатоза как в стационарных, так и в амбулаторных условиях.
