Урок по теме «Периодический закон и периодическая система химических элементов Д. И. Менделеева»
| Вид материала | Урок |
СодержаниеПодготовительный период Вопросы для Задание№2 « По улицам ходили» ( работа в группах) Задание№5 « Что в имени моём» Химический кроссворд |
- Тема урока: «Периодический закон и периодическая система химических элементов, 266.68kb.
- Урок а «Периодический закон и периодическая система химических элементов Д. И. Менделеева.», 106.31kb.
- Химических элементов д. И. Менделеева. 8 Класс, 47.65kb.
- Закон и периодическая система химических элементов Д. И. Менделеева" Значение и место, 131.75kb.
- Урока «периодический закон и периодическая система химических элементов д. И. Менделеева», 105.86kb.
- Звездный час квн по теме Периодический закон и периодическая система химических элементов, 105.35kb.
- Бековского района пензенской области, 115.96kb.
- И. А. Моу «исош №1» п. Ивня Игра по химии «Умники и умницы» Тема: «Периодический закон, 114.97kb.
- Конкурсное задание «учебное занятие»13 апреля, 71.51kb.
- Применение коллективного способа обучения при изучении темы «Периодический закон, 94.15kb.
Обобщающий урок по теме
« Периодический закон и периодическая система химических элементов
Д.И.Менделеева»
Цели:
Обобщить знания школьников по теме, выявить степень усвоения материала, расширить кругозор, повысить творческую активность учащихся, умение работать коллективно, работать с дополнительной литературой.
Оборудование:
Портрет Д.И.Менделеева; кроссворд (на плакате); журнальные, газетные материалы о Д.И.Менделееве; таблица- периодическая система химических элементов Д.И .Менделеева
Подготовительный период
За две недели до итогового урока учитель ориентирует учащихся на то, что они должны знать и уметь по данной теме. В кабинете вывешиваются памятки, перечень вопросов, на которые следует обратить внимание. Предлагаются также темы рефератов.
Вопросы для подготовки к уроку по теме «Периодический закон и периодическая
система химических элементов Д.И.Менделеева в свете теории строения атома»
1. Д.И.Менделеев: жизнь и деятельность.
2. Периодический закон и периодическая система химических элементов Д.И.Менделеева (ПСХЭ). Структуры периодической системы: большие и малые периоды, группы и подгруппы. Зависимость свойств элементов и образуемых ими соединений от положения элемента в периодической системе и строения атома.
3. В чем причина периодичности изменения свойств элементов?
4. Дайте определение понятиям «период», «группа», «подгруппа» с точки зрения строения атома.
5. Расположите элементы в порядке усиления неметаллических свойств: водород, фтор, сера, азот, хлор.
6. Определите положение элементов в периодической системе (период, группа, подгруппа) по электронным формулам:
а) 1s22s22p63s23p4; б) 1s22s22p1; в) 1s22s22p63s1; г) 1s22s2; д) 1s22s22p63s23p63d104s24p5.
7. Значение периодического закона и ПСХЭ Д.И.Менделеева.
Модель решения задания 6. В атоме элемента с электронной формулой
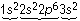 три электронных слоя, значит, элемент находится в 3-м периоде. Последним в атоме заполняется s-подуровень, следовательно, это элемент главной подгруппы. На внешнем электронном слое атома находятся два электрона, поэтому это элемент II группы – магний Мg.
три электронных слоя, значит, элемент находится в 3-м периоде. Последним в атоме заполняется s-подуровень, следовательно, это элемент главной подгруппы. На внешнем электронном слое атома находятся два электрона, поэтому это элемент II группы – магний Мg.Темы рефератов
1. Великий закон сегодня.
2. Современное содержание периодического закона.
3. История открытия периодического закона.
4. Жизнь и деятельность Д.И.Менделеева.
5. Три службы Родине.
6. Значение периодического закона Д.И.Менделеева для науки и техники.
7. Научный подвиг Д.И.Менделеева.
8. История открытия какого-либо (по выбору) химического элемента.
Ход урока
Учитель: Сегодня мы посетим с вами сказочную страну «Менделеевская». Жители страны живут по своим законам, имеют свои обычаи.
Другого ничего в природе нет
Ни здесь, ни там, в космических глубинах:
Все -от песчинок малых до планет-
Из элементов состоит единых.
Как формула, как график трудовой,
Строй менделеевской системы строгий.
Вокруг тебя творится мир живой,
Входи в него, вдыхай, руками трогай.
Задание №1
На границе страны детей встречают стражники ( 2 учащихся консультанта) и задают вопросы для того, чтобы попасть в эту страну:
1 Кто и когда закон открыл?
2. Как звучит современная формулировка периодического закона?
3.Где учился Д.И.Менделеев. Кто были его родители?
4. Найдите электронную конфигурацию атома химического элемента неона
а) 1s22s2 – I гр.;
б) 1s22s22p3 – V гр.;
в) 1s22s22p4 – VI гр.;
г) 1s22s22p6 – VIII гр.
5. Что общего в строении атомов:
а) всех химических элементов;
б) элементов одной и той же группы главной подгруппы?
6. Что такое изотопы? В чем различие между ними?
7.В чем вы видите значение периодического закона для науки, техники, промышленности?
Задание№2 « По улицам ходили» ( работа в группах)
Карточка 1. Напишите электронную формулу и постройте энергетическую диаграмму для следующих атомов: калия, магния, кальция. Какую валентность могут проявлять эти элементы в соединениях?
Карточка 2. Укажите знаком «
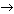 » ослабление металлических свойств и усиление неметаллических в следующих пятерках элементов. Объясните, на каком основании расставлены знаки.
» ослабление металлических свойств и усиление неметаллических в следующих пятерках элементов. Объясните, на каком основании расставлены знаки.
Карточка 3. У атомов каких элементов внешние электроны прочнее связаны с ядром:
а) хлора или брома;
б) фтора или йода;
в) кремния или фосфора?
Проверяют и комментируют выполненные задания ученики-консультанты.
Задание 3 « Расскажи мне обо мне»
1. Дать характеристику элементу №23
2. Дать характеристику элементу №45
3. Дать характеристику элементу №37
 При характеристике элемента рекомендуем придерживаться следующего плана:
При характеристике элемента рекомендуем придерживаться следующего плана:1. Положение элемента в ПСХЭ Д.И.Менделеева и строение его атома.
2. Характер простого вещества – металл, неметалл или переходный металл.
3. Сравнение свойств заданного простого вещества со свойствами простых веществ, образованных соседними по подгруппе элементами.
4. Сравнение свойств заданного простого вещества со свойствами простых веществ, образованных соседними по периоду элементами.
5. Состав высшего оксида, его характер (основный, кислотный, амфотерный).
6. Состав высшего гидроксида, его характер (кислота, основание, амфотерный гидроксид).
7. Состав летучего водородного соединения (для неметаллов).
Задание №4 «Составь код»
Учитель: Некоторые жители страны не могут попасть домой. Давайте им поможем.
1. Какая из приведенных схем соответствует строению атома натрия:

а) 2 8 3 б) 2 8 1 в) 2 8 7 г) 2 8 4
2. Укажите электронную формулу атома азота:
a) Is22s22p63s23p2; б) Is22s22p3; в) ...2s22p3; г) Is22s22p1.
3. Какая из приведенных схем распределения электронов по орбиталям соответствует атому бора:

4. Сколько энергетических уровней имеется в атоме с порядковым номером 29:
а)1; 6)3; в) 4; г) 5?
5. Схема распределения электронов по энергетическим уровням 2, 7 соответствует атому:
а) хлора; б) фтора; в) брома; г) азота.
6. Электронная формула Is22s22p63s23p4 соответствует атому:
а) серы; б) кислорода; в) бериллия; г) кремния.
7. Укажите электронную формулу наружного уровня атомов элементов главной подгруппы I группы:
a) Is1; б)...2s1; в)...3s1; г) ...(3d10)4s1
8. Число электронов на внешнем энергетическом уровне элементов главной подгруппы VII группы:
а) 2; 6)3; в) 5; г) 7 1. Какая из приведенных схем соответствует строению атома натрия:

а) 2 8 3 б) 2 8 1 в) 2 8 7 г) 2 8 4
2. Укажите электронную формулу атома азота:
a) Is22s22p63s23p2; б) Is22s22p3; в) ...2s22p3; г) Is22s22p1.
3. Какая из приведенных схем распределения электронов по орбиталям соответствует атому бора:

4. Сколько энергетических уровней имеется в атоме с порядковым номером 29:
а)1; 6)3; в) 4; г) 5?
5. Схема распределения электронов по энергетическим уровням 2, 7 соответствует атому:
а) хлора; б) фтора; в) брома; г) азота.
6. Электронная формула Is22s22p63s23p4 соответствует атому:
а) серы; б) кислорода; в) бериллия; г) кремния.
7. Укажите электронную формулу наружного уровня атомов элементов главной подгруппы I группы:
a) Is1; б)...2s1; в)...3s1; г) ...(3d10)4s1
8. Число электронов на внешнем энергетическом уровне элементов главной подгруппы VII группы:
а) 2; 6)3; в) 5; г) 7
Задание№5 « Что в имени моём»
Какие химические элементы названы в честь ученых, в память успехов в астрономии, в честь городов, в честь стран и континентов. Записывают в тетради название и порядковые номера; время ограничено. Проверяются консультантами.
Учитель :Молодцы ребята сколько вы много знаете о химических элементах. А теперь давайте погадаем кроссворд.
Задание №6
Химический кроссворд
Разгадывают кроссворд все ученики. Консультанты оценивают участие одноклассников в этом конкурсе.
Ключевое слово – фамилия русского ученого, девизом всей деятельности которого были слова: «Посев научный взойдет для жатвы народной».

По горизонтали:
1. Химический элемент VII группы 4-го периода ПСХЭ Д.И.Менделеева, впервые выделенный из руды в 1774 г. К.Шееле.
2. Химический элемент VI группы, который образует в свободном состоянии несколько аллотропных модификаций и является типичным полупроводником.
3. Химический элемент, который получил название от характерных для него синих (цвет индиго) спектральных линий.
4. Первый элемент ПСХЭ Д.И.Менделеева.
5. Химический элемент, получивший свое название в честь континента.
6. Химический элемент, конфигурация внешнего энергетического уровня которого 3s23p5.
7. Газ, дающий красное свечение газосветных ламп и утверждающий, что он – это не он.
8. Металл, занимающий второе место по тепло- и электропроводности.
9. Радиоактивный элемент, названный в знак признания заслуг выдающегося русского ученого.
Ответы. 1. Марганец. 2. Селен. 3. Индий. 4. Водород. 5. Европий. 6. Хлор. 7. Неон. 8. Медь.
9. Менделевий.
Ключевое слово – Менделеев.
Учитель подводит итоги урока, отмечает активных учеников.
