Учебно-методический комплекс по дисциплине: «Высокомолекулярные соединения» для студентов 4 курса очной формы обучения Направление 020100 Химия
| Вид материала | Учебно-методический комплекс |
- Учебно-методический комплекс по дисциплине: «Элементоорганическая химия» для студентов, 602.47kb.
- Учебно-методический комплекс по дисциплине цикла гсэ. Ф. 06 Для студентов очной формы, 809.49kb.
- Учебно-методический комплекс по дисциплине цикла опд. Ф. 17 Для студентов очной формы, 350.17kb.
- Учебно-методический комплекс для студентов очной формы обучения по специальностям:, 555.7kb.
- Учебно-методический комплекс для студентов очной формы обучения по специальностям:, 805.3kb.
- Учебно-методический комплекс дисциплины цикла ен. Н-в. 00 для студентов очной и заочной, 322.68kb.
- Учебно-методический комплекс по дисциплине цикла дс. 04 для студентов очной формы обучения, 784.69kb.
- Учебно-методический комплекс по дисциплине цикла опд. Ф. 12 Для студентов очной формы, 1316.74kb.
- Учебно-методический комплекс по дисциплине цикла опд. В. 01а для студентов очной формы, 669.3kb.
- Учебно-методический комплекс по дисциплине цикла опд. Ф. 05 Для студентов очной и заочной, 647.4kb.
ПРИМЕР ЛЕКЦИИ
Синтез полимеров. Полимеризация.
В лекции будут рассмотрены следующие вопросы:
- Особенность процесса получения полимеров полимеризацией.
- Радикальная полимеризация: инициирование, реакции передачи цепи, рост макрорадикалов, обрыв цепи.
- Влияние различных факторов на радикальную полимеризацию.
Полимеры синтезируются из НМС (мономеров) путем многократно повторяющихся однотипных реакций. Образование макромолекул полимера может быть следствием разрыва двойных связей (например, олефинов), раскрытия циклов в циклических соединениях, перегруппировок в функциональных группах полифункциональных веществ (ступенчатая полимеризация), реакций функциональных групп полифункциональных веществ с выделением побочных продуктов (поликонденсация).
Полимеризацией называется реакция синтеза ВМС путем последовательного присоединения молекул мономера в результате разрыва двойных связей или раскрытия цикла к активному центру растущей макромолекулы, звенья которой остаются идентичными по составу и взаимному сочетанию атомов молекулам мономера. Полимеризация подчиняется законам цепных реакций.
1. Особенность процесса:
- молекула мономера содержит кратные связи или неустойчивый цикл
- процесс протекает без образования существенных количеств побочных продуктов
- полимер и мономер имеют один и тот же элементарный состав
- в условиях, применяющихся при введении процесса, реакция обычно практически необратима.
Процесс полимеризации протекает с разрывом одних валентных связей и с возникновением новых. Разрыв может происходить так, что электронная пара ковалентной связи остается целиком у одного из двух ранее связанных атомов (гетеролитический разрыв): в других случаях эта пара разделяется и у каждого атома остается по одному электрону (гомолитический разрыв):

гетеролитический гомолитический
разрыв разрыв
Гетеролитический разрыв приводит к образованию ионов, а гомолитический - к возникновению свободных радикалов с неспаренными электронами. В соответствии с этим различают ионную полимеризацию, протекающую через стадию образования ионов, и радикальную, в которой участвуют свободные радикалы.
Такие мономеры, как винилхлорид и винилиденхлорид, обычно полимеризуются по радикальному механизму, а изобутилен, простые виниловые эфиры - по ионному. Многие мономеры (стирол, акрилаты, бутадиен, этилен) способны в зависимости от метода возбуждения полимеризации реагировать как по ионному, так и по радикальному механизму.
2. Радикальная полимеризация
Радикальная полимеризация является одним из наиболее распространенных методов синтеза полимеров из НМС. Процесс образования каждой макромолекулы включает следующие реакции: возникновение свободного радикала, последовательное присоединение к нему молекул мономера с сохранением каждый раз в концевом звене свободной валентности (т.е. с сохранением свойств свободного радикала) и, наконец, прекращение роста макрорадикала. Схематически такой процесс можно изобразить следующим образом:
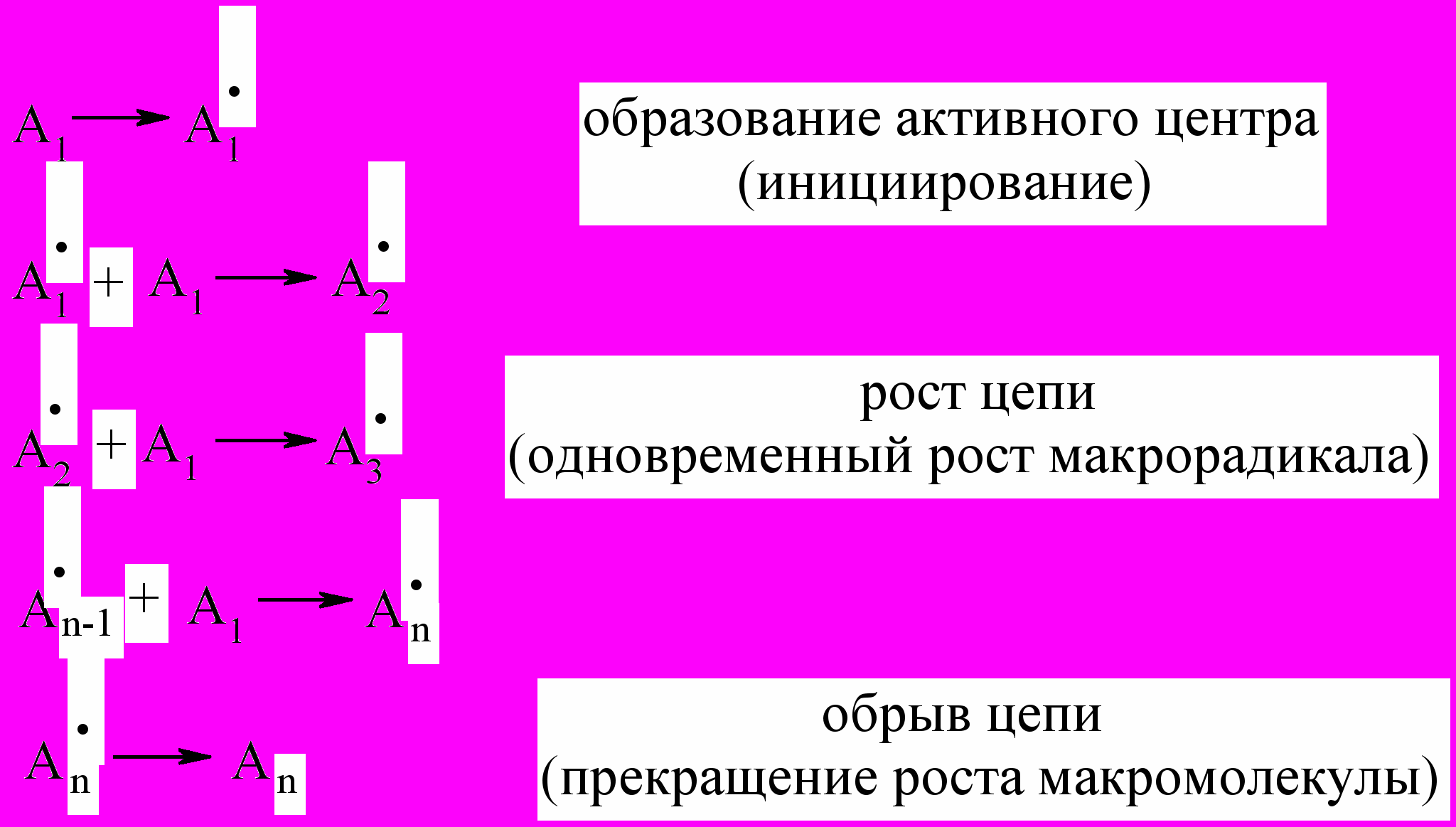

При радикальной полимеризации происходит присоединение радикала к молекуле мономера с появлением нового радикала, удлиненного на один остаток мономера по сравнению с исходным радикалом. Следовательно, при радикальной полимеризации наблюдается не только передача энергии одного элементарного акта, необходимой для осуществления следующего, но также увеличение длины самого радикала, рост его при последовательном присоединении к нему мономерных молекул. Растущая полимерная частица остается свободным радикалом (макрорадикалом) вплоть до обрыва цепи вследствие столкновения со вторым радикалом или других каких-либо причин.
Факт образования длинных цепей показывает, что рост цепи является гораздо более вероятным процессом, чем обрыв или ее инициирование. Важная особенность радикальной полимеризации состоит в том, что прекращение роста макрорадикала не обязательно означает, что цепная реакция окончена. Иногда свободная валентность растущего макрорадикала насыщается при его столкновении активным концом с подвижными атомами или функциональными группами молекул мономера, полимеров, растворителей и т.д. Переход подвижных атомов к макрорадикалу приводит к возникновению нового радикала, который инициирует новую цепь - происходит передача цепи. Для выявления влияния различных факторов на процесс радикальной полимеризации рассмотрим каждую стадию в отдельности.
Инициирование. Образование первичных радикалов (инициирование) может быть вызвано действием тепла (термическая полимеризация), света (фотополимеризация), радиоактивного облучения (радиационная полимеризация), специальными инициаторами (инициированная «химическая» полимеризация) и т.д.
В чистом виде термическая полимеризация наблюдается редко, т.к. ничтожные примеси кислорода и других веществ могут выполнить роль инициаторов, ингибиторов и т.д. особенно при повышенной температуре, искажая «чисто термический» характер реакции. Общая скорость термической полимеризации пропорциональна квадрату концентрации мономера. Благодаря высокой энергии активации термического инициирования термическая полимеризация протекает медленно, а скорость ее сильно зависит от температуры. Например, ММА при 70°С образуется только 0,0081% полимера в час, а при 130°С - 0,125%. При термической полимеризации нарушается регулярность строения макромолекулы. Все выше сказанное является причиной того, что практического интереса она не представляет.
Фотополимеризация инициируется освещением мономера, помещенного в кварцевый сосуд, ртутной лампой, снабженной светофильтром (обычно с ~ 3000 А). Реакцию проводят в атмосфере азота. Степень освещения легко дозировать и регулировать, поэтому метод нашел широкое применение при изучении процесса полимеризации. При наличии двух различных типов двойной связи в молекуле мономера можно, применяя соответствующие длины волн, вызвать полимеризацию за счет одной такой связи, не затрагивая второй, предполагаемый механизм: молекула мономера, поглотив квант света, возбуждается; при соударении возбужденной молекулы со второй молекулой мономера может произойти дезактивация возбужденной частицы с рассеянием избыточной энергии и образования бирадикала, который диспропорционируется в монорадикалы:
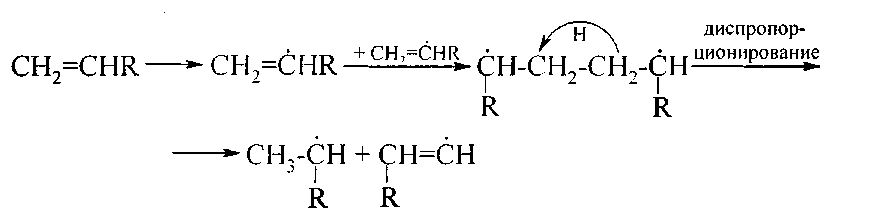
Скорость фотополимеризации пропорциональна квадратному корню из интенсивности облучения.
Скорость полимеризации возрастает в присутствии фотосенсибилизаторов (бензоил, динитрил азодиизомасляной кислоты), которые распадаются на свободные радикалы под действием света даже при комнатной температуре.
У разных мономеров скорость фотополимеризации различна. Например, винилиденхлорид, метилметакрилат, хлоропрен, винилметилкетон и др. имеют значительную скорость фотополимеризации, а стирол и -метилстирол под влиянием света полимеризуются медленно.
Радиационная полимеризация во многом напоминает светополимеризацию. Скорость полимеризации пропорциональна корню квадратному из интенсивности облучения (интенсивность не более 100 рентген в минуту).
Облучение проводится -, -, -лучами, ускоренными электронами, протонами и т.д., а возникающие при этом свободные радикалы инициируют полимеризацию. Максимальная скорость полимеризации наблюдается у винил-ацетата, а минимальная - у стирола. Если молекулы растворителя при облучении легко расщепляются на свободные радикалы, то полимеризации в растворе протекает быстрее, нежели в отсутствии растворителя. Однако при увеличении количества растворителя резко возрастает число свободных радикалов, обрывающих цепь, что ведет к снижению молекулярной массы полимера.
Рассмотренные виды радикальной полимеризации вследствие малой скорости образования свободных радикалов протекают сравнительно медленно и, кроме того, часто сопровождаются нежелательными побочными процессами. На практике чаще всего применяют химическое инициирование, полимеризацию проводят в присутствии специально добавленных веществ - инициаторов, легко распадающихся на свободные радикалы в условиях полимеризации.
Среди инициаторов наиболее широкое распространение нашли перекиси (перекись бензоила, гидроперекиси бутила, изопропилбензола, персульфаты M2S2О8; M=Na, К, NH4) и азо- и диазосоединения (диазоаминобензол, динит-рил-азо-изомаеляной кислоты).
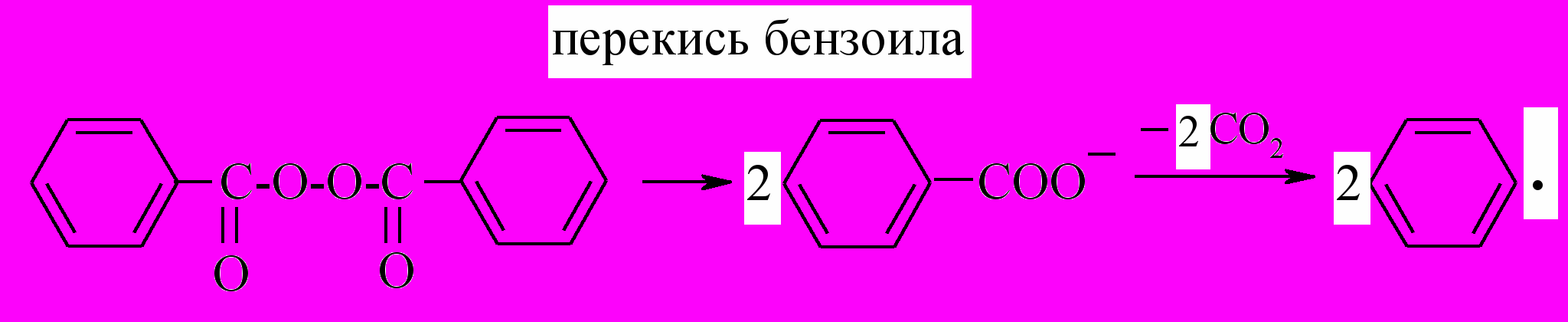
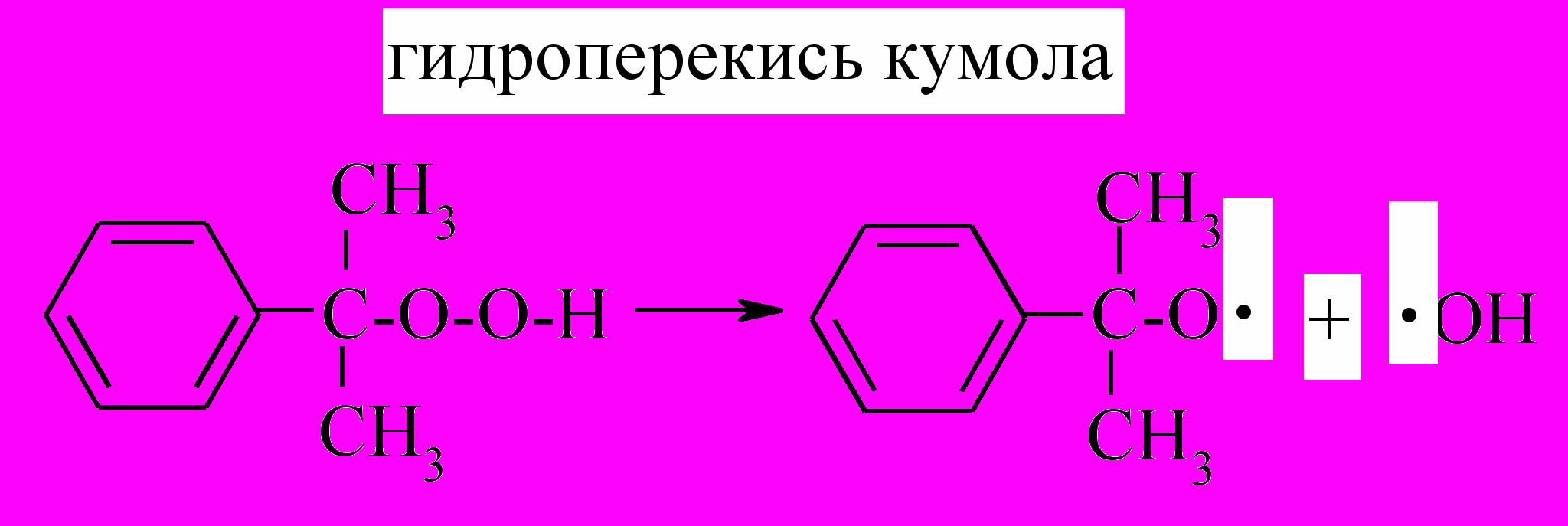
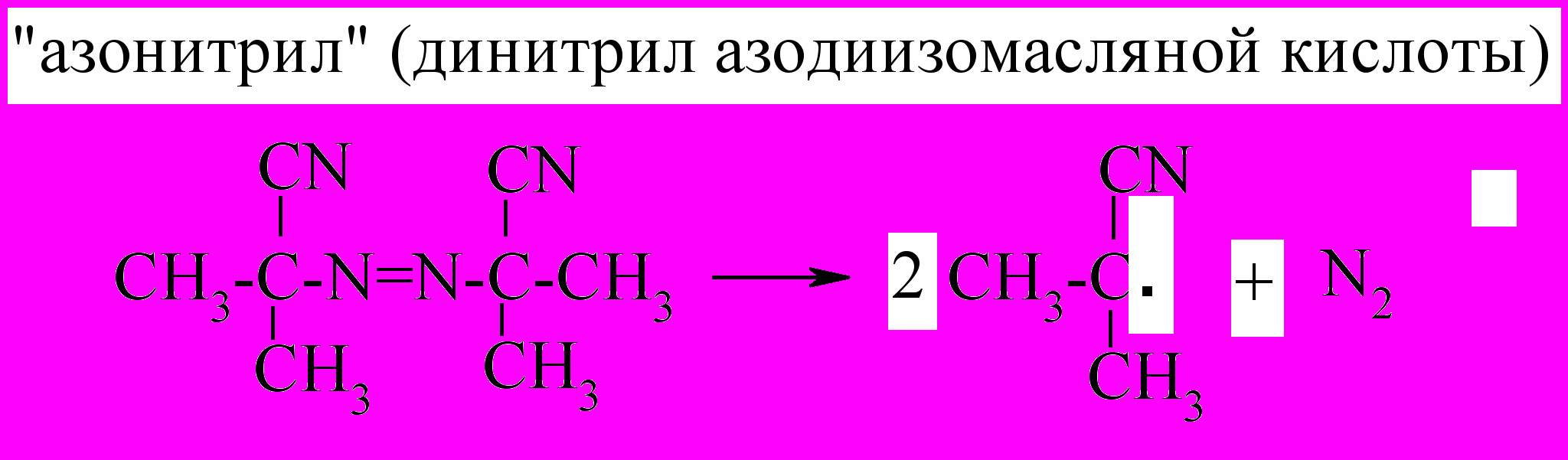
Полученные свободные радикалы присоединяют молекулу мономера с образованием новых радикалов и т.д.
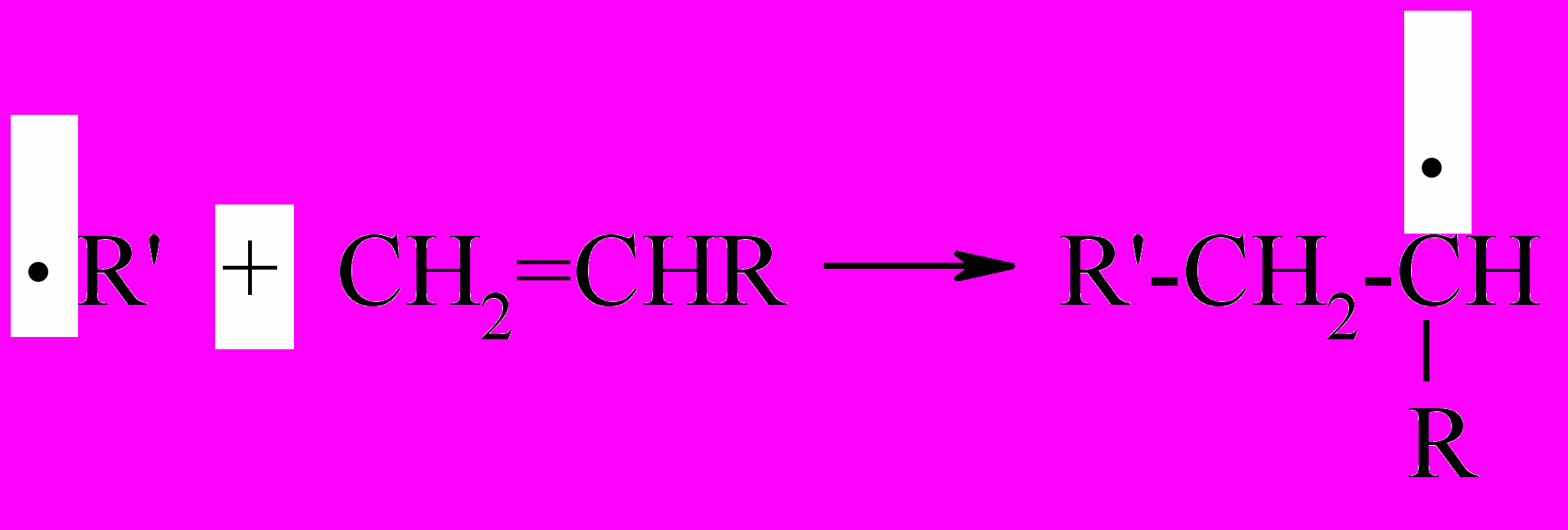
В соответствии с приведенным механизмом действия инициатора макромолекула должна содержать его осколки, что подтверждается экспериментально. В том, что инициатор расходуется во время реакции и его осколки становятся частью макромолекулы, заключается принципиальное отличие инициированной полимеризации от каталитических процессов подобного рода.
Исследования показывают, что не все радикалы, образовавшиеся из инициатора, инициируют полимеризацию (если это меченые атомы, то легко проследить). Поэтому возникло понятие «эффективность инициирования», представляющее собой долю полученных при распаде инициатора свободных радикалов, участвующих в инициировании.
При диссоциации в жидкой среде образовавшаяся пара радикалов оказывается «в клетке». Радикалы близко расположены друг к другу и могут рекомбинировать. Это явление называется первичной рекомбинацией или клеточным эффектом. В дальнейшем вследствие беспорядочного диффузионного движения молекул расстояние между первичными радикалами увеличивается. Тем не менее считают, что вероятность рекомбинации остается, т.е. в состав цепи войдут только те радикалы, которым удалось избежать первичной рекомбинации.
Скорость распада перекисных и гидроперекисных инициаторов можно увеличить повышением температуры, но можно и введением в реакционную среду восстановителей, играющих роль активаторов (окислительно-восстановительная полимеризация). Например, перекись водорода (окислитель) - соли 2-х валентного железа (восстановитель):

Вместо солей пользуются восстановителями: третичные амины, сульфиты, тиосульфаты, оксикислоты, аскорбиновая кислота и др.
Окислительно-восстановительные системы позволяют эффективно проводить полимеризацию при низких температурах, причем разветвлений у макромолекул синтетических диеновых каучуков не наблюдается.
Рост макрорадикалов. Рост цепи длится всего несколько секунд и заканчивается ее обрывом. Скорость полимеризации на начальных этапах реакции является постоянной величиной, по мере возрастания вязкости системы скорость падает в результате образования значительных количеств полимера. Например, рост макрорадикалов винилацета после полимеризации 57% мономера в 3 раза меньше начальной и в 22 раза меньше, когда процесс достигает 65% полимеризации мономера. До наступления изменения константы скорости роста цепи средняя молекулярная масса полимера практически не зависит от времени полимеризации.
Цепная полимеризация часто сопровождается реакциями передачи цепи. Передача цепи протекает обычно при взаимодействии активных центров или растущих радикалов с примесями или растворителем. Например, если растущая цепь обладает достаточной энергией для разрыва связи находящейся молекулы в растворе АВ, то при соударении такого радикала с молекулой АВ происходит обрыв молекулярной цепи с одновременным возникновением нового свободного радикала по схеме:
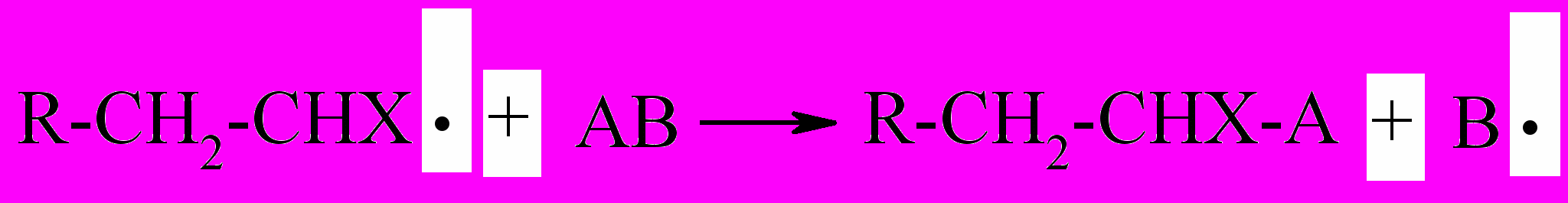
Новый радикал может инициировать образование новой молекулярной цепи:

Реакционная цепь распадается на несколько молекулярных цепей, что приводит к снижению молекулярной массы.
При полимеризации передача цепи может происходить через молекулы растворителя, различные вещества, специально вводимые в полимеризующуюся систему, макромолекулы полимера.
Передача цепи через полимер с образованием разветвленных полимеров наблюдается при полимеризации многих мономеров на глубоких стадиях превращения. Эту реакцию используют для получения привитых сополимеров.
Путем введения в реакционную среду веществ, через которые легко осуществляется передача цепи, можно регулировать среднюю молекулярную массу и получать полимеры с меньшей степенью полидисперсности и разветвленности. Такие вещества называют регуляторами. В качестве регуляторов полимеризации применяют хлорированные углеводороды (тетрахлорэтилен, СCl4), меркаптаны, меркаптаноуксусную кислоту и др.
Обрыв цепи. Процесс, приводящий к насыщению свободной валентности растущего радикала и не сопровождающийся возникновением нового радикала, называется обрывом цепи. В зависимости от величины, активности и строения макрорадикала, от вязкости среды, температуры, состава реакционной смеси и др. факторов, механизм обрыва может быть различным:
- - растущие макрорадикалы присоединяются друг к другу (рекомбинация);
- - радикалы диспропорционируются;
- - продукты распада инициатора присоединяются к радикалу (обрыв на инициаторе);
4 - ингибиторы присоединяются к радикалу (обрыв на ингибиторе).
Теперь остановимся на механизме 2-х видов обрыва:
1 - макрорадикалы, сталкиваясь своими активными концами, соединяются в неактивную макромолекулу, на концах которой находятся осколки инициатора:
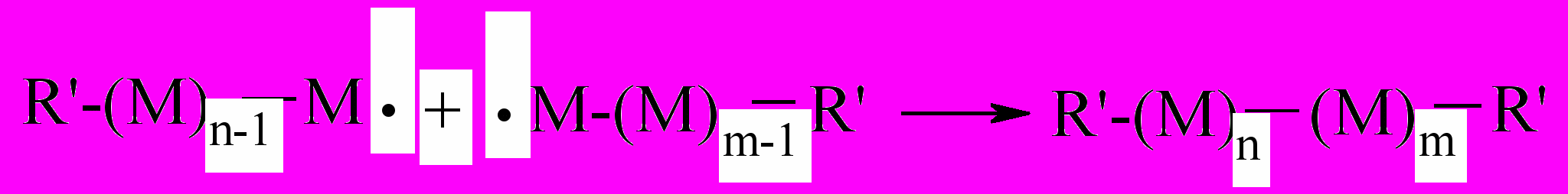
М - мономерный остаток. Скорость рекомбинации мало зависит от температуры, что связано с незначительной активацией этого процесса.
2 - при диспропорционировании один растущий радикал насыщается вследствие отщепления Н, Cl и т.д. от второго радикала; в результате образуются две макромолекулу, одна из которых содержит двойную связь в концевом звене.
При таком механизме обрыва осколки инициатора будут находиться только на одном конце макромолекулы (при рекомбинации осколки на обоих концах).
Ингибиторы. При передаче цепи может образоваться малореакционноспособный радикал, который не способен продолжить реакционную цепь. Это приводит к обрыву реакционной цепи и полному прекращению реакции полимеризации. Это ингибиторы процесса полимеризации. Ингибиторами могут быть вещества различных классов органических и неорганических соединений. Количество ингибитора, достаточное для предохранения мономера от полимеризации в течение длительного времени колеблется от 0,1 до 1% от веса мономера.
Явление обрыва и передачи цепи широко используется на практике для предотвращения преждевременной полимеризации при хранении мономеров и для регулирования процесса полимеризации.
Механизм ингибирования на примере гидрохинона, действие которого сводится к начальному окислению ингибитора в хинон кислородом воздуха, а затем хинон, присоединяя свободные радикалы или растущие цепи, образует, например, неактивные эфиры гидрохинона:
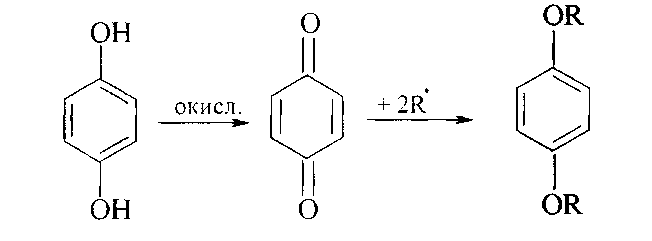
В результате резко сокращается концентрация свободных радикалов и полимеризация практически не осуществляется. Ингибиторы используются при перегонке мономеров, при проведении химических реакций, синтезе и т.п.
При производстве клеящих и пропитывающих составов полимеризацию останавливают при помощи ингибиторов на стадии образования промежуточных вязких продуктов, а перед применением добавляют дополнительное количество инициатора, достаточное для взаимодействия с ингибитором и возбуждения дальнейшей полимеризации.
Действие регуляторов отличается от действия ингибиторов тем, что новые радикалы, полученные в результате передачи цепи, настолько активны, что их появление не оказывает заметного влияния на скорость полимеризации. Однако, вызывая преждевременный обрыв цепи, они снижают молекулярную массу полимера.
Участие ингибиторов и регуляторов в обрыве и передачи цепи подтверждается наличием продуктов их распада и полимерах.
Роль кислорода и примесей при радикальной полимеризации. Кислород, поглощающийся мономером из атмосферы, занимает в процессах радикальной полимеризации особое место. Присутствие О2 может облегчить или затруднить полимеризацию в зависимости от природы мономера и условий процесса. Например, замедляет фотополимеризацию винилацетата, но ускоряет - стирола. Двойное поведение О2 объясняется способностью образовывать при реакции с мономерами перекиси или гидроперекиси.
Если полученные перекиси устойчивы - полимеризация замедляется, если нестойки (разлагаются на радикалы) - полимеризация может ускоряться. Иногда с растущими цепями О2 дает перекисные радикалы ... -CH2-CHR-О-О, активность которых недостаточна для присоединения новых мономерных молекул. Обрыв происходит вследствие взаимодействия двух таких радикалов между собой (меньшая энергия). Образующиеся при этом полимеры низкомолекулярны.
Различные примеси и загрязнения (в мономере) по своему действию аналогичны во многом кислороду. Степень вредности примесей определяется их химической природой и реакционной способностью по отношению к активным частицам (радикалы, атомы и др.), возникающим при полимеризации. Ввиду цепного характера реакции полимеризации даже ничтожные загрязнения могут играть существенную роль. Например, бутилен при полимеризации этилена и пропилена ускоряет полимеризацию.
3. Влияние различных факторов на радикальную полимеризацию
Один и тот же фактор может по-разному влиять на инициирование, рост и обрыв цепи (на передачу цепи). Рассмотрим влияние температуры:
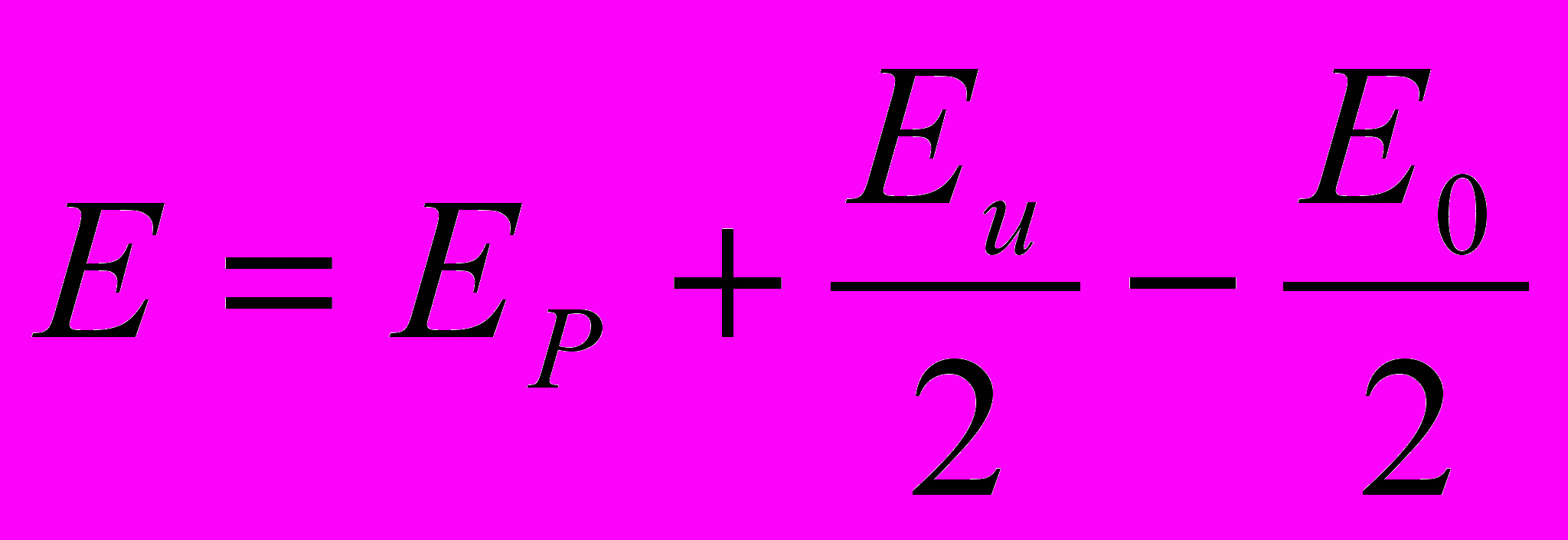
Е - общая энергия активации;
Ер - энергия активации роста (7 ккал/моль);
Еи - энергия активации инициировании (30 ккал/моль);
Е0 - энергия активации обрыва цепи (3-5 ккал/моль).
Получаем Е порядка 20 ккал/моль, что соответствует повышению скорости в 2-3 раза при возрастании температуры на 10°С. Еи велика по сравнению с Ер и Е0, следовательно, повышение температуры значительно больше влияет на инициирование, чем на рост и обрыв цепи. Поэтому влияние температуры на радикальную полимеризацию связано, прежде всего, с изменением скорости инициирования.
Средняя степень полимеризации уменьшается с увеличением температуры (падает с возрастанием температуры). Это положение подтверждено многочисленными экспериментами. Молекулярная масса полимера падает с ростом температуры полимеризации. Кроме всего вышеперечисленного повышение температуры усиливает рост побочных реакций.
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ОРГАНИЗАЦИИ САМОСТОЯТЕЛЬНОЙ РАБОТЫ СТУДЕНТОВ
Изложены в прилагаемых пособиях:
- В.М. Кареева Методические указания для самостоятельной работы по дисциплине «Высокомолекулярные соединения». – ТвГУ, Тверь. – 2001.
- В.М. Кареева Задачи и тестовые задания по дисциплине «Высокомолекулярные соединения». – ТвГУ, Тверь. – 2003.
ПРИМЕРЫ РЕЙТИНГОВЫХ ЗАДАНИЙ ПО ДИСЦИПЛИНЕ
«Высокомолекулярные соединения»
Контрольная работа №1
1. Что является катализатором анионной полимеризации:
а) вещества основного, электродонорного характера, щелочные металлы, их гидриды и амиды;
б) органические соединения металлов 1 и 2 групп периодической системы Д.И. Менделеева;
в) органические пероксиды, гидроперекиси, азотсоединения;
г) протонные кислоты (H2S04, H3P04, НСЮ4) и кислоты Льюиса (соединения формулы МеХn, где Me - металл, X - галоген: BF3, A1C13, SnCl4)?
2. Во сколько раз изменится средняя степень полимеризации х полимера при полимеризации метилакрилата в массе, инициированной разложением азо-бис-изобутиронитрила при 70°С, если увеличить концентрацию инициатора в 4 раза (влиянием реакции передачи цепи пренебречь):
а) не изменится;
б) увеличиться в 2 раза;
в) уменьшится в 2 раза;
г) уменьшится в 4 раза;
д) увеличиться в 4 раза.
3. При радикальной сополимеризации стирола (А) и винил ацетата (В) константы сополимеризации равны rА=55 и rв=0,01. Сополимер какой структуры образуется, если мономерная смесь имела состав 1:1?
а) АААА В АААА;
б) ВВВВ А ВВВВ;
в) АВАВАВАВ;
г) ААААВВВВ.
Контрольная работа №2
1. Какие мономеры нужно выбрать для получения полимера класса полиамидов?
а) NH2-(CH2)5-COOH;
б) HO-R-OH + HOOC-R -СООН;
в) NH2-R-NH2 + HOOC-R -СООН;
г) NaO-R-ONa + HOOC-R-COOH.
2. Как можно повысить молекулярную массу полимера, получаемогометодом обратимой поликонденсации при данной степени превращения «Р»?
а) повышением температуры;
б) повышением концентрации катализатора;
в) удалением выделяющегося НМС;
г) введением монофункционального мономера.
3. Как изменится молекулярная масса поликонденсационного полимера, если в мономерную смесь ввести монофункциональный мономер?
а) не изменится;
б) увеличится;
в) уменьшится.
Контрольная работа №3
1. Какими методами можно определить среднемассовую молекулярную массу полимера:
а) методами светорассеяния, ультрацентрифугирования, диффузионным;
б) измеряя свойства, зависящие от числа частиц в растворе: осмотическое давление, эбулио- и криоскопия;
в) измеряя вязкость растворов;
г) химический метод по количеству концевых групп.
2. Что можно сказать о качестве растворителя, если зависимость приведенной вязкости раствора полимера от концентрации описывается уравнением:
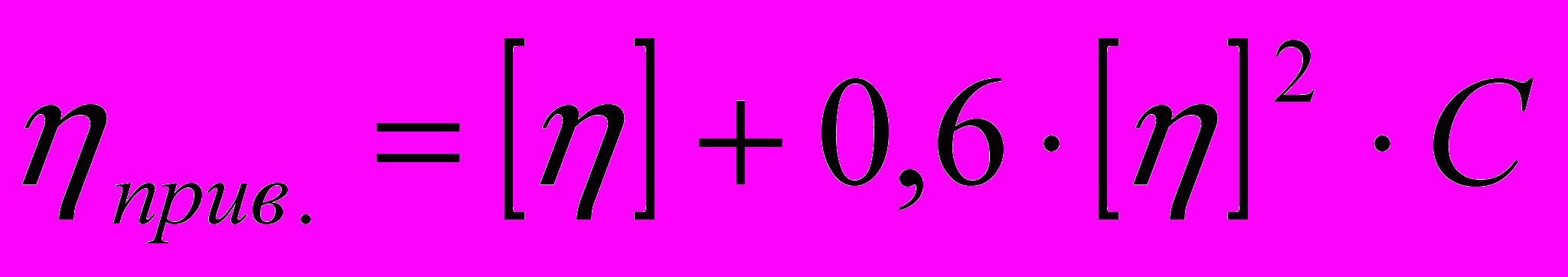
а) хороший растворитель;
б) 9-растворитель;
в) плохой растворитель;
г) однозначно ответить нельзя.
3. Зависимость осмотического давления от молекулярной массы полимера и природы растворителя в соответствии с выводами Флори-Хаггинса
выражается уравнением:
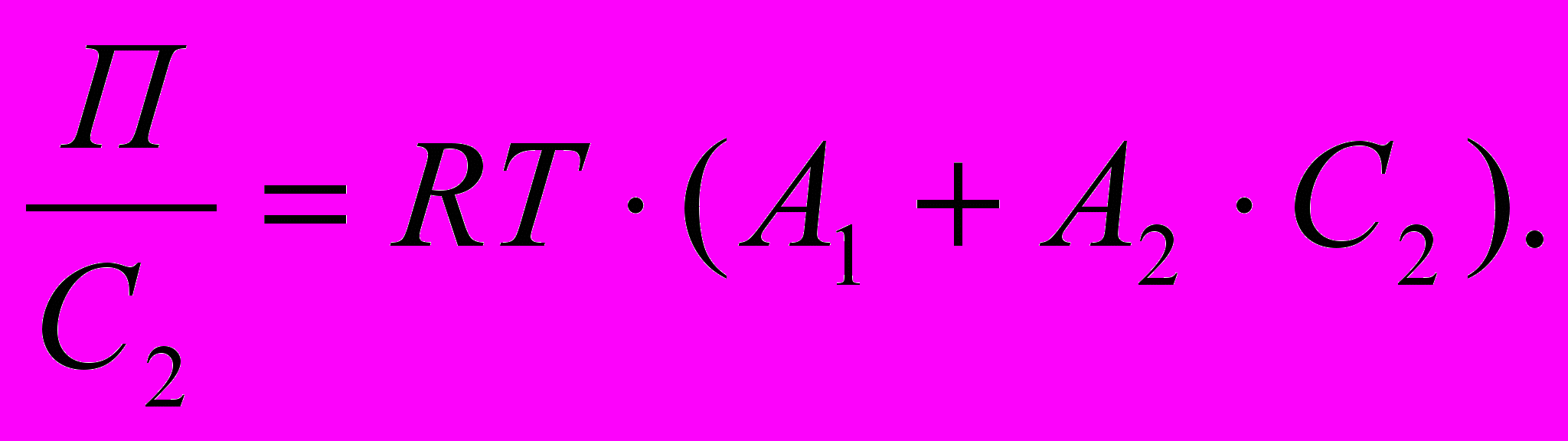
Как графически можно представить эту зависимость для полимергомологов в одном растворителе:
а) веер прямых, пересекающихся в одной точке
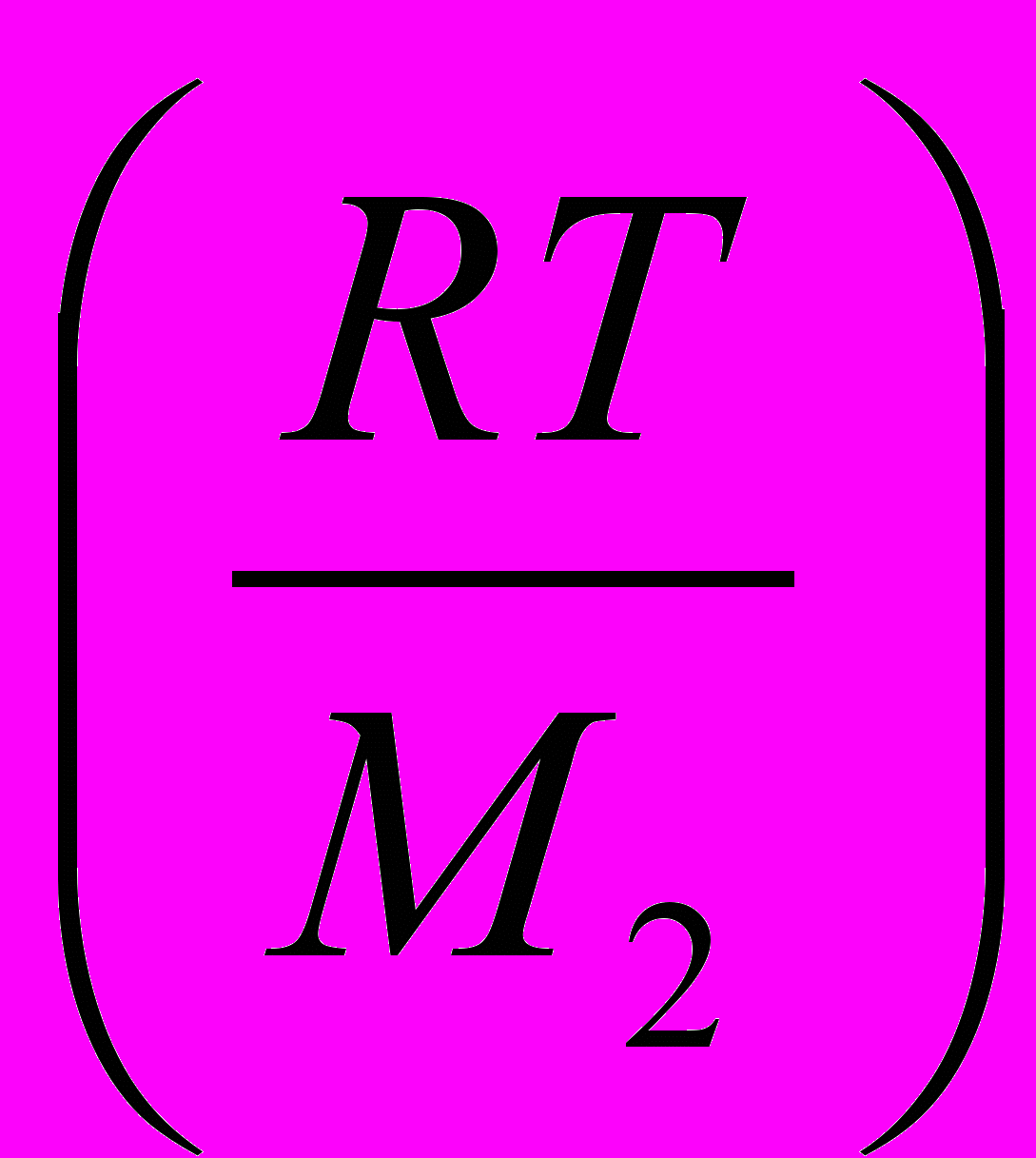 ;
;б) параллельные прямые с наклоном в зависимости от константы Хаггинса;
в) прямые, параллельные оси абсцисс (А2=0).
ПРИМЕРЫ ЭКЗАМЕНАЦИОННЫХ БИЛЕТОВ
Тверской государственный университет
БИЛЕТ №12
НАИМЕНОВАНИЕ ДИСЦИПЛИНЫ:
Химия ВМС
- Высокоэластическое состояние полимеров (термодинамика). Нижний предел молекулярной массы, необходимый для проявления высокоэластической деформации.
- Способы получения полистирола. Химические превращения полистирола. Получение ионообменных смол.
- Гидродинамические свойства макромолекул в растворах. Вязкость разбавленных растворов (относительная, удельная, приведенная, характеристическая).
Зав. кафедрой _______________
«____» ______________
Тверской государственный университет
БИЛЕТ №18
НАИМЕНОВАНИЕ ДИСЦИПЛИНЫ:
Химия ВМС
- Промышленные процессы синтеза полиамидов (периодический, непрерывный, каскадное полиамидирование).
- Гидродинамические свойства макромолекул в растворах. Вязкость разбавленных растворов (относительная, удельная, приведенная, характеристическая).
- Высокоэластическое состояние полимеров (термодинамика). Нижний предел молекулярной массы, необходимый для проявления высокоэластической деформации.
Зав. кафедрой _______________
«____» ______________
РАЗДАТОЧНЫЙ МАТЕРИАЛ И НАГЛЯДНЫЕ ПОСОБИЯ
При чтении лекций по теме 1: Синтез полимеров – студентам демонстрируются образцы полимеризационных и поликонденсационных полимеров в разной модификации: порошки, крошка, волокна, пленки, изделия. Например, светопроводящие оптические волокна и стекла, полиамидные и полиэфирные пленки, нетканые материалы из поликапроамида, колбасная оболочка, медицинские нити, волокна для защиты ценных бумаг и т.д.
