Ростовые и метаболические эффекты терапии рекомбинантным гормоном роста и половыми стероидами у девочек с синдромом Шерешевского-Тернера 14. 00. 03 Эндокринология
| Вид материала | Автореферат диссертации |
- С раневой инфекцией под влиянием квч терапии, 32.59kb.
- Общие принципы терапии больных с синдромом зависимости от алкоголя щие принципы терапии, 86.25kb.
- Оганов Рафаэль Гегамович 16. 00-18. 00 Дискуссия Боль в спине. Принципы терапии в практике, 637.85kb.
- Экспериментальные и клинические исследования, 89.43kb.
- Клинико-экономический анализ консервативной тактики лечения пациентов с синдромом диабетической, 457.09kb.
- Анестезиология и реаниматология, 184.1kb.
- Обучение гештальт-терапии – особенная деятельность, 53.82kb.
- Использование циклоферона в терапии папилломавирусной инфекции, 94.1kb.
- Ограничение употребления алкоголя, поваренной соли и жиров часто делает медикаментозную, 141.41kb.
- Программа обучения в клинической ординатуре по специальности «Эндокринология», 455.08kb.
1 2
Динамика уровней ИФР-1 и ИФРСБ-3 на фоне терапии рГРУ всех девочек с СШТ определялись уровни ИФР-1 и ИФРСБ-3 как составляющих ростовой оси ГР – ИФР-1 – ИФРСБ-3, отражающих активность ростового процесса. Ввиду выраженной вариабельности уровня показателей в зависимости от возраста, абсолютные данные были трансформированы в показатели SDS. Мы наблюдали статистически значимое возрастание показателей SDS ИФР-1 по сравнению с базальными показателями (р<0,001) в течение всего периода терапии. Также отмечалось статистически значимое возрастание ИФРСБ-3 (табл. 5, 6). Таблица 5. SDS ИФР-1 на фоне терапии рГР у девочек с СШТ.
* – р<0,001 – по сравнению с данными, полученными до лечения. ** – р<0,05 – по сравнению с данными, полученными при предыдущем измерении. Таблица 6. SDS ИФРСБ-3 на фоне терапии рГР у девочек с СШТ.
* – р<0,001 – по сравнению с данными, полученными до лечения. ** – р<0,05 – по сравнению с данными, полученными при предыдущем измерении. Необходимо отметить, что уровни абсолютных показателей ИФР-1 и ИФРСБ-3 не превышали допустимых верхних значений нормы для данных показателей, что свидетельствует о безопасности ростстимулирующей терапии. Для определения предикторной роли ИФР-1 и ИФРСБ-3 в отношении ростового ответа на фоне терапии рГР мы провели корреляционный анализ по Спирмену. Выявлена статистически значимая прямая корреляционная взаимосвязь SDS скорости роста и SDS ИФР-1 (r = 0,61, p = 0,000000) и взаимосвязь SDS роста и SDS ИФР-1 (r = 0,37, p = 0,0023), рис. 3. Статистически значимой корреляции для SDS ИФРСБ-3, SDS роста и SDS скорости роста выявлено не было. 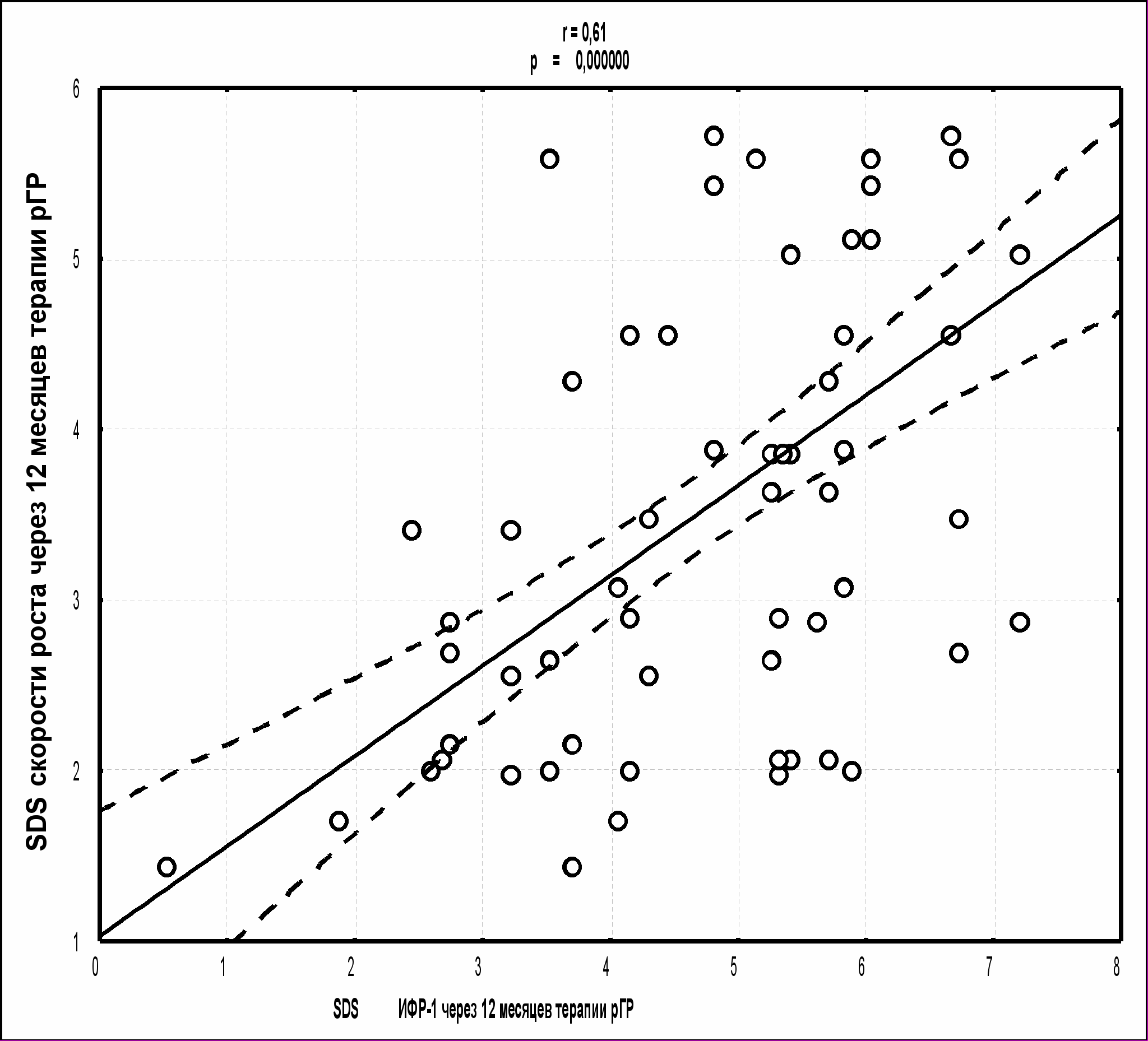 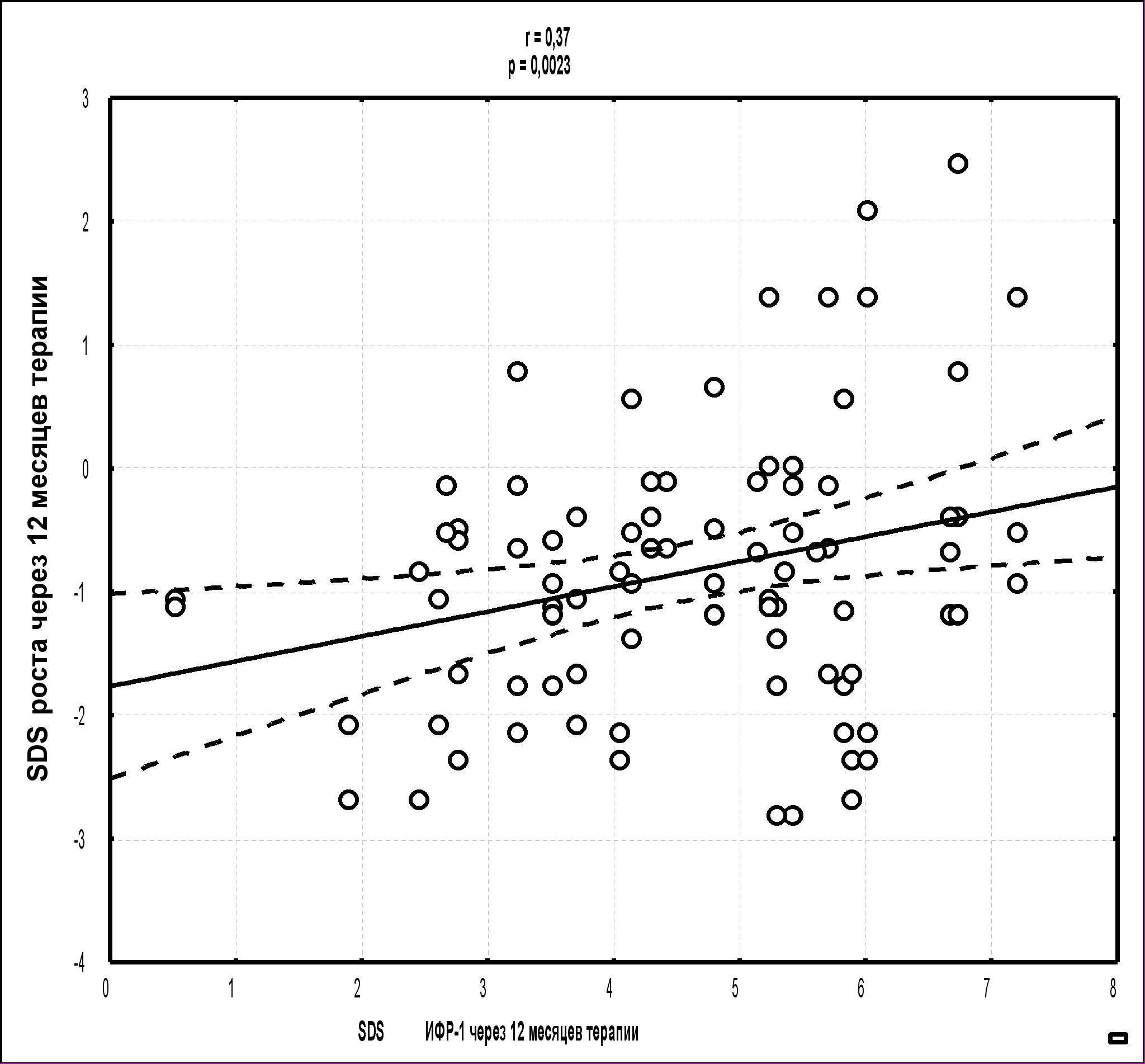 Рис.3. Корреляционная взаимосвязь SDS ИФР-1 с SDS скорости роста и SDS роста через 12 месяцев терапии рГР у девочек с СШТ (n = 92). Таким образом, нарастание уровня SDS ИФР-1 и ИФРСБ-3 на фоне терапии рГР у девочек с СШТ в сочетании с прямой корреляционной связью SDS ИФР-1 с SDS роста и скорости роста на первом году терапии свидетельствует о взаимосвязи эффективности ростстимулирующей терапии и изменении уровня ИФР-1. Исследование делеционного полиморфизма гена рецептора гормона роста (d3-GHR) и его влияние на ростовой ответ. Обследовано 76 девочек с СШТ в возрасте от 5 до 15,2 лет (средний возраст 11,1±2,6 лет), половое развитие у всех девочек соответствовало Таннер 1. Общая частота аллельных вариантов гена рецептора гормона роста (d3-GHR) составила: fl/fl («дикий» тип) - 63%, d3/fl (гетерозиготная делеция экзона 3) – 28%, d3/d3 (гомозиготная делеция экзона 3) – 9 %. Данные представлены на рисунке 4.  Рис.4. Частота распределения вариантов делеционного полиморфизма гена рецептора гормона роста у девочек с СШТ. Через 1 год терапии рГР у девочек с СШТ, имеющих гомозиготную делецию экзона 3 (d3/d3) гена рецептора гормона роста (GHR), показатели SDS роста и скорости роста были статистически значимо выше, чем у пациенток, имеющих другие аллельные варианты делеционного полиморфизма GHR (табл. 6). Таблица 6. Ростовые показатели у девочек с СШТ на фоне терапии рГР в зависимости от вариантов делеционного полиморфизма гена рецептора гормона роста.
Через 1 год терапии SDS роста у пациенток с гомозиготной делецией экзона 3 (d3/d3) GHR был статистически значимо выше, чем у пациенток с «диким» типом гена (fl/fl) GHR и составил -2,31±0,47 и -2,51±0,60, соответственно (р<0,05). Скорость роста через 1 год терапии у девочек с гомозиготной делецией 3 экзона (d3/d3) GHR была выше, чем у пациенток с «диким» типом (fl/fl) GHR и гетерозиготной делецией 3 экзона (d3/fl) GHR и составила 8,50±1,10 см/год. SDS скорости роста через 1 год терапии у пациенток с гомозиготной делецией экзона 3 (d3/d3) GHR был статистически значимо выше, чем у пациенток с «диким» типом гена (fl/fl) GHR и составил 3,44±2,18 и 1,61±2,52, соответственно (р<0,05). Полученные данные свидетельствуют в пользу взаимосвязи наличия гомозиготной делеции экзона 3 (d3/d3) гена рецептора гормона роста (GHR) у девочек с СШТ с эффективностью ростстимулирущей терапии рГР. Метаболические эффекты применения рГР при СШТ Девочки с СШТ относятся к группе риска по развитию сердечно-сосудистых заболеваний ввиду частого наличия пороков сердечно-сосудистой системы, склонности к гиперлипидемии, артериальной гипертензии. На сегодняшний день описано липолитическое действие рГР (снижение общего холестерина, фракции ЛПНП, индекса атерогенности, увеличение фракции ЛПВП) при лечении соматотропной недостаточности. Нами проводилось изучение динамики основных показателей липидного спектра на фоне терапии рГР. Таблица 8. Показатели липидного спектра у девочек с СШТ на фоне терапии рГР.
Данные средних показателей по группе у девочек СШТ приведены в таблице 8. Отмечалось статистически значимое снижение уровня общего холестерина и фракции ЛПНП после одного года лечения, сохранившееся после двух лет лечения, что подтверждает клинически значимое благоприятное влияние терапии рГР на липидный обмен. Статистически значимых изменений уровней триглицеридов, ЛПВП и индекса атерогенности в течение двух лет терапии выявлено не было. При исследовании уровней гликозилированного гемоглобина и тощаковой глюкозы до лечения и на фоне применения рГР в течение 2-х лет у девочек с СШТ не было выявлено статистически значимых изменений среднего уровня Hb1Ac и глюкозы, а также колебаний данного параметра выше верхней границы нормы. Наблюдаемый факт свидетельствует о безопасности проводимой терапии. Для оценки влияния терапии рГР на минерализацию скелета у девочек с СШТ мы проводили исследование МПКТ поясничного отдела у 28 девочек с СШТ. Из них 15 пациенток в возрасте от 8,5 до 12,9 лет (средний возраст 11,0±1,4 лет) получали терапию рГР в течение 1 года, 13 девочек в возрасте от 7,8 до 13,1 лет (средний возраст 10,8±1,7 лет) терапию рГР не получали. Данные пациенток с СШТ на фоне терапии рГР и без лечения представлены в таблице 9. Таблица 9. Антропометрические данные и показатели состояния МПКТ у пациенток с СШТ
* - различия между группами при р<0,05. При сравнительном анализе, девочки, получавшие и не получавшие терапию рГР сопоставимы по возрасту и костному возрасту. У девочек, получавших терапию, снижения МПКТ выявлено не было (Z-критерий = -0,79±0,13), среди девочек, не получавших терапию, отмечалось наличие остеопении (Z-критерий = -1,44±1,2). Между группами девочек на фоне терапии рГР и без нее выявлены статистически значимые различия абсолютных показателей МПКТ (p=0,011), Z-критерия для хронологического возраста (p=0,023) и Z-критерия для костного возраста (p=0,028). Процентное состояние МПКТ в пересчете на хронологический и костный возраст представлено на рисунке 5. 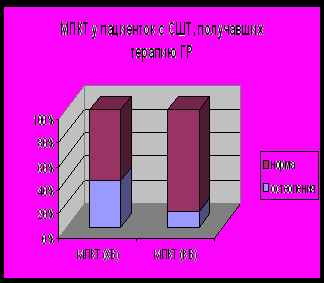 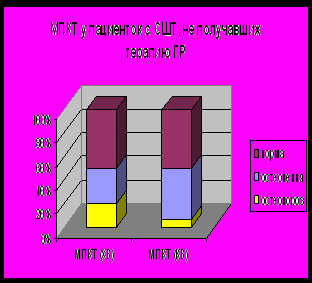 Рис. 5. МПКТ поясничного отдела позвоночника у девочек с СШТ без и на фоне терапии рГР. При анализе процентного распределения состояния МПКТ у девочек, получавших лечение рГР, отмечалось наличие остеопении у 40% по паспортному и у 13% по костному возрасту. У девочек, не получавших терапию рГР, отмечалось наличие остеопении (у 28% по хронологическому и у 42% по костному возрасту) и остеопороза (у 31% по хронологическому и у 8% по костному возрасту). Наличие остеопороза и остеопении у нелеченых девочек с СШТ по сравнению с умеренной остеопенией у леченых, а также статистически значимые различия у данных пациенток между показателями МПКТ, Z-критерия для хронологического и костного возраста свидетельствуют в пользу благоприятного влияния терапии рГР на минерализацию костной ткани. Индукция полового развития у девочек с СШТ Для оценки целесообразности инициации пубертата низкими дозами половых стероидов с целью оптимизации ростового прогноза, у 17 девочек с СШТ (средний возраст 13,2±0,9 лет) через 1 год применения рГР проводилась индукция пубертата низкими дозами натуральных эстрогенов. Антропометрические данные пациенток приведены в таблице 10 Таблица 10. Антропометрические данные девочек с СШТ до терапии, на фоне терапии рГР и на фоне применения эстрогенов в сочетании рГР.
На фоне комбинированной терапии эстрогенами и гормоном роста отмечалось увеличение скорости роста по сравнению с данными до лечения рГР и половыми стероидами, при этом темпы роста были сопоставимы с темпами на монотерапии рГР. При терапии эстрогенами не наблюдалось ускорения дифференцировки скелета и отмечалось развитие вторичных половых признаков. Кроме того, отмечалось улучшение ростового прогноза по данным прогнозируемого конечного роста, рассчитанного по таблицам Bayley N, Pinneau S (1982). Необходимо отметить, что на фоне терапии эстрогенами в низких дозах было отмечено статистически значимое снижение уровня гонадотропинов и увеличение уровня эстрадиола. Существенных изменений размеров матки выявлено не было. Сравнительный анализ эффективности различных схем лечения препаратами рГР и половых стероидов у пациенток с СШТ. Нами был проведен ретроспективный анализ данных пациенток, которые не лечились рГР, а получали только терапию эстрогенами в дозе 0,5-1 мг в сутки в течение 1 года. В группу вошло 23 девочки, средний возраст которых составил 14,4±1,2 лет. Сравнительные данные с пациентками, получавшими терапию рГР и эстрогенами, представлены в табл. 11. Таблица 11. Сравнительные данные девочек с СШТ на фоне терапии рГР и эстрогенами или монотерапии эстрогенами.
У девочек на монотерапии эстрогенами отмечалась ускоренная дифференцировка костной ткани, что обуславливало ухудшение ростового прогноза. Таким образом, индукция пубертата низкими дозами эстрогенов в сочетании с рГР способствует оптимизации ростового прогноза. ВЫВОДЫ: 1. Средний возраст постановки диагноза у девочек с синдромом Шерешевского-Тернера в российской популяции составляет 8,7±3,5 лет. Отмечаются два возрастных пика постановки диагноза – первый год жизни (22,8%) и пубертатный период (43,5%). При синдроме Шерешевского-Тернера наблюдается снижение роста и темпов роста с допубертатного периода, прогрессирующее с возрастом. Применение рГР для лечения низкорослости у девочек с синдромом Шерешевского-Тернера приводит к значимому увеличению показателей роста и улучшению ростового прогноза. 2. Уровень ИФР-1 служит маркером эффективности ростстимулирующей терапии гормоном роста при синдроме Шерешевского-Тернера. На фоне применения рГР отмечалось значимое возрастание ИФР-1 и ИФРСБ-3. Отмечена прямая корреляционная взаимосвязь ИФР-1 и скорости роста на первом году терапии. 3. Общая частота аллельных вариантов гена рецептора гормона роста (d3-GHR) у девочек с синдромом Шерешевского-Тернера в российской популяции составила: fl/fl («дикий» тип) - 63%, d3/fl (гетерозиготная делеция экзона 3) – 28%, d3/d3 (гомозиготная делеция экзона 3) – 9 %, что сопоставимо с общепопуляционными данными. У пациенток с гомозиготной делецией d3/d3-GHR отмечен максимальный ответ на ростстимулирующую терапию рГР. 4. Отмечается протективный эффект терапии рГР в отношении показателей липидного спектра и минеральной плотности костной ткани у девочек с синдромом Шерешевского-Тернера. При этом значимых изменений углеводного обмена, а также серьезных побочных эффектов выявлено не было. 5. Индукция пубертата низкими дозами половых стероидов у девочек с синдромом Шерешевского-Тернера в сочетании с терапией рГР приводит к улучшению ростового прогноза. ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ: Девочкам с СШТ при задержке роста и/или снижении темпов роста показано лечение гормоном роста с целью улучшения ростового прогноза. Рекомендовано исследование уровня ИФР-1 для оценки эффективности терапии гормоном роста у девочек с СШТ. При достижении возраста физиологического пубертата (12 лет) рекомендована индукция пубертата низкими дозами препаратов натуральных эстрогенов (0,2-0,25 мг в сутки) в сочетании с гормоном роста, способствующая оптимизации ростового прогноза и своевременному половому созреванию. По теме диссертации опубликованы следующие научные работы:
Список сокращенийрГР – рекомбинантный гормон роста СШТ – синдром Шерешевского – Тернера ХВ – хронологический возраст КВ – костный возраст ИМТ – индекс массы тела ПКР – прогнозируемый конечный рост ИФР-1 – инсулиноподобный фактор роста-1 ИФРСБ-3 – инсулиноподобного фактора роста связывающий белок-3 ЛГ – лютеинизирующий гормон ФСГ – фолликулостимулирующий гормон Hb A1c – гликозилированный гемоглобин A1c ОХ – общий холестерин ТГ – триглицериды ЛПНП – липопротеиды низкой плотности ЛПВП – липопротеиды высокой плотности МПКТ – минеральная плотность костной ткани УЗИ – ультразвуковое исследование ИА – индекс атерогенности ПЦР – полимеразная цепная реакция SD – standart deviation (стандартное отклонение) SDS – standart deviation score (коэффициент стандартного отклонения) d3-GHR – делеция 3 экзона гена рецептора гормона роста fl/fl – «дикий» тип fl/d3 – гетерозиготная делеция экзона 3 d3/d3 – гомозиготная делеция экзона 3 KIGS – Международная База Данных Роста |
