Автореферат диссертации на соискание ученой степени
| Вид материала | Автореферат диссертации |
- Автореферат диссертации на соискание ученой степени, 378.33kb.
- Автореферат диссертации на соискание учёной степени, 846.35kb.
- Автореферат диссертации на соискание ученой степени, 267.76kb.
- Акинфиев Сергей Николаевич автореферат диссертации, 1335.17kb.
- L. в экосистемах баренцева моря >03. 02. 04 зоология 03. 02. 08 экология Автореферат, 302.63kb.
- Автореферат диссертации на соискание ученой степени, 645.65kb.
- Автореферат диссертации на соискание ученой степени, 678.39kb.
- Автореферат диссертации на соискание ученой степени, 331.91kb.
- Автореферат диссертации на соискание ученой степени, 298.92kb.
- Автореферат диссертации на соискание ученой степени, 500.38kb.
На правах рукописи
СТОЛОРЕНКО
Виктория Викторовна
Комплексный мониторинг эффективности лечения
распространенных форм рака яичников
14.00.14 – Онкология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Волгоград
2004
Работа выполнена на кафедре онкологии с курсом онкологии ФУВ Волгоградского государственного медицинского университета.
Научный руководитель – докотор медицинских наук,
профессор Р.А.Хвастунов
^ Официальные оппоненты: - доктор медицинских наук,
профессор Л.В. Ткаченко
Ведущая организация:
Защита состоится 2004 года в часов на заседании диссертационного совета при Ростовском научно-исследовательском онкологическом институте МЗ РФ (344037, г. Ростов-на Дону, 14 линия, 63)
С диссертацией можно ознакомиться в библиотеке Ростовского научно-исследовательского онкологического института МЗ РФ
Автореферат разослан _______________2004 г.
Ученый секретарь
диссертационного совета,
доктор медицинских наук,
профессор Г.А. Неродо
^
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы исследования
Злокачественные опухоли репродуктивной системы являются наиболее частыми в структуре онкологической заболеваемости женщин, их суммарная доля превышает 35% (Жорданиа К.И., 2002). Ежегодно в мире диагностируется 165 тыс. новых случаев злокачественных новообразований яичников и 101 тыс. смертей от них (Аксель Е.М. и соавт., 2001; Engelmann J. et al., 2000). Заболеваемость в России составляет 10,17 на 100 тыс. населения (несколько ниже европейского показателя 12,5), занимая седьмое место в структуре общей онкологической заболеваемости (5%) и третье среди гинекологического рака. За последние 10 лет отмечен заметный прирост заболевания – 8,5%.
По-прежнему остаются неутешительными результаты первичной диагностики рака яичников – 75-80% опухолей выявляются в III-IV стадиях, что значительно ухудшает возможности комбинированной и комплексной терапии. И если в вопросах лечения рака яичников I-II стадий нет особых разногласий, то при распространенном раке яичников много нерешенных проблем, что обусловлено низким процентом излеченности: 5-летняя выживаемость при III стадии составляет 35%, при IV стадии – 17% (Аксель Е.М. и соавт., 2001). Предметом активного обсуждения онкогинекологов в настоящее время являются не только частные аспекты хирургического и лекарственного лечения, но и вопросы оптимального сочетания и эффективной последовательности их применения (Новикова Е.А. и соавт., 2000; Орлова Р.В., 2000; Жорданиа К.И., 2002; Berek J.S. et al.,1998). В этой связи разработка адекватного прослеживания за эффектом лечения на всех его этапах является актуальной проблемой (Максимова Н.А., 2001; Ашрафян Л.А. и соавт., 2002). По мнению Максимовой Н.А., «помимо проблемы первичной (и уточненной) диагностики новообразований репродуктивных органов у женщин существует ряд нерешенных вопросов по мониторингу (в первую очередь – нестандартному), непосредственных результатов неоадъювантных противоопухолевых воздействий, доля которых в комплексных схемах лечения гинекологического рака возрастает в течение последних 10-15 лет. Объективизировать достигнутые результаты, т.е. определить меру эффективности – важная, порой, судьбоносная для пациента задача…» (Максимова Н.А., 2003).
В современной литературе представлены работы, посвященные отдельным этапам мониторинга: лабораторного (Винокуров В.Л. и соавт., 1991; Гуло Е.И. и соавт., 1991; Алексеева М.А. и соавт., 1995; Жорданиа К.И., 2001; Сергеева Н.С. и соавт., 2001; Ашрафян Л.А. и соавт., 2002); ультразвукового (Кобелева С.Л. и соавт., 1999; Блюменберг А.Г. и соавт., 1999; Мешкова И.Е. и соавт., 2001; Сидоренко Ю.С. и соавт., 2001; Ашрафян Л.А. и соавт., 2002), МРТ (Горицкая И.В., 1993); эндоскопического (Гуло Е.И., 2001; Муртазаев А.М., 1981) – без детализации и обоснования динамических изменений на фоне проводимого лечения и попытки выработать критерии его успешности. Все они посвящены частным диагностическим вопросам и не преследуют цель комплексной и многократной оценки распространенности рака яичников в процессе длительного противоопухолевого лечения.
Современный мониторинг специального лечения распространенного рака яичников и рецидивов должен носить комплексный характер (Блюменберг А.Г. и соавт, 1999; Ашрафян Л.А. и соавт., 2002). Четкое и рациональное его проведение увеличивает продолжительность ремиссии и улучшает качественные характеристики жизни больных прогностически неблагоприятных групп (Титова В.А. и соавт., 2002). Однако, кроме констатации такой необходимости, работ по комплексному мониторингу в .доступной нам литературе нет, что и определило направление нашего научного поиска.
^ Цель работы
Улучшить контроль эффективности лечения распространённых форм рака яичников путём создания алгоритма комплексного мониторинга, позволяющего своевременно корректировать лечебную тактику.

^ Задачи исследования
- На базе представлений о специфичности и чувствительности изучить мониторинговую ценность методов рутинного контроля за эффективностью лечения распространённого рака яичников – лабораторного мониторинга СА-125, трансабдоминального и трансвагинального УЗИ.
- Оценить специфичность, чувствительность и мониторинговую ценность методов диагностического резерва (МРТ и РКТ) при лечении распространённого рака яичников.
- Определить диагностический потенциал эндовидеотораколапароскопической техники при специальном лечении распространённого рака яичников.
- В сравнительном аспекте изучить результаты методов динамического мониторинга, выявить их преимущества и недостатки при длительном контроле за эффективностью проводимого лечения.
- Разработать рациональные диагностические алгоритмы комплексного мониторинга распространенного рака яичников.
^ Научная новизна работы
Впервые проведен контроль эффективности лечения распространенного рака яичников целым комплексом современных диагностических методов (СА-125, комплексное УЗИ, МРТ, РКТ, эндовидеотехника), изучены в сравнительном аспекте их возможности, введено понятие мониторинговой ценности метода и сформированы четкие алгоритмы диагностики на этапах мониторинга больных: на старте, в процессе и в финале лечения рака яичников.
Впервые на достаточном материале разработан и применен метод динамических лапароскопий, определена диагностическая и лечебная роль торакоскопических исследований при распространенном раке яичников, успешно апробирован способ одновременных лапароторакоскопических процедур.
Оценив в контексте работы диагностический потенциал неинвазивных и инвазивных методов мониторинга, мы разработали диагностические алгоритмы сопровождения специального лечения больных распространенным раком яичников в зависимости от этапа мониторинга.
^ Практическая значимость работы
Определен алгоритм динамического мониторинга с комплексным использованием клинико-лабораторно-инструментального метода и лапароскопическим исследованием на завершающем этапе.
Для облегчения динамического слежения и более наглядного документирования нами разработаны карты динамического слежения (УЗИ, МРТ, РКТ, лапароскопия).
Дана объективная трактовка эффектов проводимого лечения («полный регресс», «частичный регресс», «стабилизация», «прогрессирование») на основании лабораторных, УЗИ-, МРТ-, РКТ-, эндовидеотораколапароскопических и морфологических критериев, которые в повседневной практике облегчают выработку показаний к различным методам лечения распространенного рака яичников. Сформулирована УЗИ-, МРТ-, и РКТ-семиотика успешного и неэффективного лечения распространенного рака яичников. Дана клиническая оценка феномена изолированного повышения СА-125 и продемонстрирована в половине случаев его связь с рецидивом опухолевого роста.
Показана возможность применения многократных лапароскопических вмешательств при спаечном процессе в брюшной полости после предшествующих операции. Разработана методика одновременных лапароскопических и торакоскопических исследований при распространенном раке яичников.
Продемонстрирована эффективность лечебного плевродеза у тяжелого контингента больных с метастатическим плевритом, резистентным к ПХТ.
^ Основные положения, выносимые на защиту:
Динамический лабораторно-инструментальный мониторинг, рационально сочетающий использование традиционных (УЗИ, СА-125) и резервных (МРТ, лапароторакоскопия) диагностических методов позволяет улучшить контроль эффективности лечения распространенного рака яичников. Мониторинговая роль РКТ ограничена специальными показаниями.
^ Апробация диссертации состоялась на совместном заседании сотрудников кафедры онкологии с курсом ФУВ, кафедры акушерства и гинекологии ФУВ, госпитальной хирургии и хирургии ФУВ Волгоградского государственного медицинского университета и собрания врачей Волгоградского областного клинического онкологического диспансера 26 марта 2004 г.
Основные результаты исследования доложены на VII региональной конференции молодых ученых (г. Волгоград, сентябрь 2002 г.), на Невском радиологическом форуме «Из будущего в настоящее» (г. Санкт-Петрбург, апрель 2003 г.), на Российской научно-практической конференции «Миниинвазивная хирургия в клинике и эксперименте (профессиональные, учебно-методические, экономические и социальные аспекты)» (г. Пермь, 1-3 июля 2003 г.).
Публикации
Материалы диссертации опубликованы в 11 научных статьях.
^ Внедрение результатов в практику здравоохранения
Результаты исследования внедрены в практику работы областного клинического онкологического диспансера г. Волгограда, межрайонных диспансеров Волгоградской области, на кафедре онкологии с курсом ФУВ Волгоградского государственного медицинского университета.
Материалы исследования используются в учебном процессе на курсе онкологии ФУВ Волгоградского государственного медицинского университета.
^
Объем диссертации и ее структура
Диссертация изложена на 209 страницах машинописного текста, состоит из введения, обзора литературы, описания материалов и методов исследования, результатов собственных наблюдений в 4 главах, заключения, выводов, практических рекомендаций, библиографического указателя, содержащего 167 отечественных и 166 зарубежных источников. Работа иллюстрирована 27 таблицами и 66 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
^
Материалы и методы исследования
В основу исследования положены клинические сведения о 231 больной опухолями яичников, лечившейся с 1999 по 2004 год в гинекологическом отделении Волгоградского областного клинического онкологического диспансера.
Мы изучали результаты комплексного мониторинга у 231 пациентки, большинство из которых составили больные распространенным (первичным и рецидивным) раком яичников (табл. 1).
Группу наших наблюдений характеризовало: преобладание возрастной категории 45-65 лет (86%), серозных аденокарцином – 181 (78%), низко- и умереннодифференцированных опухолей (73%).
Таблица 1.
^
Распределение больных в зависимости от характера процесса
| Характер процесса | Число обследованных пациенток | |
| абс. число | % | |
| Доброкачественные опухоли матки и придатков | 44 | 19 |
| Первичный ранний рак яичников (стадии I-II) | 23 | 10 |
| Первичный распространенный рак яичников (стадии III-IV) | 128 | 56 |
| Рецидивы рака яичников | 36 | 15 |
| Итого | 231 | 100 |
^ Хирургический этап лечения был реализован у 172 больных: радикально прооперированы были 44 больные с доброкачественными опухолями и 23 пациентки с раком яичников I-II стадий, циторедуктивные операции были выполнены 99 пациенткам первичным раком яичников. При этом 41 (41,4%) операций были оптимальными, 21 (21,2%) субоптимальными, 23 (23,2%) неоптимальными, 1 (1,1%) диагностическая лапаротомия и 13 (13,1%) лапароскопических операций без конверсии при нерезектабельном процессе. Вторичные циторедуктивные операции выполнены 6 пациенткам с рецидивным раком яичников.
Полихимиотерапию получали все 187 пациенток со злокачественными опухолями яичников. Исключительно лекарственное лечение проведено 29 больным первичным и 30 больным рецидивным раком яичников. Послеоперационные курсы полихимиотерапии проведены всем пациенткам. Неоадъювантную ПХТ получали 30 больных первичным и 2 пациентки рецидивным раком яичников.
В процессе мониторинга мы выделили 3 этапа:
На I этапе 151 пациентке проводили первичную диагностику и оценку распространенности рака яичников. В результате – детализирована комплексная семиотика первичного рака яичников с акцентом на оценку резектабельности процесса.
На II этапе у 99 больных решали задачи оценки эффективности проводимой полихимиотерапии.
На III этапе у 43 больных проводили диагностику рецидивов заболевания с акцентом на семиотику, определяли показания для вторичной циторедукции. Особое внимание мы уделили клинической интерпретации феномена изолированного повышения СА-125.
Мониторинг осуществлялся комплексом методов:
- Лабораторное определение СА-125 иммуноферментным анализом, набор ConAg (Швеция).
- Ультразвуковой анализ исследования на сканерах SSD-1100 и SSD-4000 фирмы ALOКA в В-режиме с применением конвексного датчика 3,5 мГц (трансабдоминальное) и конвексного датчика 5 мГц (трансвагинальное).
- МРТ-исследования на отечественном томографе «Образ-2» с индукцией магнитного поля порядка 0,15 Т и зарубежном аппарате «Magnetom» фирмы «Siеmens» с индукцией магнитного поля 1,5 Тл.
- РКТ-сканирование на спиральном компьютерном томографе «Somatom+4» фирмы «Siеmens».
- Эндовидеотораколапароскопические вмешательства на оборудовании фирмы Carl Storz.
Всего выполнено 726 определений СА-125 231 пациентке с кратностью 1-7, 627 трансабдоминальных и трансвагинальных исследований 231 пациентке с кратностью 1-5, 85 МРТ-исследований 52 пациенткам с кратностью 1-3, 26 РКТ-исследований 24 пациенткам с кратностью 1-2, 108 эндовидеоскопических исследований 90 пациенткам с кратностью 1-3.
Расчет диагностического потенциала методик производили по следующим формулам (Rubin Ph., 1993):
Чувствительность (%)=______а______
а+в
Специфичность (%)=_______г_______
г+б
а – действительно положительные результаты,
б – ложноположительные,
в – ложноотрицательные,
г – действительно отрицательные.
^ Статистическую обработку материала мы производили путем расчета средней арифметической, среднеквадратического отклонения, коэффициента Стьюдента при помощи компьютерной программы «БИОСТАТИСТИКА» на процессоре IntelPentiumIV.
^ Лабораторный мониторинг (определение СА-125)
На I этапе по результатам лабораторного мониторинга мы получили следующие данные (рис. 1):
- Уровень СА-125 достоверно повышался при раке яичников (401,4+305,5 Ед/мл) по сравнению с группой сравнения – 56,4+33,1 Ед/мл (р<0,05).
- СА-125 является стадиоспецифичным маркером: при раннем раке яичников средний уровень маркера составил 82,4+53,5 Ед/мл, при распространенном – 520,1+264,5 Ед/мл (р<0,05) (рис. 1).
- Чувствительность СА-125 в первичной диагностике злокачественных опухолей яичников составила 90,5%, специфичность – 79,6%.
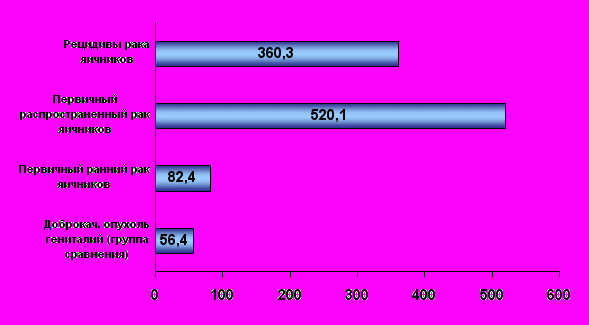 Рис. 1. Средний уровень СА-125 в зависимости от характера процесса.
Рис. 1. Средний уровень СА-125 в зависимости от характера процесса.Контроль эффективности противоопухолевого лечения на II этапе мы производили, во-первых, у больных после неоадъювантной полихимиотерапии и получили следующие данные (табл. 2).
Анализ таблицы 2 показывает, что стабилизация маркера на цифрах, превышающих 250 Ед/мл и более с числом курсов, превышающим 4, без тенденции к дальнейшему снижению СА-125 является неблагоприятным признаком, ассоциированным с нерезектабельностью опухоли и нерезультативностиью лекарственного лечения.
^ Итоговый эффект по завершению лечения мы констатировали по критериям ВОЗ (табл. 3).
Сывороточная концентрация СА-125 при рецидивах заболевания (на III этапе мониторинга) составила 360,3+298,5 Ед/мл. Границы колебаний – 11,5-1010 Ед/мл. Маркернегативные рецидивы рака яичников отмечены в 8 (22%) случаях. Чувствительность СА-125 в диагностике рецидивов составила 78%, специфичность – 43%.
Таблица 2
Динамика СА-125 на фоне предоперационных курсов полихимиотерапии
| Объем операции после ПХТ | Число больных | Среднее число курсов ПХТ | Уровень СА-125 до ПХТ | Уровень СА-125 до операции |
| Оптимальная циторедуктивная операция | 8 | 3,2 | 515,5+145,6 | 75,0+23,0 |
| Субоптимальная циторедуктивная операция | 6 | 5,1 | 613,4+167,0 | 23,5+10,8 |
| Неоптимальная циторедуктивная операция | 9 | 4,0 | 550,9+133,2 | 149,0+33,5 |
| Диагностическая лапаротомия | 1 | 5,0 | 229,1+89,3 | 266,0+67,2 |
| Диагностическая лапароскопия | 6 | 4,7 | 755,7+197,2 | 283,3+45,2 |
| Всего | 30 | | | |
Таблица 3
Концентрация СА-125 в зависимости от полученного эффекта специального лечения (n=99)
| Эффект лечения | Число наблюдений | Уровень СА-125, Ед/мл |
| Ремиссия | 64 | 22,7+3,2 |
| Стабилизация | 17 | 262,4+22,4 |
| Прогрессирование | 18 | 639,8+150,2 |
Таким образом, о роли лабораторного мониторинга на всех этапах можно сделать следующие заключения:
- Лабораторный мониторинг может быть использован для первичной диагностики и ориентировочного стадирования распространенного рака яичников и менее пригоден для ранней диагностики злокачественного процесса.
- Стабилизация сывороточного уровня Са-125 на цифрах 250 Ед/мл и более является плохим прогностическим критерием. Снижение концентрации Са-125 на 70-80% под действием терапии относится к маркерам результативного лечения.
- Информативность СА-125 в диагностике и, соответственно, мониторинге больных рецидивными опухолями резко падает.
^ Комплексный эхографический мониторинг
Данные неинвазивных методов мониторинга мы подразделили на 2 категории: А – признаки, характеризующие злокачественность первичной опухоли, Б – признаки, указывающие на распространенность заболевания.
На I этапе мониторинга к эхографическим признакам категории А мы относим наличие опухоли неправильной формы гетерогенной структуры, как правило, размерами более 8 см, с бугристыми неровными контурами (рис. 2), распространяющиеся в дугласово пространство, либо билатеральное расположение опухолей. Признаками категории Б считаем асцит, метастазы по париетальной брюшине, в большом сальнике, внутренних органах, забрюшинных лимфатических узлах. К основным допплерографическим характеристам рака яичников мы относим множественные сосудистые локусы с преимущественно центральной локализацией, максимальной артериальной скоростью кровотока– 26,7+2,3 см/с и максимальной венозной скоростью кровотока– 10,8+1,24 см/с и индексом резистентности-0,35.

а

Рис. 2. Эхографические критерии злокачественности категории А: большие размеры образования (10х14 см), гетерогенная структура опухоли, с неровными, местами нечеткими контурами (а).
Чувствительность трансабдоминального УЗИ составила 84,1%, трансвагинального – 92,1%; специфичность – 81,8% и 84,1% соответственно. При попытке стадировать рак яичников чувствительность УЗИ значительно снижалась до 67,2%. Минимальный размер регистрируемого очага при трансабдоминальном УЗИ составил 1,5 см, при трансвагинальном – 1 см.
Оценивая информативность УЗИ на II этапе мониторинга, мы получили следующие данные.
Эхографическим критериями эффективности полихимиотерапии стали уменьшение размера, изменение структуры опухоли, ее контуров (от размытых к четким), эхогенности, уменьшение или исчезновение асцита, редукция лимфатических узлов, уменьшение размеров и изменение структуры висцеральных метастазов до изоэхогенных со структурой органа. При этом наиболее информативными УЗИ-критериями мы считаем уменьшение размеров, структуры опухоли и уменьшение или исчезновение асцита.
Результаты эхографической оценки итогового эффекта лечения представлены в таблице 4.
Таблица 4
Эхографическая оценка эффективности комбинированного лечения, проведенного больным распространенным раком яичников
| Эффект лечения | Число наблюдений | |
| абс. число | % | |
| Полный регресс | 59 | 60 |
| Частичный регресс | 5 | 5 |
| Стабилизация | 17 | 17 |
| Прогрессирование | 18 | 18 |
| Всего | 99 | 100 |
При констатации полного регресса опухоли нами получено 4 ложноотрицательных результата и 1 ложноположительный. При диагностике частичного регресса зафиксирован 1 ложноотрицательный и 1 ложноположительный результат.
По данным УЗИ, на III этапе мониторинга рецидивный процесс диагностирован у 38 из 43 обследованных пациенток. При этом получено 2 ложноположительных и 6 ложноотрицательных заключений. Чувствительность трансабдоминального УЗИ составила 41,7%, специфичность – 43%, трансвагинального метода 83,3% и 71,5% соответственно. Ограниченный пространством малого таза рецидив выявлен у 15 (42%), распространенный в брюшной полости – у 23 (58%) пациенток.
Анализируя случаи ложноположительных заключений, мы обнаружили их ошибочность в констатации образований малого таза диаметром до 2 см при нечетких контурах и пониженной эхогенности. Эти находки сочетались с сомнительными данными бимануального исследования. Ложноотрицательные заключения были обусловлены мелкоочоговым поражением брюшины.
Итак, резюмируя результаты эхографического мониторинга, мы отмечаем, что:
- Комплексное эхографическое исследование является достаточно информативным методом в диагностике злокачественных опухолей яичников, что в совокупности с лабораторной диагностикой может быть рекомендовано в качестве обязательного стандарта для I этапа мониторинга распространенного рака яичников.
- УЗИ позволяет достаточно объективно отражать результаты неоадъювантной полихимиотерапии и констатировать результаты лечения в виде стабилизации или прогрессирования опухолевого процесса.
- Сложности ультразвуковой визуализации рецидивного процесса на фоне спаечной болезни и нарушенной анатомии таза после предшествующей операции обязывает включать в комплексную программу обследования резервные диагностические методы.
^
МРТ- и РКТ-мониторинг
По данным МРТ и РКТ на I этапе мониторинга, к категории признаков А мы отнесли двусторонность поражения, большие размеры образования (более 10 см) с выходом из дугласова пространства в брюшную полость, неправильную форму, гетерогенность структуры опухоли с гиперинтенсивным в Т2 сигналом для МРТ, бугристые, нечеткие контуры; к категории Б (рис. 3) – инфильтрацию париетальной брюшины, связочного аппарата матки, деформацию контура мочевого пузыря, прорастание опухоли в окружающие структуры, наличие метастазов по париетальной и висцеральной брюшине, в забрюшинных лимфатических узлах, наличие асцита. Оба метода позволяют с достаточно высокой чувствительностью – для МРТ 100% и для РКТ 93%, и специфичностью – 90% и 86%, соответственно, диагностировать распространенный рак яичников. Разрешающая способность при МРТ составила 0,5 см, при РКТ – 1,5 см.
По итогам 31 магнитно-резонансной томографии несовпадение диагнозов было зарегистрировано в 3 (10%) случаях.
РКТ продемонстрировала высокую информативность в визуализации и динамическом слежении за паренхиматозными метастазами в процессе специального лечения.
а

б

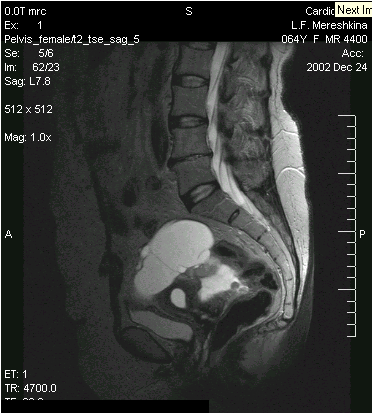
Рис. 3. МРТ, сагиттальная проекция, Т2-изображение. Распространение опухолевого конгломерата (а) за матку (б) в дугласово пространство с инфильтрацией брюшины малого таза.
На ^ II этапе мониторинга при оценке эффективности неоадъювантной полихимиотерапии МРТ более адекватно визуализировала инфильтраты париетальной брюшины, параректальной, предпузырной клетчатки, забрюшинных лимфатических узлов. Помимо аналогичных изменений структуры, контуров, интенсивности опухоли, важными критериями служит уменьшение инфильтрации париетальной брюшины, редукция метастазов в дугласовом пространстве, забрюшинных лимфатических узлах. Необходимо отметить, что при эффективной полихимиотерапии практически в 100% случаев реагировали признаки категории Б: уменьшалась инфильтрация и регрессировали метастазы париетальной брюшины, исчезала инфильтрация окружающих тканей, уменьшались деформация контуров мочевого пузыря и забрюшинные лимфатические узлы.
Констатируя эффект проведенного лечения и проверяя МРТ-данные лапароскопией, при диагностике полного регресса мы выявили 4 (29%) ложноотрицательных МРТ-заключения и были вынуждены продолжить лечение этим пациенткам. При наличии остаточной опухоли данные лапароскопии выявили 4 (66,7%) ошибочных МРТ-заключения. В 2 случаях диагноз остаточной опухоли оказался ложным, ещё 2 раза при лапароскопии выявлен диссеминированный процесс, потребовавший смены лекарственного лечения. Во всех ситуациях удалось избежать нецелесообразной лапаротомии.
На ^ III этапе мониторинга по данным МРТ и РКТ (23 исследования), изолированный местный рецидив выявлен у 4 (29%), распространенный опухолевый процесс – у 10 (71%) больных. Чувствительность МРТ составила 96%. Комментируя в сравнительном аспекте роль РКТ и МРТ в выявлении опухолевых очагов, мы отмечаем значительный приоритет МРТ, что связано с затруднениями визуализации малого таза при спаечном процессе (у всех больных предшествует оперативное лечение по поводу первичной опухоли) и сложностью распознавания перифокальной инфильтрации, которая в той или иной степени всегда сопутствует рецидиву рака яичников.
Итак, анализируя диагностическую значимость резервных методик, можно сделать следующие заключения:
- МРТ и РКТ позволяют с достаточно высокой чувствительностью и специфичностью диагностировать распространенный рак яичников.
- МРТ позволяет оценивать эффективность полихимиотерапии, решая подчас вопрос о продолжении лечения без необходимости использовать инвазивный мониторинг. При получении данных за прогрессирование заболевания методом МРТ в совокупности с данными клиники, УЗИ и лабораторного мониторинга отпадает необходимость в лапароскопии.
- Сложности ультразвуковой визуализации рецидивного процесса на фоне спаечной болезни и нарушенной анатомии таза после предшествующей операции обязывает включать в комплексную программу обследования резервные методы визуализации, где безусловный приоритет принадлежит МРТ.
^
Эндоскопический мониторинг
Лапароскопия, помимо прямой визуализации опухоли, уже на I этапе мониторинга позволяет решать вопрос ее резектабельности и морфологической верификации.
На основании 34 лапароскопий нами выработаны следующие признаки абсолютной нерезектабельности рака яичников (рис. 4, А): несмещаемый опухолевый конгломерат с вовлечением органов и брюшины малого таза у 10 (71%) пациенток, распространение опухоли на стенки таза у 9 (64%), распространение опухоли на органы малого таза и брюшной полости при выраженной диссеминации процесса у 8 (57%), невозможность выведения связок яичников у 14 (100%), невозможность выведения матки при инструментальной пальпации и тракциях со стороны промежности у 8 (57%), неподвижная при инструментальной пальпации матка у 7 (50%), инфильтративная форма рака яичников у 5 (36%) больных.
| А  |  Б |
Рис. 4, А – эндоскопическая характеристика первичного процесса в малом тазу до начала лечения, Б - эндоскопическая характеристика первичного процесса в малом тазу после 6 курсов неоадъювантной ПХТ.
На II этапе мониторинга лапароскопия была выполнена 23 пациенткам и позволила безошибочно решить вопрос о резектабельности процесса (рис. 4, А, Б) с морфологическим подтверждением результативности лекарственного лечения. Нами выполнено 9 оптимальных и субоптимальных операций, из них 7 (78%) - на фоне выраженного лекарственного патоморфоза II-IV степени. При 8 нерезектабельных опухолях в 4 (50%) случаях лекарственный патоморфоз в опухоли не определялся (табл. 5).
Таблица 5
Лекарственный патоморфоз в опухоли у больных с различными вариантами хирургического лечения после неоадъювантной ПХТ
| Характер хирургического лечения | Лекарственный патоморфоз в опухоли | Всего | |||||||
| 0 | I | II | III-IV | ||||||
| абс. | % | абс. | % | абс. | % | абс. | % | ||
| Оптимальное | - | - | 1 | 17 | 3 | 50 | 2 | 23 | 6 |
| Субоптимальное | - | - | 1 | 33,3 | 2 | 66,6 | - | - | 3 |
| Неоптимальное | 2 | 23 | 3 | 50 | 1 | 17 | - | - | 6 |
| Диагностическая лапаротомия | 1 | 100 | - | - | - | - | - | - | 1 |
| Без конверсии | 3 | 43 | 3 | 43 | 1 | 14 | - | - | 7 |
| Всего | 6 | 8 | 7 | 2 | 23 | ||||
^ Итоговый эффект по завершению лечения мы констатировали по критериям ВОЗ 20 больным комплексом диагностических методов (табл. 6) с включением эндохирургических средств.
Эндовидеолапароскопический контроль подтвердил полный регресс у 12 (60%) человек, частичный регресс констатирован у 6 (30%) пациенток, прогрессирование – у 2 (10%). Эти данные оказались точнее совокупных результатов неинвазивных методов обследования у 7 пациенток данной группы, что позволило в 4 случаях избежать немотивированного прекращения дальнейшего лечения, в 2 случаях изменить схемы терапии и исключить одну необоснованную попытку вторичной циторедукции. В 4 случаях лапароскопические данные скорректировали ошибочные УЗИ-, МРТ-, РКТ – заключения в отношении диссеминации по брюшине, в 1 - в отношении остаточной опухоли в малом тазу, в 2 – в отношении субклинического асцита. Отмечая приоритетную роль эндовидеоскопической визуализации миллиарных перитонеальных очагов, частую их маскировку и ускользание от сонографических, рентгеновских и магнитнорезонанстных технологий считаем мониторинговую лапароскопию обязательной по завершении курсов лекарственного лечения при констатации полного регресса изначально распространенных раков яичников.
Таблица 6
Комплексная оценка эффективности проводимого лечения (n=20)
| Эффект лечения | УЗИ | МРТ+РКТ | лапароскопия |
| Полный регресс | 15 | 16 | 12 |
| Частичный регресс | 5 | 4 | 6 |
| Стабилизация | - | - | - |
| Прогрессирование | - | - | 2 |
На ^ III этапе мониторинга эндоскопическая диагностика рецидивного процесса была выполнена 43 пациенткам. Рецидив заболевания подтвержден у 36 (84%) пациенток.
Местный рецидивный процесс без вовлечения верхних отделов брюшной полости мы выявили в 14 (39%) случаях. Местный рецидив в сочетании с диссеминацией по брюшине был установлен у 21 (58%) больной. У 1 (3%) пациентки диагностировано изолированное поражение легочной ткани при отсутствии местного рецидива.
Всего нами выполнено 6 (17%) вторичных циторедуктивных операций. Конверсий в лапаротомию при этом выполнено 5. В 1 случае конверсия в лапаротомию не предпринималась в связи с отсутствием на лапароскопии рецидивной опухоли брюшной полости.
Особое внимание привлекают случаи изолированного повышения СА-125 на фоне благополучных заключений неинвазивных методов диагностики. Мы имеем 8 подобных наблюдений. Рецидив заболевания диагностирован на лапароскопии у 4 (50%) пациенток, при этом у 3 (75%) – в виде умеренной милиарной диссеминации по брюшине, в 1 (25 %) случае - в виде местного рецидива.
Диагностические торакоскопии были предприняты у 4 больных с резистентным к лекарственному лечению плевритом. У всех констатирована тотальная диссеминация по плевре, произведен лечебный плевродез инсуффляцией талька (рис. 5).
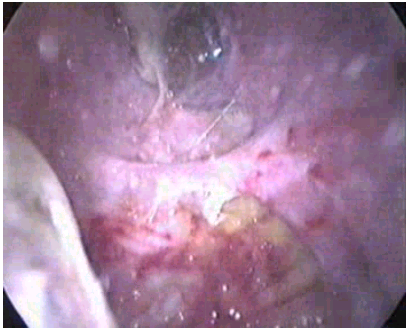
Рис. 5. Лечебный плевродез инсуффляцией талька.
Резюмируя вышесказанное, можно сделать следующие заключения:
- На I этапе мониторинга лапароскопия абсолютно показана в сложных диагностических случаях и при сомнительной резектабельности опухоли.
- На II этапе обязательно лапароскопическое подтверждение регресса опухоли в финале лечения.
- Лапароскопия на III этапе мониторинга должна выполняться при планировании вторичной циторедукции, а также для оценки эффективности лечения, являясь основной завершающей составляющей программы комплексного мониторинга.
ВЫВОДЫ
- Мониторинговая ценность маркера СА-125 высока на начальных этапах лечения распространенного рака яичников – при первичной диагностике, ориентировочном стадировании, когда чувствительность достигает 90,5% специфичность – 79,6%. В последующем динамика СА-125 истинно отражает эффект лечения в 92% случаев.
- Мониторинговая роль трансабдоминального и трансвагинального УЗИ значительна в первичной диагностике распространенного рака яичников со специфичностью, соответственно, 81,8% и 84,1% и чувствительностью 84,1% и 92,1%. Комбинация УЗИ с определением СА-125 оптимально отражает эффективность неоадъювантной ПХТ.
- На всех этапах мониторинга специфичность (90-100%) и чувствительность (87-100%) МРТ превышает показатели других неинвазивных методов. Роль РКТ ограничена мониторингом паренхиматозных метастазов рака яичников.
- Эндовидеоскопическая техника отличается самой высокой разрешающей способностью на всех стадиях лечения распространенного рака яичников, что позволяет привлекать ее потенциал в спорных диагностических ситуациях, при оценке резектабельности и изучении лекарственного патоморфоза, для выявления и слежения за милиарной внутрибрюшной и внутриплевральной диссеминацией рака яичников.
- Для первичной диагностики и стадирования распространенного рака яичников на I этапе мониторинга целесообразно использовать: СА-125+УЗИ+МРТ (при расхождении данных)+лапароскопия (при расхождении данных, отсутствии морфологической верификации, оценке сомнительной резектабельности).
- На II этапе мониторинга при анализе результата неоадъювантной ПХТ эффективен комплекс мер: СА-125+УЗИ+лапароскопия (для оценки резектабельности, изучения патоморфоза); в финале лечения для констатации полного или частичного регресса опухоли – СА-125+УЗИ+лапароскопия, при стабилизации или прогрессировании процесса – СА-125+УЗИ+МРТ.
- На ^ III этапе мониторинга для диагностики рецидивов рака яичников требуется комплексный подход: СА-125+УЗИ+МРТ+лапароскопия (при расхождении данных, изолированном росте СА-125, для определения показаний вторичной циторедукции).
^
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Оптимальной организацией лабораторного мониторинга является контроль маркера СА-125 1 раз в 2 курса полихимиотерапии и на 10-й день после хирургического лечения, что позволяет адекватно оценивать динамику опухолевого процесса.
- Ультразвуковое исследование целесообразно выполнять до операции, после нее при наличии остаточных опухолевых масс, в середине и по завершению послеоперационных курсов полихимиотерапии.
- При выполнении динамической лапароскопии места постановки портов должны находиться вне зоны послеоперационного рубца. При подозрении на выраженный спаечный процесс после предшествующих вмешательств целесообразно использовать «открытую» методику постановки оптического лапаропорта.
- Оптимальный плевродез обеспечивается введением в плевральную полость 10-15 г мелкодисперсного талька до достижения эффекта “снежной бури”.
^ СПИСОК РАБОТ,
ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Роль опухольассоциированного антигена СА-125 в диагностике и лечении рака яичников // Сборник материалов VII региональной конференции молодых исследователей Волгоградской области. Волгоград, 2003. С. 82-83.
- Лапароскопия в диагностике и лечении распространенного рака яичников // Сборник материалов Российской научно-практической конференции «Миниинвазивная хирургия в клинике и эксперименте (профессиональные, учебно-методические, экономические и социальные аспекты). Пермь, 2003. С.197-198. (соавт. Р.А. Хвастунов, Т.Ф. Девятченко, Н.С. Филатова).
- Контроль эффективности индукционной полихимиотерапии у больных распространенным раком яичников // Паллиативная медицина и реабилитация.-2003.-№ 2.-С. 73. (Материалы V конгресса с международным участием «Паллиативная медицина и реабилитация в здравоохранении», апрель 2003 г.). (соавт. Р.А. Хвастунов, Т.Ф. Девятченко, Н.С.Филатова).
- Роль МРТ в диагностике и мониторинге больных распространенным раком яичников // Паллиативная медицина и реабилитация.-2003.-№ 2.-С. 16. (Материалы V конгресса с международным участием «Паллиативная медицина и реабилитация в здравоохранении», апрель 2003 г.). (соавт. Р.А. Хвастунов, Е.Д. Лютая, Т.Ф, Девятченко).
- Ультразвуковые критерии эффективности лечения больных распространенным раком яичников // Паллиативная медицина и реабилитация.-2003.-№ 2.-С. 15. (Материалы V конгресса с международным участием «Паллиативная медицина и реабилитация в здравоохранении», апрель 2003 г.). (соавт. Е.Д. Лютая)
- Первичная диагностика и мониторинг опухолей яичников с помощью МР-томографии // Материалы Невского радиологического форума «Из будущего в настоящее». СПб, 2003.-С. 209. (соавт. Е.Д. Лютая)
- Эхография больных распространенным раком яичников в процессе специального лечения // Эхография.-2003.-т. 4-№ 1.-С. 39-43. (соавт. Р.А. Хвастунов, Е.Д. Лютая, Т.Ф. Девятченко).
- Малоинвазивная хирургия в организации мониторинга больных распространенным раком яичников в процессе специального лечения // Материалы IV Всероссийской конференции молодых ученых «Актуальные вопросы клинической и экспериментальной онкологии». М., 2003. С. 145-147.
- Диагностический потенциал МРТ и эхографии в диагностике распространенного рака яичников // Эхография.-2003.-т.4.-№ 2.-С. 214-215. (Материалы I съезда врачей ультразвуковой диагностики Южного Федерального округа, Ростов-на-Дону, 27-28 мая 2003 г.). (соавт. Р.А. Хвастунов, Е.Д. Лютая, Т.Ф. Девятченко).
- МРТ и РКТ в диагностике и мониторинге распространенного рака яичников // Материалы VII Российского онкологического конгресса. М., 2003.-С. 197-198. (соавт. Е.Д.Лютая, Р.А. Хвастунов, Е.И. Егин, Т.Ф. Девятченко).
- Роль и место эхографического исследования в современных скрининговых программах по ранней диагностике рака яичников // Эхография.-2003.-т.4.-№ 3.-С. 324. (материалы IV конференции врачей ультразвуковой диагностики Поволжья, Казань, 9-11 июня 2003 г.). (соавт. Лютая Е.Д.).
