На правах рукописи
| Вид материала | Автореферат |
- Печатная или на правах рукописи, 21.09kb.
- Удк 796/799: 378 , 770.24kb.
- На правах рукописи, 399.58kb.
- На правах рукописи, 726.26kb.
- На правах рукописи, 1025.8kb.
- На правах рукописи, 321.8kb.
- На правах рукописи, 552.92kb.
- На правах рукописи, 514.74kb.
- На правах рукописи, 670.06kb.
- На правах рукописи, 637.26kb.
На правах рукописи
Степина
Наталья Анатольевна
ПРОГНОСТИЧЕСКИЕ КРИТЕРИИ
РАЗВИТИЯ АТОПИЧЕСКОГО ДЕРМАТИТА
И ЕГО ПРОФИЛАКТИКА
У ДЕТЕЙ ГРУДНОГО ВОЗРАСТА
14.01.08 – Педиатрия
АВТОРЕФЕРАТ
диссертации на соискание учёной степени
кандидата медицинских наук
Астрахань – 2011
Работа выполнена
в Государственном образовательном учреждении
высшего профессионального образования
«Астраханская государственная медицинская академия
Министерства здравоохранения и социального развития
Российской Федерации»
(ГОУ ВПО «АГМА Минздравсоцразвития России»)
Научный кандидат медицинских наук, доцент
руководитель: ^ Безрукова Дина Анваровна
Официальные доктор медицинских наук, профессор
оппоненты: Эйберман Александр Семенович;
доктор медицинских наук, профессор
Башкина Ольга Александровна
Ведущая ГОУ ВПО «Российский государственный
организация: медицинский университет
Минздравсоцразвития России»
Защита состоится «__» _________2011 г. в __ часов на заседании совета по защите докторских и кандидатских диссертаций Д208.005.01 при ГОУ ВПО «АГМА Минздравсоцразвития России» по адресу: 414000, г. Астрахань, ул. Бакинская, 121.
С диссертацией можно ознакомиться в научной библиотеке Астраханской государственной медицинской академии.
Автореферат разослан «_____» __________________ 2011 г.
Учёный секретарь совета по защите
докторских и кандидатских диссертаций
Д208.005.01 кандидат медицинских наук,
доцент Заклякова Л.В.
^ ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
В России, как и во всём мире, неуклонно повышается распространённость аллергических болезней (В.А. Ревякина, 2003; Н.П. Торопова, 2003; J. Daniels, 2002; J.M. Hanifin, 2002; G. Girolomonil, 2003). По данным эпидемиологических исследований, предпринятых в Российской Федерации, аллергическими болезнями (АБ) страдает до 25 % детского населения (И.И. Балаболкин, 2007).
У детей раннего возраста среди АБ преобладает кожная патология, которая по большей части представлена атопическим дерматитом (АтД), имеющим постоянную тенденцию к росту (И.И. Балаболкин, 1999; Л.С. Намазова, 2006; A.P. Castro, 2006). Наиболее заметно повышение уровня заболеваемости среди детей первого года жизни, в группе которых атопия регистрируется в каждом третьем случае (В.А. Ревякина, 2003).
Начинаясь в раннем возрасте, АтД быстро принимает хроническое течение. Дети с АтД страдают от таких проявлений болезни, как множественные расчёсы, зуд и кожное воспаление, представляющих собой кардинальные особенности данного заболевания (Г.И. Смирнова, 2002; R. Schiffner, 2005; J.M. Spergel, 2003). Основными чертами АтД сегодня являются следующие: формирование болезни уже с первых месяцев жизни, упорное течение, частые обострения, рост инвалидизирующих форм заболевания, низкая эффективность лечения (Г.И. Смирнова, 2006; J.M. Hanifin, 2002). АтД – это первая клиническая манифестация «аллергического марша» и существенный фактор риска (ФР) формирования аллергического ринита и бронхиальной астмы у детей (И.И. Балаболкин, 2003; Д.Ш. Мачарадзе, 2007; R. Valenta, 2000).
Обозначенные проблемы обусловливают поиск новых мер профилактики АтД, внедрение современных способов прогнозирования, донозологической диагностики данного заболевания.
Изучение факторов, способствующих формированию аллергически измененной реактивности, и их использование с прогностической целью является ключевым в решении проблемы профилактики АтД.
^ Цель исследования
Установить клинико-прогностическое значение факторов риска, способствующих развитию атопического дерматита у детей на первом году жизни для оптимизации мероприятий по его профилактике.
^ Задачи исследования
Провести комплексную оценку состояния здоровья детей первого года жизни с риском развития АтД.
- Изучить микрофлору кишечника у детей первого года жизни с риском развития атопической патологии и больных АтД.
- Оценить особенности окислительной модификации белков у детей первого года жизни с риском развития атопической патологии и больных АтД.
- Выявить клинико-прогностическое значение факторов риска развития АтД и разработать алгоритм его прогноза на первом году жизни.
- Определить эффективность использования адаптированной молочной смеси на основе умеренно гидролизованного белка для профилактики АтД у детей первого года жизни с риском атопии.
^ Научная новизна
Установлено, что дети первого года жизни из группы риска по развитию АтД, проживающие на территории г. Астрахань, в доклиническом периоде имеют изменения в состоянии микрофлоры кишечника. Рассчитан коэффициент взаимной сопряжённости между показателями, характеризующими состояние микрофлоры кишечника в доклиническом периоде АтД и развитием заболевания на первом году жизни.
Доказано, что у детей грудного возраста с АтД регистрируется достоверное повышение интенсивности перекисного окисления белков (ПОБ) в сыворотке крови и в смешанной слюне, в том числе и в доклиническом периоде. Установлена корреляционная зависимость высокой и средней силы между концентрацией продуктов ПОБ в сыворотке крови и слюне у детей грудного возраста с клиническими проявлениями АтД и здоровых детей.
Установлен количественный вклад состояния дезадаптации в неонатальном периоде в ранний дебют АтД.
Впервые составлен алгоритм прогноза АтД для детей первого года жизни с наследственной отягощённостью по атопии с учётом показателей ПОБ слюны.
^ Практическая значимость
Получены данные о высокой распространённости отягощённого генеалогического анамнеза по атопии на территории г. Астрахань среди детей первого года жизни и высокой частоте реализации риска развития АтД в первые месяцы жизни. Эта информация необходима для организации своевременного проведения процедуры прогнозирования и составления плана эффективных профилактических мероприятий среди данной категории детей.
Предложенные прогностические таблицы с учётом показателей ПОБ слюны расширяют представления о ФР, способствующих развитию АтД. Они показывают, что клинико-прогностическое значение ФР перинатального периода существенно превышает риск наследственной предрасположенности к атопии, а некоторые протекторные факторы постнатального периода способны нивелировать наследственную отягощённость.
Внедрённый в практику детских поликлиник и стационаров вариант использования адаптированной молочной смеси (АМС) на основе умеренно гидролизованного белка у детей первого года жизни с риском атопии позволит снизить заболеваемость АтД на первом году жизни.
^ Положения, выносимые на защиту
Дети с АтД на первом году жизни имеют отклонения в состоянии здоровья, в том числе – высокую частоту микроэкологических нарушений кишечника ещё до манифестации патологического процесса. У данной группы неонатальный период чаще протекает с синдромом дезадаптации.
- Интенсивность процессов ПОБ в сыворотке крови и слюне у детей грудного возраста с АтД выше по сравнению с условно здоровыми детьми. Показатели ПОБ в слюне в доклиническом периоде сопоставимы с показателями ПОБ у больных АтД.
- Оценка наиболее информативных ФР лежит в основе прогнозирования манифестации АтД у детей грудного возраста с наследственной отягощённостью по атопии. Наибольшее прогностическое значение имеют материнские ФР, факторы перинатального периода.
- Применение АМС на основе умеренных белковых гидролизатов, обладающих пребиотическими свойствами, для искусственного вскармливания детей первого года жизни с риском атопии является эффективным средством профилактики АтД.
^ Внедрение результатов работы в практику
Результаты исследований используются в практической работе педиатров детской поликлиники № 1 МУЗ «Городская клиническая больница № 4 им. В.И. Ленина», МУЗ «Городская детская поликлиника № 3», детское поликлиническое отделение № 2 «Городской поликлиники № 10» г. Астрахань, а также включены в учебный план педиатрических кафедр ГОУ ВПО «АГМА Минздравсоцразвития России». Материалы диссертации включены в методическое пособие для врачей «Прогнозирование и профилактика атопической патологии у детей, проживающих в условиях сочетанного воздействия антропогенной нагрузки и йодного дефицита» (Астрахань, 2010).
^ Апробация работы
основные положения диссертации обсуждены в ходе следующих мероприятий: VII и VIII Астраханской межрегиональной научно-практической конференции «Лекарство и здоровье человека» (2008, 2009), научно-практической конференции педиатров России «Фармакотерапия и диетология в педиатрии» (Иваново, 2008; Ставрополь, 2010), XVI съезда педиатров России «Актуальные проблемы педиатрии» (Москва, 2008), XVI Российского национального конгресса «Человек и лекарство» (Москва, 2009), II Российской научно-практической конференции «Аллергические и иммунологические заболевания – проблема XXI века» (Санкт-Петербург, 2010), I Конгресса врачей первичного звена здравоохранения юга России, VI конференции врачей общей практики (семейных врачей) юга России (Ростов-на-Дону, 2010).
Работа апробирована на межкафедральной конференции с участием кафедр ГОУ ВПО «АГМА Минздравсоцразвития России» и работников практического здравоохранения (г. Астрахань, декабрь 2010 г.).
Публикации: по теме диссертации было издано 13 работ, в том числе 2 публикации в изданиях, включённых в перечень ВАК РФ.
^ Структура диссертации.
Диссертация изложена на 163 страницах машинописного текста, состоит из введения, обзора литературы, описания материалов и методов исследования, трёх глав собственных исследований, обсуждения, выводов, практических рекомендаций и списка литературы. Текст иллюстрирован 27 таблицами, 23 рисунками. Библиографический список насчитывает 263 источника, в том числе – 167 отечественных и 96 зарубежных.
^
Связь с планом научных исследований.
Диссертация выполнена в соответствии с планом научно-исследовательских работ Астраханской государственной медицинской академии, в рамках отраслевой научно-исследовательской программы «Возрастные особенности детского организма в норме и патологии». Госрегистрация № 01200904222.
^СОДЕРЖАНИЕ РАБОТЫ
Работа выполнена на кафедре поликлинической педиатрии с курсом семейной медицины ГОУ ВПО «АГМА Минздравсоцразвития России», на базе МУЗ «Городская клиническая больница № 4 им. В.И. Ленина», МУЗ «Городская детская поликлиника № 3», МУЗ «Городская детская клиническая больница № 1».
Проведение исследований одобрено этическим комитетом ГОУ ВПО «АГМА Минздравсоцразвития России».
^
Материалы и методы исследования
Объектом настоящего исследования являлись дети первого года жизни с отягощённым генеалогическим анамнезом по атопии (больные АтД и условно здоровые), проживающие на территории г. Астрахань. Предметом изучения были пренатальные (родительские) и перинатальные факторы, а также факторы постнатального периода, способствующие реализации риска атопической патологии и формированию АтД на первом году жизни.
Для решения поставленных задач на первом этапе исследования методом случайной выборки было анкетировано 756 семей, проживающих в различных районах г. Астрахань для выявления уровня распространённости контингента детей с риском атопии.
Из числа детей с наследственной отягощённостью по атопии для клинического наблюдения были сформированы две группы детей, переведённых на раннее искусственное вскармливание в связи с невозможностью грудного. Дети основной группы (n=21, из них: 9 девочек, 12 мальчиков) получали адаптированную молочную смесь (АМС ГА-1, АМС ГА-2), созданную на основе умеренно гидролизованного белка молочной сыворотки с добавлением пребиотических волокон – олигосахаридов. Дети контрольной группы (n=21, из них: 9 девочек, 12 мальчиков) получали другую адаптированную смесь на основе коровьего молока, которая не обладала вышеуказанными свойствами. Группы подбирались с позиций доказательной медицины по принципу «копия-пара».
На втором этапе исследования была дана оценка состояния здоровья детей группы риска, проведён поиск наиболее значимых ФР, осуществлена диагностика АтД, реализованы клинико-анамнестические, физиометрические, лабораторные методы исследования.
Поиск ФР проводился с использованием данных анкетного опроса и первичной медицинской документации (ф. 096-у, ф. 112-у) у детей с проявлениями заболевания на первом году жизни (92 человека: 43 девочки и 49 мальчиков) и условно здоровых детей с наследственной отягощённостью по атопии, не имевших клинических проявлений АтД (94 человека: 46 девочек, 48 мальчиков).
Диагноз АтД формировали в соответствии с рекомендациями научно-практической программы «Атопический дерматит у детей: диагностика, лечение и профилактика» (2000). Из 92 детей основной группы лёгкое течение АтД отмечено у 8, среднетяжёлое – у 77, тяжёлое – у 7 детей.
Оценка состояния микрофлоры кишечника у 117 детей первого года жизни, которые по наследственной предрасположенности вошли в группу высокого риска по развитию АтД (в том числе у 41 ребёнка с установленным диагнозом АтД), проведена с применением стандартных методов бактериологического исследования фекалий, рекомендованных МНИИЭМ им. Г.Н. Габричевского.
Оценка общих сывороточных и аллергенспецифических Ig класса Е у детей, больных АтД, проведена с использованием тест-системы полуколичественного иммуноферментного анализа производства ООО НПО «Иммунотекс».
Изучены процессы ПОБ в слюне среди детей первого года жизни на доклиническом этапе (n=78), при проявлениях АтД (n=53), в периферической крови среди детей с установленным диагнозом АтД (n=36) и условно здоровых (n=19). Оценку интенсивности окислительной модификации белков проводили по методу R.L. Levine (1990) в модификации Е.Е. Дубининой (1995) при длинах волн 356, 370, 430 нм.
На третьем этапе был разработан алгоритм прогноза развития АтД на первом году жизни, проведён анализ эффективности использования АМС ГА-1,2 для профилактики АтД у детей первого года жизни с риском атопии.
Статистическая обработка полученных результатов проводилась на персональном компьютере с использованием программы «Microsoft Excel-2007» (в частности, её модулей «Анализ данных» и «Мастер диаграмм») и пакета программ по статистической обработке данных Statistica for Windows и Statistica 6.0.
Среди прочих общепринятых методик с помощью коэффициента детерминации r2 определялась доля влияния анализируемого признака на результативный. Оценка сопряжённости данных, сгруппированных по качественному признаку, проводилась с помощью коэффициента ассоциации Юла (Q). Прогностическая информативность количественных изменений исследуемых параметров выявлялась по специальной электронной программе (А.А. Джумагазиев, 1992) с использованием последовательного анализа А. Вальда в модификации А.А. Генкина (Е.В. Гублер, 1990).
В процессе исследования были отобраны наиболее весомые для прогноза признаки, для каждого из которых рассчитан прогностический коэффициент (ПК).
^ Результаты исследования
На первом этапе исследования была установлена высокая распространённость АБ среди родителей, имевших детей грудного возраста. Так, среди 756 анкетированных семей в 37,96 % случаев был установлен неблагоприятный аллергологический анамнез.
Выявлено, что в группе детей с отягощённым семейным анамнезом, проживающих на территории г. Астрахань, достоверно чаще встречается АтД на первом году жизни (р<0,001).
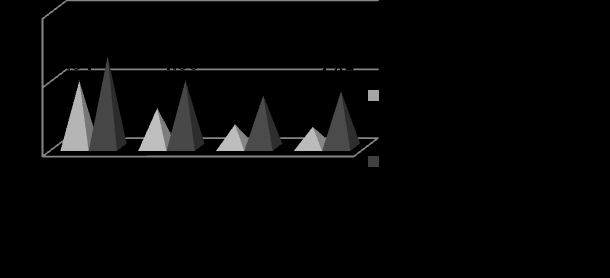
Проведённые наблюдения показали, что у детей группы высокого риска по развитию АтД одной из серьёзных проблем является ранняя клиническая манифестация заболевания. Пик клинических проявлений (23,9 %) приходится на второй месяц жизни (см. рис. 1).
^ Рис. 1. Помесячная динамика начала клинических проявлений
АтД на первом году жизни
Учитывая столь ранние сроки начала клинических проявлений АтД, проанализировано состояние здоровья матерей на момент наступления беременности, особенности перинатального периода.
Установлено, что, среди женщин основной группы отмечалась более высокая распространённость экстрагенитальной патологии (р<0,001), полиорганности поражения (р<0,001), отягощения акушерского анамнеза (р<0,01), чем в группе сравнения.
Женщины в основной группе достоверно чаще были подвержены производственным вредностям (χ2=3,89, Q=0,45, p<0,05), вредным привычкам: курению (χ2=3,85, Q=0,46, p<0,05), употреблению во время беременности большого количество кофе (χ2=3,91, Q=0,45, p<0,05), а также злоупотреблению молоком и молочными продуктами (χ2=5,39, Q=0,45, p<0,02), облигатными аллергенами – шоколадом, цитрусовыми фруктами, мёдом (χ2=9,44, Q=0,58, p<0,001).
Среди матерей основной группы не только чаще встречались АБ (АтД, р<0,05; пищевая аллергия р<0,05), но и в большинстве случаев отмечалось обострение АБ (АтД, р<0,05; пищевая аллергия, р<0,05; лекарственная аллергия, р<0,05; поллиноз, р<0,05).
Среди детей с клиническими проявлениями АтД на первом году жизни с наследственной отягощённостью по атопии со стороны матери регистрировались более высокие показатели общих IgE – 49,8±3,87 МЕ/мл, чем среди детей с наследственной отягощённостью по линии отца – 27,6±1,41 МЕ/мл, р<0,001.
Низкое качество здоровья женщин предопределило качество течения беременности и состояния здоровья новорождённых. Установлена достоверная разница в исследуемых группах: по частоте возникновения гестозов (χ2=11,92, Q=0,54, р<0,001), угрозы преждевременных родов (χ2= 14,62, Q=0,57, р<0,002), фетоплацентарной недостаточности (χ2=8,76, Q=0,41, р<0,001), внутриутробной гипоксии плода (ВУГП) (χ2=12,3, Q=0,52, р<0,001).
^ Рис. 2. ПК аллергических болезней матери
Преобразуя в данном исследовании качественные показатели в их количественное значение, диссертанту удалось показать, что обострение АБ у матери значительно увеличивает прогностическое значение данного фактора для формирования АтД на первом году жизни (см. рис. 2).
Наиболее существенными для реализации риска АтД на первом году жизни являются такие пренатальные (материнские) и перинатальные ФР, как антибактериальная терапия беременной (ПК=5,74), злоупотребление облигатными аллергенами (ПК=4,70), гестоз (ПК=4,48), ВУГП (ПК=4,29), производственные вредности у матери (ПК=4,07).
Ассоциативной связью средней силы обладают такие факторы, как возраст женщины (старше 30 лет) (ПК=3,77), курение до и во время беременности (ПК=3,61), злоупотребление молоком и молочными продуктами (ПК=3,48), угроза преждевременных родов (ПК=3,4), фетоплацентарная недостаточность (ПК=3,1), отягощённый акушерский анамнез (ПК=2,79), наличие перинатальных инфекций (ПК=2,72), токсикоз (ПК=2,45), острые респираторные инфекции во время беременности (ПК=2,41).
Интранатальный период в основной группе отличался высокой частотой оперативного родоразрешения по экстренным показаниям (χ2=3,95, Q=0,52, р<0,05). Состояние острой гипоксии (асфиксии) чаще встречалось среди детей основной группы (χ2=7,43, Q=0,57, р<0,01).
Таким образом, для реализации риска атопии оперативное родоразрешение по экстренным показаниям (ПК=4,56) и асфиксия в родах (ПК=4,86) являются существенными по прогностической значимости факторами. Протективным свойством обладает такой фактор, как физиологичные роды в сроке 38–40 недель (ПК=-2,06).
При оценке характера течения неонатальной адаптации новорождённых установлено, что в основной группе не менее 88,04±3,74 % детей, а в группе сравнения – 52,13±5,16 % имеют отклонения в состоянии здоровья (р<0,001). Выраженная дезадаптация у детей основной группы отмечена в 31,52±4,84 %, в группе сравнения – в 11,70±3,56 % (р<0,001).
Корреляционный анализ между степенью выраженности процесса дезадаптации у новорождённых и сроком манифестации АтД показал, что между данными признаками существует отрицательная корреляционная связь средней силы (r=-0,69, р<0,02). Суммарный вклад состояния дезадаптации в неонатальном периоде на ранний дебют АтД, по нашим данным, составляет 47,6 % (r2).
Неонатальный период у детей основной группы существенно чаще, чем у новорождённых группы сравнения протекал с патологией (см. табл. 1).
Таблица 1
^ Основные патологические состояния, обусловившие
состояние дезадаптации в неонатальном периоде
| Характер патологии | Основная группа, % | Группа сравнения, % | р |
| Пролонгированная гипербилирубинемия | 28,26±4,69 | 12,77±3,44 | <0,02 |
| Отклонения в неврологическом статусе | 84,78±3,74 | 52,13±5,15 | <0,001 |
| Клинические проявления внутриутробного инфицирования (ВУИ) | 10,87±3,24 | 3,19±1,8 | <0,05 |
| Висцеральные признаки соединительнотканной дисплазии | 29,34±4,75 | 11,71±3,3 | <0,005 |
| Ранние аллергические проявления | 22,82±4,37 | 2,13±1,4 | <0,001 |
| Дисфункции желудочно-кишечного тракта (ЖКТ) | 58,69±5,14 | 24,47±4,43 | <0,001 |
В структуре поражения центральной нервной системы (ЦНС) в неонатальном периоде в основной группе чаще отмечались признаки синдрома вегето-висцеральных нарушений (р<0,02), синдрома угнетения (р<0,05).
Среди дискинезии ЖКТ наиболее часто встречались запоры в сочетании с метеоризмом (р<0,001).
Анализируя факторы неонатального периода, мы установили, что для детей с наследственной предрасположенностью к атопии сильными по прогностической значимости факторами риска являются: ранние аллергические проявления (ПК=9,12), дисфункция ЖКТ в виде запора в сочетании с метеоризмом (ПК=7,87), отклонения в неврологическом статусе с клиническими проявлениями вегето-висцеральных нарушений (ПК=6,11), синдрома угнетения (ПК=4,19), клинические признаки ВУИ (ПК=5,32), проведение реанимационных мероприятий (ПК=4,86). Ассоциативной связью средней силы обладают: висцеральные признаки соединительнотканной дисплазии (ПК=3,99), пролонгированная гипербилирубинемия (ПК=3,45). Слабыми по прогностической значимости являются: гемолитическая болезнь новорождённых (ПК=1,3), признаки морфофункциональной незрелости, в том числе задержка внутриутробного развития (ЗВУР) (ПК=1,2).
Протекторами в неонатальном периоде у детей с наследственной предрасположенностью к атопии выступают следующие факторы: отсутствие отклонений в неврологическом статусе (ПК=-4,98), отсутствие дисфункций со стороны ЖКТ (ПК=-2,6), антропометрические показатели при рождении на уровне адаптивных (рост 50–52 см, масса 3200–3650 г) – ПК=-2,26, прикладывание к груди в родильном зале (ПК=-1,98), отсутствие ранних аллергических проявлений (ПК=-1,22).
Анализ факторов постнатального периода показал, что наибольшими протективными свойствами, способными нивелировать негативное воздействие предшествующих факторов, могут выступать: соблюдение матерью во время лактации правил гипоаллергенной диеты (ПК=-3,44); сохранение грудного вскармливания до 6 месяцев (ПК=-3,59); сохранение грудного вскармливания до 1 года (ПК=-5,27); отсутствие клинических проявлений пищевой аллергии (ПА) до 6 месяцев (ПК=-3,84); отсутствие клинических проявлений ПА до 3 месяцев (ПК=-2,71); отсутствие патологических изменений со стороны ЦНС в возрасте 3 месяцев (ПК=-3,06); темпы физического развития, соответствующие возрастным нормам (ПК=-1,75).
В результате проведённых лабораторных исследований была выявлена высокая частота микроэкологических нарушений у детей из группы риска в возрасте 2 месяцев (84,2 %). Снижение количества нормальных симбионтов отмечалось в 14,47 %, изолированный избыточный рост условно-патогенной микрофлоры (УПМ) с преобладанием высоких титров представителей рода энтеробактерий (Klebsiella, Enterobacter, Citrobacter), клостридий, а также St. аureus составлял 47,36 %, а сочетание снижения роста нормальных симбионтов с избыточным ростом представителей УПМ – 22,36 %.
Обращает на себя внимание высокая распространённость дисбиотических нарушений в группе детей с последующим развитием АтД, в отличие от группы детей без АтД (см. рис. 3).
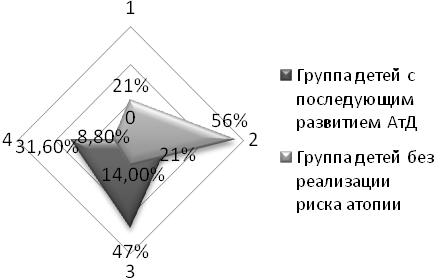
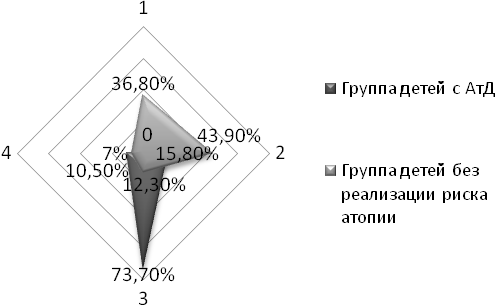
| ^ Рис. 3. Показатели микрофлоры кишечника у детей группы риска в доклиническом периоде заболевания | Рис. 4. Показатели микрофлоры кишечника у детей с АтД и без признаков заболевания |
| ^ 1 – оптимальные показатели микрофлоры кишечника; 2 – изолированный рост УПМ; 3 – сочетанное снижение уровня нормальных симбионтов с избыточным ростом УПМ; ^ 4 – изолированное снижение количества нормальных симбионтов | |
При повторном исследовании микрофлоры кишечника детей в возрасте 4–6 месяцев (см. рис. 4) у всех испытуемых с манифестацией АтД сохранялись дисбиотические изменения различной степени выраженности, в том числе – высокие титры представителей УПМ в двух- и трёхкомпонентных ассоциациях на фоне снижения количества нормальных симбионтов.
Напротив, в группе детей без проявлений АтД на первом году жизни в повторных исследованиях титры УПМ были достоверно ниже, двух- и трёхкомпонентные ассоциации представителей УПМ встречались значительно реже (p<0,05, p<0,01, соответственно).
Установлено, что сильной ассоциативной связью с развитием АтД обладает снижение уровня бифидобактерий < 1010-1011 КОЕ/г (Q=0,81), лактобактерий < 106-107 КОЕ/г (Q=0,67) и повышение уровня Klebsiella spp. > 104 (Q=0,68), гемолизирующих E.coli (Q=0,68). Ассоциативной связью средней силы обладает снижение E.coli типичных <107-108 КОЕ/г (Q=0,48) и повышение дрожжеподобных грибов рода Candida >103 (Q=0,47).
Нестабильность клеточных мембран является одним из важнейших звеньев в патогенезе многих хронических заболеваний, в том числе и АтД. В связи с этим нам представлялось важным определить содержание продуктов ПОБ в сыворотке крови и в слюне у детей с АтД и использовать их в качестве дополнительных ПК для составления прогноза АтД.
При обследовании детей грудного возраста с диагнозом АтД установлено, что интенсивность процессов ПОБ за счёт повышения содержания всех видов карбонильных производных в сыворотке крови и смешанной слюне у них выше по сравнению с условно здоровыми детьми (см. табл. 2).
Таблица 2
^ Показатели ПОБ в слюне и сыворотке крови
у грудных детей (М±m)
| Группа | Показатели ПОБ (в ед. опт. плотности) | |||||
| 356 нм | 370 нм | 430 нм | ||||
| в слюне | в крови | в слюне | в крови | в слюне | в крови | |
| Условно здоровые | 0,043± 0,006 | 3,83± 0,1 | 0,041± 0,006 | 3,29± 0,1 | 0,027± 0,008 | 2,08± 0,1 |
| Группа с АД | 0,093 ±0,01 (p<0,005) | 4,33± 0,07 (p<0,001) | 0,096± 0,01 (p<0,05) | 2,94± 0,09 (p<0,02) | 0,046± 0,007 (p<0,05) | 2,34± 0,06 (p<0,05) |
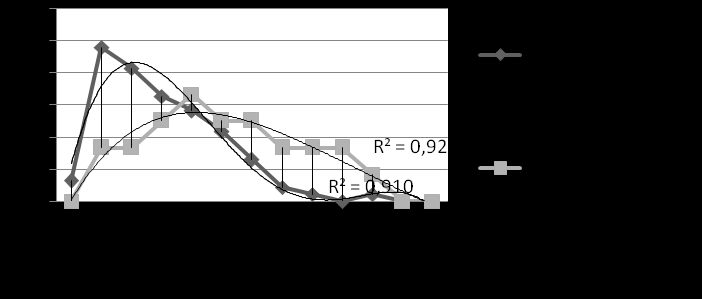
Получив достоверные различия в показателях ПОБ (как в смешанной слюне, так и в сыворотке крови) между группой детей с клиническими проявлениями АтД и группой условно здоровых детей, мы установили корреляционную зависимость высокой и средней силы между концентрацией продуктов ПОБ в сыворотке крови и слюне в данных группах. Наиболее высокая зависимость в группе детей, больных АтД (прямая, сильная), отмечена при 356 нм – r=+0,98 (р<0,01) (см. рис. 5).
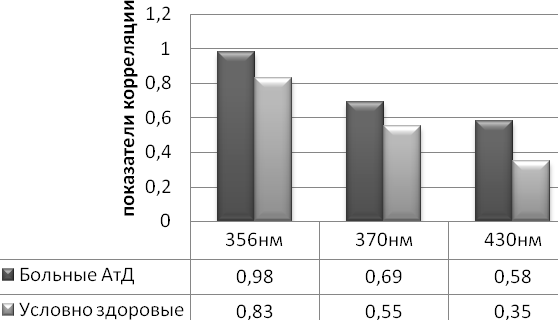
^ Рис. 5. Корреляционные зависимости между
концентрацией продуктов ПОБ в сыворотке крови
и смешанной слюне у детей с клиническими проявлениями
АтД и условно здоровых детей
Установлено также, что среди детей с АтД на первом году жизни показатели ПОБ слюны в среднем были достоверно выше в доклиническом периоде, составляли 0,088±0,01 (при 356 нм), 0,091±0,02 (при 370 нм), 0,39±0,009 (при 430 нм) и были сопоставимы с показателями ПОБ детей с клиническими проявлениями АтД (0,093±0,01, 0,096±0,01, 0,046±0,007), что позволило расценивать данные процессы как напряжённость резервно-адаптационных возможностей организма, готовых к срыву в виде проявлений АтД.
Наибольшую прогностическую значимость имеют показатели ПОБ в сыворотке крови при 356 нм (ПК=+7,46), в слюне – при 356 нм (ПК=+6,94).
Процедура прогнозирования, в первую очередь, необходима для планирования и проведения профилактических мероприятий.
На третьем этапе исследования был проведён анализ эффективности использования АМС ГА-1,2 для профилактики АтД у детей первого года жизни с риском атопии.
У детей, получающих смесь АМС (ГА)-1,2, отмечалась хорошая переносимость предлагаемого продукта: регистрировались лишь транзиторные нарушения функции ЖКТ, которые купировались без проведения какой-либо лекарственной терапии в течение 2–5 дней. В группе сравнения функциональные нарушения в период адаптации к новому питанию продолжались более 7 дней в 23,8 %, что потребовало медикаментозной и (или) диетической коррекции.
Анализ антропометрических данных по окончании 8 и 28 недель наблюдения показал, что в основной группе прибавка массы тела и роста соответствовали средневозрастным. В группе сравнения практически у четверти наблюдаемых детей физическое развитие детей было оценено как дисгармоничное (см. рис. 6).
^ Рис. 6. Динамика антропометрических показателей
(количество детей в группах, имеющих гармоничное физическое развитие)
Использование в питании АМС (ГА)-1,2 с пребиотическими свойствами способствовало повышению показателей бифидобактерий в составе микрофлоры кишечника (F=16,545, р<0,001). На фоне высоких показателей нормофлоры снижался уровень УПМ: St. аureus, Cаndida при повторном исследовании встречались в 4 раза реже по сравнению с первым исследованием. В группе сравнения оставались низкими показатели бифидобактерий – на уровне показателей входящих значений (F=0,727, р>0,05), количество лактобактерий в динамике снизилось (F=9,5757, р<0,01), значения E. сoli практически не изменились (F=2,7142, р>0,05). Увеличилось количество случаев высевов по таким показателям, как энтеробактер, клостридии, клебсиелла, Candida, гемолизирующие E. coli, чего в основной группе не наблюдалось.
Профилактические свойства АМС (ГА)-1,2 подтвердил тот факт, что у детей основной группы изменения кожных покровов зарегистрированы всего в 19,05 % случаев, причём данные изменения носили кратковременный характер (до 14 дней). В группе сравнения изменения кожи отмечались чаще (42,86 %), в том числе у 5 детей (23,81 %) в результате наблюдения и обследования был поставлен диагноз «атопический дерматит» (р<0,05).
ВЫВОДЫ
Дети с манифестацией АтД на первом году жизни чаще имеют такие отклонения в состоянии здоровья в неонатальном периоде, как патологические изменения ЦНС (р<0,001), пролонгированная гипербилирубинемия (р<0,02), клинические проявления внутриутробного инфицирования (р<0,05), висцеральные признаки соединительнотканной дисплазии (р<0,05), дисфункции ЖКТ (р<0,001). На сроки манифестации АтД у детей с наследственной предрасположенностью оказывает влияние степень выраженности дезадаптации в неонатальном периоде
(r=-0,69, р<0,02).
- Микроэкологические нарушения кишечника с увеличением титра представителей условно-патогенной микрофлоры, снижение уровня нормальных симбионтов предшествуют клиническим проявлениям АтД. Сильной ассоциативной связью с развитием АтД обладает снижение уровня бифидобактерий
< 1010-1011 КОЕ/г (Q=0,81), лактобактерий < 106-107 КОЕ/г (Q=0,67) и повышение уровня Klebsiella spp. > 104 (Q=0,68), гемолизирующих E.coli (Q=0,68).
- Окислительная деструкция белков является доклиническим индикатором повреждения ткани при формировании АтД в грудном возрасте. Уровень производных 2,4-динитрофенилгидразонов у детей в доклиническом периоде АтД сопоставим с таковыми у детей с клиническими проявлениями заболевания.
- Наиболее неблагоприятными клинико-анамнестическими факторами риска развития АтД на первом году жизни среди перинатальных являются: обострение у матери во время беременности АтД (ПК=6,62), пищевой аллергии (ПК=4,86), антибактериальная терапия во время беременности (ПК=5,74) и клинические проявления внутриутробного инфицирования (ПК=5,32). Среди факторов постнатального периода наиболее значимы: ранние аллергические проявления (ПК=9,12), дисфункция ЖКТ в виде запора в сочетании с метеоризмом (ПК=7,87), искусственное вскармливание с первого месяца жизни (ПК=6,62), злоупотребление матерью во время лактации молоком и молочными продуктами (ПК=6,11), гипоксически-ишемическое поражение ЦНС с синдромом вегето-висцеральных нарушений (ПК=6,11), высокий уровень производных 2,4-динитрофенилгидразонов в сыворотке крови (ПК=7,46) и в слюне (ПК=6,94).
- Применение гипоаллергенной адаптированной молочной смеси с добавлением пребиотических волокон у детей первого года жизни с риском атопии при невозможности грудного вскармливания способствует становлению оптимальных показателей микрофлоры кишечника, гармоничному физическому развитию и профилактике АтД.
^ Практические рекомендации
Разработанные прогностические таблицы могут быть рекомендованы к широкому использованию в амбулаторно-поликлинических и стационарных учреждениях для составления индивидуального сценария развития АтД на первом году жизни у детей с отягощённым наследственным анамнезом.
- Показатели перекисного окисления белков рекомендуется использовать как дополнительные критерии прогнозирования АтД у детей первого года жизни.
- У детей из группы риска по атопии необходимо проводить мониторинг состояния микрофлоры кишечника на первом и третьем месяце жизни, что позволит контролировать адаптационные возможности на доклиническом этапе.
- У детей первого года жизни с риском атопии при невозможности грудного вскармливания необходимо использовать гипоаллергенную адаптированную молочную смесь на основе умеренно гидролизованных белков.
^ СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ
ДИССЕРТАЦИИИ
Список научных работ соискателя по теме диссертации,
опубликованных в научных журналах, рекомендованных ВАК РФ
Степина, Н. А. Опыт применения гипоаллергенной адаптированной молочной смеси для профилактики атопического дерматита у детей первого года жизни / А. А. Джумагазиев, Н. А. Степина, Д. А. Безрукова, А. Б. Мясищева // Вопросы детской диетологии. – 2009. – № 5. – Т. 7. – С. 65–70.
- Оценка эффективности применения гипоаллергенной смеси, обогащённой пребиотиками, для профилактики атопического дерматита / А. А. Джумагазиев, Д. А. Безрукова, Н. А. Степина, А. Б. Мясищева // Вопросы современной педиатрии. – 2010. – № 1. – Т. 9. – С. 22–28.
Список научных работ опубликованных соискателем
по теме диссертации в других источниках
- Степина, Н. А. Окислительная модификация белков слюны у детей раннего возраста / Н. А. Степина, А. Б. Мясищева, Д. А. Безрукова // Лекарство и здоровье человека : сб. мат-лов VII Астраханской межрегиональной научно-практической конференции (г. Астрахань, 8–10 октября 2008 г.). – Астрахань, 2008. – C. 93–94.
- Степина, Н. А. Влияние частичных белковых гидролизатов с пребиотиками на реализацию риска атопической патологии у детей грудного возраста / Н. А. Степина, А. А. Джумагазиев, Д. А. Безрукова, Е. Г. Гаджиева // Фармакотерапия и диетология в педиатрии : сб. мат-лов научно-практической конференции педиатров России (г. Иваново, 16–17 сентября 2008 г.). – Иваново, 2008. – С. 129.
- Степина, Н. А. Йодная профилактика у детей раннего возраста в условиях антропогенной нагрузки / А. А. Джумагазиев, А. Б. Мясищева, Н. А. Степина, Д. А. Безрукова // Питание и здоровье : сб. мат-лов X Всероссийского конгресса нутрициологов (г. Москва, 1–3 декабря 2008 г.). – М., 2008. – С. 29–30.
- Степина, Н. А. Условно-патогенная микрофлора кишечника у детей первого года / Н. А. Степина, А. А. Джумагазиев, Д. А. Безрукова // Актуальные проблемы педиатрии : сб. мат-лов XVI съезда педиатров России (г. Москва, 16–19 февраля 2008 г.). – М., 2009. – С. 373–374.
- Степина, Н. А. Перекисное окисление белков слюны у детей грудного возраста с различной степенью обеспеченности йодом / Д. А. Безрукова, А. Б. Мясищева, Н. А. Степина, О. А. Шелкова // Человек и лекарство : сб. мат-лов XVI Российского национального конгресса (г. Москва, 6–10 апреля 2009 г.). – М., 2009. – С. 376.
- Степина, Н. А. Дефицит йода и оксидантная активность у детей грудного возраста / А. А. Джумагазиев, А. Б. Мясищева, Д. А. Безрукова, Н. А. Степина, Д. Л. Тёплый, О. Н. Позднякова // Актуальные проблемы педиатрии : сб. научн. работ / под ред. проф. А. Г. Муталова. – Уфа, 2008. – С. 57–58.
- Степина, Н. А. Оздоровление часто болеющих детей в условиях природного йодного дефицита / А. Б. Мясищева, О. А. Шелкова, Н. А. Степина, Д. А. Безрукова // Лекарство и здоровье человека : сб. мат-лов VIII Астраханской межрегиональной научно-практической конференции (г. Астрахань, 3–4 декабря 2009 г.). – Астрахань, 2009. – C. 121–123.
- Степина, Н. А. Прогностическая информативность наследственной отягощённости по развитию атопического дерматита у детей грудного возраста / Н. А. Степина, А. А. Джумагазиев // Фармакотерапия и диетология в педиатрии : сб. мат-лов научно-практической конференции (г. Ставрополь, 21–22 сентября 2010 г.). – Ставрополь, 2010. – С. 119.
- Степина, Н. А. Наследственные факторы риска развития атопического дерматита у детей первого года жизни / А. А. Джумагазиев, Н. А. Степина, Д. А. Безрукова // Аллергические и иммунологические заболевания – проблема XXI века : сб. мат-лов II Российской научно-практической конференции (г. Санкт-Петербург, 17–18 декабря 2010 г.). – СПб., 2010. – С. 13–14.
- Степина, Н. А. Родительские факторы риска в развитии атопического дерматита в грудном возрасте / А. А. Джумагазиев, Н. А. Степина, Д. А. Безрукова // Актуальные вопросы деятельности врача первичного звена здравоохранения : формирование принципов здорового образа жизни, профилактика, ранняя диагностика, эффективная фармакотерапия : сб. статей I Конгресса врачей первичного звена здравоохранения юга России, VI Конференции врачей общей практики (семейных врачей) юга России (г. Ростов-на-Дону, 2010 г.). – Ростов-на-Дону, 2010. – С. 74–77.
- Степина, Н. А. Прогнозирование и профилактика атопической патологии у детей, проживающих в условиях сочетанного воздействия антропогенной нагрузки и йодного дефицита : методическое пособие для врачей / Д. А. Безрукова, А. А. Джумагазиев, Н. А. Степина. – Астрахань, 2010. – 32 с.
^ Список сокращений
| АБ – аллергические болезни АМС ГА-1,2 – адаптированная молочная смесь гипоаллергенная АтД – атопический дерматит ВУГП – внутриутробная гипоксия плода ВУИ – внутриутробное инфицирование ЖКТ – желудочно-кишечный тракт | ЗВУР – задержка внутриутробного развития ПА – пищевая аллергия ПОБ – перекисное окисление белков ПК – прогностический коэффициент УПМ – условно-патогенная микрофлора ФР – факторы риска |
Степина Наталья Анатольевна
ПРОГНОСТИЧЕСКИЕ КРИТЕРИИ
РАЗВИТИЯ АТОПИЧЕСКОГО ДЕРМАТИТА
И ЕГО ПРОФИЛАКТИКА
У ДЕТЕЙ ГРУДНОГО ВОЗРАСТА
14.01.08 – Педиатрия
АВТОРЕФЕРАТ
диссертации на соискание учёной степени
кандидата медицинских наук
Подписано в печать 04.04.2011. Тираж 100 экз. Заказ № 2712.
______________________________________________________
Издательство ГОУ ВПО «АГМА Минздравсоцразвития России» 414000, г. Астрахань, ул. Бакинская, 121
