Конспект лекций «материаловедение»
| Вид материала | Конспект |
- Конспект лекций по теме: «Материаловедение» для специальности 120100 "Технология, 104.18kb.
- Конспект лекций по теме: «Материаловедение» для специальности 120100 "Технология, 5022.76kb.
- Е. в конспект лекций «материаловедение» ч. 1 конспект, 33.7kb.
- Конспект лекций «материаловедение», 249.86kb.
- Конспект лекций «материаловедение», 137.13kb.
- Конспект лекций 2008 г. Батычко В. Т. Административное право. Конспект лекций. 2008, 1389.57kb.
- Конспект лекций 2010 г. Батычко Вл. Т. Муниципальное право. Конспект лекций. 2010, 2365.6kb.
- Конспект лекций 2011 г. Батычко В. Т. Семейное право. Конспект лекций. 2011, 1718.16kb.
- Конспект лекций 2011 г. Батычко Вл. Т. Конституционное право зарубежных стран. Конспект, 2667.54kb.
- Конспект лекций «материаловедение», 197.98kb.
© СЗТУ кафедра МТМиП, Шадричев Е.В конспект лекций «МАТЕРИАЛОВЕДЕНИЕ» ч.1
Глава 2. КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ
2.1. КРИСТАЛЛИЗАЦИЯ
(ЭНЕРГЕТИЧЕСКОЕ ОБОСНОВАНИЕ ПРОЦЕССА)
Вещество может находиться в трех состояниях: газообразном, жидком и твердом, и при определенных условиях (давлении р, температуре Т) переходить из одного состояния в другое. Так, при нормальном давлении металл, достигнув температуры плавления Tпл, расплавляется, становится жидким, а при температуре кипения переходит в газообразное состояние. В каждом из этих агрегатных состояний вещество может находиться бесконечно долго при заданных внешних условиях, что является признаком равновесного состояния.
Из термодинамики известно, что все самопроизвольные процессы в природе протекают в направлении уменьшения энергии системы. Поэтому равновесному состоянию вещества отвечает минимум свободной энергии F, которую для твердых и жидких тел можно записать как
F = Е-ТS, (2.1)
где Е - полная внутренняя энергия системы (сумма потенциальной и кинетической); S - энтропия (мера внутреннего беспорядка).
Свободная энергия - часть полной энергии вещества, которая может обратимо изменять свою величину при изменении температуры. Так как энтропийный член ТS возрастает с повышением температуры, то F уменьшается,
И
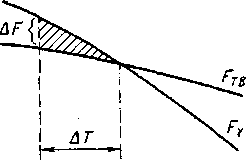 зменение свободной энергии металла в жидком Fж и твердом Fтв состояниях с увеличением температуры показано на рис. 2.1. При Т>Т0 устойчивым является жидкое состояние, так как Fж< Fтв, при Т<Т0 - твердое, поскольку Fтв<Fж. Очевидно, что при Т=Т0 переход металла из жидкого состояния в твердое, кристаллическое - кристаллизация - невозможен, так как оба состояния одинаково устойчивы, т. е. равновероятны. Поэтому Т=Т0 называется равновесной или теоретической температурой кристаллизации (плавления). Чтобы кристаллизация завершилась, процесс должен быть энергетически выгоден системе, т. е. ее свободная энергия должна понизиться (Fтв<Fж). Для этого, как видно из рис. 2.1, расплав надо охладить до некоторой температуры Ткр, называемой фактической температурой кристаллизации. Охлаждение жидкости ниже равновесной температуры кристаллизации Т0 называется переохлаждением, а Т=Т0-Ткр - степенью переохлаждения.
зменение свободной энергии металла в жидком Fж и твердом Fтв состояниях с увеличением температуры показано на рис. 2.1. При Т>Т0 устойчивым является жидкое состояние, так как Fж< Fтв, при Т<Т0 - твердое, поскольку Fтв<Fж. Очевидно, что при Т=Т0 переход металла из жидкого состояния в твердое, кристаллическое - кристаллизация - невозможен, так как оба состояния одинаково устойчивы, т. е. равновероятны. Поэтому Т=Т0 называется равновесной или теоретической температурой кристаллизации (плавления). Чтобы кристаллизация завершилась, процесс должен быть энергетически выгоден системе, т. е. ее свободная энергия должна понизиться (Fтв<Fж). Для этого, как видно из рис. 2.1, расплав надо охладить до некоторой температуры Ткр, называемой фактической температурой кристаллизации. Охлаждение жидкости ниже равновесной температуры кристаллизации Т0 называется переохлаждением, а Т=Т0-Ткр - степенью переохлаждения.Рис. 2.1. Зависимость свободных энергий твердой Fтв и жидкой Fж фаз от температуры
Итак, «движущей силой» кристаллизации является разность свободных энергий жидкой и твердой фаз F=Fж-Fтв, растущая с увеличением степени переохлаждения расплава (рис. 2.1).
^ 2.2. СУЩНОСТЬ ПРОЦЕССА КРИСТАЛЛИЗАЦИИ
(МЕХАНИЗМ ЗАРОЖДЕНИЯ КРИСТАЛЛОВ)
Наблюдения показывают, что при переохлаждении расплава до Tкр жидкость переходит в кристаллическое состояние не мгновенно и не одновременно во всем объеме. Кристаллизация возникает локально из одного или нескольких центров и распространяется с конечной скоростью, захватывая постепенно весь объем. Развитие кристаллизации - результат двух одновременно протекающих диффузионных процессов: зарождения кристаллов и их дальнейшего роста, как это схематически показано на рис. 2.2.
Как происходит зарождение кристаллов? Что является зародышами - центрами кристаллизации?

Рис. 2.2. Схема развития процесса кристаллизации

Хорошо известно, что такую роль могут играть мельчайшие частицы самого кристалла, либо каких-то примесей, попавшие в расплав (более подробно это будет обсуждаться в разделе 2.5.2.). Но зародыши могут возникать также и в чистом расплаве. Чтобы понять это, надо вспомнить, что представляет собой расплав.
Затраченная на плавление энергия настолько увеличивает амплитуду колебаний атомов, что они получают возможность отойти от своих «правильных» положений, расстраивая дальний порядок, свойственный кристаллу. Однако при не слишком сильном перегреве атомы в жидкости расположены не полностью хаотически, как в газе. В пределах нескольких межатомных расстояний сохраняется упорядоченное расположение атомов - ближний порядок, который одинаков для любого атома жидкости. Об этом свидетельствует сохранение координационного числа при плавлении веществ с плотными упаковками (т. е. большинства металлов) и незначительное изменение ряда их физических свойств. Поэтому при температурах, близких к Тпл , расплав по многим свойствам напоминает твердое тело, что позволяет говорить о «квазикристаллической» структуре расплава. При этом в жидком металле возможны небольшие образования с упорядоченной структурой. Наиболее крупные из них могут стать центрами кристаллизации - зародышами, рост которых в переохлажденном расплаве приводит к образованию поликристаллической структуры затвердевшего металла.
^ 2.3. ЗАВИСИМОСТЬ СКОРОСТИ КРИСТАЛЛИЗАЦИИ ОТ СТЕПЕНИ ПЕРЕОХЛАЖДЕНИЯ РАСПЛАВА
Теория показывает, что способность к дальнейшему росту получают лишь зародыши, размер которых r достигает некоторой критической величины rкр. Зародыши меньшего размера не являются устойчивыми образованиями, которые могли бы противостоять разрушительной силе тепловых колебаний атомов, и распадаются. Зародыши с rrкр растут до полного исчерпания расплава.
Образование зародышей с r=rкр происходит за счет присоединения атомов из расплава, для чёго необходима активная диффузия атомов. Скорость диффузии Vд, как известно, уменьшается с понижением температуры и, следовательно, с увеличением степени переохлаждения расплава T. С этой точки зрения вероятность образования зародышей с rrкр уменьшается с увеличением T. С другой стороны, вероятность образования кристаллов, как отмечалось выше, увеличивается с ростом разности свободных энергий F и, следовательно, T (см. рис. 2.1). В связи с этим, скорость образования зародышей Vз, равная числу зародышей, появляющихся в единицу времени в единице объема (т. е. размерность 1/см3с), должна зависеть от T так, как показано на рис.2.3.

Рис. 2.3. Зависимость скорости образования зародышей Vз от степени переохлаждения
Аналогичную зависимость от степени переохлаждения имеет и скорость роста зародышей Vр - скорость увеличения линейных размеров кристалла в единицу времени (размерность – см/с). Это объясняется тем, что рост кристаллов происходит путем осаждения на их грани островков двухмерных зародышей и присоединения к ним атомов из расплава (рис. 2.4). Поэтому Vр , как и Vз, зависит от соотношения F и Vд, а значит и T.
Р
 ис. 2.4. Схема роста кристалла: образование двухмерного зародыша (ДЗ) на плотноупакованной грани и присоединение к нему атомов из расплава. Наиболее прочно удерживаются атомы (1, 2) контактирующие с наибольшим числом соседей (соответствует числу заштрихованных плоскостей); одиночный атом (3) слабо связан с гранью и может вернуться в расплав
ис. 2.4. Схема роста кристалла: образование двухмерного зародыша (ДЗ) на плотноупакованной грани и присоединение к нему атомов из расплава. Наиболее прочно удерживаются атомы (1, 2) контактирующие с наибольшим числом соседей (соответствует числу заштрихованных плоскостей); одиночный атом (3) слабо связан с гранью и может вернуться в расплавКристаллизация, как уже говорилось (см. рис. 2.2) включает два одновременно протекающих диффузионных процесса: образования зародышей кристаллов и дальнейшего роста тех из них, чей размер rrкр . Поэтому скорость кристаллизации V (относительное количество (%) образовавшихся кристаллов в единицу времени) определяется скоростями образования зародышей Vз и их роста Vр1 и имеет подобную им зависимость от степени переохлаждения (рис. 2.5).
При T=0 F=0, следовательно, Vз = Vр = 0 - кристаллизация не происходит (V = 0). При переохлаждении расплава с ростом T увеличивается F, соответственно возрастают Vз, Vр и V. Однако с повышением вязкость жидкости увеличивается, диффузия атомов затормаживается. Это приводит к замедлению скорости роста кристаллов Vр, а при достаточно больших степенях переохлаждения - и к уменьшению скорости образования зародышей Vз. Поэтому функция V =f(T) проходит через максимум и при очень больших T V0, в этом случае кристаллическая фаза не образуется, затвердевание происходит путем «замораживания» жидкого аморфного состояния. В обычных условиях при реальных, не слишком высоких скоростях охлаждения расплава этого не происходит. Кристаллизация технических металлов завершается при малых степенях переохлаждения T 1...20 °С (т. е. падающие участки кривых на рис. 2.5 не реализуются).
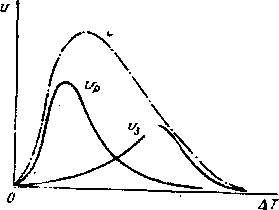
Рис. 2.5. Зависимости скорости зарождения U3, роста Uр кристаллов и средней скорости кристаллизации v от степени переохлаждения ΔТ
Металлы в аморфном состоянии (металлические стекла) получают при сверхбыстром охлаждении расплава со скоростями больше или равными 106 град/с (для сравнения - скорость охлаждения при закалке сталей в воде приблизительно 2102 град/с). Такие скорости охлаждения достигаются, например, при «размазывании» струи расплава по поверхности вращающегося массивного медного диска. В настоящее время удается получать аморфные металлы и сплавы в виде ленты шириной 2...15 мм и толщиной до 50 мкм или проволоки <20 мкм.
Аморфные металлы обладают рядом ценных свойств: имеют высокую прочность (превышающую прочность высокопрочных сталей), твердость, износостойкость, коррозионную стойкость, уникальные физические свойства. Это обусловлено в основном тем, что для таких материалов характерна однородная, однофазная структура, в которой отсутствуют границы зерен, дислокации, флуктуации состава и другие дефекты.
^ 2.4. РАЗМЕР ЗЕРНА В ЗАКРИСТАЛЛИЗОВАВШЕМСЯ МЕТАЛЛЕ (ВЛИЯНИЕ СТЕПЕНИ ПЕРЕОХЛАЖДЕНИЯ РАСПЛАВА)
Величина зерна - важный параметр металлического материала, так как при прочих равных условиях его механические свойства определяются дисперсностью структуры. В частности, измельчение зерна увеличивает протяженность межзеренных границ, являющихся барьером для скольжения дислокаций, и соответственно повышает прочность (см. раздел 1.3). Очевидно, что величина зерна определяется соотношением скоростей зарождения Vз и роста Vр кристаллов. Увеличение Vр должно приводить к укрупнению зерна, увеличение Vз - к появлению большого числа зародышей и, следовательно, к измельчению зерна. Установлено, что величина зерна V (объем кристаллика) может быть выражена соотношением
V=1,1(Vр /Vз )3/4 [см3] (2.2)
Поскольку Vр и Vз зависят от степени переохлаждения T расплава (см. рис. 2.3 и рис. 2.5), то и размер зерна является функцией T.
При малых степенях переохлаждения число зародышей мало (мала F и значит - Vз), а скорость их роста велика (велика скорость диффузии Vд и соответственно Vр), поэтому зерно получается крупным. При больших T Vр начинает отставать от Vз (вследствиё увеличения F и уменьшения Vд) - измельчается.
2.5. ПРИНЦИПЫ ПОЛУЧЕНИЯ Мелкого ЗЕРНА В
^ МЕТАЛЛЕ В ПРОЦЕССЕ КРИСТАЛЛИЗАЦИИ
Обычно следует стремиться к получению мелкозернистой структуры, так как такой металл обладает лучшими механическими свойствами, в частности более высокой прочностью. Это особенно важно, если закристаллизовавшийся металл используется в изделиях, не подвергающихся дальнейшей обработке, изменяющей его структуру. Такая ситуация имеет, например, место при эксплуатации термически не обрабатываемых литых изделий.
^ 2.5.1. Влияние скорости охлаждения расплава
Из предыдущего раздела следует, что размер зерна в затвердевшем металле уменьшается с увеличением степени переохлаждения T. Поскольку величина T пропорциональна скорости охлаждения расплава Vохл, то измельчение зерна может быть достигнуто ускорением охлаждения расплава.
На величину зерна влияют все факторы, от которых зависит Vохл. Такими факторами являются: температуры расплава и формы, в которую он заливается, объем и конфигурация формы, теплофизические свойства материала, из которого она изготовлена и др. С этим связано, например, одно из важнейших преимуществ литья в металлические формы (кокиль) по сравнению с литьем в песчано-глинистые формы. Ускоренный отвод теплоты через стенки металлической формы увеличивает T и соответственно обеспечивает получение мелкого зерна и более высоких механических свойств отливки.
П
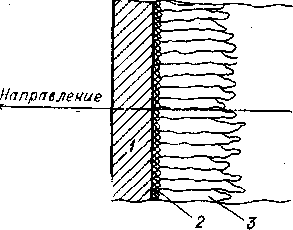 о этой же причине размер зерна не одинаков по сечению отливки. Наиболее мелкое зерно в наружной, корковой зоне (рис. 2.6), где максимальная скорость охлаждения.
о этой же причине размер зерна не одинаков по сечению отливки. Наиболее мелкое зерно в наружной, корковой зоне (рис. 2.6), где максимальная скорость охлаждения. Рис. 2.6. Схема кристаллического строения литого металла: 1 - стенка изложницы (формы); 2 - корковая зона; 3 - зона столбчатых кристаллов
Со скоростью охлаждения связаны размеры и форма кристаллов, примыкающих к корковой зоне отливки (зона столбчатых кристаллов). Они пре имущественно растут перпендикулярно стенке формы в направлении наилучшего теплоотвода. В этом направлении создается наибольшее переохлаждение, способствующёе образованию зародышей (растет F), а скорость роста достаточно высока, так как температура расплава (и скорость диффузии) повышаются от поверхности к центру отливки. Поэтому и получаются крупные вытянутые кристаллы. В массивных отливках возможно появление и третьей зоны крупных равноосных кристаллов в центре отливки, где металл, равномерно остывая, затвердевает в последнюю очередь.
Понятно, что такая неоднородность структуры создает и неоднородность механических свойств по сечению отливки.2 Этот факт, наряду с условиями эксплуатации литого изделия, Должен учитываться при его конструировании.
^ 2.5.2. Влияние примесей. Модифицирование
Описанный выше механизм образования зародышей называется самопроизвольным. или гомогенным, так как реализуется в высокочистых однородных расплавах.
В реальных условиях расплавы технических металлов всегда содержат растворенные примеси и (или) твердые частицы различного происхождения. Эти объекты, являясь центрами кристаллизации, облегчают образование зародышей, увеличивают их количество и, следовательно, уменьшают размер зерна. Такое образование зародышей называется гетерогенным, поскольку существует готовая граница раздела двух разнородных фаз - жидкой и кристаллической.
Гетерогенный механизм образования зародышей позволяет управлять величиной (и формой) зерна в отливке путем введения в расплав специальных примесей - модификаторов. Этот процесс называется модифицированием и применяется для улучшения структуры (главным образом измельчения зерна) и механических свойств металла. Наиболее эффективными модификаторами являются примеси тугоплавких элементов (не растворяющихся в расплаве), имеющих одинаковый тип решетки с основным металлом - эти факторы наилучшим образом способствуют образованию и росту зародышей.
Важно подчеркнуть, что модифицирование фактически не влияет на химический состав металла, так как модификаторы вводятся в очень небольших количествах (сотые доли процента от массы расплава).
Модифицирование позволяет на порядок уменьшить размер зерна в металле, что приводит к значительному улучшению его механических свойств. Введение модификаторов может вызвать и более сложные изменения в структуре сплавов. Это используется, например, для эффективного повышения прочности и пластичности литейных алюминиевых сплавов - силуминов.
В заключение этой темы необходимо отметить следующее:
1. Описанные в разделе 2.5 способы получения мелкого зерна в отливках являются наглядным примером того, как уже на стадии кристаллизации (производства) металла данного химического состава можно влиять на его свойства через целенаправленное изменение структуры. Еще более яркая иллюстрация такого влияния — это получение металлических стекол (раздел 2.3).
2. Рассмотренные выше закономерности кристаллизации, в частности зависимость скорости кристаллизации и размера зерна от степени переохлаждения, справедливы и для фазовых превращений, происходящих в твердом состоянии.3 Поэтому они важны для понимания сути процессов термической обработки и рекристаллизации - явления, протекающего при нагреве пластически деформированного металла (глава 3).
1Из соображений размерности и V ~ (Vз Vр 3)1/4 [1/c].
2 Зависимость механических свойств от структуры отливок определяется не только размерами, формой и взаимным расположением кристаллов (о чем говорилось в этом разделе), но и такими дефектами литых изделий, как раковины, поры, трещины, химическая неоднородность (ликвация). Эти дефекты являются концентраторами напряжений (см. раздел 1.3), уменьшают прочность и ударную вязкость.
3 Действительно, если при каком-либо фазовом превращении образование и рост частиц новой фазы происходят диффузионным путем, то закономерности этого процесса всегда определяются зависимостями скорости диффузии атомов и разности свободных энергий фаз от степени переохлаждения исходной фазы.
