Роль пробиотика пробифор в лечении рецидива и поддержании ремиссии язвенного колита 14. 00. 05 внутренние болезни
| Вид материала | Автореферат |
- Роль гравитационной хирургии в лечении стероид-зависимых и стероид-резистентных форм, 318.64kb.
- Рекомендации по применению препарата профеталь® в терапии неспецифический язвенный, 22.28kb.
- Тема : Хирургическое лечение осложнённого неспецифического язвенного колита. Болезнь, 118.83kb.
- Обоснование механизмов действия гирудорефлексотерапии в комплексном лечении бронхиальной, 390.9kb.
- Plantago ovata (Мукофальк®) в терапии язвенного колита составитель, 509.52kb.
- Г. С. Солдатова, В. К. Мазо, Г. Г. Егиазарян продукты серии «нутрикон» и их роль, 1669.11kb.
- Коллапсотерапия в комплексном лечении деструктивного туберкулёза лёгких 14. 00., 428.25kb.
- Расписание лекций по дисциплине «внутренние болезни», 62.03kb.
- Рабочая учебная программа по специальности аспирантуры «внутренние болезни» Кафедра, 517.71kb.
- Расписание лекций по дисциплине «внутренние болезни», 61.13kb.
Таблица 7
^ Состав кишечной микрофлоры у исследуемых пациентов первой, второй и третьей групп через 1 год от начала лечения
| Признаки | Количество пациентов с наличием признака в группах | ^ Всего (n=125) | ||||||
| Первая (n=42) | Вторая (n=42) | Третья (n=41) | ||||||
| n | % | n | % | n | % | n | % | |
| Номер графы | 1 | 2 | 3 | | ||||
| ^ E.coli нормальные штаммы, количество: сниженное | 53 | 11,9 | 10 | 23,8 | 181 | 43,9 | 33 | 26,4 |
| ^ E.coli гемолитические штаммы | 03 | 0 | 3 | 7,2 | 71 | 17,1 | 10 | 8 |
| ^ E.coli лактозонегативные штаммы | 7 | 16,7 | 3 | 7,2 | 3 | 7,3 | 13 | 10,4 |
| ^ Бифидобактерии, количество: -нормальное | 382,3 | 90,5 | 261,3 | 61,9 | 151,2 | 36,6 | 79 | 63,2 |
| -сниженное | 42,3 | 9,5 | 161,3 | 38,1 | 261,2 | 63,4 | 46 | 36,8 |
| ^ Лактобактерии, количество: -нормальное | 372,3 | 88,1 | 251,3 | 59,5 | 111,2 | 26,8 | 73 | 58,4 |
| -сниженное | 52,3 | 11,9 | 171,3 | 40,1 | 301,2 | 73,2 | 52 | 41,6 |
| Staphylococcus | 13 | 2,4 | 4 | 9,5 | 71 | 17 | 12 | 9,6 |
| Enterococcus | 7 | 16,7 | 9 | 21,4 | 7 | 17 | 23 | 18,4 |
| ^ Грибы Candida | 0 | 0 | 0 | 0 | 2 | 4,8 | 2 | 1,6 |
| Proteus | 03 | 0 | 3 | 7,14 | 81 | 19,5 | 11 | 8,8 |
| Citrobacter | 03 | 0 | 03 | 0 | 5 1,2 | 12,2 | 5 | 4 |
| Klebsiella | 02,3 | 0 | 11,3 | 2,4 | 21,2 | 4,8 | 3 | 2,4 |
Условно-патогенная микрофлора у пациентов первой группы была представлена лактозонегативными штаммами E.coli (16,7%), во второй и третьей группе – гемолитическими штаммами E.coli, протеем, цитробактером и клебсиеллой (табл.7).
Степень выраженности дисбактериоза кишечника через год от начала терапии в исследуемых группах пациентов представлена в таблице 8.
Таблица 8
Степень выраженности дисбиотических нарушений у пациентов первой, второй и третьей групп через 1 год от начала лечения
| Показатели | Количество пациентов с наличием признака в группах | |||||
| ^ Первая группа (n=42) | Вторая группа (n=42) | Третья группа (n=41) | ||||
| n | % | n | % | n | % | |
| Номер графы | 1 | 2 | 3 | |||
| Дисбактериоз I степени | 213 | 50 | 233 | 54,7 | 211, 2 | 4,9 |
| ^ Дисбактериоз II степени | 23 | 4,8 | 73 | 16,7 | 301, 2 | 73,2 |
| ^ Дисбактериоз III степени | 0 | 0 | 51 | 11,9 | 91 | 21,9 |
| ^ Нормальная микрофлора | 192, 3 | 45,2 | 71, 3 | 16,7 | 0 | 0 |
Как следует из данных, представленных в таблице 8, частота нормализации кишечной микрофлоры, зависела от используемых терапевтических схем. Так, к окончанию наблюдения во всех группах увеличилось количество пациентов с нормальным составом кишечных бактерий и снижением степени выраженности кишечного дисбактериоза. Однако, у пациентов первой группы, получавших антибактериальные препараты с последующим назначением на протяжении года пробиотика пробифор, терапевтический эффект оказался наиболее выраженным. Так, нормализация состава кишечных бактерий и дисбактериоз I степени наблюдались соответственно у 45,2% и 50% пациентов первой, у 16,7% и 54,7% – второй и у 0 и 4,9% – третьей группы. У большинства пациентов третьей группы, которым не проводилась терапия, направленная на коррекцию микрофлоры кишечника к окончанию наблюдения сохранялись выраженные дисбиотические нарушения.
Уровень эндогенной интоксикации через месяц и год от начала лечения снизился во всех исследуемых группах независимо от типа проводимой терапии. Однако, показатели ЭКА, ОКА, РСА в первой группе оказались значительно выше, чем во второй и третьей, а во второй - существенно выше, чем в третьей. Следовательно, последовательное включение в базисную терапию язвенного колита кишечных антисептиков и пробиотиков (препарата пробифор) способствовало существенному снижению уровня эндогенной интоксикации (рис. 2).
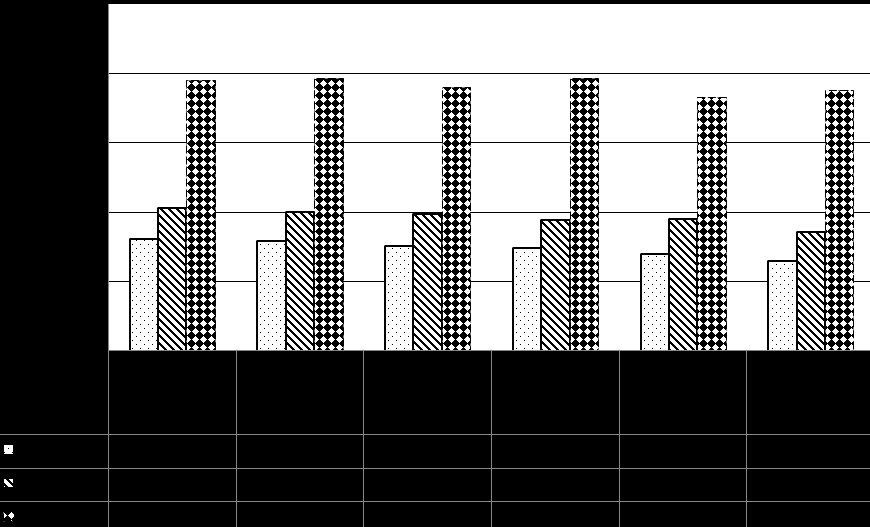
Рис. 2. Показатели эффективной (ЭКА) и общей (ОКА) концентрации, а также резерва связывания альбумина (РСА) у исследуемых пациентов в процессе лечения.
При оценке эффективности проводимой терапии к окончанию исследования оказалось, что частота ремиссии заболевания в первой группе составила 78,6%, во второй – 57,2%, в третьей – 46,3%. Рецидив язвенного колита в третьей группе наблюдался в четыре раза чаще, чем в первой и в 1,3 раза чаще, чем во второй группах (рис. 3).
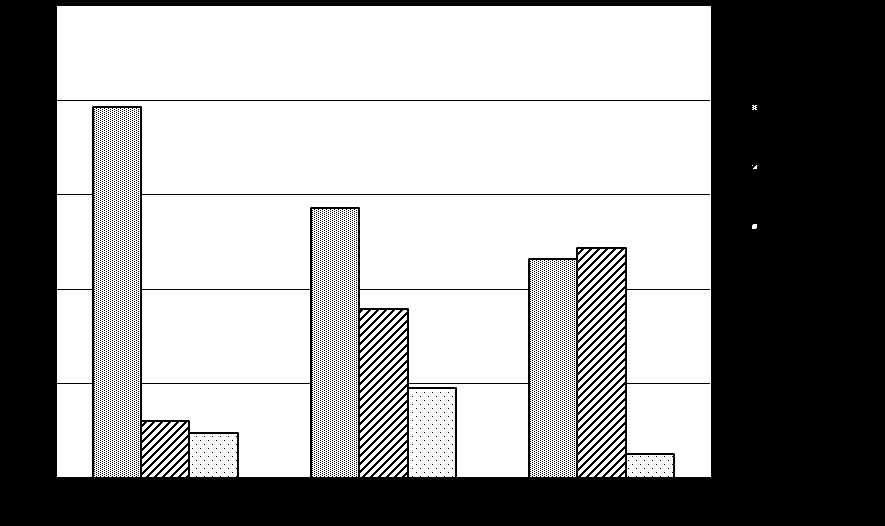
Рис 3. Эффективность проводимой терапии к окончанию исследования в группах пациентов
В итоге, через год от начала терапии у значительной части пациентов первой группы в отличие от групп сравнения отмечена нормализация состава кишечных бактерий, повышение уровня ЭКА, свидетельствующего о снижении эндотоксикоза и у 78,6% из них в течение года сохранялась ремиссия заболевания. В тоже время эффективность терапии во второй группе больных, получавших в период рецидива помимо базисной терапии антибиотики без последующего назначения пробифора, оказалась существенно выше в сравнении с третьей группой, находящейся на стандартном базисном лечении.
Полученные нами результаты свидетельствуют, что прием антибактериальных препаратов хотя и способствует элиминации условно - патогенной микрофлоры и снижению эндотоксикоза, однако без последующего приема пробиотиков результат терапии остается недостаточно эффективным. Известно, что антибиотики изменяют активность тканевых ферментов, многие из них, подавляя хемотаксис и продукцию антител, угнетают иммунную реактивность, и в отличие от пробиотиков они не участвуют в модуляции иммунного ответа и стимуляции противоинфекционной защиты (Шенкман Б. З., 1991).
Изучению механизмов действия и использованию пробиотиков, препаратов содержащих живые штаммы нормальных кишечных бактерий, в нормализации состава микрофлоры кишечника, в том числе и у пациентов ЯК, посвящена обширная литература (Григорьев П.Я., Яковенко Э.П., 2006; Парфенов А.И. с соавт., 2009; Bibiloni R. et al., 2005; Fuller R., 2005). Было установлено, что важным механизмом действия пробиотиков является антагонистический эффект в отношении патогенных и условно – патогенных штаммов кишечной микрофлоры, обусловленный действием метаболитов нормальных бактерий, основными из которых являются короткоцепочечные жирные кислоты и молочная кислота. Короткоцепочечные жирные кислоты являются основным источником питания эпителия кишки, способствуя его регенерации и росту, а также нормализации функций СО кишечника; улучшают всасывание электролитов и воды; участвуют в адаптации толстой кишки к его содержимому; влияют на моторику желудочно-кишечного тракта, а именно, снижают тонус желудка и замедляют эвакуацию, препятствуют забросу толстокишечного содержимого в тонкую кишку, в высоких концентрациях ингибируют моторику толстой кишки. Молочная кислота подавляет рост и колонизацию СО патологической микрофлорой, препятствуя ее адгезии к кишечному эпителию, способствует восстановлению нормального состава кишечных бактерий. Пробиотики участвуют в стабилизации эпителиального барьера, предотвращая транслокацию бактерий во внутреннюю среду, снижая уровень эндогенной интоксикации.
Важная роль в механизме действия пробиотиков отводится стимуляции иммунного ответа слизистых оболочек желудочно–кишечного тракта и других органов. Данные литературы свидетельствуют, что обогащение кишечной микрофлоры пробиотиками может усилить иммунные реакции и, в первую очередь, продукцию секреторного иммуноглобулина А, что предотвращает колонизацию слизистой оболочки желудочно-кишечного тракта патогенными и условно–патогенными бактериями [Rambaund J.S. et all., 2006].
Результаты собственных исследований подтвердили, что использование у пациентов с язвенным колитом пробиотиков является патогенетически обоснованным и оптимальная схема терапии, направленная на нормализацию кишечной микрофлоры у данных пациентов должна включать короткие курсы кишечных антисептиков с последующим приемом пробиотиков в течение длительных сроков. При проведении комплексной терапии, включающей коррекцию нарушений микробиоценоза кишечника, отмечено существенное повышение эффективности лечения ЯК. Полученные данные подтверждают роль нарушений кишечной микрофлоры в патогенезе заболевания и целесообразность использования пробиотиков в противорецидивной и поддерживающей терапии ЯК.
ВЫВОДЫ
- Выявление у всех пациентов с тотальным и у 92% с левосторонним поражением толстой кишки нарушений нормального состава кишечной микрофлоры, наличие прямой зависимости между выраженностью дисбиотических нарушений и степенью активности воспалительного процесса свидетельствуют о существенной роли дисбактериоза кишечника в патогенезе язвенного колита.
- Низкий уровень эффективной концентрации альбумина, свидетельствующий о наличии синдрома эндогенной интоксикации, был выявлен у всех пациентов с язвенным колитом и имел прямую корреляционную связь с объёмом поражения толстой кишки.
- У всех пациентов с язвенным колитом выявлена прямая зависимость между уровнем эндогенной интоксикации и степенью выраженности нарушений толстокишечной микрофлоры: эффективная концентрация альбумина у пациентов с дисбактериозом III степени оказалась достоверно ниже, чем при дисбактериозе II и I степени.
- Включение пробиотика пробифор в комплексную терапию рецидива язвенного колита способствовало более быстрому наступлению клинической и эндоскопической ремиссии, нормализации состава толстокишечных бактерий и снижению уровня эндогенной интоксикации.
- Использование в профилактической терапии язвенного колита пробиотика пробифор в сочетании с месалазином способствовало поддержанию нормального состава кишечной микрофлоры и сохранению клинико–эндоскопической ремиссии у 78,6% пациентов.
^ ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Учитывая высокую частоту выявляемости дисбактериоза кишечника у пациентов с левосторонней и тотальной формами язвенного колита в рутинной практике целесообразно проводить лечебные мероприятия, направленные на нормализацию кишечной микрофлоры без предварительного проведения микробиологического исследования кала.
- Оптимальной схемой терапии дисбактериоза кишечника у пациентов с язвенным колитом является назначения кишечных антисептиков с последующим приёмом пробиотика пробифор.
- Для профилактики рецидива язвенного колита в комплексную терапию данным пациентам следует наряду с препаратами 5-аминосалициловой кислоты включать пробиотик пробифор по следующей схеме: 10 доз 3 раза в день в течение месяца, ежеквартально, а также в случае появления жидкого стула «по требованию».
- С целью раннего выявления обострения, а также контроля над эффективностью терапии, возможно использование определения эффективной концентрации альбумина крови.
^ СПИСОК НАУЧНЫХ РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Колганова А.В., Яковенко Э.П., Агафонова Н.А. и др. Эффективность препарата пробифор в восстановлении кишечной микрофлоры у больных язвенным колитом // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2006. – Т. 16, № 5. Приложение 28. – С. 54.
- Колганова А.В., Яковенко Э.П., Гиоева И.З. и др. Влияние пробиотической терапии на уровень эндогенной интоксикации у пациентов с язвенным колитом // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2006. – Т. 16, № 5. Приложение 28. – С. 55.
- Колганова А.В., Яковенко Э.П., Иванов А.С. и др. Роль пробиотиков в
лечении больных ЖКБ после холецистэктомии // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2007. – Т. 17, № 5. Приложение 30. – С. 110.
4. Яковенко Э.П., Назарбекова Р.С., Колганова А.В. и др. Фармако-экономическая эффективность терапии больных с левосторонним язвенным колитом с использованием сульфасалазина и месалазина // Тезисы VIII съезда НОГР. – М.: Анахарсис, 2008. – С. 184–185.
5. Агафонова Н.А., Гиоева И.З., Казарина А.В. и др. Нарушение нормального состава кишечных бактерий: клиническое значение и вопросы терапии // Русский медицинский журнал. – 2008. – Т. 10, № 2. – С. 41–47.
6. Яковенко Э.П., Иванов А.Н., Колганова А.В. и др. Метаболические заболевания печени как системные проявления дисбактериоза кишечника. Роль пробиотиков в нормализации кишечной микрофлоры // Русский медицинский журнал. – 2008. – Т. 16, № 6. – С. 396–401.
7. Колганова А.В., Назарбекова Р.С., Иванов А.Н. и др. Влияние пробио-тика пробифор на уровень эндогенной интоксикации у пациентов язвенным колитом // Клиническая и экспериментальная гастроэнтерология. – 2009. - № 2. Приложение 1. – С. 199.
8. Колганова А.В., Назарбекова Р.С., Иванов А.Н. и др. Эффективность препарата пробифор в комплексной терапии язвенного колита // Клиническая и экспериментальная гастроэнтерология. 2009. – № 2. Приложение 1. – С. 200.
9. Колганова А.В., Назарбекова Р.С., Иванов А.Н. и др. Нарушение микрофлоры кишечника у больных язвенным колитом в зависимости от формы заболевания // Клиническая и экспериментальная гастроэнтерология. – 2009. – № 2. Приложение 1. – С. 200–201.
10. Казарина А.В., Назарбекова Р.С., Яковенко Э.П. Роль пробиотической терапии в лечении рецидива и поддержании ремиссии язвенного колита // Кремлевская медицина. Клинический вестник. – 2009. – № 2. – С.54–56.
СПИСОК СОКРАЩЕНИЙ
ОКА общая концентрация альбумина
РСА резерв связывания альбумина
СО слизистая оболочка
ЭКА эффективная концентрация альбумина
ЯК язвенный колит
