Конспект по химии лицеиста 8-1 класса (на 2008/2009 годы) 239фмл по лекциям
| Вид материала | Конспект |
- О преподавании химии в 2008/2009 учебном году, 190.58kb.
- Анализ районных олимпиадных работ по химии 2009 2010 учебного год, 22.03kb.
- Муниципальное общеобразовательное учреждение городского округа балашиха «средняя общеобразовательная, 1689.2kb.
- Тематический план лекций по общей химии для студентов 1 курса медико-профилактического, 169.84kb.
- Постановлений Правительства Рязанской области от 24. 12. 2008 n 351, от 07. 10. 2009, 1041.18kb.
- Конспект лекций 2008 г. Батычко В. Т. Административное право. Конспект лекций. 2008, 1389.57kb.
- Положение о Федеральном агентстве воздушного транспорта, 156.28kb.
- Урок за курс химии 8-11 класса Тема: «Обобщение и систематизация знаний за курс химии, 164.62kb.
- Конспект по логике материалы к лекциям для студентов по программе бакалавриата, 1071.63kb.
- Необходимость разработки программы развития гимназии на период 2010-2015 годы вызвана, 1157.54kb.







Конспект по химии лицеиста 8-1 класса (на 2008/2009 годы) 239ФМЛ Синякова Максима
по лекциям Бабаевой Светланы Яковлевны.
^ КОНСПЕКТ ПО ХИМИИ 8 КЛАССА 239ФМЛ
За 2008/2009 годы
по лекциям Бабаевой Светланы Яковлевны.

^ Первая часть из четырёх о приключениях Васи Пупкина на уроках химии.
…Первый год в 239ФМЛ…
…Пиратка/Неофициальное издание…
239corporation™
2009
Конспект по Химии для 8 класса 239ФМЛ 1
---------------------------------------------------------------------------------------------------------------------
Предмет Химии.
| Науки естественные (точные). | Физика, Химия, Биология и другие. | Математика |
| Науки гуманитарные (неточные). | Литература, История и другие. | Язык |
Уровни организации мира:
1). Субмакроуровень:
- Космос – Физика;
2).Планетарный уровень:
- Живое – Биология,
- Неживое – Физика,
- Внутри планеты – Геология;
3).Микроуровень:
- Вещество, атомы, молекулы – Химия;
4). Субмикроуровень:
- Ядра, взаимодействие, строение – Физика.
Определение. Химия – наука о веществах, их строении, их свойствах, превращении одних веществ в другие и явлениях, сопровождающих эти процессы.
Вещество. Физические свойства вещества.
Определение. Вещество – то, из чего состоит физическое тело.
Аксиома. Всякое вещество характеризуют физическими и химическими свойствами (вещество должно быть чистым).
Свойства:
1). Агрегатное состояние:
- Жидкое,
- Твёрдое,
- Газообразное,
- Плазма;
2).Физические свойства, определяемые органолептически:
- Вкус,
- Запах,
- Цвет;
Конспект по Химии для 8 класса 239ФМЛ 2
---------------------------------------------------------------------------------------------------------------------
3).Физические приборы измеряют:
- Твёрдость;
4). Температура:
- Плавления,
- Кипения,
- Возгонки;
Определение. Возгонка – переход агрегатного состояния вещества из твёрдого в газообразное, минуя жидкое.
5). Электропроводность;
6). Растворимость:
- В воде и так далее.
Аксиома. Пользуясь знаниями о физических свойствах вещества, можно предложить способ его очистки.
Атомно-молекулярное учение.
“Атомос” – неделимый.
Понятие атом ввёл Демокрит (2500 год до нашей эры)
Атомно-молекулярное учение:
1). Вещество образуется атомами;
2). Вещество образуется молекулами;
3). Вещество образуется любой комбинацией из этих частиц.
Определение. Атом – мельчайшая частица вещества, химически не делимая, физически делимая.
Определение. Атом – система, состоящая из ядра и слабо связанных с ним электронов.
Определение. Ядро – центр атома.
Определение. Молекула – мельчайшая частица вещества, химически делимая.
Определение. Ионы образуются, когда атом теряет или приобретает электроны.
Физические явления и химические реакции.
Определение. Физические явления – явления, не приводящие к образованию новых веществ.
Определение. Химические реакции – явления, в ходе которых из одних веществ (исходных) образуются другие (продукты реакции).
Правило! Исходные вещества и продукты реакции отличаются по строению и своим свойствам.
^ Конспект по Химии для 8 класса 239ФМЛ 3
---------------------------------------------------------------------------------------------------------------------
Признаки химических реакций:
1). Появление осадка;
2). Изменение цвета;
3). Шипение;
4). Вспенивание;
5). Выделение энергии в виде света,
тепла,
взрыва.
Условия, благоприятствующие ходу химической реакции:
1). Подогревание;
2). Изменение цвета;
3). Шипение.
Строение атома.
Элемент.
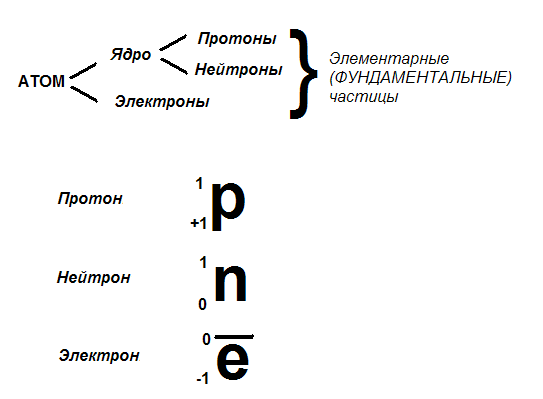
Конспект по Химии для 8 класса 239ФМЛ 4
---------------------------------------------------------------------------------------------------------------------
1
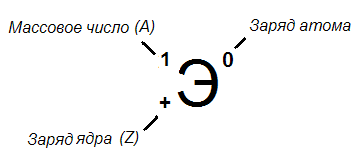 ).
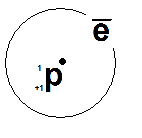
).
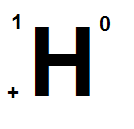
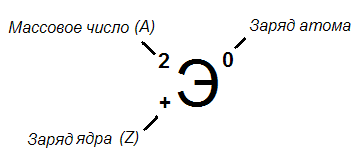
2).
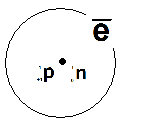
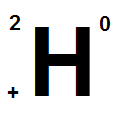
D-дейтерий
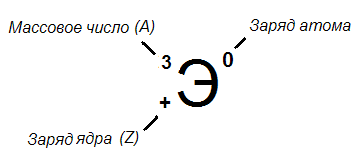
3).
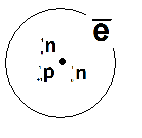
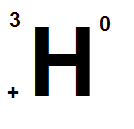
^
T- тритий
Аксиома. D и T – “тяжелые” H.
Определение. Изотопы – разновидность атомов, имеющих одинаковый заряд ядра, но разное массовое число из-за разного числа нейтронов.
^ Конспект по Химии для 8 класса 239ФМЛ 5
---------------------------------------------------------------------------------------------------------------------
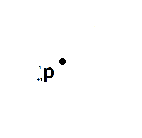
4
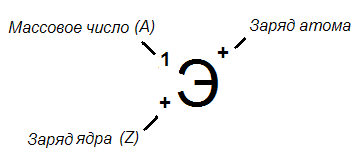 ).
). Катион H+
5
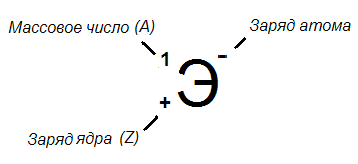 ).
).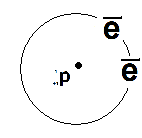
^ Анион H-
Определение. Элемент – абстрактное понятие, характеризующее совокупность атомов изотопов и ионов, заряд ядра у которых одинаков.
Массы атомов элементов.
Относительные атомные массы.
Аксиома. 1,67*10-24 грамм – масса атома водорода.
Аксиома. 1 атомная единица массы (а. е. м) = 1/12 массы изотопа углерода 12 C.
Относительная атомная масса элемента показывает во сколько раз масса данного атома больше 1/12 массы изотопа углерода 12 C.
Относительная атомная масса элементов, представленных в периодической таблице Менделеева, есть средняя относительная атомная масса всех природных изотопов этого элемента с учётом дефекта масс.
^ Конспект по Химии для 8 класса 239ФМЛ 6
---------------------------------------------------------------------------------------------------------------------
Электронное строение атома.
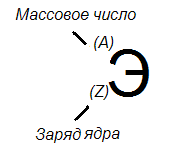
n (Э) =A-Z;
m (Э) =Z;
e (Э) =Z;
Определение. Электрон – фундаментальная частица.
Имеет двойственную природу:
частица m(e)= 1 а. е. м. / 1860
волна
Как частица имеет массу.
Теории строения атома.
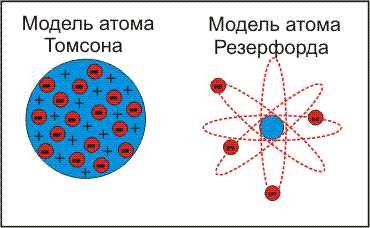
1). Модель Томпсона (булка с изюмом);
2). Модель Резерфорда;
3). Бор (квантование);
4). Квантово-механическая модель
с
 троения атома.
троения атома.