Джеймс трефил
| Вид материала | Закон |
- Джеймс А. Дискретная математика и комбинаторика [Текст] / Джеймс А. Андерсон, 42.79kb.
- Джеймс блиш города в полете 1-4 триумф времени вернись домой, землянин жизнь ради звезд, 10495.38kb.
- Джеймс Н. Фрей. Как написать гениальный роман, 2872.12kb.
- Мюриел Джеймс, Дороти Джонгвард, 4810.7kb.
- Кен Арнольд Джеймс Гослинг, 5058.04kb.
- Джеймс Джодж Бойл. Секты-убийцы (Главы из книги) Перевод с английского Н. Усовой, 844.92kb.
- Джеймс Хэрриот, 3697.74kb.
- В. К. Мершавки Доктор Джеймс Холлис известный юнгианский аналитик, директор Центра, 1972.4kb.
- В. К. Мершавки Доктор Джеймс Холлис известный юнгианский аналитик, директор Центра, 5237.48kb.
- Джеймс Боллард, 2244.23kb.
КВАНТОВЫЙ
ТУННЕЛЬНЫЙ
1925
ЭФФЕКТ
КВАНТОВАЯ МЕХАНИКА
1926
1962
УРАВНЕНИЕ ШРЁДИНГЕРА
ЭФФЕКТ ДЖОЗЕФСОНА
Представьте шарик, катающийся внутри сферической ямки, вырытой в земле. В любой момент времени энергия шарика распределена между его кинетической энергией и потенциальной энергией силы тяжести в пропорции, зависящей от того, насколько высоко шарик находится относительно дна ямки (согласно первому началу термодинамики). При достижении шариком борта ямки возможны два варианта развития событий. Если его совокупная энергия превышает потенциальную энергию гравитационного поля, определяемую высотой точки нахождения шарика, он выпрыгнет из ямки. Если же совокупная энергия шарика меньше потенциальной энергии силы тяжести на уровне борта лунки, шарик покатится вниз, обратно в ямку, в сторону противоположного борта; в тот момент, когда потенциальная энергия будет равна совокупной энергии шарика, он остановится и покатится назад. Во втором случае шарик никогда не выкатится из ямки, если не придать ему дополнительную кинетическую энергию, например, подтолкнув. Согласно законам механики ньютона, шарик никогда не покинет ямку без придания ему дополнительного импульса, если у него недостаточно собственной энергии для того, чтобы выкатиться за борт.
А теперь представьте, что борта ямы возвышаются над поверхностью земли (наподобие лунных кратеров). Если шарику удастся перевалить за приподнятый борт такой ямы, он покатится дальше. Важно помнить, что в ньютоновском мире шарика и ямки сам факт, что, перевалив за борт ямки, шарик покатится дальше, не имеет смысла, если у шарика недостаточно кинетической энергии для достижения верхнего края. Если он не достигнет края, он из ямы просто не выберется и, соответственно, ни при каких условиях, ни с какой скоростью и никуда не покатится дальше, на какой бы высоте над поверхностью снаружи ни находился край борта.
В мире квантовой механики дело обстоит иначе. Представим себе, что в чем-то вроде такой ямы находится квантовая частица. В этом случае речь идет уже не о реальной физической яме, а об условной ситуации, когда частице требуется определенный запас энергии, необходимый для преодоления барьера, мешающего ей вырваться наружу из того, что физики условились называть «потенциальной ямой». У этой ямы есть и энергетической аналог борта — так называемый «потенциальный барьер». Так вот, если снаружи от потенциального барьера уровень напряженности энергетического поля ниже, чем энергия, которой обладает частица, у нее имеется шанс оказаться «за бортом», даже если реальной кинетической энергии этой частицы недостаточно, чтобы «перевалить» через край борта в ньютоновском понимании. Этот механизм прохождения частицы через потенциальный барьер и назвали квантовым туннельным эффектом.
Работает он так: в квантовой механике частица описывается через волновую функцию, которая связана с вероятностью местонахождения частицы в данном месте в данный момент времени.

Пример образа атомной структуры, полученного при помощи электронного микроскопа, использующего квантовый туннельный эффект. Атомы золота (желтые, красные и коричневые) в три слоя на графитовой подложке
Если частица сталкивается с потенциальным барьером, уравнение гпрЁдннгЕРА позволяет рассчитать вероятность проникновения частицы через него, поскольку волновая функция не просто энергетически поглощается барьером, но очень быстро гасится — по экспоненте. Иными словами, потенциальный барьер в мире квантовой механики размыт. Он, конечно, препятствует движению частицы, но не является твердой, непроницаемой границей, как это имеет место в классической механике Ньютона.
Если барьер достаточно низок или если суммарная энергия частицы близка к пороговой, волновая функция, хотя и убывает стремительно при приближении частицы к краю барьера, оставляет ей шанс преодолеть его. То есть имеется определенная вероятность, что частица будет обнаружена по другую сторону потенциального барьера — в мире механики Ньютона это было бы невозможно. А раз уж частица перевалила через край барьера (пусть он имеет форму лунного кратера), она свободно покатится вниз по его внешнему склону прочь от ямы, из которой выбралась.
Квантовый туннельный переход можно рассматривать как своего рода «утечку» или «просачивание» частицы через потенциальный барьер, после чего частица движется прочь от барьера. В природе достаточно примеров такого рода явлений, равно как и в современных технологиях. Возьмем типичный РАДИОАКТИВНЫЙ распад: тяжелое ядро излучает альфа-частицу, состоящую из двух протонов и двух нейтронов. С одной стороны, можно представить себе этот процесс таким образом, что тяжелое ядро удерживает внутри себя альфа-частицу посредством сил внутриядерной связи, подобно тому как шарик удерживался в ямке в нашем примере. Однако даже если у альфа-частицы недостаточно свободной энергии для преодоления барьера внутриядерных связей, все равно имеется вероятность ее отрыва от ядра. И, наблюдая спонтанное альфа-излучение, мы получаем экспериментальное подтверждение реальности туннельного эффекта.
Другой важный пример туннельного эффекта — процесс термоядерного синтеза, питающий энергией звезды (см. эволюция звезд). Один из этапов термоядерного синтеза — столкновение двух ядер дейтерия (по одному протону и одному нейтрону в каждом), в результате чего образуется ядро гелия-3 (два протона и один нейтрон) и испускается один нейтрон. Согласно закону кулона, между двумя частицами с одинаковым зарядом (в данном случае протонами, входящими в состав ядер дейтерия) действует мощнейшая сила взаимного отталкивания — то есть налицо мощнейший потенциальный барьер. В мире по Ньютону ядра дейтерия попросту не могли бы сблизиться на достаточное расстояние и синтезировать ядро гелия.
Однако в недрах звезд температура и давление столь высоки, что энергия ядер приближается к порогу их синтеза (в нашем смысле, ядра находятся почти на краю барьера), в результате чего начинает действовать туннельный эффект, происходит термоядерный синтез — и звезды светят.
Наконец, туннельный эффект уже на практике применяется в технологии электронных микроскопов. Действие этого инструмента основано на том, что металлическое острие щупа приближается к исследуемой поверхности на сверхмалое расстояние. При этом потенциальный барьер не дает электронам из атомов металла перетечь на исследуемую поверхность. При перемещении щупа на предельно близком расстоянии вдоль исследуемой поверхности он как бы перебирает атом за атомом. Когда щуп оказывается в непосредственной близости от атомов, барьер ниже, чем когда щуп проходит в промежутках между ними. Соответственно, когда прибор «нащупывает» атом, ток возрастает за счет усиления утечки электронов в результате туннельного эффекта, а в промежутках между атомами ток падает. Это позволяет подробнейшим образом исследовать атомные структуры поверхностей, буквально «картографируя» их. Кстати, электронные микроскопы как раз и дают окончательное подтверждение атомарной теории строения материи.
Кварки и восьмеричный путь
1897
Все частицы в составе атомного ядра состоят из еще более фундаментальных частиц — кварков
элЕМЕНТАРНЫЕ
ЧАСТИЦЫ
1961 КВАРКИ
•
1961
И ВОСЬМЕРИЧНЫЙ ПУТЬ
СТАНДАРТНАя
1972
МОДЕЛЬ
КВАНТОВАя ХРОМОДИНАМИКА
Схематическое изображение одной из восьмеричных групп адронов. В нижнем ряду — два кси-гиперона (отрицательно и положительно заряженные); в среднем ряду — три сигма-гиперона и парный нейтральному сигма-гиперону лямбда-гиперон; в верхнем ряду — нейтрон и протон. Интересно, что по своим свойствам гиперон лямбда ноль Л° ничем не отличается от гиперона сигма ноль Е°, однако это разные частицы: они являются зеркальным отражением друг друга с точки зрения их структурного строения
На протяжении двух последних веков ученые, интересующиеся строением вселенной, искали базовые строительные блоки, из которых состоит материя, — самые простые и неделимые составляющие материального мира. атомная теория объяснила все многообразие химических веществ, постулировав существование ограниченного набора атомов так называемых химических элементов, объяснив природу всех остальных веществ через различные их сочетания. Таким образом, от сложности и многообразия на внешнем уровне ученым удалось перейти к простоте и упорядоченности на элементарном уровне.
Но простая картина атомного строения вещества вскоре столкнулась с серьезными проблемами. Прежде всего, по мере открытия все новых и новых химических элементов стали обнаруживаться странные закономерности в их поведении, которые, правда, удалось прояснить благодаря вводу в научный обиход периодической системы Менделеева. Однако представления о строении материи все равно сильно усложнились.
В начале XX столетия стало ясно, что атомы отнюдь не являются элементарными «кирпичиками» материи, а сами имеют сложную структуру и состоят из еще более элементарных частиц — нейтронов и протонов, образующих атомные ядра, и электронов, которые эти ядра окружают. И снова усложненность на одном уровне, казалось бы, сменила простота на следующем уровне детализации строения вещества. Однако и эта кажущаяся простота продержалась недолго, поскольку ученые стали открывать все новые и новые элементарные частицы . Труднее всего было разобраться с многочисленными адронами — тяжелыми частицами, родственными нейтрону и протону, которые, как оказалось, во множестве рождаются и тут же распадаются в процессе различных ядерных процессов.
Более того, в поведении различных адронов были обнаружены необъяснимые закономерности — и из них у физиков стало складываться некое подобие периодической таблицы. Использовав математический аппарат так называемой теории групп, физикам удалось объединить адроны в группы по восемь — два типа частиц в центре и шесть в вершинах правильного шестиугольника. При этом частицы из каждой восьмеричной группы, располагающиеся
на одном и том же месте
О Протон
Нейтрон О
л°Ое°
ГО
О
О.
в таком графическом представлении, обладают рядом общих свойств, подобно тому как схожие свойства демонстрируют химические элементы из одного столбца таблицы Менделеева, а частицы, расположенные по горизонтальным линиям в каждом шестиугольнике, обладают
Шесть типов кварков и их заряд (измеренный в зарядах электрона). Кроме того, у каждого кварка есть своя собс-твеная античастица
| Кварк Заряд | |
| и или р (верхний или протонный) | +2/3 |
| йштп (нижний или нейтронный) | -1/3 |
| с (очарованный) | +2/3 |
| з (странный) | -1/3 |
| Ь (красивый) | +2/3 |
| 1 (истинный) | -1/3 |
приблизительно равной массой, но отличаются электрическими зарядами (см. рисунок). Такая классификация получила название восьмеричный путь (в честь одноименной доктрины в буддистской теологии). В начале 1960-х годов теоретики поняли, что такую закономерность можно объяснить лишь тем, что элементарные частицы на самом деле таковыми не являются, а сами состоят из еще более фундаментальных структурных единиц.
Эти структурные единицы назвали кварками (слово позаимствовано из замысловатого романа Джеймса Джойса «Поминки по Финнегану»). Эти новые обитатели микромира оказались существами весьма странными. Для начала, они обладают дробным электрическим зарядом: 1/3 или 2/3 заряда электрона или протона (см. таблицу). А далее по мере развития теории выяснилось, что отдельно их не увидишь, поскольку они вообще не могут пребывать в свободном, не связанном друг с другом внутри элементарных частиц состоянии, и о самом факте их существования можно судить только по свойствам, проявляемым адронами, в состав которых они входят. Чтобы лучше понять этот феномен, получивший название пленение или заточение кварков, представьте, что у вас в руках длинный эластичный шнур, каждый конец которого представляет собой кварк. Если приложить к такой системе достаточно энергии — растянуть и порвать шнур, то он порвется где-то посередине, и свободного конца вы не получите, а получите два резиновых шнура покороче, и у каждого из них опять окажется два конца. То же и с кварками: какими бы энергиями мы ни воздействовали на элементарные частицы, стремясь «выбить» из них кварки, нам этого не удастся — частицы будут распадаться на другие частицы, сливаться, перестраиваться, но свободных кварков мы не получим.
Сегодня, согласно теории, предсказывается существование шести разновидностей кварков, и в лабораториях уже открыты элементарные частицы, содержащие все шесть типов. Самые распространенные кварки — верхний, или протонный (обозначается и — от английского up, или р — proton) и нижний, или нейтронный (обозначается d — от down, или п — от neutron), поскольку именно из них состоят единственные по-настоящему дол-гоживущие адроны — протон (uud) и нейтрон (udd). Следующий дублет включает странные кварки s (strange) и очарованные кварки с (charmed). Наконец, последний дублет состоит из красивых и истинных кварков — Ъ (от beauty, или bottom) и / (от truth, или top). Каждый из шести кварков, помимо электрического заряда, характеризуется изотопическим (условно направленным) спином. Наконец, каждый из кварков может принимать три значения квантового числа, которое называется его цветом (color) и обладает ароматом (flavor). Конечно же, кварки не пахнут и не имеют цвета в традиционном понимании, просто такое название сложилось исторически для обозначения их определенных свойств (см. квантовая хромодинамика).
стандартная модель останавливается на уровне кварков в детализации строения материи, из которой состоит наша Вселенная; кварки — самое фундаментальное и элементарное в ее структуре. Однако некоторые физики-теоретики полагают, что «луковицу можно лущить и дальше», но это уже чисто умозрительные построения. По моему личному мнению, стандартная модель правильно описывает строение вещества, и хотя бы в этом направлении наука дошла до логического завершения процесса познания.
МАРРИ ГЕЛЛ-МАНН (Murray GellMann, р. 1929) — американский физик. Родился в Нью-Йорке в семье иммигрантов из Австрии. Его книга «Восьмеричный путь» (Eightfold Way, 1964), написанная в соавторстве с Ювалем Неэманом (Yuval Ne'eman, 1925-2006) позволила систематизировать во множестве расплодившиеся элементарные частицы подобно тому, как предложенная
Дмитрием Ивановичем Менделеевым периодическая таблица помогла в свое время упорядоченно классифицировать химические элементы. За эту работу и развитие теории кварков и субатомных взаимодействий Гелл-Манн был удостоен Нобелевской премии по физике за 1969 год. Позже Гелл-Манн занялся исследованием сложных
АДАПТИВНЫХ СИСТЕМ.
кон. XIX
Кислотный дождь
Серные и азотные соединения, содержащиеся в атмосфере, повышают кислотность дождя
1863
1852 • КИСЛОТНЫЙ ДОЖДЬ
1886
ПАРНИКОВЫЙ ЭФФЕКТ
1887
КРУГОВОРОТ АЗОТА В ПРИРОДЕ
КИСЛОТЫ и ОСНОВАНИЯ
КРУГОВОРОТ ВОДЫ
1985
В ПРИРОДЕ
ОЗОНОВАЯ ДЫРА
Как мы знаем еще из школьного курса химии, чистая вода состоит из молекул, содержащих два атома водорода и один атом кислорода. Однако в каждый момент времени некоторые из этих молекул диссоциируют на положительно заряженные ионы водорода (то есть протоны, H+) и отрицательно заряженные гидроксид-ионы (OH-); одновременно с этим какие-то соседние ионы H+ и OH- соединяются с образованием молекул воды. Таким образом, даже в самой чистой воде сохраняется динамический баланс, равновесие, с присутствием определенного количества ионов водорода (протонов). Эти протоны связаны с молекулами воды, образуя ионы гид-рония — три атома водорода и один атом кислорода. В чистой воде концентрация ионов гидрония составляет 10-7 молей (см. закон авогадро) на литр.
Для оценки количества ионов водорода в воде химики используют понятие водородного показателя pH (сокр. от англ. «power of hydrogen» — «степень водорода»). Условились считать, что pH чистой воды равен 7. Такой водородный показатель соответствует химически нейтральной среде (см. кислоты и основания). С повышением концентрации ионов водорода pH понижается, и такие жидкости уже называются кислотами. Благодаря избыточному содержанию ионов водорода кислоты активно реагируют с другими веществами.
Термин «кислотный дождь» появился в середине XIX века, когда британские ученые заметили, что загрязнение воздуха в про-мышленно развитой центральной Англии привело к выпадению более кислых, чем обычно, дождей. Но только во второй половине XX века стало понятно, что кислотные дожди несут в себе угрозу окружающей среде.
Надо сказать, что обычный дождь является кислым сам по себе, даже в отсутствие заводов. Это происходит из-за того, что в процессе формирования и выпадения дождевые капли растворяют находящийся в воздухе углекислый газ и реагируют с ним с образованием угольной кислоты (H2CO3). Чистый дождь, проходящий через незагрязненный воздух, представляет собой водный раствор с pH 5,6 (к моменту удара о землю). Как мы увидим дальше, основная причина выпадения кислотных дождей — это деятельность человека, однако есть и естественные причины, начиная с извержения вулканов и разряда молнии и кончая жизнедеятельностью бактерий. В общем, даже если бы мы закрыли все фабрики и перестали ездить на машинах и грузовиках, значение pH дождя все равно было бы примерно 5,0. Поэтому сейчас принято считать дождь кислотным, если его pH ниже 5,0.
В современном промышленном мире избыточная кислотность дождя обусловлена в основном присутствием двух веществ:
— Оксиды серы. Эти соединения попадают в атмосферу естественным путем при извержениях вулканов, но значительная часть атмосферных оксидов серы образуется в результате сжигания природного топлива. Уголь и нефть
содержат небольшое количество серы. При сжигании этих видов топлива в атмосферу попадает сера в соединении с кислородом. Растворяясь в дождевых каплях, оксид серы образует серную кислоту. — Оксиды азота. При достаточно высокой температуре содержащийся в воздухе азот соединяется с кислородом с образованием оксида азота. В природе это может произойти во время разряда молнии, но основная часть оксидов образуется при сжигании бензина в двигателях внутреннего сгорания (например, в автомобилях) или при сжигании угля. При растворении этих веществ в капельках воды образуется азотная кислота.
Таким образом, дожди становятся кислотными при вымывании из воздуха серных и азотных соединений. Это явление имеет несколько последствий, губительных для природы. Например, многие исторические здания в Европе построены из известняка — строительного материала, реагирующего с кислотой. С течением времени кислотные дожди буквально разъедают поверхность этих зданий. При выпадении кислотных дождей также происходит закисление почвы и ухудшаются условия существования лесов. Некоторое время думали, что массовое отмирание верхушек деревьев в лесах на востоке США и в Германии обусловлено кислотными дождями, но теперь эта точка зрения не поддерживается. (Действительно, леса гибнут, но связано это с другими причинами.) И наконец, кислотные дожди повышают кислотность рек и озер, тем самым создавая угрозу флоре и фауне.
Методы борьбы с образованием кислотных дождей направлены на улучшение технологии удаления соединений серы из воздушных выбросов промышленных предприятий и электростанций, для чего обычно используют устройство под названием скруббер. Правительства некоторых государств даже приняли законы, ограничивающие содержание загрязняющих веществ в выхлопах транспортных средств.
Кислоты и основания
Кислоту можно определить как вещество, высвобождающее в воде ион водорода, либо как вещество, которое может передавать протон, либо как вещество, способное присоединять электронную пару
Основание можно определить как вещество, высвобождающее в воде гидроксид-ион, либо как вещество, которое может принимать протон, либо как вещество, способное отдавать электронную пару
1683 • ФЛОГИСТОН
1852 • КИСЛОТНЫЙ ДОЖДЬ
1887 • КИСЛОТЫ
И ОСНОВАНИЯ
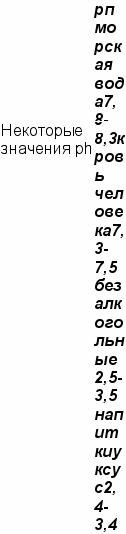
1930-е • ХИМИЧЕСКИЕ СВЯЗИ
Из нашего повседневного опыта мы знаем, что некоторые вещества обладают высококоррозионными свойствами. Например, если кислота из аккумулятора вашей машины попадет на одежду, она сразу же ее проест. Иногда мы используем аммиак и другие вещества для домашней уборки. Эти коррозионные вещества известны химикам как кислоты и основания. На поверхностном уровне их различить совсем не сложно. Кислоты кислые на вкус и окрашивают лакмусовую бумажку в красный цвет, щелочи же мыльные на ощупь и окрашивают лакмусовую бумажку в синий цвет. Однако химики редко довольствуются такого рода феноменологическими определениями. Они ищут ответ на вопрос: «Что делает вещество кислотой или основанием на молекулярном уровне?» Вот уже больше века химики бьются над определением кислот и оснований.
Первая попытка определить понятие кислоты восходит к 1778 году. Антуан Лавуазье смог объяснить, что именно происходит при горении, опровергнув бытовавшую до того теорию о ологистонЕ. Содержащийся в воздухе газ, который соединяется с веществами, когда они горят, он назвал кислородом — от греческого «производящий кислоту», поскольку он считал (как потом оказалось, ошибочно), что все кислоты содержат кислород.
Определение Аррениуса
Современный подход к этой проблеме впервые сформулировал шведский химик Сванте Аррениус (8уайе Аггпегиш, 1859-1927). Его определение, выдвинутое в 1877 году, было очень простым: если некоторое вещество при растворении в воде высвобождает ион водорода (то есть протон, Н+), значит, это кислота. Если же при растворении в воде высвобождается гидроксид-ион (ОН-), то это основание. Согласно этому определению, аккумуляторная кислота, представляющая собой водный раствор серной кислоты (Н2804), является кислотой, потому что атомы водорода серной кислоты в растворе становятся ионами водорода. Соответственно, гидроксид натрия (№ОН) является основанием, так как в воде он высвобождает гидроксид-ион. Это определение объясняет, почему кислоты и основания нейтрализуют друг друга. Когда гидроксид-ион встречается с ионом водорода, они соединяются с образованием Н2О, обычной воды.
Между прочим, Аррениус активно участвовал в дискуссии о внеземном разуме (см. парадокс ферми). Он был сторонником теории панспермии — гипотезы о том, что жизнь с планеты на планету могут переносить микроорганизмы, перемещающиеся через космос, а значит, достаточно было жизни развиться лишь однажды, а не на каждой планете, где она есть. На смену этой гипотезе пришла теория направленной панспермии, в соответствии с которой где-то в Галактике существует цивилизация, которая рассылает зародыши жизни с целью заселения подходящих планет. Однако все эти теории только отодвигают решение проблемы
происхождения жизни, потому что все равно остается вопрос, как жизнь зародилась в самом первом месте.
Определение Брёнстеда—Лаури
Определение Аррениуса довольно точное, но область его применения ограниченна — оно годится только для водных растворов (веществ, растворенных в воде). Вот пример реакции, на которую не распространяется определение Аррениуса: если вы поместите рядом сосуды с соляной кислотой (HCl) и аммиаком (NH3), вы увидите белый дымок над сосудами. Пары аммиака и соляной кислоты смешиваются в воздухе над сосудами, и происходит химическая реакция
NH + HCl — NH 4Cl,
в которой кислота и основание соединяются с образованием хлорида аммония. Поскольку в этой реакции не участвует вода, определение Аррениуса здесь просто неприменимо.
В 1923 году датский химик Йоханнес Николаус Брёнстед (Johannes Nicolaus Bronsted, 1879-1947) и британский химик Томас Мартин Лаури (Thomas Martin Lowry, 1874-1936) предложили новое определение. В соответствии с ним кислота представляет собой молекулу или ион, способные отдавать протон (то есть ион водорода H+), а основание представляет собой молекулу или ион, способные принимать протон. Если рассматриваемая реакция протекает в водной среде, это определение по сути то же, что и определение, предложенное Аррениусом, однако оно распространяется также на реакции, протекающие в отсутствие воды, такие как образование хлорида аммония, описанное выше.
Определение Льюиса
Наконец, последнее обобщение сделало определение кислот и оснований не зависящим не только от присутствия воды, но и от образования протонов. Его выдвинул в 1923 году американский химик Гилберт Ньютон Льюис (Gilbert Newton Lewis, 1875-1946). Это определение основано на том, каким способом образуются химические связи в химических реакциях между кислотами и основаниями, а не на том, присоединяются или отдаются протоны. По Льюису, кислота — это химическое соединение, способное принимать электронную пару с последующим образованием кова-лентной связи, а основание — это соединение, способное отдавать электронную пару.
Определение Льюиса включает в себя оба более ранних определения, а также объясняет те реакции, в которых не участвует водород. Например, когда диоксид серы реагирует с ионом кислорода с образованием серного ангидрида (эта реакция играет немаловажную роль в образовании кислотных дождей), ион
кислорода отдает два электрона для образования ковалентной связи — иными словами, ведет себя как основание, в то время как диоксид серы принимает электроны и, следовательно, ведет себя как кислота. Эта реакция, протекающая без протона и без воды, подходит под определение Льюиса, но не подходит ни под одно из предшествующих определений.
Показатель pH: измерение кислотности
Для водных растворов широко используется система определения концентрации кислоты или основания, которая лучше всего может быть объяснена в терминах теории Брёнстеда—Лаури. В чистой воде в каждый момент времени какие-то молекулы H2O диссоциируют на ионы водорода (H+) и гидроксид-ионы (OH-), и одновременно с этим какие-то соседние ионы H+ и OH- соединяются с образованием молекул воды. Таким образом, в воде всегда присутствуют ионы водорода (протоны). Молярная концентрация (см. закон авогадро) водорода в чистой воде составляет 10-7 моль на литр. Это означает, что одна молекула H2O из каждых 10 миллионов находится в форме ионов.
Условились считать, что водородный показатель pH (сокр. от англ. power of hydrogen — «степень водорода») чистой воды равен 7 — это математический показатель степени из выражения 10-7, взятый с положительным знаком. Мы можем повысить концентрацию ионов водорода в воде, добавив кислоту. Например, если мы добавим в чистую воду соляную кислоту (HCl), концентрация ионов водорода возрастет. Если мы достигнем точки, в которой молярная концентрация составляет 10-1 моль на литр, мы получим примерное значение кислотности желудочного сока. pH этого раствора составит 1. Таким образом, pH ниже 7 характеризует кислоту, и чем меньше значение pH, тем сильнее кислота.
Подобным образом можно понизить концентрацию ионов водорода в чистой воде, добавив основание (ионы OH- основания будут реагировать с ионами H+ с образованием молекул воды). Так, у аммиака, применяемого в домашнем хозяйстве, молярная концентрация ионов водорода составляет всего 10-11 моль на литр, и, следовательно, pH равен 11. А поскольку pH больше 7, это основание.
Клеточная теория
-
•
1663, 1839
Все живые организмы состоят из одной или нескольких клеток;
- химические реакции, происходящие в живых организмах, локализованы внутри клеток;
- все клетки ведут начало от других клеток;
- в клетках содержится наследственная информация, которая передается от одного поколения к следующему
КЛЕТОЧНАЯ ТЕОРИЯ
Первым человеком, увидевшим клетки, был английский ученый Роберт Гук (известный нам благодаря закону гука). В 1663 году, пытаясь понять, почему пробковое дерево так хорошо плавает, Гук стал рассматривать тонкие срезы пробки с помощью усовершенствованного им микроскопа. Он обнаружил, что пробка разделена на множество крошечных ячеек, напомнивших ему монастырские кельи, и он назвал эти ячейки клетками (по-английски cell означает «келья, ячейка, клетка»). В 1674 году голландский мастер Антоний ван Левенгук (Anton van Leeuwenhoek, 1632-1723) с помощью микроскопа впервые увидел в капле воды «зверьков» — движущиеся живые организмы. Таким образом, к началу XVIII века ученые уже знали, что в живых организмах есть клетки.
Однако лишь в 1838 году Маттиас Шлейден, посвятивший много лет жизни подробнейшему изучению растительных тканей, предположил, что все растения состоят из клеток. А год спустя Шлейден и Теодор Шванн высказали гипотезу, что клеточное строение имеют все живые организмы. Так была заложена основа современной клеточной теории. В 1858 году теорию дополнил немецкий патолог Рудольф Вирхов (Rudolph Virchow, 1821-1902). Ему принадлежит высказывание: «Там, где есть клетка, должна быть и предшествующая ей клетка». Иными словами, живое может возникнуть только от другого живого. Когда были переоткрыты законы менделя и ученые заинтересовались вопросами наследственности, клеточная теория была дополнена четвертым из перечисленных выше тезисов. Сегодня хорошо известно, что наследственный материал содержится в клеточной ДНК (см. центральная догма молекулярной биологии).
XIX-XX
XIX-XX
1859
1953
1958
•
БИОЛОГИЧЕСКИЕ МОЛЕКУЛЫ
РАСПРОСТРАНЕНИЕ НЕРВНЫХ ИМПУЛЬСОВ
ТЕОРИЯ ЭВОЛЮЦИИ ДНК
ЦЕНТРАЛЬНАЯ ДОГМА МОЛЕКУЛЯРНОЙ
БИОЛОГИИ
