Л. В. Титова общая характеристика работы
| Вид материала | Автореферат |
- Титова Алексея Антоновича Уважаемые родители, коллеги, представители общественности!, 217.93kb.
- Содержание лекций Модели местного самоуправления в России Местное самоуправление:, 786.51kb.
- Общая характеристика работы актуальность работы, 336.09kb.
- Общая характеристика работы актуальность работы, 236.99kb.
- Общая характеристика работы актуальность работы, 227.87kb.
- Общая характеристика работы актуальность работы, 227.87kb.
- Задачи физического воспитания детей дошкольного возраста. Общая характеристика средств, 34.6kb.
- Реферат по курсу: экология на тему: Общая характеристика экосистем, как, 726.64kb.
- Научная работа студентов, 2114.42kb.
- Научная работа студентов, 2153.55kb.
На правах рукописи
Ипатова
Ольга Евгеньевна
НЕОНАТАЛЬНЫЙ СКРИНИНГ НА АДРЕНОГЕНИТАЛЬНЫЙ СИНДРОМ В АРХАНГЕЛЬСКОЙ ОБЛАСТИ:
КЛИНИКО-ЛАБОРАТОРНАЯ ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ
14.00.09-педиатрия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Архангельск -2009
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Северный государственный медицинский университет (г. Архангельск)» Федерального агентства по здравоохранению и социальному развитию на кафедре педиатрии ФПК и ППС
Научный руководитель:
доктор медицинских наук, профессор Сибилева Елена Николаевна
Официальные оппоненты:
доктор медицинских наук, профессор Галина НиколаевнаЧумакова
доктор медицинских наук, профессор Елена Борисовна Башнина
Ведущая организация:
ГУ Эндокринологический научный центр РАМН, г. Москва
Защита диссертации состоится «____» апреля 2009г. в ______часов
на заседании диссертационного совета Д 208.004.02 при ГОУ ВПО «Северный государственный медицинский университет (г.Архангельск) Федерального агентства по здравоохранению и социальному развитию» (163061, г. Архангельск, пр. Троицкий, 51)
С диссертацией можно ознакомиться в научной библиотеке ГОУ ВПО «Северный государственный медицинский университет (г.Архангельск) Федерального агентства по здравоохранению и социальному развитию» (163061, г. Архангельск, пр. Троицкий, 51)
Автореферат разослан «____» марта 2009г.
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор Л.В. Титова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность исследования.
Неонатальный скрининг представляет собой программу массового обследования новорожденных с целью максимально раннего выявления наследственных нарушений обмена веществ. Критерием выбора заболеваний, подлежащих скринингу, является предоставление новорожденному ребенку возможности избежать в зависимости от заболевания смерти в раннем возрасте, тяжелой умственной отсталости, инвалидности в результате тяжелой соматической патологии (Петеркова В.А., 2003,2006).
До 2006 года в Российской Федерации накоплен 16-летний опыт проведения неонатального скрининга на фенилкетонурию и врожденный гипотиреоз (Ходунова А.А., Петеркова В.А., Касаткина Э.П., 2005). В 2006 году на 53 территориях (в том числе Архангельской области) в рамках реализации приоритетного национального проекта «Здоровье» осуществлено расширение данной программы до пяти заболеваний путем включения исследований на адреногенитальный синдром, галактоземию и муковисцидоз.
Частота дефицита 21-гидроксилазы, с которым связано развитие адреногенитального синдрома, в мире чрезвычайно высока. По данным зарубежных авторов в классическом варианте, установленном в ходе неонатального скрининга, составляет от 1: 280 (Аляска) до 1: 37 220 (Швейцария) новорожденных детей (Дедов И.И., Петеркова В.А., 2000, 2002; Speiser P.W., 2004; Van der Kamp H.J. 2004). Данные о частоте этого заболевания у новорожденных детей в России по результатам неонатального скрининга впервые опубликованы Т. В. Семичевой в конце 2007 года.
К настоящему времени публикации результатов неонатального скрининга на адреногенитальный синдром в регионах России немногочисленны. Алгоритм оценки результатов неонатального скрининга на 17-гидроксипрогестерон (далее 17ОНР) представлен в России на основе анализа данных скрининговых программ, выполняемых в США, Швеции, Швейцарии, Италии в соответствии с общими рекомендациями Рабочей группы Европейского общества педиатров-эндокринологов в 2001 году.
Пороговый уровень (Cut-off) 17гидроксипрогестерона (далее 17ОНР), который зависит от массы тела новорожденного ребенка, срока гестации, по данным европейских исследователей составляет от 30 до 90 нмоль/л в разных странах (Van der Kamp H.J. 2005, Thompson R.. 1989, Robinson J.A. 1986, Gruñeiro-Papendieck L. 2001,2008, Allen D.B. 1997 и др.)
Изучение пренатального стресса человека в неблагоприятных условиях Европейского Севера С.Г. Сухановым (1993) и К.Н Ковровым (1997) показало, что у плодов с высоким риском развития перинатальной патологии развивается стрессорная реакция, в которую вовлекаются звенья эндокринно-иммунного комплекса. Распространенность случаев течения беременности с высоким риском перинатальной патологии в условиях высоких широт, где расположена Архангельская область, превышает аналогичный уровень в среднеширотных регионах страны. Наиболее чувствительными к факторам пренатального стресса являются вилочковая железа и надпочечники, что сочетается с нарушениями темпов структурно-функцонального становления этих органов. Влияние адаптивных изменений надпочечников, характерных для плодов и новорожденных «северян» по сравнению со среднеширотной нормой, на уровень 17ОНР не изучено.
Цель и задачи исследования.
Цель работы – разработать пути оптимизации неонатального скрининга на адреногенитальный синдром у новорожденных детей в Архангельской области с целью повышения его диагностической точности.
Для достижения цели решались следующие задачи:
- Изучить частоту классических форм адреногенитального синдрома среди новорожденных детей, их распространенность в детской популяции в Архангельской области.
- Разработать рекомендации по обследованию новорожденных детей с повышенными уровнями 17ОНР в условиях Архангельской области в соответствии с региональными пороговыми значениями неонатального уровня 17ОНР при различных сроках гестации.
- Изучить влияние низкой массы тела и неонатальной транзиторной гипертиреотропинемии на уровень 17ОНР у новорожденных детей.
- Изучить влияние сезонов года и широты региона рождения на уровень 17ОНР у новорожденных детей.
- Определить экономическую эффективность проведения неонатального скрининга на врожденный адреногенитальный синдром в Архангельской области.
Положения, выносимые на защиту.
- У новорожденных детей Архангельской области в раннем неонатальном периоде установлены более низкие, чем у детей европейской популяции, медиана и верхний предел нормативных значений 17ОНР в различные гестационные сроки.
- Низкие показатели верхнего предела нормативных значений 17ОНР в группах доношенных детей и недоношенных детей (начиная с 33 – 34 недель гестации) требуют снижения порогового уровня данного показателя при проведении неонатального скрининга в Архангельской области с целью предупреждения ложно – негативных результатов.
- В Архангельской области доношенные новорожденные с низкой массой тела при рождении (менее 2000 грамм) имеют достоверно более высокие значения уровня неонатального 17ОНР в сравнении с доношенными детьми с массой тела более 2000 грамм.
- Имеются колебания уровня 17ОНР у новорожденных детей Архангельской области в зависимости от климатических факторов и региона проживания.
- Имеется корреляционная связь между уровнем 17ОНР и неонатальной транзиторной гипертиреотропинемией у новорожденных детей в зимний период.
Научная новизна исследования.
Разработаны региональные показатели пороговых значений уровня 17ОНР для новорожденных детей с учетом гестационного возраста.
Впервые в Архангельской области в результате популяционного исследования изучена зависимость неонатального уровня 17ОНР от климатических факторов и региона рождения, неонатальной транзиторной гипертиреотропинемии.
Впервые определена экономическая эффективность проведения неонатального скрининга на врожденный адреногенитальный синдром в Архангельской области.
Практическая значимость исследования.
Предложены региональные стандарты оценки уровня 17ОНР у новорожденных детей при проведении неонатального скрининга.
Результаты проведенных исследований позволяют разработать оптимальную схему интерпретации клинико-лабораторных данных неонатального скрининга на АГС.
Внедрение результатов исследования позволит снизить затраты на дополнительные обследования детей с ложноположительными результатами скрининга.
Апробация работы.
Материалы диссертации представлены на международной научно – практической конференции, посвященной 35-летию Архангельской областной детской клинической больницы им П.Г. Выжлецова (17 -18 октября 2007 года, г. Архангельск); на VI Всероссийской научно – практической конференции «Задачи детской эндокринологии в реализации национального проекта «Здоровье» (3-4 июня 2008 года, г. Уфа); на итоговой научной сессии СГМУ и СНЦ СЗО РАМН «Повышение качества жизни семьи и развитие здравоохранения Европейского Севера» (17 ноября 2008, года г. Архангельск); на заседании городского общества эндокринологов г. Архангельска (13 января 2009 года).
По теме диссертации опубликовано 7 печатных работ, в том числе 1 в журнале, рекомендованном ВАК для публикации диссертаций. Результаты работы внедрены в клиническую практику ГУЗ «Архангельская областная детская клиническая больница им.П.Г.Выжлецова» (акт внедрения от 24.02.2009), а также в учебный процесс на кафедрах педиатрии ФПК и ППС и педиатрического факультета ГОУ ВПО «Северный государственный медицинский университет (г.Архангельск) Федерального агентства по здравоохранению и социальному развитию» (акт внедрения от 22.01.2009). Работа выполнена в рамках региональной научно-технической программы «Здоровье населения Европейского Севера» (№ государственной регистрации 01200507712).
Структура и объем диссертации.
Диссертация изложена на 126 страницах машинописного текста и состоит из введения, трех глав (обзор литературы, объекты и методы исследования, результаты исследования и их обсуждение), выводов и практических рекомендаций. Работа иллюстрирована 20 таблицами и 19 рисунками. Библиография включает 192 источника (114 - отечественных авторов и 78 - зарубежных).
СОДЕРЖАНИЕ РАБОТЫ
Объект и методы исследования
1. Настоящее исследование проводилось на территории Архангельской области. Основными объектами исследования были новорожденные дети. В основе исследования – анализ результатов неонатального скрининга.
Неонатальный скрининг на 17ОНР осуществляется на территории Архангельской области, включая территорию Ненецкого автономного округа, с 01.08.2006 года. Выборка для изучения уровня 17ОНР была сформирована на популяционной основе, учтены все новорожденные дети в течение календарного года скрининга с августа 2006 по июль 2007 года включительно (14163 человека) в обследуемой популяции, характеризующейся четкими географическими границами - Архангельская область, включая территорию Ненецкого автономного округа.
В последующем вся выборка была ранжирована на группы в зависимости: от наличия у каждого ребенка второго показателя – ТТГ; от уровня ТТГ (более или менее 5 мМЕ/мл); от сезона рождения; от широты региона рождения.
При анализе парных показателей ТТГ и 17ОНР общее количество результатов в выборке уменьшилось с 14163 до 9595, учитывая, что скрининг на врожденный гипотиреоз не был в течение года постоянным и отсутствовал частично с марта по июнь.
Для проведения статистического анализа парных показателей в наиболее контрастные сезоны года (лето: июнь – август; зима: ноябрь – февраль) были отобраны все 906 новорожденных детей родившихся летом, и 3339 новорожденных детей, родившихся зимой. Первая группа значительно меньше второй ввиду того, что отбор результатов 17ОНР производился по обязательному наличию у новорожденного второго показателя ТТГ, а в летние месяцы из-за отсутствия скрининга на ТТГ таких пар было меньше.
Для анализа парных показателей 17ОНР и ТТГ>5 мМЕ/мл во всей популяции новорожденных отобраны все дети, родившиеся летом с повышенным уровнем ТТГ в количестве 60 человек, родившиеся зимой – 272 ребенка.
Для проведения анализа уровня 17ОНР в зависимости от широты региона рождения популяция новорожденных детей в количестве 14163 ребенка была распределена на 3 группы. В первую группу вошли 506 детей, родившихся в Ненецком автономном округе (тундра); во вторую группу – 7058 детей, родившихся в городах Архангельск, Новодвинск, Северодвинск, Онежском, Лешуконском и Мезенском районах (северная тайга); в третью группу были включены 6545 новорожденных детей, родившихся во всех остальных территориях Архангельской области (средняя тайга).
Сбор информации осуществлялся со специальных бланков из фильтровальной бумаги, на которые были нанесены образцы крови и в которых содержались сведения об обследуемом ребенке согласно требованиям нормативных документов. Забор образцов крови был осуществлен на 4 - 7 сутки жизни из пятки новорожденного, фильтровальная бумага с образцом крови высушивалась на открытом воздухе (метод сухого пятна). При сборе информации учитывались гестационный возраст, масса новорожденного, место и сезон рождения, задержка внутриутробного развития по массе тела у доношенных новорожденных детей, результаты гормональных диагностических исследований, сроки верификации диагноза.
2. Количественное определение уровня 17ОНР и ТТГ проводилось в иммуногенетической лаборатории медико-генетической консультации ГУЗ «Архангельская областная детская клиническая больница им. П.Г. Выжлецова». Уровень ТТГ определялся методом иммуноферментного анализа с использованием стандартных наборов «Неонатальный ТТГ», Россия. Уровень 17ОНР определялся флюороиммунометрическим методом с помощью стандартных наборов «Дельфия неонатальный 17 альфа-ОН-прогестерон» Wallac, Финляндия.
3. Клиническое обследование 26 новорожденных детей со значениями выше порогового уровня 17ОНР, выявленными в результате неонатального скрининга, осуществлялось в период госпитализации новорожденных в ГУЗ «Архангельская областная детская клиническая больница им. П.Г. Выжлецова» по разработанным схемам (приложение 1 и 2). Изучены 71 история новорожденных детей контрольной группы сравнения, находившихся на лечении по поводу различных заболеваний перинатального периода в отделениях патологии новорожденных и недоношенных детей (в период с августа 2006 года по декабрь 2007 года). Проанализированы истории болезни и карты амбулаторного пациента (форма 025/у) 16 детей с установленным в доскрининговый период (с 1986 по 2006 годы) диагнозом адреногенитальный синдром.
4. Образцы пятен крови 5 пациентов с адреногенитальным синдромом и членов их семей направлялись для проведения молекулярно-генетического обследования в генетическую лабораторию ФГУ «Эндокринологический научный центр Росмедтехнологий» г. Москва.
5. Статистическая обработка материала. Полученные данные исследований были подвергнуты статистической обработке на IBM Pentium с использованием пакета прикладных программ STATISTICA 6.0 и программ статистического анализа Microsoft Exel, версия 2003 года. Оценка соответствия изучаемого распределения 17ОНР закону нормального распределения проводилась по критерию нормальности Колмогорова-Смирнова.
Для анализа структуры выборки гормонов с неправильным ассиметричным распределением был применен центильный метод. Использовался критерий Манна – Уитни (показатель Т) для сравнения двух независимых выборок; тест Крускела – Уолиса (критерий Н) использовался для сравнения более двух независимых выборок.
В целях изучения взаимосвязи исследуемых признаков проведен анализ корреляции. Поскольку распределение изучаемых признаков не было нормальным, для исследования связи двух количественных признаков применялся метод непараметрического корреляционного анализа по Спирмену (ρ); для исследования связи порядкового и количественного признаков применялся метод непараметрического корреляционного анализа по Кендаллу (τ).
Для сравнения относительных частот признака в двух группах использовался двусторонний критерий статистической значимости различий между двумя пропорциями.
Критический уровень значимости при проверке статистических гипотез принимался равным 0,05.
Результаты собственных исследования и их обсуждение
В Архангельской области в периоде новорожденности диагноз классической формы адреногенитального синдрома был установлен у 5 детей за 26 месяцев скрининга. Частота встречаемости АГС в нашем регионе за данный период составила 1: 5 934. Распространенность данной формы составила 7,2 случая на 100 000 детского населения.
До начала скрининга на АГС с 1986 года в ГУЗ АОДКБ данный диагноз был установлен клинически по обращаемости у 16 детей, из них мальчики составили 7 человек (43,7 %), девочки 9 человек (56,3 %). Структура по форме заболевания была представлена следующим образом: вирильная форма - 8 детей (50%), сольтеряющая форма – 8 детей (50%). До начала проведения скрининга медиана возраста постановки диагноза в группе девочек с сольтеряющей формой заболевания составила 14 дней (от 1 до 82 дней), в группе мальчиков с сольтеряющей формой – 30 дней (от 13 до 99 дней). Медиана возраста постановки диагноза в группе девочек с вирильной формой заболевания составила 10,2 месяца (от 18 дней до 9 лет), в группе мальчиков с вирильной формой – 4 года (от 1 месяца до 6 лет). Всего за 20 лет до начала скрининга было рождено 331 712 детей, частота АГС составила в среднем 1: 20 732.
С началом проведения скрининга структура АГС изменилась следующим образом: простая вирильная форма выявлена у 2 детей (40%), сольтеряющая форма – у 3 новорожденных (60%). При распределении детей по полу в период до скрининга соотношение мальчики: девочки составляло 1: 1,3; по результатам скрининга соответственно – 4: 1.
Всем детям в Архангельской области с установленным при проведении скрининга диагнозом АГС было проведено молекулярно-генетическое исследование для выявления мутаций в гене CYP 21. Выявлены следующие изменения: у детей с сольтеряющей формой в гомозиготном состоянии del 8 пар нуклеотидов в 3 экзоне (2 ребенка) и I2Spl (1 ребенок); у одного ребенка с вирильной формой компаунд P30L/30kbdel. Тяжесть клинических проявлений соответствовала установленным мутациям, характер которых определял различную степень снижения активности 21-гидроксилазы. У второго ребенка с вирильной формой не выявлена ни одна из 16 определяемых мутаций.
При проведении центильного анализа данных 17ОНР установлено, что у новорожденных детей в Архангельской области 50% значений располагаются в интервале от 4,5 до 9,5 нмоль/л, медиана составила 6,58 нмоль/л, а значение 99 перцентиля во всей популяции не превышает установленной лабораторной нормы. Исследования данных 17ОНР в популяции новорожденных Тюменской области показали, что 50 % значений располагаются в интервале от 6,21 до 13,9 нмоль/л, в популяции доношенных новорожденных Краснодарском крае – от 5,7 до 19,7 нмоль/л. В нашем исследовании значения 17ОНР имеют более низкие уровни по сравнению с данными выше указанных исследований.
Нами были определены центильные значения 17ОНР во всей популяции (n=14163) в зависимости от срока гестации у новорожденных детей Архангельской области, результаты представлены в таблице 1.
Таблица 1
Центильные значения 17ОНР (нмоль/л) в зависимости от срока гестации у новорожденных детей Архангельской области
| Срок гестации (неделя) | Число детей | 17ОНР нмоль\л | ||||
| Р 10 | Р 25 | Р 50 | Р 75 | Р 99 | ||
| 25-28 | 49 | 8,24 | 17,13 | 26,76 | 45,81 | 312,39 |
| 29-30 | 32 | 7,62 | 9,01 | 18,65 | 31,44 | 189,47 |
| 31-32 | 97 | 6,43 | 9,25 | 13,52 | 25,33 | 73,72 |
| 33 | 77 | 5,13 | 7,58 | 12,47 | 22,32 | 86,81 |
| 34 | 114 | 4,86 | 7,56 | 10,76 | 14,95 | 50,17 |
| 35 | 210 | 4,52 | 6,74 | 10,77 | 16,46 | 50,30 |
| 36 | 264 | 4,17 | 5,87 | 9,095 | 12,67 | 35,48 |
| 37 и более | 13 320 | 2,98 | 4,42 | 6,44 | 9,15 | 25,0 |
Медиана и 99 перцентиль 17ОНР в европейской популяции для доношенных новорожденных имеют значения соответственно 12,0 нмоль/л и 30,3 нмоль/л. В Архангельской области они составили соответственно 6,44 нмоль/л и 25,0 нмоль/л.
Медиана 17ОНР в различные гестационные сроки у недоношенных детей Архангельской области в 1,5 – 2 раза ниже соответствующих величин у детей европейской популяции. Выше перечисленные данные могут указывать на особенности функционирования коры надпочечников в раннем неонатальном периоде у детей высокоширотного региона. Данное положение не противоречит результатам морфологических исследований С.Г.Суханова (1993), в ходе которых установлено, что в надпочечниках плодов и новорожденных «северян» замедлены темпы замещения провизорной (фетальной) коры окончательной (дефинитивной). Полученные нами при популяционном исследовании данные уровня 17ОНР, по сути, совпадают с результатами А.В. Ткачева (1987-2004), С.Г. Суханова (1986-1993), З.Д. Губкиной (1989 - 2007) и др., полученными у взрослых, о том, что у человека в условиях Севера функциональные резервы эндокринной системы снижены.
Вместе с тем более низкие уровни 17ОНР у новорожденных детей Архангельской области на различных сроках гестации могут свидетельствовать о более раннем, опережающем формировании зрелых функций адреналовой системы у жителей Севера. Это также подтверждается данными морфогистологических исследований С.Г. Суханова (1993), показавшими, что для новорожденных Архангельской области характерно раннее формирование, но тонкого слоя дефинитивной коры надпочечников.
Низкие показатели верхнего предела нормативных значений (99 перцентиль) 17ОНР в группах доношенных детей (25 нмоль/л) и недоношенных детей 33 – 34 недель гестации (50 нмоль/л) требуют снижения Cut –off при проведении неонатального скрининга в Архангельской области с целью предупреждения ложно – негативных результатов.
При применении стандартных наборов «Дельфия неонатальный 17 альфа-ОН-прогестерон» (Wallac, Финляндия) производитель рекомендует принимать во внимание модификации тест-систем, которые приводят к изменению получаемых результатов и определению новых пороговых уровней. Учитывая более низкие региональные показатели пороговых значений 17ОНР, для расчета порогового уровня 17ОНР мы ввели поправку на основе вычисления абсолютной и относительной погрешности для различных модификаций стандартного набора, которая составила (- 16%) от рекомендуемого в наборе порогового уровня для исключения ложно-негативных результатов.
Для изучения влияния веса новорожденного на уровень 17ОНР нами было проведено сравнение показателей неонатального уровня 17ОНР в группах доношенных (более 36 недель) детей с различной массой тела при рождении. В 1-ю группу были включены 43 доношенных новорожденных ребенка с массой тела менее 2000 г, во вторую - 1299 доношенных новорожденных детей с массой тела более 2000 г. Средняя масса тела при рождении в группах значимо отличалась и составила 1825,3 + 32,7г и 3391,1 + 12,7г в двух группах соответственно (р=0,00001). Медиана, интерквартильный размах и верхний предел нормативных значений (99 перцентиль) 17ОНР у доношенных детей с различной массой тела при рождении представлены в таблице 2 и на рисунке 1.
Таблица 2
Центильные значения 17ОНР (нмоль/л) у доношенных детей с различной массой тела при рождении
| 17ОНР (нмоль/л) | n | Среднее значение | Медиана | SD | Центиль | ||
| 25 | 75 | 99 | |||||
| Масса <2000г | 43 | 10,30 | 9,11 | 6,18 | 5,7 | 13,83 | 34,71 |
| Масса >2000г | 1299 | 5,93 | 5,19 | 3,7 | 3,5 | 7,47 | 19,46 |
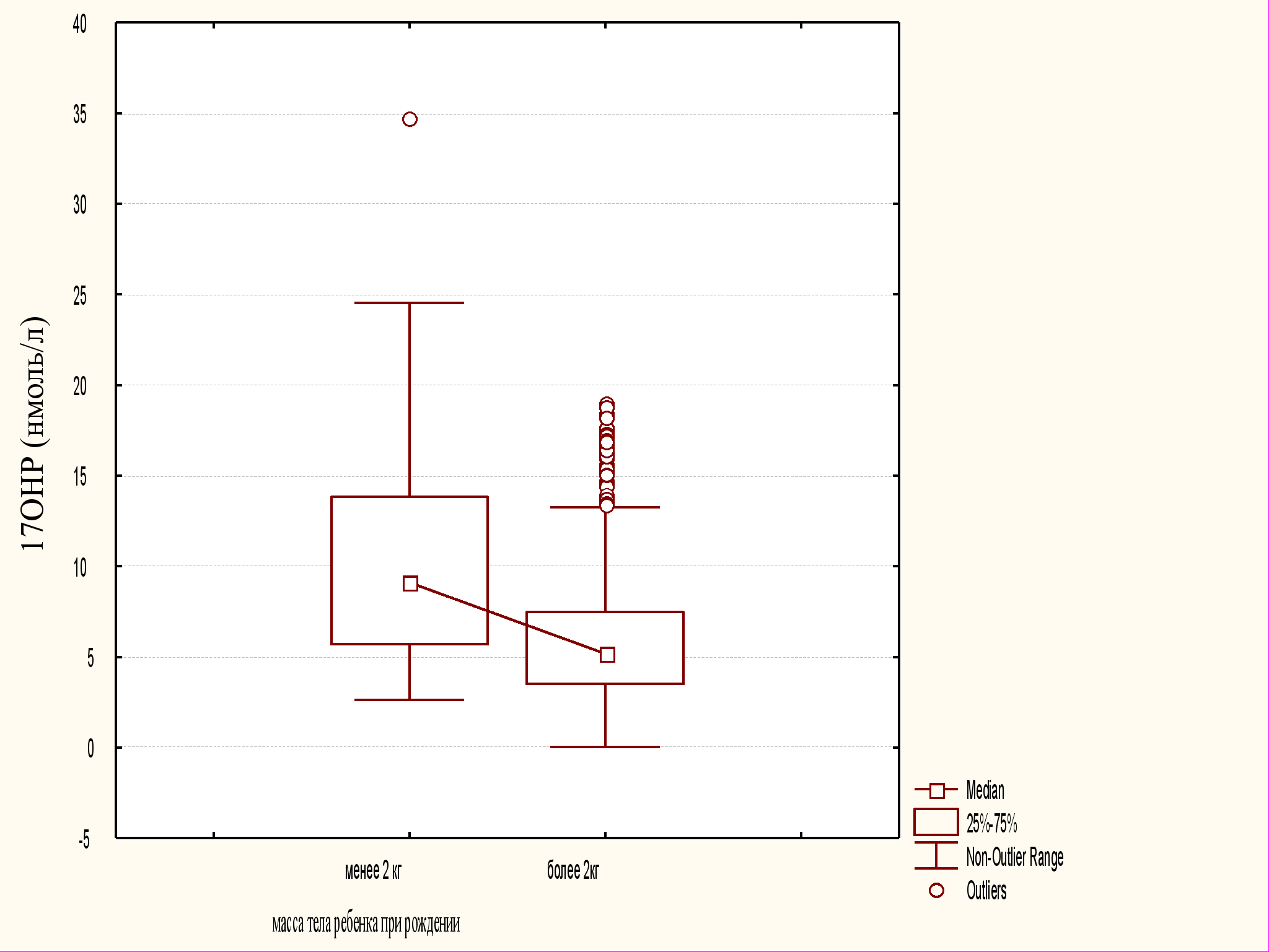
р=0,000057
Рис. 1 Медиана и интерквартильный размах 17ОНР у доношенных детей с различной массой тела при рождении
Таким образом, в Архангельской области доношенные новорожденные с низкой массой тела при рождении (менее 2 000 грамм) имеют достоверно (р=0,000057) более высокие значения уровня неонатального 17ОНР.
Архангельская область географически расположена в высоких широтах, где наиболее контрастными сезонами по длительности светового дня являются лето (июнь – август) и зима (ноябрь – февраль).
С целью изучения влияния фотопериодизма на гипофизарно– тиреоидно – адреналовую систему новорожденных детей нами был проведен анализ изменений уровня 17ОНР и ТТГ более 5 мМЕ/мл в зависимости от продолжительности светового дня и сезона года. Зависимость уровня 17ОНР при ТТГ > 5 мМЕ/мл от сезона года представлена на рисунке 2.
В группе детей, родившихся зимой и имевших уровень ТТГ более 5 мМЕ/мл, медиана 17ОНР составила 7,15 нмоль/л; интерквартильный размах 17ОНР 5,42 – 10,41 нмоль/л. В группе новорожденных, родившихся летом и имевших уровень ТТГ более 5 мМЕ/мл, медиана 17ОНР составила 4,06 нмоль/л; интерквартильный размах 17ОНР 2,66 – 6,05 нмоль/л. Различия двух данных независимых групп были достоверны (р <0,0001); в зимние месяцы уровни 17ОНР при имевшейся гипертиреотропинемии были увеличены в 1,5-2 раза в сравнении с летними месяцами. Можно предполагать с определенной долей вероятности, что в летний период усиливается процесс превращения 17ОНР в кортизол. Для окончательного ответа на данный вопрос необходимы дальнейшие исследования с одновременным определением кортизола.
р < 0,0001
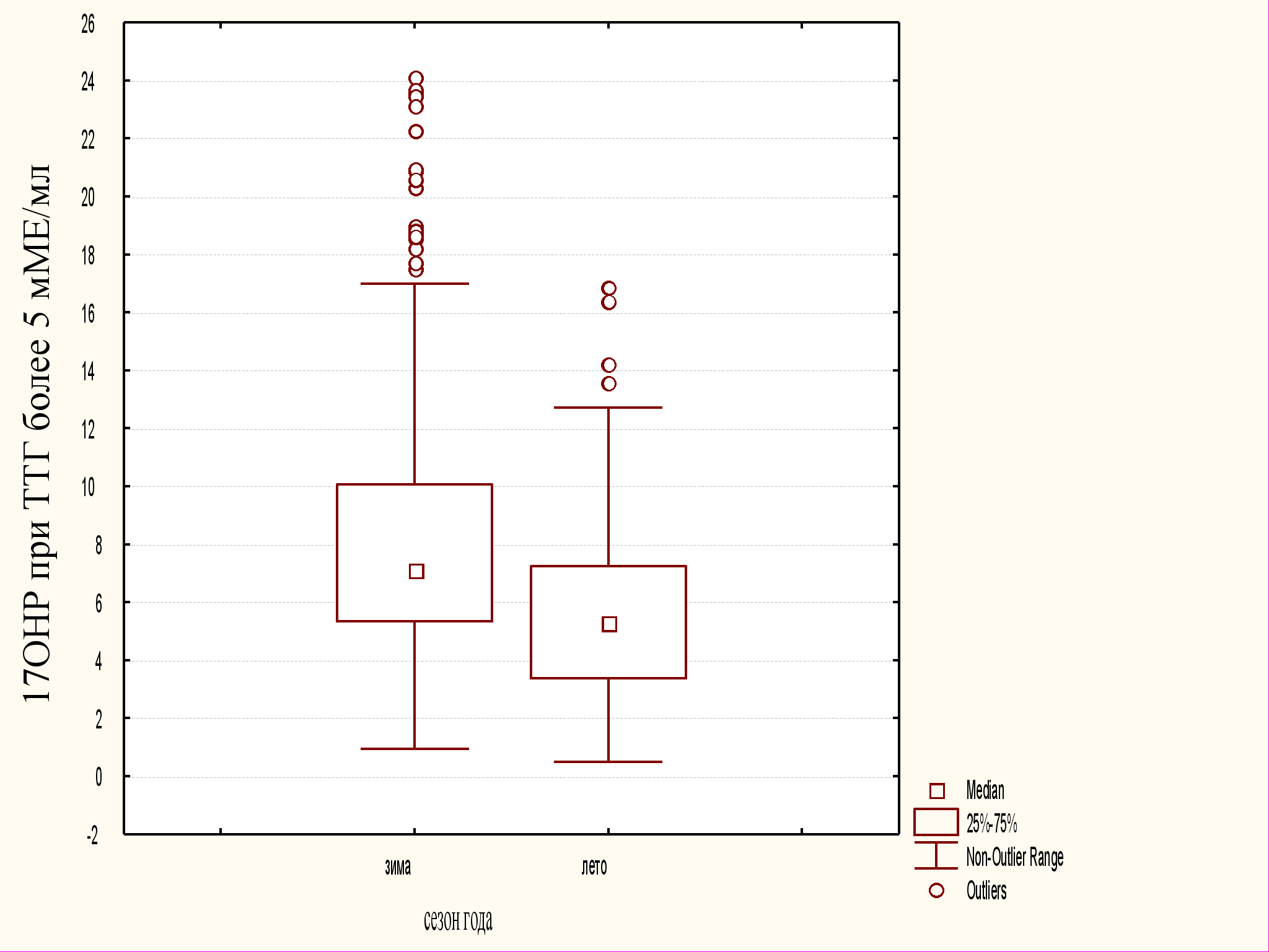
Рис. 2 Зависимость уровня 17ОНР при ТТГ > 5 мМЕ/мл от сезона года
Такая же закономерность установлена при изучении зависимости уровня ТТГ более 5 мМЕ/мл от сезона года. Медиана в группе «лето» составила 6,44 мМЕ/мл, 50% значений находились в интервале 5,61 – 8,96 мМЕ/мл. Медиана в группе «зима» составила 7,19 мМЕ/мл, 50% значений находились в интервале 5,92 – 9,92 мМЕ/мл. При сравнении двух данных независимых групп установлено, что показатели первой группы значимо ниже (р = 0,003).
При проведении корреляционного анализа показателей 17 ОНР и ТТГ в указанные периоды выявлена слабая положительная парная корреляция показателей 17ОНР и показателей ТТГ > 5 мМЕ/мл в зимний период (r = 0,15). Коэффициент корреляции для двух данных показателей был статистически значимым - р = 0,0108. Достоверной корреляции показателей 17ОНР и показателей ТТГ > 5 мМЕ/мл в летний период не выявлено (r= - 0,02; р = 0,86).
Сопоставление трех климатогеографических зон высокоширотного региона по одному количественному признаку – уровню 17ОНР осуществлено непараметрическим методом рангового анализа вариаций по Краскелу – Уоллису. Медианы и квартили уровня 17ОНР в указанных генеральных совокупностях достоверно значимо отличались (р=0,00006). Медиана и интерквартильный размах 17ОНР у новорожденных детей в различных климатогеографических зонах представлена на рисунке 3.
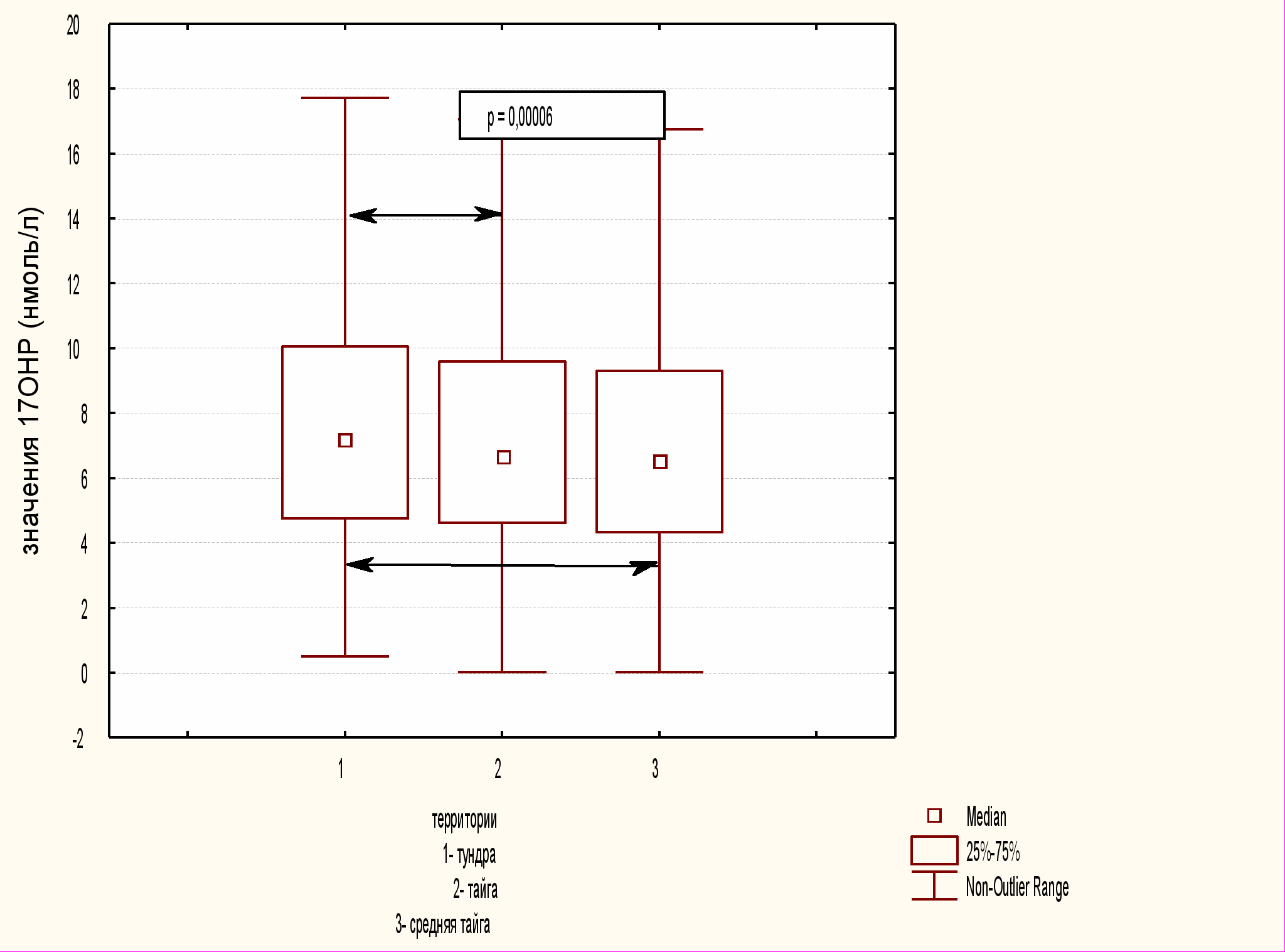
р = 0,039
р = 0,0008
Рис. 3 Медиана и интерквартильный размах 17ОНР у новорожденных детей в различных климатогеографических зонах
Выявлена слабая отрицательная корреляция показателей 17ОНР и климатогеографической зоны, где родился ребенок (r = - 0,028). Коэффициент корреляции для двух данных показателей оказался статистически значимым – р < 0,00001.
Гормональное влияние на реализацию компенсаторных приспособительных реакций новорожденных к изменяющимся условиям внешней и внутренней систем организма многогранно и касается почти всех жизнеобеспечивающих систем организма, причем ключевую роль занимают глюкокортикоиды и тиреоидные гормоны. За период времени с 01.08.2006 года по 31.12.2007 года нами среди 20 542 результатов неонатального 17ОНР, ретесты с уровнями 17 – ОНР выше пороговых значений составили 112 случаев (0,54%). Медиана 17ОНР при рождении в основной группе составила 39,21 нмоль/л, размах колебаний 17ОНР варьировал от 31,01 до 2184,14 нмоль/л. С целью проведения анализа причин ложно-положительных результатов неонатального 17ОНР нами были изучены особенности течения перинатального периода среди 26 новорожденных детей (соотношение мальчики: девочки составило 1:1; доношенные: недоношенные - 1:1,3), госпитализированных для обследования, из 112 детей с транзиторным повышением уровнем 17ОНР в период новорожденности.
Контрольную группу составили 71 ребенок сопоставимого возраста, пола и степени недоношенности с показателями неонатального 17ОНР ниже порогового уровня. При формировании сравниваемых групп была учтена степень недоношенности детей, таким образом, показатель низкой массы был исключен как фактор, влияющий на показатель 17ОНР. Дети с ложноположительными результатами 17ОНР не отличались значимо по показателям физического развития при рождении. Масса тела детей в основной группе составила 2405,2 + 1045,9г, в группе сравнения она была 2794,9 + 825г (р= 0,058).
Частота встречаемости (%) патологических состояний неонатального периода при транзиторном повышении 17ОНР представлена на рис. 4.
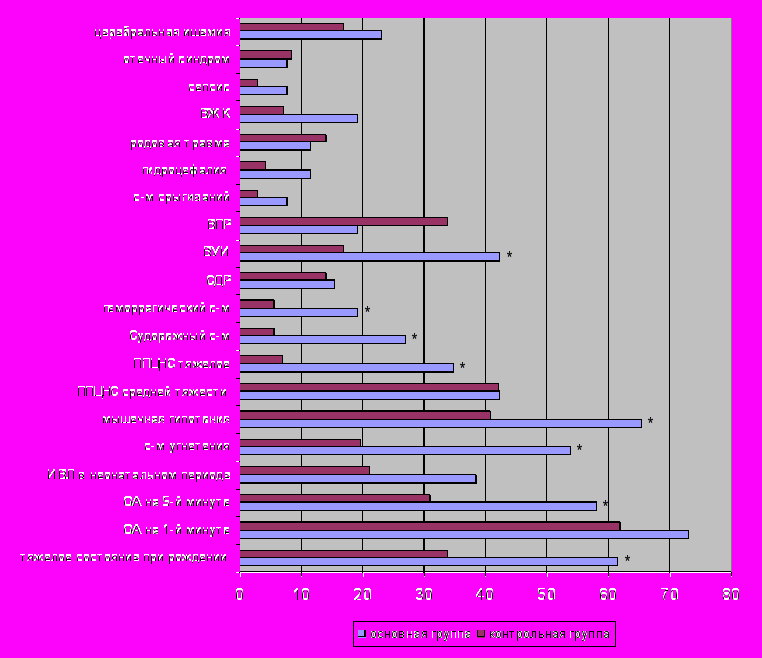
Рис. 4 Частота встречаемости (%) патологических состояний неонатального периода при транзиторном повышении 17ОНР (* р< 0,05)
При транзиторном повышении 17ОНР в ходе скрининга достоверно чаще регистрировались у детей в неонатальном периоде тяжелое состояние при рождении (р=0,015) с низкой оценкой по шкале Апгар на 5 – й минуте жизни (р=0,016); перинатальное поражение ЦНС тяжелой степени (р=0,009) с синдромом угнетения (р=0,001) и мышечной гипотонией (р=0,034); судорожный (р=0,004) и геморрагический(р=0,043) синдромы; внутриутробная инфекция (р=0,01).
Проведенное исследование позволило установить клинико-лабораторные особенности результатов неонатального скрининга на адреногенитальный синдром в Архангельской области, выявить региональные закономерности колебаний уровня 17ОНР у новорожденных детей. Полученные данные являются методологической основой для обоснования рекомендаций по клинико-лабораторной интерпретации результатов скрининга.
Выводы
- В Архангельской области распространенность классических форм адреногенитального синдрома составила 7,2 случая на 100 000 детского населения. Частота адреногенитального синдрома у новорожденных составила 1: 5 934.
- У новорожденных детей Архангельской области в раннем неонатальном периоде, родившихся при сроке гестации 33-40 недель, установлены более низкие, чем у детей европейской популяции, медиана и верхний предел нормативных значений 17ОНР.
- С целью предупреждения ложно – негативных результатов при проведении неонатального скрининга в Архангельской области необходимо снизить пороговый уровень 17ОНР у новорожденных детей, начиная с 33 по 40 неделю гестации.
- В Архангельской области доношенные новорожденные с низкой массой тела при рождении (менее 2 000 грамм) имеют более высокие значения уровня неонатального 17ОНР.
- Установлены сезонные различия уровней 17ОНР у новорожденных детей Архангельской области, характеризующиеся более высокими значениями зимой, что свидетельствует о напряженном функционировании гипофизарно – адреналовой системы в период наименьшего светового дня. Установлена корреляционная связь между уровнем 17ОНР и внутригодовыми колебаниями содержания ТТГ в этой же группе детей.
- Уровни 17ОНР у новорожденных детей Архангельской возрастают с увеличением широты региона рождения.
- При проведении массового скрининг – обследования новорожденных детей на каждый затраченный 1 рубль бюджета области было сэкономлено 7,8 рублей. Общая экономическая эффективность в Архангельской области за исследуемый период, учитывая значительную территориальную протяженность и низкую плотность населения в регионе, составила 25 613 741,96 рублей.
Практические рекомендации
1. Врачам – лаборантам иммуногенетической лаборатории, врачам – генетикам, детским эндокринологам ГУЗ АОДКБ при проведении неонатального скрининга с помощью стандартных наборов «Дельфия неонатальный 17 альфа-ОН-прогестерон» (Wallac, Финляндия с рекомендуемыми пороговыми значениями 17гидроксирогестерона 30 нмоль/л для доношенных детей и 60 нмоль/л – для недоношенных детей) снижать пороговый уровень для новорожденных Архангельской области до 25 и 50 нмоль/л соответственно с целью предупреждения ложно-негативных результатов.
2. Врачам – лаборантам иммуногенетической лаборатории медико-генетической консультации, врачам – генетикам при применении других модификаций стандартного набора «Дельфия неонатальный 17 альфа-ОН-прогестерон» (Wallac, Финляндия), требующих снижения порогового уровня, рассчитывать его с учетом поправки, которая должна составлять (- 16%) от рекомендуемого в наборе порогового уровня для предупреждения ложно-негативных результатов.
3. Педиатрам, неонатологам, детским эндокринологам проводить обследование новорожденного ребенка с повышенным уровнем 17ОНР в отделениях патологии новорожденных ГУЗ АОДКБ в соответствии с разработанными протоколами обследования.
4. Педиатрам, неонатологам, детским эндокринологам при клинической интерпретации результатов неонатального скрининга на АГС необходимо учитывать массу тела доношенного ребенка менее 2000г, наличие патологических состояний неонатального периода.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ
ПО ТЕМЕ ДИССЕРТАЦИИ
- Периоперационное ведение пациентов с адреногенитальным синдромом / Е.Н. Сибилева, Н.Д. Ширяев, О.Е. Ипатова // III Всероссийская научно-практическая конференция «Достижения науки в практику детского эндокринолога»: Тезисы докладов. – Москва, 2005. - С 168.
- Результаты неонатального скрининга на адреногенитальный синдром в Архангельской области (первый опыт) / О.Е. Ипатова, Е.Н. Сибилева // Материалы межрегиональной научно-практической конференции. – Архангельск, 2007. – С.65-69.
- Итоги проведения неонатального скрининга на наследственные заболевания в Архангельской области в рамках реализации национального проекта «Здоровье» / Е.Г. Петрова, О.Е. Ипатова // Информационное письмо для педиатров, неонатологов, руководителей учреждений здравоохранения. - Архангельск, 2007. - 6 с.
- Реализация национального проекта «Здоровье» в части неонатального скрининга в Архангельской области (итоги первого года) / Е.Г. Петрова, О.Е. Ипатова, А.А. Турабова, А.В. Быкова, Т.В. Пятлина, Е.Ю. Халмрадова, Т.А. Шкулева, Т.Б. Ревякина // Материалы ежрегиональной научно-практической конференции. – Архангельск, 2007. – С.104-108.
- Частота и структура адреногенитального синдрома в Архангельской области в период скрининга и до него / О.Е. Ипатова // VI Всероссийская научно-практическая конференция «Задачи детской эндокринологии в реализации национального проекта «Здоровье»: Тезисы докладов. – Уфа, 2008. - С 51-52.
- Клинические аспекты неонатального скрининга на наследственные заболевания в Архангельской области Е.Г. Петрова, О.Е. Ипатова // Информационное письмо для педиатров, неонатологов, руководителей учреждений здравоохранения. - Архангельск, 2008. - 6 с.
- Частота и структура адреногенитального синдрома в Архангельской области / О.Е. Ипатова, Е.Н. Сибилева // Экология человека. - Архангельск, 2008. - № 5, - С.28-30.
