Контрольные вопросы к занятию по теме: Кислотно-основные свойства органических соединений
| Вид материала | Контрольные вопросы |
СодержаниеЭкспериментальная часть Экспериментальная часть Задачи для самостоятельного решения. |
- Программа элективного курса по химии «строение и свойства кислородсодержащих органических, 667.3kb.
- Календарно-тематический план лекций по биоорганической химии 1 курс (2 семестр) специальность, 65.41kb.
- Kirgizistan-tüRKİye manas üNİversitesi ders biLGİ formu, 147.19kb.
- Тематический план лекций модуля 1 с органической химии для студентов 2 курса фармацевтического, 25.24kb.
- Тест по теме: «Строение и классификация органических соединений» Задания уровня, 1355.16kb.
- Лекция Классификация и изомерия органических соединений, 296.86kb.
- Курсовая работа по теме: «Биотрансформация органических соединений, как одно из направлений, 393.69kb.
- Тематический план лекций и самостоятельной работы по органической химии (осенний семестр), 91.46kb.
- 10 класс. Тема урока: «Причины многообразия органических соединений» Тип урока, 145.21kb.
- Методические указания по изучению курса «Страховое право», 149.11kb.
Контрольные вопросы к занятию по теме:
Кислотно-основные свойства органических соединений
- Основные положения теории Бренстеда-Лоури.
- Типы органических кислот (ОН, ЅН, NH, СН-кислоты).
- Типы органических оснований (π-основания, р-основания).
- Сила кислот и оснований Бренстеда. Шкала кислотности рКа и рКв.
- Факторы, определяющие кислотность и основность: электроотрицательность, поляризуемость кислотного (основного) центра, стабилизация аниона за счет сопряжения, влияние электронных эффектов, связанных с кислотным (основным) центром, эффект сольватации.
- Теория Льюиса.
Экспериментальная часть
Опыт 1. Получение этилата натрия и его гидролиз.
В сухую пробирку поместите 1мл абсолютного этанола и внесите размером с рисовое зерно кусочек металлического натрия, предварительно очищенного от керосина с помощью фильтровальной бумаги. Соберите выделяющийся водород, прикрыв пробирку пробкой. Затем уберите пробку и поднесите пробирку отверстием к пламени горелки. Смесь водорода с воздухом сгорает с характерным «лающим» звуком.
Белый осадок этилата натрия растворите в 2 – 4 каплях этанола и добавьте 1 каплю спиртового раствора фенолфталеина. Отметьте цвет раствора. После этого внесите в пробирку 2 – 3 капли воды. Объясните появление окраски.
Напишите уравнения реакции получения этилата натрия и уравнение его гидролиза.
Опыт 2. Обнаружение кислотных свойств многоатомных спиртов.
Получение глицерата меди (ΙΙ).
В пробирку внесите 2 капли 2%-ного раствора сульфата меди (ΙΙ) CuSO4 и добавьте 2 капли 10%-ного раствора гидроксида натрия NaOH. Образуется голубой хлопьевидный осадок гидроксида меди (ΙΙ) Cu(ОН)2. Добавьте к нему 1 каплю глицерина и встряхните пробирку. В результате образуется глицерат меди, раствор которого имеет синий цвет.
Напишите уравнения реакции глицерина с гидроксидом меди (ΙΙ) с образованием хелатного комплекса глицерата меди.
Опыт 3. Обнаружение кислотных свойств фенолов. Образование феноксида
натрия и разложение его кислотой.
В пробирку поместите 3 капли «жидкого» фенола, 3 капли воды и встряхните. К возникшей мутной эмульсии добавьте по каплям 10 %-ный раствор гидроксида натрия до образования прозрачного раствора. При подкислении этого раствора несколькими каплями 10%-ной НСl наблюдается помутнение.
Напишите уравнения протекающих реакций.
Опыт 4. Обнаружение основных свойств алифатических и ароматических
аминов.
В две пробирки внесите по 2 капли воды.
а) В первую пробирку поместите 1 каплю анилина С6Н5NH2, а во вторую пробирку – 1 каплю диэтиламина (С2Н5)2NH и встряхните. Сравните растворимость этих аминов в воде. С помощью универсальной индикаторной бумаги определите приблизительное значение рН растворов в обеих пробирках.
б) К эмульсии анилина в первой пробирке добавьте 1 каплю 10%-ной НСl. Содержимое пробирки становится прозрачным. Во вторую пробирку к раствору диэтиламина прибавьте 3 капли насыщенного раствора пикриновой кислоты, перемешайте и поместите пробирку в стакан с холодной водой. Через некоторое время выпадает осадок пикрата диэтиламина.
Напишите уравнения протекающих реакций.
Контрольные вопросы к занятию по теме:
Алифатические углеводороды (алканы, алкены).
1. Алканы. Номенклатура, изомерия. Способы получения.
2. Электронное строение и физические свойства алканов.
3. Химические свойства алканов. Реакции радикального замещения,
механизм. Реакции окисления.
4. Циклоалканы; классификация, изомерия. Особенности электронного
строения.
5. Особенности химических свойств малых циклов (реакции присоединения).
Реакции замещения. Циклогексан, его свойства.
6. Алкены. Номенклатура, изомерия. Способы получения.
7. Особенности химического строения алкенов: sp²-гибридизация, σ- и π-
связи. Физические свойства алкенов.
8. Химические свойства алкенов. Правило Марковникова.
Экспериментальная часть
Опыт 1. Получение и свойства метана.
В пробирку, снабженную пробкой с газоотводной трубкой, поместите смесь равных частей обезвоженного ацетата натрия и натронной извести на высоту около 10 мм. Держа пробирку в горизонтальном положении, нагрейте ее в пламени горелки (рис.1). Выделяющийся при нагревании метан подожгите. Обратите внимание на то, что метан горит несветящимся
пламенем (иногда пламя окрашивается в желтый цвет за счет натрия, содержащегося в стекле.
Убедившись, что метан горит, тут же опустите конец газоотводной трубки в пробирку с заранее приготовленным раствором перманганата калия (1капля 0,1н КМnО4 и 5 капель воды), а затем в пробирку с бромной водой. Что наблюдаете и почему?
 Рис.1
Рис.1При нагревании ацетата натрия с натронной известью (смесь NaOH и Ca(OH)2) выделяется метан согласно уравнению
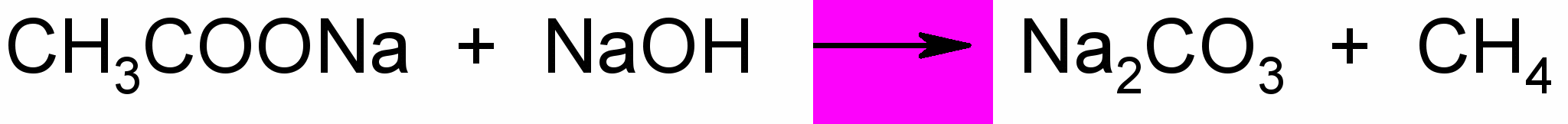
Образующийся углекислый натрий можно обнаружить, добавив в остывшую пробирку 2-3капли 2н НСl. Выделяются пузырьки СО2. Если быстро соединить пробирку с газоотводной трубкой и опустить ее конец в заранее приготовленную пробирку с несколькими каплями насыщенного раствора Ва(ОН)2, то можно наблюдать помутнение баритовой воды вследствии выделения белого осадка ВаСО3. Напишите уравнения протекающих реакций.
Опыт 2. Свойства алканов
На предметное стекло нанесите на некотором расстоянии друг от друга по 1капле раствора перманганата калия, бромной воды, и концентрированной серной кислоты. Смешайте каждую из капель с каплей вазелинового масла (смесь углеводородов). Что наблюдаете ? Сделайте вывод о реакционной способности алканов.
Опыт 3. Открытие углерода и водорода
Присутствие углерода и водорода в органических соединениях в большинстве случаев можно обнаружить по обугливанию вещества при осторожном прокаливании на открытом пламени.
Наиболее точным методом открытия углерода и водорода является сожжение органического вещества в смеси с мелким порошком оксида меди. Исследуемое вещество прокаливают в смеси с СuO. Углерод, сгорая за счет кислорода, дает угольный ангидрид СО2, а водород образует воду. Оксид мели при этом частично восстанавливается до металлической меди:

Для открытия СО2 используют реакцию с баритовой или известковой водой, вызывающей помутнение растворов последних при пропускании через них углекислого газа:
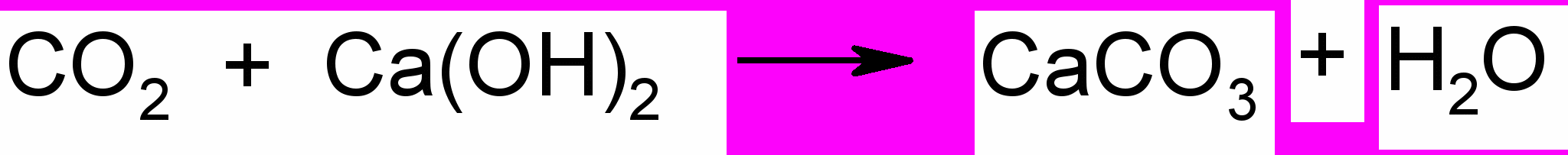
Для открытия воды используют безводный медный купорос. Белый порошок безводного СuSO4 синеет при попадании на него воды, что связано с образованием голубого кристаллогидрата:

Для проведения опыта в пробирку насыпьте черного порошка оксида меди на высоту около 10 мм, добавьте 0,5г исследуемого вещества и тщательно перемешайте. В верхнюю часть пробирки поместите небольшой комок ваты, на который тонким слоем насыпьте обезвоженный порошок СuSO4 . Закройте пробирку пробкой с газоотводной трубкой, при этом конец трубки должен упираться в вату. Нижний конец трубки опустите в другую пробирку, содержащую 0,5 мл баритовой или известковой воды. Нагрейте пробирку с исследуемым веществом на пламени горелки. Через несколько секунд из газоотводной трубки начнет выделяться пузырьки газа. Как только баритовая или известковая вода помутнеет, эту пробирку следует удалить. Продолжайте нагревать пробирку, пока пары воды не достигнут белого порошка обезвоженного СuSO4, находящегося на ватном тампоне, и не вызовут его посинения, вследствии образования кристаллогидрата.
Опыт 4. Получение и свойства этилена.
В пробирку 1 поместите 10 капель концентрированной серной кислоты,
6 – 8 капель этанола и несколько кристалликов оксида алюминия. Закройте пробирку 1 пробкой с газоотводной трубкой и закрепите пробирку в лапке штатива (рис.2).
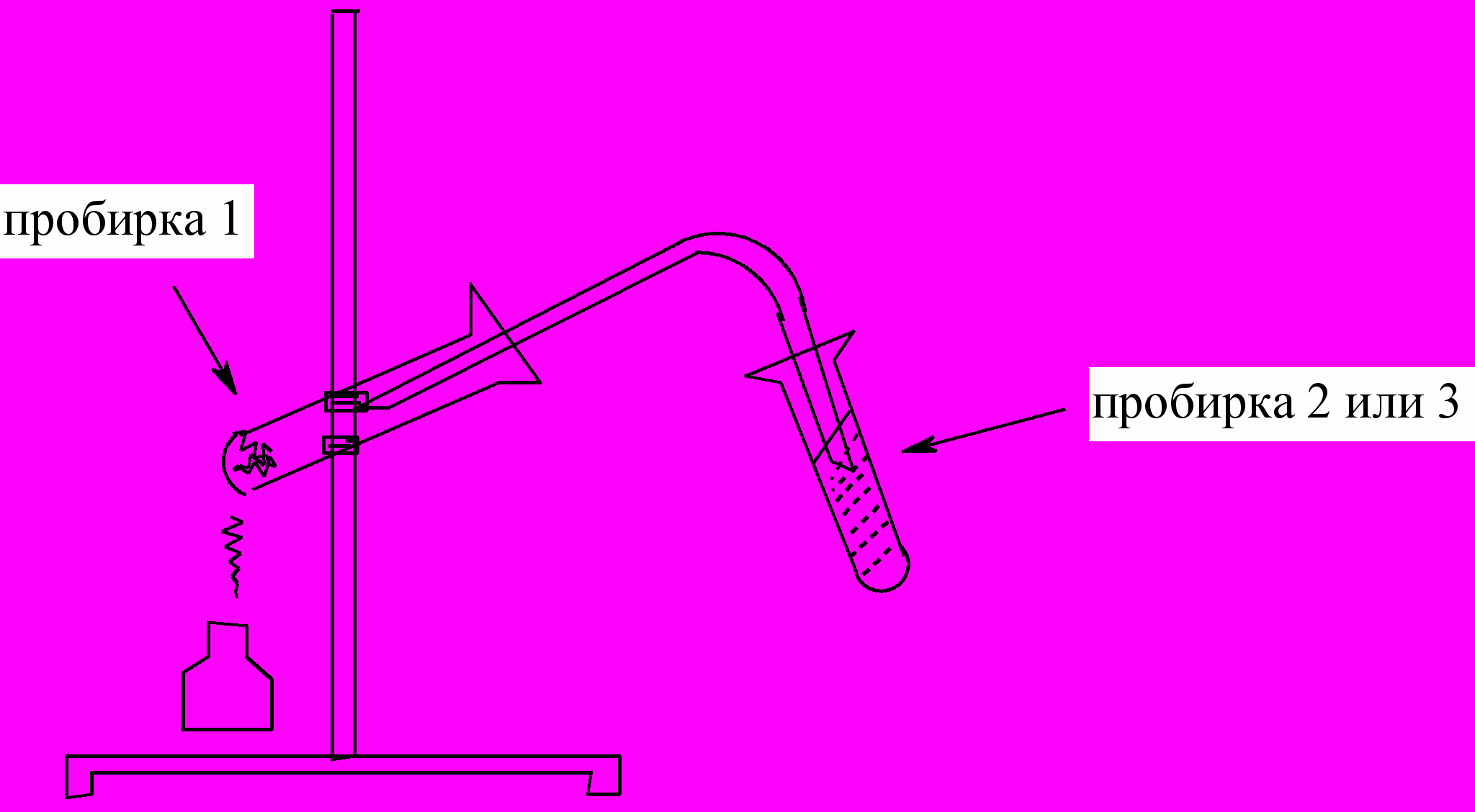
Рис.2
Нагревайте пробирку 1 сначала медленно, а затем усильте нагревание. Подожгите выделяющийся газ у конца газоотводной трубки и отметьте свечение пламени. Временно отставьте горелку и прекратите нагревание.
Доказательства наличия двойной связи в молекуле органического соединения:
● бромирование – в пробирку 2 поместите 6 капель бромной воды. Опустите в нее газоотводную трубку так, чтобы конец трубки был погружен в бромную воду. Осторожно нагрейте реакционную смесь в пробирке 1. Как только бромная вода обесцветится, уберите пробирку 2.
● окисление – в пробирку 3 поместите 1 каплю 2%-го раствора КМnО4 и 5 капель воды, опустите в нее конец газоотводной трубки. Нагрейте пробирку 1. Отметьте изменение окраски раствора в пробирке 3.
Напишите уравнения реакции получения этилена из этанола, а также реакции бромирования и мягкого окисления этилена.
Задачи для самостоятельного решения.
- Напишите структурные формулы одновалентных радикалов
а) состава – С3Н7, - С4Н9 ; б) соответствующих метилбутану; Назовите все радикалы.
2. Напишите структурные формулы следующих углеводородов:
а) метилизобутилизопропилметан; б) диметил-втор.бутилметан;
в) 3 – этилгептан; г) 5-(2-метилбутил)-4-этилдекан.
3. Назовите по систематической и рациональной номенклатуре следующие углеводороды:
а)
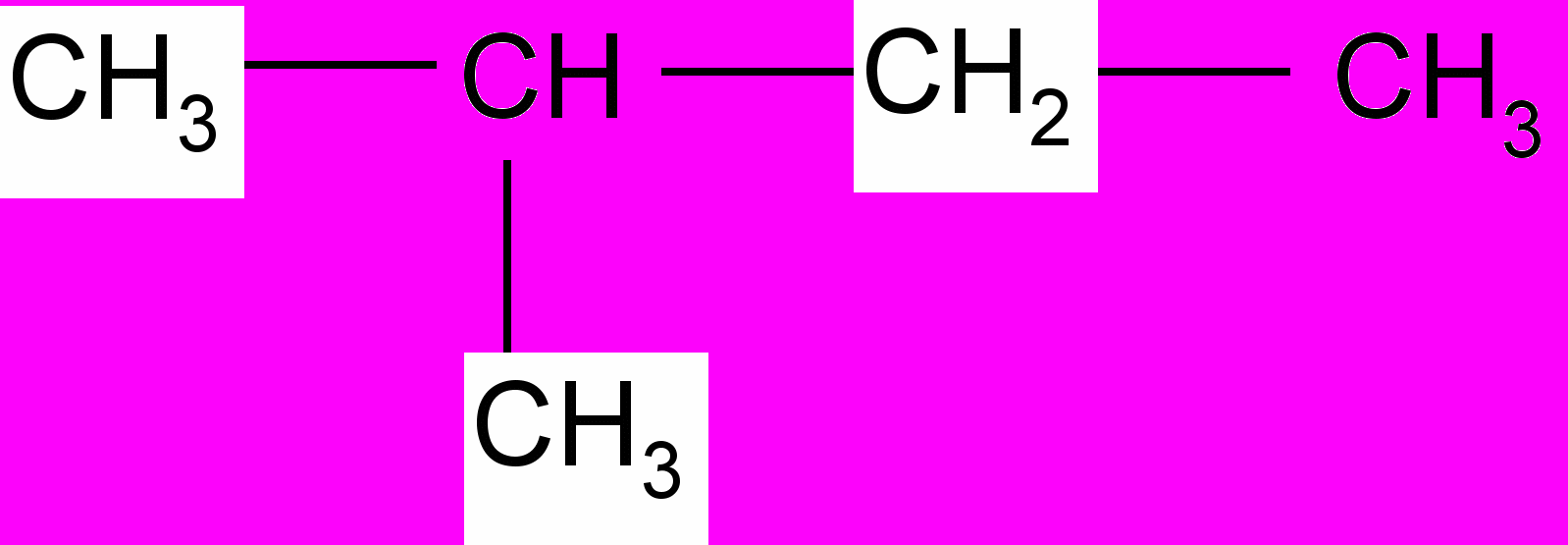
б)
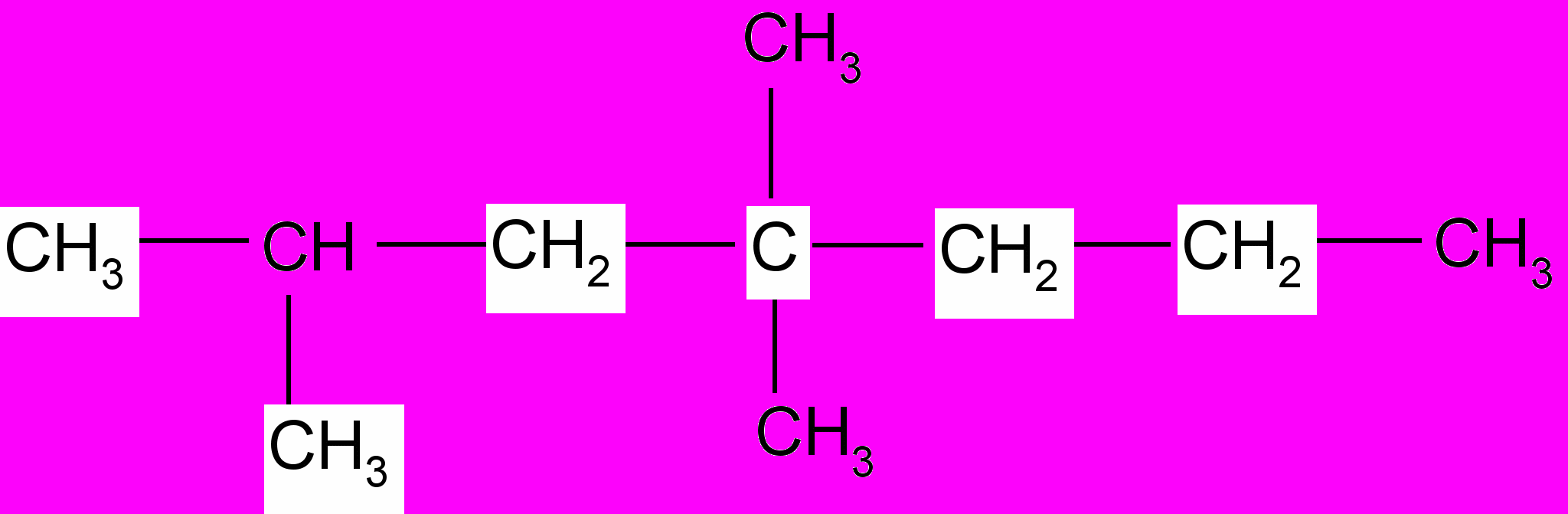
в)
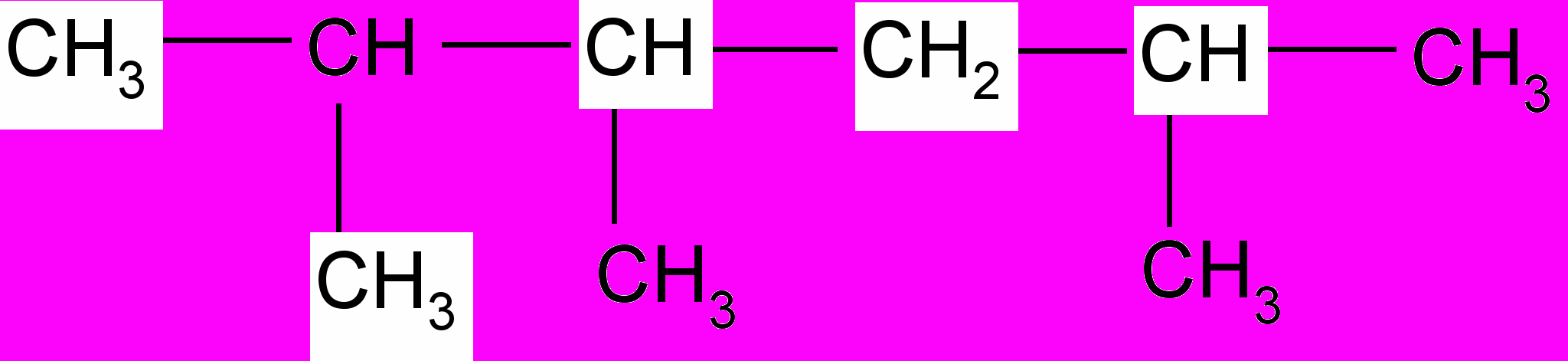
4. Напишите структурные формулы всех углеводородов, изомерных триметилпропилметану, и назовите их.
5. Расположите следующие углеводороды в порядке возрастания их температур кипения: гексан, изогексан, пентан, 2,3-диметилбутан.
6. Какие первичные галогеналкилы при взаимодействии с металлическим натрием могут образовать только углеводороды следующего строения:
а) 2,5-диметилгексан; б) 2,7-диметилоктан?
7. Напишите реакции сульфохлорирования, сульфоокисления и нитрования (по Коновалову) 2-метилпентана.
8. Напишите структурную формулу органического вещества состава С5Н12, если известно,что при его бромировании получается преимущественно третичное бромпроизводное, а при нитровании (по Коновалову) – третичное нитросоединение.
Контрольные вопросы к занятию по теме:
Алифатические углеводороды (алкины, алкадиены).
1. Алкадиены; классификация, изомерия, номенклатура.
2.Особенности химического строения алкадиенов с сопряженными связями.
3.Химические свойства сопряженных диенов. Диеновый синтез.
4. Алкины. Номенклатура, изомерия. Получение алкинов.
5. Электронное строение ацетилена: sp- гибридизация, σ- и π- связи.
Физические свойства алкинов.
6.Химические свойства ацетиленовых углеводородов (реакции
присоединения, замещения, окисления, полимеризации).
Экспериментальная часть
Опыт 1. Получение ацетилена
В пробирку 1 поместите кусочек карбида кальция, добавьте 10 капель воды. Немедленно начинается выделение газообразного ацетилена. Обратите внимание на характерный запах технического ацетилена, обусловленный наличием примесей ( фосфористого водорода РН3). Химически чистый ацетилен запаха не имеет.
Закройте пробирку пробкой с газоотводной трубкой и подожгите выделяющийся ацетилен у конца газоотводной трубки и отметьте свечение пламени.
Доказательства наличия тройной связи в молекуле ацетилена:
● бромирование – в пробирку 2 поместите 6 капель бромной воды. Опустите в нее газоотводную трубку так, чтобы конец трубки был погружен в бромную воду. Происходит обесцвечивание бромной воды.
● окисление – в пробирку 3 поместите 1 каплю 2%-го раствора КМnО4 и 5
капель воды, опустите в нее конец газоотводной трубки. Отметьте изменение
окраски раствора в пробирке 3.
Напишите уравнения реакций получения ацетилена из карбида кальция и
Качественные реакции с бромной водой и с раствором КМnО4.
Опыт 2.Образование ацетиленида меди.
В конце реакции удалите пробку с газоотводной трубкой из пробирки 1. Введите в отверстие пробирки 1 полоску фильтровальной бумаги, смоченной бесцветным аммиачным раствором хлорида меди (І). На бумаге появляется красновато-коричневое окрашивание вследствие образования ацетиленида
меди (І).
По окончании выделения ацетилена в пробирку 1 добавьте 1 каплю 1%-го спиртового раствора фенолфталеина. При этом появляется малиновое окрашивание.
Напишите уравнение реакции взаимодействия ацетилена с аммиачным раствором хлорида меди (І).
В фармацевтическом анализе реакция с аммиачным раствором хлорида меди (І) используется для установления подлинности некоторых лекарственных веществ, содержащих концевую тройную связь.
Задачи для самостоятельного решения.
- Напишите структурные формулы следующих углеводородов:
а) 2,4-гексадиен; б) 2,3-диметил-1,3-бутадиен; в) изобутилацетилен; г) метил-втор.бутилацетилен; д) 2,5-диметил-3-гексин; е) 3,4-диметил-1-пентин.
2. Напишите структурные формулы изомерных диеновых углеводородов состава С5Н8. Назовите углеводороды.
3. Напишите структурные формулы изомерных ацетиленовых углеводородов состава С6Н10 и назовите их.
4. По способу Лебедева получите дивинил. Для дивинила напишите реакции гидрирования, бромирования и гидрохлорирования.
5. Получите 5-метил-1-гексин из 5-метил-1-гексена.
6. С помощью какой реакции можно различить метилацетилен и диметилацетилен?
7. Напишите схему реакции Кучерова для этилацетилена.
8. Из ацетилена получите следующие углеводороды:
а) метилацетилен; б) этилацетилен; в) 4-метил-1-пентин; г) 5-метил-2-гексин
9. Для 1-бутина напишите реакции со следующими веществами: водородом в присутствии катализатора; с бромом; с бромоводородом; с металлическим натрием; с водой в присутствии катализатора.
