Вступ. Актуальність
| Вид материала | Документы |
- Вступ актуальність теми, 953.91kb.
- Вступ актуальність теми, 1309.02kb.
- Загальна характеристика роботи актуальність теми, 260.19kb.
- Вступ актуальність наукової роботи, 372.88kb.
- Загальна характеристика роботи актуальність теми, 286.74kb.
- Загальна характеристика роботи актуальність теми, 407.04kb.
- Вступ актуальність теми, 307.5kb.
- Вступ актуальність теми, 1185.39kb.
- Вступ актуальність теми, 481.06kb.
- План: Вступ Актуальність проблеми забезпечення безпеки в інформаційних системах Нормативно-правова, 339.55kb.
Вступ.
Актуальність. Резус – фактор був відкритий в 1940 році Ландштейнером і Вінером в еритроцитах macacus rhesus. Анти сироватка, отримана імунізацією кроля еритроцитами мавпи, аглютинувала приблизно 85 % зразків еритроцитів людини незалежно від їх групової приналежності. Нові антитіла були названі антитілами анти резус, а антиген, який їх викликає, - резус – фактором.
Переливання крові яка містить резус – фактор, резус – негативному реципієнту може викликати утворення імунних антитіл. В результаті цього повторна трансфузія резус – позитивної крові в ряді випадків супроводжується тяжким гемолітичним ускладненням. Сенсибілізація до резус – фактора може наступити у жінок після вагітності резус – несумісним плодом. В цьому випадку посттрансфузійна реакція нерідко виникає вже після першого переливання резус – позитивної крові.
Спостерігалися жінки, які були сенсибілізовані до резус – фактора в дитинстві введенням їм внутрім´язово материнської крові з лікувальною ціллю (стимуляції ). Високий титр резус – антитіл з´являється у них на протязі першої вагітності резус – несумісним плодом. В зв´язку з цим незалежно від метода гемотерапії необхідно дотримуватися принципу резус – сумісності [1].
Крім основного резус – фактора Фішер і Рейс виділили його різновиди׃ rh', rh", Hr0, hr', hr".Для запобігання плутанини прийнята змішана номенклатура резус – антигенів ׃ Rh0 (D ), rh " (E ), hr' (c ), Hr0 (d ), hr" (e ), які стали позначатись другими буквами .
Мета полягає в аналізі та дослідженні статистичного розподілу ресус-фактора в Рівненській області.
Об’єкт дослідження: пацієнти віддлення трансфузіології Рівненської обласної клінічної лікарні.
Предмет дослідження: статистичний аналіз резус-фактора крові паціїнтів
Основні завдання роботи:
- аналіз методичної та наукової літератури даної теми.
- Проведення експеримента та дослідження розподілу резус-фактора в Рівненській області.
РОЗДІЛ 1. ЗАГАЛЬНА ХАРАКТЕРИСТИКА РЕЗУС -ФАКТОРА ТА ЙОГО ФУНКЦІЙ.
1.1 Склад крові та її функції.
Кров – це рідка сполучна тканина організму. Кров вищих тварин і людини циркулює в системі замкнених судин і забезпечує оптимальні умови для життєдіяльності організму [1].
Основні функція крові:
- дихальна функція - переносить кисень і поживні речовини до органів та тканин, виводить вуглекислий газ і продукти обміну;
- бере участь у терморегуляції;
- захисна функція (фагоцитарна);
- бере участь у гомеостазі, який регулюється нервовою системою, підтримує сталість внутрішнього середовища організму;
- регуляторна - розносить по організму фізіологічно активні речовини, які регулюють та об`єднують діяльність різних органів та систем, тобто здійснює гуморальну регуляцію функцій організму;
- поживна - розносить поживні речовини від кишківника до клітин;
- видільна - видалення з клітин та тканин кінцевих продуктів обміну речовин.
Морфологічні та корпускулярні елементи крові в сумі складають велику адсорбційну поверхню, яка забезпечує максимальну інтенсивність хімічних каталітичних процесів, пов’язаних з обміном речовин. Будучи рівноважною фізико-хімічною системою, кров реагує як єдине ціле на різні екзо - і ендогенні дії. Всі компоненти цієї системи настільки тісно пов’язані між собою, що найменші зміни в одній з них діють належним чином на стан інших.
Кров, яка рухається, як жива тканина, має свої біологічні особливості, завдяки яким успішно вирішена проблема її приживлення в організмі реципієнта.
Кров людини можна розглядати як колоїдний розчин завису клітинних елементів: еритроцити, лейкоцити і кров’яні пластинки. Кожен з цих компонентів має свою терапевтичну дію і може бути використаний в лікувальній практиці окремо.
Походження компонентів крові різне. Еритроцити, зернисті лейкоцити і тромбоцити поступають з кісткового мозку. Лімфоцити утворюються з стовбурових клітин кісткового мозку і проходять в лімфатичній тканині стадію лімфобластів і пролімфоцитів. Моноцити, по сучасних уявленнях, мають також кістковомозкове походження. Основна частина білків крові ‹альбумін, фібриноген, ά – і β- глобуліни, протромбін› синтезуються в печінці, γ- глобуліни утворюються плазматичними клітинами ‹імуноцитами›, попередниками яких є В- лімфоцити.
К
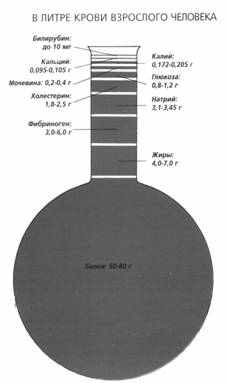 ров (sanguis) складається з плазми й форменних елементів (клітин крові). Плазма складає 55-60% від загального об’єму крові, і на 90- 93 % складається з води. Плазма відрізняється від сироватки наявністю в ній білка- фібриногену. Решта білків- альбуміни і глобуліни присутні як в плазмі, так і в сироватці. Крім того, в рідкій частині крові містяться біологічно активні речовини
ров (sanguis) складається з плазми й форменних елементів (клітин крові). Плазма складає 55-60% від загального об’єму крові, і на 90- 93 % складається з води. Плазма відрізняється від сироватки наявністю в ній білка- фібриногену. Решта білків- альбуміни і глобуліни присутні як в плазмі, так і в сироватці. Крім того, в рідкій частині крові містяться біологічно активні речовини ‹ гормони, вітаміни, ферменти, гемопоетини › білкової та небілкової природи, вуглеводи, ліпіди, продукти метаболізму та біля 0,9 % електролітів. Найважливіше значення мають білки, які складають 7-8 %. Вони відрізняються по амінокислотному складу, фізико-хімічних властивостях, розчинності. Інші 40-50% - відводиться на формені елементи. Це еритроцити - червоні кров'яні тільця, лейкоцити - білі кров’яні клітинки й тромбоцити - кров'яні пластинки. Кров складає приблизно 7% від загальної ваги тіла. При вазі в 70 кг її об’єм дорівнює 5-5,5 л [1].
Еритроцити - це високоспеціалізовані клітини, призначені для переносу газоподібних речовин (кисню й вуглекислоти). У мазку еритроцити мають своєрідну форму - двоякоувігнутих дисків; ядро в них відсутнє. При русі по капілярах вони легко деформуються. Діаметр еритроцитів коливається від 7,2 до 8,5 мкм. Еритроцит зовні вкритий мембраною, а всередині майже повністю заповнений білковою речовиною – гемоглобіном (Нв). Нв складається з білка глобіну (600 Н) і залізовмісної сполуки – гемму ( Ч,А. Fe) (С3032 Н4816 О872 N780 S8 Fe4). В 1 л крові міститься 130-160 г Нв.
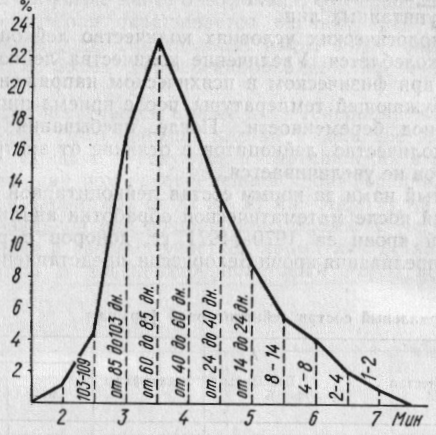
Вік циркулюючих еритроцитів
Основна функція Нв – транспортування кисню від легенів до тканин. У легенях під час вдиху Нв тимчасово з’єднується у нестійку сполуку, що називається оксигемоглобіном (Нв + О2 → НвО2). Кров, яка насичена О2 – артеріальна, має яскраво-червоний колір.
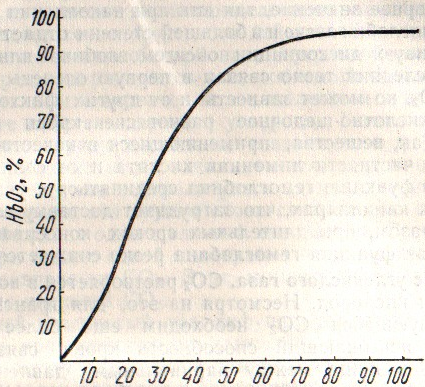
Парціальний тиск О2,мм. рт .ст.
Крива дисоціації оксигемоглобіна(по Б.І.Збарському)
Утворення оксигемоглобіна і його дисоціація – процеси чисто фізичні. Гемоглобін при цьому не окислюється, а валентність заліза в гемі не міняється. При анемічних станах здатність гемоглобіну зв´язувати кисень значно зростає,так як в зв´язку з зниженням напруження кисню в тканинах підвищується дисоціація оксигемоглобіна [2].
З кривої дисоціації оксигемоглобіна видно,що в звичайних умовах альвеолярного повітря при парціальному тиску кисню біля 100 і вуглекислого газу – 40 мм.рт.ст. 99% гемоглобіна переходить в оксигемоглобін.
У тканинах Нв приєднує СО2 (Нв + СО2 → НвСО2 – карбгемоглобін, також нестійка сполука). Кров насичена СО2 – венозна, темно-червоного забарвлення (10% СО2 переносить Нв).
Нв здатний приєднувати чадний газ СО що виділяється при неповному згорянні палива, і утворювати з ним стійку сполуку – карбоксигемоглобін (Нв + СО → НвСО). У цій сполуці він втрачає здатність приєднувати і переносити О2. У результаті настає важке отруєння організму.
У 1 мм3 крові утримується 3,5-5,9 млн. еритроцитів (у чоловіків) й 3,5-5,3 млн. (у жінок). У переносі газоподібних продуктів велике значення мають розміри поверхонь еритроцитів. Відомо, що поверхня одного еритроцита складає 142 мкм2. Отже, загальна поверхня еритроцитів, що циркулюють у крові, буде дорівнює приблизно 3000-3820 м2.
У
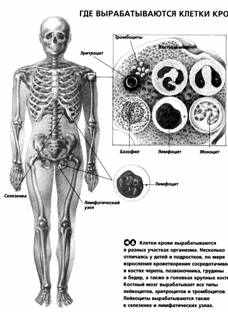 дорослої людини еритроцити виробляються червоним кістковим мозком, який зберігається в епіфізах довгих трубчастих кісток, в хребцях, ребрах і грудині, і надходять у загальне судинне русло. Тривалість життя еритроцитів у середньому складає 2-3 місяця. Є дані, згідно яким в організмі щодня руйнується приблизно 1/100 частина всіх еритроцитів. Розпад віджилих еритроцитів відбувається переважно в селезінці.
дорослої людини еритроцити виробляються червоним кістковим мозком, який зберігається в епіфізах довгих трубчастих кісток, в хребцях, ребрах і грудині, і надходять у загальне судинне русло. Тривалість життя еритроцитів у середньому складає 2-3 місяця. Є дані, згідно яким в організмі щодня руйнується приблизно 1/100 частина всіх еритроцитів. Розпад віджилих еритроцитів відбувається переважно в селезінці.Лейкоцити - це різнорідна по своїм морфологічним й функціональним властивостям група клітин крові. Розрізняють зернисті й незернисті лейкоцити. До зернистих лейкоцитів відносять: нейтрофільні, еозинофільні й базофільні лейкоцити, а до незернистих - лімфоцити й моноцити [2].
У дорослої людини в 1 мм3 крові нараховується 6000-8000 лейкоцитів. Однак кількість їх непостійна й може мінятися в залежності від стану організму. Нейтрофільні лейкоцити: паличкоядерні –1,6%, сегментоядерні – 47-72%, еозинофіли 0,5-5%, базофіли 0-1%, лімфоцити 20-37%, моноцити 3-11%.
Зернисті лейкоцити утворюються в червоному кістковому мозку, а незернисті - у лімфатичних вузлах, вилочковій залозі, мигдалинах і фолікулах. Термін життя лейкоцитів у середньому складає 10-12 днів.
На відміну від еритроцитів лейкоцити мають ядро. Розмір їх коливається від 7 до 11 мкм. Вони здатні активно переміщатися завдяки амебоїдним рухам. У лейкоцитах утримується велика кількість ферментів, здатних розщеплювати різні речовини. На цій властивості лейкоцитів заснована їхня роль у захисті організму від мікробів й сторонніх речовин.
Тромбоцити (кров'яні пластинки) - дрібні тільця різної форми, розміром 2-3 мкм. Вони відіграють важливу роль при згортанні крові. У 1 мм3 крові їх утримується від 200 000 до 300 000. Тривалість життя тромбоцитів in vivo -4-6 днів.
П
 ри будь-якому ушкодженні кровоносної системи відкривається внутрішня або зовнішня кровотеча. Велика втрата крові дуже небезпечна. Людина може без особливої шкоди для себе втратити до 15% крові, але перевищення цього порога часто призводить до смерті. Повільна тривала кровотеча веде до анемії, а стрімка втрата крові викликає шок, при якому тиск падає так низько, що кров перестає надходити в серце.
ри будь-якому ушкодженні кровоносної системи відкривається внутрішня або зовнішня кровотеча. Велика втрата крові дуже небезпечна. Людина може без особливої шкоди для себе втратити до 15% крові, але перевищення цього порога часто призводить до смерті. Повільна тривала кровотеча веде до анемії, а стрімка втрата крові викликає шок, при якому тиск падає так низько, що кров перестає надходити в серце.В організмі є особлива система, що не допускає надлишкової втрати крові. Це механізм згортання. Кістковий мозок виробляє особливі клітини - тромбоцити, що за розміром навіть менші від еритроцитів. При найменшому ушкодженні кровоносної судини тромбоцити спрямовуються до пошкодження і приклеюються до його стінок і один до одного, утворюючи тромб.
Склеюючись, тромбоцити - як, утім, і сама ушкоджена тканина - виділяють речовини, що запускають механізм згортання. Вони також виділяють гормон серотонін, що стимулює звуження кровоносних судин, тим самим зменшуючи кровотік.
Зклеєні тромбоцити спонукають виділення тромбоцитарного фібриногену (фактор 5) - один з розчинених у плазмі білків, до утворення ниток нерозчинного білка фібрину, і кров згортається. Фібринові нитки переплітаючись, утворюють напівтвердий згусток, який спонтанно скорочується. Потім з цієї маси виділяється сироватка, і утворюється твердий згусток. Загальний обсяг крові відновлюється через декілька годин після зупинки кровотечі по мірі всмоктування води з тканин, але для відновлення клітин крові організму потрібно декілька тижнів [2].
1.2 Антигени і антитіла крові людини і їх клінічне значення.
Міжвидова серологічна різниця, основана на реакції аглютинації, преципітації чи гемоліза, які проходять між кров´ю різних тварин чи кров´ю людини і тварин, були відомі давно. В подальшому вияснилось, що така різниця може існувати і в середині окремого виду .
В 1901 році Ландштейнер описав основні групи крові людини системи АВО в залежності від наявності в еритроцитах ізоантигенів, а в сироватці крові – ізоантитіл. Це відкриття дозволило науково обґрунтувати переливання крові, зробити його ефективним і безпечним методом лікування [3].
Наука про ізоантигени і ізоантитіла крові часто називається наукою про групи крові, що не зовсім точно, так як антигенне диференціювання не обмежується форменними елементами крові, в тому числі еритроцитами . Вона відноситься до загальнобіологічних законів і поширена в рівній мірі між тваринами, рослинами і бактеріями.
Антиген – речовина, яка має здатність викликати в організмі вироблення антитіл і вступати з ними в реакцію. Антигени, які мають обидві із вказаних властивостей, називаються повноцінними, а тільки однією із них –неповноцінними .
Антитіла крові людини представлені двома великими групами ׃ природніми і імунними. До природніх антитіл відносяться групові аглютиніни α і β , які успадковуються від батьків, до імунних – резус –антитіла, а також анти- А і анти – В антитіла, які виникають в результаті імунізації. Ізоаглютиніни α і β називають ще повними або сольовими, антитілами, так як вони викликають аглютинацію еритроцитів при кімнатній температурі ( від 15 до 25º ) в сольовому середовищі .
Неповні аглютинуючі, чи білкові, антитіла, до яких відносяться резус – антитіла, викликають аглютинацію еритроцитів тільки в білковому чи колоїдному середовищі. Додавання до цього середовища фізіологічного розчину натрію хлориду знижує якість реакції чи повністю її знищує.
Неповні блокуючи антитіла викликають утворення аглютинінів еритроцитів тільки при додаванні антиглобулінової сироватки.
Антигени крові людини
В організмі людини є велика кількість антигенів, які забезпечують імунологічну специфічність всіх тканин і органів. Еритроцитарні антигени поділяються на декілька систем, які виникли в процесі філогенетичного розвитку виду(таблиця ) [4].
Антигени містяться не тільки в еритроцитах, але і в лейкоцитах, тромбоцитах, що може бути в деяких випадках причиною виникнення посттрансфузійних реакцій, а також несумісності організму матері і плода.
Антигенним диференціюванням володіють як форменні елементи так і сироваткові гамма-глобуліни, які мають декілька типів з різними властивостями. Антигенні ознаки сироваткового білка передаються по спадковості не залежно від систем антигенів форменних елементів і являються також причиною деяких посттрансфузійних реакцій.
Основні антигенні системи (по П.Н.Косякову в модифікації Л.В.Іванова)

Системи МΝ , Келл , Даффі , Левіс та інші.
Антигени М і Ν обов´язково присутні в організмі людини або одночасно (МΝ) , або по одному (М і Ν ). Диференціювання цих антигенів починається з 7 – 9 тижня розвитку ембріона. Система МΝ представлена великою кількістю факторів, які мають невелике практичне значення через низьку антигенність. Це відноситься і до систем Келл, Даффі, Левіс та ін., які як і система МΝ, поки не враховуються в практичній трансфузіології. Але слід мати на увазі, що інколи посттрансфузійні реакції можуть бути спричинені несумісністю крові по цих факторах [4].
Таким чином, з усіх систем слід виділити антигени А, В і Rh0 (D ), які в більшості випадків бувають причиною посттрансфузійних реакцій і ускладнень.
Найбільш значущий в трансфузіології є антиген Келл (К). По імуногенній активності цей фактор займає друге місце після антигену резус. Ізосенсибілізація до нього може призвести до розвитку посттрансфузійних ускладнень, а також являється причиною гемолітичної хвороби новонароджених. Фактор (К) частково руйнується під дією протеолітичних ферментів. Частота виявлення антигена Келл складає біля 10%. Особи, гомозиготні по цьому фактору(КК), зустрічаються в 0,3% випадків.
Система Даффі представлена двома антигенами: Fyª і Fyb. Фактор Fyª зустрічається у 74%осіб російської національності, фактор Fyb –у 85%. Особи, які являються гетерозиготами Fy(a+b+), складають 48%. У деяких народів (ескімоси) частота виявлення антигена Fyª -100% . Фактор Fyª являється більш імуногенним.
Система MNSs – це складна поліморфна система, яка об’єднує 2 самостійні системи антигенів MN, Ss і біля 30 супутніх антигенів: Hu, He, Mia, Vw, Mur та інші. Група крові М зустрічається у 36% людей, N-у 16%, MN-у 48%. Антитіла анти – М і анти - N мають ізоімунну природу. Природні антитіла анти-М і анти-N зустрічаються дуже рідко. Подібно антитілам анти-S і анти-s вони можуть служити причиною посттрансфузійних реакцій. Групу крові S мають 10% людей, групу s-45%, групу Ss-44%.
Система Левіс об’єднує 4 антигени: Lea,Leb,Lec,Led. Антигени Le тісно пов’язані з групами крові АВО. Особи, які містять антигени Leb і Led, являються секреторами групових речовин А, В і Н, які можна знайти в їх слині, травних соках та інших секретах.
Антигени АВО - групи кровi.
В 1901 роцi австрiйський вчений Ландштейнер, а пiсля нього чеський медик Янський довели, що в людей iснують 4 основнi групи кровi, якi успадковуються вiд батькiв за певними законами генетики. Їх позначають 1 (0), II (А), III (В), IУ (АВ). В Європi найчастiше трапляються перша — 46%, друга — 42%, рiдше третя — 9%, найрiдше — четверта 3%.
Групова належнiсть кровi залежить вiд особливих склеювальних речовин
(бiлкiв) — аглютиногенів (антигенів ) (А i В), що мiстяться в еритроцитах, та аглютинiнiв (антитіл) (α і β), що є у плазмi кровi.
-
Групи крові
Антигени
Антитіла
О або ( I )
---------------
α β
А або ( II )
A
β
В або ( III )
B
α
АВ або ( IV )
AB
-----------------
В кровi одної особи нiколи немає збiгу однойменного аглютинiну й аглютиногену (α з А, β з В), помилкове. змiшування їх пiд час переливання кровi приводить до склеювання або аглютинацiї еритроцитiв i наступного гемолiзу з утворенням токсичних речовин.
Для запобігання ускладнень , які можуть виникнути в результаті взаємодії нормальних аглютинінів реципієнта з еритроцитами донорської крові, звичайно переливають тільки одногрупну кров. Якщо її немає, то по життєвих показах допустимо переливання так званої сумісної в груповому відношенні крові по наступній схемі ׃
Група крові Допустиме переливання реципієнту з групою крові донора
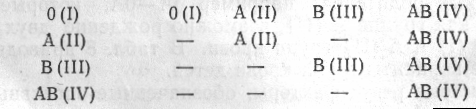
При переливанні сумісної в груповому відношенні крові звичайно не приймають до уваги можливість руйнування еритроцитів хворого ізоаглютинінами α і β крові донора, а це може спостерігатися при масивних гемотрансфузіях, коли виникає ”зворотній гемоліз ”. Тому до трансфузій сумісної в груповому відношенні крові О (І ) групи слід застосовувати в крайніх випадках (при відсутності одногрупної крові ) і переливати її при можливості в невеликих кількостях.
В зв´язку з частими посттрансфузійними реакціями при гемотрансфузіях необхідно притримуватися наступних правил ׃
1) реципієнт групи О ( І ) отримує кров групи О( І );
2) реципієнт групи А ( ІІ ) отримує кров групи А (ІІ );
3) реципієнт групи В (ІІІ ) отримує кров групи В (ІІІ ) ;
4) реципієнт групи АВ (ІV ) отримує кров групи АВ (ІV ).
Якщо хворому перелита кров універсального донора і є подальша необхідність в гемотрансфузії, то необхідно використовувати для цієї цілі відмиті еритроцити групи О(І).

Варіанти успадкування груп крові системи АВО(по П.Н.Косякову)
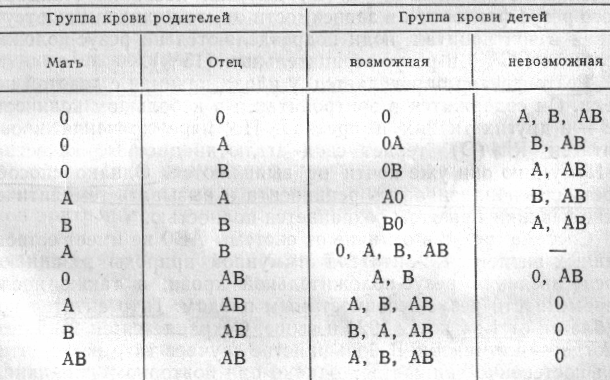
Передача антигенів по спадковості проходить відповідно з законом Менделя. При з´єднаннні двох статевих клітин ознаки кожної з них якби об´єднуються, і людина від батька і матері отримує два набори хромосом з відповідними генами. Якщо у батьків однакові гени, народжується дитина гомозиготного типу, якщо різні - то гетерозиготного. Так всі особи О(І) групи відносяться до гомозиготного, а (АВ)IV групи - до гетерозиготного типу. У людей А(ІІ) і В(ІІІ) груп можливе неспівпадання фенотипа з генотипом. Так, генотипи ОА і АА визначаються як група крові А(ІІ), генотипи ОВ і ВВ- як В(ІІІ). У гетерозиготних батьків, наприклад ОА-ОА, які визначаються як група А(ІІ), можливе народження двох фенотипів – О(І) і А(ІІ) груп крові.
Резус – фактор був відкритий в 1940 році Ландштейнером і Вінером в еритроцитах macacus rhesus. Анти сироватка, отримана імунізацією кроля еритроцитами мавпи, аглютинувала приблизно 85 % зразків еритроцитів людини незалежно від їх групової приналежності. Нові антитіла були названі антитілами анти резус, а антиген, який їх викликає, - резус – фактором.
Переливання крові яка містить резус – фактор, резус – негативному реципієнту може викликати утворення імунних антитіл. В результаті цього повторна трансфузія резус – позитивної крові в ряді випадків супроводжується тяжким гемолітичним ускладненням. Сенсибілізація до резус – фактора може наступити у жінок після вагітності резус – несумісним плодом. В цьому випадку посттрансфузійна реакція нерідко виникає вже після першого переливання резус – позитивної крові.
Спостерігалися жінки, які були сенсибілізовані до резус – фактора в дитинстві введенням їм внутрім´язово материнської крові з лікувальною ціллю (стимуляції ). Високий титр резус – антитіл з´являється у них на протязі першої вагітності резус – несумісним плодом. В зв´язку з цим незалежно від метода гемотерапії необхідно дотримуватися принципу резус – сумісності.
Крім основного резус – фактора Фішер і Рейс виділили його різновиди׃ rh', rh", Hr0, hr', hr".Для запобігання плутанини прийнята змішана номенклатура резус – антигенів ׃ Rh0 (D ), rh " (E ), hr' (c ), Hr0 (d ), hr" (e ), які стали позначатись другими буквами .
Відповідні їм антитіла стали позначатись таким чином ׃ анти - rh' ( C ), анти – Rh0(D ), анти - rh"(E ), анти - hr' (c ), анти - Hr0(d ), анти - hr"(e ).
Генетика резус – фактора.
Утворення резус антигенів контролюється трьома парами алельних генів : Dd, Cc і Ee, які розміщені на двох хромосомах. Кожна хромосома здатна нести тільки 3 гени і 6 , причому лише один ген з кожної пари – D чи d, С чи с, Е чи е. Гени D і d, С і с, Е і е являються по відношенню один до одного алельними. Тому еритроцити, які не містять антигени rh′( C ) чи rh″( E ), завжди містять алельні антигени hr′( c ) чи відповідно hr″( e ) і, навпаки hr′( c ), hr″( e ) – негативні еритроцити незмінно виявляються rh′( C ), rh″( E ) – позитивними. Вказані 6 антигенів резус зустрічаються в еритроцитах у вигляді одного із 18 можливих комбінацій. Фенотипічно кожна людина містить 5, 4 чи 3 антигена резус в залежності від кількості генів, по яких він гомозиготний. Але фенотипічна формула виражається шести буквами,наприклад cDe\CDe,які означають три гени резус, успадкованих з хромосомою одного з батьків, 3-хромосомою іншого. Найбільш часто зустрічаються комбінації генів резус наступні: CDe - 53,2%, CDE -15,8%, cDE - 14,5%, cde - 12,3%.
Ряд антигенів системи Rh-Hr не мають своїх алелей, а являють собою різновид одного з відомих антигенів, який утворився в результаті мутації відповідного гена. Існує варіант антигена Rh0(D)-Du, а також варіанти антигенів С, Е, с і е, які позначуються символами Сu, Сw, Еu, Еw, сv, еx.
В антигенному відношенні фактор Du слабший фактора D; Сu слабший С; Еu слабший Е.
Кров деяких здорових людей не містить ні одного з відомих факторів системи Rh-Hr, а також антигена LW. Припускають що такий фенотип, позначений Rh зустрічаеться в осіб, гомозиготних по гену Xr0, який пригнічує продукцію антигенів резус і LW. Особи з фенотипом Rhnull, зустрічаються в регіонах де поширені міжродинні шлюби. Не проявляючи фенотипічно антигенів резус, особи з фенотипом Rhnull можуть нормально передавати їх по спадковості.
В клінічній практиці основне значення має фактор Rh0(D), який через високу антигенність в більшості випадків є причиною сенсибілізації і виникнення посттрансфузійних гемолітичних реакцій. В зв´язку з цим антиген Rh0 (D) отримав назву стандартного резус – фактора, і в залежності від його наявності чи відсутності в еритроцитах люди поділяються на резус – позитивних ( 85% ) і резус – негативних (15% ).
Резус – фактор визначається у плода починаючи з 9 тижня. Він міститься в еритроцитах і в невеликій кількості – в інших тканинах і органах. По мірі зберігання крові резус – антиген втрачає свої аглютинаційні властивості, до 15 – го дня він вже майже не виявляється. Але властивість сенсибілізувати реципієнта і викликати гемолітичні реакції при цьому зберігається повністю.
Система резус на відміну від системи АВО не має природніх антитіл. Резус – антитіла імунної природи виникають після введення резус – позитивної крові, а також після вагітності резус – несумісним плодом. Титр антитіл коливається від 1: 4 до 1 : 1024 і вище. Зберігається він 2 – 5 років, іноді, - все життя. В більшості випадків титр резус – антитіл поступово знижується, але при повторному попаданні резус – позитивних еритроцитів він різко підвищується.
Сенсибілізація до резус – фактора.
В крові природніх резус - антитіл практично не зустрічається, тому перша резус - несумісна трансфузія закінчується благополучно. Посттрансфузійна реакція в результаті резус-несумісності може виникнути після попередньої сенсибілізації людини до резус-фактору. Сенсибілізація резус - негативних людей до резус - фактору може наступити в результаті резус -несумісних гемотрансфузій, вагітностей резус-несумісним плодом чи гемотерапії резус - несумісною кров’ю [5].
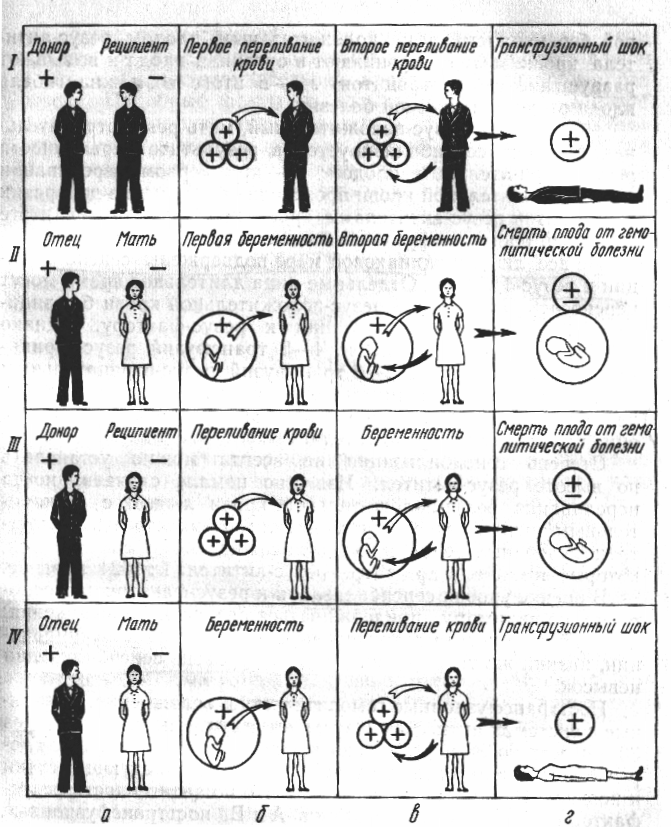
На малюнку (4) наведена схема можливих шляхів сенсибілізації до резус-фактору і її наслідки:
І. а – донор резус-позитивний, реципієнт резус-негативний; б – резус-негативний реципієнт сенсибілізується переливанням резус - позитивної крові донора; в – при повторному переливанні резус-позитивної крові відбувається її гемоліз резус - антитілами реципієнта; г – в результаті гемолізу резус-несумісної донорської крові можливий посттрансфузійний шок.
ІІ. а – батько резус-позитивний, мама резус - негативний; б – сенсибілізація матері відбувається при вагітності резус - позитивним плодом; в – при повторній вагітності резус - позитивним плодом резус - антитіла із організму матері проникають в його організм і руйнують еритроцити; г – як наслідок можлива загибель плода від гемолітичної хвороби.
ІІІ. а - донор резус - позитивний, реципієнт (жінка) резус - негативний; б – при переливанні резус - позитивної крові реципієнт сенсибілізується; в – при першій вагітності резус - позитивним плодом резус - антитіла крові матері проникають в його організм і руйнують еритроцити; г – як наслідок можлива загибель плода від гемолітичної хвороби.
ІV. а – батько резус - позитивний, мати резус - негативний; б – мати сенсибілізується в результаті вагітності резус - позитивним плодом; в – при першому переливанні резус - позитивної крові проходить руйнування донорських еритроцитів резус - антитілами крові жінки; г – в результаті можливий посттрансфузійний шок.
Не всі люди в однаковій мірі підлягають сенсибілізації до резус - фактору. Окремі особи довгий час можуть переносити переливання резус - несумісної крові без видимих ознак сенсибілізації до резус - фактору. Але в переважній більшості після 4 - 5трансфузії резус - негативним чоловікам і 2 - 3 трансфузій резус - негативним жінкам резус - позитивної крові у них розвивається більш чи менш виражена посттрансфузійна реакція і виявляються резус-антитіла.
Схема шляхів сенсибілізації до резус-фактора та можливі її результати(поDamerow)
Варіанти успадкування резус - фактора

В системі резус – фактори, позначені великими буквами, в якійсь мірі домінують над позначеними малими буквами. В зв´язку з цим при дослідженні резус – придатності еритроцити генотипів DD і Dd аглютинуються однаково. Резус – позитивний фенотип крові може бути представлений двома генотипами гомозиготним DD і гетерозиготним Dd. Резус – негативний тип крові завжди гомозиготний( dd ). В такій же взаємозалежності знаходяться фактори Сс і Ее. Фактори С, D, Е кодомінантні і не пригнічують один одного, так само як і фактори с, d, е. Успадкування пар факторів системи резус проходить за тими ж законами, що і антигени системи АВО.
Якщо батьки гомозиготні по фактору D(DD і DD) чи d (dd і dd), то у них можуть народитися діти тільки з цим типом крові.
Поняття про резус - конфлікт
Резус - фактор – це ціла система антигенів, що представлена поруч алелей D, C, E. Резус-негативна кров також має особливі антигенні властивості, у ній виявлений фактор Hr, що має три різновиди – d, c, e. В даний час описано близько 36 можливих генотипів системи Rh-Hr. Найбільш часто зустрічаються D-, E-, C-антигени. У розвитку імунологічного конфлікту між материнським організмом і організмом плоду основне значення має фактор D. Приблизно 1,5% від усіх вагітностей у резус-негативних жінок ускладнюється еритроцитарною сенсибілізацією.
Rh-негативними є до 30% жінок-басків (народність, що проживає в Іспанії і Франції), 15% білих жінок, 10% іспанок Латинської Америки, 6-8 % негрів і 2% представниць жовтої раси.
Антигени системи резус по своїх антигенних властивостях йдуть слідом за антигенами системи AB0 і, будучи введеними в організм людини, викликають вироблення анти резус - антитіл. Резус - фактор міститься в основному в еритроцитах. У крові людини природних антитіл стосовно резус - фактора немає. На підставі розходження серологічних властивостей антитіла поділяють на «повні» і «неповні». У розвитку імунологічних ушкоджень плоду основне значення мають «неповні» антитіла, оскільки вони можуть проникати через плаценту. «Повні» антитіла з великою молекулярною масою в значно меншій кількості проникають через плацентарний бар'єр і тому відіграють другорядну роль у розвитку патології. Вага захворювання в основному залежить від виду антитіл, що продукуються імунною системою організму матері. Первинною відповіддю матері на вплив стороннього антигену є вироблення Ig. Наступний вплив (реакція в анамнезі) приводить до продукції материнського Ig, що є єдиним з імуноглобулінів, здатних проникати через плаценту, завдяки малому розміру. Повторне влучення в кровоток матері навіть невеликої кількості еритроцитів плоду приводить до швидкого і масивного вироблення антирезусних Ig. У половині випадків для розвитку первинної імунної відповіді досить попадання 50-75 мол. еритроцитів, а для вторинного – 0,1 мол.
Внаслідок несумісності організмів матері і плоду по еритроцитарних антигенах розвивається гемолітична хвороба плоду і немовляти. Патогенез даного захворювання досить вивчений. Еритроцити плоду, проникаючи в організм матері, спонукають її імунну систему до продукції антитіл, що, проникаючи через плацентарний бар'єр, попадають у кровоток плоду. У результаті утворення «неповних» антитіл у плоду спостерігається розпад еритроцитів і інших тканин, ураження нирок, ендотелію, гангліїв головного мозку. При утворенні «повних» антитіл відбувається аглютинаційний тромбоз капілярів, що приводить до ішемічного некрозу тканин плоду. Посилений гемоліз еритроцитів спричиняє підвищення рівня непрямого білірубіна в крові плоду. Оскільки функціональна здатність печінки плоду і немовляти перетворювати непрямий білірубін у прямій обмежена, то рівень першого постійно зростає. Клінічно це виявляється жовтушністю шкіри. Непрямий білірубін токсичний і не виводиться нирками, він порушує тканинний метаболізм, включаючи дихальні ферменти і процеси фосфорилювання. У результаті в печінці порушується синтез білків, що веде до гіпопротеїнемії і посилення проникності судин, зниженню онкотичного тиску в плазмі крові. Дана обставина веде до збільшення печінки, що виникає в наслідок серцевої недостатності та застою у великому колі кровообігу, що в свою чергу призводить до випотівання рідини в тканини і порожнини – розвивається анасарка.
Імунізація жінок з резус-негативною кров'ю протягом вагітності зустрічається дуже рідко. Під час нормальної вагітності еритроцити проникають через плацентарний бар'єр у 5% вагітних протягом 1-го триместру, у 15% - протягом 2-го триместру й у 30% - наприкінці 3- го триместру. Необхідно додати, що кровотеча при амніоцентезі в другому і третьому триместрах має місце в 20% вагітних, а при мимовільних чи штучних абортах – у 15% жінок. У переважній більшості випадків кількість клітин плоду, що попадають у кров матері, невелика і недостатня для виникнення первинної імунної відповіді. Частота дородової первинної ізоімунізації протягом першої резус-несумісної вагітності складає менш 1%. Найбільш ймовірний час одержання первинного стимулу - післяпологовий період. Різні оперативні втручання (ручне відділення плаценти, Кесарський розтин ) значно збільшують можливість трансплацентарного переходу еритроцитів плоду в кровоток матері і викликають сенсибілізацію організму. Імунізація до резус-фактора може наступити також після штучних абортів, особливо в пізній термін, чи мимовільних викиднів. Якщо в майбутньої мами резус негативний, а в майбутнього тата позитивний, виникає небезпека резус-конфлікту. Але початися він може лише в тому випадку, якщо дитина успадкує резус батька. Тоді його кров буде погано сумісна з кров'ю матері.
Що являє собою резус-конфлікт? Резус-фактор плоду переборює плацентарний бар'єр і потрапляє в кров матері, а її організм, сприйнявши плід як щось чужорідне, починає виробляти захисні антитіла. Захищаючи матір, ці антитіла несуть серйозну загрозу її дитині. При важкій формі резус-конфлікту можлива внутрішньоутробна загибель плоду і викидень на будь-якому терміні вагітності.
Антитіла матері проникають через плаценту і руйнують еритроцити дитини. У крові з'являється велика кількість речовини білірубіну. Білірубін надає шкірі маляти жовтого кольору. Оскільки еритроцити плоду безупинно руйнуються, його печінка і селезінка намагаються прискорити вироблення нових еритроцитів, збільшуючись при цьому в розмірах. Зрештою, і вони не справляються із поповненням загиблих еритроцитів. Виникає стан анемії (низький вміст у крові еритроцитів, гемоглобіну). Резус-конфлікт може бути причиною загибелі головного мозку, порушення функції слуху і мови. У найважчих випадках резус-конфлікт виявляється уродженою водянкою (набряком) плоду, що може призвести до його загибелі [5].
У важких випадках дитині може допомогти штучне переливання крові. Йому вводять одногрупну резус-негативну кров і проводять реанімаційні заходи. Ця операція повинна бути проведена протягом 36 годин після народження маляти - тільки тоді вона найбільш ефективна.
Застрахувати дитину від подібних проблем можна навіть не до народження, а ще до планованої вагітності. По-перше, треба довідатися про свою групу крові і резус-фактор. Крім резус-фактора, можливий розвиток конфлікту, якщо кров матері і дитини несумісні по групі. Групова несумісність розвивається, якщо мама має першу групу крові - 0 (I), а дитина - другу А (II) чи третю В (III).
Несумісність партнерів по резус-фактору не привід для розладу чи відмовлення від мрії про дитину. Ті 15% жінок, у яких резус-фактор виявляється негативним, також здатні стати мамами. І найчастіше їхня вагітність протікає нітрохи не важче, ніж у жінок з позитивним резусом. Просто їм не можна забувати про самий ретельний і регулярний контроль свого здоров'я. Майбутній мамі, що має негативний резус-фактор, прийдеться досить часто здавати кров з вени на наявність антитіл. До тридцяти двох тижнів вагітності цей аналіз проводиться один раз на місяць, з 32-х до 35-ти тижнів - двічі на місяць, а потім аж до пологів щотижня. За рівнем антитіл у крові вагітної жінки лікар може зробити висновки про передбачуваний резус-фактор у дитини і визначити початок резус-конфлікту.
Під час першої вагітності резус-конфлікт розвивається рідко, оскільки імунна система матері вперше зустрічається з чужими еритроцитами, отже, згубних для плоду антитіл у крові матері виробляється ще мало. При повторних вагітностях ймовірність проблем підвищується. Адже в крові жінки, що родила, все ще живуть захисні антитіла («клітини пам'яті»), що залишилися від колишньої вагітності. Вони проривають плацентарний бар'єр і починають руйнувати еритроцити ще не народженої дитини.
Правильне лікування чи засоби профілактики може призначити тільки кваліфікований фахівець. У деяких випадках доводиться прибігати і до ранніх пологів, і до вже описаного вище штучного переливання крові немовляті. В даний час розвиток резус-конфлікту можна запобігти і шляхом уведення спеціального - анти-резус-імуноглобуліну - відразу після перших пологів чи переривання вагітності. Цей препарат зв'язує агресивні антитіла, що утворилися в крові матері і загрожують майбутній дитині, і виводить їх з організму. Якщо анти- резус-імуноглобулін не вводився профілактично, його можуть вводити і під час вагітності. Профілактику імуноглобуліном резус-негативним жінкам повинні проводити протягом 72 годин після пологів, відшарування плаценти, амніоцетозу, мимовільного викидня, аборту, позаматкової вагітності, переливання крові.
1.3 Методи визначення антигенів та антитіл .
