Колоректальный рак
| Вид материала | Документы |
- Колоректальный рак в генезе острой хирургической патологии органов брюшной полости, 36.52kb.
- Лекции и обзоры, 381kb.
- Тема : Колоректальный рак. Толстокишечные анастомозы Воробей, 90.82kb.
- Современные аспекты онкологии и возможности применения продуктов витамакс при злокачественных, 305.75kb.
- Рак молочной железы: вопросы-ответы, 70.08kb.
- Рак- мой личный враг, 3079.33kb.
- Предварительная программа VI конгресс Российского общества онкоурологов Москва, 5-7, 63.34kb.
- Методические указания для студентов 5 курса медицинских факультетов, 131.01kb.
- Когда предотвратить легче, чем лечить тревожная статистика каждую минуту только в России, 136.97kb.
- Рак тіла І шийки матки, рак яєчників. Актуальність теми, 133.38kb.
Колоректальный рак
Термин «колоректальный рак» (рак толстой кишки) используется для определения опухолей ободочной и прямой кишки.
Анатомически ободочная кишка включает в себя:
- слепую кишку с червеобразным отростком,
- восходящую ободочную кишку,
- печеночный изгиб,
- поперечную ободочную кишку,
- селезеночный изгиб,
- нисходящую ободочную кишку,
- сигмовидную кишку.
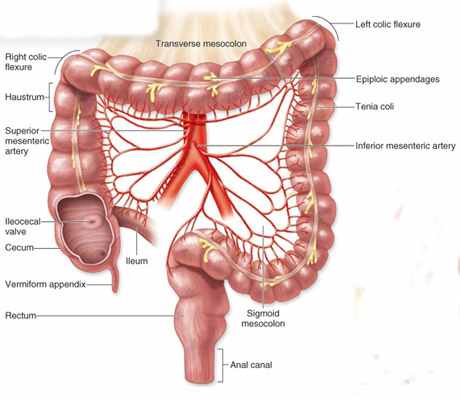
Конечный отдел прямой кишки – анальный канал.
Более 90% злокачественных опухолей толстой кишки – это различные виды аденокарцином. Типичным раком анального канала является плоскоклеточный (эпидермоидный).
Заболеваемость и смертность
В цивилизованных, экономически развитых странах колоректальный рак является одной из наиболее распространенных злокачественных опухолей. В структуре онкологической заболеваемости в мире колоректальный рак в настоящее время занимает четвертое место.
В Гомельской области заболеваемость колоректальным раком составила 39,8 на 100 тысяч населения, имеется неуклонный рост заболеваемости, 5 лет назад она составляла 34,5 на 100 000 населения.
Ежегодно в мире регистрируется около 800 тысяч вновь заболевших больных колоректальным раком, из них более половины (440 тысяч) умирает. При этом около 130 000 вновь заболевших приходится на США.
По смертности колоректальный рак занимает третье место (после рака легкого и желудка у мужчин, после рака молочной железы и желудка у женщин).
Наиболее высока заболеваемость раком толстой кишки в экономически развитых странах мира: США, Канада, Новая Зеландия, страны Западной Европы. В США, например, в штате Коннектикут заболеваемость раком ободочной кишки составляет 58,7 на 100 тысяч населения, прямой кишки – 28,8 на 100 тысяч населения. Для сравнения – в Африке (в г. Дакар, Сенегал) этот показатель составил для ободочной кишки 1,3, для прямой – 2,5.
Развитые страны несут огромные экономические потери в связи с высокой заболеваемостью колоректальным раком. Например, в США стоимость лечения больных колоректальным раком занимает в настоящее время второе место, составляя 6,5 млрд. долларов в год (первое место занимает рак молочной железы – 6,6 млрд. долларов в год).
Частота распределения рака толстой кишки
в различных сегментах следующая:
| Сегменты толстой кишки | Частота возникновения рака |
| Слепая и восходящая ободочная кишка | 27% |
| Поперечная ободочная кишка | 10% |
| Нисходящая и сигмовидная ободочная кишка | 36% |
| Прямая кишка и анальный канал | 19% |
| Другие локализации | 8% |
Предрасполагающие факторы заболевания
Риск развития колоректального рака в европейской популяции – 4–5%.
Это означает, что в течение жизни один из 20 человек заболевает раком этой локализации.
Одним из основных предрасполагающих факторов является характер питания населения.
Следующие диетические факторы повышают риск возникновения рака ободочной кишки:
- избыточное употребление животных жиров,
- употребление пищи с недостаточным содержанием растительной клетчатки,
- избыточное питание,
- употребление алкоголя (особенно пива).
Следующие факторы понижают риск возникновения колоректального рака:
- употребление пищи с высоким содержанием растительной клетчатки,
- витамины D и C, кальций.
Важными факторами риска являются генетические синдромы:
- семейный диффузный полипоз,
- синдром Пейтца–Егерса,
- синдром Гарднера,
- болезнь Тюрка и др.
Некоторые формы колоректального рака являются наследственными. К ним относится наследственный неполипозный колоректальный рак (синдром Lynch I и синдром Lynch II).
К предраковым заболеваниям толстой кишки относятся:
- единичные и множественные аденомы (полипы) толстой кишки,
- неспецифический язвенный колит,
- болезнь Крона.
Выявление полипов играет исключительно важную роль в предупреждении возникновения рака, так как рак толстой кишки чаще всего развивается из полипов.
Риск перерождения полипа толстой кишки в рак велик: при полипе размером менее 1 см – 1,1%, 1–2 см – 7,7%, более 2 см – 42%, в среднем – 8,7%.
К факторам риска также относятся:
- возраст пациента старше 50 лет,
- ранее перенесенный рак женских гениталий и молочной железы,
ранее перенесенный рак ободочной кишки.
TNМ клиническая классификация рака ободочной кишки
(6-е издание, 2002 год)
Т – первичная опухоль
|
N – регионарные лимфатические узлы
Регионарными лимфатическими узлами являются периколические, а также лимфатические узлы, располагающиеся вдоль подвздошно-ободочной, правой толстокишечной, средней толстокишечной, левой толстокишечной, сигмовидных и нижней мезентериальной артерий.
|
М – отдаленные метастазы
|
ГРУППИРОВКА ПО СТАДИЯМ
| Стадия 0 | TIS | N0 | M0 |
| Cтадия I | T1, T2 | N0 | M0 |
| Cтадия IIA | T3 | N0 | M0 |
| Cтадия IIB | T4 | N0 | M0 |
| Cтадия IIIA | Т1, T2 | N1 | M0 |
| Cтадия IIIB | T3, T4 | N1 | M0 |
| Cтадия IIIC | Любая T | N2 | M0 |
| Cтадия IV | Любая T | Любая N | M1 |
TNМ клиническая классификация рака прямой кишки
(6-е издание, 2002 год)
Т – первичная опухоль
- ТХ – недостаточно данных для оценки первичной опухоли.
- Т0 – первичная опухоль не определяется.
- Тis – преинвазивная карцинома (carcinoma in situ): интраэпителиальная инвазия или инвазия собственной пластинки слизистой оболочки.
- Т1 – опухоль инфильтрирует подслизистую основу.
- Т2 – опухоль инфильтрирует мышечную оболочку.
- Т3 – опухоль инфильтрирует подсерозную основу или параректальную клетчатку.
- Т4 – опухоль распространяется на другие органы или структуры и/или прорастает висцеральную брюшину.
-
Примечание: опухоль, макроскопически прорастающая в другие органы или структуры, классифицируются как Т4. Однако, если инвазия в соседние органы и структуры микроскопически не подтверждена, опухоль классифицируется как рТ3.
N – регионарные лимфатические узлы
Регионарными лимфатическими узлами являются периректальные, а также лимфатические узлы, располагающиеся вдоль нижней мезентериальной, прямокишечных и внутренней подвздошной артерий.
- NХ – недостаточно данных для оценки состояния регионарных лимфатических узлов.
- N0 – нет признаков метастатического поражения регионарных лимфатических узлов.
- N1 – метастазы в 1–3 регионарных лимфатических узлах.
- N2 – метастазы в 4 и более регионарных лимфатических узлах.
М – отдаленные метастазы
|
ГРУППИРОВКА ПО СТАДИЯМ
| Стадия 0 | TIS | N0 | M0 |
| Cтадия I | T1, T2 | N0 | M0 |
| Cтадия IIA | T3 | N0 | M0 |
| Cтадия IIB | T4 | N0 | M0 |
| Cтадия IIIA | Т1, T2 | N1 | M0 |
| Cтадия IIIB | T3, T4 | N1 | M0 |
| Cтадия IIIC | Любая T | N2 | M0 |
| Cтадия IV | Любая T | Любая N | M1 |
Современные принципы скрининга
колоректального рака
Своевременное выявление колоректального рака предполагает диагностику его на ранних, доклинических стадиях, когда отсутствуют всякие клинические проявления этого заболевания. Скрининг, или раннее выявление колоректального рака, проводится с помощью пальцевого обследования, эндоскопического метода и гемокульт-теста.
Около 70% всех раков прямой кишки выявляется при пальцевом исследовании прямой кишки. Вот почему является обязательным пальцевое обследование прямой кишки при профилактических осмотрах у гинеколога, уролога и врачей других специальностей, а у людей старше 40 лет оно обязано проводиться ежегодно.
Сигмоидоскопия и тотальная колоноскопия являются важными методами скрининга колоректального рака. Однако возможность использования этих методик для широкого скрининга представляется сомнительной из–за их большой сложности и высокой стоимости. Поэтому большинство онкологов рекомендуют ограничиться применением указанных методов обследования в первую очередь среди лиц, имеющих факторы повышенного риска возникновения колоректального рака.
Исследование кала на скрытую кровь (гемокульт-тест)является основным методом скрининга. Гемокульттест (гваяковая проба, модифицированная Грегором) был разработан в 60–х гг. ХХ века, к настоящему времени апробирован на миллионах людей. К основным достоинствам этого метода следует отнести простоту исследования и его относительную дешевизну.
Основанием для проведения указанного теста является то, что колоректальные аденомы и карциномы в той или иной степени кровоточат. При проведении скрининга среди формально здорового населения от 2 до 6% обследованных имеют положительный гемокульт–тест. При дальнейшем обследовании пациентов, имеющих положительный гемокульт–тест, колоректальный рак выявляется в 5–10%, а железистые аденомы – в 20–40% случаев. В 50–70% случаев тест бывает ложноположительным.
Клиническая картина
По клиническому течению удобно выделять рак правой половины ободочной кишки, рак левой половины ободочной кишки и рак прямой кишки и анального канала.
Для рака правой половины ободочной кишки (слепая, восходящая ободочная, печеночный изгиб) характерна следующая триада симптомов:
1) гипертермическая реакция (субфебрильная температура и выше);
2) слабость, анемия, похудание;
3) наличие пальпируемой опухоли в брюшной полости.
Для рака правой половины ободочной кишки характерен так называемый токсико-анемический синдром, длительное скрытое течение, симптомы кишечной непроходимости наступают поздно.
Для рака левой половины ободочной кишки (селезеночный изгиб, нисходящая ободочная, сигмовидная кишка) характерна другая триада признаков:
1) наличие патологических выделений из заднего прохода (кровянистых, слизистых, гнойных),
2) наличие кишечных расстройств (тенезмы, запоры, поносы или их чередование)
3) нарушение кишечной проходимости (хроническая или острая обтурационная кишечная непроходимость).
Для рака прямой кишки и анального канала характерна яркая клиническая симптоматика. Патологические выделения из заднего прохода – самый характерный симптом при этом заболевании.
1) Кровотечение из заднего прохода наблюдается у 75–90% всех больных. Выделение крови происходит чаще с калом при дефекации. Реже наблюдаются слизь и гной в кале.
2) Расстройство функции кишечника: запоры, поносы или их че- редование.
3) Тенезмы – частые ложные позывы на низ, до 15–20 раз в сутки. Здесь необходимо проводить дифференциальный диагноз с дизентерией, больные с этими симптомами часто попадают в инфекционную больницу.
4) Боли в заднем проходе при дефекации, а в запущенных стадиях – вне связи с ней, постоянно.
5) Общие проявления: анемия, похудание, плохой аппетит, слабость, землистый цвет кожи – в начальных стадиях рака прямой кишки бывают редко, характерны для уже запущенных форм.
Диагностика
Алгоритм обследования при колоректальном раке включает в себя следующие методы исследования и в такой последовательности:
1. Пальцевое исследование per rectum и per vaginam. Оно позволяет выявить 70% всех ректальных карцином и определить степень их местного распространения.
2. Ректороманоскопия. Жестким ректоскопом возможно осмотреть до 30 см дистального отдела толстой кишки, то есть анальный канал, всю прямую кишку и дистальный отдел сигмовидной кишки. При этом необходима биопсия подозрительных патологических образований с целью их морфологического исследования.
3. Ирригоскопия. Использование бариевой клизмы, с двойным контрастированием (с воздухом) позволяет исследовать рельеф слизистой толстой кишки, выявляя практически все колоректальные раки и подавляющее число полипов размером более 1 см. До сих пор бытует метод обследования толстой кишки введением бария per os. Это методологически порочное исследование часто дает неверные результаты и должно быть решительно осуждено.
4. Фиброколоноскопия. Гибким колоноскопом с волокнистой оптикой возможно осмотреть все отделы толстой кишки, от ануса до баугиниевой заслонки, выявить не только рак, но и небольшие полипы, произвести биопсию всех подозрительных участков.
5. УЗИ. Применяется с целью оценки распространённости процесса, выявления отдалённых и регионарных метастазов.
Таковы основные методы обследования толстой кишки при подозрении на колоректальный рак. Все остальные методы: КТ, МРТ, ангиография, радионуклидное исследование, лапароскопия, определение РЭА и других маркеров – являются дополнительными методами исследования, применяются по особым показаниям в специализированных учреждениях для уточнения степени распространенности опухолевого процесса.
Лечение
Единственным радикальным методом лечения колоректального рака является хирургический. При раке правой половины ободочной кишки операция выполняется в объеме правосторонней гемиколэктомии, при раке левой половины – левосторонняя гемиколэктомия. При небольших опухолях сигмовидной кишки возможна резекция сигмовидной кишки. При выполнении этих операций обязательным является удаление всех регионарных лимфоузлов по ходу магистральных питающих сосудов:
a.ileocolica, a. colica dextra, a. colica media, a. mesenterica inferior, что должно сопровождаться высокой перевязкой этих сосудов.
При опухолях, локализующихся в ректосигмоидном и верхнеампулярном отделе прямой кишки, операцией выбора является чрезбрюшная (или передняя) резекция прямой кишки. При раке среднеампулярного отдела прямой кишки операцией выбора является брюшноанальная резекция прямой кишки с низведением в анальный канал сигмовидной и других отделов ободочной кишки.
При раке нижнеампулярного отдела прямой кишки и анального канала обычный объем операции – брюшнопромежностная экстирпация прямой кишки с формированием одноствольной сигмостомы в левой подвздошной области.
Лучевая терапия
Дальнейшее улучшение отдаленных результатов лечения рака прямой кишки возможно при применении комбинированных методов лечения, включая лучевую и химиотерапию. При операциях по поводу рака прямой кишки общепринятой во всех передовых клиниках мира является предоперационная лучевая терапия. По стандартной методике она проводится коротким курсом по 5 Гр ежедневно, 5 сеансов, в СОД=25 Гр.
Химиотерапия
Колоректальный рак является относительно резистентной к воздействию цитостатиков опухолью. В течение длительного времени единственными препаратами, активными при этой форме злокачественных опухолей оставались 5–фторурацил и его производные. В 90–х гг. ХХ века в онкологическую практику вошли принципиально новые препараты, обладающие противоопухолевой активностью при колоректальном раке: иринотекан, производное платины III поколения оксалиплатин, ралтитрексид, а также новые пероральные фторпиримидины – UFT и капецитабин.
Клиническое изучение этих препаратов показало, что их использование в составе лекарственных комбинаций позволяет повысить общую эффективность химиотерапии больных колоректальным раком и увеличить их шансы на продление жизни. Исследования показали, что медиана выживаемости больных метастатическим колоректальным раком при чисто симптоматической терапии составляла лишь 8 мес., при химиотерапии с использованием комбинации 5–фторурацила с лейковарином увеличилась до 12 мес. Применение адъювантной химиотерапии целесообразно после радикальных операций по поводу рака ободочной кишки при обнару- жении в удаленном препарате метастазов в регионарных лимфоузлах. Применение адъювантной химиотерапии в том или ином варианте (5–фторурацил с лейковарином, как общепринятый «золотой стандарт», оксалиплатин, иринотекан и др.) позволяет значительно улучшить результаты радикальных операций при раке ободочной кишки.
Отдаленные результаты лечения
Отдаленные результаты лечения после радикальных операций при колоректальном раке зависят от стадии процесса. При стадии за- болевания по Dukes А и В (I и II а стадии по отечественной классифи- кации) 5–летняя выживаемость составляет 80%, 10–летняя – 74%; при стадии Dukes C (III б стадия) 5–летняя выживаемость составляет 46%, 10–летняя – 36%; при стадии Dukes D (IV стадия) 5–летняя вы- живаемость составляет 5,4%, 10–летняя – 5%.
Таким образом, улучшение результатов лечения колоректального рака определяется ранней диагностикой, своевременным адекватным лечением и применением комбинированных методов лечения.
