Габдулхакова Раиля Мунировича. Отправитель: Ученый секретарь диссертационного совета профессор Лазишвили Гурам Давидович автореферат диссертации
| Вид материала | Автореферат диссертации |
СодержаниеРезультаты исследования 2. Тяжесть состояния, причины смерти. Структура и особенности 3. Прогнозирование исходов при сочетанной травме Apache ii Apache ii Аpache ii |
- Гусаима Александра Борисовича. Отправитель: Ученый секретарь диссертационного совета, 580.12kb.
- Сквозновой Татьяны Михайловны. Отправитель: Ученый секретарь диссертационного совета, 864.64kb.
- Автореферат диссертации на соискание ученой степени, 406.83kb.
- Автореферат диссертации на соискание ученой степени, 370.58kb.
- Автореферат диссертации на соискание ученой степени, 375.62kb.
- Автореферат диссертации на соискание ученой степени, 487.74kb.
- Автореферат диссертации на соискание учёной степени, 489.45kb.
- Автореферат диссертации на соискание ученой степени, 602.44kb.
- Автореферат диссертации на соискание ученой степени, 521.35kb.
- Автореферат диссертации на соискание ученой степени, 813.51kb.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
- Эпидемиология сочетанной травмы
Эпидемиологию сочетанной травмы изучали по результатам обследования 455 пострадавших. Сочетанные повреждения наблюдаются среди населения преимущественно работоспособного возраста (73,4%), и в основном мужчин - 61% (χ²=43,9; р<0,001 в сравнение с женским полом). Среди госпитализированных доминировали рабочие и служащие (50,3%), значительную прослойку составили пенсионеры (26,6%), доля неработающих составила 11,4%, частных предпринимателей - 7,9%, студентов и учащихся - 3,7%. Каждый третий пострадавший поступил в состоянии алкогольного опьянения.
В структуре пострадавших при дорожно-транспортной травме в мегаполисе в преобладающей степени доминировали пешеходы - 81,5% (χ²=213,3; р=0,0005 в сравнение с водителями и пассажирами). Если средний возраст водителей составил 36,6±9,44 лет, то пешеходы на 13,8 лет были старше (F=19,6; р=0,0001), при этом среди пешеходов отмечались более высокие баллы по шкалам APACHE II, МODS и летальность на 10,4% была выше (хотя и статистически не значимая) в сравнение с водителями. В мегаполисе среди пострадавших в результате падений с большой высоты значительную долю (32,5%) составляли суициды.
адений с большшй высоты 29,3% составляют суицидыЧастота госпитализаций для всей когорты достоверно различается по временам года (χ²=9,69; df=3; р=0,021). Наибольшее количество поступлений отмечается осенью - 27,9% (19,8%) (χ²=7,84; df=1; р=0,005 в сравнение с весной) наименьшее весной - 19,8%. При ДТП периодичность госпитализаций различалась в значительной степени (χ²=21,9; df=3; p=0,0001): наибольшее число пострадавших поступило в осенний период - 35,4% (χ²=14,7; p=0,0001 в сравнение с весной) и наименьшее весной - 20,3%. При кататравме для всей когорты посезонно периодичность госпитализации так же статистически различается (χ²=21,1; df=3; p=0,0001): возрастает в летний период - 35,8% и снижается осенью – 13% (χ²=17,6; p<0,001). При умышленной травме для всей когорты не отмечается статистически значимых различий (χ²=4,9; df=3; p=0,178).
При анализе частоты госпитализаций по месяцам в течение года так же отмечаются достоверные различия (χ²=42,9; df =11; p<0,001). Наибольшее количество (34,3% от всех пострадавших) госпитализировано в январе, октябре и июне, когда среднемесячная госпитализация возрастала в 1,6 раза (χ²=32,1; p=0,0005 в сравнение с среднемесячной госпитализацией в остальные месяцы).
Пик госпитализаций от ДТП приходится на октябрь, ноябрь, когда их количество возрастало в 2-3 раза (χ²=50,8; p=0,0005 в сравнение с среднемесячной госпитализацией в остальные месяцы). Наибольшее количество кататравм приходится на январь июнь, август месяцы, когда их число возрастает в 2-3 раза (χ²=6,8; p=0,001 в сравнение с среднемесячной госпитализацией в оставшиеся месяцы). Количество умышленных травм увеличивается в мае, июне (χ²=5,2; p=0,023).
При анализе числа госпитализаций по дням недели выявлено, что наибольшее их количество приходилось на пятницу, субботу и наименьшее – вторник, четверг (χ²=14,1; df=6; p=0,007). Пик госпитализаций от ДТП приходился на пятницу и понедельник, когда поступило 35,4% (χ²=8,5; p=0,004 в сравнение с вторником и четвергом) от всего количества пострадавших в результате ДТП; при кататравме на пятницу-субботу- 37,4% (χ²=4,3; p=0,039 в сравнение с вторником и четвергом); умышленной травме понедельник, пятницу - 41,4% (χ²=3,3; p=0,071 в сравнение с вторником и четвергом).
При исследовании периодичности госпитализаций в течение суток для всей когорты выявлены статистически значимые различия (χ²=57,3; df=3; p<0,001): наибольшее количество госпитализаций отмечалось в период с 06 ч. 00 мин. до 11 ч. 59 мин. – 26,6 % (χ²=15,9; p=0,0006 в сравнение с промежутком времени 00 ч.- 05 ч. 59 мин.) и особенно, в период с 18 ч. 00 мин. по 23 ч. 59 мин. - 36,5 % (χ²=50,4; p=0,0005 в сравнение с промежутком времени 00 ч. - 05 ч. 59 мин.). Число госпитализаций от ДТП в эти промежутки времени также было наибольшим и составляло в период с 06 ч. 00 мин. до 11 ч. 59 мин. - 26,9% (χ²=13,9; p=0,0008 в сравнение с промежутком времени 00 ч. – 05 ч. 59 мин.) и с 18 ч. 00 мин. по 23 ч. 59 мин. - 37,6% (χ²=39,6; p=0,0005 в сравнение с промежутком времени 00 ч. - 05 ч. 59 мин.). При кататравме наибольшее число госпитализаций отмечалось в промежутке времени 21ч. 00 мин. – 02 ч. 59 мин., составляя соответственно 35,3% (χ²=12,5; p=0,0005 в сравнение с промежутком времени 03 ч. 00 мин. – 08 ч. 59 мин.). При умышленной травме наибольшее число пострадавших госпитализировано в ночное и утреннее время в промежутке от 21 ч. 00 мин. до 08 ч. 59 мин. – 82,8% (χ²=22,4; p<0,001 в сравнение с промежутком времени 09 ч. 00 мин. – 20 ч. 59 мин.).
Как видно из вышеизложенного число госпитализаций возрастает в 1,5-2 раза в октябре, январе, июне в пятницу, субботу в промежутке времени между 18.00 и 24.00 часами.
Таким образом, прослеживается закономерность поступления пострадавших с тяжелой сочетанной травмой по временам года, месяцам, дням недели, часам в течение суток, что позволяет организовать работу бригад скорой медицинской помощи, стационаров в режиме ожидания, проводить упреждающую профилактическую работу.
2. Тяжесть состояния, причины смерти. Структура и особенности
формирования синдрома полиорганной дисфункции
Из всей когорты пострадавших, госпитализированных в исследуемый промежуток времени 27 человек (5,9%) погибли в первые 3 часа с момента поступления в стационар ввиду наличия у них крайне тяжелых несовместимых с жизнью повреждений. Показатели, характеризующие тяжесть травмы, выраженность органных дисфункций при поступлении с использованием различных систем среди 428 пострадавших, проживших три и более часов представлены в таблице 2. Статистически значимые различия среди выживших
Таблица 2
Основные показатели, характеризующие тяжесть состояния при поступлении выживших и умерших больных (n= 428), MSD.
| Показатель | Все пострадавшие (n=428) | Выжившие (n=289) | Умершие (n=139) |
| Возраст (годы) | 45,8±17,9 | 45,6±14,0 | 46,1±16,5 |
| Догоспитальное время (мин) | 52,7±32,1 | 50,4±21,5* | 56,4±30,1 |
| АIS (баллы) | 9,77±4,50** | 8,08±3,33*** | 13,3±4,57 |
| ЦИТО-1 (баллы) | 9,3±4,71** | 7,41±3,22*** | 13,1±4,97 |
| СПб НИИ скор. пом. (баллы) | 6,94±4,83** | 4,91±3,10*** | 11,1±5,06 |
| ISS (баллы) | 23,4±16,1** | 15,5±7,89*** | 39,8±16,4 |
| NISS (баллы) | 26,7±15,0** | 19,8±8,25*** | 41,1±15,6 |
| PTS (баллы) | 26,0±4,71** | 19,0±7,79*** | 40,3±15,0 |
| RTS (баллы) | 6,17±1,663** | 6,99±0,978*** | 4,14±1,74 |
| APACHE II (баллы) | 16,5±9,32** | 12,1±6,51*** | 25,6±7,54 |
| SAPS II (баллы) | 36,5±19,1** | 26,9±12,3*** | 56,6±14,6 |
| LODS (баллы) | 4,56±4,14** | 2,44±2,18*** | 8,76±3,92 |
| MODS (баллы) | 5,47±4,29** | 3,3±2,64*** | 9,97±3,58 |
| SOFA (баллы) | 6,29±3,80** | 4,26±1,95*** | 10,5±3,25 |
| GCS (баллы) | 11,3±2,85** | 12,7±1,81*** | 8,32±2,74 |
Примечание: * р<0,05; ** р<0,01; *** р<0,001 по сравнению с умершими
и умерших наблюдались по догоспитальному времени (F=5,28; р=0,022), а так же системам оценки тяжести состояния (р<0,001).
Оценка тяжести состояния, выраженность органных дисфункций, летальность в зависимости от тяжести травмы по шкале ISS представлена в таблице 3. Как видно из данной таблицы при ISS=30-45 баллов летальность превысила 50%, а при ISS>45 выжили лишь два из десяти пострадавших.
Таблица 3
Тяжесть состояния, выраженность органных дисфункций (баллы), летальность в различных группах больных (n= 428), MSD
| ISS, баллы | Система оценки тяжести, баллы | Леталь- ность, % | |||||
| AIS | ISS | APA- CHE II | SAPS II | LODS | MODS | ||
| До 15 (n=81) | 5,03 ±0,97 | 11,0 ±2,87 | 9,5 ±5,50 | 19,2 ±10,3 | 1,27 ±1,61 | 1,67 ±1,41 | 2,3 |
| 16-29 (n=178) | 9,61 ±2,33 *** | 22,9 ±4,31 *** | 12,7 ±6,51 *** | 28,2 ±12,3 *** | 2,69 ±2,25 *** | 3,88 ±2,66 *** | 14,0 ** |
| 30-45 (n= 86) | 13,1 ±4,01 *** | 37,3 ±6,77 *** | 22,1 ±8,14 *** | 49,7 ±18,1 *** | 7,64 ±3,54 *** | 8,31 ±3,35 *** | 52,3 *** |
| >45 (n=83) | 16,2 ±4,09 *** | 53,7 ±12,9 *** | 28,1 ±6,68 *** | 60,1 ±11,6 *** | 9,67 ±4,42 *** | 11,4 ±3,72 *** | 81 *** |
Примечание: ** р<0,01; *** р<0,001 по сравнению с ISS до 15 баллов.
Тяжесть травмы, выраженность системных расстройств при поступлении обусловили высокую летальность (36,5%). Кривая 28 суточной выживаемости представлена на рис.1.
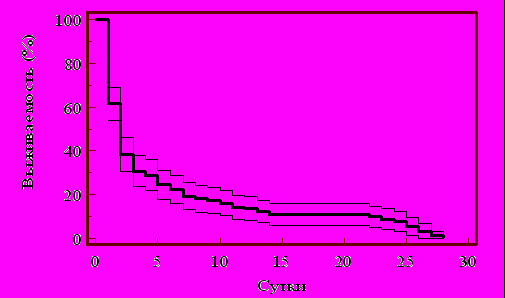
Рис. 1. Кривая 28 суточной выживаемости Каплан-Мейера и её 95% ДИ
В указанный промежуток времени умерли 149 (89,8%) пациентов. Медиана выживаемости составляла 2 суток (в течение первых 48 часов погибло 96 человек, что составило 57,8% от всех умерших). Из рисунка мы констатируем, что пик летальности приходится в первые трое суток, и второй незначительный подъем наблюдался на 3-4-ой неделе после травмы. Подавляющее большинство пострадавших (65,5% от всех умерших) погибает в первые трое суток (таблица 4). Причинами смерти в первые трое суток в 65,7% случаев явилась острая массивная кровопотеря, 18,5% отек, дислокация головного мозга, 10,2% жировая эмболия, 5,6% пневмония. Основной причиной смерти в более поздние сроки явились гнойно-септические осложнения (77,6%).
Таблица 4
Структура причин летальных исходов в различные сроки (n=166).
| Причины смерти | Летальность в различные сроки после травмы, %, | ||||
| До 3 ч. | 3-24 ч. | 1-3 сут. | >3 сут. | В целом | |
| Острая кровопотеря, СПОН | 92,6*** | 75,8** | 43,8 | - | 42,8 |
| Отек, дислокация головного мозга | 7,4 | 18,2 | 25,0 | 5,2 | 13,9 |
| Жировая эмболия | - | 6,1 | 18,8 | 6,9 | 9,0 |
| Пневмония, интоксикация | - | - | 12,5 | 13,8 | 8,4 |
| Сепсис | - | - | - | 63,8*** | 22,3 |
| О язвы | - | - | - | 6,9 | 2,4 |
| Тромбоэмболия | - | - | - | 3,4 | 1,2 |
| Всего умерло, абс. | 27 | 33 | 48 | 58 | 166 |
Примечание: ** р<0,01; *** р<0,001 по сравнению с группой в целом
Наиболее часто встречаемыми синдромами органных дисфункций по шкале MODS были: дисфункция ЦНС, респираторная и сердечно-сосудистая дисфункции, шоковый синдром диагностирован у 59,3% пострадавших (рис. 2). С увеличением количества пораженных органов и систем возрастает летальность. Так, если среди пострадавших с 1-4 баллами по шкале MODS летальность составила 5%; 5-8 баллами 27,4-%, при 9-12 баллах достигла 71%, а при 13 и более составила 100%. Летальность в зависимости от тяжести органной дисфункции представлена в таблице 5. Как видно из представленного, наибольший относительный вклад в структуру тяжелой полиорганной дисфункции и летальность внесли дисфункции ЦНС, сердечно-сосудистой, дыхательной систем, гемостаза.
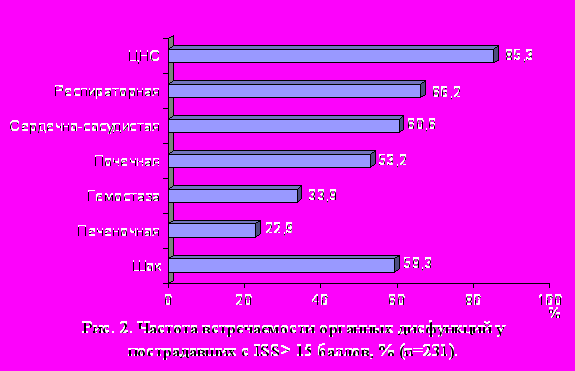
Таблица 5
Структура и летальность в зависимости от тяжести органной дисфункции у пострадавших с ISS > 15 баллов (n=231), %.
| Орган/ Система | Показатель | Количество баллов | ||||
| 0 | 1 | 2 | 3 | 4 | ||
| ЦНС | Доля, % | 14,8 | 36,5 | 30,7 | 13,9 | 4,3 |
| Лет-ть, % | 2,9 | 4,8 | 28,2 | 64,5 | 91 | |
| Сердечно- сосудистая | Доля, % | 39,4 | 35,7 | 11,3 | 10,4 | 3,5 |
| Лет-ть, % | 9,9 | 13,4 | 44,4 | 69,6 | 87,5 | |
| Респираторная | Доля, % | 33,8 | 38,5 | 17,7 | 6,1 | 3,9 |
| Лет-ть, % | 2,6 | 18,0 | 46,3 | 71,4 | 88,9 | |
| Почки | Доля, % | 46,8 | 39,4 | 9,6 | 2,61 | 1,74 |
| Лет-ть, % | 14,8 | 26,4 | 40,9 | 50,0 | 75,0 | |
| Гемостаза | Доля, % | 66,2 | 18,2 | 11,3 | 3,9 | 0,4 |
| Лет-ть, % | 13,7 | 31,0 | 50,0 | 77,8 | 100 | |
| Печень | Доля, % | 77,1 | 20,3 | 1,74 | 0,87 | - |
| Лет-ть, % | 21,9 | 25,5 | 60 | 100 | - | |
Наибольшее число баллов MODS отмечается в 1-е сутки, при этом среди умерших оно почти в 2 раза выше (F=100,4; р<0,001), чем среди выживших (таблица 6). На вторые сутки количество баллов среди выживших снижается в 2,2 раза (F=73,2; р<0,001 ), тогда как среди умерших всего на 18,1% (F=7,57; p=0,007). К 3-м суткам у выживших количество баллов по шкале MODS снижается в 4 раза (F =96,9; df=2; p<0,001), умерших на 14,7% (F=3,49; df=2; p=0,033) по сравнению с 1-ми сутками, то есть крутизна снижения количества баллов MODS значительно более выражена в группе выживших.
Таблица 6
Динамика изменений количества баллов по шкале MODS в первые трое суток после травмы.
| Показатель | Дата с момента госпитализации, сутки | ||
| 1 | 2 | 3 | |
| Выжившие MODS, баллы (n=176) | 3,79 ±2,63*** | 1,72 ±1,84*** | 0,94 ±1,23*** |
| Умершие MODS, баллы (n=55) | 7,96 ±2,89 | 6,52 ±2,59 | 6,82 ±3,49*** |
***р<0,001 по сравнению с первыми сутками, ___ подчеркивание р<0,001 по сравнению с умершими
Таким образом, при тяжелой сочетанной травме наибольшее количество баллов шкале MODS отмечается при поступлении в ОРИТ и упорство проявлений ПОД в последующие сроки является важным признаком неблагоприятного исхода.
Для определения информационной ценности динамического исследования количества баллов MODS в предсказании летального исхода нами проведены ROC и логистический регрессионный анализы (таблица 7). Мы
Таблица 7
Информационная способность в предсказании летального исхода изменяющегося в динамике количества баллов по шкале MODS (n=231).
| Показатель | Срок исследования, сутки | ||
| 1 | 2 | 3 | |
| AUROC | 0,850 (0,787-0,893) | 0,937 *** (0,898-0,965) | 0,973 *** (0,943-0,990) |
| Точка разделения | >4 | >4 | >4 |
| Чувствительность | 44,4 | 62,9 | 88,9 |
| Специфичность | 95,6 | 95,5 | 95,5 |
| Безошибочность | 83,5 | 87,8 | 93,9 |
| Коэффициент регрессии | 0,48 ±0,07 | 0,88 ±0,12 | 1,49 ±0,25 |
| р | <0,001 | <0,001 | <0,001 |
| OШ (95%ДИ) | 1,62 (1,41-1,85) | 2,41 (1,91-3,06) | 4,45 (2,75-7,21) |
***р<0,001 в сравнение с первыми сутками
сопоставили количество баллов MODS в 1,2,3-и сутки c летальным исходом. Полученные данные показывают, что AUROC и чувствительность шкалы MODS в предсказании летального исхода в динамике возрастают: так прогрессирование MODS приводит к увеличению шанса летального исхода на вторые сутки в 2,41, третьи 4,45 раза.
Таким образом, логистический регрессионный и ROC анализы позволили нам выявить, что увеличивающееся в динамике количество баллов MODS имеет большее прогностическое значение, нежели число баллов при поступлении в ОРИТ.
Безусловно, представляет важный научно-практический интерес вопрос о том, в какой степени та или иная органная дисфункция влияют на исход. Согласно проведенного нами логистического регрессионного анализа определяющими гибель пациентов были дисфункция ЦНС (p<0,001), ССД (p<0,001), количество органов с дисфункцией (p<0,001), ОРД (p<0,01), дисфункция гемостаза (p<0,01) (таблица 8).
Таблица 8
Взаимосвязь между органной дисфункцией и госпитальной смертью
| Система/Орган | Коэффициент регрессии | р | ОШ (95%ДИ) |
| Респираторная | 0,67±0,24 | 0,0053 | 1,95 (1,22-3,12) |
| Сердечно-сосудистая | 1,20 ± 0,22 | 0,0001 | 3,31(2,16-5,07) |
| ЦНС | 1,87 ± 0,28 | 0,0001 | 6,47 (3,83-10,93) |
| Почечная | 0,42± 0,23 | 0,066 | 1,53 (0,97-2,40) |
| Гемостаза | 1,033± 0,38 | 0,0064 | 2,81(1,34-5,90) |
| Печеночная | 0,649± 0,623 | 0,297 | 1,91(0,56-6,49) |
| Количество органов | 1,21± 0,19 | 0,0001 | 3,36 (2,30-4,91) |
Причинами гибели пострадавших через 7 суток после травмы были дисфункция ЦНС (n=169; bk=1,61±0,33; р<0,001; ОШ=5,01 (95%ДИ=2,64-9,49); количество органов с дисфункцией (n=144; bk=0,99±0,20; р<0,001; ОШ=2,68 (95%ДИ=1,80-4,01), респираторная (n=124; bk=0,97±0,39; р=0,001; ОШ=2,64 (95%ДИ=1,48-4,73), сердечно-сосудистая (n=113; bk=0,90±0,25; р=0,0003; ОШ=2,45 (95%ДИ=1,51-3,97) и печеночная дисфункции (n=44; bk=1,55±0,72; р=0,032; ОШ=4,73 (95%ДИ=1,14-19,5), но не почечная (р=0,145) и системы гемостаза (р=0,239). Как видно из представленного, через 1 неделю изменилась структура относительного вклада органных дисфункций в развитие риска летального исхода: по-прежнему остается высокой значимость дисфункции ЦНС и возрастают в 1,35 раза значимость респираторной и в 2,4 раза печеночной дисфункций.
Таким образом, наибольший относительный вклад в развитие летального исхода при сочетанной травме вносят количество органных дисфункций, дисфункции ЦНС, сердечно-сосудистой системы, гемостаза, а к концу первой недели возрастают значимость респираторной и печеночной дисфункций.
Шоковый синдром диагностирован у 59,3% пострадавших. Степень тяжести шокового синдрома наиболее тесно коррелировала с индексом тяжести травмы (р<0,001), количеством баллов по MODS (р<0,001), APACHE II (р<0,001), SAPS II (р<0,001), объёмом перелитой в первые сутки эритроцитарной массы (р<0,001). При этом наиболее сильная связь отмечалась с количеством баллов по шкале MODS. По всей видимости, в реализации ПОД при тяжелой травме одно из центральных мест занимает шоковый синдром.
С целью изучения особенностей реализации ПОД при шоковом синдроме нами исследована взаимосвязь его тяжести с синдромами органных дисфункций. Наблюдалась тесная связь со степенью тяжести респираторной, сердечно-сосудистой, гематологической, почечной, церебральной дисфункций, причем наиболее сильная связь отмечалась с респираторной дисфункцией (р<0,001).
Длительность шокового синдрома составила 1,5±0,68 суток, то есть на вторые сутки, как правило, удавалось его купировать.
Таким образом, проведенные исследования показывают, что наиболее ранними синдромами органной дисфункции являются респираторная, сердечно-сосудистая и дисфункция ЦНС. Учитывая установленное наличие шокового синдрома у 59,3% больных, в большинстве случаев сценарий реализации МОД на наш взгляд выглядел следующим образом: Шок – ССД – ОРД -Дисфункция ЦНС - Поч.Д – ГД -Печ.Д. Шоковый синдром и ССД, как правило, на вторые сутки удается коррегировать, и причиной дальнейшей манифестации ПОД являются дисфункция ЦНС, ОРД.
Наиболее поздним компонентом ПОД были острые язвы желудка и тонкого кишечника с кровотечениями- 3,96%. Присоединение данного осложнения сопровождалось высокой летальностью (83,3%).
Синдром острой жировой эмболии развился у 10,5% пострадавших в 1-3 –и сутки (1,7±0,8 сут.). Прослеживалась зависимость частоты синдрома острой жировой эмболии от тяжести травмы (при ISS до 15 баллов у 2,6%, при ISS 16-29 баллов 10,7%, ISS>=30 у 14,5% пострадавших). У 93% пострадавших была закрытая травма трубчатых костей, средний возраст составил 40,5±10,7 года. Летальность среди больных с синдромом жировой эмболии составила 35%.
Из 279 больных с ISS>15 баллов находившихся в ОРИТ более 48 часов у 171 (61,3%) наблюдалось 199 случаев гнойно-септического осложнения, среди них у 47,7% отмечались лёгочные осложнения (пневмонии, плевриты, трахеобронхиты). Тяжелый сепсис развился у 16,8% пострадавших, причиной его развития у 81,0% была пневмония, 12,8% нагноения ран мягких тканей, 6,4%- перитонит. Летальность у больных с данным осложнением составила 68,1%.
У 3,1% пациентов развился делирий. Как правило, он наблюдался у лиц злоупотребляющих алкоголем.
Таким образом, главными факторами, определившими исход травмы, явились тяжесть травмы и выраженность ПОД.
3. Прогнозирование исходов при сочетанной травме
Безусловно, прогнозирование возможной вероятности летального исхода позволяет определить стратегию лечения пострадавшего. Для решения поставленной в работе задачи нами последовательно изучены информационная ценность наиболее часто применяемых в клинической практике анатомо-морфологических систем оценки тяжести травмы, интегральных систем оценки тяжести состояния, а так же систем количественной оценки вероятности летального исхода. Проспективные исследования проведены у 295 пострадавших, находившихся в ОРИТ более 48 часов.
При исследовании прогностической ценности анатомо-морфологических систем оценки тяжести травмы нами выявлена их низкая чувствительность в прогнозировании летального исхода (таблица 9). Так чувствительность системы
Таблица 9
Прогностическая значимость систем оценки тяжести травмы (n=295).
| Система | Точка разделе-ния (баллы) | Чувстви-тельность, % | Специ-фич-ность, % | AUROC (95% ДИ) |
| AIS | >8 | 10,7 | 97,5 | 0,740 (0,686-0,789) |
| ЦИТО 1 | >7 | 25,0 | 96,7 | 0,755 (0,702-0,803) |
| СПб НИИ скорой пом. | >4,3 | 25,0 | 98,3 | 0,761 (0,708-0,808) |
| NISS | >27 | 46,4 | 97,5 | 0,871 (0,828-0,907) |
| ISS | >25 | 39,3 | 97,5 | 0,866 (0,821-0,902) |
| PTS | >23 | 31,1 | 95,8 | 0,799 (0,749-0,843) |
AIS-90 составила 10,7%, ЦИТО-I и Санкт-Петербургской НИИ скорой помощи -25%, PTS-31,1%; ISS-39,3%. Виду их низкой чувствительности предложенные системы оценки тяжести травмы не пригодны для прогнозирования вероятности исхода в каждом конкретном случае, а позволяют лишь проводить стратификацию пострадавших в зависимости от риска летального исхода.
При изучении информационной ценности интегральных систем оценки тяжести состояния нами выявлено, что наибольшей чувствительностью и безошибочностью в предсказании летального исхода в первые сутки, среди исследованных систем, обладает методика SAPS II (таблица 10).
Динамическая оценка количества баллов органных дисфункций так же имела большую прогностическую ценность, так чувствительность системы MODS увеличивалась с 42,9% в первые сутки до 84,7% на третьи, безошибочность соответственно с 86,4 до 94,5%.
При количественной оценке вероятности летального исхода в 1-е сутки с использованием специальных прогностических модельных систем TRISS, ASCOT выявлена их удовлетворительная дискриминационная способность, а так же отсутствие различий прогнозируемой летальности от фактической (p>0,05) (таблица 11). Оценка прогноза с использованием динамической системы 24-hour ICU Trauma Score производилась в начале 2-х суток, с учетом проводимой инфузионно-трансфузионной терапии, церебральных и дыхательных нарушений. Данная методика показала хорошую дискриминационную способность (AU ROC>0,9), а прогнозируемая летальность не отличалась от фактической.
Таблица 10
Прогностическая значимость систем оценки тяжести состояния.
| Показа- тель | Точка раз-деления (баллы) | AU ROC (95% ДИ) | Чувстви-тельность, % (95% ДИ) | Специфич-ность, % (95% Д И) | Безоши- бочность, % | ||
| До 24 часов (n=295). | |||||||
| APACHE II | >15 | 0,861 (0,816-0,898) | 39,3 (29,6-47,2) | 95,8 (93,6-97,7) | 85,1 | ||
| SAPS II | >39 | 0,887 (0,846-0,921) | 60,7 (50,2-69,1) | 94,9 (92,6-97,0) | 88,5 | ||
| RTS | <5,967 | 0,870 (0,826-0,906) | 42,9 (34,1-47,7) | 98,3 (96,3-99,5) | 87,8 | ||
| Glasgow | <11 | 0,898 (0,859-0,931) | 53,6 (42,9-62,5) | 94,1 (91,7-96,3) | 86,4% | ||
| LODS | >3 | 0,869 (0,825-0,905) | 50,1 (39,6-58,5) | 95,0 (92,6-97,0) | 86,4 | ||
| SOFA | >5 | 0,861 (0,818-0,906) | 44,7 (34,8-52,2) | 96,3 (94,0-98,0) | 86,4 | ||
| MODS | >4 | 0,859 (0,814-0,896) | 42,9 (33,3-50,0) | 96,7 (94,4-98,4) | 86,4 | ||
| >24 часов (n=295). | |||||||
| LODS | >1 | 0,899 (0,859-0,931) | 53,6 (43,7-60,7) | 96,7 (94,4-98,3) | 88,5 | ||
| SOFA | >3 | 0,939 (0,905-0,963) ** | 62,6 (52,4-69,9) | 96,3 (93,9-98,0) | 89,8 | ||
| MODS | >3 | 0,937 (0,903-0,962) ** | 60,7 (50,8-67,7) | 96,7 (94,4-98,3) | 89,8 | ||
| >48 часов (n=291) | |||||||
| LODS | >1 | 0,908 (0,869-0,939) | 57,7 (47,2-65,2) | 96,7 (94,4-98,3) | 89,7 | ||
| SOFA | >3 | 0,974 (0,949-0,989) *** | 80,8*** (72,4-84,0) | 99,2 (97,4-99,9) | 95,9 | ||
| MODS | >3 | 0,972 (0,946-0,988) *** | 84,7*** (74,9-91,2) | 96,7 (93,5-98,5) | 94,5 | ||
** p<0,01; *** p<0,001 по сравнению со счетом до 24 ч.;
подчеркивание - p<0,05 в сравнение со счетом > 24 ч.
Таблица 11
Прогнозируемая летальность, стандартизированное отношение смерти и площадь под кривой операционных характеристик при оценке прогноза.
| Методика | n | Летальность, % | СОС | AU ROC (95% ДИ) | |
| Факти- ческая | Прогнозируемая (95% ДИ) | ||||
| TRISS | 295 | 19 | 15,6 (12,8- 18,3) | 1,22 | 0,89 (0,85-0,92) |
| ASCOT | 295 | 19 | 23,9 (20,7-27,2) | 0,80 | 0,88 (0,85-0,91) |
| 24-hour ICU Trauma Score | 295 | 19 | 18,3 (15,8- 20,8) | 1,04 | 0,91 (0,88-0,93) |
| APACHE II | 295 | 19 | 23,6 (21,3-25,8) | 0,82 | 0,86 (0,82-0,90) |
| SAPS II | 295 | 19 | 18,9 (16,4-21,5) | 1,02 | 0,89 (0,85-0,92) |
| SAPS II (expanded) | 295 | 19 | 8,43 (7,1-9,8) ** | 2,25 | 0,89 (0,84-0,92) |
| MPM II0 | 295 | 19 | 17,3 (15,4-19,2) | 1,10 | 0,87 (0,82-0,90) |
| LODS | 295 | 19 | 16,1 (14,0-18,3) | 1,18 | 0,87 (0,82-0,90) |
| MPM II24 | 295 | 19 | 7,7 (6,5-8,9) *** | 2,46 | 0,89 (0,86-0,93) |
| MPM II48 | 295 | 19 | 5,1 (4,1-6,2) *** | 3,72 | 0,89 (0,85-0,92) |
| MPM II72 | 291 | 17,9 | 5,7 (4,5-6,9) *** | 3,12 | 0,89 (0,85-0,93) |
| TRIOS | 291 | 17,9 | 11,3 (9,5-13,1) * | 1,58 | 0,93 (0,89-0,96) |
*p<0,05; ** p<0,01; *** p<0,001 в сравнение с фактической летальностью
При оценке прогноза с использованием стандартных интегральных прогностических систем нами выявлено, что прогнозируемая летальность при использовании систем APACHE II, SAPS II, MPM II0, LODS не отличалась от фактической, причем наилучшее СОС отмечалось у SAPS II. При использовании расширенной методики SAPS II (expanded), динамических систем MPM II24, MPM II48, MPM II72, TRIOS фактическая летальность была достоверно выше прогнозируемой (p<0,05). В целом прогностические модельные системы показали удовлетворительную дискриминационную способность (AU ROC>0,8).
Среди специальных систем оценки прогноза в 1-е сутки ASCOT и TRISS обладали одинаковой чувствительностью, среди стандартных систем наиболее высокую чувствительность показала SAPS II, среди специальных динамических систем 24-hour ICU Trauma Score, стандартных TRIOS (таблица 12).
Результаты c2-теста Hosmer-Lemeshow в группах риска между прогнозируемыми с использованием различных модельных систем и фактическими исходами представлены в таблице 13. Для методик TRISS прогнозируемые величины выживания и летального исхода достоверно отличались от фактических цифр (р<0,05). То есть системы TRISS оказалась непригодной для оценки прогноза. Тогда как системы ASCOT и 24-hour ICU Trauma Score показали полное согласие прогнозируемых исходов с фактическими (р>0,05).
Таблица 12
Информационная ценность модельных прогностических модельных систем.
| Система | Чувствительность (95% ДИ) | Специфичность (95% ДИ) | ППЦ, % | ОПЦ, % | ПЭ, % |
| TRISS (n=295) | 53,6 (44,1-59,7) | 97,5 (95,3-98,9) | 83,4 | 90,0 | 89,2 |
| ASCOT(n=295) | 53,6 (43,1-62,0) | 95,0 (92,6-97,0) | 71,5 | 89,8 | 87,1 |
| 24-h ICU Trauma Score (n=295) | 64,3 (52,5-74,7) | 86,7 (83,9-89,1) | 53,0 | 91,2 | 82,4 |
| APACHE II (n=295) | 39,3 (29,6-47,2)* | 95,9 (93,6-97,7) | 68,8 | 87,1 | 85,1 |
| SAPS II (n=295) | 60,8 (50,2-69,1) | 95,0 (92,6-97,0) | 74,0 | 91,2 | 88,5 |
| SAPS II (expan-ded) (n=295) | 35,7 (26,2-43,6)* | 95,8 (93,6-97,7) | 66,7 | 86,5 | 84,4 |
| MPM II0 (n=295) | 42,9 (33,0-50,7) | 95,9 (93,5-97,7) | 70,6 | 87,8 | 85,8 |
| LODS (n=295) | 39,3 (29,8-46,4) * | 96,7 (94,5-98,4) | 73,4 | 87,2 | 85,8 |
| MPM II24 (n=295) | 35,8 (26,8-41,8) * | 97,5 (95,4-98,6) | 77,0 | 86,7 | 85,8 |
| MPM II48 (n=295) | 39,3 (30,6-44,1) * | 98,4 (96,3-99,5) | 50,1 | 93,0 | 87,1 |
| MPM II72 (n=291) | 38,5 (30,0-41,7) * | 99,2 (97,4-99,9) | 91,0 | 88,2 | 88,8 |
| TRIOS (n=291) | 53,8 (44,4-59,0) | 98,3 (96,3-99,5) | 87,6 | 90,8 | 90,4 |
*p<0,05 по сравнению с SAPS II
Таким образом, из специальных прогностических систем ASCOT и 24-hour ICU Trauma Score показали хорошую калибровку и пригодность для количественной оценки прогноза исходов.
При оценке прогноза в группах риска с использованием стандартных систем нами выявлена пригодность только систем SAPS II и MPM II72 (р>0,05).
Таким образом, проведенные нами исследования показали пригодность систем SAPS II, ASCOT и 24-hour ICU Trauma Score и MPM II72 при оценке прогноза летального исхода у каждого конкретного пациента.
Безусловно, представляется чрезвычайно важным прогнозирование исходов в поздних этапах посттравматического периода. Для решения поставленной задачи нами исследованы 259 пострадавших, которые прожили более 14 суток после травмы. Преобладающее большинство (95%) пострадавших в период поздних проявлений тяжелой травмой погибли от тяжелого сепсиса. При этом количественная оценка вероятности летального исхода проводилась в первые сутки. Проведенные исследования показали, что системы TRISS (c²=17,2; df=8; р=0,029) и ASCOT (c²=16,9; df=8; р=0,031) не пригодны для оценки вероятности летального исхода в поздних этапах посттравматического периода, тогда как интегральная система 24-hour ICU Trauma Score показала хорошую калибровку и свою пригодность в предсказании вероятности летального исхода (c²=2,44; df=3; р=0,49).
Таблица 13
Тест согласия Hosmer-Lemeshow для модельных прогностических систем
| Система | Число наблюдений, n | Показатели статистического анализа | ||
| c² | df | p | ||
| ASCOT | 295 | 9,71 | 8 | 0,286 |
| TRISS | 295 | 33,1 | 8 | <0,001 |
| 24-hour ICU Trauma Score | 295 | 3,77 | 4 | 0,438 |
| АPACHE II | 295 | 21,5 | 8 | 0,006 |
| SAPS II | 295 | 12,4 | 8 | 0,133 |
| SAPS II (expanded) | 295 | 20,1 | 8 | 0,010 |
| LODS | 295 | 14,8 | 5 | 0,011 |
| MPM II0 | 295 | 19,2 | 8 | 0,014 |
| MPM II24 | 295 | 29,3 | 8 | <0,001 |
| MPM II48 | 295 | 37,7 | 8 | <0,001 |
| MPM II72 | 291 | 14,9 | 8 | 0,061 |
| TRIOS | 291 | 16,3 | 8 | 0,038 |
Среди стандартных систем показали свою пригодность SAPS II (c²=10,9; df=8; р=0,21) и SAPS II (expanded) (c²=9,97; df=8; р=0,27), тогда как остальные системы оказались непригодными.
Таким образом, при количественной оценке прогноза в период поздних проявлений тяжелой сочетанной травмы (свыше 14 суток) лучшую пригодность показали интегральные системы, которые основаны на комплексной оценке тяжести повреждений, функционального состояния органов и систем, проводимого лечения.
Представляет важный научный и практический интерес то, что пол и возраст влияют на исход травмы. Так летальность во всей исследуемой когорте среди пострадавших старше 65 лет была на 10,5% выше, чем в остальных возрастных группах (р>0,05). Однако с увеличением индекса тяжести травмы влияние возраста на исход становилось статистически значимым: среди пострадавших старше 65 лет летальность при ISS= 16-29 баллов была выше на 19,6% (р<0,05), а при ISS>=30 - 22,5% (р<0,05) в сравнение с пострадавшими до 65 лет. На исход травмы заметное влияние так же оказывал пол пострадавших: летальность среди мужчин при ISS= 15-29 баллов на 13,7% (р<0,05), ISS>= 30 - на 19,1% была выше (р<0,05), чем среди женщин.
