Учебное пособие по курсу "Биотехнология" для студентов фармацевтического факультета нижний новгород 2005 г
| Вид материала | Учебное пособие |
- Учебное пособие по курсу "Биотехнология" для студентов фармацевтического факультета, 376.65kb.
- Учебное наглядное пособие для студентов экономического факультета Нижний Новгород, 356.34kb.
- Учебное пособие Нижний Новгород 2007 Балонова М. Г. Искусство и его роль в жизни общества:, 627.43kb.
- Учебное пособие Нижний Новгород 2002 удк ббк к найденко В. В., Губанов Л. Н, Петрова, 1219.74kb.
- Учебно методическое пособие Рекомендовано методической комиссией факультета вычислительной, 269.62kb.
- Учебное пособие по патофизиологии для студентов фармацевтического факультета, 677.92kb.
- Учебное пособие Нижний Новгород 2003 удк 69. 003. 121: 519. 6 Ббк 65. 9 (2), 5181.42kb.
- Учебное пособие Нижний Новгород 2010 Печатается по решению редакционно-издательского, 2109.64kb.
- Учебное пособие для студентов факультета очно-заочного обучения Нижний Новгород 2010, 795.89kb.
- Учебно-методическое пособие для студентов, обучающихся по специальности 030501 Нижний, 1855.66kb.
6.10.Применение иммобилизованных клеток для утилизации отходов. Утилизация разнообразных органических отходов, жидких стоков различных отраслей промышленности, сельского хозяйства, бытовой деятельности человека является чрезвычайно злободневной и острой проблемой, вклад в решение которой биотехнологических (микробиологических) методов трудно переоценить. Большую роль в очистке воды играют микроорганизмы-деструкторы пестицидов, поверхностно-активных веществ, нефтяных загрязнений ксенобиотиков и т.д. Микробиологическая очистка сточных вод способствует также получению альтернативных энергоресурсов и сырья, поскольку продуктом обработки во многих случаях является биогаз (смесь метана и углекислого газа в соотношении 3 : 1). Масштабы некоторых из биотехнологических очистных процессов огромны: уже существуют биореакторы емкостью 4000-5000 м3 и выше.
В основе биотехнологии очистки сточных вод лежат два подхода, в одном из которых используют аэробные, а в другом - анаэробные микроорганизмы. В аэробной очистке применяют активный ил (биопленку), представляющий собой скопление разнообразных микроорганизмов, видовой состав которых регулируется конкретными экологическими условиями. В большинстве случаев в развитых странах используют именно аэробную очистку.
Активный ил представляет собой темно-коричневые хлопья размером до сотен микрон, причем он состоит примерно на 70% из живых организмов и около 30% составляют частицы неорганической природы. Живые организмы вместе с твердым носителем, к которому они прикреплены, образуют так называемый зооглей-симбиоз популяций организмов, покрытый общей слизистой оболочкой. Зооглей может формироваться как за счет флокуляции, так и адгезии клеток на поверхности носителя. Микроорганизмы, входящие в состав активного ила, относятся к различным родам: Actinomyces, Actinobacter, Bacillus, Corynebacterium, Desulfiomaculum, Microcjccus, Pseudomonas, Sarcina и другие, которые окисляют спирты, жирные кислоты, парафины, ароматические углеводороды, нафтены, фенолы, осуществляют деградацию нефти (фенолы и формальдегид уже в незначительных концентрациях угнетают развитие микроорганизмов).
Аэробный способ очистки сточных вод основан на использовании системы из двух аппаратов: аэротенк и вторичный отстойник. Аэротенк - это открытое сооружение, через которое пропускается аэрируемая сточная вода и суспензия активного ила, в отстойнике же осуществляется доочистка воды. Применение активного ила по данной технологии относится, по существу, к методам, связанным с использованием иммобилизованных клеток. Однако кроме этого существуют промышленные методы использования активного ила, где иммобилизацию используют в "чистом" виде. Речь идет о биофильтрах, представляющих собой проточные емкости с принудительной или естественной циркуляцией, содержащие консорциум клеток активного ила, прикрепленных к поверхности пористого носителя, которым служит обладающая достаточной механической прочностью керамика, щебень, гравий, песок, керамзит, кольца Рашига, стекловолокно, нити синтетических волокон, металлические полимерные материалы.
Глубина и скорость очистки сточных вод в биофильтрах выше, чем в аэротенках (скорость в 10-15 раз выше и достигается практически полная очистка), однако содержание органики в очищаемых водах не должно превышать 500 мг/л (иначе трудно осуществить полную аэрацию биофильтра), кроме того, сточные воды перед биофильтром должны быть очищены от взвешенных частиц, в противном случае биофильтры быстро забиваются и происходит заиливание. Биофильтры целесообразно применять для очистки локальных стоков.
В последние годы конструкция биофильтров совершенствуется, например, в качестве носителя используют мелкозернистую полимерную или металлическую сетку. Биомассу клеток наращивают в пустотах внутри прокладок из пористого полиэфира, прокладки удерживают внутри реактора с помощью сеток и периодически удаляют из реактора. Густую биомассу отжимают, и пустые прокладки вновь возвращают в реактор. Запуск промышленных аэротенков и биофильтров в эксплуатацию занимает обычно десятки суток, время же их непрерывного функционирования составляет десятки месяцев.
Анаэробные способы очистки применяются, как правило, для обработки высококонцентрированных стоков и осадков, содержащих большое количество органических веществ. Процесс брожения осуществляется в метантенках. Анаэробное превращение органических веществ происходит под действием бактериальной микрофлоры (в ее состав входит до тысячи микроорганизмов) через четыре последовательных этапа: фаза гидролиза (расщепления) биополимерных молекул (белков, липидов, полисахаридов и других) на более простые, например, мономеры, аминокислоты, углеводы и другие; фаза ферментации мономеров до низших кислот и спиртов, аммиака, сероводорода; ацетогенная фаза (образование Н2, СО2, формиата, ацетата); непосредственно метаногенная фаза, которая ведет к конечному продукту расщепления - метану. Кроме метана, продуктом является углекислый газ (их смесь образует биогаз). В результате действия метанногенного консорциума микроорганизмов происходит резкое снижение концентрации органических загрязнений в отходах или сточных водах с одновременным образованием биогаза, который можно в дальнейшем использовать как энергоноситель или углеродный субстрат для синтеза микробной (кормовой) биомассы. Активное использование метаногенеза при сбраживании органических отходов является, по современным представлениям, одним из наиболее перспективных путей совместного решения экологических и энергетических проблем.
Конструкционное оформление метантанков весьма разнообразно, в общем случае это строго герметичный ферментер объемом до нескольких сотен кубометров с перемешиванием и рубашкой для обогрева, работающий в периодическом режиме загрузки отходов или сточных вод с постоянным отбором биогаза и выгрузкой твердого осадка по мере развития процесса. Обеспечение задержки (фиксирования) клеток в объеме метантенка при его работе и выгрузке позволяет значительно интенсифицировать процесс и увеличить выход биогаза.
Эффективность действия метантанков с иммобилизованными клетками в 2.5-3 раза выше, чем со свободными (во столько раз увеличивается выход биогаза с единицы объема метантенка), недостатком процессов с иммобилизованными клетками является то, что они приспособлены для переработки растворимой органики. С этой точки зрения метантенки с иммобилизованной биомассой чрезвычайно удобны для обработки сточных вод предприятий пищевой промышленности, например молокоперерабатывающих, спиртовых заводов, целлюлозно- бумажных производств и т.д. (их стоки не содержат значительного количества взвесей).
Важную роль в процессах очистки сточных вод играет денитрификация, осуществляемая, например бактериями Pseudomonas sp. Сущность денитрификации отражает схема:
NO3- + источник углерода ® N2 + CO2 + биомасса
Отдельной и важной задачей представляются процессы биодеградации сложных смесей углеводородов и их производных в средах, загрязненных нефтью. Сточные воды нефтяной промышленности обычно очищают биологическим способом или с помощью коагулянтов. Самые значительные утечки нефти происходят в море. Очистку морской поверхности от нефти проводят путем ее биодеградации природным симбиозом бактерий, способных расти на компонентах нефти и окислять их (конечными продуктами окисления являются СО2 и Н2О). Эти микроорганизмы действуют, по существу, в иммобилизованном состоянии на поверхности капель нефтепродуктов, причем, чем больше степень дисперсности нефти, тем быстрее осуществляется биодеградация. Наибольший эффект наблюдается, когда нефть эмульгирована в воде.
К числу острых экологических проблем относится проблема удаления из воды металлов (кадмия, свинца, цинка, урана, плутония), трития. Биотехнологический принцип решения этой проблемы состоит в применении иммобилизованных клеток микроорганизмов (бактерий) и микроводорослей, аккумулирующих металлы. Механизм процесса состоит в основном в комплексообразовании катионов металлов с функциональными группами клеточной стенки (натрием, фосфатными), в ион-ионном взаимодействии с заряженными группами, а также в адгезии частиц оксидов металлов (например, оксида урана) на поверхности клеток в результате электростатического взаимодействия.
Иммобилизацию клеток проводят адсорбцией на шариках из поливинилхлорида, полипропилена, цилиндрических частицах из стекла; включением в гели каррагинана, альгината, ПААГ.
Промышленные установки по извлечению металлов из сточных вод действуют в США и Венгрии. Экономический эффект их использования очень значителен: применение 10 г клеток (сырая биомасса), иммобилизованных в альгинатный или каррагинановый гели при очистке сточных вод от трития, эквивалентно действию 1г платинового катализатора.
Некоторые микроорганизмы (мицелиальные грибы и бактерии, выделенные из золоторудных месторождений, а также дрожжи) способны к аккумуляции золота, которое в техногенных условиях встречается в элементарном состоянии, а также в виде ионов - Au+ и Au3+. Адсорбируемое золото в некоторых случаях связывается с маннаном клеточной стенки.
Для практической реализации процессов удаления металлов из сточных вод (аккумулирования с целью концентрирования или выделения, например, урана из морской воды, золота) необходимо пропускать большие массы воды через колонные аппараты с иммобилизованными клетками, периодически меняя колонки или их содержимое; отделять клетки от носителя; выделять из них, если необходимо, металл т.д. Эта технология существенно упрощается, если использовать методы обратимой электроиммобилизации клеток.
Следует отметить, что с точки зрения технической микробиологии и биотехнологии биологическая очистка воды (в том числе с помощью иммобилизованных клеток микроорганизмов) представляется необыкновенным процессом. Его необычность состоит в том, что обработке подвергается огромное количество воды. В развитых странах в сутки биологически очищается больше воды, чем вырабатывается в год таких крупнотоннажных продуктов, как сталь, молоко, пиво, сахар. В РФ биологически очищается сточных вод в год больше, чем добывается угля и нефти, производится чугуна, стали, цемента, зерна, вместе взятых, в течение пятилетки.
Очистка воды является тем чрезвычайно крупномасштабным процессом, где необходимость и возможность применения иммобилизованных клеток полностью доказаны, причем реально может быть использован наиболее доступный тип иммобилизации - адсорбционный.
6.11.Биогеотехнология. Приложение биотехнологии к добыче, обога-щению и переработке руд и угля, отделению и концентрированию металлов, экстракции остаточных порций нефти из иссякающих месторождений относится к области биогеотехнологии.
Одним из направлений биогеотехнологии является получение металлов из бедных руд и производственных отходов. Традиционные способы извлечения металлов в таких случаях непригодны и не обеспечивают комплексное и рациональное использование руд и охрану окружающей среды.
В основе биотехнологии извлечения металлов из руд, концентратов, горных пород лежат химические процессы, осуществляемые микроорганизмами или их метаболитами: окисление сульфитных минералов, серы, Fe2+, разложение силикатов. В большинстве случаев клетки микроорганизмов используют в иммобилизованном состоянии – в виде биопленки на поверхности частиц руды, горной породы или минералов.
Для выщелачивания металлов из сульфидных и смешанных руд и концентратов, из отходов пирометаллургического производства и для удаления серы из угля используют Thiobacillus ferroxidans, Leptospirillum ferroxidans в ассоциации с Т.thiooxidans, T.organoparus. Микроорганизмы (грибы, бактерии, дрожжи) и их метаболиты используют для извлечения химических элементов из силикатных и карбонатных руд, для выщелачивания золота.
К процессам, непосредственно катализируемым бактериями, относятся окисление железа:
4FeSO4 + O2 + 2H2SO4 ® 2Fe2(SO4)3 + 2H2O
и окисление серы:
S8 + 12O2 + 8H2O ® 8H2SO4
Ряд минералов окисляется некоторыми выщелачивающими микроорганизмами, например пирит:
4FeS2 + 15O2 + 2H2O ® 2Fe2(SO4)3 + 2H2SO4
и сфалерит:
ZnS + 2O2 ® ZnSO4
Ион трехвалентного железа служит сильным окисляющим агентом, переводящим в раствор многие минералы, например халькоцит:
CuS + 2Fe2(SO4)3 ® 2CuSO4 + 4FeSO4 + S
и уранит:
UO2 + Fe2(SO4)3 ® UO2 SO4 + 2FeSO4
Выщелачивание, происходящее при участии иона трехвалентного железа, который образуется в результате жизнедеятельности бактерий, называют “непрямой “ экстракцией.
В настоящее время бактериальное выщелачивание, известное как биогидрометаллургия или биоэкстрактивная металлургия, применяется в промышленных масштабах для перевода в растворимую форму меди и урана (выщелачивание отвалов и бедных руд). Бедную руду или отвальную породу перевозят из карьера в расположенную поблизости местность с естественным уклоном, который дает возможность собирать используемые растворы. Во- избежании загрязнения подпочвенных и поверхностных вод выбирают непроницаемые для воды участки. Для начала процесса выщелачивания отвал смачивают водой, подкисленной серной кислотой до рН= 1.5 – 3.0. Кислый раствор просачивается сквозь руду и, поскольку он содержит углекислый газ и кислород, создает благоприятную среду для размножения природных ацидофильных тиобацилл. Из выщелачиваемых отвалов вытекают растворы, содержащие металлы, они направляются в отстойники, откуда извлекаются путем осаждения или экстракции, а отработанные выщелачивающие растворы вновь поступают в отвал.
Промышленное применение нашел также процесс удаления серы из угля. Предварительная обработка бактериями T.ferrоoxidans приводит к окислению значительной доли серы (в виде пирита) до серной кислоты (60-98% за 7-10 суток). Обработку угля проводят открытым способом, но ведется поиск методов введения микроорганизмов в пласты угля.
Закрепленные на поверхности раздела (жидкость-твердое тело и жидкость-жидкость) микроорганизмы применяют для увеличения добычи нефти. Традиционными методами можно извлечь из месторождений лишь часть ее, около 50% нефти остается в капиллярах пор породы месторождений.
Интенсификация добычи нефти осуществляется микроорганизмами и продуктами их жизнедеятельности. Для этого используют стимуляцию деятельности природной микрофлоры месторождений путем введения в скважины питательных веществ (мелассы, молочной сыворотки, микроорганизмов, продуцирующих нужные метаболиты, а также введением определенных биопродуктов, наработанных вне месторождений.
В скважину вводят несколько сот литров посевного материала, содержащего раствор мелассы. Увеличение выхода нефти составляет 16-200%. Этот эффект обусловлен влиянием следующих продуктов жизнедеятельности микроорганизмов: газов – СО2, СН4, N2, Н2 (уменьшение вязкости и увеличение давления); полисахаридов – альгината, ксантана, курдлана, декстрана, пуллулана, эмульсана (уменьшение межповерхностного натяжения между нефтью и водой); поверхностно-активных веществ – глицеридов, липидов, пептидолипидов, софролипидов и других (уменьшение натяжения); органических кислот – муравьиной, масляной, молочной и других (увеличение проницаемости пород путем растворения карбонатов и доломитов); низкомолекулярных растворителей – спиртов, кетонов (уменьшение вязкости).
Биотехнологические методы добычи полезных ископаемых экономически выгодны. Новые методы добычи позволяют разрабатывать бедные и сложные по составу месторождения, осваивать глубинные места залегания, обеспечивать комплексную утилизацию сырья, исключить загрязнение окружающей среды элементами сырья, хотя экологическое влияние массированного использования микроорганизмов изучено недостаточно.
6.12.Биосенсоры на основе иммобилизованных ферментов.
Высокая эффективность биологических катализаторов и специфичность их действия делают ферменты идеальными реагентами для аналитической химии. Благодаря этим особенностям с помощью ферментов обнаруживаются вещества при предельно низкой концентрации (до 10-12 моль/л) в присутствии множества других соединений. К настоящему времени созданы искусственные аналитические системы различных конструкций (биосенсоры, датчики, ферментные электроды, проточные анализаторы), потенциометрического, амперометрического, калориметрического, пьезоэлектрического и оптического типа, содержащие иммобилизованные ферменты и клетки и предназначенные для автоматического детектирования продуктов энзиматических превращений. Например, если использовать иммобилизованную глюкозооксидазу, то концентрацию окисляемой кислородом глюкозы определяют, регистрируя количество выделившегося в ходе реакции пероксида водорода полярографическим, колориметрическим или люминесцентным методом.

Технологические варианты сенсоров с иммобилизованными ферментами весьма разнообразны - колонки, трубки, полые волокна и пр. С их помощью на практике определяют концентрацию широкого спектра соединений - глюкозы, аминокислот, мочевины, пенициллина, АТФ, НАДН, ФМН, стероидов, триглице-ридов, желчных кислот и многих других. Так, американскими исследователями сконструирован микродатчик на основе глюкозооксидазы и рутениевого красите-ля, иммобилизованных в полиакриламидной матрице с использованием суб-микронных оптических волокон. Микробиосенсор, не вызывая повреждений, может быть введен в клетку и даже в отдельные ее компартменты для измерения содержания в них глюкозы и кислорода. Предложены датчики на базе иммунодетекции для проведения экспресс-анализов на присутствие производных диоксина и оценки содержания биогенных аминов (с помощью моноамино-оксидазы) в пищевых продуктах в связи с процессами их старения. Для определения мочевины ферментным электродом требуется всего 30 с.
Биосенсоры на основе иммобилизованных ферментов помогают выполнять десятки быстрых и точных анализов при диагностике заболеваний, контролировать содержание вредных веществ (инсектицидов, пестицидов, удобрений) в пищевых продуктах и в воздухе. Биосенсоры нашли применение в решении аналитических задач в химической и микробиологической промышлен-ности, а также в научных исследованиях.
Начаты разработки новых поколений биодатчиков на базе аффинных взаимодействий (биосродства) типа фермент-ингибитор, антитело-антиген, агонист (антагонист)- клеточный рецептор на основе полупроводниковых устройств-термисторов и пьезоэлектрического эффекта.
Термистор представляет собой полупроводниковый резистор, сопротивление которого изменяется с изменением температуры. Датчик представляет собой термистор, на поверхности которого находятся иммобилизо- ванные клетки или молекулы ферментов или антител. Он с высокой чувствитель- ностью регистрирует изменения температуры, происходящие при протекании биохимических реакций с анализируемыми веществами.
Особенно высокой чувствительностью обладают пьезоэлектрические биосенсоры. Принцип их действия основан на изменении частоты переменного тока, при которой пьезоэлектрик, например кристалл кварца, колеблется в резонансном режиме. Химически чистый и физически однородный кристалл пьезоэлектрика характеризуется постоянной резонансной частотой колебаний, которая для кварца составляет 9 или 14 МГц. Если на кристалл налипает то или иное вещество, частота резонансных колебаний меняется в соответствии с уравнением:
dν/ν = -dm/Apt ,
где v - частота колебаний; dv - ее приращение; dm - изменение массы кристалла; А - поверхность кристалла; р - его плотность; t - его толщина.
Пьезоэлектрики регистрируют изменение массы порядка 10-12г. Биосенсоры на их основе содержат иммобилизованный на пьезокристалле фермент, антитело, антиген или нить ДНК (РНК). О наличии детектируемого агента, вступающего в ферментативную, иммунную реакцию или образующего гибридную молекулу (ДНК (РНК) с иммобилизованным биообъектом, свидетельствует формирование соответствующего комплекса на пьезоэлектрике, которое увеличивает его массу и меняет частоту резонансных колебаний. С помощью пьезоэлектрического биосенсора с иммобилизованным антигеном можно обнаружить антитела в сыворотке крови, разведенной в 1000 раз.
Правда, в водном растворе кристалл реагирует слабее (изменением резонансной частоты) на увеличение своей суммарной массы, чем на воздухе. Поэтому предполагают погружать пьезоэлектрический биосенсор в раствор, где будет формироваться фермент-субстратный (фермент-ингибиторный) или иммунный комплекс, а далее определять колебательные характеристики кристалла в воздухе. Высокая чувствительность пьезоэлектриков к изменениям массы в воздушной среде позволяет использовать их в биосенсорах на газы, загрязняющие атмосферу.
Учеными из Университета Пердью (США) разработаны био-оптические лазерные диски “BioCD”, которые, в перспективе, предполагается применять при проведении детального анализа крови. Принцип действия “BioCD” аналогичен принципам, положенным в основу традиционных компакт-дисков. В частности, как и обычные носители, “BioCD” имеют дорожки. Правда, они используются не для записи информации, а для хранения специальных веществ, реагирующих на строго определенный тип белков. Другими словами, треки “BioCD” напоминают микроскопические пробирки с реактивами. Для проведения анализа достаточно нанести каплю крови на поверхность диска и считать результаты при помощи лазерного привода.
По словам Дэвида Нолта, руководителя проекта, человеческая кровь содержит порядка десяти тысяч различных белков, которые, в идеале, должны регистрировать био-оптические диски. Ведь даже незначительные изменения концентрации некоторых из этих белков могут предвещать развитие серьезных заболеваний. Следует отметить, что в настоящее время при проведении детальных исследований крови применяется очень дорогое оборудование стоимостью до 50 тысяч долларов и выше. Вместе с тем, появление био-оптических детекторов позволит значительно снизить стоимость проведения процедур, поскольку считывать данные можно будет посредством лишь незначительно модифицированных CD-приводов. Правда, в настоящее время предложенная методика нуждается в серьезных доработках, и прежде чем “BioCD” появятся на рынке, пройдет не менее десяти лет.
Иммобилизованные клетки микроорганизмов обычно применяют в комбинации с амперометрическими или потенциометрическими (газовыми) электродами для регистрации отдельных веществ и комплексных физиолого-биохимических параметров, которые трудно или вовсе невозможно оценить с помощью изолированных ферментов: потребление кислорода (показатель органического загрязнения природных или сточных вод), измеряемое амперометрически по поглощению О2 или потенциометрически по образованию СО2 клетками гриба Trichosporon cutaneum или бактерий Azotobacter vinelandii, E- coli и др.; токсичность водного раствора или воздуха, измеряемая сенсорами на базе иммобилизованных цианобактерий, у которых активность фотосистемы II снижается при наличии в среде токсических компонентов, особенно гербицидов; мутагенное действие тестируемого агента, определяемое стандартными методами обнаружения мутантных клеток, например, растущих и соответственно выделяющих СО2 лишь на обогащенной среде.
Микробные биосенсоры, в отличие от ферментных, не требуют регенерации кофакторов, стабильны (срок службы от 5 до 60 дней), причем стабильность может быть повышена периодическим погружением иммобилизованных клеток в свежую питательную среду. Недостаток микробных биосенсоров - медленный отклик на детектируемый агент (обычно от 10 до 60 мин), что объясняется затратами времени на транспорт этого агента внутрь клетки и его ферментативное расщепление, предшествующее появлению вне клеток продуктов, взаимодействующих с электродом (О2, СО2 и др.). Клетка в некоторых случаях откликается и на посторонние агенты, поэтому иммобилизованные на биосенсоре клетки целесообразно обрабатывать ингибиторами побочных ферментативных реакций, не специфичных по отношению к детектируемому агенту.
Известны биосенсоры с соиммобилизованными клетками и изолированными ферментами, что позволяет осуществлять многостадийные ферментативные реакции. Так, соиммобилизация уреазы и нитрифицирующих бактерий на О2-электроде дает чувствительный биосенсор на мочевину. Возможно также совместное применение двух и более видов микроорганизмов в составе одного биосенсора.
Использование тканей растений и животных перспективно, но применяются сравнительно редко. Во многих случаях они более стабильны, чем ферменты и клетки, а порой более специфичны, чем микробные клетки. Так, глутаматный биосенсор на основе ткани свиной почки не откликается на мочевину, аланин, аргинин, гистидин и другие аминокислоты. Сложные органические соединения, такие как АМФ, дофамин, аскорбиновая кислота, в растительных тканях разлагаются до простых ионных или газообразных продуктов, что дает возможность регистрировать их ионоселективными (газовыми) электродами. Иммобилизация тканевых срезов - укрытие под сеткой или под мембраной - подкупает своей простотой. Например, дофамин регистрируют с помощью
«бананотрода» - тонкого среза мякоти банана, иммобилизованного на О2-электроде.
Созданы датчики, в которых используют рецепторные системы различных организмов: пучок нервов или отдельные нервы из усов краба (биосенсор на аминокислоты и пуриновые основания), щупальца синих крабов, раков (биосенсоры на аминокислоты и гормоны), собачий нос (обнаружение контрабандных наркотиков и взрывчатки). Иногда предпочитают не весь рецепторный орган, а лишь клетки или даже их органеллы, непосредственно отвечающие за узнавание того или иного агента. Таковы биосенсоры с изолированными рецепторами растений на ауксины и токсины.
Рецепторные биосенсоры дают быстрые ответы на детектируемый агент, высокоспецифичны, баснословно чувствительны: биосенсор на базе щупалец атлантического синего краба отвечает на 10-13 моль/л глутамина. Однако изолированные рецепторы недостаточно стабильны. Продление их жизни ищут на путях инкапсулирования рецепторов в бислойные липидные мембраны, в том числе в липосомы.
6.13.Иммобилизованные ферменты в медицине. Иммобили-зованные ферменты имеют огромное значение для медицины. В частности, большой рынок сбыта занимают тромболитические ферменты, предназначенные для борьбы с сердечнососудистыми заболеваниями. Так, в отечественную клиническую, практику внедрен препарат «стрептодеказа», содержащий стрептокиназу - активатор предшественника протеиназы плазмина, предотвра-щающий образование тромба в кровеносной системе.
Ферменты, разрушающие некоторые незаменимые аминокислоты (например, аспарагиназа), используют для борьбы со злокачественным ростом опухолей. Протеолитические ферменты (трипсин, химотрипсин, субтилизин, коллагеназа), иммобилизованные на волокнистых материалах (целлюлоза, полиамидные волокна, декстран и др.), применяют для эффективного лечения ран, язв, ожогов, абсцессов, а их белковые ингибиторы - в заместительной терапии для лечения эмфиземы и панкреатитов.
В 2004 г. появилось сообщение о том, что британская компания “Cell Tran”, разработала уникальную технологию заживления ран, которая, в перспективе, может существенно ускорить процесс реабилитации пациентов с тяжелыми ожогами или язвами. Материал, получивший название “MySkin”, представляет собой специальную мембрану, созданную из безопасного, с медицинской точки зрения, полимера. Поверхность мембраны покрыта питательным веществом, создающим благоприятные условия для размножения клеток. В процессе лечения у пациента сначала берется небольшой образец ткани, который затем выращивается в лаборатории до образования колонии. Далее клетки сформировавшейся кожи помещаются на мембрану, а повязка закрепляется на поврежденном участке тела. Поскольку бандаж “MySkin” использует ткани самого пациента, то выращенные клетки не только не отторгаются, но, напротив, очень быстро приживаются на ране.
Как сообщается, повязки “MySkin” будут применяться, в первую очередь, при заживлении диабетических язв. Такие язвы могут оставаться открытыми в течение многих месяцев, доставляя немало проблем, как самим пациентам, так и лечащим врачам. Кроме того, бандажи “MySkin” смогут помочь людям, пострадавшим в пожарах. О сроках появления "самозаживляющих бинтов" в продаже пока ничего не известно, однако медики намерены вывести новый продукт на рынок как можно скорее.
Исключительно важны с практической точки зрения работы, посвященные направленному транспорту лекарственных веществ. В этом отношении особенно выгодны инкапсулированные ферменты типа искусственной клетки. Так, микрокапсулы, стенки которых представлены оболочкой эритроцита («тень эритроцита»), а их содержимое заполнено ферментом аспарагиназой, переносятся кровотоком к зонам скопления аспарагина и поэтому применяются для лечения аспарагинзависимых опухолей, в частности саркомы. Колонки, заполненные микрокапсулами с ферментом, используют для диализа в аппарате «искусственная почка», которая работает в 100 раз эффективнее обычного аппарата.
Таким образом, использование иммобилизованных ферментов во многих жизненно важных отраслях народного хозяйства становится все более массовым. Выгодное сочетание избирательности и эффективности с долговечностью и стабильностью иммобилизованных ферментов в корне меняет химическое производство, способы добывания сырья, способствует созданию новых биотехнологических процессов и методов терапии, совершенствует медицинскую диагностику, анализ, органический синтез и оказывает огромное влияние на образ жизни человека.
7.РЕАКТОРЫ С ИММОБИЛИЗОВАННЫМИ КЛЕТКАМИ
Каталитические системы с иммобилизованными клетками должны обеспечивать технологические и экономические преимущества по сравнению с традиционными процессами микробиологического синтеза на основе свободных клеток. Помимо свойств непосредственно иммобилизованного биокатализатора (нерастворимость, высокая активность, собственная система регенерации кофакторов и т.д.) важную роль в реализации таких преимуществ играет аппаратурное оформление процессов с иммобилизованными клетками, иными словами, выбор конструкции реакторов, где осуществляются биокаталитические процессы.
Любую систему, у которой существует ограничивающая ее поверхность и в которой протекают биохимические процессы, называют реактором (биореактором). С точки зрения организации массопотоков реакторы, в том числе промышленные, могут работать в периодическом режиме, периодическом режиме с доливом субстрата, полунепрерывном (полупериодическом) и непрерывном поточном режимах.
Высокая концентрация микроорганизмов в рабочем объеме реактора с иммобилизованными клетками определяет необходимость создания высоких скоростей массопередачи, что особенно важно для аэробных процессов, когда недостаточно интенсивная массоподача кислорода может лимитировать скорость образования целевого продукта. Эти требования приводят к необходимости перемешивания среды в рабочем объеме. Отсюда следует, что биокатализатор должен быть стоек к механическому истиранию его гранул и частиц. Тем не менее, механическая прочность иммобилизованных биокатализаторов часто бывает недостаточной, поэтому ее следует компенсировать путем разработки реакторов соответствующей конструкции. Исходя из этого удобно классифицировать реакторы для иммобилизованных клеток по относительному движению частиц твердой фазы (биокатализатора). По этому признаку все виды реакторов можно разделить на два типа - с отсутствием или с наличием движения частиц твердой фазы.
Отметим, что типы реакторов по этой классификации достаточно условны и отражают лишь наиболее общие принципы их устройства и функционирования. На практике те или иные реакторы могут сочетать принципы обоих типов, представлять разнообразные их модификации. Рассмотрим более подробно конкретные виды реакторов.
Реактор периодического действия (рис.5а) устроен просто: он представляет собой емкость с мешалкой, в которую помещают биокатализатор и раствор субстрата (питательную среду). После окончания процесса, иммобилизованные клетки отделяют от продуктов центрифугированием или фильтрацией и биокаталитический цикл начинается с начала. Очевидно, что такие реакторы недостаточно производительны, характеризуются большими потерями биокатализатора и находят лишь ограниченное применение, хотя следует отметить, что для традиционной микробиологической промышленности, основанной на использовании свободных клеток микроорганизмов, такой тип реактора является наиболее распространенным.
Проточный реактор с перемешиванием (рис.5б) отличается от предыдущего тем, что после каждого каталитического цикла отделение биокатализатора не происходит, субстрат периодически доливается, периодически же отделяются продукты. Эффективность такого реактора выше, чем у периодического. В идеальном проточном реакторе с перемешиванием содержимое находится в равновесном состоянии и система напоминает хемостат - один из вариантов непрерывного культивирования свободных клеток микроорганизмов.
Проточные реакторы могут иметь неподвижный или перемешиваемый слой катализатора. Рассмотрим сначала реакторы с неподвижным слоем. Иммобилизованные клетки (в форме гранул, стружки, дисков, зерен, волокон и т.д.) могут быть легко упакованы в колонне, образуя неподвижный слой. Субстрат проходит через слой биокатализатора сверху или снизу. Если профиль потока жидкости точно перекрывает поперечное сечение реактора, то реактор работает по поршневому принципу. Концентрация субстрата максимальна на входе, а концентрация продуктов - на выходе из реактора, следовательно, эти реакторы особенно удобны для процессов, сопровождаемых ингибированием продуктами. Реакторы такого рода нашли промышленное применение, в частности для очистки сточных вод, получения уксусной, яблочной, аспарагиновой кислот, глюкозо-фруктозного сиропа, а также для процессов с иммобилизованными ферментами. Кроме проточного реактора с неподвижным слоем (рис.5в) применяют серию таких реакторов, а также проточный реактор с неподвижным слоем с рециркуляцией (рис.5г).
Для микробиологических процессов, проходящих с выделением газов (при получении этанола, например, выделяется СО2), для эффективного их отвода целесообразно использовать наклонный проточный реактор или горизонтальный проточный реактор с фиксированным слоем биокатализатора (рис. 5д).
Проточные реакторы с перемешиваемым слоем биокатализатора могут быть с взвешенным (псевдоожиженным или кипящим) слоем, а также движущимся фиксированным слоем. Реакторы с взвешенным слоем характеризуются тем, что субстрат поступает снизу достаточно быстро, так чтобы поддерживать частицы во взвешенном состоянии, но не настолько быстро, чтобы частицы уносились вместе с выходящим потоком жидкости. В данном случае реализуется режим, промежуточный между полным перемешиванием (как в проточном реакторе с перемешиванием) и отсутствием перемешивания (как в реакторе поршневого типа). Схема реактора с перемешиванием представлена на рис.5е. Реакторы с взвешенным слоем целесообразно применять, когда псевдоожижение осуществляют газовой фазой (при аэрации или при выделении газа в катализируемом процессе), а также для переработки вязких субстратов.
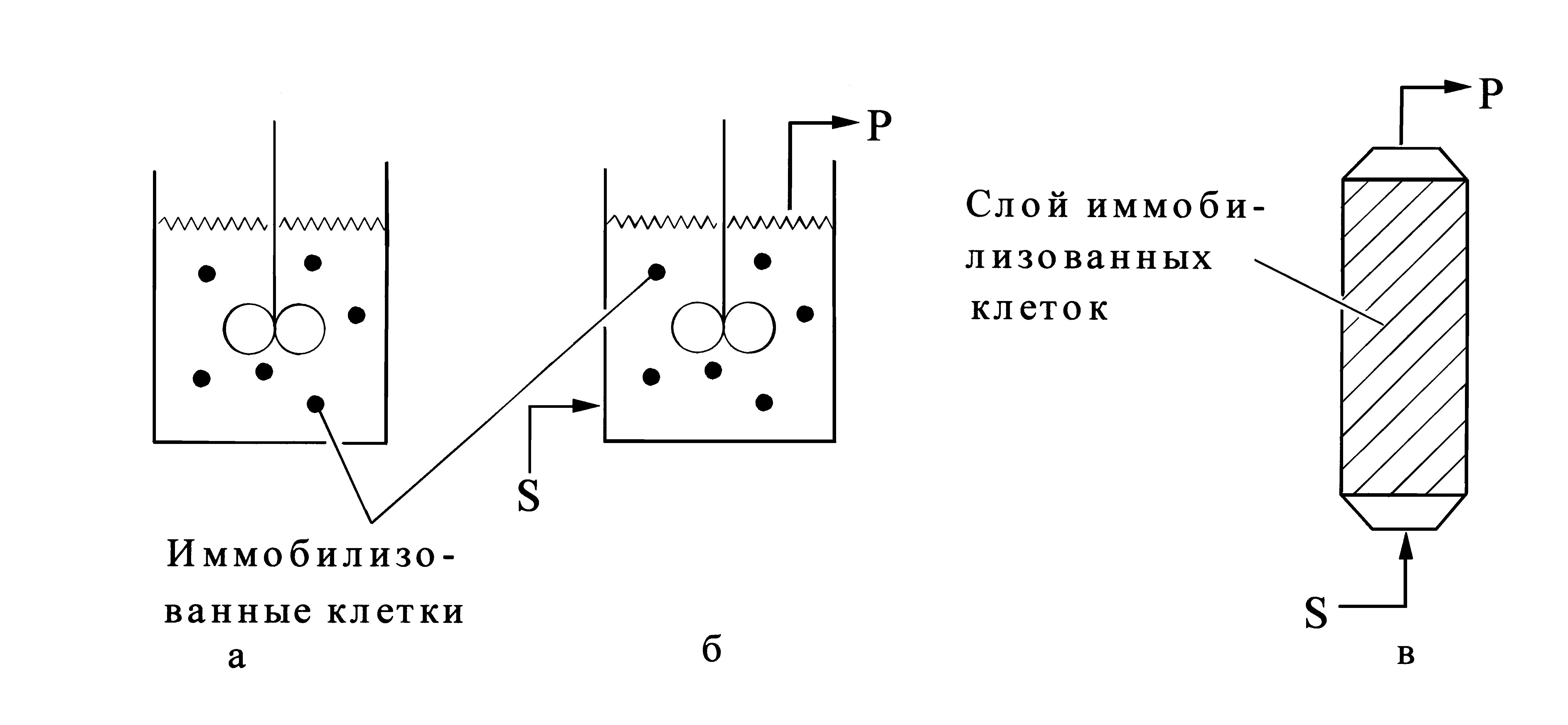
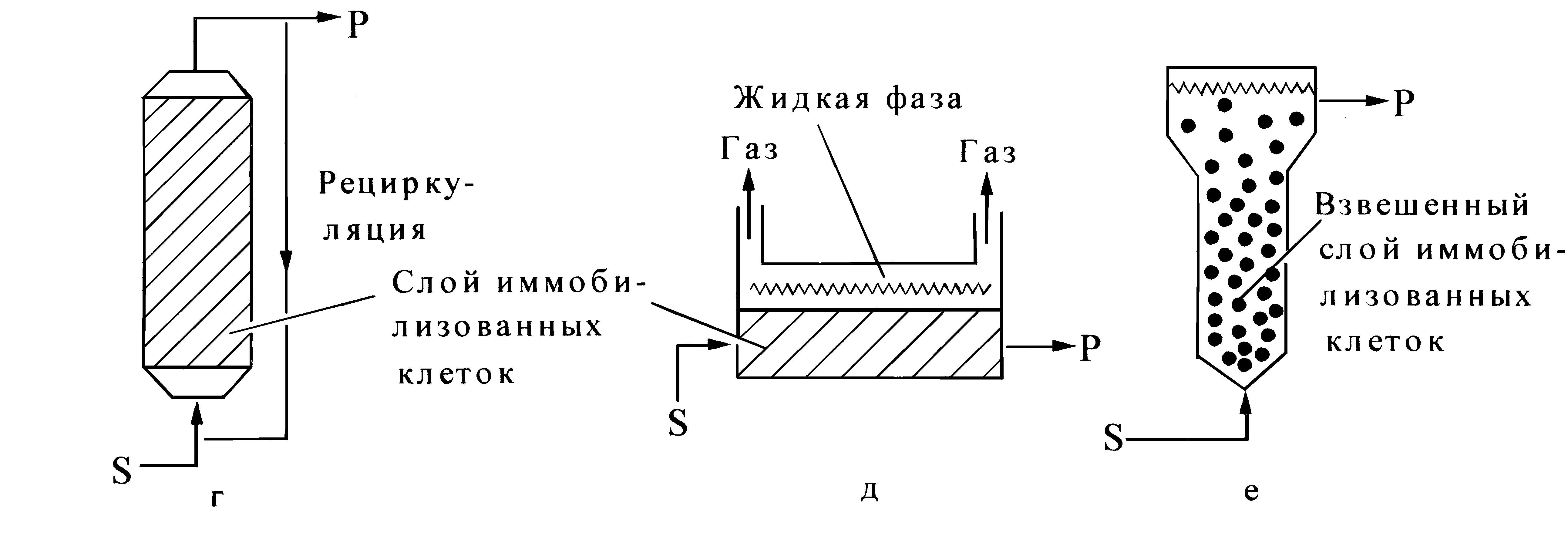
Рис.5 Типы реакторов
а - периодического действия; б - проточный с перемешиванием; в - с неподвижным слоем (проточный); г - с рециклом; д - горизонтальный с неподвижным слоем; е - проточный с взвешенным (“кипящим”) слоем
Относительная скорость движения жидкости и гранул в реакторах со взвешенным слоем невелика, что невыгодно с точки зрения обеспечения биокатализатора субстратом. Более удобными представляются реакторы с движущимся фиксированным слоем биокатализатора, когда расположение его гранул фиксировано друг относительно друга (это исключает также механическое повреждение гранул).
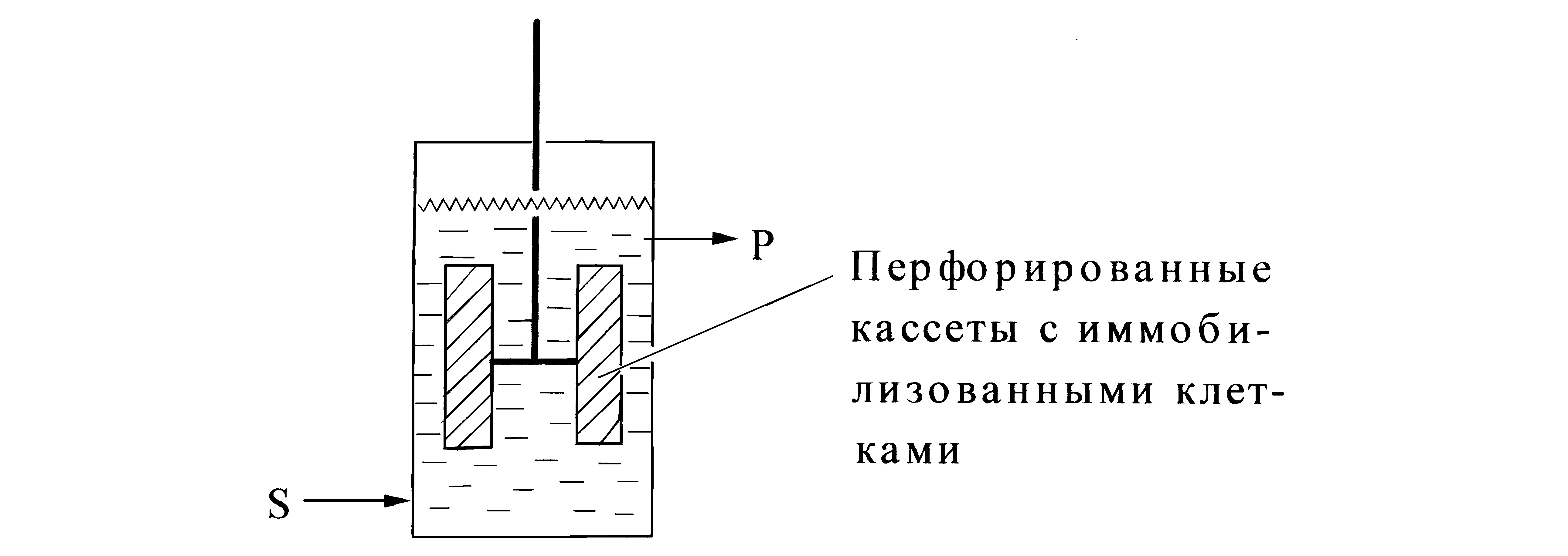
Предложен ряд вариантов реакторов с вращающимся перфорированным контейнером (рис.6а), с кассетами диффузорами и мешалкой (рис.6б), а также реакторы типа "активный ротор" с перфорированными кассетами, выполняющими роль мешалки (рис.6в).
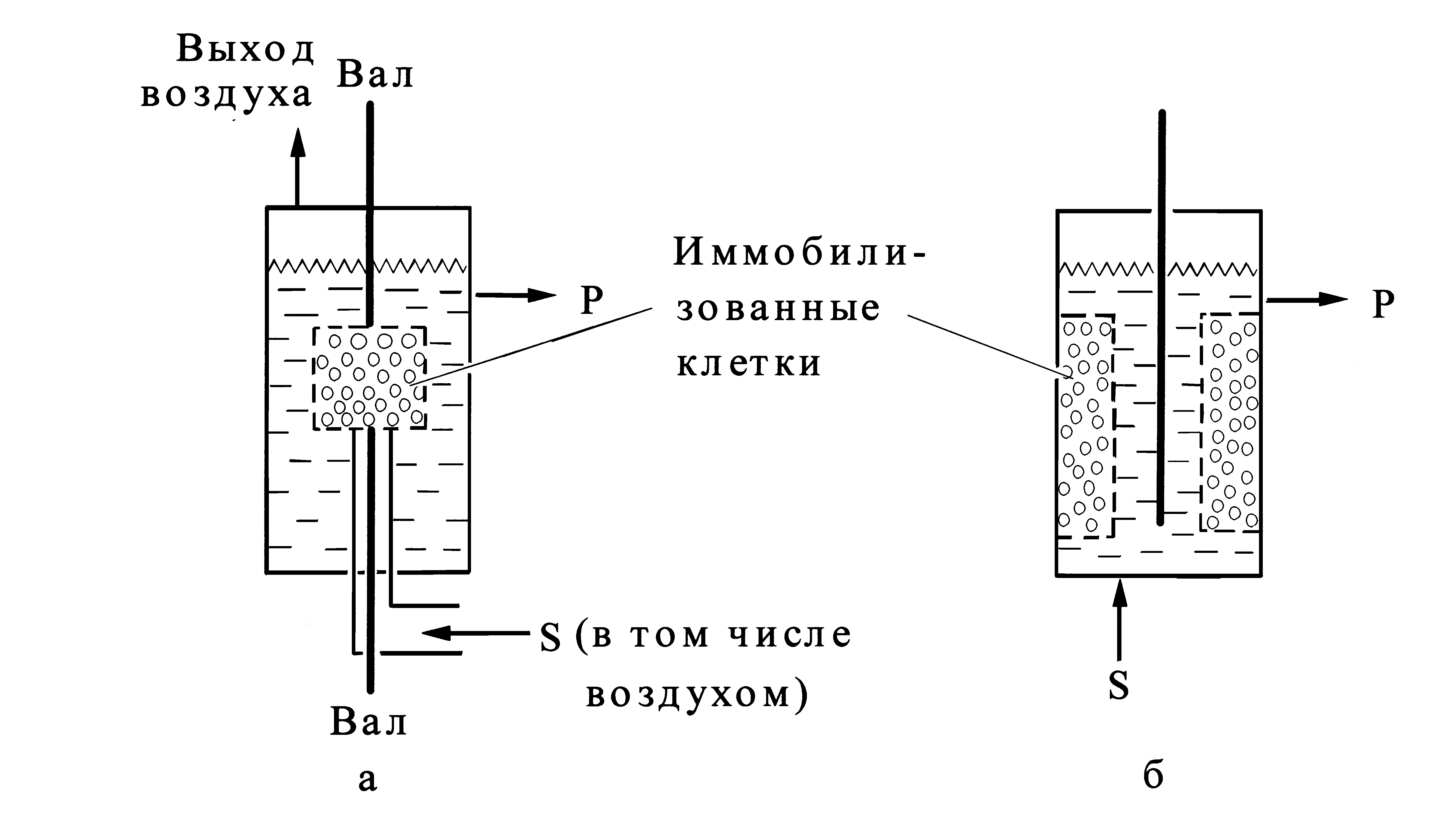
в
Рис.6 Реакторы с движущимся фиксированным слоем биокатализатора
а – с вращающимся перфорированным ротором; б – с кассетами – диффу-зорами; в – типа активный ротор
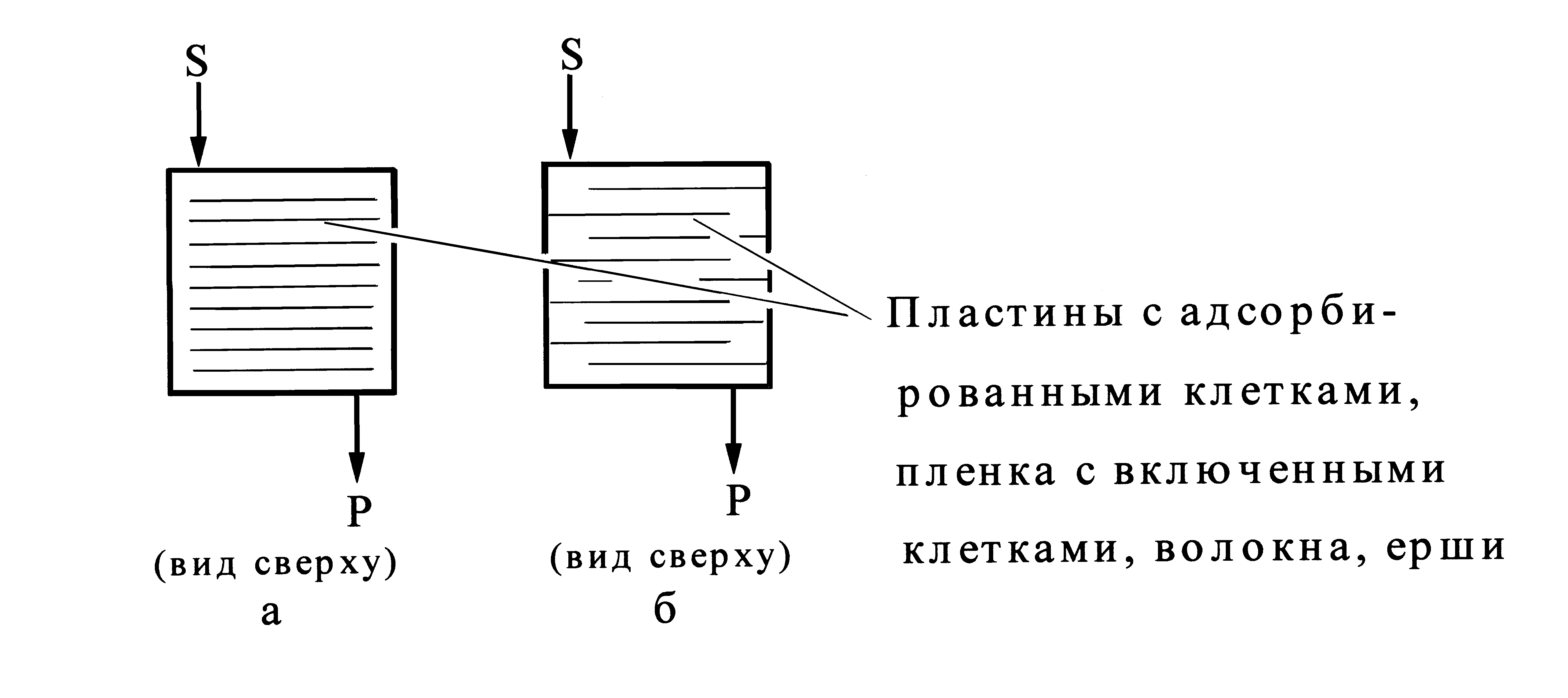
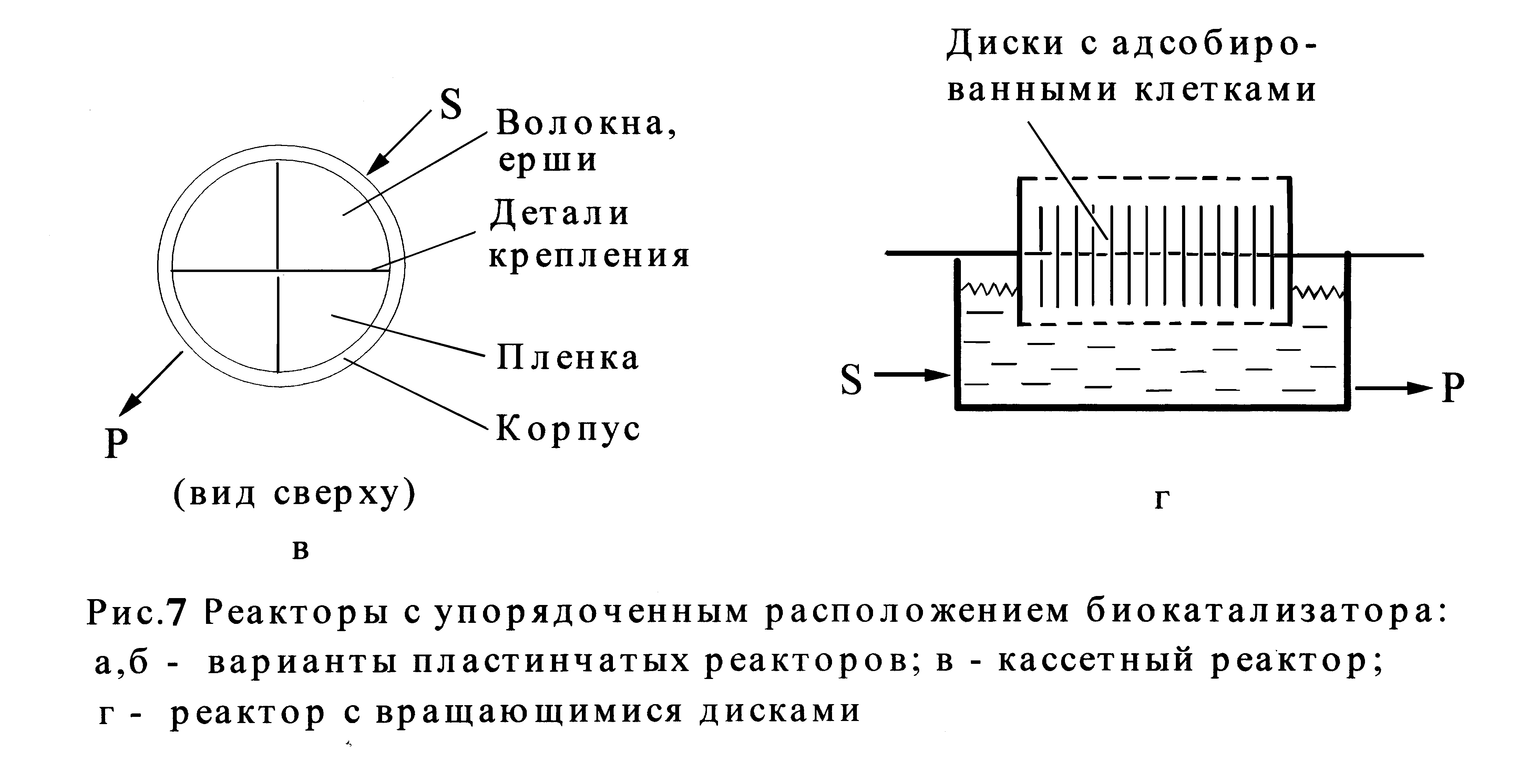
В больших реакторах возникает эффект неоднородности слоя биокатализатора, вследствие чего поток жидкости проходит преимущественно по зонам с низким гидравлическим сопротивлением. Одним из возможных решений проблемы представляется использование проточных реакторов с упорядоченным расположением биокатализатора. Примером служит реактор с носителем в виде пакета пластин (пластинчатый реактор рис.7а,б), покрытых слоем микроорганизмов. Можно использовать и реактор, в корпусе которого заключена кассета (в том числе съемная), на которой размещена пленка-адсорбент или волокна, ерши и другие элементы, обладающие развитой поверхностью и служащие адсорбентом микроорганизмов (рис.7в). К данной категории относится также горизонтальный реактор с параллельно расположенными вращающимися дисками, выполненными в виде кассеты, закрепленной на оси (рис.7г). Реактор с вращающимися дисками применяют для получения этанола, другие виды реакторов с упорядоченным расположением биокатализатора используют при очистке сточных вод, в процессах бактериального выщелачивания руд.
8. МЕМБРАННЫЕ РЕАКТОРЫ
Мембранный реактор представляет собой аппарат, в котором одновременно осуществляется проведение двух процессов - управляемого культивирования свободных микроорганизмов в объеме реактора и удаление продуктов (и замены их субстратом) с помощью мембранного модуля. В зависимости от расположения мембранного модуля мембранные реакторы разделяют на те, у которых мембрана является элементом конструкции самого реактора, а также на реакторы с выносными фильтрационными модулями (по форме реакторы могут быть плоскими, половолокнистыми и др.). Эксплуатация реакторов первого типа происходит в более строго контролируемых условиях, однако замена мембраны осложнена (замена мембраны необходима, так как она неизбежно засоряется клеточными обломками и коллоидными частицами). Этот недостаток исключается в реакторах второго типа, однако им присуща опасность заражения, а также циклически неконтролируемых изменений давления и концентрации компонентов в выносном фильтрационном модуле.
Материал фильтрационных мембран может быть различным - керамические и металлокерамические фильтры, стерилизуемые полимерные матрицы, ионообменные мембраны. По типу мембраны разделяются на фильтрационные и диализные: в первом случае массоперенос через мембрану осуществляется за счет разницы давления над и под мембраной; во втором - за счет градиента концентраций над и под мембраной.
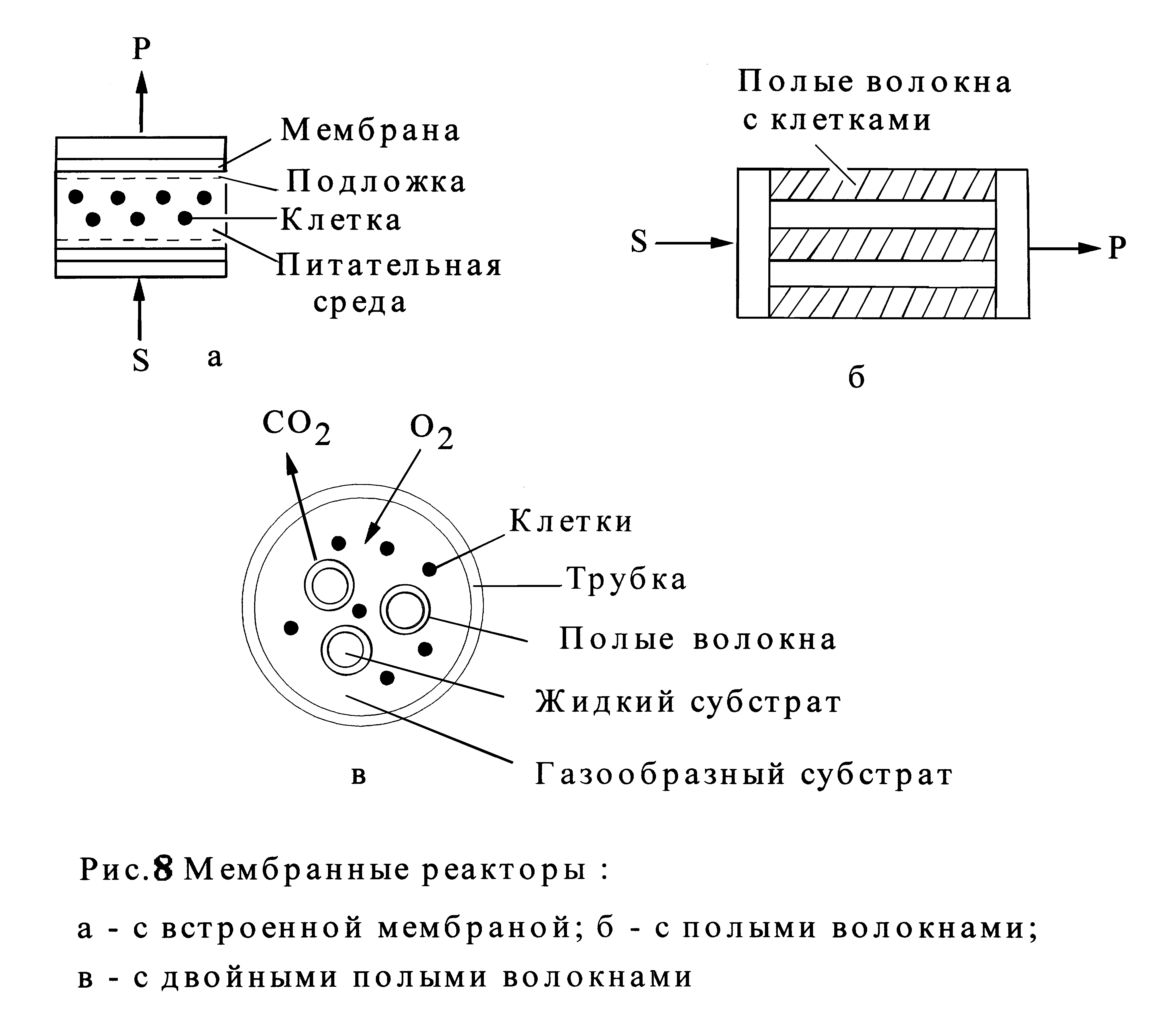
Принципиальная схема мембранного реактора, у которого мембрана является элементом его конструкции, приведена на рис.8а Реактор с выносным модулем представляет собой реактор с перемешиванием (с гомогенной средой) и циркуляцией среды через модуль. Третий тип мембранного реактора относится к тому случаю, когда клетки каким-либо образом прикреплены к мембране или находятся внутри самой мембраны. Чаще всего для этого используют мембраны, представляющие полые волокна, на поверхности которых закреплены клетки и через которые поступает субстрат и одновременно отводятся продукты (рис.8б). Модификацией такого реактора является реактор с двойными полыми волокнами (рис.8в), когда в пористое полое волокно большого диаметра (трубку) заключены полые пористые волокна меньшего диаметра и в межволоконном пространстве находятся клетки. Этот реактор целесообразно использовать, когда субстраты и (или) продукты находятся в жидкой и газообразной фазе. Газообразные компоненты реакционной системы подаются (удаляется) через стенку волокна большего диаметра, а жидкая компонента - через волокно меньшего диаметра.
Установлено, что мембранные реакторы можно использовать для культивирования практически всех эукариотических и прокариотических микроорганизмов, как в аэробных, так и в анаэробных режимах. Их применяют, в частности, для получения ферментов, антибиотиков, витаминов, аминокислот, органических кислот, этанола, бутанола, ацетона, акриламида.
Мембранные реакторы относятся к ферментационному оборудованию нового поколения. В настоящее время ведутся исследования по использованию функциональных мембран с активными переносчиками, иммобилизованными ферментами, аффинными сорбентами и т.д. В настоящий момент применение мембранных реакторов тормозится определенным дефицитом мембранных материалов и необходимостью ломки традиций и стереотипов.
9. ПОЛИМЕРНЫЕ БИОМАТЕРИАЛЫ
Под полимерными биоматериалами обычно понимают полимерные материалы и изделия из них, которые используются в медицине или биотехнологии. Такие материалы часто получают путем целенаправленного модифицирования хорошо известных полимеров. За последние годы значительно возросли ассортимент, масштабы производства и значение биоматериалов.
Радиационно-химическая технология в настоящее время стала одним из наиболее эффективных способов получения полимерных биоматериалов. Работы по использованию радиационно-химических методов для синтеза полимерных биоматериалов проводятся в следующих направлениях: радиационное модифицирование различных полимеров и изделий из них с целью получения гемосовместимых (длительно работающих в контакте с кровью) полимеров, полимерных сорбентов, протезов сосудов и т.д.; иммобилизация различных биологически активных веществ (БАВ) (ферменты, лекарства и т.д.) в полимерные матрицы с использованием радиационной полимеризации; радиационно-химический синтез полимеров-носителей лекарственных препаратов; радиационное сшивание полимеров с целью получения механически прочных гидрогелей (носители БАВ, перевязочные материалы глазные линзы и т.д.). Преимуществом радиационно-химических методов получения полимерных биоматериалов по сравнению с традиционными является чистота материалов (нет необходимости добавлять дополнительные ингредиенты (инициаторы полимеризации) при синтезе), возможность проведения процессов при пониженных температурах и легкость регулирования скорости процессов путем изменения мощности дозы излучения. Достоинством радиационно-химических методов является также то, что биоматериалы в некоторых случаях можно стерилизовать на тех же источниках ионизирующих излучений, которые уже были использованы для их получения. Необходимо отметить, что в большинстве случаев для получения полимерных биоматериалов требуются небольшие дозы излучения, как правило, не превышающие 30 кГр, что позволяет использовать источники излучений невысокой мощности.
Недостатком радиационно-химических методов является необходимость применения, как правило, сравнительно дорогостоящих и сложных в эксплуатации источников γ-излучения и электронных ускорителей.
9.1.Получение гемосовместимых полимерных материалов
Получение гемосовместимых полимерных материалов - весьма сложная проблема. При контакте полимеров кровью инициируются биохимические реакции, вызывающие изменение физиологических функций крови, «запускается» свертывающая система крови с последующим тромбообразованием на поверхности полимера. Важными факторами, повышающими гемосовместимость полимеров, являются такие их свойства, как минимальная способность к адгезии и агрегации тромбоцитов, отсутствие активации контактных факторов свертывания крови, участие в реакции лизиса образующегося тромба и селективная способность к адсорбции белков плазмы крови, в особенности альбумина. Согласно современным представлениям, первой стадией при контакте полимера с кровью является быстрая сорбция белков из плазмы крови. Природа и конформационное состояние белка определяют последующие биохимические реакции.
Проблемы сорбции белков на различных полимерных поверхностях рассматривались в многочисленных исследованиях. К сожалению, в настоящее время уровень наших знаний не позволяет достаточно эффективно прогнозировать природу и свойства полимерной поверхности, полностью удовлетворяющей требованию гемосовместимости.
Из изложенного ясно, что для получения гемосовместимых материалов поверхность полимеров необходимо модифицировать. С этой целью:
1. Создают полимеры с поверхностями, обладающими пониженной адсорбционной способностью по отношению к белкам и близкими по своей природе к естественной среде организма. В основном это гидрогелевые поверхности
2. Создают полимерные материалы с определенной доменной структурой поверхности (полиуретаны).
3. Создают углеродные полимерные материалы (полиацетилены).
4. Создают полимеры, поверхность в которых по своей природе моделирует антикоагулянты крови), что достигается введением в поверхностные слои полимеров сульфо- и карбоксильных групп, созданием отрицательного заряда на поверхности полимеров). Чаще всего стараются получить гепариноподобную поверхность, так как широко распространенный метод получения гемосовместимых материалов путем введения гепарина имеет ряд недостатков, обусловленных частичной утратой активности гепарина при ковалентной иммобилизации, его слабой антикомплементной активностью и биодеструкцией.
5. Вводят в поверхностные гидрогелевые слои физиологически активные вещества (антикоагулянты крови, ферменты и т.д.), взаимо-действующие с компонентами крови и приостанавливающие процесс тромбообразования.
При выборе метода модифицирования поверхности полимеров необходимо учитывать, что основные физико-механические показатели исходного полимера при модифицировании не должны существенно измениться. Одним из наиболее эффективных методов модифицирования полимеров является радиационная прививочная полимеризация.
Достоинствами ее как метода модифицирования полимерных материалов с целью повышения их гемосовместимости являются, во-первых, высокая универсальность, позволяющая в широком диапазоне температур модифицировать практически любые полимерные материалы (шовный материал, катетеры, трубки, таблетки, порошки, трансплантаты и т.д.); во-вторых, возможность создания на поверхности полимеров модифицированных слоев различной толщины. Толщина слоя зависит от условий проведения прививочной полимеризации — мощности дозы, выбора растворителя для мономера и т.д. При этом модифицированный слой прочно связан с подложкой и не отмывается при контакте со средой живого организма.
Все это способствует достаточно широкому использованию радиационной прививочной полимеризации для решения проблем, связанных с повышением гемосовместимости различных полимерных материалов и изделий из них. Основной задачей таких исследований является создание полимеров с функционализированной поверхностью, определенными гидрофильно-гидрофобными свойствами и отрицательным зарядом на поверхности. Значительное количество работ выполнено по модифицированию различных полимеров с использованием высокогидрофильных мономеров, таких как N-винилпирролидон, 2-гидроксиэтил-метакрилат, акриламид и его производные. В ряде исследований для модификации брали достаточно сложные сополимеры. Так, для производства протезов сосудов использовали, в основном, полиуретаны, полиэфиры и натуральный каучук.
Радиационную прививочную полимеризацию в большинстве случаев осуществляли прямым методом из водно-спиртовых растворов при небольших дозах облучения. В некоторых случаях, особенно при прививке акриламида, применяли метод с предоблучением.
В результате проведенных работ получены разнообразные модифицированные полимерные материалы с гидрогелевыми поверхностями. Эти материалы достаточно прочны, мягки и обладают высокой набухаемостью в воде. Биомакромолекулы в таких материалах характеризуются повышенной диффузией. Полимерные гидрогели, полученные радиационно-химическими методами, испытаны на гемосовместимость в экспериментах in vitro и in vivo на обезьянах, овцах и собаках. В обобщенном виде испытания на гемосовместимость радиационно-привитых полимерных гидрогелей показали следующее: с повышением содержания воды от 15 до 85% происходит уменьшение сорбции белков и повышается скорость десорбции, на гидрогелях имеет место тромбообразование, но связь тромбов с гидрогелевой поверхностью заметно ослаблена по сравнению с их связью с немодифицированными полимерами. Существенно важным является значительное понижение поверхностного натяжения между гидрогелем и водным раствором. Гидрогелевое покрытие на полимерах должно быть приготовлено из очень чистых мономеров. Так, незначительная примесь метакриловой кислоты б 2-гидроксиэтилметакрилате значительно ухудшает качество гидрогелевого покрытия и его гемосовместимые свойства.
Интересные результаты были получены при изучении радиационно привитых на полиэтилен (ПЭ) сополимеров 2-гидроксиэтилметакрилата (гидрофильный мономер) с этилметакрилатом (гидрофобный мономер). При низком содержании воды (~ 10%) указанные привитые сополимеры характеризовались неожиданно низкими показателями адсорбции тромбоцитов, что было обусловлено не содержанием воды, а составом сополимера. При более высоком содержании воды адсорбция тромбоцитов обратно пропорциональна содержанию воды. Очевидно, что состав сополимера и состояние воды в нем имеют важное значение. Поверхность радиационно-привитых сополимеров очень неоднородна (имеются бугры, выступы и т.д.), толщина модифицированного слоя, как правило, 15-45 мкм. Предполагается, что для повышения гемосовместимости необходимо определенное сочетание на поверхности гидрофильных и гидрофобных участков.
9.2. Использование радиационного сшивания для получения полимерных биоматериалов
В настоящее время существенно возрос интерес к получению полимерных биоматериалов путем радиационного сшивания. Этот метод наиболее часто применяется для получения гидрогелей, главным образом на основе полиакриламида, поливинилового спирта, полиэтиленоксида и поли(N-винилпирролидона). Преимуществом радиационного сшивания является сравнительная простота выполнения, возможность широкого регулирования густоты сетки путем подбора условий облучения (мощность дозы, доза), возможность использования пониженных температур, чистота получаемого продукта (отсутствие инициаторов) и одновременная стерилизация. Радиационно-сшитые гидрогели используются как носители БАВ (ферменты, лекарства и т.д.) в качестве имплантантов, протезов, глазных линз, медицинских мембран, перевязочных материалов и биологических сред для изучения и культивирования микроорганизмов.
На основе радиационно-сшитого поливинилового спирта получены биомембраны для селективного транспорта макромолекул, а также материалы, использующиеся в качестве суставных хрящей. Показана перспективность использование гидрогелей поливинилового спирта в качестве перевязочного материала и отмечено его преимущество перед марлей: гомогенная адгезия по всей ране и легкое удаление без повреждения кожи.
Гидрогели на основе поли(N-винилпирролидона) обладают высокой гидрофильностью и хорошей биосовместимостью и могут использоваться в качестве материала для лечения ожоговых ран и трофических язв. Данные материалы продаются в Польше под торговыми марками “HDR” и “AQUA-Gel”. Разработана терапевтическая система на основе геля поли(N-винилпирролидона) для использования в акушерской практике для ускорения родов и производства абортов. В этом случае гель представляет собой тонкий стержень, содержащий простагландин.
Технология получения гидрогелей для перевязочных материалов в настоящее время достаточно подробно разработана, и они прошли широкие клинические испытания. Важно, что есть возможность получать гели для перевязок, содержащие лекарственные препараты (например, хлорамфени-кол). При больших ранениях такой гидрогель существенно эффективней обычных перевязочных материалов.
В медицине применяются покрытия силиконового каучука коллагеном с последующим радиационным сшиванием и стерилизацией. Другим природным продуктом, который используется для получения биоматериалов, является желатин. Изучен радиолиз желатины, выявлены условия образования пространственных структур при облучении ее растворов. Предложено использовать радиационно-сшитую композицию поливинилового спирта с желатином в качестве перевязочного материала.
Радиационное сшивание использовано для изготовления медицинских изделий из полисилоксанов: биологически инертных пористых шнуров, шприцованных трубок, капилляров и разных имплантантов. При радиационном сшивании полидиметилсилоксана в особочистых условиях существенно повышается его гемосовместимость. Радиационносшитый поливинилметилсилоксан использован для изготовления тонких мембран для получения лекарственных препаратов (например, левоноргистрел).
Радиационное сшивание транс-1,4-полиизопрена использовано для создания термоусадочных материалов для связывания крупных кровеносных сосудов. Материалы прошли широкие испытания in vitro и in vivo (на собаках). Радиационное модифицирование позволяет улучшить свойства медицинских протезов на основе полиолефинов. С использованием радиационного сшивания получены также полимерные биоматериалы, обладающие повышенной адгезией к коже человека.
В Израиле налажен выпуск синтетического перевязочного материала, получаемого путем радиационной прививки гидрофильных мономеров на полиуретан. Материал водонепроницаем, прозрачен, хорошо прикрепляется к коже и пропускает лекарства. Материал выпускается под названием «Омидерм».
Разработаны методы получения искусственной роговой оболочки и контактных линз с высокой набухаемостью в воде на основе радиационно-сшитого поливинилового спирта с добавкой хондроитинсульфата натрия. Для существенного повышения проницаемости контактных линз по кислороду предложено облучать их ускоренными тяжелыми ионами массой 2-100. С использованием радиационной полимеризации созданы гидро-гелевые материалы для мягких контактных линз. Эти материалы производятся в КНР.
Для создания офтальмологических материалов нашел применение радиационно-сшитый коллаген, выделенный из склеры глаза животных. Этот материал использован для создания временных аллодренажей при антиглаукоматозных операциях.
Несомненно, что в ближайшие годы можно ожидать появления на рынке новых полимерных биоматериалов, полученных с использованием методов радиационной полимеризации.
9.3. Получение полимерных имплантантов
Технические приемы и методы, которые используются в радиационной полимеризации могут быть применены для получения различного рода имплантантов, главным образом для лечения пораженных участков кожи, а также для создания протезов. Разработаны методы получения имплантантов коллагена путем облучения смеси мономеров или полимеров с коллагеном. Имплантанты хорошо совместимы с кровью и не вызывают воспалений. Имплантанты применяются в хирургии и могут использоваться как субстраты в биотехнологии. Изучены протезы на основе полиэфируретана с радиационно модифицированной внутренней поверхностью. Модифицирование осуществлялось путем радиационной прививки 2-гидрокси-метилакрилата или акриламида на внутреннюю поверхность трубок. Протезы изучались in vivo. Исследованы гистологические и механические свойства протезов. Установлена их повышенная тромборезистентность. Разработан метод модифицирования наполнителей для полимеров, используемых в зубоврачебной технике. Наполнители на основе стеклянных или кварцевых волокон модифицированы радиационной прививкой акриловой кислоты из паровой фазы. Подробно изучены физико-механические свойства смол, содержащих различное количество модифицированного наполнителя. Отмечены преимущества используемого модифицированного наполнителя по сравнению с наполнителем, модифицированным силанами. С использованием облучения смесей глинозема с акриловой кислотой созданы полимерно-керамические материалы для стоматологии. С помощью радиационной прививочной полимеризации созданы имплантанты для лечения кожи на пораженных ожогом участках человеческого тела. Для этой цели обычно используют силиконовый каучук, модифицированный прививкой гидрофильных мономеров или модифицированный вулканизованный натуральный каучук. С использованием радиационной технологии создан метод гидрофилизации силиконовых контактных глазных линз. В результате гидрофилизации краевой угол снижается с 150° до 20°, а эффект гидрофильности сохраняется длительное время. Радиационно-модифицированные полимеры использованы для инициирования роста различных клеток
9.4. Иммобилизация лекарственных препаратов
В области использования радиационной полимеризации для иммобилизации лекарственных веществ наибольшие успехи достигнуты при иммобилизации противоопухолевых составов в полимерные матрицы. В качестве противоопухолевых веществ используются адриамицин, митомицин-С и 5-фторурацил. В ряде случаев лечение иммобилизованными противоопухолевыми препаратами сочетается с гормонотерапией. Иммобилизованные противоопухолевые вещества, как правило, используются в виде полимерных таблеток или игл, которые вводятся в опухоль. Применение иммобилизованных противоопухолевых препаратов имеет следующие преимущества по сравнению с их введением в виде инъекций или орально: небольшая концентрация лекарственных препаратов в крови, лекарство распределяется непосредственно в небольшой области от введенного препарата. При этом имеет место некроз раковых клеток в пределах 0.5-1 см2 около образца, а диффузия противоопухолевых препаратов прекращается в некрозном слое. Это сводит к минимуму побочные эффекты от применения лекарств. Длительность использования иммобилизованных противоопухолевых препаратов — несколько месяцев. При этом скорость выделения лекарств не изменяется. Такие препараты прошли широкие испытания во многих клиниках Японии.
Для иммобилизации противоопухолевых препаратов обычно используют различные сополимеры и композиции полиэтиленгликоль-метакрилатов с различными полимерами (полистирол, поливинилформаль, полиэтиленгликоль, полиметилметакрилат, полиэтиленоксид). Подчеркивается, что облучение необходимо проводить в бескислородной среде, а доза не должна превышать 10 кГр, в противном случае активность противоопухолевых препаратов существенно снижается
Скорость выделения лекарств регулируют введением в полимерную матрицу порообразующего агента или адсорбента (например, активированного угля).
Технология использования иммобилизованных противоопухолевых препаратов может быть улучшена за счет варьирования гидрофильно-гидрофобных свойств полимерной матрицы, а также использования биодеградируемых полимеров (полипептиды или полилактиды).
В Пастеровском институте (Париж) в рамках программы Международ-ного агенства по атомной энергии (МАГАТЭ) проведены исследования с иммобилизованными моноклональными антителами. Иммобилизация последних осуществлена путем низкотемпературной полимеризации 2-гидроксиэтил-метакрилата. Чувствительность реакций иммобилизованного антитела с антигеном зависит от выбора мономера и его концентрации для создания пористой среды. Важной проблемой является минимизация неспецифических реакций полимерного носителя с антигеном. Для этого необходимо увеличивать гидрофобность полимерной матрицы. Иммобилизованные препараты обычно изготавливаются в виде микросфер или микрокапсул. Для иммобилизации антител используются также микросферы, получаемые полимеризацией акролеина или его сополимеры с 2-гидроксиэтилметакрилатом или метакриловой кислотой.
Преимуществом радиационной полимеризации для иммобилизации антител является достаточно высокая чистота получаемого продукта. Эти препараты можно использовать для иммунологического анализа.
Проведены исследования по иммобилизации антагониста кальция в предварительно полимеризованный гель поли (2-гидроксиэтилметакрилата). Путем радиационного сшивания геля и добавок метилметакрилата и N-винилпирролидона можно широко варьировать скорость выделения лекарства.
Исследована иммобилизация гидрокортизона в гели, полученные радиационной полимеризацией акриловой кислоты. Скорость выделения регулируется дозой облучения и обработкой гелей ацетатом цинка.
9.5. Иммобилизация компонентов крови
Одной из актуальнейших проблем в настоящее время является создание искусственных кровезаменителей, которые могли бы длительное время храниться при обычных условиях не требуя сложной и дорогой аппаратуры. Одним из наиболее перспективных направлений является иммобилизация различных компонентов крови в полимерные композиции с использованием прежде всего радиационных методов полимеризации.
Так гемоглобин был иммобилизован в полимерную матрицу из поли(2-гидроксиэтилметакрилата) с использованием радиационной низкотемпера-турной полимеризации. Особое внимание было уделено выбору оптимальных условий иммобилизации для защиты гемоглобина. Гемоглобин удобен для изучения состояния иммобилизованной молекулы в полимерной матрице, так как он имеет характерное оптическое поглощение. Гемоглобин в мембране подвергался обратимой оксигенации, которая имеет почти то же самое значение, что и в нативном гемоглобине. Описан способ получения полу-синтетической крови на основе иммобилизованного карбоксигемоглобина.
В работах для иммобилизации гемоглобина использована радиационная полимеризация фосфолипидов. Фосфолипиды содержали две длинные полимеризуемые октадекадиенильные группы. Искусственные красные кровяные клетки были получены путем капсулирования гемоглобина с использованием радиационной полимеризации бислойных фосфолипидов — липосом. Искусственные кровяные клетки оказались механически стабильными, легко выдерживали замораживание. Кислородный транспорт подобных систем оказался подобен транспорту нативного гемоглобина. Проводились испытания in vivo (мыши), которые указали на биосовместимость таких клеток.
9.6. Получение «умных» полимеров и их использование для иммобилизации биологически активных веществ
За последние годы все возрастающее значение для медицины и биотехнологии приобретают «умные» полимеры. Так называют полимеры, способные реагировать (сжиматься или набухать) на небольшие изменения во внешней среде (температура, рН, электрическое поле и т.д.). «Умные» полимеры с иммобилизованными БАВ используются для выделения лекарств при определенных условиях, как правило, при заданной температуре или рН. Обычно «умные» полимеры получают традиционными методами, однако в последнее время, для этой цели стала использоваться также радиационная полимеризация. Среди «умных» полимеров наибольшее число публикаций посвящено поли(N-изопропилакриламиду) (поли-N-ИПАА). Данный полимер имеет в воде нижнюю критическую температуру растворения (НКТР) ~32°С, т.е. близкую к температуре человеческого тела. Выше 32°С происходит фазовое разделение, обусловленное конформационным переходом макромолекулы поли-N-ИПАА из рыхлой глобулы в компактный клубок, что сопровождается резким уменьшением размеров макромолекулы.
Было изучено поведение гидрогелей, полученных на основе поли(N-изопропилакриламида) и скорость диффузии иммобилизованных в них лекарственных препаратов в условиях имитирующих человеческий организм. Было установлено, что при 370С и рН=1,4 (нормальные условия в желудке человека) происходит медленное выделение иммобилизованных в гидрогель индометацина и амилазы, но при изменении величины рН до 7,4 (условия в кишечнике) выделение лекарств значительно ускоряется. Таким образом, можно создавать лекарственные формы, позволяющие доставлять препарат к пораженному органу без значительных потерь.
Другим направлением использования таких “умных” полимеров является создание сигнал-чувствительных систем, состоящих из биосенсора, активатора и резервуара для коррекции нарушений в работе различных органов в организме человека. Так для больных диабетом разрабатываются специальные системы с биосенсором на глюкозу, которые запускаются по принципу включение - выключение для выделения определенных порций инсулина, иммобилизованного в гелях, т.е. работающие по принципу поджелудочной железы.
10. ЛАБОРАТОРНЫЙ ПРАКТИКУМ
