Анализ клинической картины и оптимизация терапии аффективных расстройств при хронических заболеваниях
| Вид материала | Автореферат |
СодержаниеПримечание: * - p Развитие аффективного расстройства (Y |
- С. В., Софронов А. Г. Особенности клинической картины осложненных алкогольной зависимостью, 124.63kb.
- Н. А. Корнетов, А. Н. Корнетов,, 1189.39kb.
- Клиническая эффективность йодантипирина в терапии хронических гепатитов в и с эффективность, 114.07kb.
- Рабочая программа по военно-полевой терапии для специальности, 630.47kb.
- Н. А. Корнетов Отделение аффективных состояний, 552.8kb.
- Рабочая программа Для специальности: 060108 «Фармация» Факультет, 730.02kb.
- Учебно-методический комплекс махачкала 2009 Рабочая программа по госпитальной терапии, 375.26kb.
- Тема: Лечебная физкультура при заболеваниях органов пищеварения, 34.59kb.
- Квалификационные тесты по клинической трансфузиологии для врачей общей клинической, 187.56kb.
- Исследование клинической динамики посттравматических стрессовых расстройств (птср), 534.59kb.
Таблица 4
Клинические проявления аффективных расстройств,
выявленных при язвенной болезни двенадцатиперстной кишки
и бронхиальной астме (в % к итогу в каждой группе)
| Клинические проявления аффективного расстройства | Язвенная болезнь двенадцатиперстной кишки, % | Бронхиальная астма, % | Уровень значимости |
| Тревога | 80 | 75 | p<0,01 |
| Эмоциональная лабильность | 48 | 53 | p>0,01 |
| Дисфория | 13 | 7 | p<0,01 |
| Тоска | 10 | 18 | p<0,05 |
| Апатия | 12 | 11 | p<0,01 |
| Страх | 10 | 12 | p<0,05 |
Таблица 5
Продолжительность депрессивного эпизода
при язвенной болезни двенадцатиперстной кишки и бронхиальной астме
( в % к итогу в каждой группе больных)
| Соматическое заболевание | Продолжительность депрессивного эпизода | ||
| 1 – 6 месяцев | 6 – 12 месяцев | 12 месяцев и более | |
| Язвенная болезнь двенадцатиперстной кишки | 47,61±0,21* | 28,72±0,51* | 23,81±0,24* |
| Бронхиальная астма | 50,00±0,01 | 29,171,09** | 20,81±0,10 |
| Контрольная группа | 4,12±0,41** | 6,94±0,31** | 89,01±1,01* |
Примечание: * - p<0,01; ** - р<0,05
В психопатологическом плане структура тревожно-депрессивного синдрома при язвенной болезни и бронхиальной астме характеризовалась статистически достоверными (р<0,05) симптомами как ситуационная тревога, эмоциональная неустойчивость, эмоциональная слабость и двигательное возбуждение.
Большинство из выделенных признаков обнаруживало наличие тесной связи с экзогенными и, в частности, ситуационными факторами.
Пациенты с признаками «маскированной» депрессии предъявляли жалобы на симптоматику, практически резистентную для традиционных методов лечения соматического заболевания.
Результаты клинико-психологического исследования сравнивались с данными, полученными в результате анализа психопатологической карты.
При исследовании тревоги и депрессии с помощью госпитальной шкалы (HADS) у 27,2% больных язвенной болезнью выявлялась клинически выраженная тревога (11,80,4 балла), субклиническая тревога была отмечена у 10,4% (8,60,5 балла). В процентном соотношении подгруппа пациентов с депрессией в 77,1% случаев имела показатели клинически выраженной тревоги, субклиническая тревога отмечалась у 22,9% обследованных этой группы. В контрольной группе отмечалась выраженная депрессия и показатели по тревоге и депрессии соответственно 12,40,7 и 14,40,6 балла. Уровень значимости (р<0,05).
На основании опросника Смишека определялась акцентуация характера пациентов. Различия статистически достоверны во всех группах (р<0,01).
При язвенной болезни независимо от наличия или отсутствия аффективных расстройств незначительно доминировал дистимический тип личности (24,7% больных). Демонстративный тип личности был обнаружен у 19,5% обследуемых пациентов, педантичный тип акцентуации отмечался у 16,24% обследуемых.
По Смишеку большинство больных с бронхиальной астмой имело демонстративный тип характера, который отмечался у 39,1% обследуемых, реже встречался застревающий тип акцентуации - 20,8% случаев, дистимический тип был определен у 17,5% больных.
В результате исследования реактивной и личностной тревожности с использованием шкалы Спилбергера-Ханина было установлено, что у значительного числа пациентов с язвенной болезнью (30,5%) статистически достоверно (р<0,01) имелся высокий уровень тревоги по шкале личностная тревога (средний балл - 50,21±3,4). Среди них в подгруппе с аффективными расстройствами было 25 человек (52,1% в собственной подгруппе), в подгруппе без аффективных расстройств 24 пациента (22,11%). В результате исследования реактивной и личностной тревожности с использованием шкалы Спилбергера-Ханина у 45 (37,5%) пациентов с бронхиальной астмой был выявлен высокий уровень тревоги по шкале личностная тревога (средний балл - 48,21±3,1). Среди них в подгруппе с аффективными расстройствами было 30 пациентов (71,4% в собственной подгруппе), в подгруппе без аффективных расстройств - 15 человек (14,1%).
У большинства лиц, страдающих соматическими заболеваниями, результаты реоэнцефалографии и компьютерной томографии не выявили каких-либо специфических особенностей по сравнению с больными контрольной группы.
Для пациентов с язвенной болезнью и бронхиальной астмой было характерно нарушение синхронизации биоэлектрической активности мозга (ЭЭГ). Наиболее существенным фактом при язвенной болезни (57,3% случаев) и при бронхиальной астме (53,3% наблюдений) также как и в контрольной группе (79,5%), полученным при регистрации фоновой ЭЭГ, явилось депрессия альфа - ритма в сочетании с нарастанием индекса бета - активности (р<0,05).
Данные, полученные с помощью кардиоинтервалографии, свидетельствовали о том, что для большинства пациентов с язвенной болезнью двенадцатиперстной кишки было характерно доминирование тонуса парасимпатического отдела вегетативной нервной системы (92 пациента - 60,5%), причем преобладание парасимпатических реакций более заметно проявлялось в группе пациентов с аффективными расстройствами (77,72%). Кардиоинтервалография у пациентов с бронхиальной астмой также установила преобладание тонуса парасимпатического отдела вегетативной нервной системы (80 пациентов - 66,7%), причем в группе пациентов с аффективными расстройствами ваготония была зарегистрирована в 78,57% случаев.
Сравнение групп пациентов с благоприятным течением бронхиальной астмы и язвенной болезни двенадцатиперстной кишки показало, что по абсолютному большинству медико-социальных характеристик и показателей психологического статуса достоверные различия отсутствуют, что говорит о возможности реализации единых подходов к оптимизации терапии аффективных расстройств при различных соматических заболеваниях.
В пятой главе анализируется эффективность использования различных видов медикаментозной терапии и эклектичной психотерапии при лечении аффективных расстройств у больных с соматическими заболеваниями.
Для обоснования использования антидепрессантов при лечении аффективных расстройств у больных с хроническими соматическими заболеваниями в терапевтическую фазу программы межрегионального клинико-эпидемиологического исследования было включено 3506 пациентов. При этом 1558 (44,4 %) пациентов в дополнение к рекомендованной по поводу соматического заболевания терапии получали пиразидол (основная группа) и 1948 (55,6 %) – терапию без антидепрессанта (контрольная группа). Сравнение пациентов по ведущим медико-социальным характеристикам не выявило значимых различий между основной и контрольной группами.
Восьминедельная терапия пиразидолом в суточной дозе 75 мг (50 мг у больных старше 70 лет) привела к существенному улучшению психического состояния больных. Суммарный балл CES-D снизился на фоне лечения в среднем на 13,18±0,24 баллов (на 45,10±0,18 %) – с 29,22±0,58 до 16,04±0,35 баллов (t=54,2612, p<0,0001). В контрольной группе существенного изменения этого показателя не произошло, снижение составило всего 3,16±0,11 балла (11,30±0,34 %) – с 27,98±0,37 до 24,82±0,32 баллов (t=18,0058, p<0,0001). Снижение суммарного балла CES-D в основной группе достоверно отличается от его снижения в контрольной группе (t=105,6200; p<0,0001). Полная редукция аффективных (депрессивных) расстройств (снижение суммарного балла CES-D до 18 и ниже) на фоне лечения пиразидолом имела место у 62,72±0,42 % пациентов. Закономерно, что более выраженный эффект лечения был характерен для больных со сравнительно нетяжелыми психопатологическими состояниями. Снижение суммарного балла CES-D до 18 и ниже отмечено у 81,20±0,56 % пациентов, набравших 18-24 балла и выше – у 53,30±0,58 % больных соответственно (t=95,6962, p<0,0001). В контрольной группе полная редукция депрессивных расстройств отмечалась всего у 17,74±0,32 % пациентов.
Таким образом, полученные результаты подтвердили обоснованность и высокую эффективность использования антидепрессантов (в частности, пиразидола) при лечении аффективных расстройств у больных с хроническими заболеваниями.
Для оценки терапевтической эффективности различных групп антидепрессантов (селективных ингибиторов обратного захвата серотонина (СИОЗС), селективных стимуляторов обратного захвата серотонина (ССОЗС) и обратимых ингибиторов моноаминооксидазы типа А (ОИМТА)) в зависимости от типа аффективного расстройства при хронических соматических заболеваниях в течении двух лет на различных клинических базах г. Воронежа и области в разные периоды проходили клиническое изучение прозак (флуоксетин), пиразидол и коаксил . Всего этими препаратами прошли курсовое лечение 90 пациентов, страдающих язвенной болезнью двенадцатиперстной кишки и бронхиальной астмой, которые в период лечения находились в возрасте от 20 до 50 лет.
Оценка терапевтического действия всех препаратов и динамика депрессивного состояния в ходе лечения осуществлялась методом клинического наблюдения за больными, а также по унифицированной схеме с помощью международной шкалы депрессий Гамильтона (HAM-D).
Полученные данные показали особенности психотропной активности каждого из трех рассматриваемых препаратов, которые касались как преобладающих компонентов действия в спектре их антидепрессивного влияния, степени их выраженности, так и особенностей и скорости их выявления в динамике на лечении. Обнаруженные индивидуальные характеристики анализируемых антидепрессантов нашли подтверждение при сопоставлении степени их терапевтического эффекта и клинических характеристик самого депрессивного состояния, с учетом типологии депрессии (табл. 6).
Таблица 6
Соотношение терапевтического эффекта антидепрессантов и типа
депрессивного состояния (общий/«значительный» в % в числу больных)
| Антидепрессант | Тип депрессии | ||
| адинамическая | тоскливая | тревожная | |
| ССОЗС (Коаксил) | 88,9 / 77,8 | 100,0 / 100,0 | 89,5 / 68,4 |
| ОИМТА (Пиразидол) | 42,8 / 42,8 | 50,0 / 50,0 | 100,0 / 90,0 |
| СИОЗС (Флуоксетин) | 78,6 / 7,2 | 75,0 / 25,0 | 70,6 / 47,1 |
Данный факт подтверждает целесообразность дифференцированного подхода при назначении антидепрессивной медикаментозной терапии: при тревожной депрессии препаратами выбора являются ОИМАО-А, при тоскливой – ССОЗС, при адинамической – СИОЗС.
Для повышения эффективности лечения к проводимой медикаментозной терапии предложено добавить эклектичную психотерапию, сочетающую приемы личностно-ориентированной и рациональной терапии. Совместно с сертифицированными специалистами по психотерапии Воронежского областного психоневрологического диспансера на первом этапе психотерапии разбиралась «структура и содержание личностного конфликта», учитывались ценностные ориентации больного, влияющие на стабильность и возможность разрешения данного конфликта. На следующем этапе осуществлялась постепенная корректировка ценностей больного, его установок, «изменение отношения к причинам конфликтов», коррекция внутренней картины болезни путем «разъяснения, убеждения и перевоспитания» пациента, расширения его кругозора, более активного включения в социальную жизнь. Данный вариант психотерапии сочетался с системой психологической коррекции, включающей в себя тренинг социальных навыков.
Для оценки эффективности комбинированной терапии были сформированы 4 выборки равного объема в соответствии с предполагавшимся методом лечения: а) фармакологическая терапия; б) психотерапия; в) комбинированная фармакологическая терапия и психотерапия; г) плацебо-контроль. Режим терапевтического воздействия рационально корректировался в зависимости от клинической оценки состояния пациента на момент каждого из еженедельных осмотров. Применялись психотропные средства из группы антидепрессантов (коаксил, флуоксетин, пиразидол), рекомендованные для лечения аффективных расстройств при психосоматических заболеваниях.
Результаты исследования подтвердили эффективность использования комбинированного подхода, включающего медикаментозную терапию с учетом типологии аффективного расстройства и разработанный вариант эклектичной психотерапии (табл. 7).
Таблица 7
Сравнительная эффективность различных вариантов терапии аффективных расстройств, встречающихся при хронических соматических заболеваниях, в %
| Метод лечения | Язвенная болезнь двенадцатиперстной кишки | Бронхиальная астма |
| Базисная терапия соматотропными препаратами | 16,1 | 15,5 |
| Терапия психотропными средствами + базисное лечение | 59,6 | 67,6 |
| Психотерапия + базисное лечение | 44,5 | 47,5 |
| Комбинированная терапия | 81,5 | 84,7 |
В шестой главе представлены элементы системы интеллектуальной поддержки деятельности врача при выборе рациональной терапии аффективных расстройств при психосоматических заболеваниях.
На основе оптимизированного набора наиболее значимых факторов риска разработаны прогностические модели развития аффективного расстройства, определения его типа и тяжести.
Развитие аффективного расстройства (Y1):
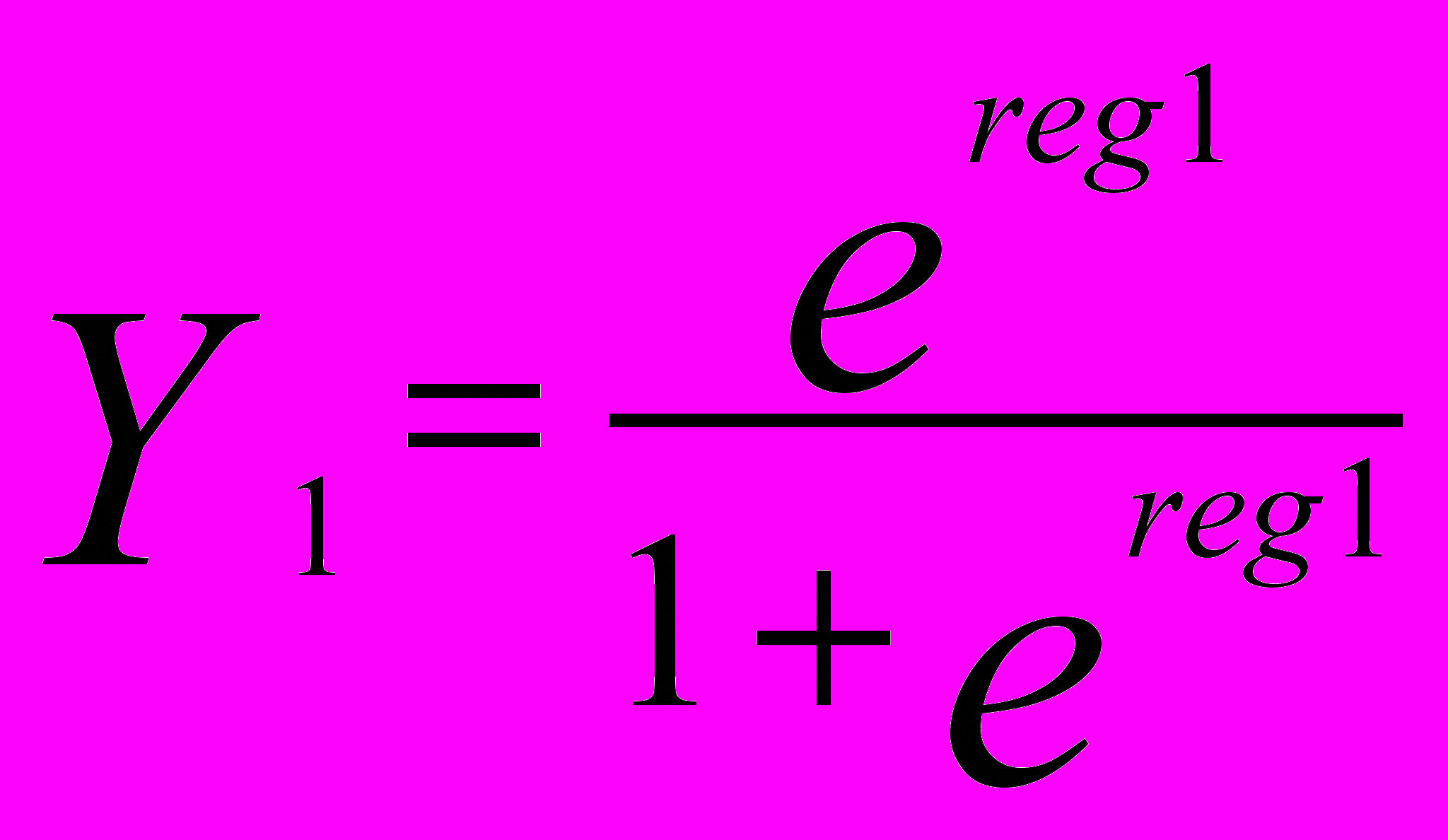 ,
,reg1 = -9,2654 - 3,8685*X1 – 2,3577*X2 + 5,3119*X3 + 0,5387*X4 +
+ 1,4331*X5 + 0,1272*X6
где X1 – пол; X2 – профессиональный статус; X3 – отягощенная наследственность по остальным заболеваниям; X4 – наличие психотравм; X5 – тип акцентуации; X6 – реактивная тревожность.
Степень тяжести депрессии по Гамильтону (Y2):
Y2 = 0,33231*X6 – 6,2929*X1*X5 – 0,088433*X1*X6 + 6,7419*X2*X5 +
+ 9,1748*X3*X4 – 0,1078*X3*X6
где X1 – пол; X2 – возраст; X3 – проф. статус; X4 – наследственность по психическому заболеванию; X5 – цереброорганические факторы; X6 – личностная тревожность.
Длительность депрессии (Y3):
Y3 = -0,0333 – 0,1755*X1 + 0,0008*X2 – 0,0862*X3 + 0,2074*X4 + 0,0288*X5 + + 0,0029*X6 + 0,0774*X7
где X1 – пол; X2 – возраст; X3 – проф. статус; X4 – отягощенная наследственность по остальным заболеваниям; X5 – наличие психотравм; X6 – реактивная тревожность; X7 – неврологическая симптоматика.
Тип депрессии (Y4 – тревожный, Y5 – тоскливый, Y4 – адинамический):
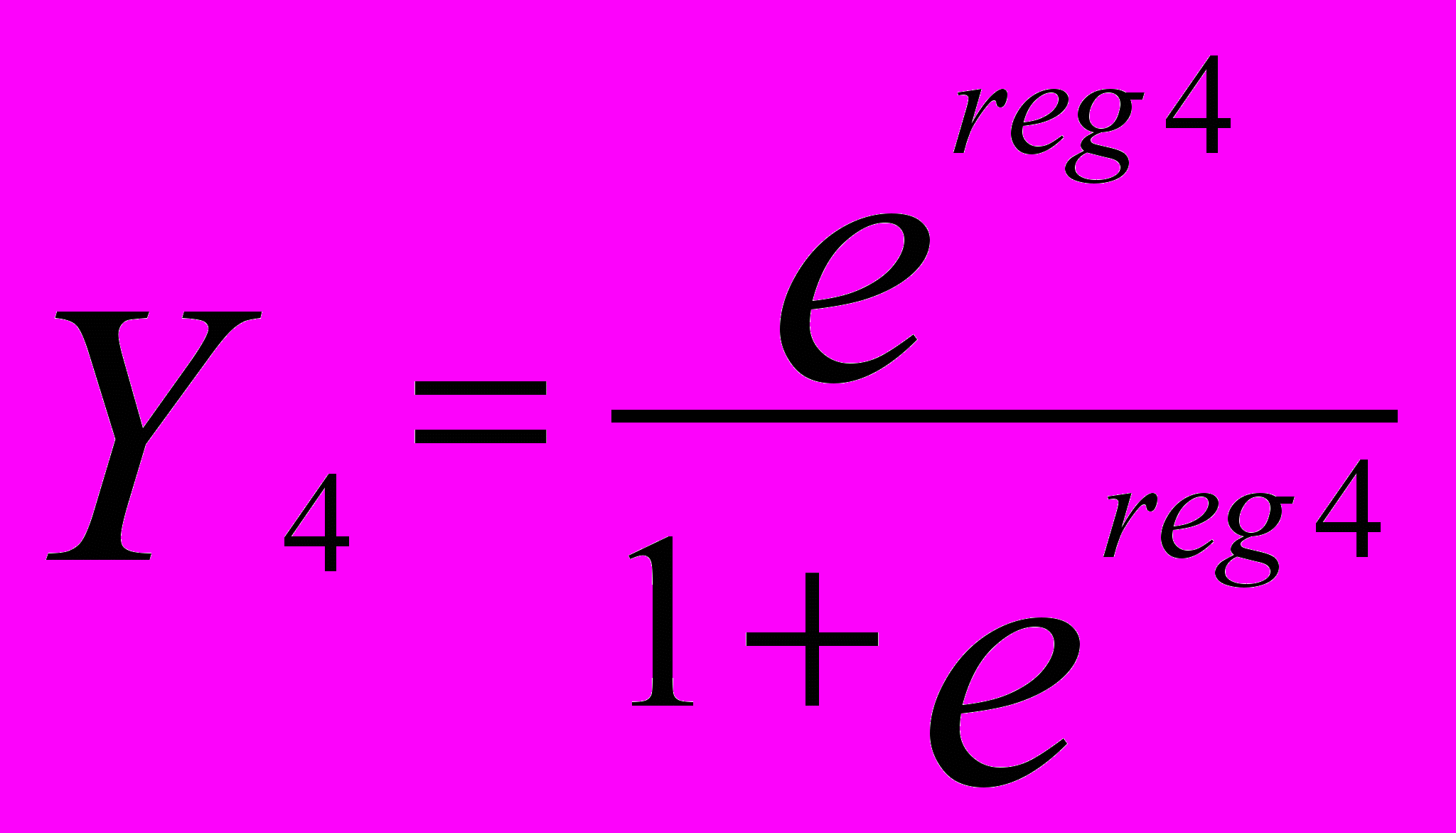 ,
,reg4 = -6,1914 – 0,8003*X1 + 0,8827*X2 + 0,0092*X3 + 0,6947*X4 +
+ 0,2608*X5 + 0,1229*X6
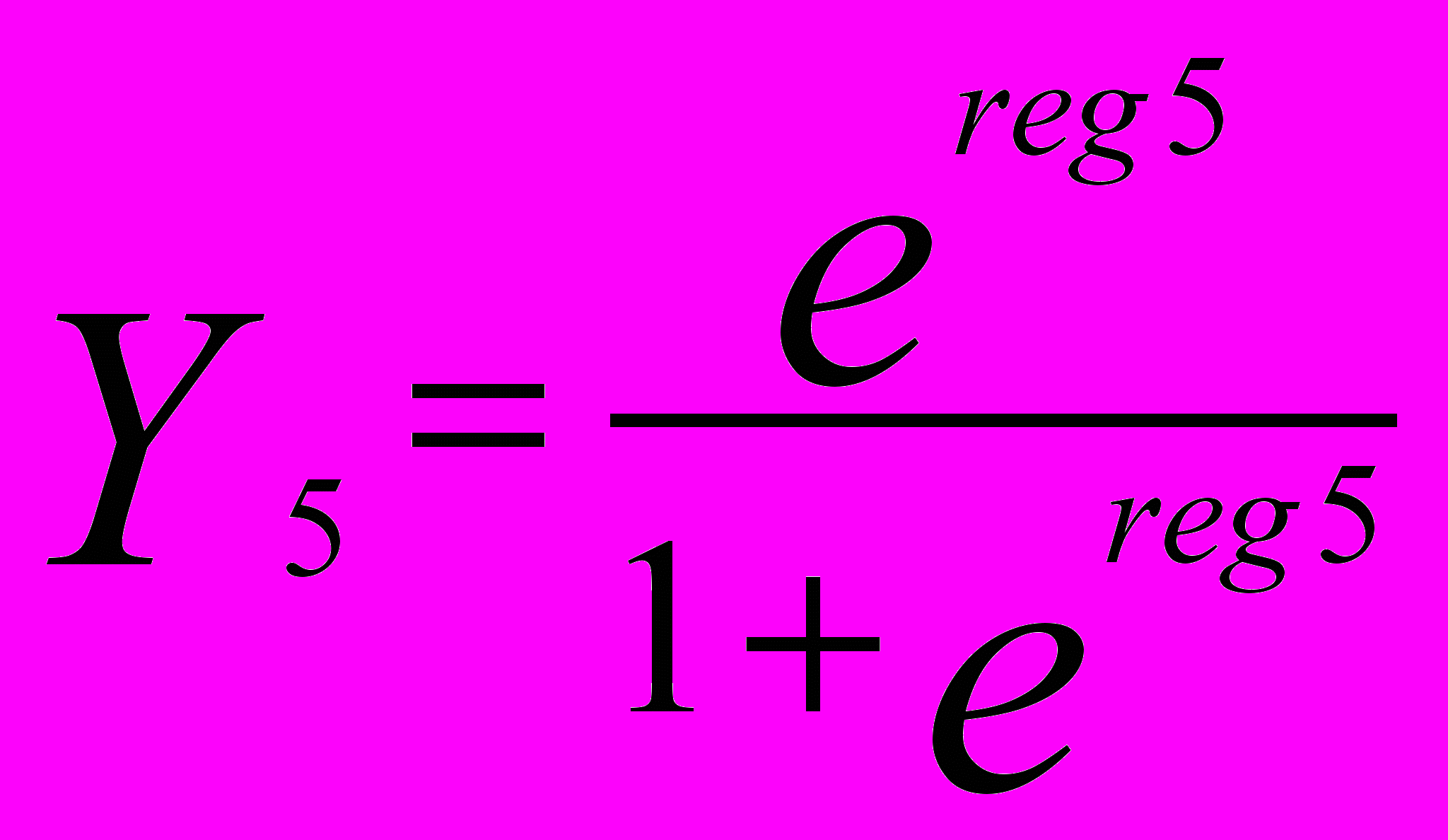 ,
,reg5 = -18,9953 – 17,4122*X1 + 7,8961*X2 + 18,1178*X3 + 1,3934*X4 +
+ 4,6425*X5 – 0,2685*X6
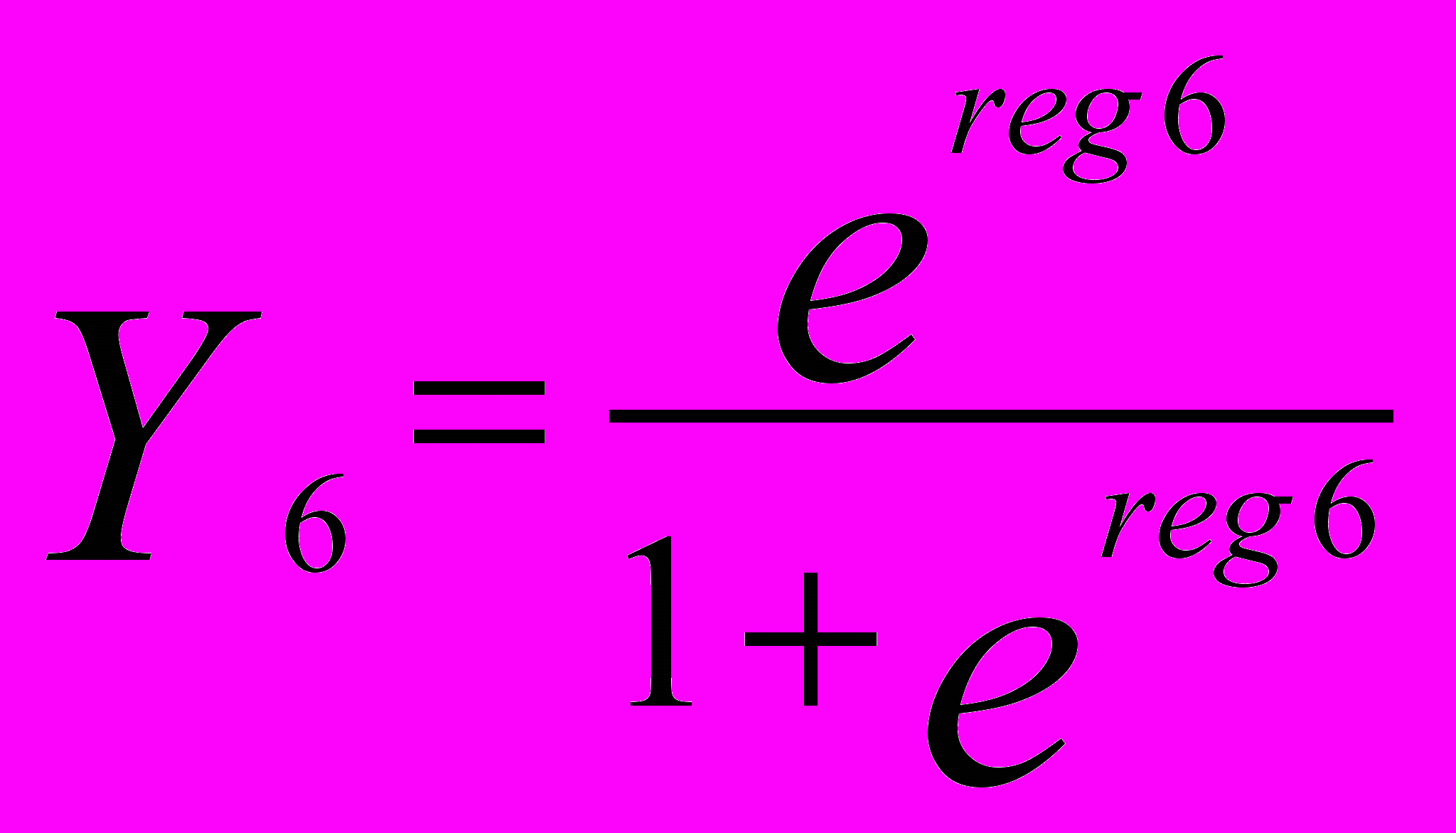 ,
,reg6 = -2,2924 + 0,2390*X1 – 1,5935*X2 – 0,2782*X3 – 0,7903*X4 – 0,8849*X5 + + 0,0368*X6
где X1 – пол; X2 – возраст; X3 – наследственность по психическому заболеванию; X4 – цереброоргнанические факторы; X5 – тип акцентуации; X6 – личностная тревожность.
Результаты верификации разработанных моделей подтвердили их адекватность – средняя ошибка не превышала 15 %, что является достаточным для практического использования.
Для решения задачи прогнозирования клинического излечения (или достижения быстрой и полной ремиссии) аффективного расстройства при хронических соматических заболеваниях был использован метод экспертной оценки. На основе опроса группы экспертов отобраны наиболее значимые прогностические факторы, и на их основе сформирована таблица-матрица, содержащая прогностические баллы. Для получения прогноза с помощью таблицы-матрицы необходимо сложить прогностические баллы, соответствующие выявленным у больного признакам.
Для интерпретации полученной суммы предлагается следующая шкала:
- до 30 баллов – прогноз благоприятный;
- 31 балл и более – прогноз неблагоприятный.
Полученный прогноз клинического излечения должен учитываться при выборе адекватной тактики лечения аффективных расстройств при хронических соматических заболеваниях. В частности, предлагается при наличии неблагоприятного прогноза усилить терапевтическую схему лечения за счет эклектичной психотерапии.
На основе обобщения результатов проведенного исследования предлагается алгоритм ведения пациентов с хроническими соматическими заболеваниями, у которых обнаружено или возможно развитие аффективного расстройства (рис. 3).
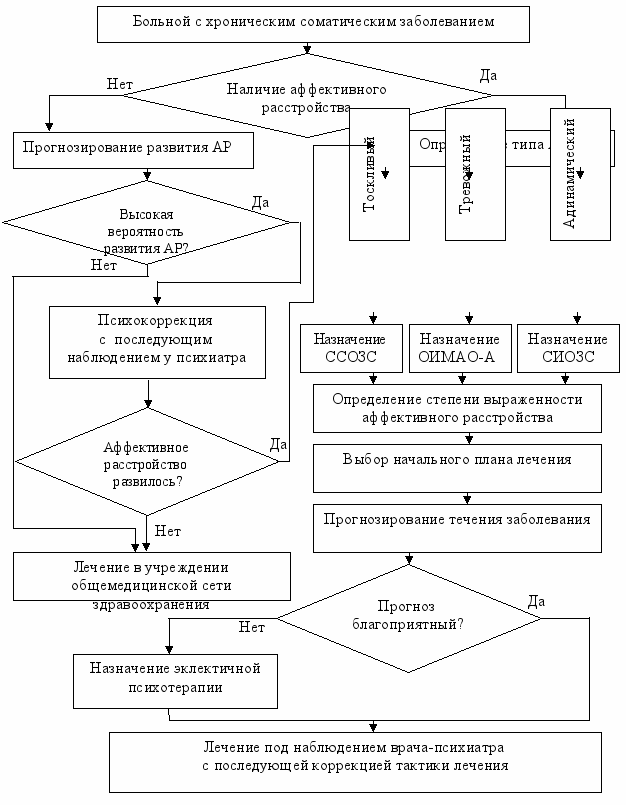
Рис. 3. Схема алгоритма ведения пациентов
с хроническими соматическими заболеваниями,
обратившихся к врачу-психиатру по поводу психических нарушений
На начальном этапе врачом-психиатром определяется наличие или отсутствие аффективного расстройства на основе клинико-анамнестической и клинико-психопатологической карт, разработанных в отделении клинико-биологических исследований пограничных состояний МНИИП МЗ РФ, шкалы оценки депрессии Гамильтона (HDRS).
Если установлено, что на данный момент аффективное расстройство отсутствует, осуществляется индивидуальное прогнозирование вероятности развития аффективного расстройства и его характеристик на основе разработанного комплекса прогностических моделей. При этом, если прогноз благоприятный (вероятность развития аффективного расстройства меньше 0,5), то пациент направляется на лечение соматического заболевания в учреждениях общемедицинской сети здравоохранения к специалисту соответствующего профиля. Если прогноз неблагоприятен (вероятность развития аффективного расстройства больше 0,5), больному рекомендуется психокоррекция с последующим наблюдением у психиатра. Далее вновь анализируется состояние пациента, и если аффективное расстройство не развилось, больной продолжает лечение по основному соматическому заболеванию.
В случае, когда аффективное расстройство выявлено, на основе вышеперечисленных шкал, а также госпитальной шкалы тревоги и депрессии (HADS) и шкалы самооценки Ч.Д. Спилбергера – Ю.Л. Ханина определяется тип аффективного расстройства: тоскливый, адинамический, тревожный. В соответствии с типом аффективного расстройства назначаются соответственно селективные стимуляторы обратного захвата серотонина (коаксил), селективные ингибиторы обратного захвата серотонина (флуоксетин) и обратимые ингибиторы моноаминооксидазы (пиразидол). Далее по шкале Гамильтона оценивается степень выраженности (тяжести) заболевания и в соответствии с этим выбирается начальная доза лечения.
Следует отметить, что при проведении настоящего исследования было установлено, что наилучший результат достигается при комбинации медикаментозного лечения с эклектичной психотерапией. Однако назначение всем пациентам данного типа немедикаментозного лечения невозможно в силу ряда субъективных и объективных причин, в связи с чем предлагается выборочное назначение эклектичной психотерапии только тем пациентам, у которых имеется прогнозируется неблагоприятный прогноз клинического излечения.
После назначения терапевтической схемы осуществляется постоянный контроль за состоянием пациента врачом-психиатром. В качестве контрольных точек следует отметить 7 дней, 1, 3 и 6 месяцев. При этом для оценки динамики рекомендуется использовать шкалу оценки депрессии Гамильтона (HDRS).
При отсутствии положительной динамики осуществляется коррекция лечения в соответствии с предложенным алгоритмом (рис. 4).
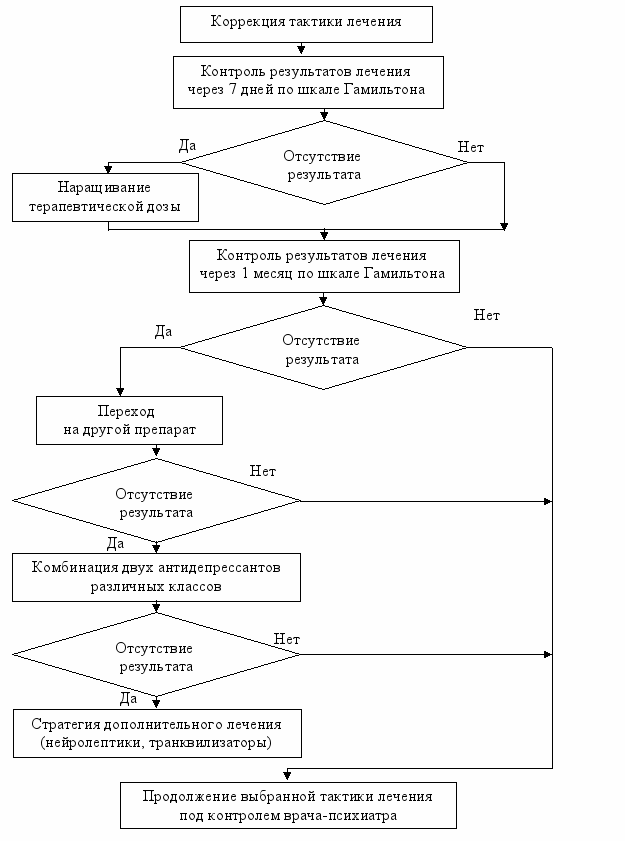
Рис. 4. Схема алгоритма коррекции тактики лечения аффективных
расстройств у больных с хроническими соматическими заболеваниями
Предложенные алгоритмы и модели были апробированы в клинической практике Европейской клиники «Сиена-Мед» (г. Воронеж), Медицинской амбулатории Воронежской региональной организации медико-социально-психологической реабилитации инвалидов и малоимущих граждан «Преодоление» (г. Воронеж), Медицинской амбулатории Воронежского регионального фонда «Фонд помощи больным раком» в течение 2007-2009 гг. (215 больных с аффективными расстройствами). Полученные результаты подтвердили клиническую эффективность предложенного подхода, основанного на использовании системы интеллектуальной поддержки деятельности врача-психиатра.
Для наглядной иллюстрации процесса принятия решений врачом-психиатром приведены результаты ситуационного моделирования, представленные в виде клинических примеров.
В заключении рассмотрены основные результаты работы.
В приложении приведены таблицы, иллюстрирующие первичный материал и клинические примеры.
