Многоэлементный состав крови у мужчин без и с ишемической болезнью сердца 14. 00. 06 кардиология
| Вид материала | Автореферат |
- Задачи : Формирование 2-х клинических групп обоего пола: 30 пожилого возраста (65-86, 118.29kb.
- Задачи : Формирование 2-х клинических групп обоего пола: 30 пожилого возраста (65-86, 127.2kb.
- Диагностическое и прогностическое значение уровней рарр-а и маркеров воспаления у больных, 308.52kb.
- Результаты лечения больных ишемической болезнью сердца электромагнитным излучением, 46.66kb.
- Применение инфракрасного широкополосного излучения модулированного терагерцовой частотой, 58.61kb.
- Керимович хроническая сердечная недостаточность у больных ишемической болезнью сердца:, 509.58kb.
- «Факторы коронарного ангиогенеза и влияние на них различных методов лечения у больных, 366.72kb.
- «Диагностическое и прогностическое значение фно-α у больных ишемической болезнью сердца», 288.88kb.
- Влияние гелиогеомагнитной активности на функциональное состояние сердечно-сосудистой, 333.23kb.
- «динамика функционального состояния почек у больных ишемической болезнью сердца и хронической, 502.36kb.
1 2
При сравнении биохимических показателей в группе с ИБС и без ИБС (табл.2) достоверно выше в группе ИБС оказались значения общего холестерина (p<0,05), триглицеридов (р=0,000). Достоверной разницы в содержании холестерина липопротеидов низкой плотности, холестерина липопротеидов высокой плотности, АСТ, АЛТ и глюкозы не выявлено (p>0,05).
Таблица 2
Биохимические показатели в обследуемых группах
| | ИБС (-) | ИБС (+) | | ||
| M | ±m | M | ±m | Р | |
| ОХС, ммоль/л | 5,09 | 0,21 | 5,72 | 0,19 | p<0,05 |
| ТГ | 1,12 | 0,15 | 2,17 | 0,22 | 0,000 |
| ХС-ЛВП | 1,12 | 0,07 | 1,02 | 0,04 | p>0,05 |
| ХС-ЛНП | 3,74 | 0,19 | 4,22 | 0,18 | p>0,05 |
| АЛТ | 19,12 | 1,33 | 21,66 | 1,43 | p>0,05 |
| АСТ | 17,56 | 1,38 | 18,28 | 1,31 | p>0,05 |
| Мочевина | 6,53 | 0,23 | 5,89 | 0,29 | p>0,05 |
| Глюкоза | 4,25 | 0,17 | 4,29 | 0,15 | p>0,05 |
В обеих группах проведено сравнение гемодинамических показателей (табл. 3). Больные ИБС имели схожие гемодинамические показатели, что и в группе без ИБС. Достоверных различий по систолическому давлению, диастолическому давлению, пульсовому давлению, среднему гемодинамическому давлению и частоте сердечных сокращений не получено (p>0,05).
Таблица 3
Средние значения гемодинамических показателей в обследуемых группах
| Показатели | ИБС (-) | ИБС (+) | Р | ||
| M | ±m | M | ±m | ||
| САД, мм рт.ст | 124,9 | 1,55 | 132,5 | 2,30 | p>0,05 |
| ДАД, мм рт.ст | 80,3 | 0,92 | 82,4 | 1,39 | p>0,05 |
| Пульсовое АД | 42,7 | 1,12 | 43,6 | 1,57 | p>0,05 |
| АД сред.гемодин. | 94,53 | 1,04 | 95,5 | 1,7 | p>0,05 |
| ЧСС | 66,8 | 3,6 | 69,4 | 3,5 | p>0,05 |
Всем пациентам записывали электрокардиограмму в 12-отведениях. Электрокардиографические показатели в обеих группах представлены в таблице 5.
Таблица 4
Электрокардиографические показатели в обследуемых группах
| Показатели | ИБС (-) | ИБС (+) | Р | ||
| M | ±m | M | ±m | ||
| PQ | 0,12 | 0,002 | 0,16 | 0,004 | р=0,000 |
| QRS | 0,09 | 0,003 | 0,11 | 0,002 | p>0,05 |
| QT | 0.39 | 0.003 | 0,38 | 0,05 | p>0,05 |
При сравнении электрокардиографических показателей больные с ИБС имеют достоверно более удлиненный интервал PQ по сравнению контрольной группой (0,15±0,004 и 0,12±0,002, соответственно), по остальным показателям (QRS, QT) достоверной разницы не получено (p>0,05).
При записи ЭКГ у пациентов с ИБС выявлены следующие нарушения ритма – атриовентрикулярная блокада I степени у 3 мужчин, редкая предсердная и желудочковая экстрасистолия у 9 мужчин.
Таким образом, в группе с ИБС достоверно выше частота встречаемости таких нарушений липидного обмена как гиперхолестеринемия, гипертриглицеридемия. В биохимическом анализе крови достоверно выше оказались повышенными уровни общего холестерина, триглицеридов. По гемодинамическим показателям достоверной разницы в обеих группах не выявлено. В группе ИБС выявлено достоверное удлинение интервала PQ.
Содержание химических элементов крови в группе без ИБС
Методом РФА СИ определено содержание микроэлементов в крови у мужчин без клинико-инструментальных признаков ИБС. Сравнение содержание микроэлементов в группе без ИБС проводилось с данными Эмсли Дж. (1997) (нейтронно-активационный метод) и Скального А.В.(2000) (АЭС-ИСП, МС-ИСП) (табл. 5).
Таблица 5
Содержание микроэлементов в крови в группе без ИБС
| | Эмсли Дж.,1997 (мкг/мл) | Скальный А.В.,2000 (мкг/л) | ni | Xi | 5% CI | 95% CI | ↑> 10 раз | ↑< 10 раз |
| Cr | 0,006-0,11 | 0,1-0,5 | 6 | 0,81 | 0,24 | 4,22 | + | |
| Mn | 0,0016-0,075 | 0,3-1,0 | 22 | 1,44 | 0,36 | 6,78 | + | |
| Co | 0,0002-0,04 | 0,05-0,10 | 35 | 1,48 | 0,74 | 2,03 | + | |
| Cu | 1,01 | 0,75-1,3 | 36 | 1,01 | 0,34 | 3,34 | | |
| Zn | 7,0 | 0,70-1,10 | 38 | 7,13 | 4,81 | 12,04 | | |
| Se | 0,171 | 60-120 | 32 | 0,09 | 0,05 | 0,16 | | |
| Mo | 0,001 | 0,30-1,20 | 17 | 0,04 | 0,02 | 0,26 | + | |
| As | 0,0017-0,09 | Н/д | 17 | 0,15 | 0,02 | 0,67 | | + |
| Br | 4,7 | Н/д | 38 | 4,42 | 2,77 | 7,21 | | |
| Rb | 2,49 | Н/д | 38 | 1,85 | 1,22 | 2,92 | | |
| Ti | 0,054 | Н/д | 7 | 2,81 | 2,26 | 8,00 | + | |
| Ni | 0,01-0,05 | <0,01-0,1 | 6 | 0,18 | 0,09 | 0,69 | | + |
| Ga | <0,08 | Н/д | 20 | 0,09 | 0,04 | 0,15 | | |
| Ge | 0,44 | Н/д | 15 | 0,08 | 0,03 | 0,25 | | |
| Sr | 0,031 | 20-70 | 32 | 0,12 | 0,06 | 0,31 | | + |
| Y | 0,0047 | Н/д | 18 | 0,12 | 0,05 | 1,14 | + | |
| Zr | 0,011 | Н/д | 21 | 0,03 | 0,02 | 0,10 | | |
| Nb | 0,005 | Н/д | 13 | 0,03 | 0,02 | 0,11 | | + |
| Hg | 0,0078 | Н/д | 24 | 0,07 | 0,04 | 0,20 | + | |
| Pb | 0,21 | Н/д | 23 | 0,28 | 0,04 | 1,11 | | |
| Bi | 0,016 | Н/д | 21 | 0,06 | 0,04 | 0,18 | | + |
| Th | 0,00016 | Н/д | 32 | 0,05 | 0,02 | 0,19 | + | |
| U | 0,0005 | Н/д | 13 | 0,04 | 0,02 | 0,05 | + | |
| Fe | 447 | 0,80-1,40 | 38 | 467 | 398 | 627 | | |
При сравнении содержания микроэлементов в группе без ИБС по сравнению с литературными данными отмечается повышение уровня марганца, хрома, кобальта, молибдена, тяжелых и редкоземельных элементов – мышьяка, титана, никеля, стронция, ртути, висмута, иттрия, ниобия, тория, урана. Причем повышение содержания хрома, марганца, кобальта, молибдена, титана, ртути, тория и урана значительно превышает литературные данные. Несколько менее составляет превышение содержания мышьяка, никеля, стронция, иттрия, ниобия. Уровень селена и германия оказался пониженным.
Наши данные согласуются с докладом «О состоянии окружающей среды Новосибирской области в 2003 году» (2004), где на основе данных социально-гигиенического мониторинга в Новосибирской области выделены приоритетные химические загрязнители: для атмосферного воздуха – это кадмий, хром, никель, - для питьевой воды – марганец, бор, железо и др., - для продуктов питания – нитраты, кадмий, мышьяк, свинец. Таким образом, Новосибирск, входит в первую группу по степени загрязнения – территорию с высоким уровнем техногенного загрязнения.
Содержание химических элементов и их дисбаланс в группе с ИБС
Таблица 6
Содержание микроэлементов в группе с ИБС
| | Эмсли Дж.,1997 (мг/л) | Скальный А.В., 2000 (мкг/л) | Xi | 5% CI | 95% CI | ↑> 10 раз | ↑< 10 раз |
| Cr | 0,006-0,11 | 0,1-0,5 | 1,92 | 0,59 | 4,85 | + | |
| Mn | 0,0016-0,075 | 0,3-1,0 | 1,75 | 0,65 | 4,02 | + | |
| Co | 0,0002-0,04 | 0,05-0,10 | 1,6 | 0,38 | 3,13 | + | |
| Cu | 1,01 | 0,75-1,3 | 2,96 | 0,77 | 9,44 | | + |
| Zn | 7,0 | 0,70-1,10 | 7,46 | 4,81 | 17,24 | | |
| Se | 0,171 | 60-120 | 0,09 | 0,05 | 0,23 | | |
| Mo | 0,001 | 0,30-1,20 | 0,17 | 0,017 | 0,94 | + | |
| As | 0,0017-0,09 | Н/д | 0,14 | 0,05 | 0,26 | | + |
| Br | 4,7 | Н/д | 6,72 | 3,51 | 24,56 | | + |
| Rb | 2,49 | Н/д | 1,97 | 1,19 | 3,25 | | |
| Ti | 0,054 | Н/д | 4,79 | 2,29 | 6,06 | + | |
| Ni | 0,01-0,05 | <0,01-0,1 | 0,25 | 0,067 | 0,92 | | + |
| Ga | <0,08 | Н/д | 0,12 | 0,06 | 0,21 | | + |
| Ge | 0,44 | Н/д | 0,13 | 0,051 | 0,20 | | |
| Sr | 0,031 | 20-70 | 0,11 | 0,027 | 0,37 | | + |
| Y | 0,0047 | Н/д | 0,05 | 0,01 | 0,09 | + | |
| Zr | 0,011 | Н/д | 0,05 | 0,02 | 0,15 | | + |
| Nb | 0,005 | Н/д | 0,05 | 0,02 | 0,15 | | + |
| Hg | 0,0078 | Н/д | 0,09 | 0,037 | 0,31 | + | |
| Pb | 0,21 | Н/д | 0,46 | 0,099 | 2,33 | | + |
| Bi | 0,016 | Н/д | 0,05 | 0,01 | 0,09 | | + |
| Th | 0,00016 | Н/д | 0,06 | 0,039 | 0,06 | + | |
| U | 0,0005 | Н/д | 0,06 | 0,03 | 0,04 | + | |
| Fe | 447 | 0,80-1,40 | 479 | 353 | 662 | | |
Содержание химических элементов в группе с ИБС в сравнении с литературными данными Эмсли Дж. (1997) (нейтронно-активационный метод) и. Скального А.В (2000) (АЭС-ИСП, МС-ИСП) представлено в таблице 6.
Выявлено превышение, в сравнении с литературными данными, следующих микроэлементов - марганца, хрома, кобальта, меди, молибдена, брома, тяжелых и редкоземельных элементов – мышьяка, титана, никеля, стронция, циркония, ртути, свинца, висмута, галлия, иттрия, ниобия, тория, урана. Отмечается пониженное содержание селена, германия, рубидия.
Выявлено десятикратное превышение предлагаемых норм следующих микроэлементов – хром, марганец, кобальт, молибден, титан, ртуть, иттрий, торий, уран.
Сравнение многоэлементного состава крови в группах с ИБС и без ИБС
Сравнительный анализ полученных данных по элементному составу крови больных у пациентов с ишемической болезнью сердца и группой сравнения показал, что у больных с ИБС наблюдались достоверные изменения концентраций следующих элементов: хром, медь, молибден, бром, титан, свинец, висмут, германий, иттрий, цирконий, ниобий, уран. Причем содержание таких микроэлементов, как хром, медь, молибден, бром, титан, свинец, германий, цирконий, ниобий, уран в группе ИБС было достоверно выше, а иттрия и висмута было достоверно ниже, чем в группе без ИБС.
Результаты сравнительного анализа эссенциальных, условно эссенциальных и тяжелых и редкоземельных микроэлементов в группах с ИБС и без ИБС представлены в рисунках 2,3.
Error: Reference source not found
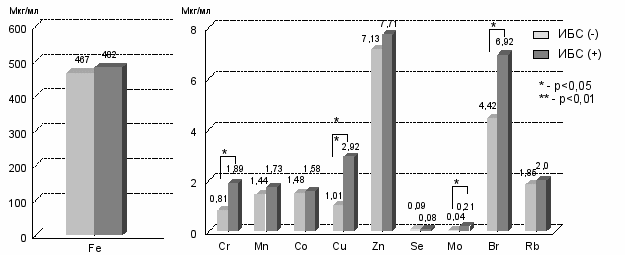
Рис. 2 Содержание эссенциальных микроэлементов в группе с ИБС и группе без ИБС
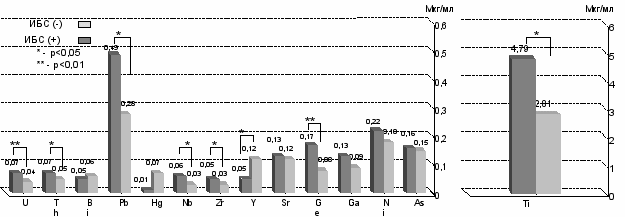
Рис. 3 Содержание тяжелых и редкоземельных микроэлементов в группе с ИБС и группе без ИБС
При обследовании выявлено повышение уровня хрома в обеих группах по сравнению с литературными данными. Причем содержание хрома в группе больных ИБС было достоверно выше, чем в группе сравнения (t=2,5). Известно, что одним из важнейших биологических эффектов хрома является его влияние на фактор толерантности к глюкозе (Bradbury J., 1997). Кроме того, хром способен влиять на гомеостаз сывороточного холестерина и предупреждать тенденцию к его росту с увеличением возраста (Oberleas D. et al., 1999). Хром обладает способностью повышать активность пероксидазы, аскорбиноксидазы, цитохромоксидазы и аскорбиновой кислоты в тканях (Тутельян В.А. и соавт., 2001).При избытке хрома может поражаться ретикулоэндотелиальная система, повышается риск развития злокачественных опухолей (Costa M., 1997).
Однако у части обследованных нами мужчин выявлен дефицит этого микроэлемента. При дефиците хрома нарушается способность включения аминокислот глицина, серина, метионина и гамма-аминоизомаслянной кислоты в метаболизм сердечной мышцы. Кроме того, проявлениями дефицита хрома является повышение уровня холестерина и триглицеридов крови, увеличение риска атеросклероза (Schroered H.A., 1994). В нашем исследовании у 21 больного ИБС (51%) и у 12 (32%) мужчин из группы сравнения отмечается снижение уровня хрома ниже нормативных показателей.
При анализе выявленных изменений отмечается значительное повышение меди в группе больных ИБС по сравнению с группой без ИБС (t=2,5). Повышение уровня меди выявлено 16 больных ИБС (39%). Влияние на сердечно-сосудистую систему этого микроэлемента имеет сложный характер: отмечается как местное влияние на сосуды и сердце, связанное с блокированием сульфгидрильных групп, так и сложное воздействие на нервную систему, включающее и симпатическое и парасимпатическое звенья. Установлено, что, в зависимости от концентрации меди, она может выступать и как прооксидант, и как антиоксидант (Наmada T., 1995). При избытке меди происходит ингибирование тиоловых групп, извращение всех видов метаболизма. Развивается избыточная реакция перекисного окисления с некрозами и прогрессирующим фибропластическим процессом (Тутельян В.А и соавт., 2001). Кроме того, в высоких концентрациях медь, инициируя образование О2 и OH (Меньщикова Е.Б., Зенков Н.К., 1993), выступает как прооксидант. Исследования финских авторов (Salonen et al., 1991) показали, что высокий уровень меди является независимым фактором риска ИБС.
В группе мужчин без ИБС содержание меди оказалось нормальным в сравнении с литературными данными, однако, обращает на себя внимание, что у 10 (26%) обследованных из группы сравнения выявлен дефицит меди. Являясь, наряду с цинком, неотъемлемой частью супероксиддисмутазы, медь выступает в роли актиоксиданта, защищая клетку от повреждения (Зенков Н.К., Меньщикова Е.Б., 1993; Ferns G.A. et al., 1997; Wang P. еt al., 1998). Сниженный уровень меди в организме сопровождается гиперхолестеринемией, гипертензией и нарушением метаболизма простогландинов (Allen G.D., Klevay L.M., 1994).
Более важным является не абсолютное содержание того или иного метаболита в отдельных тканях, а анализ антагонистических взаимоотношений между микроэлементами, например, таких как медь и цинк, определяющих общий метаболизм и конечные биологические эффекты этих микроэлементов. Антагонизм между медью и цинком может играть важную роль в патологических процессах, вызывая сдвиги в обмене незаменимых жирных кислот и синтезе простагландинов (Davis N.T., Nightingale R., 1975). Ионы цинка не участвуют в окислительно-восстановительных процессах, но они способствуют стабилизации сульфгидрильных групп, предупреждая их окисление ионами меди и железа (Dubick M.A., 1993).
Известно, что цинк тормозит процесс перекисного окисления липидов, значительно снижая выраженность ПОЛ при атеросклерозе. Являясь, активным центром цитозольного фермента супероксиддисмутазы, Zn принимает участие в реакции дисмутации О2 и Н2О2 выступая т.о., в качестве мощного антиоксиданта. Кроме того, Zn обладает противовоспалительным действием, за счет мощного ингибирования факторов активации тромбоцитов. Zn стимулирует превращение незаменимых жирных кислот в простагландины, которые являются компонентом депрессорной системы организма и способствуют снижению артериального давления (Лишманов Ю.Б., Маслов Л.Н., 1994).
В нашем исследовании уровень цинка как в группе больных, так и в группе сравнения не превышал значения, указываемые в литературе.
При обследовании выявлено достоверное повышение уровня брома в группе больных ИБС (t=3,57). В организме бром является обязательной частью многих ферментов и участвует в регуляции деятельности желез, в том числе усиливает действие инсулина. Кроме того, он принимает участие в обмене белков, жиров и углеводов (Витамины …, 2001). В некоторых источниках сообщается, что бромиды могут стимулировать воспалительный процесс и зависит это непосредственно от ионов брома (Diener W., 1998).
Чрезвычайно интересными являются данные, касающиеся обмена селена, микроэлемента, который активно изучается как в связи с ИБС, так и в связи с неишемическими повреждениями миокарда. Повышение уровня селена может служить проявлением адаптивных процессов в организме, свидетельствуя о важности данного МЭ в процессах регуляции кардиогемодинамики. Пониженный уровень селена традиционно рассматривается не только как фактор риска атеросклероза (Oster O., Prellwitz W., 1990; Kok, 1989), но и как фактор, отягощающий течение самого инфаркта миокарда (Thiele R. et al., 1997). В эксперименте показано, что этот МЭ выступает в качестве кардиопротектора, защищая миокарда от воздействия кардиотоксических веществ. Работы Salonen J.T. et al. (1996) доказывают, что низкий уровень Se в плазме является фактором риска развития инфаркта миокарда. Селен влияет на несколько клеточных процессов, участвующих в патогенезе атеросклеротических кардиоваскулярных заболеваний. Так, дефицит микроэлемента сопровождается, как правило, снижением активности глутатионпероксидазы (ГПО), в частности, в тромбоцитах и стенках артерий (Combs G.F.,1984), параллельно снижается уровень селена в эритроцитах (Yegin A. et al., 1997). ГПО – первая линия защиты клеток от накопления токсических гидропероксидов, свободных радикалов – гомотетрамерный селенопротеид, для синтеза которого необходим селен. Помимо ГПО, обнаружен еще один селенсодержащий энзим - фосфолипидгидро-пероксиглутатионпероксидаза. Ему приписывается способность восстанавливать в липидной фазе мембран гидроксипроизводные, гидропероксиды фосфолипидов, холестерола, тем самым, угнетая ПОЛ в клетке (Ursini F. et al., 1992). Кроме того, селен способствует выработке эндогенных антиоксидантов белковой и липидной природы. Надо отметить, что сам селен, а вернее селенсодержащие аминокислоты, могут оказывать самостоятельное антиоксидантное действие, так как они являются тушителями радикалов или участвуют в нерадикальном разложении липидных перекислей (Биленко М.В., 1989). Таким образом, угнетая свободнорадикальное повреждение клетки и способствуя выработке эндогенных антиоксидантов, селен выступает мощным кардиопротектором (Тулеутаев М.Е., 2003)
В нашем исследовании отмечено снижение содержания селена как в группе сравнения, так и в группе ИБС по сравнению с литературными данными. Дефицит селена в группе без ИБС выявлен у 13 (34%) обследованных, что позволяет отнести их в группу риска по развитию атеросклероза. В группе больных ИБС снижение уровня селена отмечалось у 24 (58%) обследованных.
Fe воспринимается неоднозначно в патогенезе атеросклероза и ИБС. Вследствие роли железа как промотора перекисного окисления липидов, предположили наличие взаимосвязи между пулом железа и заболеваниями сердца (Borellа Р., 2005). В патогенезе ИБС определенная роль отводиться процессу перекисного окисления липидов (ПОЛ), продукты которого повреждают кардиомиоциты. Среди химических элементов – железо – элемент с выраженным прооксидантным действием. Установлена, что существует прямая связь между высоким уровнем сывороточного железа и риском ишемического повреждения миокарда (Morrison H.I. et al., 1994). Выявлено, что повышение уровня железа способствует гиперактивности системы перекисного окисления липидов, что является фактором, утяжеляющим течение атеросклероза (Sullivau J.L., 1996). Повышенное содержание железа значительно снижает активность глутатионпероксидазы – одного из основных ферментов – антиоксидантов (Pucheu S. et al., 1993).
В нашем исследовании содержание железа в обеих группах совпадало с литературными данными. Достоверной разницы в содержании железа в группе с ИБС и без ИБС получено не было (t=0,89). Однако, отмечается тенденция к более высокому содержанию железа в группе с ИБС.
Обращает внимание повышение уровня молибдена, как в группе сравнения, так и в группе с ИБС. Причем содержание этого элемента 10-кратно превышало в обеих группах величины, приводимые в литературных источниках. Кроме того, в группе с ИБС превышение содержания молибдена было достоверно выше, чем в группе сравнения (t=3,48). Молибден входит в состав многих ферментов, в частности, активирует ксантиноксидазу, обеспечивающую обмен пуринов и завершающую образование мочевой кислоты в организме человека (Скальный А.В., 2004). При избытке молибдена отмечается артериальная гипотония, мышечная атония (Pinto Marguerite M et al., 1997). Молибден является антагонистом меди и цинка (Чернозубов И.Е., 1997).
Содержание свинца в группе без ИБС не превышало нормальных значений, а в группе с ИБС превышало нормальные величины, приводимые в литературных источниках (Дж.Эмсли, 1997). При этом в группе с ИБС содержание свинца было достоверно выше (t=2,25). Свинец является функциональным антагонистом кальция, магния и цинка. Вследствие этого свинец способен вытеснять эти эссенциальные микроэлементы из организма, что создает минеральный дисбаланс. В результате связывания ангидридов со свинцом угнетается синтез белков и активность ферментов, например АТФ-азы. Свинец нарушает синтез гема и глобина, вмешиваясь в порфириновый обмен, индуцирует дефекты мембран эритроцитов. Повышенное поступление с пищей Са, Р, Mg, снижает абсорбцию свинца, тогда как на фоне дефицита железа и перечисленных элементов способность усваивать свинец увеличивается (Скальный А.В., 2004).
Многочисленными клинико-эксперементальными исследованиями установлено, что канцирогенными для организма человека металлами, вызывающими хромосомные абберации, являются мышьяк, хром, свинец, никель, кобальт, молибден, ртуть (Titenko-Holland N., 1997., Reiss J., 1998, 1999; Hayes R.B., 1997). В нашем исследовании содержание всех этих микроэлементов было высоким, по сравнению с литературными данными, как в группе без ИБС, так и в группе ИБС.
Выявлено достоверное изменение в группе ИБС таких химических элементов, как титан, цирконий, стронций влияние которых на сердечно-сосудистую систему по литературным данным не имеет первостепенного значения. Причем превышение содержания титана в группе без ИБС десятикратно превышало нормальные значения, приводимые в литературе. Эти три элемента относятся к потенциально токсичным микроэлементам. Водорастворимые соединения циркония в кишечнике могут превращаться в оксид циркония и затем всасываться. Систематический контакт с цирконием (на протяжении 40 и более лет) может приводить к интоксикации организма (Скальный А.В., Рудаков И.А., 2004). Основное содержание титана в организме – это легкие и лимфоузлы. Известно, что кардиотоксическим эффектом обладают радионуклиды этих элементов в эксперименте (Кириченко О.Б., 2005; Кириченко О.Б. и соавт., 2003; Сухоруков Ф.В., 2001), приводящее к раннему формированию системных атеросклеротических процессов.
Отмечается высокое содержание в обеих группах такого микроэлемента, как висмут. Причем превышение нормы выявлено у 17 (44%) мужчин без ИБС и у 14 (34%) мужчин, имеющих ИБС. Это микроэлемент является токсичным ультрамикроэлементом, который индуцирует синтез низкомолекулярных белков, проникает в эритроциты (Скальный А.В., 2004).
Повышение уровня токсичных микроэлементов, как в группе с ИБС так и в группе сравнения указывает на необходимость проведения корреляционного анализа полученных данных с показателями здоровья и загрязнения этими токсикантами воздушной среды, воды и почв региона.
В группе ИБС выделена подгруппа мужчин с нарушениями липидного обмена (уровень холестерина превышал 5,2 ммоль/л, триглицеридов 1,7 ммоль/л). Проведен сравнительный анализ содержания химических элементов в группе ИБС с нарушениями липидного обмена и без таковых (рис. 4,5). Достоверной разницы в содержании микроэлементов в этих двух группах не выявлено (р>0,05).
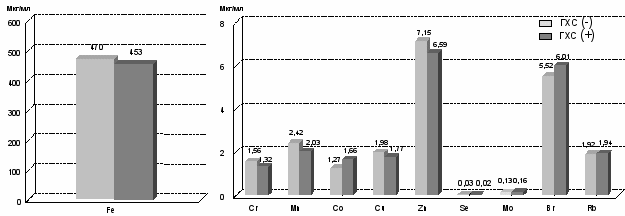
Error: Reference source not foundРис.4 Содержание эссенциальных микроэлементов у больных с ГХС по сравнению с больными без ГХС
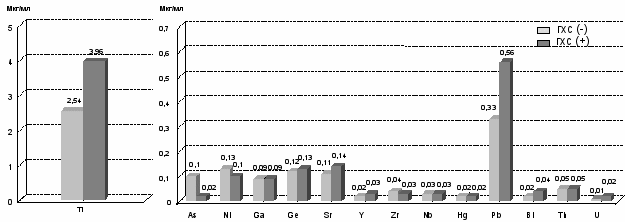
Error: Reference source not foundРис.5 Содержание тяжелых и редкоземельных микроэлементов у больных с ГХС по сравнению с больными без ГХС
Хотя достоверной разницы в группе ИБС, где есть гиперхолестеринемия и она отсутствует, не выявлено, отмечается тенденция к снижению таких значимых микроэлементов, как хром, марганец, селен, цинк.
В группе без ИБС также выявлена подгруппа мужчин с нарушениями липидного обмена. При сравнении микроэлементного состава крови в группе мужчин без ИБС с гиперхолестеринемией и без гиперхолестеринемии достоверной разницы в содержании химических элементов не выявлено (р>0,05).
При записи ЭКГ покоя в группе с ИБС были выявлены следующие нарушения ритма и проводимости: атриовентрикулярная блокада I степени у 3 мужчин; нарушения ритма (предсердная и желудочковая экстрасистолия) у 9 мужчин, всего нарушения ритма и проводимости выявлены у 12 мужчин. Проведено сравнение микроэлементного состава крови у мужчин с ИБС с нарушениями ритма и проводимости с микроэлементным составом крови больных ИБС без нарушений ритма и проводимости. Достоверной разницы в содержании многоэлементного состава крови не выявлено (p>0,05).
При сравнении многоэлементного состава крови больных с нарушениями ритма и проводимости с группой без ИБС выявлены аналогичные, как в группе ИБС в сравнении с группой без ИБС, изменения элементного состава крови.
Результаты сравнительного анализа эссенциальных и тяжелых и редкоземельных микроэлементов в группах с ИБС и без ИБС представлены в рисунках 6,7.
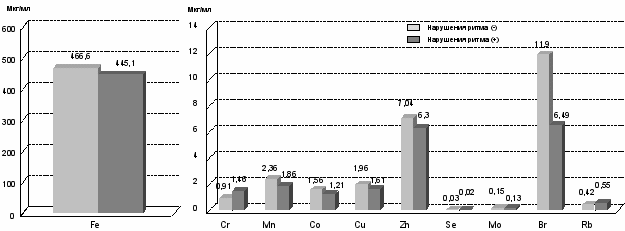 Error: Reference source not found
Error: Reference source not foundРис. 6. Содержание эссенциальных микроэлементов у больных с нарушениями ритма по сравнению с группой без ИБС
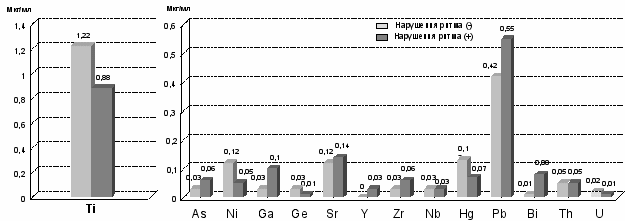 Error: Reference source not foundError: Reference source not found
Error: Reference source not foundError: Reference source not foundРис. 7 Содержание тяжелых и редкоземельных микроэлементов у больных с нарушениями ритма по сравнению с группой без ИБС
Содержание у больных с нарушениями ритма и проводимости меди, брома, титана, циркония, технеция, и урана было выше, чем в группе без ИБС, в содержание стронция, иттрия ниже.
Таким образом, проведенные исследования выявили сочетанный дисбаланс многоэлементного состава крови, как у мужчин без ИБС, так и больных с ишемической болезнью сердца, как в сторону повышения содержания, так и в сторону дефицита. Обнаружение тяжелых металлов у части больных требует дальнейшего мониторинга и выяснение причин данных дисэлементозов.
Анализ проведенных исследований заставляет сделать определенные методические выводы: во-первых, необходимы стандартизированные методы определения элементов в биосредах, во-вторых, должны учитываться региональные особенности микроэлементного статуса организма человека при разработке нормативных показателей. (Боев В.М. и соавт., 2004).
ВЫВОДЫ
В группе мужчин без ИБС обнаружен сочетанный дисбаланс химических элементов: повышение в крови уровня эссенциальных микроэлементов - марганца, хрома, кобальта, молибдена, тяжелых и редкоземельных элементов – мышьяка, титана, никеля, стронция, ртути, висмута, иттрия, ниобия, тория, урана. Выявлено значительное превышение содержания хрома, марганца, кобальта, молибдена, титана, ртути, тория, урана, иттрия. Отмечается некоторое понижение содержания уровня селена, германия.
- В группе ИБС выявлен сочетанный дисбаланс микроэлементов: также как в группе сравнения повышен уровень эссенциальных микроэлементов - марганца, хрома, кобальта, молибдена, а также брома и меди, тяжелых и редкоземельных элементов – мышьяка, титана, никеля, стронция, циркония, ртути, свинца, висмута, иттрия, ниобия, тория, урана, а также галлия. Отмечается пониженное содержание германия, рубидия.
- При сравнении многоэлементного состава крови больных ИБС с группой сравнения наблюдаются достоверное повышение содержания следующих микроэлементов – хрома, меди, молибдена, брома, титана, германия, иттрия, циркония, ниобия, свинца, висмута, урана. При этом отмечается повышение в группе с ИБС элементов – хрома, молибдена, меди, брома, титана, германия, циркония, ниобия, свинца и урана, содержание иттрия и висмута в группе с ИБС ниже, чем в группе сравнения.
- При сравнении многоэлементного состава крови в группе больных ИБС, имеющих и не имеющих нарушения липидного обмена, не выявлено достоверной разницы в содержании микроэлементов.
- При нарушениях ритма и проводимости у больных ИБС по сравнению с больными ИБС без нарушений ритма достоверной разницы в содержании микроэлементов не получено.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Для определения многоэлементного состава крови необходимо использовать стандартизированные методы определения элементов в биосредах и формировать регионарные нормы.
- Полученные результаты предлагается использовать при планировании новых дополнительных научных исследований, возможно при планировании профилактических мероприятий по первичной и вторичной профилактике ИБС.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Куценогий К.П. Возможности применения метода ренгентфлюоресцентного анализа с использованием синхротронного излучения для определения многоэлементного состава биологических субстратов в медицине / Э.Я. Журавская, О.В. Чанкина, Н.А. Андрюшина [и др.] // Актуальные вопросы современной медицины: Тез. докл. 10 научно-практ. конф. врачей, Новосибирск, 2000, с 244.
- Журавская Э.Я. Многоэлементный состав крови у больных некоторых заболеваний терапевтического профиля / К.П. Куценогий, О.В. Чанкина, Н.А. Андрюшина [и др.] // Аналитика Сибири и Дальнего Востока: Тез. докл. 6 конф., Новосибирск, 2000.- с. 379.
- Андрюшина Н.А. Многоэлементный состав сыворотки крови у мужчин в возрасте 34-54 лет без признаков ИБС / Э.Я. Журавская, К.П. Куценогий, О.В. Чанкина [и др.] // Актуальные вопросы современной медицины: Тез. докл. 12 научно-практ. конф. врачей, Новосибирск. 2002. –с. 163.
- Журавская Э.Я. Многоэлементный состав сыворотки крови у мужчин в возрасте 34-54 лет, имеющих ИБС и без признаков ИБС / Н.А. Андрюшина, К.П. Куценогий, О.В. Чанкина [и др.] // От исследований к клинической практике: Тез. росс. национ. конгресса кардиологов. – С.-Петербург, 2002. – с. 142.
- Журавская Э.Я. Содержание железа крови у мужчин в возрасте 34-54 лет г. Новосибирска / Н.А. Андрюшина, К.П. Куценогий, О.В. Чанкина [и др.] // Актуальные вопросы современной медицины: Тез. докл. 13 науч.-практ. конф. врачей. Новосибирск, 2003.-С.173.
- Андрюшина Н.А. Многоэлементный состав крови у больных ишемической болезнью сердца / Э.Я. Журавская, К.П. Куценогий, О.В. Чанкина [и др.] // Журнал «Поверхность» (Поверхность, рентгеновские, синхротронные и нейтронные исследования), 2003. – С. 10-13.
- Журавская Э.Я. О диагностическом значении определения в крови при инфаркте миокарда некоторых микроэлементов / Андрюшина Н.А., Баум В.А., Куценогий К.П. [и др.] // Тез. сетевой науч.-практ. конф., посвящ. 110 ДКБ ЗСЖД «Современные технологии в клинической практике», Новосибирск, 2003. – С. 462-463.
- Журавская Э.Я. Многоэлементный состав крови у коренных жителей Чукотки / К.П. Куценогий, Ю.П. Никитин, Н.А. Андрюшина [и др.] // Вопросы сохранения и развития здоровья населения Севера и Сибири: матер. итог. науч. конф. - Красноярск, 2003. – С.63-64.
- Andryshina N.A. Element composition of blood of the patients with coronary heart disease / E.Ya. Zhuravskaya, K.P. Koutzenogii, O.V. Chankina [et al.] // 4 International symposium on trace element in human: new perspectives. – Greece.-2003.-P.435-441.
- Журавская Э.Я. Многоэлементный состав крови у мужчин в возрасте 34-54 лет, имеющих ИБС и без признаков ИБС / Н.А. Андрюшина, К.П. Куценогий, Т.И. Савченко [и др.] // Тез. докл. конф. «Актуальные проблемы кардиологии». – Тюмень, 2004-С.-53.
- Журавская Э.Я. Содержание тяжелых металлов крови у мужчин в возрасте 34-54 лет г. Новосибирска / Н.А. Андрюшина, К.П. Куценогий, О.В. Чанкина [и др.] // Актуальные вопросы современной медицины: Тез. докл. 13 науч.-практ. конф. врачей. Новосибирск, 2004.- Гл.ХV.- С.8.
- Журавская Э.Я. Риск макро- и микроэлементозов у мужчин г. Новосибирска / Н.А. Андрюшина, К.П. Куценогий, Т.И. Савченко [и др.] // Первый съезд терапевтов Сибири и Дальнего востока: сб. тез. докл. - Новосибирск, 2005. - С.280-282.
- Zhuravskaya E.Ja. The role of SRXRF method when determining physiological specifications of chemical elements in blood of a man / K.P. Koutzenogii, L.A. Gyrgolkay, N.A. Andryshina [et al.] // Digest reports of the XVI international synchrotron radiation conference, Novosibirsk, 2006. – P.113.
- Журавская Э.Я. Микроэлементы и некоторые параметры здоровья человека / К.П. Куценогий, О.В. Чанкина, Н.А. Андрюшина [и др.] // Бюллетень СО РАМН, 2006. - №4.- С. 116-120.
- Журавская Э.Я. Cелен у жителей крупного промышленного города Западной Сибири – Новосибирске / К.П. Куценогий, Н.В. Андрюшина, Т.И. Савченко [et al.] // Актуальные проблемы профилактической медицины: Сб. матер. 10-ой город. науч.-практ.конф. врачей. – Новосибирск, 2007. – С. 23-25.
СПИСОК СОКРАЩЕНИЙ
АЭС-ИСП – атомно-эмиссионная спектрометрия с индукционно связанной аргоновой плазмой
ГПО - глутатионпероксидаза
ИБС – ишемическая болезнь сердца
ИМТ – индекс массы тела
МС-ИСП – масс-спектрометрия
ОХС – общий холестерин
ПДК – предельно допустимая концентрация
ПОЛ – перекисное окисление липидов
РФА СИ – рентгенфлюоресцентный анализ с использованием
синхротронного излучения
СОД – супероксиддисмутаза
ССЗ – сердечно-сосудистые заболевания
ТГ - триглицериды
ХС-ЛВП – липопротеиды высокой плотности
ХС-ЛНП - липопротеиды низкой плотности
ЭБМ - эссенциальных биометаллов
GPX – глутатиопероксидаза
Соискатель Н.А. Андрюшина
Подписано в печать 11.10.2007 г. Формат 60х84/8 гарнитура таймс
Объем 1,5 Тираж 100 экз. Заказ № 118
Новосибирский государственный университет экономики и управления
630099 г.Новосибирск, ул.Каменская, 56
