Н. Н. Каншин Хирургическое лечение послеоперационного перитонита, вызванного несостоятельностью кишечных швов Лекция
| Вид материала | Лекция |
- Диагностика и хирургическое лечение заболеваний гепатопанкреатодуоденальной зоны. Целями, 71.79kb.
- Тема Абсцесс, гангрена легкого и бронхоэктатическая болезнь, 394.58kb.
- План реферата Определение перитонита Классификация перитонита Этиология и патогенез, 750.09kb.
- 1. Параректальные свищи. Этиология. Патогенез. Классификация. Клиника. Диагностика., 80.83kb.
- А. Г. Краснояружский Хирургическое лечение компрессионного синдрома средостения, обусловленного, 162.81kb.
- Методические рекомендации для практического занятия №11, 107.83kb.
- Тема : Хирургическое лечение осложнённого неспецифического язвенного колита. Болезнь, 118.83kb.
- Ангелы в белых халатах, 23.11kb.
- Эндост Мотор Апекс доклад, 94.79kb.
- «Санкт-Петербургский государственный медицинский университет им акад. И. П. Павлова», 252.91kb.
Несостоятельность швов пищеводно-кишечного анастомоза
При опухолевых поражениях желудка из-за преобладания в настоящее время инфильтративно растущих низко-дифференцированных карцином наиболее часто бывает показано выполнение не парциальной резекции желудка, а тотальной гастрэктомии в сочетании с обширной лимфодиссекцией. За исключением Москвы и крупных административных центров России эту операцию во многих регионах даже и в настоящее время приходится выполнять в обычных хирургических, а не в специализированных онкологических стационарах. При этом недостаточный опыт рядовых хирургов, относительно редко выполняющих наложение пищеводных анастомозов, способствует возникновению несостоятельности пищеводно-тонкокишечного соустья.
Н.М.Кузин, О.С.Шкроб и Л.В.Успенский в статье, посвященной гастрэктомиям (1992), указывают, что в их клинике «послеоперационная летальность в значительной мере определялась квалификацией хирурга и составляла в группе больных, оперированных более квалифицированными хирургами, 0 — 3 %, в то время как в группе оперированных менее квалифицированными хирургами — 20%».
Вместе с тем формирование даже в труднодоступных анатомических областях вполне надежного механического компрессионного анастомоза новым отечественным сшивающим аппаратом многоразового использования АСК-22 (с мягкими сдавливающими элементами диаметром 22 мм) при пунктуальном соблюдении весьма несложных правил могут осуществлять хирурги не обязательно самой высокой квалификации.
Использование аппарата АСК, позволяя резко снизить опасность гастрэктомии, уменьшило бы также и количество отказов в помощи больным, у которых показана и технически выполнима радикальная операция. Однако использование данного аппарата (как и аппарата АКА-2) нежелательно при выраженном спаечном процессе в брюшной полости, способном затруднить миграцию сдавливающих элементов по тонкой кишке.
Наиболее «физиологичной», предотвращающей развитие в последующем рефлюкс-эзофагита, является гастрэктомия с использованием У-образной петли по Ру. Еще в 1990 г Herberer с соавт. сообщили, что, согласно данным анкетирования 62 центров в Европе, 90% специалистов завершают гастрэктомию анастомозированием пищевода с кишечной петлей по Ру. Именно такой тип завершающего этапа операции мы успешно используем, применяя механическое компрессионное анастомозирование с помощью аппарата АСК. При этом всегда выполняем сагиттальную диафрагмотомию по А. Г. Савиных, позволяющую анастомозу сместиться из брюшной полости в заднее средостение.
Однако большинству отечественных хирургов в различных регионах страны приводится формировать пищеводно-кишечное соустье вручную. В этом случае, как уже указывалось выше, чем реже хирург выполняет такую операцию, тем выше риск развития несостоятельности анастомоза.
Рис. 13 иллюстрирует нашу тактику, дающую возможность в значительной части случаев справиться с этим грозным осложнением.
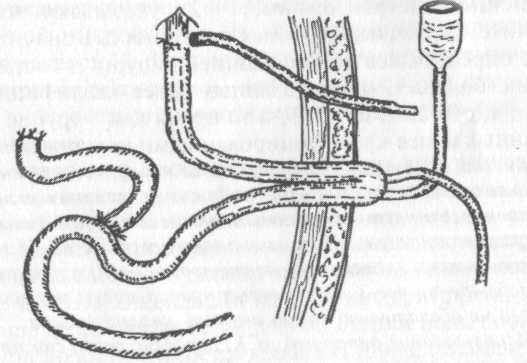
Рис. 13. Схема дренирования при несостоятельности пищеводно-кишечного анастомоза, сформированного с использованием кишечной петли по Ру
При релапаротомии к зоне несостоятельного пищеводно-кишечного анастомоза паравульнарно устанавливают «неприсасывающуюся» двухканальную дренажную трубку и, кроме того, через отдельный разрез выводят на переднюю брюшную стенку в виде «бесшовной» петлевой энтеростомы участок тонкой кишки выше У-образного Ру-анастомоза. При выраженном гнойном перитоните желательно выведение не петлевой стомы, а двух концевых энтеростом.
Завершая операцию по поводу несостоятельности пищеводного анастомоза лапаротомную рану (после тщательного многократного промывания брюшной полости и дополнительного дренирования) при тяжелом распространенном перитоните можно ушить только кожными швами (над продольным сквозным перфорированным дренажом, о чем более подробно будет сказано ниже).
По приводящему колену выведенной кишечной петли внутрипросветно (почти до уровня пищеводного анастомоза) заводят относительно мягкую широкую трубку (например, катетер Пеццера с иссеченным «донышком» его раструба) для декомпрессии и оттока по ней непроизвольно проглатываемой больным слюны. В отводящую петлю устанавливают мягкую трубку (максимально широкий катетер Фолея с заполненным воздухом баллоном) для энтерального кормления.
Жесткий стержень, подведенный под кишечную петлю, не удаляют до полного срастания кишки с тканями брюшной стенки.
После заживления несостоятельного анастомоза, подтвержденного как клинически, так и рентгенологически (отсутствие затекания жидкого контрастного вещества за контуры пищеводно-кишечного соустья), трубки удаляют и ликвидируют энтеростому путем экономной резекции кишки с наложением межкишечного анастомоза.
В случаях развития несостоятельности (менее физиологичного!) пищеводно-кишечного анастомоза, наложенного конец в бок с использованием брауновского межкишечного соустья, может быть применена схема дренирования, указанная на рис. 14.
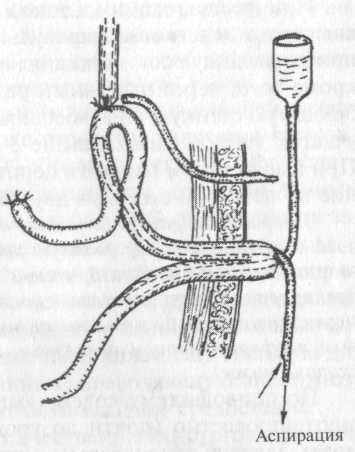
Рис. 14. Дренирование при несостоятельности пищеводно-кишечного анастомоза, наложенного конец в бок с брауновским соустьем. При выраженном гнойном перитоните следует выводить не петлевую стому, а две концевые энтеростомы
Несостоятельность желудочно-кишечного анастомоза
При дистальной резекции желудка несостоятельность желудочно-кишечного анастомоза развивается несравненно реже, чем несостоятельность культи двенадцатиперстной кишки, но все же и она периодически наблюдается в хирургической практике (обычно при нарушении техники наложения швов).
В случаях ранней диагностики несостоятельности (до развития выраженного перитонита) некоторые авторы рекомендуют выполнять ререзекцию. Однако столь ранние релапаротомии, позволяющие выполнить данное вмешательство, в хирургической практике являются редкостью. Вместо ререзекции в такой ситуации можно ограничиться дренированием по схеме, представленной на рис. 15.
В условиях развившегося перитонита можно рекомендовать следующую «щадящую» тактику. Через дефект, обнаруженный в анастомозе (обычно речь идет о передней стенке соустья) следует завести в приводящую петлю тонкой кишки «неприсасывающуюся» двухпросветную силиконовую трубку таким образом, чтобы 2-3 боковых отверстия находились также и в культе желудка (рис. 16).
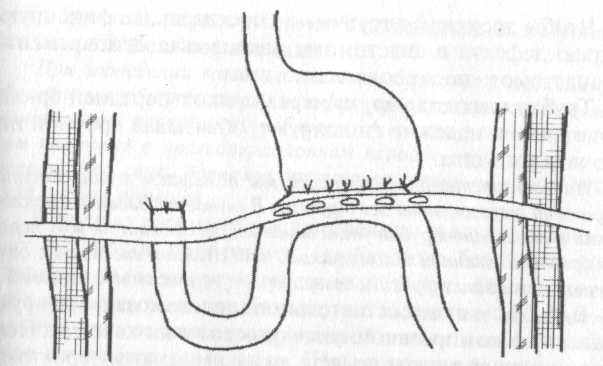
Рис. 15. Дренирование при частичной несостоятельности желудочно-кишечного анастомоза в период до выраженного развития перитонита
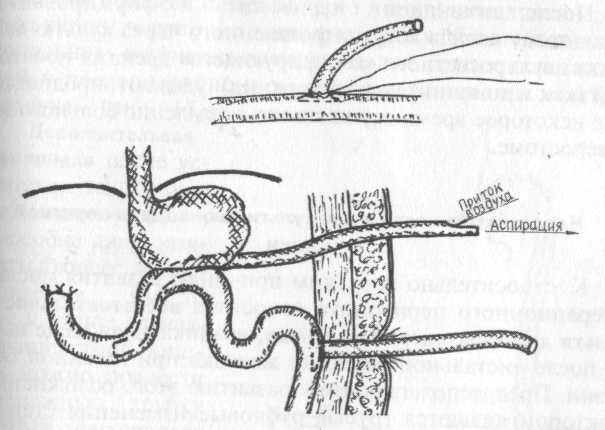
Рис. 16. Возможный вариант дренирования при несостоятельности желудочно-кишечного анастомоза в условиях выраженного гнойного перитонита.
В послеоперационном периоде при таком расположении «активного» дренажа постоянная аспирация «в струе воздуха» будет удалять в банку-сборник отделяемое как из приводящей петли тонкой кишки, так и из культи желудка.
Чтобы дренажная трубка не сместилась, ее фиксируют к краю дефекта в анастомозе, накладывая одновременно на анастомоз «подкрепляющие» швы.
Трубку выводят наружу через прокол передней брюшной стенки и надежно фиксируют, обвязывая прочной нитью кожного шва.
На «ответственные» дренажи мы помещаем тугой хомутик (короткий отрезок этой же трубки). В случае появившейся наклонности к смещению трубки увеличивается расстояние между передней брюшной стенкой и хомутиком, что служит сигналом к более прочной фиксации трубки и возвращению ее в исходное положение.
В 45-50 см от несостоятельного анастомоза формируют подвесную компрессионную еюностому на катетере Пеццера по нашей методике (или майделевскую энтеростому) для утилизации аспирируемого химуса и энтерального кормления больного.
После ликвидации перитонита и формирования «прочного» канала вокруг проведенного через культю желудка двухпросветного «аспирирующего» дренажа последний (как и дополнительные дренажи) удаляют, продолжая еще некоторое время осуществлять кормление больного по энтеростоме.
Несостоятельность швов культи двенадцати перстной кишки
К относительно нередким причинам развития послеоперационного перитонита относится несостоятельность культи двенадцатиперстной кишки, возникающая чаще всего после дистальной резекции желудка при язвенной болезни. Предрасполагающим к развитию этого осложнения фактором являются грубые рубцовые изменения стенки двенадцатиперстной кишки.
В относительно редких случаях при «точечной» несостоятельности, когда к зоне ушитой культи двенадцатиперстной кишки при операции была подведена и фиксирована в этой области тонким поверхностным швом дренажная трубка (лучше двухканальная, у которой легко можно предупреждать или устранять возможную закупорку фибрином) перитонит может не возникнуть и произойдет самостоятельное заживление.
При подведении «ответственного» дренажа к той или иной области мы обычно стремимся фиксировать его конец в этой зоне тонким поверхностным швом, т.к. при рентгенологическом контроле в послеоперационном периоде неоднократно отмечали, что конец дренажа оказывался совсем не в том месте, куда он был помещен.
В случаях развития после резекции желудка выраженных признаков перитонита, необходимо безотлагательно оперировать, используя срединный доступ. При этом следует признать почти аксиомой, что наложение на несостоятельную культю двенадцатиперстной кишки дополнительных швов почти бесперспективно. Швы в условиях нагноения и дуоденостаза могут легко прорезаться.
Лучше не ушивать, а наоборот несколько расширить имеющийся дефект и ввести через него в двенадцатиперстную кишку достаточно широкую трубку, желательно двухканальную неприсасывающуюся для осуществления по ней в послеоперационном периоде аспирации «в струе воздуха» (рис. 17).
Дополнительная тампонада после установки такого дренажа нежелательна и способна лишь затянуть процесс выздоровления. Вместо нее к культе двенадцатиперстной кишки можно подвести дренажную трубку ТММК, фиксировав ее конец в таком положении тонким поверхностным швом Для предупреждения смещения трубки.
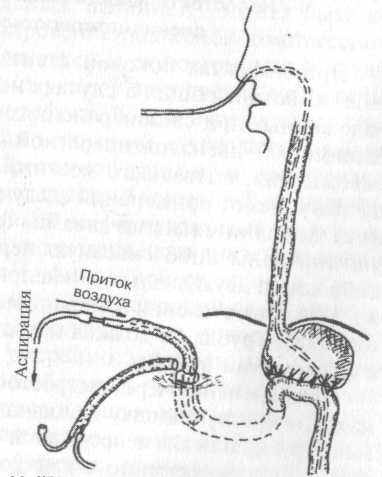
Рис. 17. Дренирование при несостоятельности культи двенадцатиперстной кишки
Аспирируемое дуоденальное содержимое необходимо утилизировать (сочетая утилизацию химуса с энтеральным зондовым питанием) по достаточно тонкому назоеюнальному зонду, проведенному во время экстренного вмешательства через гастроэнтероанастомоз в отводящую петлю
тонкой кишки.
После надежного формирования вокруг дренажа трубчатого хода дренаж из двенадцатиперстной кишки удаляют. Трубчатый свищ быстро закрывается самостоятельно.
Н.А.Ефименко предложил выводить дренаж, установленный в несостоятельную культю двенадцатиперстной кишки, в толще круглой связки печени (после отсечения от печени ее внутренней части), подшивая брюшинные листки связки к культе двенадцатиперстной кишки вокруг дренажа. В дальнейшем (после удаления дренажа) просачивания желчи не наблюдается, и свищевое отверстие быстро заживает.
Несостоятельность швов боковой стенки двенадцатиперстной кишки
При дефектах боковой стенки двенадцатиперстной кишки, возникающих в случаях несостоятельности швов, наложенных при свежих ранениях (в том числе интраопе-рационных) двенадцатиперстной кишки, в ранней стадии осложнения, вызвавшего местный перитонит, можно получить успех от применения следующей тактики. Ушив дефект дополнительными швами, фиксируют вдоль линии ушитой раны либо сквозную перфорированную трубку, либо конец двухканального «неприсасывающегося» дренажа для осуществления аспирационно-промывного лечения (рис. 18). Трубка не должна находиться в тесном контакте с кишечными швами.
Одновременно через гастростому следует провести в двенадцатиперстную кишку двухканальную «неприсасывающуюся» трубку в целях непрерывной аспирации дуоденального химуса и одновременно также содержимого желудка (при полном временном исключении питания через рот).
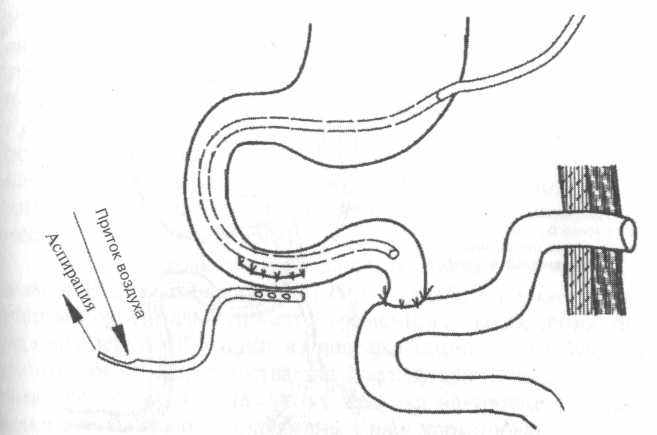
Рис. 18. Возможный план дренирования при несостоятельности швов боковой стенки двенадцатиперстной кишки.
Для утилизации дуоденального химуса (в сочетании с полноценным энтеральным питанием) может быть использовано либо формирование подвесной компрессионной еюностомы, либо наложение еюностомы по Майдлю.
Нам удалось получить успех у двух предельно тяжелых больных при обширном дефекте боковой стенки двенадцатиперстной кишки (ушить который в условиях зияющей гнойной срединой лапаротомной раны не представлялось возможным) с помощь следующей тактики. В двенадцатиперстную кишку через такой несформированный свищ в восходящем направлении была заведена двухканальная «неприсасывающаяся» трубка с фиксацией ее швом к стенке кишки. Одновременно через этот широкий свищ в нисходящем (аборальном) направлении был проведен катетер Фолея. В дальнейшем умеренно заполненный воздухом баллон катетера под воздействием перистальтики постепенно увлек конец катетера в тошую кишку (рис. 19).
В послеоперационном периоде постоянная аспирация «в струе воздуха» предотвратила полную потерю дуоденального содержимого и обильное затекание его в брюшную полость, а катетер Фолея дал возможность утилизировать аспирируемый химус (смешивая его с питательными смесями).
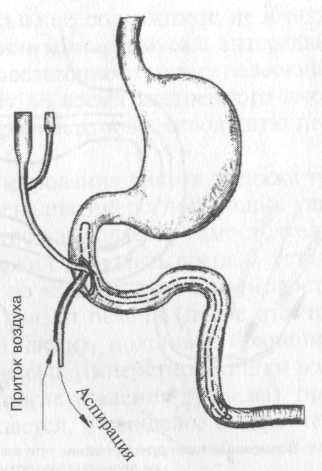
Рис. 19. Аспирация и утилизация содержимого двенадцатиперстной кишки через несформированный дуоденальный свищ
В дальнейшем в результате такого метода лечения общее состояние истощенных больных улучшилось и наступившее уменьшение размеров срединной раны позволило извлечь обе трубки из просвета двенадцатиперстной кишки. К зоне свища паравульнарно через прокол брюшной стенки была подведена «неприсасывющаяся» дренажная трубка. Из доступа вне гнойной раны наложена еюностома по Майдлю. Сведены отдельными швами кожные края значительно сузившейся к этому времени срединной раны.
Все это создало условия, необходимые как для заживления раны, так и для превращения несформированного свища в трубчатый свищ, обладающий способностью заживать самостоятельно.
Лечение боковых несформированных свищей двенадцатиперстной кишки чаще всего весьма трудоемко, требует обременительного для персонала ухода и является для хирургов широкой сферой проявления изобретательности.
В этой проблеме большое значение приобретает профилактика несостоятельности швов боковой стенки двенадцатиперстной кишки при ее травматических разрывах. Швы в такой ситуации приходится накладывать на «ушибленную» стенку кишки, причем часто в зонах, лишенных серозного покрова, и при «загрязненной» забрюшинной клетчатке. Это резко ухудшает условия заживления и лечение послеоперационного перитонита в случаях развития несостоятельности швов.
С целью повышения надежности швов М.М.Абакумовым и Е.С.Владимировой (1986) разработан малотравматичный оригинальный метод временного выключения двенадцатиперстной кишки из пассажа пищи, не требующий повторного вмешательства для последующего восстановления проходимости. На стенку желудка на уровне привратника накладывают циркулярный шов хромированным кетгутом с умеренным натяжением, блокирующим привратник. Период, на протяжении которого происходит рассасывание кетгута (или полимерной нити с известным сроком рассасывания) должен быть достаточным для заживления ушитой раны двенадцатиперстной кишки. На протяжении этого периода больной получает парэнтеральное питание (если не была наложена еюностома, например по Майдлю).
Несостоятельность швов тонкой кишки
Как уже было отмечено, можно назвать «стандартной» ситуацией развитие послеоперационного перитонита после хирургических вмешательств по поводу спаечной тонкокишечной непроходимости.
При экстренной операции в процессе выделения из прочных плоскостных сращений петель тонкой кишки хирург при возникающих повреждениях серозной оболочки или же всех слоев кишечной стенки накладывает на эти участки швы. В этих «слабых зонах» вследствие нарушения при илеусе трофики истонченных кишечных стенок в послеоперационном периоде возможно появление сквозного дефекта с истечением кишечного содержимого в брюшную полость.
В отдельных (весьма редких) случаях подведенный к зоне наложенных швов достаточно широкий дренаж может предупредить развитие перитонита и способствовать переходу несформированного кишечного свища в сформированный трубчатый свищ с последующим самостоятельным излечением.
Развивающийся послеоперационный перитонит при отсутствии подведенной к этой зоне дренажной трубки (или при ее закупорке фибрином) первоначально может расцениваться лечащим врачом как не полностью ликвидированная кишечная непроходимость. Такая ошибка часто приводит к запаздыванию с постановкой диагноза послеоперационного гнойного перитонита.
Наложение при релапаротомии швов в условиях гнойного перитонита даже на небольшую сквозную гнойную рану кишечной стенки без полноценной декомпрессии этой зоны кишки достаточно редко приводит к успеху.
Во время операции по поводу гнойного послеоперационного перитонита, вызванного возникшим в послеоперационном периоде небольшим по размерам сквозным дефектом стенки тонкой кишки можно использовать это отверстие для наложения подвесной компрессионной энтеростомы на катетере Пеццера по нашей методике. Одного больного нам удалось спасти путем наложения в условиях развившегося перитонита двух подвесных компрессионных энтеростом на два последовательно возникавших перфорационных отверстия.
При невозможности приблизить зону ушитого дефекта фиксированной в глубине брюшной полости кишки к брюшной стенке можно сформировать разгрузочную подвесную компрессионную энтеростому несколько выше (оральнее) этого участка. При этом зону ушитого дефекта кишки желательно укрыть не менее чем двумя (!) слоями Тахокмба. К зоне такого ушитого перфорационного отверстия подводят «контрольную» дренажную трубку ТММК.
Подвесная компрессионная энтеростомия с использованием катетера Пеццера обеспечивает более надежную и более полную декомпрессию зоны ушитого дефекта, чем протяженное назоеюнальное дренирование кишки, тем
более что в необходимую зону провести кишечный зонд при наличии инфильтрированных сращений не всегда удается. Кроме того, нужно учитывать, что имеющиеся на вооружении хирургов силиконовые зонды для назоеюнальной декомпрессии тонкой кишки нередко создают лишь иллюзию декомпрессии.
Мы неоднократно убеждались, что при перегибе излишне мягкого декомпрессионного зонда на уровне какого-либо из его боковых отверстий (обычно в зоне крутого изгиба кишечной петли) вся дистальная часть зонда оказывается блокированной.
Такое блокирование в случаях использования двухканально-го зонда можно выявить при рентгенологическом исследовании с введением по каналу зонда, не имеющему боковых отверстий, водорастворимого контрастного вещества с попыткой аспири-ровать контраст по второму каналу.
При небольшой по размерам несостоятельности тонкокишечного анастомоза в случаях ранней диагностики без выраженных явлений перитонита можно либо использовать описанную выше тактику, либо, резецировав зону анастомоза, сформировать новое соустье, обеспечив полноценную декомпрессию этого отдела кишечника при помощи подвесной компрессионной энтеростомии. В случаях одинакового диаметра приводящей и отводящей кишечных петель хирурги, хорошо владеющие техникой наложения кишечных швов, могут формировать (под «прикрытием» полноценной декомпрессии) новый анастомоз в том числе и конец в конец, используя современные атравматические иглы с монофиламентными нитями.
В литературе имеются многочисленные сообщения об успешном наложении в условиях перитонита тонкокишечного анастомоза конец в бок с декомпрессией этой зоны путем формирования майделевской энтеростомы. В.В.Сумин и Ф.С.Жижин (1992) описали подобную операцию, с успехом выполненную В.В.Суминым еще в 1962 г.
Такая операция, дополненная внутрипросветным подведением к анастомозу по предлагаемой нами схеме (рис. 20) аспирационной двухканальной трубки и введением мягкого зонда в отводящую петлю, позволяет одновременно осуществлять как полную разгрузку зоны анастомоза, так и утилизацию аспирируемого химуаса в сочетании с энтеральным кормлением.
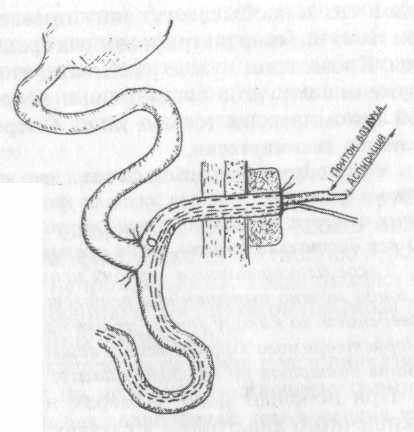
Рис. 20. Формирование в условиях перитонита тонкокишечного анастомоза конец в бок с аспирацией и утилизацией кишечного химуса через «разгрузочную» майделевскую энтеростому
При благоприятном исходе в дальнейшем ликвидируют энтеростому. Остающаяся «заглушенная» У-образная петля к каким-либо нарушениям не приводит.
В случаях, когда высокий несостоятельный («разваливающийся») анастомоз тонкой кишки фиксирован в инфильтрате в глубине брюшной полости, отсутствуют как возможность выведения концевых кишечных стом на брюшную стенку, так и возможность резекции анастомоза с наложением нового соустья.
Ретроспективно оценивая такую предельно тяжелую ситуацию, которую мы наблюдали, в частности, в одной из московских клинических больниц (с неблагоприятным исходом), считаем оправданной, в виде «операции отчаяния», следующую тактику, напоминающую уже изложенный несколько выше вариант лечения обширных боковых дефектов двенадцатиперстной кишки.
В приводящий отрезок кишки через дефект в анастомозе, края которого не удается свести швами, рекомендуем установить двухканальную («неприсасывающуюся») дренажную трубку и фиксировать ее швом к кишечной стенке. К зоне анастомоза следует дополнительно подвести такую же отсасывающую трубку для удаления частично продолжающего поступать в брюшную полость тонкокишечного содержимого. Для утилизации аспирируемого из тонкой кишки «химуса» и осуществления энтерального питания дистальнее разваливающегося анастомоза следует сформировать подвесную компрессионную энтеростому на катетере Пеццера. Рана брюшной стенки частично остается открытой.
Такая тактика может дать возможность (при трудоемком уходе) сохранить жизнь больного до момента, когда появятся условия для выполнения восстановительной операции.
При «запущенном» распространенном послеоперационном перитоните, обусловленным протяженной несостоятельностью межкишечного анастомоза (как на тонкой, так и на ободочной кишке) некоторые авторы рекомендуют выведение несостоятельного анастомоза на брюшную стенку (с фиксацией кишки швами к коже). Однако, такая экстраперитонезация анастомоза способна приводить к тяжелым осложнениям из-за прорезывания швов, фиксирующих воспаленную кишку к коже с дополнительным инфицированием брюшной полости.
Вместе с тем «управляемую» ситуацию обеспечивает резекция зоны несостоятельного анастомоза (в том числе и в верхних отделах тонкой кишки!) с раздельным выведением двух концевых «бесшовных» кишечных стом по нашей методике, о которой будет сказано несколько ниже.
После раздельного выведения двух концевых тонкокишечных стом (на расстоянии 5-8 см друг от друга) тонкокишечное содержимое, поступающее из верхнего отрезка тощей кишки в ту или иную емкость (по достаточно широкому латексному катетеру Пеццера с иссеченным «донышком» его раструба), вводят по мягкому зонду (или второму катетеру Пеццера) в отводящую кишечную петлю. Это дает возможность избежать потерь тонкокишечного содержимого и осуществлять полноценное кормление больного жидкой пищей через рот до момента выполнения в дальнейшем восстановительной операции.
Введение утилизируемого кишечного содержимого в отводящую петлю осуществляют при нахождении емкости (в которую переливают это содержимое) на очень небольшой высоте над уровнем передней брюшной стенки. При этом такое «физиологичное» вливание происходит не непрерывно, а отдельными порциями, зависящими от прохождения по кишке перистальтической волны. Не следует прибегать к «ускоренному» (форсированному) вливанию в кишку под значительным давлением.
Необходимо учитывать, что выделяющееся из верхнего отрезка кишки тонкокишечное содержимое не должно длительно находиться вне просвета кишки. В связи с этим для ухода за такими больными (в силу трудоемкости ухода) обычно приходится привлекать родственников пациента. Однако при улучшении общего состояния больной может самостоятельно выполнять несложную процедуру утилизации выделяющегося наружу тонкокишечного содержимого (в том числе и в домашних условиях после временной выписки из стационара). Мы располагаем такими наблюдениями.
Выведение концевых кишечных стом при гнойном перитоните производим полностью бесшовно через специально формируемые в брюшной стенке отверстия. Размеры таких отверстий во всех слоях брюшной стенки должны строго соответствовать диаметру выводимой кишки.
При излишне широком отверстии стенки кишки не будут иметь возможности быстро срастаться по всей своей окружности с тканями брюшной стенки. При слишком узком отверстии в брюшной стенке кишка окажется сдавленной стенками канала с блокированием ее просвета. При выведении тонкой кишки через «зауженное» отверстие вследствие затрудненного венозного оттока может возникнуть нарастающий отек наружной части кишки. При этом отечный сегмент энтеростомы начнет в буквальном смысле вытягивать из брюшной полости дополнительные участки кишки, которые в свою очередь также становятся резко отечными.
При данном осложнении, развивающемся уже в первые сутки после операции, необходимо срочно расширить отверстие в брюшной стенке, приведя его в соответствие с диаметром кишки.
Еще раз подчеркиваем, что при перитоните выведенную в виде хоботка воспаленную кишку мы не подшивает к тканям брюшной стенки. Такие швы на воспаленной кишке часто прорезываются с образованием в стенке киши сквозного дефекта, причем образовавшийся свищ может погрузиться ниже уровня кожи и вызвать развитие флегмоны брюшной стенки.
Кроме того, герметичная фиксация воспаленной кишки к коже может препятствовать свободному оттоку инфицированного раневого секрета из канала, по которому кишка проходит в толще брюшной стенки, создавая реальную опасность развития флегмоны. При разработке способа бесшовного выведения кишки мы, основывались на том факте, что выведение при гнойном перитоните дренажных трубок флегмону брюшной стенки не вызывает.
Вокруг выведенного кишечного хоботка формируем широкий (!) плотный (более высокий при тонкокишечной стоме) марлевый валик, имеющий форму бублика, следя при этом, чтобы валик не сдавил просвет кишки. Марлевый валик по его наружному краю фиксируем 3-4 швами к коже.
При выведении хоботка тонкой кишки заводим в кишку на небольшую глубину мягкую эластичную трубку (широкий катетер Пеццера с иссеченной центральной частью его раструба) и затягиваем на катетере кисетный шов, наложенный на торец кишки. Нити кисетного шва фиксируем к вершине марлевого валика (рис. 21).
В случаях выведения толстой кишки, удалив с торца кишки временный нитяной (или линейный металлический скобочный) шов, циркулярно подшиваем края открытой кишечной стомы к
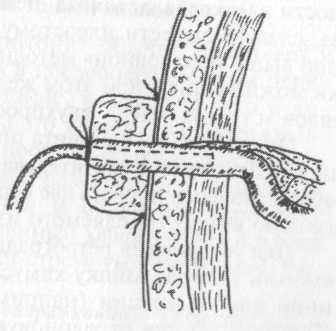
Рис. 21. Выведение при гнойном перитоните «бесшовной» концевой энтеростомы
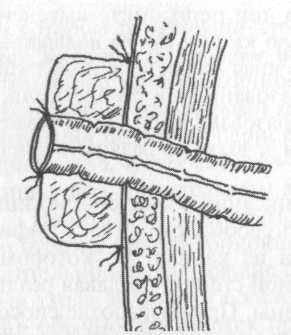
Рис. 22. Выведение при гнойном перитоните «бесшовной» концевой колостомы
вершине марлевого валика (рис. 22). Первое время отделяемого из толстой кишки обычно не бывает. После его появления марлевая «муфта» предохраняет кожные края от загрязнения.
Для сбора толстокишечного содержимого марлевый валик (вместе с кишечным хоботком) помещаем в полиэтиленовый пакет через прорезанное в боковой стенке пакета отверстие или же в стандартный калоприемник.
Марлевый валик не удаляем долго, пока кишка не срастется вполне надежно с брюшной стенкой.
Каких-либо осложнений при использовании такой методики бесшовного выведения концевых кишечных стом у многочисленных больных мы не наблюдали.
Несостоятельность швов толстой кишки
При перитоните вследствии выраженной несостоятельности илеоколоанастомоза, резецировав (!) зону анастомоза, следует вывести илеостому в виде хоботка по описанной выше «бесшовной» методике. Культю ободочной кишки можно ушить (при этом желательно фиксировать к зоне швов «страховочную» двухпросветную дренажную трубку).
Однако если у пациента при предшествовавших операциях была удалена значительная часть тонкой кишки, то необходимо формировать две стомы с целью введения в ободочную кишку отделяемого из тонкокишечного свища.
Для устранения ретроградного вытекания части вливаемого в толстую кишку химуса следует применить тот или иной вид обтурации (например, использовать обтуратор Колченогова или паралоновую губку с проведенной через ее толщу трубкой, предназначенной для введения тонкокишечного содержимого).
При несостоятельности колоколоанастомоза достаточно после его резекции вывести по бесшовной методике лишь приводящий конец ободочной кишки.
Несостоятельный колоректоанастомоз желательно сохранить, наложив несколько выше него петлевую колостому, возвышающуюся над уровнем кожи, окружив ее марлевой «муфтой».
Дренирование зоны выключенного из пассажа несостоятельного колоректоанастомоза двухканальным апирационно-промывном дренажом способно приводить к излечению с сохранением удовлетворительной проходимости анастомоза. Разъединение же низкого прямокишечного анастомоза почти обрезает путь к последующей восстановительной операции.
Нам неоднократно приходилось видеть больных с наложенной для «отключения» толстой кишки цекостомой. Подчеркиваем, что цекостома толстую кишку не отключает.
Риск развития несостоятельности колоректоанастомоза как мы убедились, резко снижается при использовании сшивающего компрессионого аппарата АСК-29, о котором говорилось выше.
Использование данного аппарата делает также относительно несложным (!) восстановительное вмешательство после операции Гартмана.
Декомпрессия тонкой кишки
Послеоперационный перитонит обычно возникает у больных, еще не получавших в послеоперационном периоде достаточно обильное питание, вследствие чего в кишечнике у них нет значительного количества содержимого. Кроме того, вследствие относительно ранней релапаро-томии (патологический процесс развивается в стационаре при внимательном наблюдении за больным) перитонит обычно не носит распространенный характер. Но и в этих условиях при операции следует стремиться по возможности опорожнить тонкую кишку.
Для форсированного интраоперационного опорожнения и промывания просвета тонкой кишки при перитоните нами совместно с заведующим лабораторией силикона в подмосковных Мытищах (ныне -ЗАО «Медсил») Л.З.Хазеном в конце 70-х годов был разработан специальный широкий (с наружным диаметром 11 мм) двухканальный «неприсасывающийся» зонд, выпускаемый под маркой ЖКС №33 (рис. 23). На зонд было получено авторское свидетельство на изобретение.
-
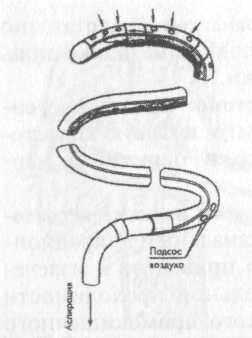
Рис. 23. «Неприсасывающийся» желудочно-кишечный зонд ЖСК- 33
При релапаротомии по поводу распространенного перитонита после удаления электроотсосом жидкого гнойного содержимого из брюшной полости следует удалить жидкое содержимое и из растянутых петель тонкой кишки (если они не сращены прочно друг с другом).
Достаточная ригидность зонда ЖКС-33 позволяет относительно легко провести его из желудка через двенадцатиперстную кишку до начального отдела тощей кишки. В дальнейшем, поэтапно сборивая на длинном зонде кишку (как при проведении шнурка на оконной занавеске), его продвигают до слепой кишки. Такое проведение зонда облегчают имеющиеся у его конца небольшие круговые утолщения.
В процессе проведения зонда по тонкой кишке осуществляют аспирацию обычным операционным электроотсосом, подключенным к каналу зонда, не имеющему (!) боковых отверстий. После опорожнения тонкой кишки по мере последующего извлечения зонда многократно промывают просвет кишки физиологическим раствором. Перед завершением операции зонд ЖСК-33 заменяют более тонким двухпросветным зондом.
При послеоперационном перитоните чаще всего не следует излишне настойчиво стремиться устанавливать постоянный декомпрессионный зонд по всей длине тонкой кишки (хотя тот или иной вид декомпрессии кишки крайне необходим). Нужно учитывать, что в отсутствии кишечной непроходимости упорные попытки провести зонд по кишечнику с высвобождением кишечных петель из инфильтрированных сращений способны травмировать кишку, принося значительно больше вреда, чем пользы.
Радикальное разъединение спаявшихся кишечных петель привело бы к инфицированию от контакта с экссудатом изолированных сращениями больших поверхностей висцеральной брюшины. Эти сращения ограничивают зону распространения послеоперационного перитонита. Данный этап операции проводят соответственно имеющейся конкретной ситуации. Санацию брюшной полости осуществляют с тщательными промываниями зон скопления экссудата.
Декомпрессионный зонд (в тех случаях, когда отсутствуют указанные выше показания к формированию разгрузочной подвесной «бесшовной» энтеростомы на катетере Пеццера) при спаявшихся кишечных петлях в условиях послеоперационного перитонита можно завести на 30-40 см за связку Трейца. После операции по зонду осуществляют постоянную эвакуацию застойного тонкокишечного химуса, в значительной степени состоящего из панкреатического сока и желчи.
Если в области передней стенки желудка нет резко выраженного тяжелого гнойного процесса, декомпрессионный зонд может быть установлен не трансназально, а через гастростому. Это, во-первых, значительно облегчает проведение зонда через двенадцатиперстную кишку и, во вторых, легче переносится пожилыми больными в послеоперационном периоде.
Такое проведение зонда через временную гастростому имеет большое значение в случаях одновременной длительной интубации трахеи или трахеостомии с целью пролонгированного вспомогательного дыхания у тяжелых больных. Нахождение в пищеводе плотного зонда и одновременно в трахее интубационной трубки с раздутой манжеткой может вызвать пролежень стенок этих органов вплоть до возникновения пищеводно-трахеального свища.
Стерильный аспирационно-промывной кишечный зонд проводят через небольшое отверстие в стенке желудка и, оставляя в желудке участок зонда с 2-3 боковыми отверстиями, заводят его через привратник в тонкую кишку. Зонд прочно фиксируют к желудочной стенке двумя «полукисетными» швами. Длинные нити этих швов вместе с верхними отделами зонда выводят наружу через прокол брюшной стенки и подшивают с умеренным натяжением к краю кожного отверстия. Дополнительно изнутри вокруг зонда подшивают стенку желудка к париетальной брюшине.
(В Москве проф. В.Б.Александров широко использует как при плановых, так и при экстренных операциях на кишечнике введение декомпрессионного зонда через временную гастростому.)
Помимо декомпрессии тонкой кишки через некоторый промежуток времени декомпрессионный зонд следует использовать для энтерального питания и лечебного воздействия на развивающийся при перитоните синдром кишечной недостаточности (в соответствии с имеющимися в современной литературе рекомендациями по «зондовой нутритивной терапии»).
